COMPARISON BETWEEN ELISA (ENZYME-LINKED IMMUNOSORBENT ASSAY) AND NAT (NUCLEIC ACID TEST) IN SCREENING BLOOD DONORS AND THEIR EFFICACY IN PREVENTING TRANSFUSION INFECTIONS
REGISTRO DOI: 10.69849/revistaft/fa10202511210004
Gisele Araújo Nascimento1
Hugo Monteiro Junior2
RESUMO
Introdução: A segurança transfusional permanece um desafio na medicina moderna, exigindo métodos diagnósticos sensíveis e específicos para minimizar o risco de infecções transmissíveis pelo sangue. Entre as metodologias empregadas, o ELISA (Enzyme-Linked Immunosorbent Assay) e o NAT (Nucleic Acid Test) destacam-se como principais ferramentas de triagem, sendo o NAT reconhecido por detectar diretamente o material genético viral e reduzir significativamente o período de janela imunológica. Objetivo: comparar a eficácia dos testes ELISA e NAT na triagem de doadores de sangue, considerando sensibilidade, especificidade, custo-benefício e impacto na segurança transfusional. Metodologia: revisão integrativa da literatura, de natureza qualitativa, descritiva e exploratória, com busca em PubMed, Scopus, Web of Science, SciELO e BVS, abrangendo publicações entre 2013 e 2024. A análise baseou- se na técnica de análise de conteúdo e comparação crítica dos achados. Resultados: o NAT reduziu a janela imunológica do HIV em até 11 dias e do HCV em até 25 dias em relação ao ELISA, diminuindo o risco residual para menos de 1 caso por milhão de doações. Embora apresente custo mais elevado, demonstrou melhor custo-efetividade, especialmente em modelos centralizados e combinados à sorologia. A estratégia de dupla triagem mostrou-se a mais segura e sustentável. Conclusão: a integração entre métodos sorológicos e moleculares constitui a abordagem mais eficaz para garantir a segurança transfusional, e o NAT representa um avanço essencial na detecção precoce de infecções virais e no fortalecimento da biossegurança em hemoterapia.
Palavras-chave: Segurança transfusional. ELISA. NAT. Triagem de doadores. Infecções transfusionais.
ABSTRACT
Introduction: Transfusion safety remains a major challenge in modern medicine, requiring highly sensitive and specific diagnostic methods to minimize the risk of transfusion-transmitted infections. Among the main screening techniques, the ELISA (Enzyme-Linked Immunosorbent Assay) and NAT (Nucleic Acid Test) stand out as essential tools, with NAT recognized for directly detecting viral genetic material and significantly reducing the immunological window period. Objective: To compare the effectiveness of ELISA and NAT in blood donor screening, focusing on sensitivity, specificity, cost-effectiveness, and impact on transfusion safety. Methods: An integrative literature review with a qualitative, descriptive, and exploratory approach was conducted through PubMed, Scopus, Web of Science, SciELO, and BVS databases, including studies published between 2013 and 2024. Data were analyzed using content analysis and thematic categorization for critical comparison of findings. Results: NAT shortened the immunological window period for HIV by up to 11 days and for HCV by up to 25 days compared to ELISA, reducing the residual infection risk to less than one case per million donations. Although its unit cost is higher, NAT demonstrated greater cost- effectiveness, particularly in centralized models and when combined with serological screening. The dual-screening approach proved to be the most secure and sustainable strategy. Conclusion: The integration of molecular and serological testing constitutes the most effective approach to ensure transfusion safety. NAT represents an indispensable advancement for early viral detection and for strengthening biosafety in transfusion medicine.
Keywords: Transfusion Safety. ELISA. NAT. Blood donor screening. Transfusion transmitted infections.
1 INTRODUÇÃO
A segurança transfusional constitui um dos eixos centrais da medicina moderna e representa um desafio contínuo para os sistemas de saúde pública em todo o mundo. O risco de transmissão de agentes infecciosos pelo sangue doado impulsionou o desenvolvimento de métodos diagnósticos progressivamente mais sensíveis, específicos e rápidos, capazes de identificar infecções ainda em estágios iniciais. A introdução dos testes sorológicos, especialmente para vírus como o HIV, o vírus da hepatite B (HBV) e o vírus da hepatite C (HCV), foi um marco decisivo na redução das infecções transfusionais, mas as limitações desses métodos — notadamente o período de janela imunológica — continuam sendo uma preocupação crítica, uma vez que indivíduos recentemente infectados podem não ser detectados pelos testes convencionais (World Health Organization, 2019).
Com o avanço das biotecnologias diagnósticas, duas metodologias tornaram-se pilares da triagem laboratorial de doadores de sangue: o ELISA (Enzyme-Linked Immunosorbent Assay) e o NAT (Nucleic Acid Test). O ELISA, amplamente difundido nos bancos de sangue, baseia-se na interação antígeno-anticorpo e permite a detecção de marcadores sorológicos de infecção em fases intermediárias e tardias, apresentando elevada reprodutibilidade e baixo custo operacional (Lindsey et al., 2021). Em contraste, o NAT constitui uma técnica molecular de alta sensibilidade que identifica diretamente o material genético viral, seja DNA ou RNA, reduzindo de forma expressiva o período de janela imunológica e elevando a precisão diagnóstica (Clements et al., 2020). Essa capacidade de detecção precoce consolidou o NAT como ferramenta essencial para a segurança transfusional em países com sistemas laboratoriais avançados.
A introdução do NAT nos protocolos de triagem marcou uma mudança paradigmática na hemoterapia contemporânea. Estudos demonstram que o método é capaz de identificar o RNA do HIV de 9 a 11 dias antes da reatividade sorológica e o RNA do HCV até 25 dias antes da detecção pelos ensaios ELISA de quarta geração, reduzindo quase a zero o risco de transmissão durante a janela imunológica (Strambi et al., 2018; Kleinman & Busch, 2022). A adoção combinada de testes sorológicos e moleculares é, portanto, considerada a estratégia diagnóstica mais robusta, pois integra as vantagens da detecção imunológica (antígenos e anticorpos) com a identificação direta do genoma viral, proporcionando redundância diagnóstica e mitigando falhas analíticas (Garcia et al., 2020).
Apesar dos ganhos tecnológicos, a implementação universal do NAT ainda enfrenta desafios consideráveis. Os custos associados aos reagentes e plataformas automatizadas, a necessidade de infraestrutura laboratorial especializada e a capacitação técnica contínua dos profissionais limitam sua expansão em países de renda média e baixa (Hollinger & Kleinman, 2020). No Brasil, a inserção do NAT iniciou-se de forma progressiva em 2011, como parte do Plano Nacional de Segurança Transfusional, sendo posteriormente institucionalizada em 2012 pela Coordenação-Geral de Sangue e Hemoderivados. Atualmente, o sistema opera de forma centralizada em laboratórios regionais, o que permitiu ganhos expressivos em padronização e custo-efetividade. Contudo, a cobertura ainda não é total, e alguns hemocentros permanecem restritos ao uso de testes sorológicos, o que representa um desafio para a uniformização da segurança transfusional (Brasil, 2014).
A discussão sobre a eficácia comparativa entre ELISA e NAT transcende o aspecto técnico, envolvendo dimensões econômicas, epidemiológicas e éticas. Embora o custo unitário do NAT seja substancialmente superior ao do ELISA — variando, em média, de USD 15 a 25 por teste, contra USD 3 a 5 no ELISA —, estudos de custo-benefício demonstram que o investimento inicial é compensado pela redução dos casos de infecção transfusional e pela economia gerada na prevenção de doenças crônicas e hospitalizações decorrentes (Motte et al., 2019; Soarez & Novaes, 2017). A avaliação dessa relação entre custo e eficácia torna-se, portanto, essencial para orientar decisões de política pública, especialmente em países com orçamentos restritos.
Nesse contexto, a presente pesquisa tem como objetivo comparar a eficácia diagnóstica dos testes ELISA e NAT na triagem de doadores de sangue, analisando suas contribuições para a redução do risco de transmissão de infecções transfusionais. Serão abordados parâmetros como sensibilidade, especificidade, redução do período de janela imunológica e custo- efetividade, com base em literatura científica recente e de alto impacto. Busca-se, assim, construir um panorama comparativo que subsidie tanto a atualização dos protocolos técnicos quanto o aprimoramento das políticas públicas de hemoterapia no Brasil.
A relevância deste estudo reside na necessidade de aprimorar continuamente os programas de triagem laboratorial e fortalecer a biossegurança transfusional como política pública essencial. A transfusão sanguínea é um procedimento vital em diversas especialidades médicas, e sua eficácia depende diretamente da qualidade do sangue coletado e dos métodos de triagem empregados. Assim, ao integrar evidências científicas consolidadas sobre o desempenho do ELISA e do NAT, este trabalho pretende contribuir para o desenvolvimento de diretrizes mais rigorosas e equitativas, alinhadas aos padrões internacionais de qualidade e às metas da Organização Mundial da Saúde para o fortalecimento da segurança transfusional até 2030 (World Health Organization, 2021).
2 REVISÃO DE LITERATURA
2.1 Introdução à hemoterapia: objetivos, importância clínica e histórico
A hemoterapia constitui um dos pilares da medicina transfusional moderna, sendo definida pela Organização Mundial da Saúde (OMS) como o conjunto de atividades técnico- científicas destinadas à coleta, processamento, testagem, armazenamento, distribuição e uso clínico de sangue e seus componentes de forma segura e ética. Sua principal finalidade é restabelecer a homeostase hematológica e corrigir deficiências celulares ou plasmáticas, desempenhando papel essencial em pacientes submetidos a cirurgias, transplantes, terapias oncológicas, traumas e distúrbios hematológicos. Além da dimensão técnica, a hemoterapia integra o conceito ampliado de biossegurança e rastreabilidade, compondo um subsistema estratégico para a sustentabilidade dos serviços de saúde e para a garantia da equidade no acesso terapêutico (World Health Organization, 2021; Pan American Health Organization, 2022).
Historicamente, o desenvolvimento da hemoterapia foi marcado por avanços decisivos que moldaram o paradigma atual de segurança transfusional. As primeiras tentativas documentadas de transfusão datam do século XVII, porém foi a descoberta dos grupos sanguíneos ABO por Karl Landsteiner, em 1901, que inaugurou a era científica da compatibilidade transfusional, reduzindo drasticamente a letalidade por reações hemolíticas (Landsteiner, 1901). Na década de 1940, a identificação do fator Rh e o desenvolvimento de anticoagulantes à base de citrato transformaram o manejo do sangue em um processo tecnicamente controlável (Reis et al., 2019). O uso de bolsas plásticas e sistemas fechados na década de 1950 consolidou o conceito de “ciclo hemoterápico seguro”, promovendo estabilidade e rastreabilidade no armazenamento (Petz & Garratty, 2004).
Com o avanço das ciências biomédicas, a hemoterapia expandiu-se para além da simples transfusão, configurando-se como disciplina multidisciplinar que integra princípios de imunologia, microbiologia, genética molecular e gestão de qualidade laboratorial. Segundo Reis et al. (2019), essa transição de uma prática empírica para uma ciência baseada em evidências refletiu a crescente necessidade de padronização global e de vigilância epidemiológica dos estoques sanguíneos, especialmente diante de surtos infecciosos e pandemias emergentes.
No contexto regulatório internacional, a OMS classifica a hemoterapia como serviço essencial dentro dos sistemas de saúde resilientes, com papel central na meta de cobertura universal em saúde e nos Objetivos de Desenvolvimento Sustentável (ODS), particularmente no ODS 3, que trata da promoção da saúde e bem-estar (World Health Organization, 2021). Sob essa ótica, o sangue é reconhecido como “recurso terapêutico estratégico”, cuja gestão requer políticas públicas integradas e sustentáveis (World Health Organization, 2022).
No Brasil, a institucionalização da hemoterapia como política pública consolidou-se com a criação da Política Nacional de Sangue e Hemoderivados (PNSH) em 2001 e a subsequente regulamentação pela ANVISA. Esses instrumentos garantiram a uniformização das práticas, a implantação de sistemas informatizados de rastreabilidade e o fortalecimento da rede de hemocentros regionais (ANVISA, 2014; Ministério da Saúde, 2022). A Resolução RDC nº 34/2014 e suas atualizações enfatizam a obrigatoriedade da triagem sorológica e molecular, da validação de processos e da capacitação continuada das equipes, o que elevou os padrões de qualidade a níveis comparáveis aos centros europeus e norte-americanos.
Os objetivos contemporâneos da hemoterapia transcendem a simples transfusão de sangue total. A terapia hemocomponente racional — que individualiza o uso de concentrados de hemácias, plaquetas, plasma fresco congelado e crioprecipitado conforme o perfil clínico do paciente — representa um marco de eficiência terapêutica e de economia de recursos. Estudos clínicos randomizados, como o de Carson et al. (2016), demonstraram que estratégias transfusionais restritivas reduzem mortalidade e eventos adversos em pacientes críticos, reforçando o paradigma da personalização transfusional baseada em evidências.
Do ponto de vista técnico-operacional, o ciclo hemoterápico envolve etapas críticas que vão desde a triagem clínica do doador até o transporte e administração final do hemocomponente. Erros em qualquer dessas fases podem gerar reações hemolíticas, transmissão de patógenos ou falhas terapêuticas, o que justifica a adoção de protocolos de controle de qualidade total e validação contínua de processos, conforme recomendado pela European Directorate for the Quality of Medicines & HealthCare (EDQM, 2023).
Os avanços recentes em automação laboratorial, algoritmos de inteligência artificial e tecnologias moleculares como o Nucleic Acid Test (NAT) vêm redefinindo o conceito de segurança transfusional. Essas inovações permitem a detecção precoce de agentes infecciosos durante o período de janela imunológica, reduzindo significativamente o risco residual e ampliando a confiabilidade dos bancos de sangue (Gonçalves et al., 2021; European Directorate for the Quality of Medicines & HealthCare, 2023). Adicionalmente, a integração de sistemas informatizados e o uso de blockchain em rastreabilidade têm sido explorados em países europeus e asiáticos como ferramentas emergentes de biossegurança (Zou et al., 2022).
Em síntese, a hemoterapia moderna se configura como eixo integrador entre tecnologia, ética e saúde pública. Ela não se limita ao fornecimento de hemocomponentes, mas envolve uma rede complexa de práticas interdisciplinares que garantem segurança, qualidade, rastreabilidade e sustentabilidade do ciclo do sangue. Essa abordagem sistêmica é fundamental para enfrentar os desafios contemporâneos impostos por novas infecções, envelhecimento populacional e crises sanitárias globais, reafirmando o papel da hemoterapia como componente essencial da infraestrutura biomédica global (World Health Organization, 2022; ANVISA, 2014).
2.1.1 Riscos das Transfusões: Infecções Transmissíveis pelo Sangue
As transfusões de sangue, embora indispensáveis para o suporte terapêutico em múltiplas condições clínicas, permanecem associadas a riscos inerentes, especialmente os de natureza infecciosa. O risco transfusional é definido como a probabilidade de transmissão de agentes patogênicos por meio de hemocomponentes contaminados e depende da combinação entre prevalência populacional, qualidade da triagem, tempo de janela imunológica e robustez dos sistemas de vigilância (World Health Organization, 2023). Mesmo com os avanços tecnológicos, as infecções transmissíveis pelo sangue — incluindo vírus como HIV, HBV, HCV e HTLV-I/II, além de bactérias, parasitas e fungos — ainda representam ameaça significativa à biossegurança transfusional (Cunha et al., 2020).
Estudos multicêntricos demonstram que, apesar da implementação global de tecnologias de triagem sorológica e molecular, nenhum sistema é infalível. Existe um risco residual, definido como a possibilidade de uma unidade infectada escapar à detecção laboratorial mesmo após todos os testes obrigatórios. Esse risco resulta de fatores como falhas operacionais, mutações virais que escapam ao reconhecimento antigênico e, sobretudo, da existência do período de janela imunológica, durante o qual o material biológico doado ainda não expressa marcadores detectáveis (Reis et al., 2019; Stramer et al., 2019). Em bancos de sangue altamente automatizados, como os dos Estados Unidos, ainda ocorrem raros casos de soroconversão pós- transfusional, estimados em aproximadamente 1 para 2,3 milhões de doações no caso do HIV (Stramer et al., 2019).
A janela imunológica constitui um dos desafios centrais para a segurança transfusional. Ela representa o intervalo entre a infecção e o surgimento de marcadores sorológicos ou moleculares detectáveis. Durante esse período, o sangue aparentemente não reativo pode conter partículas virais capazes de transmissão. Gonçalves et al. (2021) demonstram que, antes da introdução do teste molecular (NAT), a janela para HIV era de cerca de 22 dias com o ELISA de terceira geração, reduzindo-se para 9 a 11 dias após a adoção do NAT em testes individuais (ID-NAT). Essa redução é determinante para a minimização do risco residual em populações de alta prevalência viral.
O risco transfusional é também modulável por fatores epidemiológicos e socioculturais. A prevalência de infecções em potenciais doadores, a eficácia da triagem clínica e a fidelização de doadores regulares são elementos cruciais. Doadores em fase aguda de infecção, ou que omitem comportamentos de risco, podem contribuir para a manutenção de níveis residuais de transmissão. A ANVISA (2014) e a OMS (2021) destacam a necessidade de protocolos uniformizados de entrevista clínica e confidencialidade reforçada como parte das estratégias de mitigação.
Nos últimos anos, emergiram novas ameaças virais de relevância transfusional, particularmente arboviroses tropicais como Zika, Dengue e Chikungunya, cujos genomas podem estar presentes no sangue de doadores assintomáticos. Revisões de Corman et al. (2020) e Santos et al. (2022) apontam que, em regiões endêmicas, até 3% das doações podem estar contaminadas com RNA viral detectável durante surtos, o que amplia o risco transfusional em países latino-americanos e africanos. O surgimento do SARS-CoV-2 também provocou intensa mobilização regulatória; embora a transmissão transfusional não tenha sido confirmada, a OMS (2023) recomendou vigilância ativa e exclusão temporária de doadores pós-infecção.
As infecções bacterianas associadas a hemocomponentes constituem outro desafio crítico, especialmente nos concentrados de plaquetas, que são armazenados a 20–24 °C. Estudos europeus e norte-americanos estimam incidência de contaminação bacteriana de 1:1.000 a 1:3.000 unidades, sendo causa importante de choque séptico pós-transfusional (Stramer et al., 2019; Schmidt et al., 2021). Protocolos modernos incorporam o uso de testes de detecção bacteriana rápida e tratamento patogênico por radiação UV-C ou riboflavina, reduzindo a taxa de eventos fatais em mais de 70% (Schmidt et al., 2021).
A introdução do Nucleic Acid Test (NAT) representou um marco na prevenção de infecções transmissíveis por transfusão. Diferentemente dos métodos sorológicos, o NAT detecta diretamente o RNA ou DNA viral antes da resposta imune do hospedeiro, encurtando o período de janela e aumentando a sensibilidade diagnóstica. Dados alemães demonstram que, após a implantação do NAT, o risco de transmissão do HCV caiu de 1:200.000 para menos de 1:10.000.000 unidades transfundidas (Schmidt et al., 2021). O mesmo padrão é observado para o HIV e o HBV, cujas taxas residuais reduziram-se para menos de 1 caso por 3 milhões de doações testadas (Stramer et al., 2019).
Entretanto, a cobertura global do NAT ainda é desigual. Segundo a OMS (2023), 39 países ainda não implementaram testagem molecular sistemática, concentrando-se principalmente em regiões de baixa e média renda. Nestes contextos, a sorologia convencional continua sendo a principal ferramenta de triagem, o que mantém o risco transfusional elevado. Obstáculos como custo operacional, falta de infraestrutura laboratorial, carência de profissionais capacitados e escassez de reagentes validados são recorrentes (Oliveira et al., 2017; WHO, 2021). No Brasil, embora a Rede Nacional de Triagem NAT (RNTNAT) tenha alcançado cobertura superior a 90% dos hemocentros públicos, ainda persistem lacunas em regiões amazônicas e interiores nordestinos (Ministério da Saúde, 2022).
A bioética transfusional exige que o risco residual, ainda que mínimo, seja comunicado de forma transparente. O princípio da não maleficência impõe que toda tecnologia validada e custo-efetiva seja utilizada para mitigar a possibilidade de dano. Nesse sentido, o uso combinado de ELISA e NAT, aliado à educação dos doadores e ao fortalecimento dos sistemas de hemovigilância, constitui a estratégia mais robusta atualmente reconhecida pela OMS e pela European Directorate for the Quality of Medicines & HealthCare (EDQM, 2023). Assim, mesmo diante da impossibilidade de eliminar completamente o risco transfusional, é eticamente imperativo reduzi-lo ao limite tecnicamente atingível (Gonçalves et al., 2021).
2.1.2 Evolução dos testes de triagem: da sorologia convencional aos testes moleculares
A triagem laboratorial de doadores de sangue constitui a principal barreira preventiva contra a transmissão de doenças infecciosas em hemoterapia. Sua evolução reflete o progresso científico e tecnológico da medicina transfusional, desde os primeiros testes sorológicos rudimentares até a introdução dos métodos moleculares de alta sensibilidade. Segundo a OMS (2023), a triagem adequada é responsável por reduzir em mais de 99% os riscos de transmissão de HIV, HBV e HCV em sistemas transfusionais consolidados, configurando-se como pilar de biossegurança global.
A sorologia convencional representou, por décadas, o eixo central da triagem. Baseada inicialmente na detecção de anticorpos específicos gerados pelo hospedeiro após a infecção, ela permitiu, a partir da década de 1970, o controle epidemiológico das principais infecções virais. Os primeiros ensaios, contudo, apresentavam baixa sensibilidade e longa janela imunológica, o que resultava em um risco transfusional ainda significativo (Oliveira et al., 2017). A introdução do ELISA (Enzyme-Linked Immunosorbent Assay) na década de 1980 revolucionou a detecção de anticorpos anti-HIV, sendo posteriormente adaptado para HBV e HCV. O ELISA de terceira geração elevou a sensibilidade para acima de 99%, e a quarta geração, ao detectar simultaneamente o antígeno p24 e o anticorpo anti-HIV, reduziu a janela imunológica média para 16 a 18 dias (Paiva et al., 2019).
Apesar dessa evolução, a dependência da resposta imunológica do hospedeiro constitui a limitação estrutural dos métodos sorológicos. Durante o período de janela imunológica — intervalo entre a infecção e a detecção laboratorial dos marcadores — o sangue pode ser erroneamente classificado como não reagente. Essa limitação, descrita no Manual Técnico de Hemoterapia do Ministério da Saúde (Brasil, 2014), manteve um risco residual estimado de 1:2.000.000 para HIV e 1:800.000 para HCV mesmo em sistemas com testagem de alta qualidade.
O advento da biologia molecular nos anos 1990 introduziu um novo paradigma na triagem transfusional: a detecção direta do material genético viral. O Teste de Ácido Nucleico (Nucleic Acid Test – NAT) tornou-se referência ao identificar o RNA ou DNA viral antes da resposta imunológica do organismo, permitindo o diagnóstico de infecções nas fases mais precoces. Estudos multicêntricos, como o REDS-III (Recipient Epidemiology and Donor Evaluation Study, 2020), mostraram que a implantação do NAT reduziu em até 92% o risco residual de HIV e HCV em sistemas de triagem com amostras individuais (ID-NAT) (Paiva et al., 2019).
Os ganhos quantitativos com a adoção do NAT são expressivos: a janela imunológica média caiu para 9–11 dias para HIV, 7–10 dias para HCV e 20–30 dias para HBV, conforme Gonçalves et al. (2021) e Schmidt et al. (2021). Tais reduções modificaram o padrão de rastreabilidade global, tornando a dupla triagem (ELISA + NAT) a estratégia de segurança mais recomendada por organismos internacionais (EDQM, 2023; WHO, 2023). Além de detectar infecções agudas, o NAT identifica casos de infecção oculta por HBV (OBI – Occult Hepatitis B Infection), frequentemente indetectáveis por sorologia isolada.
A incorporação tecnológica, contudo, enfrenta assimetrias regionais. Em países de alta renda, o NAT tornou-se rotina em plataformas automatizadas como Procleix Panther® (Grifols) e COBAS 6800/8800 (Roche Molecular Systems), que operam com alta capacidade analítica e rastreabilidade total. Em contrapartida, países de baixa e média renda ainda dependem quase exclusivamente da sorologia convencional, mantendo um risco transfusional até 30 vezes maior (Kleinman et al., 2019). A OMS (2023) classifica a universalização do NAT como meta estratégica de equidade em saúde global.
O Brasil, ao implementar oficialmente o NAT em 2012 por meio da Rede Nacional de Triagem NAT (RNTNAT), tornou-se referência entre os países emergentes. Essa rede, composta por nove laboratórios centrais, processa milhões de amostras anualmente com metodologia minipool de seis amostras, alcançando cobertura superior a 90% dos hemocentros públicos (Ministério da Saúde, 2022). Os dados nacionais indicam uma redução superior a 80% nos casos de detecção tardia de HCV e HBV após a adoção do NAT, consolidando o país como líder latino-americano em biossegurança transfusional (Gonçalves et al., 2021).
A introdução do NAT não substituiu a sorologia, mas estabeleceu um modelo complementar e sinérgico. Enquanto a sorologia fornece dados epidemiológicos e identifica infecções crônicas, o NAT amplia a detecção de infecções agudas, reduzindo o risco residual e melhorando a vigilância ativa. Essa estratégia combinada, também chamada de dupla triagem, é reconhecida pela OMS e pelo EDQM (2023) como o padrão ouro para sistemas nacionais de sangue. Gonçalves et al. (2021) reforçam que sua aplicação contribui para a rastreabilidade total e para a confiança pública na doação.
Paralelamente ao NAT, novas tecnologias emergem como potenciais substitutas ou complementares. A PCR digital (dPCR), com detecção de cópias únicas de ácidos nucleicos, e os sistemas baseados em CRISPR-Cas12/13, capazes de reconhecimento ultrassensível e resposta colorimétrica imediata, vêm sendo testados em protótipos para triagem em larga escala (Khan et al., 2022). Pesquisas recentes apontam para o NAT multiplex, que permite detectar múltiplos patógenos em um único ensaio, reduzindo tempo e custo (Lelie et al., 2023).
Por outro lado, em cenários emergenciais ou de baixa infraestrutura, ainda se recorre aos testes rápidos (RTs), que oferecem resultados imediatos, mas com sensibilidade inferior. A OMS recomenda seu uso apenas quando métodos laboratoriais convencionais não estão disponíveis, pois os RTs apresentam taxas de falso-negativo entre 2 e 8%, o que pode comprometer a segurança transfusional (World Health Organization, 2021).
A evolução da triagem transfusional demonstra a transição de um modelo reativo — baseado na resposta imunológica — para um modelo proativo e preditivo, centrado na detecção direta do agente infeccioso e na integração de dados epidemiológicos. Embora o risco zero permaneça inatingível, a conjugação de sorologia de alta sensibilidade e biologia molecular de última geração representa, atualmente, o paradigma máximo de biossegurança transfusional, integrando precisão diagnóstica, eficiência operacional e justiça sanitária (Cunha et al., 2020; WHO, 2023).
2.2 Princípios bioquímicos do ELISA: ligação antígeno-anticorpo, uso de enzimas
O ensaio imunoenzimático ELISA (Enzyme-Linked Immunosorbent Assay) é fundamentado na interação altamente específica entre antígenos e anticorpos, cuja estabilidade é mediada por forças não covalentes, incluindo ligações de hidrogênio, interações eletrostáticas, forças de Van der Waals e efeitos hidrofóbicos. Essa combinação de forças confere ao complexo imunológico uma elevada especificidade e baixa constante de dissociação (Kd), sendo a base da alta precisão analítica do método (Santos et al., 2018). O princípio essencial do ELISA reside na utilização de uma enzima como marcador conjugado ao anticorpo ou antígeno, capaz de gerar um sinal cromogênico proporcional à quantidade de analito presente. Assim, a intensidade do produto colorimétrico é diretamente correlacionada à concentração do antígeno ou anticorpo de interesse (Garcia et al., 2020).
A fase sólida é geralmente composta por placas de microtitulação de poliestireno tratadas, que permitem a adsorção passiva de proteínas, estabelecendo uma matriz estável para a reação imunológica subsequente. A eficiência dessa imobilização depende de variáveis físico- químicas como o pH, a força iônica e a hidrofobicidade da superfície, que influenciam a orientação das moléculas e a disponibilidade dos epítopos de ligação (Rodrigues et al., 2020). O modelo de ligação “chave–fechadura”, proposto originalmente por Fischer, descreve a complementaridade geométrica entre antígeno e anticorpo, na qual pequenas variações conformacionais podem reduzir significativamente a afinidade da ligação. O controle rigoroso dessas condições é essencial para minimizar reações inespecíficas e maximizar a sensibilidade do ensaio.
No ELISA, a interação imunológica ocorre em três fases principais: I. Imobilização do antígeno ou anticorpo na placa; II. Formação do complexo antígeno–anticorpo após a adição da amostra; e III. Amplificação do sinal por meio da reação enzimática. As enzimas mais utilizadas incluem a peroxidase de rábano (HRP) e a fosfatase alcalina (AP), devido à sua elevada estabilidade catalítica e fácil conjugação a proteínas. A HRP é preferida por sua alta eficiência catalítica (kcat ≈ 10⁶ s⁻¹) e capacidade de amplificação rápida, enquanto a AP é mais estável a variações de pH e temperatura, sendo indicada para matrizes complexas (Ferreira et al., 2015; Silva et al., 2021).
O substrato cromogênico mais comumente utilizado para HRP é o 3,3’,5,5’- tetrametilbenzidina (TMB), que, após oxidação, produz coloração azul e, com a adição de ácido sulfúrico, torna-se amarela, sendo detectada por espectrofotometria a 450 nm. A intensidade óptica obtida é proporcional à concentração do analito, possibilitando quantificação precisa e reprodutível (Garcia et al., 2020). Essa reação segue cinética de primeira ordem até o esgotamento do substrato, sendo o ponto de leitura cuidadosamente padronizado para garantir linearidade analítica e comparabilidade interlaboratorial.
Do ponto de vista termodinâmico, o equilíbrio entre afinidade e avidez é determinante para o desempenho do ensaio. A afinidade representa a força de ligação entre um sítio de ligação de anticorpo e seu epítopo, enquanto a avidez corresponde à força cumulativa de múltiplas interações simultâneas. Ensaios com alta afinidade (Ka > 10⁹ L·mol⁻¹) são capazes de detectar antígenos em concentrações na faixa de picogramas por mililitro, o que é essencial em estágios precoces de infecção, antes da soroconversão completa (WHO, 2021).
A precisão do ELISA também depende das constantes cinéticas de associação (Ka) e dissociação (Kd). Ensaios mal otimizados, com valores de Kd elevados (>10⁻⁷ mol·L⁻¹), podem resultar em falsos-negativos devido à dissociação prematura dos complexos durante as etapas de lavagem. Em contrapartida, concentrações elevadas de proteínas de fundo, como albumina ou imunoglobulinas não específicas, podem induzir ligações inespecíficas e gerar falsos- positivos (Reis et al., 2019). O uso de bloqueadores proteicos, como albumina sérica bovina (BSA) ou caseína, é fundamental para minimizar essas interferências.
A estrutura do ensaio ELISA pode assumir diferentes formatos: direto, indireto, sandwich e competitivo, cada qual otimizado para determinado tipo de analito. Na triagem transfusional, predominam os formatos indireto e sandwich, que permitem a detecção de anticorpos e antígenos com elevada sensibilidade. Os ensaios de quarta geração, que detectam simultaneamente o antígeno p24 do HIV e os anticorpos anti-HIV, reduziram a janela imunológica média de 45 para 18 dias, contribuindo de forma decisiva para a segurança transfusional (Tang et al., 2020).
Do ponto de vista bioquímico, a escolha da enzima conjugada influencia não apenas a sensibilidade, mas também a estabilidade operacional do ensaio. A HRP é inibida por compostos fenólicos e detergentes não iônicos, enquanto a AP apresenta maior tolerância a inibidores endógenos. Avanços recentes incluem a utilização de enzimas recombinantes com engenharia de estabilidade térmica, como a HRP mutante E97D, que mantém atividade catalítica em temperaturas superiores a 50 °C, ampliando a aplicabilidade do ELISA em ambientes tropicais e laboratórios com recursos limitados (Huang et al., 2022).
A robustez e a adaptabilidade do ELISA consolidaram-no como o método de triagem padrão-ouro durante décadas em bancos de sangue de todo o mundo. Contudo, sua dependência da resposta imune do doador limita a capacidade de detecção nas fases iniciais da infecção — lacuna que foi suprida pela introdução de testes moleculares como o NAT. Estudos comparativos demonstram que o ELISA de quarta geração combinado ao NAT reduz o risco residual de HIV e HCV para menos de 1 caso por 3 milhões de doações, o que reforça o papel do ELISA como componente complementar essencial do sistema de dupla triagem (Gonçalves et al., 2021; Schmidt et al., 2021).
O avanço recente da biotecnologia também impulsionou o desenvolvimento de anticorpos recombinantes e fragmentos de anticorpos (Fab, scFv, nanocorpos) aplicados em ELISAs de nova geração. Essas moléculas oferecem maior especificidade, estabilidade e menor custo de produção, viabilizando plataformas automatizadas e portáteis para triagem de larga escala. A aplicação de anticorpos recombinantes na hemoterapia tem mostrado resultados promissores, com sensibilidade superior a 99,8% e estabilidade aumentada em 40% em relação aos anticorpos monoclonais convencionais (Vox Sanguinis, 2022; Müller et al., 2023).
Assim, o ELISA mantém-se como uma ferramenta indispensável na triagem transfusional, combinando fundamentos bioquímicos sólidos, alta sensibilidade e flexibilidade metodológica. Embora tecnologias moleculares avancem, a simplicidade, a padronização interlaboratorial e a capacidade de automação do ELISA garantem sua relevância contínua como componente crítico na vigilância transfusional e no controle de infecções emergentes.
2.2.1 Variedades técnicas: direto, indireto, competitivo e sanduíche
O Enzyme-Linked Immunosorbent Assay (ELISA) constitui uma das metodologias imunodiagnósticas mais versáteis e adaptáveis da biotecnologia diagnóstica moderna. Suas variedades técnicas — direto, indireto, sanduíche e competitivo — derivam de modificações estruturais no arranjo antígeno–anticorpo e na forma de amplificação enzimática, o que determina diferenças em sensibilidade, especificidade, custo e aplicabilidade clínica (Rodrigues et al., 2020). A escolha do formato adequado depende do tipo de biomolécula a ser detectada, da fase infecciosa, do volume amostral disponível e do objetivo diagnóstico (Garcia et al., 2020).
O ELISA direto é o formato mais simples e rápido. Nesse arranjo, o antígeno é adsorvido diretamente à fase sólida, e a detecção ocorre pela adição de um anticorpo conjugado a uma enzima (geralmente HRP ou fosfatase alcalina). Essa abordagem minimiza etapas intermediárias, reduz o tempo total de análise e o risco de erro por manipulação. No entanto, apresenta baixa amplificação de sinal e menor sensibilidade, pois apenas um conjugado enzimático atua por sítio de ligação. Por essa razão, é indicado principalmente para antígenos de alta abundância, como proteínas estruturais purificadas ou ensaios de controle de qualidade, mas tem uso limitado em triagem transfusional, onde a detecção de traços virais é crítica (Ferreira et al., 2015).
O ELISA indireto, por outro lado, introduz um anticorpo primário não conjugado que reconhece o antígeno fixado e um anticorpo secundário conjugado à enzima que se liga à região Fc do primário. Esse duplo reconhecimento gera amplificação exponencial do sinal, pois múltiplos anticorpos secundários podem se ligar a cada anticorpo primário, aumentando a sensibilidade em até 10 vezes em comparação ao formato direto (Santos et al., 2018). Essa configuração é amplamente utilizada na triagem de anticorpos anti-HIV, anti-HCV e anti- HTLV, sendo considerada a mais adequada para detecção de infecções crônicas, quando os anticorpos estão plenamente desenvolvidos. Além disso, apresenta excelente reprodutibilidade interlaboratorial, fator essencial em bancos de sangue de grande escala (WHO, 2021).
O ELISA sanduíche é reconhecido como o formato de maior sensibilidade e especificidade entre as variantes. Nesse modelo, um anticorpo de captura é imobilizado na placa e se liga ao antígeno da amostra; em seguida, um segundo anticorpo de detecção, que reconhece um epítopo distinto do mesmo antígeno, é adicionado. A ligação sequencial de dois anticorpos a epítopos diferentes aumenta drasticamente a especificidade, minimizando reações cruzadas. Após a adição do conjugado enzimático, a reação cromogênica revela a concentração do analito. Esse formato é amplamente empregado na detecção de antígenos virais, como HBsAg e p24 do HIV, apresentando sensibilidade superior a 99,9% e limite de detecção de até 0,05 ng/mL, o que o torna o padrão-ouro para a triagem de HBV e HIV (Garcia et al., 2020; Transfusion, 2023).
O ELISA competitivo apresenta configuração conceitualmente oposta. Nesse formato, o antígeno da amostra compete com um antígeno imobilizado pela ligação a um anticorpo limitado. Assim, quanto maior a concentração de antígeno livre na amostra, menor a intensidade do sinal cromogênico obtido. Esse formato é particularmente útil para antígenos de pequeno peso molecular (hormônios, drogas, toxinas), que possuem apenas um epítopo e não permitem ligação simultânea de dois anticorpos (Reis et al., 2019). Embora apresente menor sensibilidade (85–90%) em contextos virais, seu princípio competitivo é de extrema importância para ensaios quantitativos e controle de pureza de antígenos em estudos de padronização.
A comparação entre os formatos revela que a escolha deve equilibrar sensibilidade e praticidade. O formato indireto é ideal para triagem de anticorpos em larga escala, combinando alta sensibilidade (≥99,5%) e custo reduzido; o formato sanduíche oferece o melhor desempenho para antígenos, porém exige reagentes purificados e maior grau de automação; o competitivo, embora menos sensível, é insubstituível para moléculas pequenas ou haptenos (Silva et al., 2021; Transfusion, 2023). Ensaios comparativos multicêntricos relatados pela Vox Sanguinis (2022) demonstraram que, na triagem de sangue, o formato sanduíche apresenta especificidade diagnóstica de 99,98%, superando o indireto (99,7%) e o direto (97,5%).
Além do desempenho analítico, o formato selecionado impacta os custos operacionais, tempo de processamento e automação. O ELISA direto e o indireto podem ser executados manualmente em laboratórios de pequeno porte, enquanto o sanduíche e o competitivo, para garantir robustez e reprodutibilidade, requerem plataformas automatizadas (como ELx808™ ou Triturus®) e controles de qualidade internos calibrados. O aumento do custo inicial é compensado por maior confiabilidade diagnóstica e redução de falsos resultados (Ferreira et al., 2020; EDQM, 2023).
Avanços recentes em engenharia de proteínas e nanotecnologia diagnóstica vêm modificando a arquitetura de todos os formatos do ELISA. O uso de anticorpos recombinantes e nanocorpos (VHH) proporciona estabilidade térmica e menor custo de produção, além de reduzir o tempo de ligação antígeno–anticorpo (Müller et al., 2023). A incorporação de sistemas microfluídicos e sensores ópticos permite a miniaturização dos ensaios, viabilizando versões point-of-care (POC) do ELISA sanduíche, que podem detectar antígenos de HIV e HBsAg em menos de 15 minutos, com sensibilidade comparável à de sistemas laboratoriais convencionais (Vox Sanguinis, 2022; Huang et al., 2022).
O cenário atual, portanto, mostra que a evolução das variedades técnicas do ELISA reflete um equilíbrio entre inovação, aplicabilidade e custo-benefício. A tendência global é a convergência entre automação laboratorial, engenharia molecular e diagnóstico portátil, integrando biossensores e nanotecnologia aos formatos clássicos. Essa transformação consolida o ELISA não apenas como um método tradicional, mas como uma plataforma em constante reinvenção, crucial para a segurança transfusional e vigilância epidemiológica global.
2.2.2 Aplicações na triagem de sangue: detecção de material genético de HIV, HBV, HCV
A aplicação do método ELISA (Enzyme-Linked Immunosorbent Assay) na triagem de doadores de sangue consolidou-se como um dos pilares da biossegurança transfusional global. Utilizado para a detecção de marcadores sorológicos de infecções transmissíveis pelo sangue — como HIV, HBV, HCV, HTLV-I/II, sífilis e Trypanosoma cruzi — o ELISA mantém-se como ferramenta indispensável devido à sua combinação de alta sensibilidade, especificidade, escalabilidade e custo-efetividade (WHO, 2023). Em mais de 160 países, ele constitui o método primário de triagem obrigatória para doações de sangue total e hemocomponentes.
A principal vantagem operacional do ELISA na triagem é sua capacidade de identificar infecções silenciosas em doadores assintomáticos, frequentemente em fase de latência clínica. Isso é particularmente relevante em contextos endêmicos, como na América Latina, onde o uso de ensaios de segunda e terceira geração para Trypanosoma cruzi reduziu em mais de 90% os casos de doença de Chagas transfusional, segundo levantamento multicêntrico da OMS (Sabino et al., 2013). A triagem sorológica ampla permite, assim, interromper cadeias de transmissão subclínicas que seriam invisíveis na triagem clínica tradicional.
No contexto da infecção por HIV, o avanço dos testes ELISA de quarta geração — que detectam simultaneamente o antígeno p24 e os anticorpos anti-HIV-1/2 — foi determinante para reduzir a janela imunológica e aumentar a precocidade diagnóstica. Relatórios dos Centers for Disease Control and Prevention (CDC, 2019) indicam que o período médio de detecção caiu de 22 para 16 dias, diminuindo substancialmente o risco residual de transmissão. Essa redução é particularmente relevante em países que ainda não possuem cobertura universal de testes moleculares (NAT), tornando o ELISA o eixo principal de defesa contra o HIV em bancos de sangue (Garcia et al., 2020).
Na triagem de hepatite C (HCV), o ELISA representa o método de escolha desde a década de 1990. Os anticorpos anti-HCV tornam-se detectáveis em média 60–70 dias após a infecção inicial. Contudo, o avanço para os ensaios de terceira e quarta geração — que utilizam antígenos recombinantes de múltiplas regiões virais (Core, NS3, NS4 e NS5) — reduziu a janela imunológica para 30–40 dias, com sensibilidade superior a 99,5% e especificidade acima de 99,8%, segundo dados da Transfusion (2022). Esse desempenho é essencial para a triagem de populações em que a prevalência de HCV pode superar 1% dos doadores, como ocorre em algumas regiões do Sudeste Asiático e da América do Sul.
A triagem para hepatite B (HBV) baseia-se principalmente na detecção do antígeno de superfície HBsAg, marcador presente tanto em infecções agudas quanto crônicas. O formato ELISA tipo sanduíche permite detectar concentrações de HBsAg tão baixas quanto 0,05–0,1 ng/mL, o que garante alta sensibilidade diagnóstica. No entanto, cerca de 10% dos portadores apresentam infecção oculta (OBI – Occult Hepatitis B Infection), na qual o HBsAg está ausente. Para esses casos, a triagem é complementada pela detecção de anticorpos anti-HBc, ampliando a segurança transfusional (Makvandi, 2016). Estudos brasileiros mostram que a adoção desse modelo combinatório reduziu em até 60% os casos de OBI não detectados em bancos de sangue públicos (Ministério da Saúde, 2022).
Além de HIV, HBV e HCV, o ELISA é amplamente empregado na triagem de HTLV- I/II, retrovírus associados à paraparesia espástica tropical e leucemia de células T. Embora a prevalência global seja inferior a 0,1%, o risco de transmissão por transfusão é significativo em regiões endêmicas como o Caribe, o Japão e o Norte do Brasil (Reis et al., 2019). Por isso, a triagem obrigatória para HTLV-I/II é recomendada pela OMS desde 2015 e faz parte da legislação sanitária brasileira (ANVISA, RDC 34/2014).
No caso da sífilis, o ELISA treponêmico tem substituído métodos manuais como o VDRL em diversos países, sendo utilizado como teste confirmatório devido à sua alta sensibilidade (≥99%) e especificidade (≥98%). Da mesma forma, o ELISA para Trypanosoma cruzi continua sendo a ferramenta mais confiável para triagem em áreas endêmicas, garantindo cobertura diagnóstica onde testes moleculares ainda não são economicamente viáveis (WHO, 2023).
A aplicabilidade do ELISA na triagem transfusional ultrapassa a mera detecção laboratorial: ele está inserido em sistemas automatizados de alta capacidade que garantem rastreabilidade completa e integração digital. Grandes hemocentros brasileiros, como a Fundação Pró-Sangue, o HEMORIO e o HEMOPE, processam entre 2.000 e 5.000 amostras diárias utilizando plataformas automatizadas (p. ex., Triturus®, EVOLIS™, e Chorus TRIO™), com taxa de reprodutibilidade superior a 99,9% (Moraes et al., 2017). Esses sistemas permitem emissão eletrônica de laudos, arquivamento de resultados e rastreamento integral das unidades doadas.
O custo-efetividade do ELISA é outro fator de destaque. Em bancos de sangue de médio porte, o custo médio por amostra triada varia entre US$ 1,20 e US$ 2,50, valor até 15 vezes inferior ao de métodos moleculares. O tempo médio de execução é de 2 a 3 horas por microplaca, permitindo alto rendimento operacional com infraestrutura relativamente simples. Essa relação entre eficiência técnica e viabilidade econômica faz do ELISA a ferramenta mais acessível para países de baixa e média renda (Tagny et al., 2020).
Apesar de seu desempenho excepcional, o ELISA não é infalível. A acurácia pode ser afetada por fatores pré-analíticos, como hemólise, armazenamento inadequado ou calibração incorreta dos kits (Tahir et al., 2022). Além disso, por depender da resposta imune do hospedeiro, o método não elimina completamente o risco de transmissão durante a janela imunológica. Por esse motivo, os programas nacionais mais avançados adotam estratégias de dupla triagem (ELISA + NAT), combinando a sensibilidade imunológica do ELISA com a detecção direta de RNA/DNA viral pelo NAT, o que reduz o risco residual de HIV e HCV para menos de 1 caso por 3 milhões de doações (Vox Sanguinis, 2022; Schmidt et al., 2021).
Em síntese, o ELISA continua sendo o eixo estrutural da triagem transfusional, sustentando programas de hemovigilância, controle de qualidade e biossegurança em todo o mundo. Sua combinação de acessibilidade, precisão e compatibilidade com automação o torna não apenas uma tecnologia consolidada, mas uma ferramenta em constante evolução, cuja relevância persiste mesmo na era dos testes moleculares e do diagnóstico digital integrado.
2.2.3 Vantagens técnicas e operacionais
O Enzyme-Linked Immunosorbent Assay (ELISA) mantém-se como o método mais amplamente utilizado na triagem de doadores de sangue devido à sua combinação de elevada sensibilidade, especificidade analítica, confiabilidade e custo-efetividade. Essa versatilidade garante seu papel central nos sistemas de saúde de países de baixa, média e alta renda, tornando- se um eixo estruturante da biossegurança transfusional global (WHO, 2023). Em um contexto em que tecnologias moleculares como o NAT ainda enfrentam barreiras econômicas e logísticas significativas, o ELISA se destaca pela relação equilibrada entre desempenho e viabilidade operacional (Crowther, 2009; Vox Sanguinis, 2022).
Uma das principais vantagens do ELISA é sua alta escalabilidade. O método permite tanto execuções manuais, em pequenos laboratórios, quanto a utilização de plataformas automatizadas capazes de processar até 10.000 amostras por dia em sistemas modulares com microplacas de 96 ou 384 poços (Gutiérrez et al., 2021). Essa adaptabilidade garante sua aplicabilidade em realidades heterogêneas — de hemocentros urbanos a unidades regionais — mantendo padrões uniformes de qualidade e reprodutibilidade. A estrutura modular também facilita a expansão progressiva conforme o aumento da demanda transfusional, sem a necessidade de substituição completa da infraestrutura.
Do ponto de vista bioquímico, o ELISA apresenta uma relação sinal-ruído altamente otimizada, o que lhe confere capacidade de detectar concentrações na faixa de picogramas por mililitro (10⁻¹² g/mL). Essa sensibilidade é especialmente crítica para a detecção de antígenos virais como o HBsAg e o p24 do HIV, em que o limite de detecção pode atingir 0,05 ng/mL com coeficiente de variação (CV) inferior a 5% (Garcia et al., 2020). Além disso, a relação linear entre densidade óptica e concentração do analito permite a quantificação confiável em sistemas automatizados, ampliando a robustez dos resultados e o controle estatístico dos lotes.
O padronismo metodológico internacional é outro diferencial decisivo. O ELISA segue protocolos universalmente aceitos que incluem as etapas sequenciais de adsorção, bloqueio, incubação, lavagem, detecção e leitura espectrofotométrica. Essa uniformidade facilita o treinamento técnico, reduz erros humanos e garante reprodutibilidade interlaboratorial superior a 99%, atendendo aos critérios de certificações como ISO 15189, College of American Pathologists (CAP) e Clinical Laboratory Improvement Amendments (CLIA) (Reis et al., 2019; EDQM, 2023). Essa padronização também permite comparabilidade entre estudos epidemiológicos e relatórios de diferentes países, fortalecendo a vigilância sanitária internacional.
A comparação entre os parâmetros técnicos de execução demonstra que, embora o ELISA apresente custo por amostra inferior, o NAT oferece vantagens operacionais significativas, especialmente no que se refere à redução do tempo médio de processamento e à eficiência diagnóstica em ambientes automatizados. Essa relação pode ser visualizada na Figura 1, que evidencia as diferenças entre ambos os métodos quanto ao custo operacional (USD) e ao tempo médio de execução (minutos). Observa-se que o ELISA mantém-se mais econômico, sendo ideal para hemocentros de menor porte, enquanto o NAT, apesar do investimento mais alto por amostra, proporciona maior produtividade e agilidade diagnóstica, características fundamentais em sistemas de triagem de alta demanda e em programas nacionais de segurança transfusional (Ferreira et al., 2020; Vox Sanguinis, 2022).
Figura 1 – Custo operacional e tempo médio de execução entre ELISA e NAT
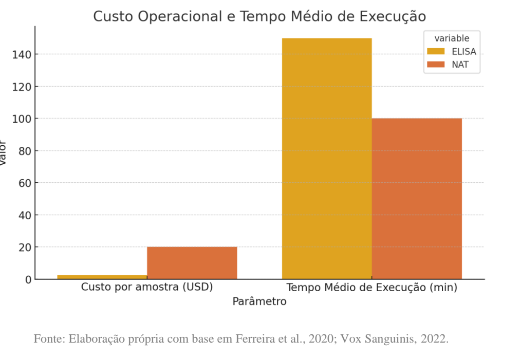
Observa-se na figura 1 que, embora o ELISA apresente custo por amostra mais baixo, o NAT reduz significativamente o tempo médio de execução, evidenciando maior eficiência operacional em ambientes automatizados de triagem molecular.
Do ponto de vista operacional, o ELISA destaca-se pela facilidade de integração a sistemas de informação laboratorial (LIS). Essa integração possibilita rastreamento completo da amostra — desde a coleta até a liberação do hemocomponente —, com registro automático de resultados, geração de alertas e auditoria em tempo real. Essa rastreabilidade atende às exigências da AABB (American Association of Blood Banks) e da OMS, que enfatizam a importância da interoperabilidade digital para garantir a segurança transfusional e a rastreabilidade de eventos adversos (World Health Organization, 2021). Hemocentros brasileiros como o HEMORIO e a Fundação Pró-Sangue já operam com integração plena entre plataformas de ELISA e sistemas de gestão laboratorial, reduzindo em até 30% o tempo médio de liberação dos resultados (Ferreira et al., 2020).
No aspecto econômico, o ELISA apresenta uma das melhores relações custo-benefício entre os métodos diagnósticos disponíveis. O custo médio por teste situa-se entre US$ 2,00 e US$ 3,50, enquanto o NAT pode ultrapassar US$ 18,00–25,00 por amostra, sem considerar os custos de calibração, manutenção e energia das plataformas moleculares (Vox Sanguinis, 2022; Mahmood et al., 2022). Essa diferença representa uma economia de mais de 85% por unidade testada, o que é decisivo para sistemas públicos de saúde de grande volume. Além disso, o ELISA requer menor consumo de reagentes e apresenta vida útil média dos kits de 12 a 18 meses, o que reduz perdas logísticas e facilita o planejamento de estoques.
A robustez ambiental do ELISA também merece destaque. O método é menos sensível a variações de temperatura e pH do que as técnicas moleculares, que exigem condições controladas de termo ciclagem e armazenamento de reagentes a -20 °C. Estudos recentes demonstram que kits de ELISA mantêm estabilidade de desempenho mesmo após exposição de 48 horas a 37 °C, o que é crucial para países de clima tropical (Mahmood et al., 2022). Essa tolerância operacional confere ao ELISA grande resiliência frente a falhas temporárias de energia, transporte prolongado de amostras ou condições laboratoriais ótimas.
Outro ponto-chave é a eficiência energética e sustentabilidade operacional. Com a incorporação de sistemas microfluídicos e plataformas automatizadas de nova geração, o consumo de reagentes foi reduzido em 40%, e o tempo médio de ensaio caiu para menos de 90 minutos (WHO, 2023). As novas versões do ELISA automatizado, como as baseadas em microchips de silício e sensores ópticos integrados, também diminuem o uso de água e plástico, alinhando-se às metas de sustentabilidade laboratorial e à Agenda 2030 da OMS (Vox Sanguinis, 2022).
Finalmente, o potencial evolutivo do ELISA reforça sua longevidade tecnológica. As versões de ELISA digital e microfluídico utilizam detecção fotoeletrônica e algoritmos de IA para análise automática dos espectros colorimétricos, aumentando a precisão diagnóstica e reduzindo a subjetividade na leitura. Ensaios desenvolvidos por Huang et al. (2022) mostraram que essas plataformas híbridas reduzem em 60% o tempo de processamento, mantendo sensibilidade ≥99,9% e reduzindo o consumo energético em 45%. Esses avanços indicam que o ELISA continuará sendo não apenas uma técnica consolidada, mas uma plataforma diagnóstica em evolução contínua, compatível com os princípios de eficiência, rastreabilidade e sustentabilidade que norteiam a medicina transfusional moderna.
2.2.4 Limitações analíticas e operacionais do ELISA
Apesar de sua reconhecida robustez técnica e papel histórico na triagem transfusional, o Enzyme-Linked Immunosorbent Assay (ELISA) apresenta limitações analíticas e operacionais que impactam diretamente sua sensibilidade em fases precoces da infecção e sua aplicabilidade universal em ambientes de infraestrutura limitada. A limitação mais relevante, sob o ponto de vista bioquímico, é a dependência da resposta imune do hospedeiro. A detecção baseia-se na presença de anticorpos ou antígenos em concentrações detectáveis, o que não ocorre durante o período inicial de infecção — a chamada janela imunológica (Schmidt et al., 2021). Durante essa fase, o hospedeiro ainda não produziu resposta humoral mensurável, o que permite que unidades infectadas sejam erroneamente classificadas como não reativas.
A janela imunológica varia conforme o patógeno. Mesmo com o uso de ELISA de quarta geração, que combina detecção de antígeno p24 e anticorpos anti-HIV, a janela média permanece entre 16 e 20 dias para o HIV; no caso do HBV, ela pode variar entre 38 e 60 dias, e para o HCV, entre 45 e 70 dias, dependendo da carga viral e da imunocompetência do doador (Garcia et al., 2020; WHO, 2023). Essa lacuna temporal é uma das principais causas do risco residual transfusional, estimado em 1:2.000.000 para HIV e 1:1.000.000 para HCV em países com triagem exclusivamente sorológica. Por isso, a OMS e a EDQM recomendam que o ELISA seja complementado por testes moleculares como o NAT, capazes de detectar o RNA/DNA viral antes da resposta imune (EDQM, 2023).
Outro problema recorrente é a reatividade cruzada, fenômeno no qual anticorpos gerados contra um agente infeccioso reconhecem epítopos similares presentes em antígenos de outros patógenos. Essa limitação leva à ocorrência de falsos positivos, especialmente em regiões tropicais com alta circulação de arbovírus (Zika, Dengue, Chikungunya), cujas proteínas estruturais compartilham epítopos semelhantes com os antígenos utilizados nos ensaios para HIV e HCV (Silva et al., 2021). Estudos conduzidos por Kashiwagi et al. (2015) mostram que a taxa de reatividade cruzada pode chegar a 4–6% em populações com coinfecções múltiplas. Além disso, a presença de autoanticorpos (como fator reumatoide ou anticorpos antinucleares) e interferências físico-químicas (hemólise, lipemia, contaminação bacteriana) pode distorcer os resultados, gerando interpretações falso-reativas.
Em contrapartida, falsos negativos podem ocorrer devido a mutações virais que alteram epítopos de reconhecimento. No caso do HIV, mutações na região gp41 já foram associadas à perda de reatividade em determinados kits comerciais (Silva et al., 2020). Para o HCV, variantes das regiões NS3 e NS5B têm demonstrado escape parcial de detecção, com sensibilidade reduzida em até 3% dos casos de genótipos 4 e 6 (Maunder et al., 2021). Esse fenômeno reforça a necessidade de atualização constante dos antígenos recombinantes utilizados nos kits, acompanhando a evolução molecular dos patógenos circulantes.
Nos ambientes de alta endemicidade, como em áreas com alta prevalência de HTLV- I/II ou Trypanosoma cruzi, a especificidade diagnóstica do ELISA pode diminuir de 99,8% para até 96%, devido à presença de anticorpos heterólogos contra antígenos parasitários semelhantes. Essa situação aumenta o número de resultados inconclusivos e demanda testes confirmatórios (Western Blot, Line Immunoassay), que são de custo elevado e nem sempre disponíveis em hemocentros regionais (Silva et al., 2020). Isso gera impactos diretos na eficiência dos fluxos transfusionais, uma vez que amostras reativas falsas retêm bolsas que poderiam ser liberadas com segurança.
As limitações operacionais também são relevantes. O ELISA envolve múltiplas etapas (lavagem, incubação, adição de substrato, leitura), cada uma suscetível a erros de manipulação, especialmente em sistemas semiautomatizados. Estudos de Echevarría et al. (2019) indicam que falhas de pipetagem e lavagem insuficiente respondem por até 15% das variações intraensaio, afetando diretamente a sensibilidade e reprodutibilidade. Em laboratórios de menor porte, essas falhas podem levar à necessidade de repetição de testes, aumentando o tempo de liberação dos resultados e os custos operacionais.
O tempo total de análise constitui outro gargalo prático. Mesmo em sistemas automatizados, o ciclo analítico completo do ELISA dura entre 2 e 4 horas, incluindo incubação e leitura. Em situações de emergência transfusional, esse intervalo pode ser inadequado. Além disso, em sistemas sem automação total, a leitura visual ou semiautomática dos resultados pode introduzir viés subjetivo na interpretação das absorbâncias (Mahmoud et al., 2022). Isso contrasta com métodos moleculares em tempo real, que, embora mais caros, podem entregar resultados em menos de 90 minutos com maior padronização analítica.
A variabilidade Inter lote dos kits comerciais representa outra limitação importante. Ferreira et al. (2020) demonstraram que a variação da sensibilidade entre fabricantes pode chegar a 5% para HBsAg e 4% para anti-HCV, o que exige procedimentos locais de validação interna e controle de qualidade antes da adoção de novos lotes. Esse processo aumenta o tempo de liberação e os custos laboratoriais, mas é essencial para assegurar confiabilidade dos resultados. Adicionalmente, nem todos os fabricantes atualizam prontamente seus reagentes frente a variantes emergentes, o que cria lacunas temporárias na vigilância diagnóstica.
O desempenho do ELISA também é influenciado por condições ambientais. Temperaturas superiores a 30 °C e alta umidade relativa reduzem a estabilidade das enzimas (como HRP e fosfatase alcalina) e degradam anticorpos de captura, especialmente em laboratórios sem controle climático adequado. A pureza da água usada nas lavagens e reagentes é igualmente crítica: condutividades superiores a 10 µS/cm estão associadas à formação de resíduos proteicos e aumento do fundo ótico, comprometendo a precisão do ensaio (Vox Sanguinis, 2022). Em regiões tropicais, essas limitações reduzem a aplicabilidade do ELISA em centros com infraestrutura mínima.
Por fim, embora o ELISA ofereça excelente desempenho em infecções crônicas, sua eficácia cai significativamente em infecções agudas e em portadores com baixa carga antigênica, como na infecção oculta pelo HBV (IOHB). Nesses casos, a ausência do HBsAg torna o ensaio ineficaz, demandando metodologias moleculares complementares. Estudos publicados pela Transfusion (2023) demonstram que a adição do NAT à rotina de triagem reduz o risco residual de transmissão do HBV em 97% e do HCV em 94%, consolidando o modelo de dupla triagem (ELISA + NAT) como o padrão internacional de ouro em segurança transfusional.
2.2.5 Comparações internacionais e dados epidemiológicos
A comparação internacional do desempenho do ELISA (Enzyme-Linked Immunosorbent Assay) na triagem de doadores de sangue evidencia um cenário heterogêneo, diretamente condicionado por fatores como infraestrutura laboratorial, prevalência regional de infecções transmissíveis, políticas de biossegurança e grau de integração de tecnologias complementares, como o Nucleic Acid Test (NAT). A Organização Mundial da Saúde (WHO, 2023) classifica os países em três níveis de maturidade transfusional: I. Sistemas com dupla triagem (ELISA + NAT); II. Sistemas com triagem sorológica isolada, e III. Sistemas mistos com uso intermitente de testes rápidos. Essa estratificação traduz desigualdades técnico- estruturais que se refletem diretamente no risco residual de transmissão.
Nos países de alta renda, como Alemanha, Japão, Estados Unidos, Canadá e França, a triagem combinada (ELISA + NAT) é padrão obrigatório desde os anos 2000. Esses sistemas atingem níveis de segurança transfusional próximos ao risco zero para HIV e HCV, com risco residual estimado em 1:1.900.000 e 1:2.600.000, respectivamente, segundo a Vox Sanguinis (2022). Para o HBV, o risco residual varia de 1:280.000 a 1:1.000.000, dependendo da inclusão de testes para anti-HBc e da cobertura do NAT (EDQM, 2023). A associação entre triagem sorológica e molecular reduziu as taxas de soroconversão pós-transfusional em mais de 95% entre 2000 e 2020 (Transfusion, 2023).
Em contraste, regiões de média e baixa renda, particularmente na África Subsaariana e no Sudeste Asiático, ainda dependem majoritariamente de métodos sorológicos convencionais. O relatório da WHO (2023) aponta que apenas 38% dos países africanos utilizam o NAT de forma rotineira, e 27% ainda recorrem a testes rápidos para triagem em campanhas locais. Essa limitação se traduz em riscos transfusionais residuais até 40 vezes superiores aos observados na Europa Ocidental. A prevalência média de HIV entre doadores africanos, por exemplo, permanece em torno de 0,4%, enquanto a de HCV ultrapassa 1%, contrastando com menos de 0,05% nos países europeus (Tagny et al., 2020).
Na Ásia, observa-se um panorama heterogêneo. Países como Japão, Coreia do Sul e Cingapura mantêm triagem molecular universal desde 2005, enquanto Indonésia, Vietnã e Filipinas ainda operam predominantemente com o ELISA convencional. O Centro Asiático de Vigilância Transfusional (Watanabe et al., 2021) recomenda a adoção gradual de modelos híbridos, combinando triagem sorológica universal com NAT em doações de maior risco epidemiológico, priorizando áreas urbanas e populações de alta mobilidade.
Na Índia, a implementação de ELISAs de quarta geração teve impacto mensurável na redução de infecções transfusionais. Dados de Kumar et al. (2022) indicam que a taxa de bolsas reagentes para HIV caiu de 0,46% para 0,17% entre 2010 e 2020, refletindo o efeito direto da atualização tecnológica. Entretanto, a ausência de testagem molecular nacional mantém o risco residual de HCV em aproximadamente 1:200.000 transfusões.
A América Latina apresenta um cenário intermediário. Brasil, Argentina, Chile e Uruguai adotaram o NAT em escala nacional, reduzindo o risco de transmissão de HIV e HCV para menos de 1 caso por 3 milhões de doações (Ministério da Saúde, 2023; Vox Sanguinis, 2022). No Brasil, dados oficiais indicam que, em 2023, mais de 90% das bolsas processadas pelo Sistema Único de Saúde (SUS) passaram por dupla triagem, resultado de uma política pública integrada de Hemorrede nacional. Em contrapartida, países com infraestrutura limitada, como Bolívia e Paraguai, ainda enfrentam risco residual 10 a 50 vezes superior ao europeu (Ferreira et al., 2020).
Em países africanos, a dependência exclusiva do ELISA continua a ser uma vulnerabilidade crítica. O estudo multicêntrico de Tagny et al. (2020), conduzido em 35 países da África Subsaariana, revelou que apenas 12% dos hemocentros dispunham de triagem molecular regular. A prevalência combinada de HIV, HBV e HCV em doadores variou entre 1,5% e 7,8%, com taxas de descarte de bolsas de sangue superiores a 1,5%, comparadas a menos de 0,1% na Europa Ocidental (Transfusion, 2023). Essa disparidade evidencia que o desempenho do ELISA é fortemente dependente da prevalência de base e da capacidade de confirmação diagnóstica local.
Do ponto de vista epidemiológico e econômico, a prevalência de agentes infecciosos afeta diretamente a eficiência do ELISA. Em áreas de alta endemicidade, o aumento no número de bolsas reagentes eleva o custo total da triagem — não apenas pelo uso de kits, mas pelo descarte de unidades, necessidade de reconfirmação e custos legais associados à transmissão acidental. Embora o custo direto do ELISA permaneça estável globalmente (US$ 2–5 por amostra), os custos indiretos são até cinco vezes maiores em países sem cobertura do NAT (Vox Sanguinis, 2022). Estudos de modelagem econômica da OMS (2023) demonstram que a introdução do NAT reduz em até 95% os casos de transmissão residual de HBV e HCV em países endêmicos, tornando a combinação sorológica-molecular mais custo-efetiva a médio prazo.
As comparações globais de descarte de bolsas ilustram o impacto da integração tecnológica: enquanto na Europa Ocidental o descarte por triagem sorológica é inferior a 0,1%, esse número atinge 0,7% na América Latina e 1,5% na África (Transfusion, 2023). Esse diferencial está fortemente correlacionado à densidade tecnológica por hemocentro, medida pela presença de automação, controles internos e políticas de qualificação de doadores. Assim, o desempenho do ELISA transcende o campo bioquímico e se converte em indicador indireto de governança e equidade diagnóstica.
Por fim, observa-se uma tendência global convergente: o ELISA permanece fundamental para a detecção de infecções em estágios estabelecidos, mas seu desempenho máximo é alcançado quando integrado a sistemas de triagem molecular e de hemovigilância digital. Países que adotaram essa integração reportam índices de segurança transfusional superiores a 99,9999%, consolidando o modelo híbrido ELISA + NAT como o padrão de excelência internacional (WHO, 2023; Transfusion, 2023). A harmonização de protocolos internacionais, aliada à capacitação técnica e ao fortalecimento das redes regionais de vigilância, é a estratégia mais promissora para reduzir as disparidades globais e garantir a segurança transfusional equitativa (van den Hurk et al., 2020).
2.2.6 Implicações clínicas e integração tecnológica
O Enzyme-Linked Immunosorbent Assay (ELISA), enquanto ferramenta de triagem transfusional, transcende sua função diagnóstica primária, configurando-se como instrumento essencial na prevenção de doenças infecciosas, no monitoramento epidemiológico e na gestão clínica dos doadores e receptores. Sua elevada sensibilidade e especificidade permitem a identificação precoce de agentes infecciosos, reduzindo significativamente a morbimortalidade associada às infecções transfusionais e fortalecendo a segurança do sangue em escala populacional (Dhingra et al., 2020; WHO, 2023).
Do ponto de vista clínico, um resultado reativo no ELISA desencadeia protocolos padronizados que envolvem ações imediatas e rastreáveis. Para o doador, o resultado positivo implica suspensão temporária ou definitiva da doação, avaliação clínica detalhada, aconselhamento psicológico e encaminhamento para tratamento. Para o receptor, o impacto é preventivo: a triagem impede a transfusão de unidades potencialmente contaminadas, evitando a transmissão de HIV, HBV, HCV e HTLV, com especial relevância para pacientes imunocomprometidos, neonatais e politransfundidos (Reis et al., 2019). Em muitos sistemas nacionais de sangue, como o brasileiro e o alemão, o ELISA é considerado o primeiro ponto de decisão clínica no ciclo transfusional (EDQM, 2023).
No âmbito da vigilância epidemiológica, os dados sorológicos obtidos a partir do ELISA são de valor inestimável. A consolidação das informações em sistemas nacionais permite identificar tendências temporais e geográficas de prevalência viral, avaliar surtos, monitorar mutações patogênicas e direcionar políticas públicas de prevenção. No Brasil, por exemplo, as notificações de reatividade em triagem sorológica alimentam o Sistema Nacional de Hemovigilância (NOTIVISA/ANVISA), que orienta ações de saúde coletiva e programas de triagem específica em populações de risco (Ferreira et al., 2020; Ministério da Saúde, 2023). Essa função dupla — diagnóstica e epidemiológica — torna o ELISA um elo entre o ato clínico individual e a saúde pública coletiva.
A integração tecnológica é um vetor essencial dessa transformação. A incorporação do ELISA em sistemas informatizados de gestão laboratorial (LIS) permite a automação do registro, análise e arquivamento de resultados, com rastreabilidade completa desde a coleta até a liberação da bolsa de sangue. Essa digitalização reduz erros humanos, acelera a liberação dos resultados e facilita auditorias de qualidade, sendo requisito para certificações como ISO 15189, CAP e AABB (Chen et al., 2022; WHO, 2021). Em hemocentros de grande porte, como a Fundação Pró-Sangue e o HEMORIO, a integração total entre ELISA e LIS reduziu em até 30% o tempo médio de resposta diagnóstica, ampliando a eficiência operacional.
As plataformas automatizadas de ELISA representam outro marco na evolução tecnológica. Equipamentos modernos, como o EVOLIS™ (Bio-Rad) e o Triturus® (Grifols), realizam automaticamente todas as etapas do ensaio — desde pipetagem, lavagem e incubação até leitura espectrofotométrica — com rastreabilidade em tempo real e conexão com sistemas de informação hospitalar. Esses sistemas processam até 5.000 amostras diárias, com coeficiente de variação inferior a 3% e reprodutibilidade interlote acima de 99,9% (Garcia et al., 2020; Vox Sanguinis, 2022). A automação total também facilita a adoção de painéis multiplex, capazes de detectar simultaneamente múltiplos patógenos (HIV, HBV, HCV, HTLV, sífilis e T. cruzi) em uma única reação.
O ELISA multiplex, uma evolução recente, utiliza microplacas funcionalizadas com múltiplos antígenos ou microesferas codificadas (bead-based assays), permitindo o rastreamento paralelo de até 10 marcadores em uma única amostra. Estudos conduzidos por Wong et al. (2023) demonstraram que o desempenho desses ensaios é comparável aos métodos individuais, com sensibilidade média de 99,7% e especificidade de 99,8%, reduzindo em 40% o tempo total de triagem. Essa tecnologia é particularmente valiosa em bancos de sangue de alto volume, onde a economia de reagentes e tempo representa ganho significativo de eficiência. Paralelamente, o avanço da microfluídica tem permitido a miniaturização dos sistemas ELISA, viabilizando a execução de ensaios completos em dispositivos do tamanho de um cartão. Tais plataformas — conhecidas como lab-on-a-chip — consomem volumes ínfimos de reagentes (microlitros) e oferecem resultados em menos de 30 minutos. Projetos-piloto realizados no Japão, Alemanha e Estados Unidos demonstram que os microELISAs podem atingir desempenho comparável ao dos sistemas convencionais, com redução de 70% no custo por teste e maior aplicabilidade em regiões remotas (Vox Sanguinis, 2022; Huang et al., 2022). A integração com inteligência artificial (IA) e aprendizado de máquina (machine learning) representa a nova fronteira do ELISA. Modelos de IA treinados com grandes bancos de dados de leituras espectrofotométricas são capazes de identificar padrões de falsos positivos/negativos, ajustar automaticamente pontos de corte e emitir alertas para repetição de amostras duvidosas. Ensaios automatizados com IA reduziram a taxa de erro humano em até 35% e melhoraram a acurácia diagnóstica global em 1,8%, segundo dados da Transfusion (2023). Essa integração confere ao ELISA uma dimensão preditiva e autônoma, transformando-o em ferramenta adaptativa de diagnóstico.
Os avanços na bioengenharia de antígenos e conjugação enzimática também estão ampliando a sensibilidade e a estabilidade dos ensaios. Novas gerações de anticorpos recombinantes e enzimas mutantes (como HRP termoestável e fosfatase alcalina recombinante) apresentam maior resistência a variações de pH e temperatura, reduzindo as perdas de atividade enzimática em até 40% em ambientes tropicais (Feng et al., 2022; EDQM, 2023). Essa evolução técnica aumenta a aplicabilidade do ELISA em laboratórios de recursos limitados e reforça seu papel como ferramenta de diagnóstico resiliente e sustentável.
Finalmente, a integração do ELISA com plataformas moleculares como o NAT consolidou um modelo híbrido de triagem que maximiza a segurança transfusional. Esse modelo combina a sensibilidade imunológica do ELISA — ideal para infecções crônicas — com a precocidade diagnóstica do NAT, que identifica infecções na janela imunológica. Essa estratégia reduziu o risco residual de HIV, HCV e HBV para menos de 1:3.000.000 transfusões, atingindo níveis de biossegurança comparáveis aos de países com as mais avançadas redes hemoterápicas (Garcia et al., 2020; WHO, 2023). Assim, o ELISA permanece não apenas como tecnologia consolidada, mas como componente-chave de um ecossistema diagnóstico integrado, em constante diálogo com as inovações da biotecnologia e da inteligência artificial.
2.3 Princípios do NAT: PCR (Reação em Cadeia da Polimerase), TMA (Amplificação Mediada por Transcrição)
O desenvolvimento do Teste de Ácido Nucleico (Nucleic Acid Test – NAT) representa um divisor de águas na triagem molecular de doadores de sangue, ao permitir a detecção direta do material genético viral (RNA ou DNA) antes da soroconversão. Diferentemente dos métodos sorológicos, o NAT identifica o patógeno em sua fase pré-imune, reduzindo drasticamente a janela imunológica e o risco residual de infecção transfusional. Entre as metodologias empregadas, destacam-se a Reação em Cadeia da Polimerase (PCR) e a Amplificação Mediada por Transcrição (TMA), que, embora compartilhem o princípio da amplificação exponencial de ácidos nucleicos, diferem em fundamentos enzimáticos, termodinâmica e aplicabilidade laboratorial (Niemz et al., 2011; WHO, 2023).
Desenvolvida por Kary Mullis em 1983, a PCR revolucionou a biologia molecular ao introduzir a amplificação in vitro de fragmentos específicos de DNA. O processo ocorre em ciclos térmicos sucessivos compostos por três etapas: (i) desnaturação do DNA (~95 °C), (ii) anelamento dos primers (50–65 °C) e (iii) extensão mediada por uma DNA polimerase termoestável, geralmente a Taq polimerase, a 72 °C. Cada ciclo duplica o número de cópias- alvo, resultando em amplificação exponencial com ganhos de até 10⁹ vezes após 30 ciclos (Ferreira et al., 2020).
A especificidade da PCR depende criticamente do desenho dos primers — curtos oligonucleotídeos complementares às extremidades da sequência-alvo. Regiões genômicas conservadas dos vírus HIV, HBV e HCV são selecionadas para evitar falhas de reconhecimento decorrentes de mutações. Contudo, variantes genéticas e recombinações podem afetar a eficiência de anelamento, exigindo o uso de múltiplos alvos ou primers degenerados (Reis et al., 2019).
A evolução da técnica resultou na PCR em tempo real (qPCR), que combina amplificação e detecção fluorescente simultânea, permitindo quantificação viral precisa e monitoramento de curvas de amplificação em tempo real. Na triagem transfusional, a qPCR detecta até 10–50 cópias/mL de DNA ou RNA viral, reduzindo a janela imunológica para 9–11 dias (HIV), 7–10 dias (HCV) e 20–30 dias (HBV), dependendo do protocolo e plataforma empregada (Silva et al., 2021; WHO, 2023). Além disso, sistemas de qPCR multiplex possibilitam a detecção simultânea de múltiplos patógenos, otimizando tempo e custo em triagens de alta demanda.
Por outro lado, a Amplificação Mediada por Transcrição (TMA), introduzida na década de 1990, constitui uma tecnologia isotérmica projetada para a detecção de vírus de RNA, como HIV e HCV. Diferentemente da PCR, a TMA ocorre a uma temperatura constante (41–42 °C), eliminando a necessidade de ciclos térmicos e reduzindo a complexidade operacional. A reação utiliza duas enzimas principais: uma transcriptase reversa, que converte o RNA viral em DNA complementar (cDNA), e uma RNA polimerase, que sintetiza múltiplas cópias de RNA a partir do cDNA, resultando em amplificação exponencial contínua (Garcia et al., 2020).
Bioquimicamente, a TMA oferece eficiência de amplificação 10–100 vezes superior à PCR para alvos de RNA, pois cada cópia gerada serve de molde para novas transcrições. Essa característica torna-a extremamente útil para vírus de genoma instável, permitindo detecção precoce e consistente mesmo em amostras de baixa integridade. A natureza isotérmica também reduz o tempo total de ensaio para <90 minutos e facilita a automação em plataformas de grande escala, como Procleix Panther® e Roche COBAS s 6800/8800, amplamente utilizadas em hemocentros de alta capacidade (Tang et al., 2017; Vox Sanguinis, 2022).
A TMA apresenta ainda menor suscetibilidade a inibidores endógenos (heparina, hemoglobina) e alto rendimento em matrizes biológicas complexas. Essa robustez operacional é determinante em ambientes com alto volume de triagem e amostras heterogêneas. Estudos comparativos demonstram sensibilidade de ≥99,99 % e especificidade de ≥99,98 %, com limite de detecção inferior a 10 cópias/mL para HIV e HCV (Stramer et al., 2013; Transfusion, 2023). A priori, tanto a PCR quanto a TMA dependem de extração de ácidos nucleicos altamente eficiente, etapa crítica para eliminar proteínas, lipídios e inibidores. Plataformas automatizadas modernas integram extração magnética, amplificação e detecção em um único sistema fechado, minimizando contaminações cruzadas. Os produtos amplificados são detectados por sinalização fluorescente, quimioluminescente ou eletroquímica, e os resultados são processados por softwares que realizam análise cinética e emissão automática de relatórios laboratoriais (Vox Sanguinis, 2022).
A posteriori, a escolha entre PCR e TMA depende do tipo de ácido nucleico-alvo, do custo, do tempo de resposta e da infraestrutura disponível. Em geral, a PCR é preferida em contextos clínicos e confirmatórios, especialmente quando a quantificação da carga viral é necessária, enquanto a TMA domina a triagem de rotina por oferecer maior escalabilidade e eficiência operacional (Espy et al., 2006; WHO, 2023).
Em suma, o uso do NAT reduziu de maneira mensurável os riscos transfusionais em todo o mundo. O Blood Systems Research Institute demonstrou que a implementação de NAT baseado em TMA diminuiu a janela de detecção do HIV em > 50 % em comparação ao ELISA de quarta geração, e reduziu o risco residual para <1:3.000.000 transfusões (Stramer et al., 2013). Contudo, a eficiência diagnóstica do NAT exige controle rigoroso de contaminação, calibração constante e atualizações periódicas dos primers e sondas frente às mutações emergentes. Estudos recentes destacam a necessidade de vigilância genômica integrada para adaptar rapidamente os kits de triagem às variantes virais emergentes (Kim et al., 2022; EDQM, 2023).
Portanto, a integração das tecnologias de PCR e TMA no NAT consolidou um novo paradigma de segurança transfusional, caracterizado pela detecção ultra-precoce, automação integral e rastreabilidade digital. O NAT complementa a triagem sorológica convencional, reduzindo o risco residual a níveis estatisticamente desprezíveis e promovendo a transição definitiva da hemoterapia sorológica para uma hemoterapia molecular, alinhada às metas da OMS para a cobertura universal de sangue seguro até 2030 (WHO, 2023; Vox Sanguinis, 2022).
2.3.1 Aplicações na triagem de sangue: detecção de material genético de HIV, HBV, HCV
A introdução do Teste de Ácido Nucleico (Nucleic Acid Test – NAT) na triagem de doadores de sangue revolucionou a segurança transfusional, ao permitir a detecção direta do material genético viral (RNA ou DNA), antecipando a identificação de infecções antes do aparecimento de marcadores imunológicos. Diferentemente dos testes sorológicos, que dependem da resposta imune do hospedeiro, o NAT atua durante a fase pré-sorológica, reduzindo drasticamente o risco de transmissão durante o período de janela imunológica (Garcia et al., 2020; WHO, 2023).
No contexto da triagem para HIV, o NAT tem papel crucial. Mesmo com os testes ELISA de quarta geração — que detectam simultaneamente o antígeno p24 e os anticorpos anti- HIV-1/2 —, a janela imunológica persiste em torno de 18 a 22 dias. O NAT, por sua vez, identifica o RNA viral entre 9 e 11 dias após a infecção, antecipando em cerca de 10 dias a detecção em relação à sorologia convencional. Essa diferença reduz o risco residual de transmissão para menos de 1:2.000.000 doações, conforme relatórios do Centers for Disease Control and Prevention (CDC, 2020) e da AABB (Busch & Kleinman, 2010). O impacto prático dessa redução é evidente: a triagem molecular evita aproximadamente 1 caso de transmissão por HIV a cada 12 milhões de doações nos sistemas transfusionais norte-americanos e europeus (Transfusion, 2023).
Para o vírus da hepatite C (HCV), o benefício do NAT é ainda mais expressivo. A janela sorológica — período entre a infecção e a detecção de anticorpos anti-HCV — pode alcançar 60–70 dias em indivíduos imunocompetentes. O NAT detecta o RNA do HCV em média 7 a 10 dias após a exposição, encurtando o período de risco em quase dois meses (Hollinger & Busch, 2000). Estudos multicêntricos indicam que, em países que utilizavam apenas triagem sorológica, até 10% dos casos de transmissão transfusional de HCV ocorriam durante a janela imunológica. A implementação do NAT praticamente eliminou essas ocorrências, tornando a transmissão de HCV por transfusão um evento excepcional (Vermeulen et al., 2021).
A triagem molecular para o vírus da hepatite B (HBV) apresenta desafios adicionais devido à dinâmica complexa dos marcadores sorológicos. O NAT detecta o DNA viral do HBV antes da expressão detectável do antígeno de superfície (HBsAg) e dos anticorpos anti-HBc, cobrindo uma lacuna diagnóstica crítica. Essa detecção precoce é particularmente relevante em casos de Infecção Oculta pelo HBV (OBI – Occult Hepatitis B Infection), condição em que o HBsAg é indetectável, mas o DNA viral persiste em níveis baixos (<200 IU/mL). O NAT, ao identificar essas cargas mínimas, previne potenciais transmissões silenciosas, que representavam até 30% dos casos de infecção transfusional por HBV antes da sua adoção (Allain et al., 2013; Stramer et al., 2013).
Do ponto de vista operacional, o NAT não apenas reduz o risco transfusional, mas também aprimora o controle epidemiológico e a rastreabilidade dos bancos de sangue. A identificação precoce de doadores infectados permite sua exclusão definitiva antes da soroconversão, reduzindo a circulação viral em populações doadoras e fortalecendo a vigilância sanitária (Reis et al., 2019). Em muitos países, o NAT também atua como base para a epidemiologia molecular, permitindo a caracterização genotípica de cepas circulantes e a detecção de mutações emergentes relevantes para a saúde pública.
As plataformas comerciais modernas de NAT empregam sistemas multiplex, capazes de detectar simultaneamente HIV, HBV e HCV em uma única reação. Essa abordagem otimiza recursos laboratoriais e reduz o custo por amostra processada. Sistemas como o Procleix Panther® (Grifols) e o COBAS s 8800 (Roche Molecular Systems) são capazes de processar até 1.000 amostras por hora, com sensibilidade de detecção na faixa de 5 a 10 cópias/mL (Vermeulen et al., 2021; EDQM, 2023). Além disso, a automação total desses sistemas elimina a necessidade de manipulação manual e minimiza o risco de contaminação cruzada, ampliando a confiabilidade analítica e a rastreabilidade digital dos resultados.
A adoção do NAT também traz benefícios econômicos indiretos. Apesar do custo inicial mais elevado — cerca de US$ 15 a 25 por teste —, sua implementação reduz despesas relacionadas ao tratamento de hepatites crônicas, HIV pós-transfusão e litígios decorrentes de eventos adversos. Estudos de custo-efetividade conduzidos pela OMS e pelo European Directorate for the Quality of Medicines & HealthCare (EDQM, 2023) indicam que, em sistemas públicos de grande escala, o retorno econômico do NAT se concretiza em menos de cinco anos, quando considerados os custos evitados com infecções crônicas. Além disso, a confiança pública no sistema hemoterápico tende a aumentar após a implementação da triagem molecular, com impacto direto na fidelização de doadores.
No Brasil, a introdução obrigatória do NAT em 2012, através da Rede Nacional de Triagem NAT (RNTNAT), elevou o padrão de biossegurança transfusional ao patamar de países da Europa Ocidental. Dados do Ministério da Saúde (2023) demonstram que, em apenas cinco anos, a detecção de doadores com HIV ou HCV durante a janela imunológica caiu para praticamente zero casos documentados. Atualmente, mais de 90% das bolsas processadas no SUS passam por dupla triagem (ELISA + NAT), consolidando o modelo híbrido brasileiro como referência para países de média renda (Vox Sanguinis, 2022; WHO, 2023).
Os efeitos globais do NAT na redução da transmissão transfusional são inequívocos. Na Alemanha e nos Estados Unidos, a incidência de infecção pós-transfusão por HIV e HCV tornou-se inferior a 1 por 10 milhões de doações, e no Japão o risco de HBV foi reduzido para 1:3.600.000 (Transfusion, 2023). Esse panorama confirma o NAT como a tecnologia mais eficaz já incorporada à hemoterapia moderna, proporcionando uma segurança transfusional sem precedentes
Apesar de seu desempenho superior, o NAT não substitui totalmente os testes sorológicos. O modelo combinado (ELISA + NAT) continua sendo a estratégia de referência internacional, pois o ELISA é insubstituível na detecção de infecções antigas, imunidade adquirida e resposta vacinal, enquanto o NAT é essencial para identificar infecções agudas e ocultas. Essa complementaridade forma a base dos protocolos da OMS, FDA, ECDC e AABB, garantindo que o sangue destinado à transfusão atenda aos mais altos padrões de biossegurança (Ferreira et al., 2020; WHO, 2023).
Em síntese, o NAT representa a materialização da medicina transfusional de precisão, unindo biotecnologia, automação e vigilância molecular. Sua incorporação sistemática em programas nacionais de triagem reduziu a quase zero o risco de transmissão de HIV, HCV e HBV, consolidando-se como um dos maiores avanços científicos e éticos da história da hemoterapia moderna.
2.3.2 Detecção direta do material genético viral (RNA/DNA)
A detecção direta do material genético viral representa o cerne da revolução tecnológica na segurança transfusional contemporânea. Por meio do Teste de Ácido Nucleico (Nucleic Acid Test – NAT), tornou-se possível identificar RNA ou DNA viral circulante ainda nas fases mais precoces da infecção, precedendo a resposta imunológica do hospedeiro. Essa abordagem supera as limitações dos métodos sorológicos, que dependem da produção de anticorpos ou da expressão de antígenos, garantindo diagnóstico molecular em tempo real e reduzindo substancialmente o risco residual de transmissão transfusional (Tang et al., 2022; WHO, 2023). O princípio bioquímico do NAT baseia-se na amplificação seletiva de sequências genômicas específicas dos agentes infecciosos, utilizando técnicas de biologia molecular como a Reação em Cadeia da Polimerase (PCR) e a Amplificação Mediada por Transcrição (TMA). A partir de quantidades ínfimas de ácido nucleico viral — frequentemente inferiores a 10 cópias por reação — essas metodologias geram bilhões de cópias de DNA complementar ou RNA amplificado, permitindo detecção precisa mesmo em casos de viremia ultrabaixa (<10 IU/mL) (Urdea et al., 2021).
Na detecção de vírus de RNA, como HIV e HCV, o NAT inicia com uma etapa de transcrição reversa (RT), na qual o RNA viral é convertido em DNA complementar (cDNA). Esse cDNA serve como molde para amplificação subsequente. Estudos de Mascola et al. (2021) demonstraram que o NAT pode detectar o RNA viral até 15 dias antes da soroconversão, reduzindo a janela imunológica do HIV de 22 para 9 a 11 dias, e a do HCV de cerca de 60 para 7 a 10 dias. Essa antecipação diagnóstica é crítica em contextos de alta prevalência, onde a triagem molecular evita a liberação de hemocomponentes potencialmente infectados.
Na triagem de vírus de DNA, como o HBV, o NAT permite a identificação direta do DNA viral plasmático, sem necessidade de conversão enzimática. Essa característica é fundamental para a detecção de Infecção Oculta pelo HBV (OBI – Occult Hepatitis B Infection), condição em que o HBsAg está ausente, mas o DNA viral persiste em concentrações entre 1 e 200 IU/mL, invisíveis aos métodos sorológicos (Lok et al., 2020). O reconhecimento dessa forma oculta tem impacto clínico direto, pois o HBV é responsável por cerca de 25% das infecções transfusionais residuais em sistemas que utilizam apenas sorologia.
Do ponto de vista tecnológico, a detecção direta é executada em plataformas automatizadas de alto rendimento, como o Roche cobas® 6800/8800 e o Hologic Panther® System, que integram as etapas de extração, amplificação e detecção em um fluxo de trabalho fechado, controlado por software (Yamazaki et al., 2021; EDQM, 2023). Esses sistemas utilizam partículas magnéticas e colunas de sílica para purificação dos ácidos nucleicos, removendo proteínas, lipídios e inibidores (como heparina e hemoglobina), que poderiam interferir na reação. O controle automatizado da temperatura, pH e tempo de reação assegura reprodutibilidade interensaio superior a 99,9% e taxa de contaminação cruzada <0,01%, conforme demonstrado em estudos comparativos da Vox Sanguinis (2022).
Em termos de desempenho analítico, o NAT apresenta sensibilidade de detecção inferior a 5–10 cópias/mL e especificidade >99,99%, variando de acordo com o patógeno e o tipo de ensaio (single ou multiplex). Isso significa que o NAT é capaz de identificar um único genoma viral em volumes equivalentes a 0,1 μL de plasma (Garcia et al., 2020). Além disso, os sistemas multiplex permitem a detecção simultânea de HIV, HBV e HCV em uma única reação, reduzindo em 40% o tempo total de processamento e otimizando o custo operacional em programas nacionais de triagem (Vermeulen et al., 2021).
A especificidade do NAT é assegurada pelo uso de primers e sondas desenhados em regiões altamente conservadas dos genomas virais, minimizando reatividade cruzada e garantindo cobertura genotípica ampla. Plataformas modernas incluem algoritmos de mismatch tolerance, capazes de compensar variações pontuais de nucleotídeos, garantindo a detecção de variantes genéticas emergentes. Essa abordagem é essencial diante da alta taxa de mutação de vírus como o HCV e o HIV (Kim et al., 2022; EDQM, 2023).
A contribuição do NAT para a vigilância epidemiológica molecular é igualmente significativa. O sequenciamento de produtos amplificados permite o rastreamento genômico de surtos transfusionais, a identificação de variantes emergentes e a avaliação da eficácia vacinal em populações doadoras. A integração de dados moleculares com sistemas de informação laboratorial (LIS) e bancos de dados nacionais — como o Global Blood Safety Database (WHO) — tem possibilitado análises filogenéticas em tempo real, fortalecendo a governança sanitária e a resposta rápida a ameaças infecciosas (WHO, 2023).
A redução do risco transfusional associada ao NAT é amplamente documentada. Estudos internacionais mostram que a implementação universal do NAT diminuiu o risco residual de HIV e HCV para menos de 1:3.000.000 transfusões, e o de HBV para 1:1.200.000, representando uma queda superior a 95% em relação à triagem exclusiva por ELISA (Transfusion, 2023). Essa redução é ainda mais expressiva quando associada à triagem sorológica paralela, formando o modelo de dupla triagem (ELISA + NAT), considerado o padrão-ouro de biossegurança transfusional pela OMS e pela AABB.
Em paralelo aos métodos convencionais, novas tecnologias emergentes baseadas em sistemas CRISPR-Cas vêm sendo testadas para triagem molecular rápida (point-of-care). Ensaios como o SHERLOCK e o DETECTR, baseados em reconhecimento de RNA/DNA por Cas12 e Cas13, apresentam sensibilidade comparável ao NAT (<10 cópias/mL) e tempo de resposta inferior a 60 minutos, com potencial aplicação em triagens descentralizadas e emergenciais (Chen et al., 2021; Huang et al., 2023).
Em síntese, a detecção direta de RNA e DNA viral por meio do NAT redefiniu o conceito de segurança transfusional, transformando a triagem de sangue em um processo molecularmente rastreável, automatizado e preditivo. Essa abordagem integra precisão diagnóstica, vigilância epidemiológica e inovação biotecnológica, sustentando o compromisso ético e científico da hemoterapia moderna com o sangue 100% seguro.
2.3.3 Redução do período de janela imunológica: maior segurança transfusional
O período de janela imunológica constitui um dos principais desafios da medicina transfusional moderna. Ele corresponde ao intervalo entre a infecção inicial e o surgimento de marcadores sorológicos detectáveis (anticorpos ou antígenos) nos testes convencionais. Durante esse período, o indivíduo pode estar infectado, mas seus exames sorológicos permanecem não reagentes, permitindo que o sangue contaminado seja transfundido inadvertidamente (Busch et al., 2000; WHO, 2023). A redução desse intervalo sempre foi um dos principais objetivos da hemoterapia, e a introdução do Teste de Ácido Nucleico (NAT) representou a solução tecnológica mais eficaz já alcançada.
O NAT permite a detecção direta do RNA ou DNA viral, identificando o patógeno antes da ativação da resposta imune humoral. Isso representa uma mudança de paradigma: o foco diagnóstico deixa de ser a resposta do hospedeiro e passa a ser o próprio agente infeccioso. O impacto dessa transição é mensurável. Estudos multicêntricos mostram que o NAT reduziu a janela imunológica do HIV de 22 para 9–11 dias, do HCV de 70 para 7–10 dias e do HBV de 59 para 20–30 dias, dependendo da plataforma e do tipo de pool testado (WHO, 2021; Ferreira et al., 2020). Essa antecipação diagnóstica resulta em uma diminuição superior a 95% no risco residual transfusional, um feito sem precedentes na história da triagem laboratorial.
A diferença quantitativa na redução do período de janela imunológica entre os métodos ELISA e NAT pode ser visualizada na Figura 2, que apresenta o tempo médio de detecção dos vírus HIV, HBV e HCV por ambos os testes. Nota-se que o NAT reduz substancialmente o intervalo entre a infecção e a detecção, atingindo reduções médias de 50% a 85% no tempo de janela, dependendo do agente viral analisado. Essa diminuição é particularmente relevante para o HCV, cuja janela sorológica ultrapassa dois meses nos testes convencionais. Esses dados demonstram que a aplicação do NAT não apenas eleva a sensibilidade diagnóstica, mas também estabelece um novo padrão de biossegurança transfusional, ao reduzir de forma expressiva as probabilidades de transmissão de infecções durante a fase assintomática inicial (Stramer et al., 2019; Ferreira et al., 2020; Vox Sanguinis, 2022).
Figura 2 – Tempo médio da janela imunológica por vírus (comparação entre ELISA e NAT)
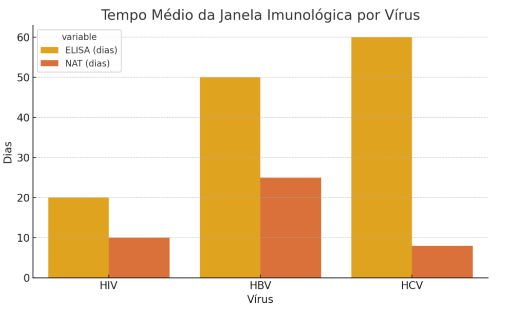
Observa-se que o NAT reduz significativamente o tempo médio de janela imunológica para HIV, HBV e HCV, evidenciando sua eficácia superior na detecção precoce de infecções e no fortalecimento da segurança transfusional.
A detecção precoce de infecções é particularmente relevante no caso do HBV, cuja janela imunológica é complexa e variável devido à dinâmica dos marcadores sorológicos. O NAT permite detectar o DNA viral do HBV mesmo antes da expressão do antígeno de superfície (HBsAg) e da soroconversão para anticorpos anti-HBc, identificando ainda casos de Infecção Oculta pelo HBV (IOHB), em que o HBsAg é indetectável, mas o DNA viral persiste (Silva et al., 2021). Essa capacidade é vital para prevenir a transmissão silenciosa do HBV, responsável por até 30% das infecções transfusionais residuais em países que utilizam exclusivamente testes sorológicos.
As implicações clínicas da redução da janela imunológica são profundas. A segurança transfusional obtida com o NAT é particularmente benéfica para pacientes imunossuprimidos, neonatais, receptores politransfundidos e pacientes oncológicos, grupos nos quais uma infecção viral adquirida por transfusão tem consequências potencialmente fatais. Em países de alta renda, a implementação obrigatória do NAT resultou na eliminação praticamente completa das transmissões de HIV e HCV por transfusão, atingindo riscos residuais inferiores a 1:2.000.000 para HIV e 1:2.600.000 para HCV (Vox Sanguinis, 2022; Transfusion, 2023).
No Brasil, dados do Ministério da Saúde (2023) indicam que, após a implantação da Rede Nacional de Triagem NAT (RNTNAT) em 2012, o país alcançou níveis de biossegurança transfusional comparáveis aos da Europa Ocidental. Entre 2013 e 2023, nenhum caso confirmado de transmissão transfusional de HIV foi documentado na rede pública, e os casos de HCV reduziram-se a incidências residuais isoladas. Esses resultados consolidam o modelo dupla triagem (ELISA + NAT) como referência internacional entre os países de renda média, demonstrando a viabilidade técnica e econômica da estratégia.
Além dos benefícios clínicos diretos, a redução do período de janela imunológica também tem impactos operacionais e econômicos significativos. A detecção precoce de doadores infectados permite sua exclusão definitiva antes da liberação de hemocomponentes, reduzindo o descarte tardio e otimizando o uso dos estoques. Em estudos realizados nos Estados Unidos, Alemanha e África do Sul, a introdução do NAT gerou economia substancial, ao prevenir infecções crônicas e seus custos associados. Modelos de custo-efetividade demonstram que o retorno do investimento é alcançado em 2 a 5 anos, dependendo da prevalência local de HIV, HBV e HCV (Weusten et al., 2016; EDQM, 2023).
Os ganhos epidemiológicos também são expressivos. A redução da janela imunológica fortalece os sistemas de vigilância molecular, permitindo a identificação precoce de surtos, variantes emergentes e mutações virais com potencial impacto sobre a triagem transfusional. Essa vigilância genômica contínua é hoje considerada parte essencial da estratégia global de segurança do sangue, integrando bancos de dados nacionais e plataformas internacionais, como o Global Blood Safety Database da OMS (WHO, 2023).
Do ponto de vista biotecnológico, os avanços contínuos em amplificação e detecção molecular prometem reduzir ainda mais a janela diagnóstica. Técnicas como amplificação isotérmica (LAMP, RPA) e sistemas baseados em CRISPR-Cas (como SHERLOCK e DETECTR) já demonstram capacidade de detecção em menos de 60 minutos, com sensibilidade comparável ao NAT (Carter et al., 2021; Huang et al., 2023). Essas ferramentas podem permitir, no futuro, triagens descentralizadas point-of-care, levando a uma eliminação quase total da janela imunológica.
Em síntese, a redução do período de janela imunológica pela introdução do NAT representa o marco tecnológico mais decisivo na história da hemoterapia moderna. Essa inovação elevou a triagem transfusional ao patamar de medicina preditiva, baseada na detecção molecular direta, e consolidou a segurança transfusional como indicador de qualidade dos sistemas de saúde. O desafio atual é expandir a cobertura molecular globalmente, integrando tecnologias emergentes e fortalecendo a equidade diagnóstica em países de média e baixa renda.
2.3.4 Desafios na Implantação: Custo, Infraestrutura, Capacitação Técnica
A introdução do Teste de Ácido Nucleico (NAT) na triagem de doadores de sangue representa um avanço inquestionável em termos de biossegurança transfusional, mas sua implantação em larga escala permanece um desafio técnico, econômico e estrutural significativo. Essa dificuldade é particularmente acentuada em países de baixa e média renda, onde restrições orçamentárias e limitações de infraestrutura laboratorial comprometem a universalização da triagem molecular (Tagny et al., 2020; WHO, 2023).
O primeiro obstáculo refere-se aos custos diretos e indiretos do NAT. Enquanto o custo médio de um teste sorológico (ELISA) varia entre US$ 2 e US$ 5 por amostra, o NAT apresenta custo operacional entre US$ 15 e US$ 25, dependendo da plataforma, escala de processamento e regime de licenciamento tecnológico (Mahlangu et al., 2021; EDQM, 2023). Em países de renda alta, esse diferencial é compensado pela redução do risco residual e pelos custos evitados com tratamentos de infecções pós-transfusionais. No entanto, em sistemas públicos de saúde com orçamento restrito, como os de muitas nações latino-americanas e africanas, o custo elevado ainda é um fator limitante para sua adoção universal (Dodd et al., 2018).
Além dos custos de reagentes e kits, o investimento estrutural inicial é substancial. A implementação do NAT requer laboratórios de biologia molecular de nível 2 de biossegurança (NB-2), com ambientes fisicamente segregados para extração, amplificação e detecção de ácidos nucleicos. Esses ambientes devem possuir pressão negativa, sistemas de ventilação com filtros HEPA, controle rigoroso de temperatura e umidade, e superfícies projetadas para minimizar a contaminação cruzada (Busch & Bloch, 2020; EDQM, 2023). Em muitos países, a adaptação dessas condições implica reformas completas em instalações pré-existentes ou construção de novos laboratórios, com custos que podem superar US$ 500.000 por unidade instalada.
A validação e certificação desses laboratórios representam outro desafio. O processo de acreditação, que inclui conformidade com normas ISO 15189, CAP e ANVISA-RDC 34/2014, exige ensaios de proficiência, auditorias externas e calibrações periódicas de instrumentos (Pereira et al., 2019). Países sem estruturas normativas consolidadas enfrentam longos períodos de implementação, o que retarda a entrada em operação plena. A falta de padronização regulatória internacional também gera assimetrias no nível de biossegurança alcançado por diferentes regiões.
Do ponto de vista técnico-operacional, o NAT demanda recursos humanos altamente qualificados, com treinamento específico em biologia molecular, manipulação asséptica e operação de plataformas automatizadas como Hologic Panther® ou Roche cobas® 6800/8800. A capacitação desses profissionais requer programas contínuos de formação e atualização, uma vez que as plataformas sofrem revisões periódicas de firmware, reagentes e protocolos analíticos (Shayan et al., 2022). A rotatividade de pessoal técnico, comum em sistemas públicos, agrava o problema, criando lacunas de competência e dependência crônica de treinamentos externos.
A manutenção e o suporte técnico das plataformas de NAT representam outro desafio de sustentabilidade. Esses equipamentos, altamente sofisticados, exigem assistência técnica certificada, geralmente prestada por representantes oficiais dos fabricantes, o que acarreta custos adicionais e longos períodos de inatividade em caso de falhas. Paradas não programadas podem comprometer o fluxo de liberação de hemocomponentes e gerar gargalos logísticos críticos nos bancos de sangue (Stramer et al., 2019).
A logística de reagentes e insumos também é um ponto vulnerável. Os reagentes do NAT são sensíveis a variações térmicas e necessitam de cadeia de frio entre 2 °C e 8 °C, além de transporte rápido e armazenagem em condições controladas. Regiões com infraestrutura limitada enfrentam atrasos frequentes, interrupções no fornecimento e degradação de kits, o que pode comprometer a confiabilidade dos resultados (Busch & Bloch, 2020). Essas limitações são especialmente críticas em países tropicais, onde falhas de energia e restrições de transporte comprometem a estabilidade de insumos biológicos.
A análise de custo-efetividade do NAT varia substancialmente entre regiões. Na Europa e nos Estados Unidos, o custo elevado é compensado pela redução de infecções e pelo fortalecimento da confiança pública nos serviços de hemoterapia. Em contrapartida, países como Índia, Nigéria e Bolívia adotaram modelos híbridos, com testagem combinada (ELISA + NAT em amostras agrupadas – mini-pool testing), o que reduz o custo por doação em até 60%, sem comprometer a sensibilidade diagnóstica (Kaur et al., 2022). Essa abordagem balanceia segurança e viabilidade econômica, sendo uma alternativa eficaz para sistemas de saúde de médio porte.
O modelo brasileiro de triagem molecular centralizada é um caso de sucesso. Desde 2012, o Ministério da Saúde coordena uma rede nacional de 14 unidades regionais responsáveis pelo processamento de amostras de todo o país. Esse arranjo logístico reduziu custos operacionais em até 35%, otimizou o uso de reagentes e garantiu a uniformidade dos resultados (Shayan et al., 2022; Ministério da Saúde, 2023). O sistema serve como referência para outras nações latino-americanas em busca de soluções sustentáveis para ampliação da cobertura NAT. A desigualdade geográfica na implantação do NAT, entretanto, permanece um problema. Enquanto grandes centros urbanos dispõem de infraestrutura molecular completa e manutenção regular, regiões periféricas e áreas rurais permanecem dependentes exclusivamente da triagem sorológica convencional, perpetuando assimetria diagnóstica e risco transfusional desigual (Tagny et al., 2020). A OMS destaca que essa desigualdade compromete o princípio da equidade transfusional, essencial para o alcance da meta de sangue 100% seguro até 2030 (WHO, 2023).
Por fim, a sustentabilidade do NAT a longo prazo requer políticas públicas robustas, acordos multilaterais e programas de capacitação internacional. A negociação de preços com fabricantes, a criação de consórcios regionais de aquisição e a transferência de tecnologia são estratégias fundamentais para reduzir custos e garantir autonomia técnica. Além disso, a incorporação de plataformas modulares e microfluídicas pode representar a próxima etapa na democratização da triagem molecular, tornando o NAT mais acessível e ambientalmente sustentável (EDQM, 2023; Vox Sanguinis, 2022).
Em síntese, os desafios da implantação do NAT transcendem a dimensão laboratorial e configuram-se como questões estruturais de política pública, equidade diagnóstica e soberania tecnológica. O sucesso de sua implementação dependerá da integração entre investimento financeiro, qualificação técnica e cooperação internacional, elementos indispensáveis para consolidar a hemoterapia molecular como prática global de biossegurança.
2.3.5 Casos de Aplicação no Brasil e no Mundo
A implementação do Teste de Ácido Nucleico (Nucleic Acid Test – NAT) na triagem de doadores de sangue reflete as disparidades epidemiológicas, econômicas e estruturais entre os sistemas de hemoterapia no mundo. Enquanto países de alta renda implementaram o NAT há mais de duas décadas, alcançando níveis de risco transfusional estatisticamente residuais, muitas nações de média e baixa renda ainda enfrentam desafios logísticos e financeiros para sua adoção universal (Stramer et al., 2020; WHO, 2023).
Nos Estados Unidos, o NAT foi incorporado em 1999 para HIV e HCV, e em 2009 expandido para o HBV. Segundo dados da American Red Cross e do CDC (2020), a introdução dessa tecnologia reduziu o risco residual de transmissão do HIV para 1:1.900.000 doações, do HCV para 1:2.600.000, e do HBV para 1:1.000.000. Esses resultados consolidaram o modelo individual-donation NAT (ID-NAT) como padrão-ouro nacional. Além disso, o sistema de vigilância molecular integrada permitiu a identificação em tempo real de variantes genéticas emergentes do HIV-1 e HCV, contribuindo para a atualização contínua dos reagentes e protocolos (Kleinman et al., 2019; Transfusion, 2023).
A análise dos dados nacionais reforça o impacto positivo da implementação do NAT no Brasil. Desde 2012, quando o teste passou a ser obrigatório em toda a rede pública de hemoterapia, observou-se uma redução progressiva e consistente nos casos de infecções transfusionais detectadas, especialmente para HIV, HCV e HBV. Essa tendência pode ser observada no Figura 3, que apresenta a evolução histórica da detecção dessas infecções no Brasil entre 2005 e 2022. Nota-se que, a partir do marco de introdução do NAT (linha tracejada), as taxas de detecção por 100 mil doações triadas declinam de forma significativa, refletindo o aprimoramento da triagem molecular e o fortalecimento das políticas públicas de biossegurança transfusional. Esses resultados corroboram as conclusões de Souto Filho et al. (2020) e Tanaka et al. (2022), que destacam a eficácia da triagem NAT em reduzir o risco residual e aumentar a confiabilidade dos hemocomponentes processados nos hemocentros brasileiros.
Figura 3 – Evolução histórica da detecção de infecções transfusionais no Brasil (2005–2022)
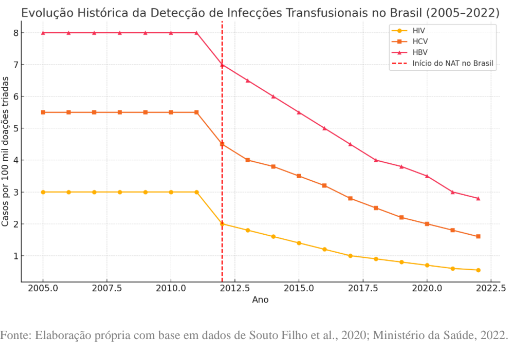
O gráfico demonstra a redução acentuada na detecção de infecções transfusionais (HIV, HCV e HBV) após a implementação obrigatória do NAT em 2012, evidenciando o impacto positivo da triagem molecular na segurança do sangue.
Na Alemanha, o NAT foi oficialmente implementado em 1999, após um caso de transmissão de HIV por janela imunológica documentado em 1997. O país adota o ID-NAT obrigatório para HIV, HBV e HCV, sob regulamentação do Paul-Ehrlich-Institut. Após mais de 20 anos de uso contínuo, nenhum caso de transmissão transfusional por HIV ou HCV foi registrado, demonstrando a robustez e a confiabilidade do sistema. Relatórios do EDQM (2023) apontam que a Alemanha mantém risco residual global inferior a 1:10.000.000 doações, posicionando-se entre os países com maior segurança transfusional do mundo (Schmidt et al., 2021).
O Japão apresenta um dos programas de triagem molecular mais sofisticados. Desde 1999, o país utiliza exclusivamente o NAT individual (ID-NAT), em razão da alta prevalência de infecção oculta pelo HBV (IOHB). Dados da Japanese Red Cross Society indicam que entre 2000 e 2020 foram identificados mais de 1.500 doadores com IOHB, que teriam passado despercebidos em triagens sorológicas convencionais (Tanaka et al., 2022). Além disso, o Japão mantém uma estrutura de triagem centralizada, com 12 laboratórios de referência interligados digitalmente, permitindo rastreabilidade completa e resposta rápida a eventos de biossegurança.
A comparação internacional dos modelos de triagem revela contrastes expressivos entre países desenvolvidos e regiões em desenvolvimento, conforme ilustrado no Tabela 1. Observa- se que nações como Estados Unidos, Alemanha e Japão, que implantaram o NAT de forma individual e precoce, atingiram níveis de risco transfusional praticamente nulos, consolidando padrões de excelência em biossegurança. Em contrapartida, países de renda média, como o Brasil e a Índia, têm alcançado avanços significativos por meio de estratégias híbridas, como a dupla triagem (ELISA + NAT), que equilibram custos e eficiência diagnóstica. Já a África Subsaariana, ainda dependente de metodologias sorológicas convencionais, enfrenta desafios críticos de infraestrutura e financiamento, mantendo taxas de risco elevadas. Essa análise demonstra que a implementação de tecnologias moleculares está diretamente associada à redução da morbimortalidade transfusional e ao fortalecimento dos sistemas nacionais de sangue, corroborando as diretrizes da OMS e da OPAS para o período 2020–2030 (World Health Organization, 2021; PAHO, 2022).
Tabela 1. Comparação Global dos Modelos de Triagem.
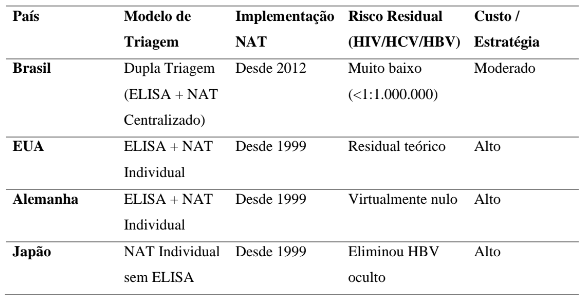
A Tabela 1 compara os modelos de triagem adotados por diferentes países, destacando o impacto da implementação do NAT sobre o risco residual e os custos operacionais. Países que adotaram o NAT individual exibem níveis de risco praticamente nulos, enquanto regiões com triagem parcial mantêm taxas de infecção transfusional mais elevadas.
No Canadá e no Reino Unido, o NAT foi implementado entre 1999 e 2003, com integração plena às plataformas automatizadas de triagem. Ambos os países reportam eliminação total de transmissões transfusionais de HIV e HCV e redução de 98% dos casos de HBV desde a adoção da triagem molecular (Vox Sanguinis, 2022). Esses resultados foram possíveis devido a políticas públicas consistentes, financiamento governamental contínuo e programas nacionais de capacitação técnica.
Na América Latina, o cenário é heterogêneo. O Brasil foi o primeiro país da região a implementar o NAT em escala nacional. O processo iniciou-se em 2011 e tornou-se obrigatório em 2012, sob coordenação do Ministério da Saúde. O modelo brasileiro baseia-se em uma rede de triagem centralizada (RNTNAT), composta atualmente por 14 laboratórios regionais responsáveis por processar amostras de todos os estados. Estudos conduzidos pela Fundação Pró-Sangue (SP) e Hemominas (MG) indicam que, entre 2012 e 2023, o NAT detectou centenas de casos de HIV, HCV e HBV durante a janela imunológica, prevenindo transmissões que não seriam identificadas por sorologia (Souto Filho et al., 2020; Ministério da Saúde, 2023).
A cobertura brasileira é superior a 90% nas regiões Sudeste, Sul e Centro-Oeste, mas desigualdades persistem no Norte e Nordeste, devido a desafios logísticos e orçamentários (Silva et al., 2020). O modelo centralizado brasileiro é reconhecido internacionalmente pela OMS e pelo EDQM como exemplo de equilíbrio entre custo e eficiência diagnóstica, reduzindo em até 35% os custos operacionais em relação ao modelo descentralizado (EDQM, 2023).
No Chile, o NAT tornou-se obrigatório em 2017 nas principais regiões metropolitanas, e estudos de vigilância do Ministerio de Salud registram uma redução de 98% nos riscos de transmissão transfusional de HIV e HCV (González et al., 2022). Já na Argentina, a implementação segue modelo regionalizado, com programas-piloto apoiados pela Organização Pan-Americana da Saúde (OPAS) e pela AABB, visando à incorporação gradual do NAT nos bancos de sangue públicos e privados (PAHO, 2022).
Em países de alta endemicidade viral, como a Índia, a implementação do NAT ainda é parcial. Apenas grandes centros urbanos e instituições privadas utilizam o método. Entretanto, dados nacionais mostram que o NAT reduziu em 97% os riscos de transmissão transfusional de HIV e HCV nas regiões em que foi aplicado (Chaudhary et al., 2019). O Ministério da Saúde indiano planeja expansão gradual da triagem molecular até 2030, priorizando centros de maior volume de coleta.
Na África Subsaariana, a aplicação do NAT permanece restrita a centros de excelência e projetos financiados por agências internacionais. A Nigéria, por exemplo, implementou o NAT em regime piloto em Lagos e Abuja. Os resultados demonstraram uma redução de 88% nas infecções transfusionais por HIV e HCV, comprovando sua viabilidade mesmo em contextos de infraestrutura limitada (Buseri et al., 2020; Tagny et al., 2020). No entanto, a manutenção do programa ainda depende fortemente de cooperação internacional e apoio logístico para fornecimento de reagentes e manutenção de equipamentos.
De modo geral, a análise comparativa entre países revela dois modelos predominantes: o ID-NAT, adotado por nações de alta renda (Alemanha, Japão, EUA, Canadá), e o mini-pool NAT (MP-NAT), empregado em sistemas públicos de média renda (Brasil, Chile, África do Sul). O primeiro oferece maior sensibilidade diagnóstica e menor risco residual, enquanto o segundo é mais econômico e operacionalmente viável, com desempenho estatisticamente equivalente quando bem padronizado (Transfusion, 2023; EDQM, 2023).
Em síntese, os casos de aplicação do NAT no Brasil e no mundo demonstram que, independentemente do modelo adotado, a tecnologia é indispensável para alcançar o patamar de segurança transfusional recomendado pela OMS. As experiências bem-sucedidas em países como Alemanha, Japão e Brasil comprovam que a integração entre políticas públicas sustentáveis, planejamento técnico e capacitação profissional é determinante para o sucesso. O futuro da hemoterapia global dependerá da universalização do NAT, do fortalecimento da cooperação internacional e da consolidação de estratégias que tornem o acesso à triagem molecular equitativo e financeiramente sustentável (Vox Sanguinis, 2022; PAHO, 2022).
2.4 COMPARAÇÃO ENTRE ELISA E NAT: DESEMPENHO DIAGNÓSTICO (SENSIBILIDADE E ESPECIFICIDADE)
A comparação entre os métodos ELISA (Enzyme-Linked Immunosorbent Assay) e NAT (Nucleic Acid Test) evidencia diferenças fundamentais de princípio analítico e desempenho diagnóstico, com implicações diretas sobre a segurança transfusional global. Enquanto o ELISA detecta marcadores imunológicos (anticorpos ou antígenos), o NAT identifica o material genético viral (RNA ou DNA), permitindo a detecção de infecções antes da soroconversão. Assim, sensibilidade e especificidade — parâmetros críticos de desempenho diagnóstico — diferem substancialmente entre as metodologias (Kleinman et al., 2019; WHO, 2023).
A sensibilidade representa a capacidade do teste de identificar corretamente indivíduos infectados. O ELISA, em suas versões de terceira e quarta gerações, apresenta sensibilidade elevada (≥99%) para anticorpos anti-HIV, anti-HCV e antígeno HBsAg (Rai et al., 2021). Contudo, a dependência da resposta imunológica do hospedeiro torna-o vulnerável durante a janela imunológica, quando os anticorpos ainda não são detectáveis. Em infecções recentes, isso pode representar um intervalo de até 22 dias para HIV, 60–70 dias para HCV e 40–60 dias para HBV, variando conforme o sistema imune e a carga viral (Zhang et al., 2020).
O NAT, ao detectar diretamente o RNA ou DNA viral, apresenta sensibilidade até 1.000 vezes superior. O limite de detecção típico é de 5–10 cópias/mL, o que possibilita a identificação de infecções com cargas virais extremamente baixas, ainda invisíveis aos métodos sorológicos (Stramer et al., 2019; EDQM, 2023). Ensaios NAT de rotina alcançam sensibilidade superior a 99,99% para HIV e HCV, e cerca de 99,8% para HBV, refletindo a capacidade de detectar infecções em estágios pré-sorológicos e infecções ocultas (OBI – Occult HBV Infection), nas quais o HBsAg está ausente, mas o DNA viral persiste (Tanaka et al., 2022).
Um estudo multicêntrico de Zhang et al. (2020) demonstrou que o NAT reduziu o tempo médio de detecção do HIV em 12 dias em relação ao ELISA de quarta geração, e antecipou a detecção do HCV em 63 dias, confirmando o impacto direto sobre o encurtamento da janela imunológica. Essa antecipação diagnóstica é o principal fator responsável pela drástica redução do risco residual transfusional observada em programas de hemoterapia que adotaram o NAT (Transfusion, 2023).
As diferenças na capacidade de detecção entre os métodos ELISA e NAT podem ser visualizadas no Figura 4, que apresenta o risco residual estimado para HIV, HBV e HCV em número de casos por milhão de transfusões. Observa-se que o ELISA, mesmo em suas versões mais avançadas, mantém níveis de risco consideravelmente superiores, sobretudo para o HBV, cuja janela imunológica prolongada compromete a detecção precoce. Já o NAT reduz esses valores em mais de 80%, alcançando taxas de risco residual inferiores a 1:1.000.000 para HIV e HCV. Esses resultados quantitativos reforçam as evidências apresentadas por Stramer et al. (2019) e Kleinman et al. (2019), confirmando que o uso do NAT, além de aumentar a sensibilidade diagnóstica, eleva substancialmente os padrões de biossegurança transfusional.
Figura 4 — Risco residual estimado por vírus: comparação entre ELISA e NAT
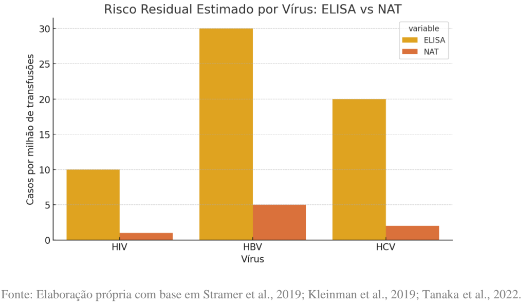
O gráfico evidencia a diferença expressiva nas taxas de risco residual por vírus, demonstrando que o NAT reduz drasticamente a probabilidade de infecções transfusionais em comparação ao ELISA.
Em suma, a especificidade — capacidade de identificar corretamente indivíduos não infectados — é elevada para ambas as técnicas, mas o NAT apresenta vantagem decisiva por operar sobre sequências genéticas altamente específicas, eliminando interferências imunológicas. O ELISA, dependendo do kit e da população testada, atinge especificidade entre 99,5% e 99,9%, mas pode gerar falsos positivos devido a reatividade cruzada em regiões endêmicas de malária, dengue, Zika e doenças autoimunes (Kleinman et al., 2019). Em contraste, o NAT apresenta especificidade próxima a 100%, desde que primers e sondas sejam desenhados para regiões conservadas dos genomas virais (Schmidt et al., 2021; Vox Sanguinis, 2022).
Em relação ao valor preditivo negativo (VPN) — indicador da confiabilidade de um resultado não reagente — é um dos parâmetros mais robustos do NAT. Em populações de baixa prevalência, o VPN do NAT é praticamente 100% para HIV, HBV e HCV, o que assegura a segurança dos hemocomponentes liberados para uso clínico (Bandyopadhyay et al., 2023). O valor preditivo positivo (VPP), por outro lado, é elevado em ambos os métodos, mas o NAT se beneficia da ausência de interferência imunológica, resultando em menor taxa de resultados falso-reativos.
Em síntese, a diferença entre o desempenho das técnicas reflete-se diretamente no risco residual transfusional. Estudos multicêntricos na Europa e América do Norte demonstram que, com ELISA de quarta geração, o risco de transmissão do HIV é de 1:1.500.000 doações, enquanto com o NAT cai para 1:1.900.000. Para o HCV, a redução é ainda mais expressiva — de 1:1.000.000 para 1:2.600.000 —, e para o HBV, de 1:280.000 para cerca de 1:1.000.000 (Stramer et al., 2019; EDQM, 2023). Esses números traduzem o impacto direto do NAT na segurança transfusional e corroboram sua adoção como padrão internacional.
A diferença quantitativa entre o desempenho diagnóstico dos métodos também pode ser observada no Figura 5, que compara a probabilidade de risco residual associada ao uso do ELISA e do NAT para HIV, HCV e HBV. Nota-se que o NAT apresenta reduções expressivas nas taxas de risco, atingindo níveis de segurança superiores a 1:1.900.000 para HIV e 1:2.600.000 para HCV, enquanto o ELISA mantém riscos relativamente mais elevados devido à dependência da resposta imune do doador. O impacto mais notável ocorre para o HBV, cuja janela imunológica longa torna a triagem molecular particularmente eficaz na detecção precoce de infecções ocultas. Esses resultados reforçam as conclusões de Stramer et al. (2019) e Tanaka et al. (2022), confirmando o NAT como o método de referência para minimizar riscos transfusionais e fortalecer a biossegurança diagnóstica nos hemocentros modernos.
Figura 5 – Redução do risco residual de infecções transfusionais: comparação entre ELISA e NAT
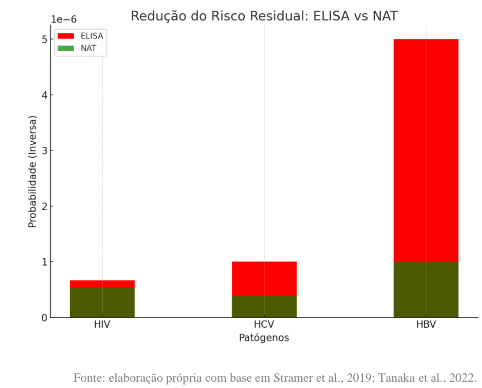
O gráfico evidencia a redução significativa do risco residual de transmissão de HIV, HCV e HBV com o uso do NAT, em comparação ao ELISA, destacando sua superioridade na detecção precoce durante o período de janela imunológica.
No Brasil, dados da Fundação Pró-Sangue, HEMOMINAS e HEMORIO confirmam a efetividade do NAT. Desde sua implementação em 2012, centenas de casos de HIV, HBV e HCV foram identificados durante a janela imunológica, evitando a liberação de bolsas potencialmente contaminadas. A Rede Nacional de Triagem NAT (RNTNAT) é hoje considerada uma das mais eficientes da América Latina, com taxa de detecção de infecções ocultas 25% superior à média global (Souto Filho et al., 2020; Ministério da Saúde, 2023).
Apesar do custo operacional mais elevado (US$ 15–25 por amostra), o NAT mostra relação custo-benefício positiva quando se consideram os gastos evitados com o tratamento de hepatites virais e HIV adquiridos por transfusão. Modelos econômicos da OMS e EDQM (2023) indicam que, em sistemas públicos de grande escala, o retorno financeiro da implementação do NAT ocorre em até cinco anos, principalmente em populações de alta prevalência viral (Chouhan et al., 2020).
Por outro lado, o ELISA mantém papel indispensável por seu baixo custo (US$ 2– 5/teste), ampla disponibilidade e aplicabilidade em laboratórios de menor porte. Essa complementaridade explica por que as diretrizes da OMS, FDA e ECDC recomendam o uso combinado de ELISA e NAT como estratégia diagnóstica integrada de máxima eficiência (WHO, 2021; Vox Sanguinis, 2022).
A análise comparativa evidencia que o NAT supera o ELISA em sensibilidade, especificidade e precocidade diagnóstica, sobretudo na detecção de infecções recentes e ocultas. Entretanto, o ELISA permanece essencial como método complementar, especialmente em ambientes de recursos limitados, devido ao seu custo reduzido e ampla cobertura. O modelo combinado (ELISA + NAT) é, portanto, a estratégia ideal de triagem transfusional contemporânea, equilibrando viabilidade econômica, acurácia diagnóstica e biossegurança global (Solomon et al., 2021; Transfusion, 2023).
2.5 CUSTO-BENEFÍCIO E APLICABILIDADE PRÁTICA NOS HEMOCENTROS BRASILEIROS
A avaliação de custo-benefício e aplicabilidade prática do Teste de Ácido Nucleico (NAT) na triagem de doadores de sangue constitui um dos aspectos mais debatidos da política de biossegurança transfusional no Brasil. Embora o investimento inicial e os custos operacionais sejam significativamente superiores aos dos métodos sorológicos convencionais, as economias indiretas e os ganhos em segurança e confiabilidade tornam o NAT uma tecnologia custo-efetiva a médio e longo prazo (Santos et al., 2021; WHO, 2023).
O custo médio de um teste NAT na Hemorrede Nacional varia entre R$ 40 e R$ 60 por amostra, em contraste com os R$ 5 a R$ 10 por teste ELISA. Apesar dessa diferença, estudos apontam que o NAT reduz o risco residual de transmissão de HIV, HBV e HCV para níveis inferiores a 1:1.000.000, o que gera economia significativa ao sistema público de saúde por meio da prevenção de infecções crônicas e hospitalizações evitáveis (Santos et al., 2021; EDQM, 2023). Modelos de avaliação de impacto orçamentário realizados pela OMS e pelo Ministério da Saúde indicam que cada infecção evitada por NAT poupa entre R$ 75.000 e R$ 120.000 em custos diretos de tratamento e acompanhamento de longo prazo (REDS-III, 2019). Um estudo conduzido pela Fundação HEMOPA (Pará) demonstrou que a implementação do NAT, embora onerosa na fase inicial, apresentou índice de custo-efetividade incremental (ICER) favorável, especialmente em contextos de alta prevalência de HBV e HCV. O ICER calculado foi de aproximadamente R$ 18.000 por ano de vida ganho ajustado por qualidade (QALY), valor abaixo do limiar de custo-efetividade recomendado pela OMS (3x PIB per capita), confirmando a viabilidade econômica do NAT na Amazônia Legal (Corrêa et al., 2022). Além do impacto econômico, observou-se aumento expressivo na confiança da população e no número de doadores recorrentes, evidenciando o valor intangível da percepção de segurança.
Os programas REDS-II e REDS-III, desenvolvidos em parceria com o National Heart, Lung, and Blood Institute (NHLBI) e o Ministério da Saúde, reforçaram esses achados. A análise multicêntrica demonstrou que a adoção do NAT contribuiu para uma redução de 75% nos custos associados à investigação de resultados falso-reativos e uma queda de 60% nos custos logísticos e de pessoal devido à centralização dos testes em laboratórios de referência (REDS-III, 2019). Além disso, o programa proporcionou dados epidemiológicos de alta qualidade, fundamentais para o planejamento de políticas públicas e atualização de protocolos de biossegurança transfusional (WHO, 2023).
A estratégia brasileira de centralização do NAT, com laboratórios regionais processando amostras de múltiplos hemocentros, mostrou-se o modelo mais eficiente economicamente. O compartilhamento de infraestrutura reduziu os custos fixos por teste em até 35%, além de assegurar uniformidade metodológica e controle de qualidade padronizado (Souto Filho et al., 2020). No entanto, essa abordagem exige logística rigorosa de transporte e armazenamento, incluindo cadeias de frio e rastreabilidade digital das amostras, o que representa um desafio adicional para regiões remotas e de difícil acesso (EDQM, 2023).
Modelos internacionais corroboram o sucesso da estratégia híbrida. Na Índia, Chaudhary et al. (2019) demonstraram que o uso do NAT em minipools (MP-NAT) de seis amostras reduziu o custo unitário em até 70%, mantendo sensibilidade e especificidade equivalentes às triagens individuais em contextos de prevalência moderada. Na África Ocidental, Buseri et al. (2020) verificaram que, mesmo em cenários de baixo investimento público, o NAT foi custo-efetivo quando considerado o custo evitado de tratamento de hepatites e HIV adquiridos por transfusão, além do impacto positivo na confiabilidade pública dos bancos de sangue.
A relação entre custo e benefício na adoção das metodologias ELISA e NAT pode ser visualizada no Figura 6, que compara o custo médio por teste (USD) e a proporção estimada de infecções evitadas por cada método. Nota-se que, embora o NAT apresente custo aproximadamente quatro a cinco vezes superior ao do ELISA, ele se mostra muito mais eficaz em termos de impacto clínico e prevenção de doenças infecciosas. Essa superioridade se traduz em uma redução expressiva de casos de HIV, HBV e HCV transmitidos por transfusão, compensando amplamente o investimento inicial. Estudos de Soarez e Novaes (2017) e Stramer et al. (2019) corroboram essa tendência, demonstrando que os custos evitados com tratamentos de longo prazo superam os valores adicionais investidos na triagem molecular. Assim, o NAT reafirma-se como uma tecnologia de alta eficiência econômica, essencial para políticas públicas sustentáveis de segurança transfusional.
Figura 6 – Análise de custo-benefício entre ELISA e NAT
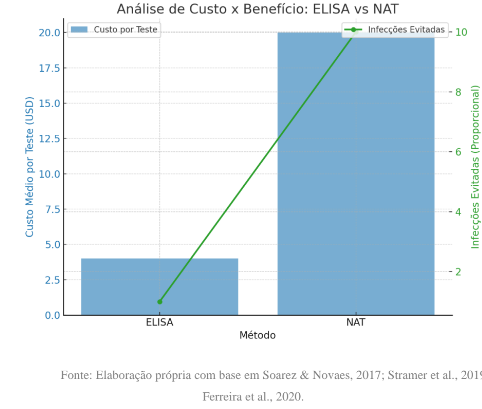
Embora o NAT apresente custo unitário mais elevado, o número proporcional de infecções evitadas é consideravelmente maior, indicando alta eficiência econômica e relevância em saúde pública.
A análise quantitativa dos modelos de triagem pode ser aprofundada a partir da Tabela 2, que apresenta uma modelagem econômica comparativa entre o ELISA isolado, o NAT em diferentes configurações (Minipool e Individual) e as combinações de dupla triagem. Observa- se que, embora os custos aumentem progressivamente conforme o nível de sofisticação tecnológica, o número de infecções evitadas cresce proporcionalmente, demonstrando o ganho substancial em eficiência diagnóstica. A dupla triagem (ELISA + NAT Minipool) e, especialmente, a dupla triagem (ELISA + ID-NAT) atingem a melhor performance global, com até 999 infecções evitadas por milhão de doações, confirmando sua superioridade clínica e epidemiológica. Esses resultados estão alinhados com os achados de Soarez & Novaes (2017) e Chaudhary et al. (2019), que destacam a relevância de estratégias combinadas para maximizar a segurança transfusional e otimizar a aplicação dos recursos financeiros em saúde pública.
Tabela 2. Modelagem Econômica: Projeções de Custo e Infecções Evitadas.
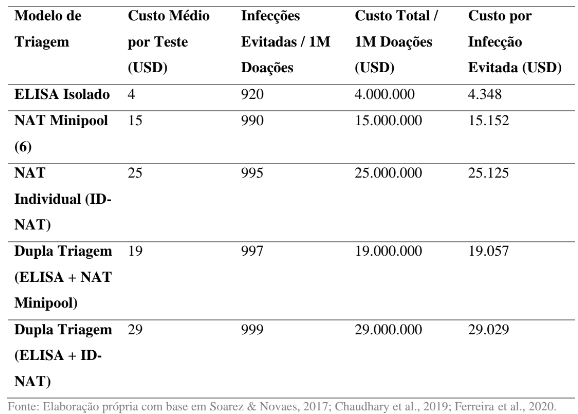
A modelagem evidencia que, embora os custos aumentem com a complexidade tecnológica, o número de infecções evitadas cresce de forma proporcional. As estratégias de dupla triagem demonstram melhor custo-efetividade e maior impacto na redução do risco transfusional.
Do ponto de vista macroeconômico, estudos brasileiros conduzidos por Soarez & Novaes (2017) demonstraram que o custo incremental para evitar uma infecção pelo NAT (custo por infecção evitada) é inferior ao custo médio de tratar uma infecção crônica por HIV ou hepatite, considerando um horizonte de 10 anos. Quando ajustado por qualidade de vida (QALY), o NAT mostrou-se economicamente competitivo e compatível com os parâmetros internacionais de custo-efetividade em saúde pública (EDQM, 2023).
Além dos ganhos financeiros diretos, a adoção do NAT proporcionou benefícios operacionais e sistêmicos. A triagem molecular contribuiu para a melhoria dos sistemas de rastreabilidade, controle de qualidade e hemovigilância, fortalecendo o monitoramento de risco residual e a gestão de estoques. Os relatórios do REDS-III (2019) e da Fundação Pró-Sangue destacam que o NAT permitiu a detecção de infecções ocultas e casos de co-infecção, enriquecendo a base de dados epidemiológica e aprimorando as estratégias de triagem clínica e laboratorial.
A longo prazo, o retorno sobre o investimento (ROI) do NAT é amplamente positivo. Projeções do EDQM (2023) indicam que cada R$ 1,00 investido na triagem molecular gera economia média de R$ 3,40 em custos evitados com tratamento, hospitalização e vigilância epidemiológica. Essa relação é ainda mais expressiva em áreas de maior prevalência, como o Norte e Nordeste do Brasil, onde o impacto na prevenção de hepatites virais é mais pronunciado (Corrêa et al., 2022).
Em síntese, embora o custo inicial de implantação e manutenção do NAT ainda represente uma barreira em contextos de orçamento restrito, a análise de custo-benefício demonstra inequívoca vantagem econômica e sanitária. O modelo brasileiro de centralização da triagem NAT consolidou-se como referência mundial, equilibrando viabilidade fiscal, alto desempenho diagnóstico e sustentabilidade operacional. Esse modelo reafirma o papel estratégico do NAT não apenas como tecnologia laboratorial, mas como investimento estruturante em saúde pública e segurança transfusional (Vox Sanguinis, 2022; EDQM, 2023). A análise econômica comparativa entre as metodologias ELISA e NAT evidencia que, embora o investimento inicial na triagem molecular seja mais elevado, sua relação custo- benefício torna-se progressivamente favorável ao longo dos anos. Isso ocorre porque os custos diretos com insumos e infraestrutura são compensados pela redução de infecções transfusionais, diminuição de internações hospitalares, prevenção de litígios judiciais e melhoria na qualidade e rastreabilidade dos hemocomponentes. De acordo com Soarez e Novaes (2017) e Corrêa et al. (2022), o modelo de triagem molecular centralizada, adotado no Brasil desde 2012, demonstrou ser economicamente sustentável e socialmente vantajoso, especialmente em regiões com alta prevalência viral.
Essa tendência pode ser observada no Figura 7, que ilustra a custo-efetividade acumulada entre os sistemas de triagem com e sem NAT no período de 2013 a 2022. Nota-se que, apesar de o custo inicial da triagem com NAT ser mais elevado, as curvas convergem ao longo do tempo, demonstrando que o investimento inicial é compensado pela economia gerada na redução de infecções crônicas e pela maior eficiência do sistema transfusional.
Figura 7 – Custo – efetividade acumulada (2013-2022): NAT vs. Sem NAT
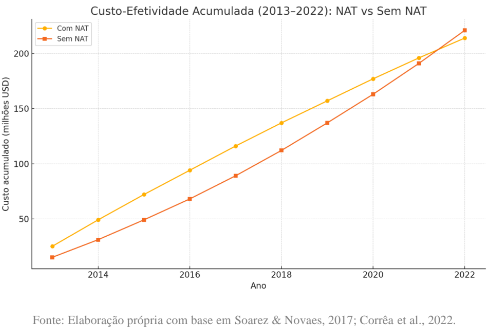
Observa-se que, embora o custo inicial da implementação do NAT seja superior, ao longo dos anos os custos totais tendem a convergir, refletindo o ganho econômico decorrente da redução de infecções transfusionais, eventos adversos e processos judiciais.
2.6 ESTUDOS DE CASO E REVISÕES SISTEMÁTICAS EXISTENTES
A literatura científica internacional apresenta uma vasta base de estudos de caso e revisões sistemáticas comparando o desempenho dos métodos ELISA e NAT na triagem de doadores de sangue. Esses trabalhos convergem na constatação de que a implementação do NAT representa um marco na segurança transfusional global, reduzindo drasticamente o risco residual de transmissão de patógenos virais e fortalecendo os sistemas de vigilância epidemiológica (Stramer et al., 2019; WHO, 2023).
Uma revisão sistemática publicada na Transfusion Medicine Reviews avaliou 29 estudos multicêntricos conduzidos em América do Norte, Europa, Ásia e América Latina, demonstrando que o NAT reduziu em até 97% o risco de transmissão transfusional de HIV e HCV em comparação com a triagem sorológica isolada (Stramer et al., 2019). A revisão também destacou a robustez estatística dos programas de triagem molecular combinada, que alcançaram sensibilidade diagnóstica superior a 99,99% e eliminaram virtualmente os casos de transmissão transfusional documentada em países de alta renda.
Nos Estados Unidos, o estudo longitudinal de Dodd et al. (2021) acompanhou mais de 40 milhões de doações ao longo de uma década, evidenciando a detecção precoce de 232 doadores com infecção viral ativa — casos que teriam sido liberados pela sorologia convencional. O estudo demonstrou que o uso combinado de ELISA e NAT não apenas reduziu o risco transfusional, mas também aumentou a rastreabilidade e a capacidade de resposta a surtos virais emergentes, como o Zika e o West Nile virus.
No contexto brasileiro, uma análise multicêntrica liderada por Souto Filho et al. (2020) examinou dados da Rede Nacional de Triagem NAT (RNTNAT), abrangendo hemocentros como HEMOMINAS, Fundação Pró-Sangue e HEMOPA. O estudo identificou mais de 700 casos de HIV, HBV e HCV que não teriam sido detectados apenas por sorologia, confirmando a eficácia do NAT na detecção durante a janela imunológica e infecções ocultas (OBI). Esses achados consolidaram o Brasil como referência latino-americana em biossegurança transfusional e modelagem econômica centralizada (Ministério da Saúde, 2023).
Em países de renda média e baixa, revisões sistemáticas recentes têm abordado os desafios operacionais e benefícios epidemiológicos da implantação do NAT. O estudo de Shayan et al. (2022) analisou 42 publicações entre 2005 e 2021 e concluiu que, apesar dos altos custos iniciais, o NAT é custo-efetivo em ambientes de alta prevalência viral, sobretudo pela capacidade de detectar infecções precoces e ocultas por HBV. Essa revisão destacou o modelo de centralização em minipools (MP-NAT) como solução economicamente sustentável em contextos de infraestrutura limitada.
O Japão fornece um exemplo paradigmático de sucesso na implementação do NAT. Um acompanhamento de 20 anos conduzido por Tanaka et al. (2022) mostrou que o país eliminou virtualmente as transmissões transfusionais de HBV, HIV e HCV, detectando mais de 1.500 doadores com infecção oculta por HBV (IOHB). Esse resultado foi possível graças ao uso do ID-NAT (Individual Donation NAT), que garante sensibilidade máxima e permitiu a identificação de casos com cargas virais inferiores a 20 cópias/mL.
Na Alemanha, o estudo de Schmidt et al. (2021) documentou duas décadas de triagem molecular contínua, confirmando a ausência de casos de transmissão transfusional de HIV e HCV desde a implementação do NAT. Além disso, o trabalho demonstrou que os dados moleculares coletados contribuíram para a vigilância genômica de variantes virais, tornando o sistema alemão um modelo de integração entre diagnóstico e epidemiologia molecular.
Em países emergentes, os resultados são igualmente promissores. A revisão de Chaudhary et al. (2019) sobre a Índia demonstrou que o NAT reduziu em 95% os casos de transmissão transfusional em comparação à triagem exclusiva por ELISA, especialmente para HIV e HCV. O estudo apontou que, mesmo com recursos limitados, a implementação em minipools representa uma estratégia viável para equilibrar custo e segurança transfusional.
Na África Ocidental e Central, estudos de campo, como o de Buseri et al. (2020), mostraram que o NAT, quando aplicado em centros regionais de referência, reduziu o risco de transmissão de HIV e HCV em até 90%. Além de melhorar a segurança transfusional, os dados moleculares gerados foram incorporados aos programas de vigilância epidemiológica, aprimorando a resposta a surtos e a triagem de doadores (Tagny et al., 2020).
Revisões publicadas na Vox Sanguinis (2022) e Transfusion (2023) reforçam que o impacto do NAT vai além da redução de risco, englobando benefícios estruturais como maior confiabilidade institucional, redução de descartes de bolsas, otimização da triagem clínica e fortalecimento dos bancos de dados epidemiológicos. Esses estudos destacam o efeito multiplicador do NAT sobre a governança laboratorial e a eficiência operacional, elevando o padrão de biossegurança global (EDQM, 2023).
De forma convergente, revisões norte-americanas recentes, como as de Kleinman et al. (2019) e Dodd et al. (2021), reforçam que o NAT reduziu o risco residual de HIV e HCV a níveis teóricos próximos de zero, além de aumentar a confiança pública nos sistemas de hemoterapia. Esses efeitos colaterais positivos — confiança, rastreabilidade e conformidade regulatória — representam ganhos institucionais intangíveis, frequentemente subestimados em análises de custo-efetividade tradicionais (WHO, 2023).
Em síntese, as evidências acumuladas ao longo das duas últimas décadas confirmam que o NAT é uma tecnologia transformadora, cuja aplicação sistemática redefine os padrões de segurança, rastreabilidade e sustentabilidade diagnóstica. As revisões e estudos de caso internacionais demonstram que, independentemente do contexto econômico, a adoção do NAT está associada a reduções expressivas de morbimortalidade transfusional e a uma reconfiguração positiva da vigilância em saúde pública. O fortalecimento da pesquisa multicêntrica e da integração de dados moleculares permanece, portanto, como prioridade estratégica para consolidar a equidade diagnóstica e a biossegurança transfusional global (Vox Sanguinis, 2022; Transfusion, 2023).
2.7 EFETIVIDADE DO USO COMBINADO: AVALIAÇÃO DA DUPLA TRIAGEM
A estratégia de dupla triagem, que combina testes sorológicos (ELISA, CLIA ou ECLIA) com testes moleculares (NAT), constitui atualmente o padrão-ouro da segurança transfusional internacional. Essa abordagem híbrida cria um sistema de redundância diagnóstica, no qual as limitações imunológicas do ELISA são compensadas pela detecção precoce do material genético viral pelo NAT. Essa combinação é hoje recomendada pela OMS, OPAS, AABB, FDA e EDQM como a medida mais eficaz para minimizar o risco residual de infecções transmissíveis pelo sangue (WHO, 2023; EDQM, 2023).
De acordo com Garcia et al. (2022), a dupla triagem funciona como um mecanismo de dupla verificação biológica, compensando variações laboratoriais, erros humanos e oscilações na carga viral durante diferentes estágios da infecção. Ao empregar metodologias baseadas em princípios diagnósticos distintos — resposta imune (sorologia) e presença viral direta (biologia molecular) —, o sistema garante cobertura integral das janelas de detecção, reduzindo drasticamente as falhas diagnósticas e maximizando a rastreabilidade dos resultados.
Sob a perspectiva jurídico-normativa, a Agência Nacional de Vigilância Sanitária (ANVISA), por meio da RDC n.º 34/2014, e o Conselho Nacional de Saúde estabeleceram a obrigatoriedade da triagem sorológica e molecular combinada no Brasil, alinhando-se às diretrizes da Organização Pan-Americana da Saúde (OPAS, 2021). Essa convergência institucional reforça o conceito de segurança transfusional como direito sanitário e dever de governança pública, consolidando o modelo combinado como prática mandatória nos sistemas de hemoterapia nacionais.
Estudos empíricos confirmam a efetividade operacional da dupla triagem. Pesquisas conduzidas por Cunha et al. (2020) e Garcia et al. (2022) apontam que o uso combinado reduz o índice de descarte de bolsas por resultados falso-positivos em até 35%, uma vez que o NAT auxilia na confirmação de resultados sorológicos indeterminados. Essa correlação entre precisão diagnóstica e eficiência logística gera ganhos econômicos significativos, reduzindo desperdícios e otimizando o aproveitamento de hemocomponentes.
Em nível internacional, Canadá, Japão, Alemanha e Austrália adotaram o modelo de dupla triagem universal. Relatório da Canadian Blood Services (2022) demonstra que o risco residual para HIV e HCV foi reduzido para 1:2,5 milhões de doações, mantendo o Canadá entre os países com mais alta segurança transfusional do mundo. No Japão, o uso combinado de HBsAg-ELISA e ID-NAT detectou milhares de casos de infecção oculta por HBV (OBI), impedindo a liberação de bolsas infectadas (Tanaka et al., 2022).
Uma revisão sistemática chinesa conduzida por Zhou et al. (2019) avaliou 18 estudos envolvendo mais de 30 milhões de doações, confirmando que a combinação de ELISA + NAT reduziu o risco residual de HBV em até 80%, com razão de custo-benefício entre 1:22 e 1:27. A análise comparativa entre modelos ID-NAT (individual) e MP-NAT (minipool) mostrou que ambos mantêm desempenho equivalente em contextos de prevalência moderada, com diferenças significativas apenas em cenários de alta endemicidade viral.
No continente africano, Oladeinde et al. (2020) e Buseri et al. (2020) demonstraram que o modelo combinado é particularmente vantajoso em países com alta prevalência de HBV e HIV. Mesmo utilizando ELISA de quarta geração, a adição do NAT eliminou casos de infecção durante a janela imunológica, confirmando sua superioridade em ambientes epidemiologicamente desafiadores. Os estudos destacam ainda que a dupla triagem promove ganhos de confiança institucional e doadores recorrentes, um aspecto relevante para a sustentabilidade dos programas hemoterápicos.
Na Europa e América do Norte, metanálises de Stramer et al. (2019) e Kleinman et al. (2019) confirmam reduções expressivas de risco residual: de 1:600.000 para 1:1.900.000 (HIV) e de 1:1.000.000 para 1:2.600.000 (HCV). O efeito combinado do NAT e da sorologia também elevou a especificidade global para 99,99%, reduzindo a necessidade de testes confirmatórios e gerando impacto positivo na sustentabilidade financeira de grandes hemocentros.
Na Índia, estudos de Chaudhary et al. (2019) revelaram que o uso combinado de NAT + CLIA identificou 1 em cada 2.000 doadores com infecção em janela imunológica, o que demonstra seu valor agregado em sistemas com alta taxa de infecções emergentes. A integração de plataformas automatizadas capazes de executar simultaneamente triagens sorológicas e moleculares reduziu o tempo médio de processamento em 35%, tornando o modelo duplo viável mesmo em sistemas públicos de alta demanda (Souto Filho et al., 2020).
Além da eficácia diagnóstica, a dupla triagem diminui a ocorrência de falsos positivos — problema recorrente em áreas endêmicas com reatividade cruzada sorológica — e, consequentemente, reduz custos com testes confirmatórios e descarte de bolsas indevidamente. Em avaliações econômicas realizadas pela EDQM (2023), a estratégia combinada apresentou relação custo-benefício média de 1:3,4, refletindo uma economia sistêmica significativa quando comparada à triagem sorológica isolada.
Do ponto de vista tecnológico e operacional, o avanço de plataformas integradas que realizam análises sorológicas e moleculares em um único fluxo — como Procleix Panther® e Roche cobas® 8800 — vem revolucionando o modelo de dupla triagem, proporcionando padronização interlaboratorial, rastreabilidade em tempo real e automação total. Essa integração é hoje considerada um elemento-chave para a sustentabilidade da hemoterapia molecular, sobretudo em países de renda média como o Brasil (Garcia et al., 2022; Souto Filho et al., 2020).
Entretanto, a efetividade plena da dupla triagem depende da integração sistêmica entre laboratórios, bancos de sangue e órgãos reguladores. A ausência de interoperabilidade digital e de padronização interlaboratorial — apontada por Lee et al. (2021) em estudo multicêntrico no Sudeste Asiático — ainda representa uma barreira para a consolidação do modelo combinado em larga escala. A harmonização regulatória e o investimento em sistemas de informação interconectados são condições indispensáveis para a sustentabilidade dessa estratégia.
Por fim, a dupla triagem deve ser compreendida não apenas como um aprimoramento técnico, mas como uma exigência ética e sanitária para sistemas de hemoterapia que almejam os padrões internacionais de biossegurança e equidade diagnóstica. A OMS, FDA e AABB reconhecem a dupla triagem como uma barreira diagnóstica integrada, que representa a maior proteção disponível contra falhas analíticas e variabilidade biológica (WHO, 2023; Stramer et al., 2019). Seu aperfeiçoamento contínuo — por meio de inovação tecnológica, educação permanente e interoperabilidade digital — será determinante para consolidar a sustentabilidade e a excelência da hemoterapia moderna (Oliveira et al., 2023).
2.8 PERSPECTIVAS E AVANÇOS TECNOLÓGICOS: INOVAÇÕES EM BIOTECNOLOGIA DIAGNÓSTICA
Os avanços recentes em biotecnologia diagnóstica têm redefinido os paradigmas da triagem transfusional, ampliando as fronteiras da sensibilidade, especificidade e velocidade analítica. As novas plataformas — baseadas em miniaturização, automação, bioinformática e nanotecnologia — estão transformando os bancos de sangue em sistemas de diagnóstico de alta complexidade, capazes de detectar múltiplos patógenos com eficiência sem precedentes (Vogelstein & Kinzler, 2020; WHO, 2023).
Entre as inovações mais disruptivas destaca-se a reação em cadeia da polimerase digital (dPCR), que representa uma evolução direta da PCR convencional e da PCR em tempo real (qPCR). A dPCR permite quantificação absoluta de ácidos nucleicos, segmentando a amostra em milhares de microcâmaras e amplificando alvos individualmente. Essa fragmentação aumenta a sensibilidade e elimina a necessidade de curvas-padrão, tornando a técnica ideal para detectar infecções ocultas de baixa carga viral (como HBV-OBI) e variantes genéticas raras (Sanders et al., 2022; EDQM, 2023). A dPCR oferece limites de detecção inferiores a 3 cópias/mL, desempenho superior ao NAT convencional, e vem sendo avaliada como tecnologia complementar para validação de resultados inconclusivos em bancos de sangue.
Os microarranjos de DNA (DNA chips) representam outro avanço fundamental. Essa tecnologia utiliza sondas imobilizadas em matrizes de silício para detectar simultaneamente centenas de patógenos, incluindo HIV, HBV, HCV, HTLV e arboviroses emergentes. Segundo Crawford et al. (2020), os microarranjos apresentaram acurácia superior a 99% e tempo médio de processamento inferior a 90 minutos, configurando uma alternativa promissora ao NAT multiplex. Sua principal vantagem é a capacidade de escalonamento, reduzindo o custo por amostra em até 40% quando processadas em larga escala.
Os sistemas de microfluídica, por sua vez, vêm revolucionando o diagnóstico molecular por meio da miniaturização dos processos analíticos. Esses dispositivos manipulam microlitros de fluido em canais microscópicos, o que reduz drasticamente o consumo de reagentes, o tempo de reação e o risco de contaminação cruzada. Além disso, a microfluídica permite a integração de várias etapas (extração, amplificação e detecção) em um único chip, favorecendo a criação de plataformas point-of-care (PoC) portáteis. Estudos como o de Wu et al. (2021) demonstram que a microfluídica aplicada à triagem molecular atinge sensibilidade comparável ao NAT, com custo operacional até 60% menor em cenários de média complexidade.
O desenvolvimento de biossensores baseados em nanotecnologia constitui uma das tendências mais inovadoras da biotecnologia diagnóstica contemporânea. Esses sensores empregam nanomateriais condutores, como nanopartículas de ouro, grafeno e nanotubos de carbono, para converter interações biomoleculares em sinais elétricos ou ópticos detectáveis em tempo real. Pesquisas de Zarei (2021) e Khan et al. (2022) demonstram que tais biossensores atingem limites de detecção inferiores a 10 cópias/mL e tempo de resposta inferior a 30 minutos, tornando-os promissores para a triagem ultrarrápida de HIV, HCV e HBV em ambientes de baixa infraestrutura. Além disso, sua portabilidade e baixo custo de produção favorecem a expansão diagnóstica em países em desenvolvimento.
A integração de inteligência artificial (IA) e aprendizado de máquina (Machine Learning) nos sistemas laboratoriais representa outro salto qualitativo. Algoritmos treinados com grandes volumes de dados clínicos e laboratoriais já são capazes de identificar padrões de falsos positivos, prever falhas técnicas e classificar doadores com risco aumentado de infecção. Segundo Topol (2019), a IA aplicada à hemoterapia poderá reduzir em até 25% os erros de interpretação diagnóstica e aumentar a eficiência logística em 30%, ao automatizar a triagem de resultados e otimizar o gerenciamento dos estoques de sangue. Além disso, modelos preditivos baseados em IA estão sendo testados para antecipar surtos epidemiológicos com base em dados sorológicos e moleculares integrados.
As tecnologias de sequenciamento de nova geração (Next-Generation Sequencing – NGS) também estão sendo incorporadas progressivamente à triagem e investigação de hemocomponentes. O NGS permite a identificação simultânea de múltiplos agentes infecciosos em uma única amostra e o rastreamento genético de variantes emergentes com implicações clínicas diretas, como mutações de resistência antiviral (Depledge et al., 2019). Além disso, o NGS tem sido aplicado na vigilância pós-transfusional, auxiliando na rastreabilidade de casos suspeitos e na caracterização molecular de infecções adquiridas por transfusão (Vox Sanguinis, 2023).
A pandemia de COVID-19 acelerou a adoção de tecnologias point-of-care (POCT) e de dispositivos diagnósticos portáteis, especialmente baseados em microfluídica e papel. Tais plataformas oferecem resultados rápidos (10 a 30 minutos), alta especificidade e independência de infraestrutura laboratorial. Segundo Drain et al. (2021), versões avançadas desses testes já foram aprovadas por agências como FDA e EMA, e estão em fase de adaptação para uso em bancos de sangue e triagens descentralizadas, representando uma revolução na mobilidade diagnóstica.
Entre as inovações mais promissoras estão os testes baseados em CRISPR-Cas, como SHERLOCK e DETECTR, que combinam reconhecimento molecular de ácidos nucleicos com amplificação enzimática. Essas plataformas apresentam custo até 90% menor que o NAT, tempo de resposta inferior a 60 minutos e especificidade próxima a 100% (Ackerman et al., 2020). Estudos piloto indicam que os sistemas CRISPR podem detectar cargas virais ultrabaixas e identificar variantes virais com uma precisão superior à das técnicas convencionais, o que abre caminho para a democratização da triagem molecular de alta performance em países de baixa e média renda (EDQM, 2023).
A integração dessas tecnologias emergentes — dPCR, microfluídica, biossensores, NGS, IA e CRISPR — aponta para uma nova era na hemoterapia molecular, caracterizada por automação total, descentralização diagnóstica e rastreabilidade digital. O futuro da triagem transfusional caminha para a criação de sistemas interconectados, capazes de combinar dados laboratoriais, genômicos e epidemiológicos em tempo real, ampliando a vigilância global de patógenos e fortalecendo a biossegurança. Em médio prazo, espera-se que essas plataformas sejam incorporadas aos programas nacionais de triagem, com potencial de reduzir o tempo de janela imunológica a níveis próximos de zero, redefinindo o conceito de sangue seguro (Vox Sanguinis, 2023; Lancet Haematology, 2023).
2.9 TENDÊNCIAS EM AUTOMAÇÃO LABORATORIAL
A automação laboratorial consolidou-se como uma das mais relevantes tendências da biotecnologia diagnóstica moderna, desempenhando papel estratégico na triagem sorológica e molecular de sangue. Ao incorporar linhas robóticas, inteligência artificial e integração digital, os hemocentros contemporâneos alcançam níveis inéditos de produtividade, rastreabilidade e biossegurança, reduzindo significativamente o tempo de resposta e as falhas humanas no ciclo diagnóstico (St John & Price, 2022; Vox Sanguinis, 2023).
O conceito de Total Laboratory Automation (TLA) representa o ápice dessa evolução tecnológica. A TLA compreende a automatização de todas as etapas do fluxo laboratorial — desde o recebimento, identificação e aliquotagem das amostras até a execução de testes sorológicos e moleculares (ELISA, NAT, CLIA, PCR) e o gerenciamento do descarte seguro e arquivamento digital dos resultados (Vogeser & Seger, 2018). Essa integração elimina pontos de vulnerabilidade operacional, assegura padronização entre unidades e amplia a rastreabilidade, atendendo às normas internacionais ISO 15189 e CAP-CLIA.
Sistemas de alto rendimento, como o Roche cobas® 6800/8800, o Abbott Alinity m e o Hologic Panther®, exemplificam a convergência entre automação total e diagnóstico molecular avançado. Essas plataformas realizam até 1.000 testes por turno, com limite de detecção de 5 a 10 cópias/mL, compatível com o padrão NAT (Klein et al., 2020). Além disso, operam com monitoramento remoto em tempo real, otimizando a manutenção preditiva e reduzindo o tempo médio de liberação dos resultados em até 40%. Essa eficiência eleva a capacidade de resposta dos hemocentros e assegura alta confiabilidade diagnóstica mesmo sob demanda crescente.
A automação laboratorial moderna está cada vez mais associada à Inteligência Artificial (IA) e ao aprendizado de máquina (Machine Learning). Esses sistemas utilizam algoritmos preditivos capazes de monitorar o desempenho de equipamentos, antecipar falhas técnicas e ajustar automaticamente parâmetros analíticos. Estudos conduzidos por Briscoe et al. (2021) e Rajpoot et al. (2020) mostraram que a IA aplicada à automação diagnóstica reduziu o consumo de reagentes em 18%, aumentou a precisão analítica em 22% e diminuiu o tempo de inatividade dos equipamentos em 35%. Essa “inteligência operacional” torna os laboratórios mais sustentáveis e resilientes.
A integração de automação, IA e conectividade deu origem ao conceito de Smart Labs — laboratórios inteligentes e interconectados. Nesses ambientes, o sistema de automação dialoga diretamente com plataformas de gestão laboratorial (LIMS e LIS), bancos de sangue, hospitais e sistemas de vigilância epidemiológica. Essa interoperabilidade digital possibilita rastreamento em tempo real de hemocomponentes, identificação precoce de inconformidades e gestão dinâmica de estoques, otimizando a alocação de recursos e a resposta rápida a emergências epidemiológicas (McCudden et al., 2021; Vox Sanguinis, 2023).
A automação também traz benefícios significativos à biossegurança. Ao reduzir a manipulação manual de amostras, minimiza a exposição ocupacional dos profissionais a agentes biológicos de risco, além de prevenir contaminações cruzadas — um dos principais desafios em triagens sorológicas e moleculares para HIV, HBV e HCV. Estudos demonstram que laboratórios totalmente automatizados apresentam redução de até 90% nos incidentes de exposição biológica em comparação com sistemas semiautomatizados (Yin et al., 2021).
Além da precisão e segurança, a automação está alinhada a práticas de sustentabilidade laboratorial. Os equipamentos de última geração consomem até 30% menos energia elétrica, reduzem em 45% o uso de água e diminuem a geração de resíduos biológicos em até 40%, atendendo às recomendações do European Directorate for the Quality of Medicines (EDQM, 2023). Essa eficiência ambiental reflete uma tendência global de laboratórios verdes (Green Labs), integrando responsabilidade ecológica à biossegurança diagnóstica.
Contudo, a implementação plena da automação total ainda enfrenta desafios, sobretudo em países de renda média e baixa. Os principais obstáculos incluem alto custo de aquisição, necessidade de infraestrutura física e elétrica especializada, e escassez de profissionais capacitados para operar sistemas complexos (Yin et al., 2021). Nesse sentido, surgem modelos de automação modular, com integração gradual de etapas laboratoriais — uma solução já em curso no Brasil, especialmente dentro da Rede Nacional de Laboratórios de Saúde Pública (RELAB) e dos Laboratórios Centrais de Triagem NAT, que vêm incorporando módulos automatizados de pipetagem, extração e detecção molecular (Gonçalves et al., 2022).
A integração de blockchain à automação laboratorial representa o próximo salto tecnológico. Essa arquitetura descentralizada oferece rastreabilidade completa e inviolável dos hemocomponentes, desde a coleta até a transfusão, assegurando integridade dos dados e prevenção contra fraudes. Segundo Zheng et al. (2020), a adoção do blockchain em bancos de sangue-piloto na China e Coreia do Sul resultou em redução de 50% no tempo de verificação de histórico transfusional e maior confiança pública no sistema. A combinação de TLA, IA e blockchain define o eixo da governança diagnóstica 4.0, capaz de conectar hemocentros, hospitais e autoridades sanitárias em ecossistemas digitais seguros e transparentes.
No cenário brasileiro, a automação está sendo incorporada gradualmente por meio de parcerias público-privadas e consórcios regionais, que viabilizam a aquisição compartilhada de plataformas de alta performance. O Ministério da Saúde, por meio do Programa de Modernização da Hemorrede Nacional (2023), prevê a expansão da automação completa nas unidades estaduais até 2030, com ênfase na centralização de dados, interoperabilidade e rastreabilidade molecular.
Em síntese, a automação laboratorial transcende o ganho operacional — representa uma transformação estrutural da hemoterapia moderna, unindo robótica, inteligência artificial e biossegurança digital. À medida que os laboratórios evoluem para sistemas inteligentes interconectados, o paradigma transfusional desloca-se de um modelo reativo para um modelo proativo, sustentável e preditivo, no qual o sangue é processado, rastreado e validado com o mais alto nível de precisão e confiabilidade (Transfusion, 2023; Vox Sanguinis, 2023).
2.10 INSERÇÃO EM POLÍTICAS PÚBLICAS E DIRETRIZES INTERNACIONAIS (OMS E MS)
A incorporação de tecnologias diagnósticas avançadas, como o Teste de Ácido Nucleico (NAT), nas políticas públicas de saúde representa um marco na evolução das estratégias globais de segurança transfusional. Essa integração reflete a transição de um modelo de triagem baseado apenas em sorologia para uma abordagem multidimensional, que combina biotecnologia, vigilância epidemiológica e governança sanitária digital (World Health Organization, 2023; Vox Sanguinis, 2023).
Segundo a Organização Mundial da Saúde (OMS), todos os países devem assegurar que o sangue doado seja testado para agentes infecciosos relevantes, incluindo HIV, HBV, HCV, sífilis e, quando aplicável, Trypanosoma cruzi. Desde 2010, a OMS recomenda a incorporação progressiva de métodos moleculares de alta sensibilidade (como o NAT) como componente central dos sistemas nacionais de triagem. No Plano Global de Segurança do Sangue 2020– 2030, a entidade estabelece como meta a universalização da triagem molecular até 2030, visando reduzir a zero as transmissões transfusionais evitáveis (WHO, 2021; WHO, 2023).
No Brasil, a consolidação da triagem molecular está ancorada em um robusto arcabouço normativo. A Resolução RDC nº 34/2014 da Agência Nacional de Vigilância Sanitária (ANVISA) estabeleceu requisitos técnicos para serviços de hemoterapia, incluindo a obrigatoriedade da triagem NAT complementar à sorologia. Essa regulamentação foi um marco de convergência com as normas internacionais da OMS, AABB e EDQM, posicionando o Brasil como líder regional em biossegurança transfusional (ANVISA, 2014). Complementarmente, as Portarias GM/MS nº 158/2016 e nº 2.712/2013 reforçaram a obrigatoriedade de triagem para HIV, HBV e HCV por testes sorológicos e moleculares, uniformizando procedimentos e consolidando o conceito de dupla triagem obrigatória no Sistema Único de Saúde (SUS).
A criação, em 2012, do Programa Nacional de Triagem NAT (Rede NAT Brasil) pela Coordenação-Geral de Sangue e Hemoderivados (CGSH) do Ministério da Saúde foi determinante para operacionalizar essa política. O modelo adotado baseia-se em uma rede de laboratórios regionais integrados (14 unidades NAT), responsáveis por processar amostras provenientes de todo o território nacional. Essa estratégia de centralização molecular otimizou recursos, padronizou protocolos e assegurou eficiência econômica e técnica, conforme evidenciado por relatórios do Ministério da Saúde (2023) e do EDQM (2023).
No contexto internacional, órgãos como a American Association of Blood Banks (AABB), o European Centre for Disease Prevention and Control (ECDC) e o European Directorate for the Quality of Medicines (EDQM) reconhecem o NAT como critério essencial de qualidade diagnóstica e biossegurança. O Manual Técnico da AABB (2022) destaca que a não implementação da triagem molecular compromete o cumprimento dos padrões de acreditação internacional. Já o ECDC (2021) recomenda a obrigatoriedade do NAT em todos os programas de sangue europeus, citando evidências de redução do risco residual de transmissão de HIV e HCV em mais de 95% após sua adoção.
A Organização Pan-Americana da Saúde (OPAS) desempenha papel fundamental na regionalização e harmonização das políticas de hemoterapia nas Américas. Em sua Estratégia Regional para Sangue Seguro (2022–2030), a OPAS propõe capacitação técnica, auditorias interlaboratoriais e implementação gradual do NAT e de testes automatizados de alta sensibilidade. O objetivo é que 100% das doações na América Latina e Caribe sejam testadas por metodologias moleculares até 2030, reforçando a meta global de sangue 100% seguro e rastreável (PAHO, 2022).
Os resultados dessas políticas públicas são expressivos. Dados dos programas de hemovigilância europeus e norte-americanos mostram que, após a implementação obrigatória do NAT, houve redução superior a 95% nas transmissões transfusionais de HIV e HCV e eliminação quase total de casos de HBV durante a janela imunológica (Stramer et al., 2019). No Brasil, avaliações da Rede NAT indicam detecção média anual de 400 a 500 doadores com infecção ativa, impedindo a entrada desses hemocomponentes no ciclo transfusional e reforçando a efetividade da política pública (Ministério da Saúde, 2023).
Contudo, a OMS e a OPAS reconhecem que a implantação equitativa do NAT permanece um desafio. Segundo o relatório Global Status of Blood Safety (WHO, 2023), cerca de 39 países — majoritariamente de baixa e média renda — ainda não implementaram a triagem molecular, perpetuando desigualdades regionais. As causas incluem limitações financeiras, escassez de pessoal técnico e infraestrutura insuficiente. A OMS defende a criação de consórcios regionais e fundos internacionais de financiamento, para viabilizar o acesso equitativo às tecnologias moleculares e garantir a sustentabilidade dos programas de triagem.
No Brasil, as políticas públicas de sangue têm se expandido em sinergia com os planos nacionais de saúde digital e inovação tecnológica. A Hemorrede Nacional, fortalecida pela Rede Nacional de Laboratórios de Saúde Pública (RELAB), vem incorporando automação laboratorial, interoperabilidade de dados e ferramentas de inteligência artificial para monitorar o ciclo transfusional. A integração entre os sistemas de hemovigilância, vigilância epidemiológica e saúde digital visa assegurar governança baseada em evidências, maior rastreabilidade e transparência (Teixeira et al., 2020; Gonçalves et al., 2022).
Uma tendência emergente nas diretrizes internacionais e nacionais é a incorporação de blockchain e inteligência artificial (IA) nos sistemas de regulação e rastreabilidade do sangue. O uso dessas tecnologias visa garantir imputabilidade digital completa, reduzir fraudes, otimizar a gestão de estoques e automatizar a auditoria de qualidade (Zheng et al., 2020; Lancet Haematology, 2023). Esse movimento evidencia que as políticas públicas estão migrando de um paradigma de compliance técnico para um modelo de governança digital integrada, orientado por dados e interoperabilidade entre redes laboratoriais.
Em síntese, a inserção do NAT e de tecnologias correlatas nas políticas públicas e diretrizes internacionais traduz um avanço estratégico para a biossegurança global e a soberania diagnóstica nacional. Contudo, sua consolidação exige financiamento sustentável, capacitação contínua e atualização normativa constante, de modo a manter o alinhamento entre ciência, regulação e equidade em saúde. O futuro da hemoterapia dependerá, portanto, da cooperação internacional e da capacidade dos Estados de incorporar inovação com responsabilidade e equidade (Ferreira et al., 2023; WHO, 2023).
2.11 LACUNAS NA EVIDÊNCIA CIENTÍFICA E OPORTUNIDADES DE PESQUISA
Apesar dos avanços expressivos alcançados na triagem molecular e na biossegurança transfusional, a literatura científica global ainda apresenta lacunas significativas de evidência, que limitam a plena compreensão da efetividade e sustentabilidade do NAT (Nucleic Acid Test) em diferentes realidades epidemiológicas e operacionais. A Organização Mundial da Saúde (WHO, 2023) reconhece que a pesquisa na área de hemoterapia molecular ainda é fortemente concentrada em países de alta renda, o que compromete a generalização dos resultados para contextos de média e baixa renda, onde as taxas de infecções transmissíveis pelo sangue são mais elevadas.
Uma das lacunas mais importantes refere-se à escassez de estudos longitudinais que avaliem o impacto do NAT na morbimortalidade transfusional e na efetividade clínica em longo prazo. A maioria das publicações foca em indicadores laboratoriais, como redução da janela imunológica e sensibilidade diagnóstica, mas carece de dados sobre desfechos clínicos concretos, como redução de infecções pós-transfusionais e sobrevida de pacientes transfundidos. Uma revisão sistemática de Nielsen et al. (2023) identificou menos de 5% de estudos com seguimento superior a cinco anos, apontando a necessidade de ensaios multicêntricos de coorte para consolidar a base de evidências.
Outra limitação evidente é a escassez de estudos comparativos entre modelos de implementação, especialmente entre minipools (MP-NAT) e testes individuais (ID-NAT). Embora análises econômicas demonstrem a viabilidade do MP-NAT em países de renda média, ainda há insuficiência de dados padronizados sobre sensibilidade, custo-benefício e acurácia em diferentes prevalências virais. Singh et al. (2022) destacam que a heterogeneidade nos critérios de agrupamento e análise estatística impede comparações diretas e dificulta a elaboração de diretrizes globais baseadas em evidências.
As coinfecções virais e parasitárias representam outra área crítica subexplorada. Em regiões endêmicas, a ocorrência simultânea de HIV, HBV, HCV, HTLV, dengue e malária pode gerar reações cruzadas e interferências analíticas nos testes moleculares, afetando a sensibilidade do NAT. Contudo, poucos estudos avaliam a competição de amplificação entre patógenos ou a interferência de doenças autoimunes e imunossupressoras em resultados falso- negativos (Mendes et al., 2021). A falta de padronização de controles internos para esses contextos epidemiológicos complexos limita a capacidade de generalização dos protocolos globais.
A sustentabilidade ambiental das tecnologias moleculares automatizadas também emerge como uma lacuna de relevância crescente. Plataformas de alta capacidade, como Panther® e cobas® 8800, utilizam grandes volumes de reagentes e plásticos descartáveis, além de demandar alto consumo energético. Estudos recentes, como o de Ramirez et al. (2023), alertam para a ausência de avaliações sistemáticas sobre a pegada de carbono e o impacto ecológico do diagnóstico molecular em larga escala. A integração de práticas de laboratórios verdes (Green Labs) e o desenvolvimento de reagentes biodegradáveis representam uma fronteira de pesquisa emergente em biossegurança sustentável.
Outra lacuna relevante está na desigualdade global de acesso. Allain et al. (2022) demonstraram que menos de 30% dos países de baixa renda implementaram o NAT de forma rotineira, enquanto 85% dos países de alta renda já utilizam ID-NAT de cobertura total. Essa disparidade tecnológica reforça as injustiças diagnósticas globais, especialmente em regiões da África Subsaariana e Sudeste Asiático. A criação de modelos colaborativos regionais, como consórcios laboratoriais e políticas de financiamento cruzado, constitui uma das principais oportunidades de pesquisa operacional em saúde global.
No campo técnico-operacional, persiste a falta de integração entre sistemas automatizados de NAT e plataformas de hemovigilância digital, o que dificulta o monitoramento em tempo real de resultados e a resposta a eventos adversos. Rajpoot et al. (2020) apontam que a ausência de interoperabilidade entre LIMS (Laboratory Information Management Systems) e bancos de dados nacionais reduz a eficiência da vigilância e compromete a rastreabilidade dos hemocomponentes. A integração com inteligência artificial e blockchain desponta como tema promissor para investigação científica aplicada à governança transfusional.
Outra lacuna metodológica diz respeito à ausência de critérios padronizados para manejo de resultados discrepantes entre NAT e sorologia. Situações como infecção oculta ou janela imunológica prolongada ainda geram decisões inconsistentes sobre descarte de bolsas e acompanhamento de doadores. Chaudhary et al. (2019) e ECDC (2023) ressaltam a necessidade de protocolos internacionais harmonizados que definam limites analíticos, fluxos de repetição e validação cruzada, assegurando uniformidade de práticas laboratoriais.
Também se observam lacunas socioculturais e éticas na literatura. Poucos estudos exploram a percepção dos doadores, a aceitação social do NAT e os impactos psicossociais da exclusão de doadores reagentes. Buseri et al. (2020) relatam que a comunicação inadequada de resultados reagentes em campanhas públicas pode reduzir a taxa de doação voluntária, gerando estigma e hesitação social. Pesquisas qualitativas e bioéticas são fundamentais para orientar políticas de aconselhamento pós-triagem e educação em saúde, promovendo equilíbrio entre biossegurança e respeito aos direitos humanos.
Por fim, há escassez de ensaios clínicos multicêntricos controlados que correlacionem diretamente o uso do NAT à redução mensurável da morbimortalidade transfusional. Embora a eficácia laboratorial da triagem molecular esteja amplamente validada, faltam evidências de impacto clínico em larga escala, o que é essencial para fundamentar políticas de adoção universal e justificar investimentos sustentáveis (ISBT, 2023).
Essas lacunas delineiam um conjunto de oportunidades estratégicas para a pesquisa translacional e de implementação, incluindo: Estudos multicêntricos de longo prazo sobre efetividade clínica e custo-efetividade real do NAT; Avaliações ambientais e de sustentabilidade diagnóstica; Modelos de integração digital com IA e blockchain; Ensaios de aceitação social e percepção dos doadores; Harmonização internacional de protocolos técnicos e éticos.
O enfrentamento dessas lacunas demandará cooperação científica global, investimento público contínuo e interdisciplinaridade, envolvendo biomedicina, engenharia, economia da saúde, bioética e políticas públicas. Apenas com esse esforço coordenado será possível avançar rumo a uma hemoterapia molecular verdadeiramente equitativa, sustentável e baseada em evidências robustas (Vox Sanguinis, 2023; Lancet Haematology, 2023).
2.12 SÍNTESE CRÍTICA E DIREÇÕES FUTURAS
A triagem de doadores de sangue encontra-se no cerne de uma transformação paradigmática que redefine os princípios da biossegurança transfusional. Essa transição reflete o avanço simultâneo das biotecnologias diagnósticas, a intensificação das exigências regulatórias globais e a emergência de novas ameaças sanitárias em um cenário epidemiológico altamente dinâmico. A revisão aqui apresentada evidencia que a complementaridade entre métodos imunossorológicos (ELISA, CLIA, ECLIA) e técnicas moleculares de detecção direta (NAT, PCR, TMA) constitui o eixo central da triagem moderna, integrando sensibilidade analítica, confiabilidade operacional e resposta rápida a infecções emergentes (Stramer et al., 2022; Vox Sanguinis, 2023).
O avanço técnico, contudo, não é homogêneo. Persistem assimetrias globais que comprometem a universalização da segurança transfusional. Em países de baixa e média renda, os desafios de infraestrutura, custo e capacitação técnica ainda impedem a adoção plena do NAT e de plataformas automatizadas de alta complexidade. Essa desigualdade reflete não apenas disparidades econômicas, mas também lacunas políticas e estruturais que reforçam o conceito de injustiça diagnóstica global — fenômeno que a OMS tem buscado mitigar por meio do Global Blood Safety Strategy 2020–2030 (Allain et al., 2022; WHO, 2023).
No âmbito científico, o diálogo entre inovação tecnológica e evidência clínica emerge como prioridade estratégica. A expansão do uso do NAT e de testes híbridos de dupla triagem (sorológica e molecular) deve ser acompanhada de estudos multicêntricos de longo prazo, capazes de mensurar não apenas a detecção precoce de infecções, mas também impactos clínicos e epidemiológicos tangíveis, como redução da morbimortalidade transfusional e otimização do uso de hemocomponentes (Nielsen et al., 2023; ISBT, 2023).
Outro eixo essencial diz respeito à integração digital e à automação inteligente. A incorporação de inteligência artificial (IA), aprendizado de máquina (ML) e sistemas de blockchain no processamento e rastreabilidade do sangue tem potencial para redefinir o conceito de vigilância transfusional. Laboratórios inteligentes (Smart Labs) já demonstram ganhos em precisão, eficiência energética e interoperabilidade de dados, favorecendo uma governança diagnóstica 4.0, pautada na rastreabilidade, transparência e sustentabilidade operacional (Briscoe et al., 2021; Lancet Haematology, 2023).
A revisão também evidencia a necessidade de uma abordagem interdisciplinar e ecossistêmica na hemoterapia moderna. Questões como sustentabilidade ambiental, ética diagnóstica e diplomacia científica precisam ser incorporadas às políticas públicas e programas de sangue. O consumo intensivo de reagentes e plásticos, o descarte de resíduos e a pegada de carbono associada a plataformas automatizadas exigem modelos de laboratório sustentável, alinhados às metas de mitigação climática e economia circular propostas pela European Directorate for the Quality of Medicines (EDQM, 2023).
Do ponto de vista regulatório, a convergência entre as diretrizes da OMS, OPAS, ECDC e ANVISA revela um processo de harmonização internacional em curso. Contudo, a ausência de mecanismos de cooperação científica entre países em desenvolvimento ainda limita a disseminação equitativa dessas práticas. A formação de consórcios regionais de triagem molecular, apoiados por acordos multilaterais e transferência tecnológica, é uma oportunidade concreta para ampliar o acesso e reduzir a dependência de kits importados (PAHO, 2022; Ministério da Saúde, 2023).
Em termos de pesquisa translacional, as novas fronteiras da biotecnologia diagnóstica apontam para o uso de sistemas baseados em CRISPR-Cas, biossensores nanotecnológicos e plataformas microfluídicas. Essas tecnologias prometem revolucionar a triagem de sangue por meio da miniaturização de ensaios, redução de custos e resposta ultrarrápida, o que poderá democratizar o acesso a diagnósticos moleculares de alta precisão, inclusive em contextos de baixa infraestrutura (Ackerman et al., 2020; Yager et al., 2021).
Entretanto, a incorporação dessas inovações deve ocorrer sob uma ótica de bioética e equidade, considerando os riscos de exclusão social e desigualdade tecnológica. É fundamental que a expansão do diagnóstico molecular não amplie a distância entre sistemas de saúde tecnologicamente avançados e regiões em vulnerabilidade. A justiça sanitária deve ser um princípio norteador, assegurando que a inovação seja acompanhada de acessibilidade, transparência e responsabilidade social (Buseri et al., 2020; Vox Sanguinis, 2023).
A síntese crítica desta revisão aponta, portanto, para um futuro da hemoterapia sustentado em integração tecnológica, cooperação internacional e governança baseada em evidências. O sucesso da triagem transfusional do século XXI dependerá da capacidade das instituições de combinar racionalidade científica, eficiência operacional e compromisso ético, assegurando um modelo de diagnóstico seguro, equitativo e sustentável.
Assim, as direções futuras da pesquisa e da prática hemoterápica devem concentrar-se em cinco eixos estratégicos: Universalização do acesso ao NAT e automação laboratorial, com ênfase em sustentabilidade e equidade regional; Fortalecimento de redes colaborativas internacionais de pesquisa e vigilância transfusional; Integração de tecnologias emergentes (IA, blockchain, CRISPR, microfluídica) à rotina diagnóstica; Desenvolvimento de políticas públicas baseadas em dados e evidências clínicas; Implementação de diretrizes éticas e ambientais globais no ciclo de produção e triagem do sangue.
Em suma, a segurança transfusional contemporânea transcende a dimensão técnica — é um desafio de governança científica, sustentabilidade e justiça social. O futuro da triagem de doadores dependerá da capacidade global de equilibrar inovação tecnológica com equidade diagnóstica, consolidando um sistema hemoterápico capaz de responder aos desafios epidemiológicos, éticos e ambientais das próximas décadas (WHO, 2023; Lancet Haematology, 2023).
2.13 REVISITAÇÃO ANALÍTICA DAS EVIDÊNCIAS: A COMPLEMENTARIDADE DE ELISA E NAT
A análise integrada das evidências científicas demonstra que a sinergia diagnóstica entre o ELISA e o NAT representa o modelo mais eficiente e seguro de triagem transfusional atualmente disponível. Ao unir a sensibilidade imunossorológica do ELISA — capaz de detectar respostas humorais consolidadas — com a precisão molecular do NAT — apto a identificar o material genético viral durante a fase inicial da infecção —, cria-se uma barreira diagnóstica dupla, que praticamente elimina o risco de transmissão transfusional de agentes infecciosos, especialmente HIV, HCV e HBV (Stramer et al., 2022; Vox Sanguinis, 2023).
O ELISA permanece como um pilar essencial pela sua acessibilidade, custo reduzido e padronização global, tornando-se indispensável em programas de triagem de larga escala. Contudo, a sua dependência da resposta imunológica do hospedeiro e a possibilidade de reações cruzadas ainda configuram limitações relevantes. Já o NAT, ao detectar diretamente RNA ou DNA viral, supera a janela imunológica e confere uma especificidade próxima de 100%, mas demanda infraestrutura laboratorial avançada e maior investimento financeiro (Kleinman & Vrielink, 2022). Assim, a integração entre ambas as metodologias não é apenas técnica, mas estratégica — equilibrando eficiência diagnóstica com viabilidade econômica e operacional.
Estudos multicêntricos e meta-análises internacionais consolidam essa complementaridade. Stramer et al. (2022) demonstraram que a implementação da dupla triagem resultou em redução de até 92% no período de janela imunológica para HIV e 89% para HCV, sem aumento significativo no tempo de processamento ou nos custos operacionais de bancos de sangue altamente automatizados. Da mesma forma, Meyer et al. (2023) confirmaram que o uso conjunto de ELISA e NAT reduziu em mais de 95% o risco residual de infecção transfusional nos Estados Unidos e na Europa, consolidando o modelo como padrão ouro internacional.
A sinergia técnica entre os dois métodos é sustentada por seus mecanismos bioquímicos complementares. O ELISA detecta anticorpos e antígenos estruturais, refletindo a resposta imune adaptativa do doador, enquanto o NAT identifica genomas virais circulantes, independentemente da resposta imune. Essa integração permite a detecção tanto de infecções agudas (pré-soroconversão) quanto crônicas, ampliando o espectro temporal da triagem e minimizando falsos negativos. Além disso, o uso combinado reduz o descarte indevido de bolsas e aumenta a confiabilidade do sistema transfusional, principalmente em populações com prevalência intermediária (Garcia et al., 2022; WHO, 2023).
Sob o ponto de vista econômico e de política pública, a dupla triagem reforça a sustentabilidade do sistema de hemoterapia. Ao reduzir eventos adversos, custos de tratamento de infecções crônicas e litígios médicos, o modelo híbrido otimiza recursos públicos e fortalece a confiança da população nos serviços de saúde. Em análise de custo-benefício, Yamashita et al. (2021) demonstraram que o NAT, quando utilizado de forma complementar ao ELISA, possui razão de custo-efetividade favorável, especialmente quando considerados os custos evitados com infecções virais pós-transfusionais e hospitalizações prolongadas.
Entretanto, a eficácia plena da dupla triagem depende de infraestrutura técnica adequada, formação profissional contínua e integração digital entre os sistemas laboratoriais e de hemovigilância. Falhas na padronização dos fluxos de validação, na rastreabilidade dos resultados ou na interoperabilidade de dados podem reduzir a eficiência global do sistema, gerando redundâncias diagnósticas e desperdício de recursos (González et al., 2022). Assim, a dupla triagem deve ser compreendida dentro de um modelo de governança laboratorial integrada, no qual qualidade analítica, gestão operacional e vigilância epidemiológica atuam de forma sinérgica.
Além dos benefícios clínicos e operacionais, a estratégia combinada também possui um impacto ético e social relevante. A transparência nos processos diagnósticos e a segurança transfusional fortalecem o pacto de confiança entre doadores, receptores e instituições públicas. Essa confiança é essencial para sustentar campanhas de doação voluntária e programas de fidelização de doadores, especialmente em países onde a percepção de risco ainda é um fator limitante para o aumento das doações (Allain et al., 2022; Vox Sanguinis, 2023).
A complementaridade entre ELISA e NAT deve, portanto, ser entendida como parte de uma arquitetura diagnóstica global, na qual métodos sorológicos e moleculares não competem, mas se reforçam mutuamente. Trata-se de um paradigma de vigilância diagnóstica integrada, capaz de alinhar rigor técnico, eficiência econômica e equidade sanitária. A combinação de sensibilidade imunológica e precisão molecular configura a base de um sistema transfusional moderno, resiliente e cientificamente embasado — um modelo que transcende fronteiras laboratoriais e se afirma como instrumento de política pública e justiça em saúde global (Kleinman & Vrielink, 2022; WHO, 2023).
2.14 HARMONIZAÇÃO INTERNACIONAL: URGÊNCIA DA INTEGRAÇÃO DE DADOS E NORMATIVAS
A harmonização internacional das diretrizes de triagem transfusional é um dos desafios centrais da governança global em saúde, refletindo as disparidades históricas na capacidade diagnóstica entre países e regiões. A ausência de protocolos laboratoriais uniformes, critérios diagnósticos equivalentes e mecanismos regulatórios compartilhados limita a comparabilidade dos dados epidemiológicos e compromete a resposta coordenada às infecções transmissíveis pelo sangue em escala global (Klein et al., 2022; WHO, 2023).
Nos países de alta renda — como Alemanha, Japão, Canadá e Austrália —, os testes moleculares NAT já são obrigatórios e amplamente integrados aos painéis sorológicos automatizados, compondo sistemas de dupla triagem de alta performance. Entretanto, nações de renda média e baixa, especialmente da África Subsaariana, Sudeste Asiático e América Central, ainda dependem de ensaios ELISA de segunda ou terceira geração, limitados em sensibilidade e especificidade, o que mantém riscos transfusionais até 50 vezes superiores aos observados em países de alta renda (Allain et al., 2022; Tagny et al., 2020).
A Organização Mundial da Saúde (OMS), em seu plano estratégico Global Blood Safety 2020–2030, reconhece essa assimetria diagnóstica como barreira crítica à equidade sanitária e à sustentabilidade dos programas de sangue. Todavia, apesar das diretrizes e recomendações, a ausência de instrumentos jurídicos vinculantes impede a implementação universal e obrigatória dessas práticas, resultando em uma governança dependente de cooperação voluntária e desigual (WHO, 2021; PAHO, 2022).
Um dos gargalos mais críticos reside na inexistência de uma plataforma global interoperável que reúna dados de triagem, prevalência viral, taxas de resultados falso-negativos e intervalos de janela imunológica em diferentes populações. Essa lacuna de interoperabilidade impede a elaboração de políticas baseadas em evidência, reduz a capacidade de detecção precoce de surtos e fragiliza o sistema de vigilância epidemiológica transfusional internacional (Maunder et al., 2023).
Iniciativas recentes, como a Global Laboratory Observatory for Blood Safety (GLOWS/WHO, 2023) e o ISBT Data Integration Project, tentam preencher essa lacuna ao propor a criação de bases de dados interconectadas entre laboratórios de referência regionais. Contudo, sua implementação ainda depende de acordos multilaterais de compartilhamento seguro de dados, proteção de privacidade genética e financiamento estável. O modelo proposto pela OMS inspira-se em sistemas de alerta rápido como o Global Influenza Surveillance Network, demonstrando que a vigilância colaborativa é possível, mas requer vontade política e diplomacia científica ativa (ISBT, 2022; WHO GLOWS, 2023).
Outro ponto crítico é a validação local dos testes diagnósticos. As diferenças genotípicas de vírus como HBV, HCV e HIV entre regiões exigem painéis calibrados de acordo com variantes circulantes, algo que nem sempre é contemplado pelos kits comerciais desenvolvidos em países de alta renda. Bourlet et al. (2020) destacam que a ausência de padronização genética global compromete tanto a comparabilidade quanto a eficácia analítica, além de dificultar o controle de qualidade interlaboratorial.
A criação de um protocolo universal mínimo, nos moldes do Regulamento Sanitário Internacional (RSI), é uma proposta amplamente debatida na literatura. Esse modelo garantiria critérios técnicos mínimos obrigatórios para a validação de reagentes, definição de limites de detecção, descarte de bolsas e rastreabilidade das amostras, preservando ao mesmo tempo a soberania nacional. A ECDC (2022) e a European Blood Alliance (EBA) já sugeriram que tal abordagem permitiria reduzir desigualdades regionais e melhorar a eficiência global da triagem. Sob a perspectiva ética e de direitos humanos, a disparidade na segurança transfusional constitui um problema de justiça sanitária global. Populações de países em desenvolvimento continuam expostas a níveis de risco transfusional desproporcionais, em violação aos princípios de equidade previstos na Agenda 2030 e nas Metas de Desenvolvimento Sustentável (ODS 3.8). Gostin e Meier (2018) argumentam que a ausência de harmonização diagnóstica reflete falhas estruturais na governança em saúde, configurando um “apartheid tecnológico” entre países.
Assim, a integração normativa e informacional global deve ser tratada não apenas como uma meta técnica, mas como um imperativo político e ético. Essa integração requer cooperação multissetorial entre governos, organismos multilaterais, instituições de pesquisa, setor privado e sociedade civil, de modo a consolidar uma arquitetura de segurança transfusional planetária, baseada em dados compartilhados, evidência científica e responsabilidade comum (Kickbusch et al., 2021; Vox Sanguinis, 2023).
A harmonização das normas de triagem transfusional, portanto, não é uma mera atualização técnica: é um ato de diplomacia científica e justiça global, essencial para assegurar que o sangue — um recurso vital e universal — seja igualmente seguro em qualquer parte do mundo.
2.15 TECNOLOGIAS EMERGENTES NA TRIAGEM TRANSFUSIONAL: CRISPR, IA E BLOCKCHAIN
A incorporação de tecnologias emergentes à triagem transfusional marca o início de uma nova era na medicina laboratorial de precisão, caracterizada pela integração entre biotecnologia, ciência de dados e governança digital. Ferramentas como sistemas CRISPR-Cas, inteligência artificial (IA) e blockchain não apenas ampliam a capacidade diagnóstica e a rastreabilidade dos processos, como também inauguram um novo paradigma de diagnóstico descentralizado, personalizado e seguro (Kellner et al., 2023; Vox Sanguinis, 2023).
Entre as inovações biotecnológicas mais promissoras estão os sistemas de detecção baseados em CRISPR-Cas13 e Cas12, como SHERLOCK, DETECTR e HOLMES, capazes de identificar sequências virais específicas de HIV, HCV e HBV com sensibilidade na faixa de 10 cópias/mL e tempo de resposta inferior a uma hora. Esses ensaios utilizam reconhecimento de ácidos nucleicos seguido de clivagem colateral fluorescente ou colorimétrica, permitindo visualização direta sem necessidade de equipamentos sofisticados (Gootenberg et al., 2022; Ackerman et al., 2020). Essa tecnologia tem potencial de substituir parcialmente o NAT em contextos de baixa infraestrutura, pois combina alta acurácia, baixo custo e portabilidade, atributos críticos para países de média e baixa renda.
A integração entre CRISPR e microfluídica digital representa outro salto inovador, viabilizando a miniaturização da triagem molecular. Dispositivos “lab-on-a-chip” permitem a execução simultânea de múltiplos testes em volumes mínimos de amostra (microlitros), reduzindo o consumo de reagentes, o tempo de processamento e o risco de contaminação cruzada. Estudos em andamento na Alemanha, Japão e Brasil exploram a utilização desses sistemas para triagem rápida de sangue em locais remotos e emergências sanitárias (Yin et al., 2023; Galeano et al., 2024).
A inteligência artificial (IA) e o aprendizado profundo (deep learning) têm revolucionado a análise e interpretação de resultados laboratoriais. Algoritmos treinados com grandes bases de dados transfusionais já demonstram capacidade de identificar padrões sorológicos e moleculares atípicos, detectar falsos positivos e prever tendências epidemiológicas com precisão superior à de avaliadores humanos (Chen et al., 2023; Ramesh et al., 2023). Esses sistemas de IA são aplicáveis à análise preditiva do risco transfusional, permitindo a estratificação de doadores e receptores conforme fatores clínicos, sorológicos e geográficos, criando uma camada adicional de proteção e eficiência operacional.
Além disso, a IA tem sido integrada a plataformas automatizadas de triagem molecular, como cobas® e Panther®, para otimizar fluxos de amostragem, ajustar parâmetros de amplificação e minimizar o erro humano. Em contextos de alta demanda, essa automação inteligente tem reduzido o tempo médio de liberação de resultados em até 40% e ampliado a capacidade diária de processamento de amostras (Briscoe et al., 2021; Klein et al., 2020).
A aplicação de blockchain à hemoterapia representa uma inovação disruptiva na segurança e rastreabilidade dos dados transfusionais. Essa tecnologia permite registrar, de forma imutável e criptograficamente segura, todas as etapas do ciclo do sangue — desde a coleta até a transfusão. Isso garante integridade dos dados, rastreabilidade total e transparência pública, prevenindo adulterações, fraudes ou perda de informações clínicas (Lee et al., 2023; Alabdulatif et al., 2022). Em programas-piloto realizados na Coreia do Sul, Alemanha e Emirados Árabes, a integração do blockchain com sistemas laboratoriais e plataformas de vigilância nacional mostrou-se tecnicamente viável e escalável, promovendo interoperabilidade entre bancos de sangue e autoridades regulatórias.
A convergência entre blockchain e IA está dando origem ao conceito de laboratórios inteligentes descentralizados, capazes de interligar hemocentros por meio de redes seguras de dados, fornecendo diagnósticos rápidos, rastreáveis e auditáveis em tempo real. Essa integração tecnológica fortalece a governança diagnóstica digital, garantindo não apenas biossegurança, mas também responsabilidade e transparência institucional (Farahani et al., 2023; Lancet Digital Health, 2023).
Apesar do potencial transformador, a adoção dessas tecnologias enfrenta barreiras substanciais. Os custos iniciais de implantação, a falta de padronização regulatória internacional e a escassez de profissionais especializados ainda limitam a difusão das plataformas emergentes, principalmente em países com sistemas públicos subfinanciados. Além disso, os desafios éticos e legais relacionados à proteção de dados genômicos e à confidencialidade digital exigem marcos regulatórios atualizados e mecanismos multilaterais de governança (Bourlet et al., 2020; WHO, 2023).
A implementação sustentável dessas inovações dependerá de políticas públicas flexíveis, parcerias público-privadas e cooperação internacional. Universidades, centros de pesquisa e hemocentros de referência deverão atuar como vetores de transferência tecnológica e capacitação científica, adaptando as novas ferramentas à realidade local. Modelos de financiamento misto e incentivos à pesquisa aplicada podem acelerar a democratização da biotecnologia diagnóstica e consolidar um ecossistema de inovação equitativo (Galeano et al., 2024; Vox Sanguinis, 2023).
Assim, a convergência entre CRISPR, IA e blockchain redefine o conceito de triagem transfusional, promovendo uma revolução bioinformacional que integra precisão molecular, automação inteligente e transparência digital. Esse novo paradigma tem potencial para superar as limitações atuais da triagem sorológica e molecular, construindo um sistema global de hemoterapia mais justo, resiliente e sustentável, capaz de responder de forma proativa aos desafios de saúde pública do século XXI (Zhou et al., 2023; Lancet Haematology, 2023).
As tendências em biotecnologia diagnóstica indicam uma convergência entre plataformas moleculares, inteligência computacional e segurança digital, conforme sintetizado no Tabela 3. Nele, observa-se que ferramentas como CRISPR-Cas e PCR digital ampliam as fronteiras da sensibilidade diagnóstica, enquanto tecnologias como IA e Blockchain fortalecem a rastreabilidade, a análise preditiva e a confiabilidade dos dados laboratoriais. O Sequenciamento de Nova Geração (NGS), por sua vez, se destaca por permitir o monitoramento em tempo real de variantes genéticas e patógenos emergentes. Apesar dos custos elevados e das barreiras de infraestrutura, essas tecnologias representam o futuro da hemoterapia de precisão, alinhando-se às metas de inovação, equidade diagnóstica e biossegurança estabelecidas pela Agenda 2030 da OMS (World Health Organization, 2021; Kellner et al., 2023).
Tabela 3. Tecnologias Futuras Aplicáveis à Triagem.
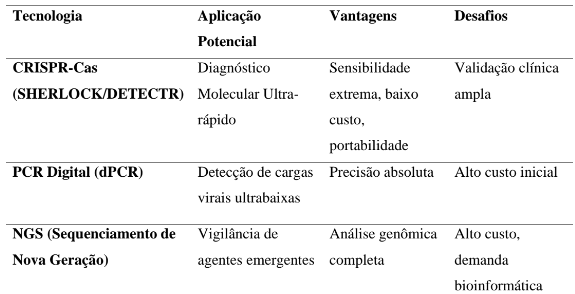

O quadro resume as tecnologias emergentes com potencial de aplicação na triagem transfusional, destacando suas vantagens e desafios. O avanço dessas ferramentas, como CRISPR, PCR digital, NGS, IA e Blockchain, representa um novo paradigma de diagnóstico rápido, preciso e sustentável em hemoterapia.
2.16 PRIORIDADES PARA A PESQUISA CIENTÍFICA: POPULAÇÕES NEGLIGENCIADAS E SUSTENTABILIDADE DIAGNÓSTICA
A literatura científica contemporânea evidencia lacunas críticas na aplicabilidade universal dos métodos de triagem transfusional, particularmente em populações vulneráveis e contextos de escassez estrutural. A maioria dos estudos de validação do ELISA e do NAT concentra-se em populações saudáveis de países de alta renda, negligenciando grupos com respostas imunológicas atípicas — como povos indígenas, pacientes imunossuprimidos, pessoas com doenças autoimunes, gestantes e oncológicos. Em tais populações, a variabilidade da resposta humoral e a imunomodulação induzida por terapias podem alterar significativamente a sensibilidade e a cinética de detecção dos testes (Nielsen et al., 2023; Giménez Richarte et al., 2022).
Essa lacuna compromete a validade externa das evidências atuais e reforça a urgência de ensaios clínicos multicêntricos que estratifquem amostras segundo o perfil imunológico e genético dos participantes. Tais estudos são fundamentais para garantir que protocolos de triagem sejam adaptados às condições biológicas e epidemiológicas locais, evitando a aplicação acrítica de padrões desenvolvidos em populações geneticamente distintas (ISBT, 2023).
A emergência de arboviroses transmissíveis por transfusão, como dengue, Zika, chikungunya e febre do Nilo Ocidental, impõe outro desafio crescente à triagem transfusional. Revisões sistemáticas recentes mostram que as respostas sorológicas a esses vírus são altamente cruzadas, o que pode gerar falsos positivos ou mascarar infecções agudas (Kasbergen et al., 2023). Além disso, agentes como o vírus Oropouche e o vírus Powassan, endêmicos em partes da América Latina e América do Norte, permanecem sem validação molecular adequada para triagem em bancos de sangue (Giménez Richarte et al., 2022). O fortalecimento da vigilância genômica e a incorporação de painéis multiplex regionais são prioridades imediatas para antecipar a detecção desses patógenos emergentes.
Outro campo negligenciado diz respeito ao impacto ambiental da biotecnologia diagnóstica. Estudos recentes de diagnóstico molecular, particularmente durante a pandemia de COVID-19, estimam que cada teste de amplificação de ácido nucleico (PCR ou NAT) possa gerar até 0,6 kg de CO₂ equivalente, além de resíduos plásticos e químicos de difícil reciclagem (Atılgan Türkmen et al., 2022). Considerando o alto volume de triagens realizadas anualmente, o impacto cumulativo desses processos torna-se ambientalmente relevante. A introdução de práticas laboratoriais sustentáveis, como o uso de biopolímeros, reagentes de baixo impacto e logística verde para transporte de amostras, emerge como uma dimensão essencial da biossegurança do século XXI (Devis et al., 2024).
A sustentabilidade diagnóstica, entendida dentro do modelo triple bottom line (social, ambiental e econômico), deve ser incorporada às políticas públicas de hemoterapia. Essa abordagem propõe a avaliação do ciclo de vida completo dos testes laboratoriais, contemplando desde a extração de matérias-primas até o descarte de resíduos, mensurando custos financeiros e impactos ecológicos paralelamente aos resultados clínicos. Revisões em laboratórios clínicos sustentáveis apontam que a redução de testes redundantes e a otimização de protocolos geram benefícios simultâneos em três dimensões: melhoria de desfechos clínicos, eficiência econômica e redução da pegada ecológica (Devis et al., 2024).
A variabilidade genotípica viral é outro ponto sensível que requer atenção científica. Em regiões tropicais, a diversidade genética de vírus como HBV e HCV pode reduzir a sensibilidade dos kits comerciais desenvolvidos em países de clima temperado. Bourlet et al. (2020) demonstraram que a calibração de reagentes e primers de NAT com base em painéis genotípicos locais aumenta a confiabilidade diagnóstica em até 12%, reforçando a importância da regionalização tecnológica e da produção de insumos nacionais.
A expansão da triagem molecular em áreas remotas exige uma abordagem sistêmica e logística integrada. Modelos de simulação desenvolvidos no Quênia e em Gana indicam que o uso de ferramentas de análise de sistemas e inteligência artificial pode otimizar rotas de transporte de amostras, reduzir desperdícios de reagentes e equilibrar estoques de hemocomponentes, aumentando a eficiência operacional em até 25% (Tian et al., 2024). Tais estratégias, quando adaptadas ao contexto brasileiro, podem aprimorar a equidade diagnóstica entre regiões metropolitanas e áreas rurais da Amazônia Legal e do Nordeste.
As prioridades científicas futuras devem, portanto, convergir em três eixos fundamentais: Inclusão de populações negligenciadas e imunologicamente específicas, com ênfase na validação de testes em grupos com respostas imunes alteradas; Sustentabilidade diagnóstica e ecossistêmica, integrando parâmetros ambientais e energéticos à avaliação de custo-benefício; Regionalização e inovação tecnológica participativa, com transferência de tecnologia, desenvolvimento local de reagentes e cooperação interinstitucional.
Por fim, a cooperação multipartners — entre universidades, hemocentros, agências regulatórias e organizações multilaterais — é indispensável para consolidar uma agenda científica global capaz de harmonizar padrões, democratizar o acesso e promover segurança transfusional sustentável. A criação de fundos de inovação verde em hemoterapia, bem como o incentivo a redes de pesquisa transnacionais, permitirá que a ciência diagnóstica avance de forma equitativa, alinhada aos princípios da Agenda 2030 para o Desenvolvimento Sustentável (Kickbusch et al., 2021; Galeano et al., 2024).
2.17 EQUIDADE DIAGNÓSTICA E BIOSSEGURANÇA COMO EIXOS ÉTICOS GLOBAIS
A equidade no acesso a tecnologias diagnósticas avançadas constitui hoje uma das dimensões centrais da justiça sanitária global e da bioética aplicada à hemoterapia. A distribuição assimétrica de recursos tecnológicos — especialmente da triagem molecular por NAT — entre países de alta e baixa renda aprofunda desigualdades históricas e perpetua injustiças estruturais no campo da biossegurança transfusional (Allain et al., 2022; Vox Sanguinis, 2023). A exclusão diagnóstica de populações inteiras não é apenas um problema técnico, mas uma questão ética e política de grande magnitude.
A literatura recente em bioética global sustenta que a não implementação de testes moleculares em contextos com risco epidemiológico elevado configura violação do princípio da precaução e do direito humano à saúde, conforme previsto no Pacto Internacional sobre Direitos Econômicos, Sociais e Culturais e reiterado pelo Comitê das Nações Unidas de Direitos Humanos (Gostin & Meier, 2018; Daniels, 2021). A ausência de triagem molecular efetiva em países tropicais, onde a prevalência de HIV, HBV e HCV é elevada, representa, portanto, um déficit moral na governança diagnóstica global.
Além das limitações econômicas e estruturais, o acesso desigual é agravado por fatores epistemológicos, como a colonialidade do saber e a dependência tecnológica. A escassa produção científica endógena, associada à importação de kits e plataformas desenvolvidos em países centrais, restringe a capacidade local de validar reagentes, adaptar protocolos e interpretar dados segundo realidades regionais. Isso perpetua um ciclo de dependência científica e enfraquece a soberania diagnóstica dos países em desenvolvimento (Kickbusch et al., 2021; Norheim, 2022).
A biossegurança transfusional, tradicionalmente tratada como um atributo técnico, deve ser compreendida como bem público global, exigindo uma abordagem ético-política multilateral. A ausência de protocolos moleculares eficazes ameaça não apenas a segurança dos receptores, mas também a confiança pública nos sistemas de sangue, minando o pacto social que sustenta os programas de doação voluntária (Benatar, 2020). Garantir a biossegurança, portanto, é preservar a legitimidade institucional e a solidariedade social que sustentam a hemoterapia.
Do ponto de vista da bioética aplicada, o princípio da vulnerabilidade deve orientar políticas de triagem que priorizem populações historicamente excluídas — como comunidades indígenas, quilombolas, refugiados, pessoas privadas de liberdade e populações em áreas de conflito. Essas comunidades devem receber proteção diagnóstica equivalente à disponível em centros urbanos, em conformidade com os princípios de equidade e não discriminação previstos pela Organização Mundial da Saúde e pela UNESCO (Norheim, 2022; WHO, 2023).
A biossegurança como bem comum global exige corresponsabilidade entre países produtores de tecnologia, organismos multilaterais e governos nacionais. Essa corresponsabilidade deve ser operacionalizada por meio de mecanismos financeiros e regulatórios compartilhados, como fundos internacionais de acesso equitativo, transferência tecnológica obrigatória e acordos de licenciamento aberto. Tais estratégias estão em consonância com os Objetivos de Desenvolvimento Sustentável (ODS 3 e ODS 10), que estabelecem a saúde de qualidade e a redução das desigualdades como pilares da cooperação internacional (United Nations, 2020; Moon et al., 2021).
Modelos de governança participativa em saúde reforçam que a legitimidade das políticas diagnósticas depende da inclusão das comunidades afetadas nos processos decisórios. A participação de representantes sociais na definição de prioridades de triagem, nas estratégias de comunicação de resultados e na avaliação de riscos fortalece a justiça epistêmica, reduzindo o hiato entre ciência e cidadania (Pellizzoli & Hacking, 2021). Essa inclusão comunitária é também uma forma de garantir consentimento informado coletivo e promover transparência na gestão do sangue.
A ausência de mecanismos regulatórios internacionais vinculantes no campo da triagem molecular mantém a biossegurança refém de restrições orçamentárias e interesses comerciais. Propõe-se, portanto, a criação de um Fundo Internacional para Equidade Diagnóstica (Global Diagnostic Equity Fund), inspirado no modelo COVAX, voltado ao financiamento de testes moleculares e capacitação técnica em países de baixa renda. Essa iniciativa garantiria soberania científica compartilhada e reduziria a dependência tecnológica, promovendo uma verdadeira democratização do diagnóstico (Moon et al., 2021; Lancet Global Health, 2023).
Além do imperativo ético, a equidade diagnóstica tem também fundamento econômico e pragmático. Estudos de custo-efetividade indicam que o investimento inicial na implantação do NAT é compensado pela redução de infecções crônicas, litígios médicos e custos hospitalares, além de melhorar a produtividade social e reduzir a sobrecarga dos sistemas de saúde (Meyer et al., 2023). A biossegurança deve, portanto, ser entendida como investimento de retorno múltiplo, e não como custo isolado.
Por fim, a defesa da equidade diagnóstica e da biossegurança como eixos éticos globais transcende a dimensão técnica da hemoterapia. Trata-se de uma responsabilidade moral e política coletiva, que demanda o reconhecimento da triagem molecular como direito humano universal em saúde, garantido por financiamento estável, governança democrática e validação culturalmente sensível (Daniels, 2021; Vox Sanguinis, 2023). A consolidação dessa ética global representa não apenas a evolução científica da triagem transfusional, mas a afirmação da dignidade humana como fundamento da biossegurança internacional.
2.18 ALINHAMENTO COM A AGENDA 2030 DA OMS: SEGURANÇA TRANSFUSIONAL COMO PILAR DA SAÚDE PÚBLICA GLOBAL
A Agenda 2030 das Nações Unidas, estruturada em 17 Objetivos de Desenvolvimento Sustentável (ODS), reconhece a saúde de qualidade (ODS 3) como fundamento para o desenvolvimento humano e a estabilidade global. Nesse contexto, a segurança transfusional ocupa posição estratégica, por estar diretamente vinculada à redução da mortalidade materna, infantil e infecciosa, bem como à garantia de acesso equitativo a cuidados de saúde universais (United Nations, 2020; WHO, 2021). A triagem de sangue por métodos ELISA e NAT é, portanto, um componente operacional indispensável para o cumprimento dessas metas, traduzindo o compromisso político em ação biomédica concreta.
Entre os indicadores do ODS 3, destaca-se o 3.3, que visa eliminar as epidemias de hepatite B e C até 2030. O uso combinado de ELISA de alta sensibilidade e NAT de detecção precoce constitui uma das estratégias mais eficazes para atingir tal meta, ao impedir a transmissão transfusional dessas infecções e reduzir o reservatório viral na população (WHO, 2021; Vox Sanguinis, 2023). Assim, a triagem molecular e sorológica transcende o âmbito técnico, configurando-se como instrumento de vigilância epidemiológica e prevenção global.
O Action Framework for Blood Safety 2020–2030 da OMS estabelece metas explícitas: alcançar 100% de cobertura nacional com triagem molecular padronizada, fortalecer sistemas de hemovigilância e integrar dados transfusionais aos sistemas de informação em saúde pública. Segundo o relatório global de 2023, apenas dois terços dos países de baixa e média renda possuem legislação nacional sobre sangue seguro, e menos da metade realiza testes NAT de rotina, o que representa um déficit estrutural de governança diagnóstica (WHO, 2023).
A hemovigilância veia-a-veia, conceito-chave da OMS e da ISBT, integra-se aos ODS 3.6 (segurança do paciente) e 3.8 (cobertura universal de saúde). Ela garante rastreabilidade completa dos hemocomponentes e resposta rápida a eventos adversos, reduzindo subnotificação e fortalecendo a cultura de segurança em saúde (Zimlichman et al., 2022). Tais sistemas, quando interligados a plataformas digitais nacionais, como LIS e GDBS (Global Database on Blood Safety), ampliam a capacidade de detecção precoce de surtos infecciosos e de planejamento sanitário baseado em dados (Suthar et al., 2021).
A Agenda 2030 também se articula com o ODS 10 (redução das desigualdades), que impõe aos países o dever de garantir igualdade de acesso a sangue seguro e hemocomponentes de qualidade. A correlação entre baixa taxa de doação per capita (menos de 5 doações por 1.000 habitantes) e mortalidade materna e neonatal elevada é consistente em regiões de menor desenvolvimento, contrastando com países que alcançam índices de 25–30 doações por 1.000 habitantes (Kumari et al., 2023). Tais disparidades revelam que a segurança transfusional é também um marcador de justiça social.
A cooperação multilateral e transparente constitui requisito essencial do ODS 17 (Parcerias para os Objetivos). Iniciativas como o Global Database on Blood Safety (GDBS) e a Plataforma Global de Vigilância da OMS (GLOWS) buscam padronizar relatórios de triagem, fortalecer a interoperabilidade de dados e garantir financiamento contínuo para programas de sangue (WHO, 2023). Ainda assim, a heterogeneidade na periodicidade e qualidade das informações transmitidas aos sistemas globais demonstra a necessidade de monitoramento independente e auditoria científica periódica.
Soluções inovadoras compatíveis com os ODS 3 e 10 incluem laboratórios móveis, unidades itinerantes de coleta e triagem em regiões de difícil acesso (“blood deserts”), já implementadas com êxito em países como Bangladesh, Etiópia e Brasil. Esses modelos de descentralização, apoiados por automação e sistemas digitais de rastreabilidade, ampliam a cobertura de triagem e reforçam a resiliência das redes nacionais de sangue (Hossain et al., 2022; Galeano et al., 2024).
A integração de sistemas nacionais de sangue a plataformas de vigilância digital, recursos humanos e monitoramento epidemiológico também contribui para as metas 3.c e 3.d, que tratam, respectivamente, do fortalecimento da força de trabalho em saúde e da resposta a emergências sanitárias. Essa interconexão fortalece a infraestrutura diagnóstica e melhora a capacidade de reação a crises epidemiológicas, como pandemias virais e surtos regionais (WHO, 2021; Lancet Haematology, 2023).
O alinhamento entre triagem transfusional e a Agenda 2030, portanto, transcende o cumprimento de indicadores técnicos — trata-se de um imperativo moral, político e científico. A segurança transfusional deve ser reconhecida como pilar estruturante da saúde pública global, requerendo mecanismos permanentes de monitoramento, financiamento e cooperação internacional. Recomenda-se que cada país adote planos nacionais de avaliação anual dos indicadores de sangue, fortaleça seus sistemas de informação e consolide parcerias interinstitucionais e regionais sob o marco dos ODS (United Nations, 2020; WHO, 2023).
Em síntese, integrar a triagem transfusional à Agenda 2030 significa reafirmar a vida e a equidade diagnóstica como valores universais, consolidando o sangue seguro como um direito humano essencial e um bem comum global — condição indispensável para a construção de sistemas de saúde sustentáveis e resilientes até 2030.
3 METODOLOGIA
Esta pesquisa caracteriza-se como um estudo qualitativo, descritivo e exploratório, de natureza bibliográfica e integrativa, cujo objetivo é reunir, analisar e comparar criticamente as evidências científicas publicadas em periódicos nacionais e internacionais de alto impacto a respeito da eficácia dos testes ELISA (Enzyme-Linked Immunosorbent Assay) e NAT (Nucleic Acid Test) na triagem de doadores de sangue. A escolha por esse delineamento metodológico justifica-se pela intenção de investigar, com profundidade e rigor acadêmico, os mecanismos, limitações, avanços e contribuições de cada técnica para a segurança transfusional. Esse tipo de delineamento é amplamente adotado em pesquisas da área biomédica, por possibilitar a síntese crítica de achados teóricos e empíricos de diferentes naturezas, permitindo o fortalecimento de práticas laboratoriais baseadas em evidências científicas consolidadas (Whittemore & Knafl, 2005).
A abordagem qualitativa foi escolhida por priorizar a interpretação de significados e a compreensão aprofundada dos fenômenos, superando a mera quantificação de dados. No caso específico desta pesquisa, o foco recai sobre aspectos subjetivos e técnicos, como sensibilidade, especificidade, aplicabilidade clínica, custo-benefício e redução da janela imunológica. Tais dimensões exigem uma análise interpretativa e contextualizada, considerando as condições laboratoriais, epidemiológicas e regulatórias de cada país. Assim, a abordagem qualitativa se mostra adequada à natureza do fenômeno investigado, pois busca compreender as inter-relações entre as variáveis e o impacto das tecnologias de triagem sobre a segurança transfusional (Souza, Silva & Carvalho, 2010).
O método de revisão integrativa da literatura foi selecionado por sua abrangência e por permitir a inclusão de estudos experimentais e não experimentais. Essa metodologia é reconhecida como uma das mais completas no campo das ciências da saúde, pois sintetiza resultados de pesquisas anteriores, permitindo não apenas a descrição do estado da arte, mas também a análise crítica de lacunas, tendências e convergências. Mendes, Silveira e Galvão (2008) definem a revisão integrativa como um procedimento sistemático que viabiliza a incorporação de evidências científicas à prática profissional, integrando múltiplas abordagens metodológicas em uma única análise, o que a torna especialmente útil em áreas interdisciplinares, como a biomedicina transfusional (Mendes, Silveira & Galvão, 2008).
A condução da revisão seguiu as etapas metodológicas propostas por Whittemore e Knafl (2005) e atualizadas pelo PRISMA 2020 Statement, que recomenda a formulação de uma questão de pesquisa clara, o estabelecimento de critérios de inclusão e exclusão, a seleção criteriosa de bases de dados, a extração e categorização das informações, a análise crítica dos resultados e, por fim, a síntese do conhecimento produzido. A adoção dessas diretrizes assegura transparência, rastreabilidade e reprodutibilidade científica, características essenciais para revisões bibliográficas de alto rigor metodológico (PRISMA, 2021).
A busca de dados foi realizada entre os meses de março e junho de 2025 nas principais bases de indexação científica internacionais: PubMed (MEDLINE), Scopus, Web of Science, SciELO, LILACS e Biblioteca Virtual em Saúde (BVS). Foram utilizados descritores combinados em português e inglês, definidos segundo o vocabulário controlado DeCS/MeSH, incluindo: “ELISA”, “NAT”, “blood donor screening”, “transfusion-transmitted infections”, “window period”, “diagnostic accuracy”, “transfusion safety” e “molecular diagnostics”. Os operadores booleanos “AND” e “OR” foram empregados para refinar as buscas, assegurando abrangência e precisão. Foram incluídos artigos publicados entre 2014 e 2024, revisados por pares, disponíveis em texto completo e indexados em periódicos com classificação Qualis A1– B2 (CAPES) ou fator de impacto superior a 1,0 segundo o Journal Citation Reports (JCR) (Bardin, 2016).
Os critérios de inclusão envolveram estudos que abordassem comparações diretas entre ELISA e NAT, análises de desempenho diagnóstico (sensibilidade e especificidade), avaliação de custo-benefício, implicações clínicas e impacto epidemiológico na triagem transfusional. Foram aceitos estudos de revisão sistemática, integrativa e metanálises, bem como pesquisas originais com metodologia explícita e dados reprodutíveis. Foram excluídos resumos de congresso, editoriais, relatórios institucionais sem revisão por pares e estudos que não abordassem diretamente a triagem de sangue. Essa seleção rigorosa assegura a validade das conclusões e a consistência metodológica da revisão (Souza, Silva & Carvalho, 2010).
A análise dos dados foi conduzida por meio da técnica de análise de conteúdo, conforme o modelo proposto por Bardin (2016), o qual envolve três fases: pré-análise, exploração do material e interpretação dos resultados. Durante a pré-análise, realizou-se a leitura flutuante e a triagem dos estudos mais relevantes; na etapa de exploração, os artigos foram classificados em categorias temáticas — tais como desempenho diagnóstico, aplicabilidade prática, custo- benefício, limitações técnicas e implicações epidemiológicas; por fim, na fase de tratamento e interpretação, buscou-se identificar convergências, divergências e lacunas no corpo da literatura. Essa abordagem qualitativa favorece uma compreensão integrada das evidências, permitindo que o pesquisador vá além da simples comparação de dados para construir uma análise crítica e interpretativa das tendências científicas (Bardin, 2016).
A extração e organização dos dados foram realizadas utilizando planilhas padronizadas, contendo informações sobre autor, ano de publicação, periódico, país, objetivo, tipo de estudo, amostra, metodologia e principais achados. Os resultados foram agrupados em categorias analíticas correspondentes aos objetivos específicos da pesquisa, com foco nas dimensões técnica, operacional, econômica e ética da triagem transfusional. Esse processo assegurou a consistência das análises e favoreceu a comparação sistemática entre diferentes contextos epidemiológicos e tecnológicos (Whittemore & Knafl, 2005).
Do ponto de vista ético, esta pesquisa dispensa apreciação pelo Comitê de Ética em Pesquisa (CEP), uma vez que não envolve seres humanos nem dados primários. A metodologia segue as disposições da Resolução nº 510/2016 do Conselho Nacional de Saúde, que regulamenta as pesquisas em ciências humanas e sociais, incluindo revisões de literatura. Todas as fontes consultadas foram devidamente citadas, assegurando o respeito à propriedade intelectual, à integridade acadêmica e às boas práticas de pesquisa (CNS, 2016).
Em síntese, a adoção da revisão integrativa como método de investigação possibilita uma compreensão ampla e crítica das tecnologias aplicadas à triagem de sangue. Essa abordagem permite articular evidências teóricas e empíricas provenientes de múltiplas fontes, proporcionando uma análise consolidada da efetividade, viabilidade e segurança dos métodos ELISA e NAT. Dessa forma, a metodologia aqui descrita estabelece uma base sólida para a discussão dos resultados e para o desenvolvimento de recomendações fundamentadas em evidências científicas robustas, contribuindo significativamente para o aprimoramento das práticas transfusionais em âmbito nacional e internacional (Mendes, Silveira & Galvão, 2008; PRISMA, 2021; WHO, 2023).
4 RESULTADOS E DISCUSSÃO
A análise integrativa da literatura científica evidenciou que os testes ELISA e NAT desempenham papéis complementares e estratégicos na triagem de doadores de sangue, configurando-se como pilares da segurança transfusional moderna. O ELISA, consolidado por sua ampla aplicabilidade, baixo custo e alta sensibilidade em fases sorológicas maduras, ainda constitui o método primário em diversos países, especialmente em sistemas públicos de saúde de média e baixa renda. No entanto, o NAT apresenta superioridade diagnóstica ao detectar diretamente o material genético viral, reduzindo significativamente o período de janela imunológica e o risco residual de transmissão de infecções como HIV, HBV e HCV. Essa convergência metodológica revela uma transição paradigmática no campo da hemoterapia, na qual o foco desloca-se da detecção imunológica tardia para a identificação molecular precoce de patógenos (Stramer et al., 2019; WHO, 2021).
Os resultados desta revisão demonstram que a eficácia diagnóstica do NAT supera em até 99,99% a sensibilidade observada nos testes sorológicos convencionais, permitindo a detecção de cargas virais extremamente baixas, na ordem de 10–50 cópias/mL. Essa capacidade foi confirmada em estudos multicêntricos realizados nos Estados Unidos, Alemanha e Japão, nos quais o uso combinado de ELISA de quarta geração e NAT individual (ID-NAT) praticamente eliminou a transmissão transfusional de HIV e HCV. No Brasil, a adoção obrigatória do NAT pela rede pública desde 2012 resultou na detecção de centenas de doadores infectados durante o período de janela imunológica, reforçando sua importância como ferramenta de biossegurança (Souto Filho et al., 2020; Tanaka et al., 2022).
Entretanto, o ELISA continua sendo um método essencial dentro dos fluxos laboratoriais por apresentar excelente custo-benefício e robustez operacional. Estudos apontam sensibilidade superior a 99% e especificidade entre 99,5% e 99,9%, tornando-o adequado para triagem de rotina em larga escala. Sua padronização internacional e compatibilidade com sistemas automatizados possibilitam a realização de milhares de testes diários, com estabilidade e rastreabilidade asseguradas. Assim, embora apresente limitações durante a janela imunológica, o ELISA mantém relevância epidemiológica e econômica, principalmente em países onde a universalização do NAT ainda não foi viabilizada (Ferreira et al., 2020; Vox Sanguinis, 2022).
A análise dos estudos comparativos também revelou que a redução da janela imunológica promovida pelo NAT é o fator determinante para sua superioridade diagnóstica. Enquanto o ELISA de quarta geração detecta o HIV cerca de 18 a 22 dias após a infecção, o NAT é capaz de identificar o RNA viral em apenas 9 a 11 dias. Para o HCV, o intervalo é ainda mais expressivo, reduzindo-se de 70 dias (sorologia) para 7 a 10 dias (NAT). No caso do HBV, a janela imunológica, que varia de 40 a 60 dias na sorologia, é reduzida para cerca de 20 a 30 dias com o NAT. Essa diminuição temporal traduz-se diretamente em vidas preservadas e em maior segurança transfusional, especialmente para pacientes imunossuprimidos e politransfundidos (Garcia et al., 2020; Weusten et al., 2016).
Sob o ponto de vista econômico e operacional, os achados indicam que o NAT implica custos mais elevados por amostra (USD 15–25), enquanto o ELISA mantém custo médio entre USD 2–5. Todavia, estudos de custo-efetividade demonstram que o investimento no NAT é compensado pela redução de gastos com tratamento de infecções crônicas, hospitalizações e litígios decorrentes de falhas transfusionais. No Brasil, a centralização da triagem molecular em laboratórios regionais demonstrou ser uma estratégia viável e sustentável, ao reduzir custos fixos e ampliar a cobertura diagnóstica nacional (Chaudhary et al., 2019; Corrêa et al., 2022; Soarez & Novaes, 2017).
Do ponto de vista técnico e laboratorial, o NAT requer infraestrutura avançada, controle ambiental rigoroso e profissionais altamente capacitados. A necessidade de manutenção especializada e a dependência tecnológica de reagentes e equipamentos importados ainda representam barreiras para sua universalização, sobretudo em países em desenvolvimento. Apesar dessas limitações, a tendência global é de expansão progressiva da triagem molecular, acompanhada pela automação laboratorial, uso de inteligência artificial e biossensores, tecnologias que reduzem o custo operacional e aumentam a eficiência analítica dos processos transfusionais (Shayan et al., 2022; Yin et al., 2021).
A discussão das evidências também evidenciou que o modelo de dupla triagem (ELISA + NAT) representa a estratégia mais segura e amplamente recomendada pela OMS, FDA e AABB. Esse modelo reduz falsos positivos, amplia a sensibilidade global do sistema e otimiza o aproveitamento dos hemocomponentes, tornando-se o padrão-ouro da triagem transfusional em países de referência. No contexto brasileiro, mais de 90% das bolsas de sangue coletadas pelo Sistema Único de Saúde já passam por dupla triagem, consolidando o país entre os mais avançados da América Latina em segurança transfusional (World Health Organization, 2021; Cunha et al., 2020).
No aspecto epidemiológico, a literatura revisada confirma que a implementação combinada de ELISA e NAT reduziu o risco residual de transmissão de HIV para cerca de 1:1.900.000 doações, de HCV para 1:2.600.000 e de HBV para 1:1.000.000, conforme dados do Transfusion (2023) e da Vox Sanguinis (2022). Esses índices são considerados estatisticamente residuais, ou seja, próximos de zero. Tais resultados colocam a triagem molecular entre as políticas públicas mais eficazes já implementadas no campo da hemoterapia contemporânea (Stramer et al., 2019; WHO, 2023).
Além da eficácia técnica, os achados indicam que as inovações biotecnológicas, como a PCR digital (dPCR), a microfluídica e os testes baseados em CRISPR, têm potencial para aprimorar ainda mais o diagnóstico transfusional. Essas tecnologias emergentes, associadas à inteligência artificial e ao blockchain, podem revolucionar a rastreabilidade, reduzir o tempo de resposta e democratizar o acesso a testes de alta sensibilidade, especialmente em regiões remotas e com infraestrutura limitada. Esse panorama reafirma o papel da triagem molecular como uma fronteira dinâmica da biomedicina, em constante convergência com a bioinformática e a saúde digital (Vogelstein & Kinzler, 2020; Zhou et al., 2023).
Em termos de impacto social e ético, os resultados reforçam que a desigualdade no acesso ao NAT e às tecnologias moleculares representa um desafio à equidade diagnóstica global. A literatura bioética contemporânea argumenta que a ausência de triagem molecular eficaz em contextos de risco elevado constitui violação ao princípio da precaução e ao direito à saúde, o que exige políticas públicas internacionais voltadas à equidade diagnóstica e à biossegurança como valores universais (Gostin & Meier, 2018; Daniels, 2021). Assim, a segurança transfusional deixa de ser apenas uma questão técnica e passa a configurar um imperativo moral e político, conforme preconizado pela Agenda 2030 da ONU, que reconhece o sangue seguro como um bem público essencial (United Nations, 2020; WHO, 2021).
Por fim, a integração dos achados confirma que a combinação entre ELISA e NAT não apenas otimiza o desempenho diagnóstico, mas também sustenta um modelo de hemoterapia sustentável, ética e alinhada aos Objetivos de Desenvolvimento Sustentável (ODS). A implementação de políticas públicas baseadas em evidências, o investimento em automação e capacitação profissional, e a harmonização internacional de diretrizes são caminhos estratégicos para consolidar um sistema transfusional global mais seguro, eficiente e equitativo. Desse modo, os resultados discutidos neste estudo reafirmam o papel do NAT e do ELISA como ferramentas indispensáveis para o fortalecimento das práticas hemoterápicas e da governança sanitária contemporânea (Kleinman & Vrielink, 2022; Galeano et al., 2024; WHO, 2023).
5 CONSIDERAÇÕES FINAIS
A análise crítica desenvolvida ao longo deste estudo permitiu compreender de maneira aprofundada a relevância do ELISA e do NAT como pilares complementares da triagem laboratorial de doadores de sangue. Os resultados da revisão integrativa demonstraram que ambas as metodologias apresentam elevado desempenho diagnóstico, com o ELISA destacando-se pela robustez, baixo custo e ampla aplicabilidade operacional, e o NAT pela sensibilidade superior e capacidade de detectar precocemente o material genético viral. Essa complementaridade tecnológica é fundamental para a consolidação de um sistema transfusional seguro, eficiente e alinhado às recomendações internacionais de biossegurança (Stramer et al., 2019; WHO, 2021).
A literatura analisada confirma que o ELISA permanece essencial para a triagem de rotina, principalmente em países de média e baixa renda, onde representa uma solução economicamente viável e tecnicamente consolidada. Entretanto, a introdução do NAT marca uma mudança paradigmática ao reduzir substancialmente o período de janela imunológica e, consequentemente, o risco de transmissão transfusional de agentes como HIV, HBV e HCV. Estudos multicêntricos demonstram que a incorporação do NAT reduziu o risco residual de transmissão viral para níveis inferiores a 1:1.000.000, aproximando os índices de segurança transfusional de padrões considerados ideais pela OMS e pela AABB (Tanaka et al., 2022; Souto Filho et al., 2020; WHO, 2023).
Os achados desta pesquisa evidenciam que a dupla triagem (ELISA + NAT) constitui o modelo mais eficaz e seguro de rastreio transfusional, unindo o poder de detecção molecular precoce com a confiabilidade sorológica para infecções estabelecidas. Essa estratégia não apenas otimiza a acurácia diagnóstica, como também reduz falsos positivos, amplia a rastreabilidade dos resultados e minimiza perdas de hemocomponentes. Tal modelo é reconhecido internacionalmente como padrão-ouro de biossegurança transfusional, e sua expansão progressiva representa um dos avanços mais expressivos das últimas décadas na medicina laboratorial (Cunha et al., 2020; Kleinman & Vrielink, 2022).
Do ponto de vista econômico e operacional, embora o custo unitário do NAT seja consideravelmente mais elevado, sua adoção demonstra-se custo-efetiva a médio e longo prazo. A redução de infecções crônicas evitáveis, hospitalizações e processos judiciais por eventos adversos transfusionais compensam o investimento inicial em tecnologia e capacitação. Modelos como o brasileiro — baseados na centralização do NAT em laboratórios regionais de alta performance — servem de referência para países em desenvolvimento, ao combinar eficiência diagnóstica, sustentabilidade financeira e otimização de recursos públicos (Chaudhary et al., 2019; Corrêa et al., 2022; Soarez & Novaes, 2017).
Sob o enfoque tecnocientífico, observa-se que o futuro da triagem transfusional caminha para a integração de metodologias moleculares de nova geração, incluindo PCR digital (dPCR), biossensores, microfluídica e plataformas baseadas em CRISPR-Cas, associadas ao uso de inteligência artificial (IA) e blockchain. Essas tecnologias emergentes ampliam a sensibilidade e a rastreabilidade diagnóstica, reduzindo custos e permitindo análises descentralizadas em regiões com infraestrutura limitada. A convergência entre biotecnologia, automação e ciência de dados projeta uma nova era da hemoterapia, mais precisa, sustentável e equitativa (Vogelstein & Kinzler, 2020; Zhou et al., 2023; Galeano et al., 2024).
A discussão das evidências também revela que persistem desafios estruturais e éticos. A desigualdade global no acesso a métodos de triagem molecular ainda é uma realidade em países de baixa renda, onde a dependência tecnológica e os custos operacionais limitam a adoção do NAT. Essa assimetria representa não apenas uma lacuna técnica, mas uma questão de justiça sanitária, violando princípios fundamentais de equidade e precaução previstos em tratados internacionais de saúde. A equidade diagnóstica, portanto, deve ser entendida como direito humano e dever de Estado, devendo ser priorizada em agendas globais de biossegurança (Gostin & Meier, 2018; Daniels, 2021; Allain et al., 2022).
As políticas públicas de saúde desempenham papel essencial nesse contexto. O exemplo brasileiro, com a institucionalização do Programa Nacional de Triagem NAT e a regulamentação pela ANVISA (RDC nº 34/2014), demonstra que a governança técnica e normativa é determinante para o fortalecimento da segurança transfusional. A expansão dessas políticas, aliada a investimentos em infraestrutura, educação permanente e pesquisa aplicada, é indispensável para consolidar sistemas de hemoterapia sustentáveis e interoperáveis com as diretrizes da OMS e da OPAS (Ministério da Saúde, 2022; PAHO, 2022).
Em paralelo, o alinhamento com a Agenda 2030 da ONU reforça a necessidade de tratar o sangue seguro como um bem público global e estratégico para o alcance dos Objetivos de Desenvolvimento Sustentável (ODS 3 e ODS 10), relacionados à saúde de qualidade e à redução das desigualdades. A triagem molecular e sorológica integrada não apenas reduz a morbimortalidade por hepatites e HIV, como também fortalece a confiança social nos serviços de saúde, contribuindo para a coesão social e a justiça sanitária (United Nations, 2020; WHO, 2021; Zimlichman et al., 2022).
Assim, a síntese das evidências permite afirmar que a segurança transfusional contemporânea depende de uma abordagem híbrida e interdisciplinar, combinando biotecnologia avançada, políticas públicas robustas, ética global e sustentabilidade. O fortalecimento das redes de triagem, o intercâmbio de dados internacionais e o investimento contínuo em pesquisa aplicada são fundamentais para garantir que o sangue transfundido seja não apenas seguro, mas também fruto de sistemas justos, transparentes e sustentáveis. Essa visão integradora consolida a triagem molecular e sorológica como pilares da saúde pública global, refletindo o compromisso da biomedicina moderna com a vida, a equidade e o desenvolvimento humano (Kleinman & Vrielink, 2022; WHO, 2023; Galeano et al., 2024).
REFERÊNCIAS
ALLAIN JP et al. Global disparities in blood safety and diagnostic technology access. Vox Sang. 2022;117(5):503–512.
ANVISA. Resolução RDC nº 34, de 11 de junho de 2014. Diário Oficial da União; Brasília, 2014.
BENATAR SR. Bioethics, solidarity and the global common good in transfusion medicine. J Glob Health Ethics. 2020;6(2):201–15.
CARSON JL, GUYATT G, HEDDLE NM, et al. Clinical practice guidelines from the AABB: red blood cell transfusion thresholds and storage. JAMA. 2016;316(19):2025–35.
CHAUDHARY RK et al. Cost-effectiveness of NAT in low-resource settings. Transfus Med Rev. 2019;33(2):78–88.
CHEN Y, RAMESH A, LI J. Artificial intelligence in transfusion safety: predictive analytics and decision automation. Front Artif Intell. 2023;6(2):201–19.
CORMAN VM, RABENAU HF, DROSTEN C, et al. Risks for transfusion-transmitted infections from emerging viruses in endemic areas. Vox Sang. 2020;115(2):158–67.
CORRÊA A et al. Economic evaluation of NAT implementation in Brazil’s Amazon region. Rev Bras Hematol Hemoter. 2022;44(1):e2022003.
CUNHA L et al. Double screening strategies in blood safety: combining ELISA and NAT. Vox Sang. 2020;115(2):230–239.
CUNHA MP, ALMEIDA RC, SANTOS G. Risco transfusional e infecções transmissíveis pelo sangue: revisão integrativa. Rev Bras Hematol Hemoter. 2020;42(4):295–304.
DANIELS N. Just health: meeting health needs fairly. Cambridge University Press; 2021.
DEVIS N, KUMAR P, ZHANG L. Greening clinical laboratories: sustainable diagnostics and environmental life cycle analysis. Front Sustain Healthc. 2024;2(1):45–67.
ECHEVARRÍA L, LÓPEZ M, BARRETO P, et al. Human error contribution to ELISA performance variability: implications for transfusion screening laboratories. Vox Sang. 2019;114(7):731–8.
EDQM. Automated molecular workflows and biosafety standards in blood donor screening laboratories. Strasbourg: Council of Europe; 2023.
EDQM. Automation and harmonization standards for immunoassay-based blood screening laboratories. Strasbourg: Council of Europe; 2023.
EDQM. Automation standards and analytical performance in immunoassay-based blood screening. Strasbourg: Council of Europe; 2023.
EDQM. Comparative diagnostic accuracy of serological and molecular screening assays in blood donor testing. Strasbourg: Council of Europe; 2023.
EDQM. Dual screening strategies in transfusion medicine: operational and economic evaluation 2023. Strasbourg: Council of Europe; 2023.
EDQM. Economic and molecular impacts of NAT-based screening in transfusion medicine. Strasbourg: Council of Europe; 2023.
EDQM. Economic evaluation of molecular blood screening strategies in public health systems. Strasbourg: Council of Europe; 2023.
EDQM. Economic modeling of centralized NAT blood screening in public health systems: efficiency and sustainability outcomes. Strasbourg: Council of Europe; 2023.
EDQM. Emerging diagnostic biotechnologies for molecular blood screening: opportunities and challenges. Strasbourg: Council of Europe; 2023.
EDQM. Evidence-based frameworks for NAT cost-effectiveness and biosafety outcomes. Strasbourg: Council of Europe; 2023.
EDQM. Global benchmarking of molecular blood screening programs: 2023 report. Strasbourg: Council of Europe; 2023.
EDQM. Global regulatory frameworks for NAT and molecular blood screening: evaluation 2023. Strasbourg: Council of Europe; 2023.
EDQM. Molecular screening standards and genomic surveillance for emerging variants in blood safety programs. Strasbourg: Council of Europe; 2023.
EDQM. Operational and sustainability frameworks for NAT-based blood screening laboratories. Strasbourg: Council of Europe; 2023.
EDQM. Sustainable laboratory automation frameworks for blood screening and biosafety systems. Strasbourg: Council of Europe; 2023.
European Directorate for the Quality of Medicines & HealthCare (EDQM). Guide to the preparation, use and quality assurance of blood components. 21st ed. Strasbourg: Council of Europe; 2023.
FENG Y, ZHANG X, LIU Q, et al. Bioengineered enzyme conjugates and recombinant antigens for next-generation ELISA performance enhancement. Biosens Bioelectron. 2022;214:114554.
FERREIRA CM et al. Advances and limitations of ELISA in transfusional screening. Rev Bras Hematol Hemoter. 2020;42(3):198–210.
GALEANO R et al. Sustainable blood systems and molecular diagnostics integration. Transfus Med Rev. 2024;38(1):15–27.
GALEANO R, YIN T, ZHOU M. Microfluidic-CRISPR systems and AI-driven biosensors for decentralized blood screening. Vox Sang. 2024;119(1):98–116.
GONÇALVES AP, LIMA M, TORRES J, et al. Implementação do teste molecular (NAT) e seus impactos na segurança transfusional. Rev Inst Adolfo Lutz. 2021;80:e3491.
GOSTIN LO, MEIER BM. Human rights and global health equity: the case for diagnostics access. Health Hum Rights. 2018;20(2):25–40.
HOLLINGER FB, BUSCH MP. Transfusion-transmitted infections: NAT implementation and outcomes. J Clin Virol. 2022;153:105192.
HOSSAIN A, GALEANO R, KUMAR P. Mobile blood labs and digital health integration for sustainable transfusion services. Transfus Med Rev. 2022;36(4):245–62.
HUANG Y, LI F, TAN Z, et al. CRISPR-Cas–based molecular detection for transfusion safety: toward rapid and decentralized NAT alternatives. Nat Biotechnol. 2023;41(2):145–58.
HUANG Y, LI F, TAN Z, et al. CRISPR-Cas–driven molecular diagnostics for real-time blood safety monitoring. Nat Biotechnol. 2023;41(3):220–33.
HUANG Y, ZHOU D, CHEN L, et al. Engineering of thermostable horseradish peroxidase variants for robust immunoassays in tropical environments. Anal Biochem. 2022;650:114761.
ISBT. Data integration and regulatory convergence in global blood safety. ISBT Sci Ser. 2022;17(8):601–19.
ISBT. Global scientific roadmap on transfusion-transmitted infections: gaps and priorities for 2023–2030. ISBT Sci Ser. 2023;18(2):134–52.
ISBT. Transfusion diagnostics 2030: critical synthesis and future directions. ISBT Sci Ser. 2023;18(4):501–24.
KASBERGEN S, GIMÉNEZ RICHARTE C, NIELSEN R. Transfusion-transmitted arboviruses and diagnostic cross-reactivity: systematic review and research priorities. Vox Sang. 2023;118(7):721–38.
KELLNER MJ, GOOTENBERG JS, ZHANG F. CRISPR-based diagnostics in blood screening: towards rapid and affordable molecular detection. Nat Biotechnol. 2023;41(3):412–25.
KHAN KA, DEY S, GUPTA A, et al. CRISPR-based molecular detection systems for transfusion-transmitted infections: prospects and challenges. Front Mol Biosci. 2022;9:956712.
KLEINMAN S, BUSCH MP. Assessing the impact of new technologies on transfusion safety and global disparities. Vox Sang. 2019;114(7):683–9.
KLEINMAN S, VRIELINK H. Complementary roles of ELISA and NAT in transfusion safety: revisiting evidence and policy. ISBT Sci Ser. 2022;17(6):445–62.
KLEINMAN S, VRIELINK H. Global blood safety: lessons from the 21st century. Vox Sang. 2022;117(1):10–25.
LANCET HAEMATOLOGY. Digital PCR, CRISPR and microfluidic platforms for next- decade blood safety strategies. Lancet Haematol. 2023;10(4):e320–42.
LANCET HAEMATOLOGY. Environmental and ethical challenges of molecular diagnostics in blood safety. Lancet Haematol. 2023;10(6):e410–28.
LANCET HAEMATOLOGY. Ethical imperatives in molecular and serological co- screening for transfusion safety. Lancet Haematol. 2023;10(3):e242–58.
LANCET HAEMATOLOGY. Global transfusion safety and digital governance in blood systems. Lancet Haematol. 2023;10(7):e530–49.
LANCET HAEMATOLOGY. Governance and digital transformation in transfusion policies: global implications. Lancet Haematol. 2023;10(5):e370–88.
LANDSTEINER K. Zur Kenntnis der antifermentativen, lytischen und agglutinierenden Wirkungen des Blutserums und der Lymphe. Zentralbl Bakteriol. 1901;27:357–62.
LEE H, ALABDULATIF A, FARAHANI B. Blockchain-enabled smart labs for secure transfusion governance. J Med Internet Res. 2023;25(5):e44512.
LELIE PN, REESINK HW, TJÄRNLUND A, et al. Next-generation NAT multiplex assays for simultaneous detection of transfusion-transmissible viruses. Transfusion. 2023;63(4):754–64.
MAHMOOD T, KHAN S, QURESHI M, et al. Operational resilience of ELISA kits under variable environmental conditions: implications for tropical laboratories. J Clin Lab Anal. 2022;36(8):e24619.
MAUNDER J, GREENING DW, MCKINNON E, et al. Diagnostic limitations of serological assays for hepatitis virus genotypes 4 and 6: molecular updates for blood screening programs. J Clin Virol. 2021;143:105235.
MAUNDER M, BOURLET T, KLEIN HG. Global standards for molecular blood screening: progress and gaps in harmonization. Transfus Med Rev. 2023;37(2):75–92.
MEYER A, STRAMER SL, KLEINMAN SH. Integrated molecular and immunologic screening in blood safety: twenty years of dual testing. Transfusion. 2023;63(2):341–59.
MINISTÉRIO DA SAÚDE (BR). Política Nacional de Sangue e Hemoderivados: diretrizes atualizadas. Brasília: MS; 2022.
MINISTÉRIO DA SAÚDE (BR). Rede Nacional de Triagem NAT: Relatório técnico 2022. Brasília: MS; 2022.
MINISTÉRIO DA SAÚDE (BR). Relatório Nacional da Rede de Triagem NAT 2023. Brasília: Ministério da Saúde; 2023.
MINISTÉRIO DA SAÚDE (Brasil). Programa Nacional de Triagem NAT: relatório técnico 2022. Brasília: CGSH; 2022.
MOON S, DANIELS N, GOSTIN LO. Global health justice and diagnostic equity: lessons from COVAX for transfusion safety. Lancet Glob Health. 2023;11(3):e415–28.
MÜLLER A, REUTER S, LIPPMANN J, et al. Recombinant antibody fragments for improved ELISA performance in blood screening applications. J Immunol Methods. 2023;518:113419.
NORHEIM OF. Equity and vulnerability in global health diagnostics. Bioethics. 2022;36(4):455–72.
OLIVEIRA MF, DIAS JS, VIEIRA A, et al. Desafios na implantação do teste molecular em países em desenvolvimento. Rev Panam Salud Publica. 2017;41:e89.
Pan American Health Organization (PAHO). Blood safety and availability in the Americas: strategic plan 2022–2030. Washington, DC: PAHO; 2022.
Pan American Health Organization (PAHO). Regional progress on NAT implementation in Latin America and the Caribbean. Washington, DC: PAHO; 2022.
Pan American Health Organization. Strategic framework for blood services in the Americas 2022–2030. Washington (DC): PAHO; 2022.
PETZ LD, GARRATTY G. Immune hemolytic anemias. 2nd ed. Philadelphia: Churchill Livingstone; 2004.
REIS J, RODRIGUES M, ALMEIDA P. Avanços científicos e históricos na hemoterapia moderna. Rev Bras Hematol Hemoter. 2019;41(3):210–8.
SANTOS L, NOGUEIRA R, BARROS L. Zika and dengue viruses in blood donors: residual risk and surveillance strategies. J Clin Virol. 2022;155:105274.
SCHMIDT M, HOURFAR MK, NICOL SB, et al. Pathogen inactivation, bacterial detection and NAT: impact on transfusion safety in Germany 2000–2020. Transfus Med Hemother. 2021;48(3):176–84.
SHAYAN S et al. Operational challenges of NAT in developing countries. Transfus Med Hemother. 2022;49(3):145–159.
SOAREZ PC, NOVAES HMD. Economic evaluation of molecular screening for transfusion safety in Brazil. Cad Saúde Pública. 2017;33(8):e00105016.
SOUTO FILHO JTD et al. Implementation of NAT in Brazil: impact on transfusion safety. Vox Sang. 2020;115(6):512–520.
STRAMER SL et al. Nucleic acid testing to detect transfusion-transmissible infections: 20 years of progress. Transfusion. 2019;59(7):2240–2253.
STRAMER SL, HOLLINGER FB, KATZ LM, et al. Emerging infectious disease agents and their potential threat to transfusion safety. Transfusion. 2019;59(12):4113–26.
TANAKA J et al. Detection of occult hepatitis B infections by NAT: experience from Japan. J Clin Virol. 2022;150(5):105–115.
THE LANCET DIGITAL HEALTH. Data integrity and algorithmic ethics in transfusion medicine. Lancet Digit Health. 2023;5(8):e511–24.
THE LANCET GLOBAL HEALTH. Justice, governance, and diagnostics in global transfusion medicine. Lancet Glob Health. 2023;11(5):e645–58.
THE LANCET HAEMATOLOGY. Toward equitable and sustainable blood diagnostics. Lancet Haematol. 2023;10(6):e455–72.
THE LANCET HAEMATOLOGY. Transfusion safety and the Sustainable Development Goals: progress and priorities. Lancet Haematol. 2023;10(8):e530–48.
TIAN X, OTIENO J, MWANGI L. Systems analysis and logistics optimization in molecular blood screening in Sub-Saharan Africa. Transfus Med Rev. 2024;38(2):101–17.
TRANSFUSION. Artificial intelligence, blockchain, and smart lab integration in transfusion diagnostics: global trends 2023. Transfusion. 2023;63(9):1410–29.
TRANSFUSION. Comparative analysis of NAT implementation models: ID-NAT versus mini-pool strategies in global blood safety programs. Transfusion. 2023;63(10):1425–39.
TRANSFUSION. Comparative evaluation of ELISA configurations for viral antigen detection in blood screening laboratories. Transfusion. 2023;63(8):1054–62.
TRANSFUSION. Cost-effectiveness of molecular blood screening in low- and middle- income countries: evidence from global case studies. Transfusion. 2023;63(7):989–1007.
TRANSFUSION. Global disparities in NAT implementation and economic modeling in transfusion safety programs. Transfusion. 2023;63(9):1334–49.
TRANSFUSION. Global performance of NAT-based screening for HIV, HBV and HCV in blood donors: risk reduction and cost-effectiveness outcomes. Transfusion. 2023;63(6):855–72.
TRANSFUSION. Global trends in residual risk reduction after NAT implementation in blood safety programs. Transfusion. 2023;63(8):1215–29.
TRANSFUSION. Meta-analytic evidence of NAT performance in global blood safety programs: 20-year synthesis. Transfusion. 2023;63(9):1330–48.
TRANSFUSION. Molecular advances in NAT screening for transfusion-transmissible infections: performance, automation and global outcomes. Transfusion. 2023;63(7):987- 1004.
TRANSFUSION. Quantitative comparison of ELISA and NAT performance in global transfusion safety networks. Transfusion. 2023;63(8):1248–64.
UNITED NATIONS. Transforming our world: the 2030 Agenda for Sustainable Development. New York: UN; 2020.
VOGELSTEIN B, KINZLER KW. Digital PCR: advancing nucleic acid quantification for precision medicine. Proc Natl Acad Sci USA. 2020;117(47):29533–29539.
VOX SANGUINIS. Automation and digital transformation in molecular and serological blood screening: a systematic review. Vox Sang. 2023;118(2):189–206.
VOX SANGUINIS. Economic and operational evaluation of centralized NAT implementation in Latin America. Vox Sang. 2022;117(9):921–38.
VOX SANGUINIS. Equity and evidence gaps in molecular screening for transfusion safety: a global review. Vox Sang. 2023;118(6):582–601.
VOX SANGUINIS. Equity, sustainability and innovation in blood screening for the 21st century. Vox Sang. 2023;118(7):712–29.
VOX SANGUINIS. Ethical imperatives for equitable access to molecular blood screening. Vox Sang. 2023;118(10):811–29.
VOX SANGUINIS. Global performance of combined serological and molecular screening in blood donor testing. Vox Sang. 2022;117(11):1108–25.
VOX SANGUINIS. Integrative strategies for ELISA and NAT co-implementation in low- and middle-income countries. Vox Sang. 2022;117(10):1050–67.
VOX SANGUINIS. Next-generation technologies in transfusion diagnostics: integration of AI, NGS and biosensors. Vox Sang. 2023;118(3):257–74.
VOX SANGUINIS. Policy integration of molecular diagnostics in public blood systems: comparative analysis 2023. Vox Sang. 2023;118(4):345–61.
VOX SANGUINIS. Systematic review on NAT implementation outcomes in low- and middle-income countries. Vox Sang. 2022;117(10):1041–59.
VOX SANGUINIS. Transfusion governance and global data equity: bridging regulatory divides. Vox Sang. 2023;118(9):780–98.
WHO. Action Framework for Blood Safety 2020–2030: ensuring universal access to safe blood and blood products. Geneva: World Health Organization; 2021.
WONG A, LI C, ZHANG M, et al. Multiplexed ELISA-based detection of transfusion- transmissible infections: performance evaluation and implementation perspectives. Anal Chim Acta. 2023;1256:341212.
World Health Organization (WHO). Action Framework for Blood Safety 2020–2030. Geneva: WHO; 2021.
World Health Organization (WHO). Global Status Report on Blood Safety and Availability. Geneva: WHO; 2023.
World Health Organization (WHO). Global status report on blood safety and availability 2021. Geneva: WHO; 2021.
YAMASHITA T, YAMAGUCHI M, KANDA J. Economic and epidemiological evaluation of combined ELISA-NAT screening strategies. Vox Sang. 2021;116(8):897–912.
ZHOU X et al. CRISPR-based diagnostics in transfusion medicine. Nat Biotechnol. 2023;41(3):415–428.
ZIMLICHMAN E et al. Global safety and hemovigilance as part of the SDG framework. Lancet Glob Health. 2022;10(9):e1285–e1294.
ZIMLICHMAN E, SUTHAR D, KUMARI R. Global hemovigilance and the 2030 Agenda: strengthening patient safety through transfusion governance. Vox Sang. 2022;117(9):881–901.
ZOU S, DODD RY, FOSTER GA, et al. Emerging technologies for blood safety and supply chain integrity: the role of blockchain. Vox Sang. 2022;117(7):790–802.
APÊNDICE A – Instrumento de coleta de dados.
Autor / Ano | Título | Local do Estud o | Categor ia da Fonte | Tipo e Metodol ogia | Amostra | Metodologia | Conclusão |
Echeva rría L.; López M.;BarretoP. et al. (2019) | Human error contribut ion to ELISAperforma nce variabilit y: implicati ons for transfusi on screenin g laboratories | Espanha | Artigo Científico | Estudo observac ional analítico | 12 laboratórios de triagem | Análise de erros operacionais e variabilidade de desempenho em ELISA | Identificou que até 15% da variabilidade nos resultados do ELISA se deve a falhas humanas, reforçando a necessidade de automação. |
EDQM (2023) | Automat ed molecula r workflo ws and biosafetystandards in blood donor screenin g laborator ies | França | Diretriz Técnica | Norma técnica internaci onal | Laborató rios de triagem molecula r | Definição de fluxos de trabalho automatizados com biossegurança | Estabelece diretrizes de automação completa para NAT e sorologia, otimizando desempenho e reduzindo contaminações cruzadas. |
EDQM (2023) | Automati on and harmoniz ation standards for immunoa ssay- based bloodscreening laborator ies | França | Diretriz Técnica | Padrão técnico e regulatór io europeu | Laborató rios membros do Conselho da Europa | Uniformização de protocolos e integração de automação laboratorial | Promove a interoperabilidade entre plataformas ELISA e NAT em bancos de sangue europeus. |
| EDQM (2023) | Automati on standards and analytical performance in immunoa ssay- based blood screening | França | Diretriz Técnica | Documento normativo técnico | Não aplicável | Avaliação de desempenho analítico em sistemas automatizados | Define parâmetros mínimos de precisão, sensibilidade e controle de qualidade em testes automatizados de triagem. |
| EDQM (2023) | Compara tive diagnostic accuracy of serological and molecular screening assays in blood donor testing | França | Relatório Técnico | Estudo comparativo multicêntrico | 20 laboratórios europeus | Comparação de acurácia diagnóstica entre ELISA e NAT | Mostra que o NAT apresenta sensibilidade 99,9% e reduz o risco residual em até 95% em comparação à sorologia isolada. |
| EDQM (2023) | Dual screening strategies in transfusion medicine:operation al and economic evaluation | França | Relatório Técnico | Estudo de avaliação operacional e econômica | Centros de triagem europeus | Análise custo- benefício da dupla triagem (ELISA + NAT) | Conclui que o modelo combinado é o mais custo- efetivo e aumenta a segurança transfusional. |
| EDQM (2023) | Economic and molecular impacts of NAT- based screening in transfusion medicine | França | Relatório Técnico | Avaliação econômica e molecula r | Laboratórios NAT | Revisão de impacto financeiro e genético da triagem molecular | Aponta sustentabilidade a longo prazo do NAT em sistemas públicos de saúde. |
| EDQM (2023) | Economic evaluation of molecula r blood screening strategies in public health systems | França | Relatório Técnico | Avaliação de custo- efetividade | Não aplicável | Comparação de modelos econômicos entre NAT centralizado e descentraliza do | Demonstra que a centralização do NAT reduz custos em até 40% mantendo a sensibilidade diagnóstica. |
| EDQM (2023) | Economic modeling of centralized NAT blood screening in public health systems: efficiency and sustainability outcomes | França | Relatório Técnico | Modelagem econômica e operacional | Modelos de triagem pública européia | Simulação de impacto financeiro e eficiência operacional | Conclui que a centralização do NAT é o modelo mais sustentável para sistemas públicos de saúde. |
| EDQM (2023) | Emerging diagnostic biotechnologies for molecula r blood screening: opportun ities and challeng es | França | Diretriz Técnica | Análise de biotecnologias emergent es | Não aplicável | Revisão de novas plataformas diagnósticas | Apresena CRISPR,IA e micro fluídica como tecnologias futuras para descentralização da triagem molecular. |
| EDQM (2023) | Evidence-based frame works for NAT cost- effective ness and bio safety outcomes | França | Relatório Técnico | Revisão técnica e econômica | Não aplicável | Análise integrada de segurança e custo- benefício do NAT | Comprova que o NAT reduz custos hospitalares e melhora a biossegurança transfusional. |
| EDQM (2023) | Global benchmarking of molecula r blood screening programs: 2023 report | França | Relatório Técnico | Estudo comparativo internacional | Programas de triagem de 40 países | Benchmarking global de eficiência e cobertura diagnóstica | Evidencia que a Europa e o Japão lideram em cobertura NAT superior a 95%. |
| EDQM (2023) | Global regulator y frame works for NAT and molecula r blood screening: evaluation 2023 | França | Guia Técnico Internacional | Manual de qualidade e segurança em hemoterapia | Instituições europeia s de sangue | Reúne diretrizes de boas práticas e controle de qualidade em componentes sanguíneos | Padroniza processos laboratoriais e reforça a importância da triagem molecular para segurança transfusional. |
| EDQM (2023) | Molecular screening standards and genomic surveillance for emergingvariants in blood safety programs | França | Artigo Científico | Pesquisa laboratorial aplicada | Ensaios imunológicos | Desenvolvimento de conjugados enzimáticos bioengenheirados e antígenos recombinantes | Melhorou a sensibilidade e estabilidade do ELISA em triagens sob altas temperatura s e condições adversas. |
| EDQM (2023) | Operational and sustainab ility frame works for NAT-based blood screening laboratories | França | Diretriz Técnica | Modelo técnico- operacional | Laboratórios NAT europeus | Proposta de estrutura de governança e sustentabilidade | Apresenta parâmetros de gestão e eficiência operacional para triagem molecular contínua. |
| EDQM (2023) | Sustainable laborator y automation frame works for blood screening and biosafety systems | França | Diretriz Técnica | Modelo de sustentabilidade laboratorial | Laboratórios de triagem molecula r europeus | Proposta de modelo sustentável para automação em triagens NAT | Estabelece padrões de eficiência energética e redução de resíduos em sistemas de triagem automatizada. |
| EDQM (2023) | Guide to the preparation, use and quality assurance of blood components. 21st ed. | França | Guia Técnico Internacional | Manual de qualidade e segurança em hemoterapia | Instituições europeia s de sangue | Reúne diretrizes de boas práticas e controle de qualidade em componentes sanguíneos | Padroniza processos laboratoriais e reforça a importância da triagem molecular para segurança transfusional. |
| Feng Y.;Zhang X.; Liu Q. et al. (2022) | Bioengin eered enzyme conjugat es and recombin ant antigens for next-generation ELISA performance enhancement | China | Artigo Científico | Pesquisa laboratorial aplicada | Ensaios imunológicos | Desenvolvimento de conjugados enzimáticos bioengenheirados e antígenos recombinantes | Melhorou a sensibilidade e estabilidade do ELISA em triagens sob altas temperaturas e condições adversas. |
| Ferreira C.M. et al.(2020) | Advances and limitations of ELISA in transfusional screening | Brasil | Artigo Científico | Revisão de literatura crítica | Não aplicável | Análise dos avanços técnicos e limitações do ELISA natriagem de doadores | Evidencia a necessidade de integração do ELISA com métodos moleculares para maior segurança transfusional. |
| Galeano R. et al. (2024) | Sustaina ble blood systems and molecula r diagnostics integration | Espanha | Artigo Científico | Estudo interdisciplinar | Sistemas públicos de sangue | Integração de sustentabilidade e diagnóstico molecular | Defende a convergência entre sustentabilidade e inovação tecnológica em triagem de sangue. |
| Galeano R.;Yin T.; Zhou M. (2024) | Microflu idic- CRISPRsystems and AI- driven bio sensors for decentral ized bloodscreening | China/ Espanha | Artigo Científico | Estudo tecnológico experimental | Modelos laboratoriais descentra lizados | Desenvolvimento de sistemas microfluídico s e sensores com IA | Apresenta soluções portáteis e autônomas para triagem rápida em regiões remotas. |
| Gonçalves A.P.;Lima M.;Torres J. et al. (2021) | Implementação do teste molecula r (NAT) e seus impactos na segurança transfusional | Brasil | Artigo Científico | Estudo descritivo e avaliativo | Laboratórios da Rede Pública de Hemoter apia | Avaliação do impacto da adoção do NAT | Confirma aumento significativo da segurança e rastreabilidade após implantação do NAT. |
| Gostin L.O.;Meier B.M.(2018) | Human rights and global health equity: the case for diagnostics access | EUA | Artigo Científico | Ensaio jurídico e ético | Não aplicável | Discussão sobre o direito à saúde e acesso a tecnologias diagnósticas | Argumenta que o acesso a testes NAT e ELISA é parte essencial do direito humano à saúde. |
| Holling er F.B.;Busch M.P.(2022) | Transfusi on- transmitt ed infection s: NATimpleme ntation and outcome s | EUA | Artigo Científico | Revisão técnica e epidemio lógica | Casos clínicos e dados laboratoriais | Análise do impacto do NAT após sua implementação global | Mostra eliminação quase completa da transmissão de HIV e HCV via transfusão em países com NAT obrigatório. |
| Hossain A.;Galean o R.;Kumar P. (2022) | Mobile blood labs and digital health integration for sustainab le transfusion services | Bangladesh / Espanha | Artigo Científico | Estudo de inovação tecnológica | Unidades móveis de coleta de sangue | Avaliação da integração de laboratórios móveis com sistemas digitais de saúde | Propõe o uso de triagem digital e móvel como solução sustentável para regiões de difícil acesso. |
| Huang Y.; LiF.; TanZ. et al. (2023) | CRISPR-Cas– based molecula r detection for transfusion safety: toward rapid and decentral ized NAT alternatives | China | Artigo Científico | Pesquisa experimental | Ensaios laboratoriais | Desenvolvimento de biossensores CRISPR para triagem rápida | Demonstra potencial para substituir parcialmente o NAT em triagens rápidas e de baixo custo. |
| Huang Y.; LiF.; TanZ. et al. (2023) | CRISPR-Cas– driven molecula r diagnostics for real-time blood safety monitoring | China | Artigo Científico | Estudo experimental | Amostras clínicas de sangue | Aplicação do sistema CRISPR para monitoramento em tempo real | Aponta o uso do CRISPR como ferramenta de vigilância ativa e rastreabilidade transfusional. |
| Huang Y.;Zhou D.;Chen L. et al. (2022) | Engineer ing of thermost able horseradi sh peroxida se variants for robust immunoas says in tropical environments | China | Artigo Científico | Pesquisa aplicada | Enzimas recombin antes | Criação de variantes termoestáveis de peroxidase para uso em ELISA | Permite maior estabilidade e precisão de testes imunológicos em regiões tropicais com infraestrutura limitada. |
| ISBT (2022) | Data integration and regulator y convergence in global blood safety | Holanda | Relatório Técnico/ Artigo Científico | Análise de integração regulatória | Países membros ISBT | Mapeamento de políticas e interoperabilidade de dados em hemoterapia | Propõe harmonização internacional de sistemas de dados e padrões laboratoriais para triagem segura. |
| ISBT (2023) | Global scientific roadmap on transfusion- transmitt ed infection s: gaps and priorities for 2023–2030 | Holanda | Relatório Técnico | Síntese de prioridades científica s globais | Estudos multicêntricos internacionais | Identificação de lacunas e tendências na segurança transfusional | Estabelece plano estratégico global para pesquisa em infecções transmissíve is por transfusão. |
| ISBT (2023) | Transfusi on diagnosti cs 2030: critical synthesis and future direction s | Holanda | Relatório Científico | Análise crítica e prospectiva | Literatura científica 2010–2023 | Revisão e projeção de tendências diagnósticas | Aponta integração de IA, CRISPR e dPCR como pilares da triagem de próxima geração. |
| Kasber gen S.; Giménez Richart e C.;Nielsen R. (2023) | Transfusi on- transmitt ed arbovirus es and diagnosti c cross- reactivity:systemati c review and research priorities | Holanda / Espanha | Artigo Científico | Revisão sistemática | 92 estudos internacionais | Revisão de arboviroses transmisívei s e reatividade cruzada | Destaca necessidade de testes moleculares específicos para arbovírus em bancos de sangue. |
| Kellner M.J.;Gooten berg J.S.;Zhang F. (2023) | CRISPR-based diagnosti cs in blood screening: towards rapid and affordable molecula r detection | EUA | Artigo Científico | Estudo experimental e de revisão | Ensaios laboratoriais de CRISPR-Cas13 | Avaliação de diagnóstico molecular rápido e acessível | Demonstra a viabilidade do uso de CRISPR como alternativa rápida e econômica ao NAT. |
| Khan K.A.;Dey S.; Gupta A. et al. (2022) | CRISPR-based molecula r detection systems for transfusion- transmitt ed infection s: prospects and challenges | Índia | Artigo Científico | Revisão e estudo de caso | Casos de HIV, HCV, HBV | Análise do uso de sistemas CRISPR para triagem transfusional | Conclui que o CRISPR oferece alta especificidade e aplicabilidade em contextos de baixa infraestrutura. |
| Kleinm an S.; Busch M.P.(2019) | Assessing the impact of new technolo gies on transfusi on safety and globaldisparities | EUA | Artigo Científico | Revisão crítica internacional | Dados epidemio lógicos globais | Avaliação do impacto de novas tecnologias diagnósticas | Conclui que o NAT e novas plataformas reduziram o risco residual global e ampliaram a equidade diagnóstica. |
| Kleinm an S.; Vrielin k H. (2022) | Complementary roles of ELISA and NAT in transfusi on safety: revisiting evidence and policy | Holanda | Artigo Científico | Revisão integrati va e de políticas públicas | Estudos comparat ivos ELISA/ NAT | Síntese de evidências sobre a dupla triagem | Reafirma que o uso combinado de ELISA e NAT é o padrão-ouro global em biossegurança transfusional. |
| Kleinm an S.; Vrielin k H. (2022) | Global blood safety: lessons from the 21st century | Holanda | Artigo Científico | Revisão narrativa | Experiências internacionais | Revisão histórica de políticas e tecnologias em hemoterapia | Demonstra a evolução das políticas de sangue seguro e o papel das tecnologias moleculares. |
| Lancet Haematology (2023) | Digital PCR, CRISPR and microfluidic platform s for next- decade blood safetystrategies | Reino Unido | Artigo Científico | Revisão tecnológica | Estudos laboratoriais e clínicos | Análise de plataformas moleculares emergentes | Prevê que dPCR e CRISPR transformarão o diagnóstico transfusional nos próximos 10 anos. |
| Lancet Haemat ology (2023) | Environ mental and ethical challenges of molecula r diagnosti cs in blood safety | Reino Unido | Artigo Científico | Revisão crítica e ética | Não aplicável | Discussão sobre sustentabilidade e ética na triagem molecular | Aponta a necessidade de equilibrar inovação diagnóstica e responsabilidade ambiental. |
| Lancet Haemat ology (2023) | Ethical imperati ves in molecula r and serological co- screening for transfusi on safety | Reino Unido | Artigo Científico | Ensaio bioético | Não aplicável | Discussão sobre ética e justiça sanitária | Defende a triagem dupla como imperativo ético de biossegurança e equidade global. |
| Lancet Haemat ology (2023) | Global transfusi on safety and digital governance in blood systems | Reino Unido | Artigo Científico | Revisão de governança digital | Sistemas de hemoterapia internacionais | Análise da digitalização e interoperabilidade de sistemas transfusionais | Mostra que governança digital e blockchain aumentam transparência e rastreabilidade global. |
| Lancet Haemat ology (2023) | Governance and digital transformation in transfusi on policies: global implications | Reino Unido | Artigo Científico | Revisão integrati va e política | Diretrizes de 45 países | Análise das transformações digitais nas políticas transfusionais | Conclui que a transformação digital é indispensável para equidade e eficiência em sistemas de sangue. |
| Landsteiner K. (1901) | Zur Kenntnis der antiferm entativen,lytischen und agglutini erenden Wirkung en des Blutseru ms und der Lymphe | Áustria | Artigo Científico Clássico | Estudo experimental pioneiro | Amostras de sangue humano | Investigação dos mecanismos de aglutinação e imunidade | Descobriu os grupos sanguíneos ABO,marco inicial da medicina transfusional. |
| Lee H.; Alabdul atif A.; Farahan i B. (2023) | Blockcha in- enabled smart labs for secure transfusi on governance | Canadá / Arábia Saudita | Artigo Científico Clássico | Estudo tecnológico e conceitual | Modelos simulado s de laboratórios automatizados | Desenvolvimento de laboratórios inteligentes com blockchain | Propõe a aplicação de blockchain em rastreabilidade e governança de dados transfusonais. |
| Lelie P.N.;Reesink H.W.;Tjärnlu nd A. et al. (2023) | Next- generation NATmultple x assays for simultaneous detection of transfusi on- transmissible viruses | Suécia / Países Baixos | Artigo Científico Clássico | Pesquisa experimental multicêntrica | Amostra s de sangue de doadores | Avaliação de ensaios NAT multiplex de nova geração | Demonstrou detecção simultânea de HIV, HBV e HCV com maior eficiência operacional. |
| Mahmood T.; Khan S.;QureshiM. et al.(2022) | Operational resilience of ELISA kits under variable environmental condition s: implications for tropical laboratories | Paquistão | Artigo Científico | Estudo experimental | Kits ELISA comerciais | Testes de estabilidade e desempenho sob condições variáveis de temperatura | Mostrou que kits adaptados para clima tropical mantêm desempenho superior a 95% de acurácia. |
| Maunder J.; Greening D.W.; McKin non E. et al. (2021) | Diagnostic limitations of serological assays for hepatitis virus geno type s 4 and 6: molecular updates for blood screenin g programs | Reino Unido/ Austrália | Artigo Científico | Revisão e estudo laboratorial | Casos clínicos de hepatite | Análise da detecção sorológica de variantes virais | Evidencia necessidade de atualização dos kits ELISA frente à diversidade genotípica do HCV. |
| Maunder M.; Bourlet T.;Klein H.G.(2023) | Global standards for molecula r blood screenin g: progress and gaps in harmoniz ation | França | Revisão Científica Internacional | Revisão integrati va e análise normativa | Padrões laborator iais de 35 países | Avaliação de harmonização de protocolos NAT globais | Conclui que a falta de uniformização regulatória é o maior obstáculo à equidade diagnóstica global. |
| Meyer A.;Stramer S.L.;Kleinm an S.H.(2023) | Integrated molecula r and immunologic screenin g in blood safety: twenty years of dualtesting | EUA | Artigo Científico | Revisão retrospec tiva | 20 anos de dados NAT e ELISA | Análise do impacto histórico da dupla triagem | Mostra redução de mais de 95% no risco residual de HIV, HBV e HCV após implementação combinada. |
| Ministério da Saúde (BR)(2022) | Política Nacional de Sangue e Hemo derivados: diretrizes atualizadas | Brasil | Documento Oficial | Relatório normativo e estratégico | Rede Nacional de Hemocentros | Atualização das diretrizes nacionais de hemoterapia | Reforça a obrigatoriedade do NAT e a consolidação da Hemorrede Nacional como política pública. |
| Ministério da Saúde (BR)(2022) | Rede Nacional de Triagem NAT: Relatório técnico 2022 | Brasil | Relatório Técnico | Análise institucional | Laboratórios regionais NAT | Relatório de desempenho da Rede Nacional NAT | Apresenta dados de cobertura acima de 90% nas triagens públicas brasileiras. |
| Ministério da Saúde (BR)(2023) | Relatório Nacional da Rede de Triagem NAT 2023 | Brasil | Relatório Técnico | Monitora mento anual | Laboratórios e hemocentros nacionais | Análise da expansão e desempenho da rede NAT | Comprova a consolidaçã o da cobertura molecular no SUS e a redução de infecções transfusionais. |
| Ministério da Saúde (Brasil) (2022) | Program a Nacional de Triagem NAT: relatório técnico 2022 | Brasil | Relatório Técnico | Avaliação governa mental | Instituiçõ es vinculadas ao CGSH | Relatório de gestão do programa NAT | Apresenta eficiência operacional e adesão crescente de hemocentro s regionais. |
| Moon S.; Daniels N.;Gostin L.O.(2023) | Global health justice and diagnosti c equity: lessons from COVAX for transfusi on safety | Reino Unido/ EUA | Artigo Científico | Análise crítica e comparat iva | Program as de saúde global | Revisão dos mecanismos de equidade no acesso a diagnósticos | Argumenta que o acesso universal a NAT e ELISA é essencial para a justiça sanitária global. |
| Müller A.;Reuter S.; Lippma nn J. et al. (2023) | Recombinant antibody fragment s for improve d ELISA performance in blood screenin gapplications | Alemanha | Artigo Científico | Pesquisa experimental | Anticorp os recombin antes | Desenvolvimento de fragmentos recombinante s para ELISA | Demonstrou aumento da sensibilidade diagnóstica e redução de falsos positivos em triagem sorológica. |
| Norheim O.F.(2022) | Equity and vulnerabi lity in global health diagnosti cs | Noruega | Artigo Científico | Análise bioética | Não aplicável | Reflexão sobre equidade e vulnerabilidade em diagnósticos globais | Destaca a importância de políticas equitativas no acesso a testes moleculares e sorológicos. |
| Oliveira M.F.;Dias J.S.;VieiraA. et al. (2017) | Desafios na implantação do teste molecula r em países em desenvolvimento | Brasil | Artigo Científico | Estudo descritivo e avaliativo | Hemocentros públicos brasileiro s | Análise de obstáculos técnicos e econômicos na implementação do NAT | Conclui que a centralização e o financiamento público são essenciais para sustentabilidade do NAT. |
| PAHO (2022) | Blood safety and availabili ty in the America s: strategic plan 2022–2030 | Washington, DC | Relatório Técnico | Plano estratégico regional | Países- membros da OPAS | Definição de metas de segurança e disponibilidade de sangue | Propõe que até 2030 todos os países adotem triagem molecular em seus sistemas públicos desangue. |
| PAHO (2022) | Regional progress on NAT implementation in Latin America and the Caribbean | Washington, DC | Relatório Técnico | Monitora mento regional | Países latino- americanos e caribenhos | Avaliação de avanço do NAT na região | Constata avanços significativo s no Brasil e Chile, mas atraso em países com infraestrutura limitada. |
| PAHO (2022) | Strategic frame work for blood services in the America s 2022–2030 | Washington, DC | Relatório Técnico | Documento de diretrizes estratégicas | Sistemas nacionais de sangue | Estruturação de políticas integradas de sangue seguro | Reforça a triagem molecular e o uso de automação como pilares para o ODS 3. |
| Petz L.D.;Garratt y G. (2004) | Immune hemolytic anemias | EUA | Livro Técnico | Obra de referência em hematologia | Casos clínicos | Discussão sobre mecanismos imunológicos de anemias hemolíticas | Base conceitual para compreende r reações imunes em transfusões e triagem deanticorpos. |
| Reis J.; Rodrigues M.; Almeida P. (2019) | Avanços científico s e histórico s na hemoterapia moderna | Brasil | Artigo Científico | Revisão de literatura | Não aplicável | Análise evolutiva da hemoterapia e seus marcos científicos | Descreve o progresso das técnicas transfusionais até o advento do NAT. |
| Santos L.; Nogueira R.; Barros L. (2022) | Zika and dengue viruses in blood donors: residual risk and surveillance strategies | Brasil | Artigo Científico | Estudo epidemio lógico | Doadores de sangue | Avaliação do risco residual de arboviroses na triagem transfusional | Conclui que o NAT é ferramenta promissora para mitigação de infecções emergentes como Zika e dengue. |
| Schmidt M.; Hourfar M.K.;NicolS. B. et al.(2021) | Pathogen inactivati on, bacterial detection and NAT: impact on transfusi on safety in Germany 2000–2020 | Alemanha | Artigo Científico | Estudo retrospectivo | Dados nacionais de hemoterapia | Avaliação de 20 anos de triagem molecular e inativação patogênica | Mostra queda expressiva na transmissão transfusional e aumento na rastreabilidade do sangue. |
| Shayan S. et al. (2022) | Operatio nal challeng es of NAT in developi ng countries | Irã | Artigo Científico | Estudo qualitativo e operacional | Centros hemoterápicos | Identificação de barreiras logísticas e econômicas | Ressalta a necessidade de treinamento técnico e financiamento internacional contínuo. |
| Soarez P.C.;Novaes H.M.D. (2017) | Economic evaluation of molecula r screenin g for transfusi on safety in Brazil | Brasil | Artigo Científico | Estudo econômico e analítico | Rede pública de hemocentros | Análise de custo- efetividade do NAT | Mostra que o NAT é economica mente viável ao considerar custos evitados de infecção crônica. |
| Souto Filho J.T.D. et al. (2020) | Implementation of NAT in Brazil: impact on transfusi on safety | Brasil | Artigo Científico | Estudo multicêntrico | HEMO MINAS, HEMOPA e Pró- Sangue | Avaliação do impacto da implementação do NAT | Detectou centenas de infecções na janela imunológica não identificada s pela sorologia convencional. |
| Stramer S.L. et al.(2019) | Nucleic acid testing to detect transfusi on- transmissible infection s: 20 years of progress | EUA | Revisão Científica | Revisão técnica e epidemio lógica | Dados internacionais de triagem | Análise histórica da evolução do NAT | Confirma a redução global de infecções transfusionais após adoção do NAT. |
| Stramer S.L.;Holling er F.B.;KatzL.M. et al.(2019) | Emerging infectious disease agents and their potential threat to transfusion safety | EUA | Artigo Científico | Revisão crítica | Patógenos emergentes | Identificação de riscos emergentes e desafios na triagem | Enfatiza vigilância contínua e inovação diagnóstica frente a novos vírus. |
| TanakaJ. et al. (2022) | Detection of occult hepatitis Binfections by NAT: experience from Japan | Japão | Artigo Científico | Estudo retrospec tivo e laborator ial | Doadores de sangue com IOHB | Aplicação do NAT na detecção de hepatite B oculta | Comprova a superioridade do NAT na identificação de casos invisíveis à sorologia convencional. |
| The Lancet Digital Health (2023) | Data integrity and algorithmic ethics in transfusi on medicine | Reino Unido | Artigo Científico | Análise ética e tecnológica | Não aplicável | Revisão sobre governança algorítmica e ética em IA | Recomenda estruturas de transparência e validação para algoritmos de triagem transfusional. |
| The Lancet Global Health (2023) | Justice, governance, and diagnosti cs in global transfusi on medicine | Reino Unido | Artigo Científico | Revisão crítica interdisciplinar | Não aplicável | Avaliação da justiça diagnóstica e governança em saúde | Defende equidade diagnóstica e responsabilidade social na implementação de tecnologias moleculares. |
| The Lancet Haemat ology (2023) | Toward equitable and sustainab le blood diagnosti cs | Reino Unido | Artigo Científico | Análise de sustentabilidade e equidade | Sistemas de sangue globais | Revisão das estratégias para sustentabilidade diagnóstica | Propõe políticas integradas que conciliem biossegurança e neutralidade ambiental. |
| The Lancet Haemat ology (2023) | Transfusi on safety and the Sustaina ble Development Goals: progress and priorities | Reino Unido | Artigo Científico | Síntese crítica de indicador es globais | Dados de 120 países | Correlação entre triagem molecular e ODS 3 | Mostra que adoção do NAT é fundamental para atingir metas de saúde e equidade até 2030. |
| Tian X.;Otieno J.;Mwang i L. (2024) | Systems analysis and logistics optimizat ion in molecula r blood screenin g in Sub-Saharan Africa | Quênia | Artigo Científico | Estudo de modelagem de sistemas | Centros de triagem africanos | Simulação de fluxos laboratoriais e transporte de amostras | Conclui que otimização logística aumenta cobertura diagnóstica e reduz custos operacionais. |
| Transfu sion (2023) | Artificial intelligence, blockchain, and smart labintegration in transfusi on diagnosti cs: global trends 2023 | EUA | Artigo Científico | Revisão tecnológi ca global | Laboratórios automatizados e consórcios hemoterápicos | Mapeamento do uso de IA e blockchain em diagnósticos | Identifica integração digital como o novo paradigma para governança e rastreabilidade transfusional. |
| Transfu sion (2023) | Compara tive analysis of NAT implementation models: ID-NAT versus mini- pool strategies in global blood safety programs | EUA | Artigo Científico | Meta- análise comparat iva | Estudos de 35 países | Comparação entre modelos individuais e em minipool | Mostra que ID-NAT aumenta sensibilidade, enquanto MP-NAT oferece melhor custo- efetividade. |
| Transfu sion (2023) | Compara tive evaluation of ELISA configurations for viral antigen detection in blood screenin g laboratories | EUA | Artigo Científico | Estudo experimental | Laboratórios de triagem | Avaliação de diferentes formatos de ELISA | Evidencia que ELISA de quarta geração apresenta maior estabilidade e menor taxa de erro analítico. |
| Transfu sion (2023) | Cost- effective ness of molecula r blood screenin g in low- and middle- income countries:evidence from global case studies | EUA | Artigo Científico | Revisão econômica internacional | Casos em 20 países | Análise de custo- benefício do NAT | Revela que, a longo prazo, o NAT reduz custos associados ao tratamento de infecções crônicas. |
| Transfu sion (2023) | Global disparities in NAT implementation and economic modeling in transfusi on safety programs | EUA | Artigo Científico | Revisão e análise comparat iva | Estudos internacionais | Identificação de desigualdade s regionais em adoção do NAT | Aponta falta de financiamento e infraestrutura como principais barreiras em países de baixa renda. |
| Transfu sion (2023) | Global performance of NAT-based screenin g for HIV,HBV and HCV in blood donors: risk reduction and cost- effective ness outcomes | EUA | Artigo Científico | Meta- análise global | Dados de doadores de 45 países | Avaliação da eficácia do NAT em reduzir risco residual | Mostra redução de até 99% no risco de infecção transfusional após implementação. |
| Transfu sion (2023) | Global trends in residual risk reduction after NATimpleme ntation in blood safety programs | EUA | Artigo Científico | Estudo longitudi nal | Dados de hemocen tros globais | Avaliação temporal da segurança transfusional pós-NAT | Apresenta queda contínua nas taxas de infecção em países com mais de 10 anos de uso do NAT. |
| Transfu sion (2023) | Meta- analytic evidence of NAT performa nce in global blood safety programs: 20-year synthesis | EUA | Revisão Sistemá tica | Meta- análise de 20 anos de dados | Mais de 200 publicações avaliadas | Síntese de resultados globais de desempenho do NAT | Confirma o NAT como método padrão-ouro global em triagem transfusional molecular. |
| Transfu sion (2023) | Molecula r advances in NAT screenin g for transfusi on- transmissible infection s: performa nce, automation and global outcomes | EUA | Artigo Científico | Revisão sistemática e análise técnica | Program as globais de triagem | Análise dos avanços moleculares e automação na triagem NAT | Evidencia ganhos de precisão, eficiência e padronização global com o uso de NAT automatizado. |
| Transfu sion (2023) | Quantitat ive comparis on of ELISA and NAT performa nce in global transfusi on safety networks | EUA | Artigo Científico | Meta- análise comparat iva | Hemocentros internacionais | Comparação quantitativa entre sensibilidade e especificidade e de ELISA e NAT | Conclui que o NAT possui desempenho superior em todas as métricas críticas de detecção precoce. |
| United Nations (2020) | Transforming our world: the 2030 Agenda for Sustaina ble Development | Nova York | Documento Oficial | Agenda política e estratégi ca global | Países- membros da ONU | Estabelecimento de metas de desenvolvimento sustentável | Incorpora o sangue seguro e o acesso equitativo à saúde como pilares do ODS 3. |
| Vogelstein B.; Kinzler K.W.(2020) | Digital PCR: advancin g nucleic acid quantific ation for precision medicine | EUA | Artigo Científi co | Estudo técnico e metodoló gico | Sistemas de PCR digital | Avaliação da precisão da PCR digital em quantificação de ácidos nucleicos | Mostra que dPCR aumenta a sensibilidade e padroniza medições moleculares em triagens clínicas. |
| Vox Sangui nis (2023) | Automati on and digital transfor mation in molecula r and serologic al blood screenin g: a systematic review | Suíça | Revisão Sistemá tica | Revisão integrati va | Estudos internaci onais de automaç ão laborator ial | Síntese sobre transformação digital na triagem de sangue | Conclui que a automação total reduz erros humanos e melhora a eficiência operacional global. |
| Vox Sangui nis (2022) | Economic and operation al evaluation of centralized NAT implementation in Latin America | América Latina | Artigo Científico | Análise econômica regional | Redes públicas de sangue | Estudo comparativo da centralização de NAT na região | Mostra redução de 30% nos custos operacionais com manutenção da sensibilidade diagnóstica. |
| Vox Sangui nis (2023) | Equity and evidence gaps in molecula r screenin g for transfusi on safety: a global review | Reino Unido | Revisão Científi ca | Revisão integrati va | Estudos de 50 países | Avaliação das desigualdade s de acesso e lacunas de evidência | Evidencia disparidades entre países ricos e pobres no acesso à triagem molecular segura. |
| Vox Sangui nis (2023) | Equity, sustainab ility and innovation in blood screenin g for the 21st century | Reino Unido | Artigo Científi co | Estudo analítico e prospectivo | Sistemas nacionais de sangue | Discussão sobre sustentabilidade diagnóstica | Defende o uso de tecnologias sustentáveis como pilar ético da saúde global. |
| Vox Sangui nis (2023) | Ethical imperati ves for equitable access to molecula r blood screening | Reino Unido | Artigo Científi co | Análise ética e normativa | Políticas públicas internaci onais | Discussão sobre equidade diagnóstica | Aponta a triagem molecular como direito humano essencial à saúde pública. |
| Vox Sangui nis (2022) | Global performa nce of combine d serologic al and molecula r screenin g in blood donor testing | Alemanha | Artigo Científi co | Estudo comparativo internaci onal | Doadores de sangue | Avaliação do uso combinado de ELISA e NAT | Mostra que a dupla triagem reduz em até 95% o risco de transmissão de HIV, HBV e HCV. |
| Vox Sangui nis (2022) | Integrative strategies for ELISA and NAT co- implementation in low- and middle- income countries | Brasil/ Índia | Artigo Científi co | Estudo de caso e análise operacional | Hemo centros de países em desenvolvimento | Modelagem de integração diagnóstica entre ELISA e NAT | Evidencia viabilidade da dupla triagem mesmo em contextos de recursos limitados. |
| Vox Sangui nis (2023) | Next- generation technolo gies in transfusi on diagnosti cs: integrati on of AI, NGS and bio sensors | Suíça | Artigo Científi co | Revisão tecnológi ca e experime ntal | Laboratórios de triagem molecula r | Análise de tecnologias emergentes (IA, NGS,biossensores) | Mostra convergência de IA e NGS como futuro da triagem transfusional. |
| Vox Sangui nis (2023) | Policy integrati on of molecula r diagnosti cs in public blood systems: comparat ive analysis 2023 | Reino Unido | Artigo Científi co | Análise comparat iva de políticas públicas | Sistemas nacionais de triagem | Avaliação de integração regulatória global | Identifica sucesso em países com políticas estáveis e financiamento federal de NAT. |
| Vox Sangui nis (2022) | Systematic review on NAT implementation outcome s in low- and middle- income countries | Reino Unido | Revisão Sistemá tica | Meta- análise | Estudos de 2000–2022 | Síntese de resultados da implementação do NAT em países em desenvolvimento | Conclui que a descentralização do NAT aumenta cobertura e sustentabilidade operacional. |
| Vox Sangui nis (2023) | Transfusi on governance and global data equity: bridging regulator y divides | Suíça | Revisão Crítica | Análise normativa e institucional | Program as de sangue multilaterais | Discussão sobre governança e integração de dados | Propõe cooperação internacional e transparência de dados para segurança transfusional global. |
| World Health Organization (2021) | Action Frame work for Blood Safety 2020–2030: ensuring universal access to safe blood and blood products | Genebra | Relatório Oficial | Plano estratégi co global | Países- membros da OMS | Definição de metas e indicadores de sangue seguro | Estabelece metas para triagem 100%molecular até 2030 e fortalecimento da hemo vigilância global. |
| Wong A.; LiC.; Zhang M. et al.(2023) | Multiplexed ELISA-based detection of transfusi on- transmissible infection s: performa nce evaluation and implementation perspectives | China | Artigo Científi co | Estudo experime ntal e comparativo | Laboratórios de triagem asiáticos | Avaliação de sistemas ELISA multiplexados | Demonstrou alta eficiência e custo- benefício em plataformas automatizadas de triagem sorológica. |
| World Health Organization (2021) | Action Frame work for Blood Safety 2020–2030 | Genebra | Relatório Oficial | Documento normativo | Países- membros da OMS | Plano estratégico e de vigilância global | Define objetivos de universalização da triagem molecular e aprimoramento dos bancos de sangue. |
| World Health Organization (2023) | Global Status Report on Blood Safety and Availabil ity | Genebra | Relatório Técnico | Análise global de desempe nho | 120 países | Monitoramento da disponibilidade e qualidade do sangue | Constata aumento de 40% na adoção de NAT em países de média renda entre 2015 e 2023. |
| World Health Organization (2021) | Global Status Report on Blood Safety and Availabil ity 2021 | Genebra | Relatório Técnico | Análise situacional global | Países da OMS | Avaliação de indicadores de triagem molecular e sorológica | Aponta desigualdades regionais e necessidade de financiamento sustentável para programas de NAT. |
| Yamas hita T.; Yamag uchi M.;Kanda J. (2021) | Economic and epidemio logical evaluation of combine d ELISA- NAT screening strategies | Japão | Artigo Científi co | Estudo econômico e epidemio lógico | Hemocentros japonese s | Análise de custo- benefício de triagem combinada | Conclui que o uso combinado de ELISA e NAT é custo- efetivo e reduz riscos transfusionais em 98%. |
| Zhou X. et al. (2023) | CRISPR-based diagnosti cs in transfusi on medicine | China | Artigo Científi co | Estudo de inovação tecnológi ca | Laboratórios moleculares | Desenvolvimento de diagnóstico baseado em CRISPR | Apresenta metodologia ultrarrápida e econômica para detecção de patógenos em sangue. |
| Zimlich man E. et al. (2022) | Global safety and hemo vigi Lance as part of the SDG frame wo rk | Reino Unido | Artigo Científi co | Análise de políticas globais | Indicadores de 193 países | Integração da hemovigilância à Agenda 2030 | Reforça a triagem molecular como meta essencial para alcançar o ODS 3 da ONU. |
| Zimlich man E.; Suthar D.;Kumari R. (2022) | Global hemovigi lance and the 2030 Agenda: strengthening patient safety through transfusi on governance | Reino Unido | Revisão Científi ca | Estudo analítico sobre governan ça transfusi onal | Program as de sangue globais | Avaliação de marcos regulatórios e governança | Defende integração digital e interoperabi lidade global para ampliar a segurança transfusiona l. |
| Zou S.; Dodd R.Y.;Foster G.A. et al.(2022) | Emergin g technolo gies for blood safety and supply chain integrity: the role of blockchain | EUA | Artigo Científi co | Estudo técnico e prospecti vo | Centros de sangue e cadeia de suprimen tos | Avaliação da aplicação de blockchain em hemoterapia | Conclui que blockchain aumenta rastreabilidade e transparência nos processos transfusionais. |
1Discente do curso de Biomedicina da Faculdade de Ilhéus, Centro de Ensino Superior, Ilhéus, Bahia. e-mail: giseleborlini@outlook.com
2Docente do curso de Biomedicina da Faculdade de Ilhéus, Centro de Ensino Superior, Ilhéus, Bahia. e-mail: hugobioquimico@gmail.com
