REGISTRO DOI: 10.69849/revistaft/cs10202511112153
Beatriz Moraes e Silva; Natália Figueiredo Dufner; Olga Maria Santos Falco; Thalyta Vieira Ramos; Ana Carolina Sousa Campos Martines; Amanda Ramos Palacio; Luana dos Santos Ribeiro; Milena Carolino Freitas
Resumo
A trombose venosa profunda (TVP) é uma condição de relevância clínica, frequentemente associada ao uso de anticoncepcionais hormonais, sobretudo aqueles que contêm estrogênios combinados com progestagênios. Esta revisão da literatura teve como objetivo avaliar o risco de TVP relacionado ao uso de contraceptivos hormonais, destacando aspectos epidemiológicos, fisiopatológicos, clínicos, diagnósticos e terapêuticos. Os dados demonstram que contraceptivos orais combinados aumentam o risco de tromboembolismo venoso (TEV), especialmente em usuárias com fatores predisponentes, como trombofilias hereditárias, obesidade, tabagismo, idade avançada e histórico pessoal ou familiar de trombose. O risco varia conforme a dose de estrogênio, tipo de progestagênio, via de administração e duração do uso. Métodos compostos apenas por progestagênios, como pílulas de progestagênio isolado (POPs), implantes subdérmicos e dispositivos intrauterinos hormonais (DIU-LNG), apresentam risco significativamente reduzido. O diagnóstico da TVP requer abordagem clínica com escore de Wells, exames laboratoriais como o D-dímero e exames de imagem, destacando-se o eco Doppler. O manejo clínico exige abordagem multiprofissional, avaliação individualizada e tomada de decisão compartilhada, priorizando a segurança, eficácia terapêutica e preferência da paciente. Conclui-se que, embora existam riscos associados ao uso de contraceptivos hormonais, estratégias de triagem e alternativas terapêuticas seguras permitem o uso racional e personalizado, reduzindo a morbimortalidade associada ao TEV.
Palavras-chaves
Trombose venosa profunda. Contraceptivos hormonais. Tromboembolismo venoso. Estrogênio. Progestagênio. Fatores de risco. Segurança terapêutica.
Introdução
A trombose venosa profunda (TVP) é uma condição clínica de grande relevância no cenário da saúde pública mundial, caracterizada pela formação de coágulos sanguíneos no interior das veias profundas, com predomínio nos membros inferiores. Quando não identificada e tratada de forma eficaz, a TVP pode evoluir para embolia pulmonar (EP), condição potencialmente fatal. Juntas, TVP e EP compõem o espectro do tromboembolismo venoso (TEV), responsável por elevados índices de morbimortalidade em diversos contextos clínicos. Estima-se que, anualmente, ocorram entre 1 a 2 casos de TEV por 1.000 habitantes na população geral, sendo essa incidência ainda maior entre mulheres expostas a fatores de risco específicos, como o uso de anticoncepcionais hormonais (Lidegaard et al., 2011).
Desde o advento da pílula anticoncepcional nas décadas de 1950 e 1960, os contraceptivos hormonais têm desempenhado um papel central na promoção da autonomia reprodutiva feminina, na redução de gravidezes não planejadas e na melhoria da saúde ginecológica. Entretanto, paralelamente aos benefícios amplamente reconhecidos, estudos científicos começaram a demonstrar associações entre o uso desses fármacos e o aumento do risco de eventos tromboembólicos (Tchaikovski; Rosing, 2010). A primeira geração de contraceptivos orais apresentou concentrações elevadas de estrogênio sintético, principalmente o etinilestradiol, o que resultava em um risco consideravelmente aumentado de TEV. Com o passar das décadas, as formulações foram modificadas, buscando reduzir a dose hormonal e introduzindo novas progestinas, com o intuito de diminuir os efeitos adversos, entre eles o risco trombótico. Ainda assim, mesmo com doses reduzidas e progestinas de última geração, o risco de trombose venosa persiste e continua sendo objeto de estudo e debate (Blondon et al., 2022).
Atualmente aponta-se que o risco de trombose associado aos anticoncepcionais hormonais varia de acordo com diversos fatores: o tipo de hormônio utilizado, a dose do estrogênio, a geração da progestina, a via de administração (oral, transdérmica, injetável, vaginal ou intrauterina), assim como características clínicas individuais da paciente. Por exemplo, os contraceptivos orais combinados (COCs), compostos por etinilestradiol associado a diferentes progestinas, têm um efeito reconhecidamente pró-coagulante, ao induzir alterações na cascata de coagulação, a fibrinólise e na função endotelial (Mørch et al., 2017). Progestinas de terceira e quarta gerações, como desogestrel e drospirenona, têm sido associadas a um risco trombótico mais elevado em comparação com progestinas mais antigas, como o levonorgestrel (Lidegaard et al., 2009).
Além dos fatores farmacológicos, aspectos clínicos e epidemiológicos das usuárias também impactam o risco de desenvolvimento de TEV. Mulheres com histórico pessoal ou familiar de trombose, portadoras de trombofilias hereditárias (como mutações do fator V de Leiden ou da protrombina), obesas, tabagistas ou acima de 35 anos apresentam risco adicional significativo (Lidegaard et al., 2011). Em muitos casos, esse risco pode ser exacerbado pela falta de triagem adequada antes da prescrição dos métodos hormonais. A ausência de protocolos clínicos padronizados para a avaliação do perfil trombótico das pacientes contribui para que mulheres potencialmente vulneráveis sejam expostas ao risco de eventos graves, como TVP e EP (Blondon et al., 2022). No contexto da saúde pública e da atenção primária, essa problemática adquire ainda maior complexidade. O uso disseminado de contraceptivos hormonais entre mulheres em idade fértil, especialmente em países em desenvolvimento, muitas vezes ocorre sem acompanhamento médico contínuo ou sem investigação prévia de comorbidades (Mørch et al., 2017). Assim, torna-se fundamental que profissionais de saúde estejam capacitados para reconhecer os fatores de risco associados, orientar as pacientes de forma adequada e, sempre que necessário, indicar métodos contraceptivos alternativos, como os dispositivos intrauterinos não hormonais, que não apresentam risco trombogênico (Fogoros; Ali, 2025).
Nos últimos anos, com o avanço das tecnologias laboratoriais e o acúmulo de dados epidemiológicos, estudos vêm propondo a implementação de estratégias de triagem mais acessíveis e eficazes para avaliação do risco trombótico. Entre elas, destaca-se a dosagem de marcadores biológicos, como a resistência à proteína C ativada, a avaliação do potencial de trombina endógena e, em casos específicos, testes genéticos para detecção de trombofilias (Lidegaard et al., 2011). Apesar de ainda não serem práticas amplamente disseminadas por questões econômicas e logísticas, tais estratégias apontam caminhos promissores para a personalização da escolha contraceptiva (Mørch et al., 2017).
Objetivo: Avaliar o risco de trombose venosa profunda associado ao uso de contraceptivos hormonais
Metodologia
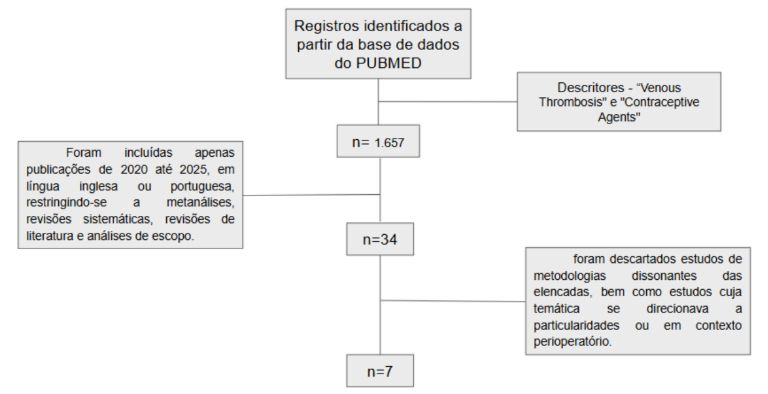
Foi realizada uma revisão de literatura na base de dados PUBMED para identificar publicações com o objetivo de avaliar e discutir a relação entre o uso de anticoncepcionais e o risco de ocorrência de trombose venosa profunda. Usaram-se os descritores “Venous Thrombosis” e “Contraceptive Agents”. Resultando em 1.657 artigos na busca. Foram incluídas apenas publicações de 2020 até 2025, em língua inglesa ou portuguesa, restringindo-se a metanálises, revisões sistemáticas, revisões de literatura e análises de escopo. Como critério de exclusão, foram descartados estudos de metodologias dissonantes das elencadas, bem como estudos cuja temática se direcionava a particularidades ou em contexto perioperatório. Foram incluídos 7 artigos na revisão.
Discussão
-Epidemiologia
A terapia hormonal combinada, especialmente com contraceptivos orais combinados (COCs), está associada a um aumento do risco de tromboembolismo venoso (TEV). Embora os estudos geralmente forneçam riscos relativos (RR), e não absolutos, o risco ainda é considerado baixo para a maioria das mulheres [Williams et al., 2024]. Em não usuárias, a taxa de TEV varia de 1,9 a 3,7 por 10.000 pessoas-ano. Usuárias de COCs têm um RR de 3,5, o que corresponde a um risco de até 0,15% ao ano. Esse risco é maior no primeiro ano de uso, mas persiste mesmo após cinco anos. Doses menores de estrogênio reduzem o risco; por outro lado, o desogestrel, por exemplo, apresenta um perfil de risco mais elevado [Williams et al., 2024]. O adesivo transdérmico tem um RR de 7,9 em comparação a não usuárias e de 2,5 em relação aos COCs com levonorgestrel, apresentando risco semelhante ao dos COCs de terceira geração. O anel vaginal tem um RR de 6,5 comparado a não usuárias e de 2,0 frente aos COCs com levonorgestrel [Williams et al., 2024]. Já os métodos compostos apenas por progestagênio apresentam risco bem menor de TEV, ou mesmo nenhum risco aumentado [Williams et al., 2024]. O DIU hormonal com levonorgestrel (LNG-IUS) não eleva o risco de TEV (RR 0,6) [Williams et al., 2024]. As pílulas somente de progestogênio (POPs) também não aumentam o risco (RR 0,9) [Williams et al., 2024]. A drospirenona, embora mais recente e potencialmente mais trombogênica, não apresentou casos de trombose em grandes estudos até o momento [Williams et al., 2024]. A medroxiprogesterona injetável (DMPA) pode aumentar o risco (RR 2,67), possivelmente devido às altas concentrações hormonais [Williams et al., 2024]. Quanto aos implantes (como o de etonogestrel), os dados são limitados: um estudo mostrou um RR de 1,4 com poucos eventos de TEV, enquanto outro não evidenciou aumento significativo no risco [Williams et al., 2024].
-Fatores de riscos
Alguns fatores, quando combinados com o uso de anticoncepcionais orais (OCs), aumentam significativamente o risco de trombose. A duração da exposição é relevante: o risco é mais alto nos três primeiros meses de uso, podendo ser até 12 vezes maior. Com o tempo, ele diminui, mas permanece acima do de não usuárias, normalizando apenas três meses após a interrupção [Barcellona et al., 2023]. A idade também influencia: mulheres acima de 35 anos têm risco significativamente maior que adolescentes, aumentando ainda mais entre 44 e 49 anos [Barcellona et al.,2023, Lavasseur et al., 2022]. Em mulheres com mais de 50 anos em terapia hormonal, o risco de tromboembolismo venoso (TEV) pode ser 6,3 vezes maior, chegando a 10,2 com progestagênios como o desogestrel [Lavasseur et al., 2022]. A obesidade é outro fator importante: mulheres com IMC acima de 30 em uso de contraceptivos combinados (COCs) podem ter risco até 24 vezes maior de TEV. De forma geral, obesas têm até 10 vezes mais risco de trombose que mulheres com IMC normal [Barcellona et al., 2023, Lavasseur et al., 2022]. O tabagismo também agrava o risco, aumentando não só a chance de trombose venosa, mas também de infarto do miocárdio, especialmente quando combinado ao uso de OCs [Barcellona et al., 2023, Lavasseur et al., 2022]. Trombofilias hereditárias são condições genéticas que afetam a coagulação do sangue, como as mutações no fator V Leiden ou na protrombina G20210A. Mulheres com essas alterações que usam COCs podem ter risco até 35 vezes maior que as não usuárias sem mutações. Trombofilias mais graves (como deficiência de antitrombina, proteína C e S) elevam ainda mais esse risco, sendo recomendadas, nesses casos, formulações com menor dose de estrogênio e progestagênios de menor risco [Barcellona et al., 2023, Lavasseur et al., 2022]. Um histórico de trombose venosa superficial (TVS) também está associado a risco aumentado de TEV, podendo chegar a 35 vezes mais em mulheres com TVS que usam COCs, fazem terapia hormonal ou engravidam [Barcellona et al., 2023, Lavasseur et al., 2022]. No contexto da COVID-19, embora a doença possa causar trombose, os dados ainda são conflitantes quanto ao impacto da terapia hormonal nesse risco. Assim, não há evidência suficiente para recomendar a interrupção dos OCs em casos leves ou moderados de COVID-19 [Barcellona et al.,2023, Lavasseur et al.,2022]. Por fim, a gravidez é um estado naturalmente pró-trombótico, com risco de trombose entre 1 e 2 por 1.000, o que representa um risco cerca de três vezes maior que o observado em usuárias de COCs. Isso reforça que, em algumas situações, a contracepção hormonal pode atuar como uma forma de prevenção da trombose associada à gestação [Barcellona et al.,2023, Lavasseur et al., 2022].
-Fisiopatologia
Os contraceptivos hormonais combinados (CHCs), que contêm estrogênio e progesterona, influenciam a coagulação do sangue por quatro principais mecanismos [Williams et al.2024]. Primeiramente, eles aumentam os níveis de fatores pró-coagulantes, como protrombina, fatores VII, VIII, X e fibrinogênio, que são essenciais para a formação de coágulos [Williams et al.,2024]. Em segundo lugar, reduzem os fatores anticoagulantes, como a proteína S e a antitrombina, que atuam na prevenção da coagulação excessiva [Williams et al., 2024]. Além disso, o uso de CHCs pode levar ao desenvolvimento de resistência adquirida à proteína C ativada (APC), um regulador natural da coagulação, favorecendo um estado de hipercoagulabilidade [Williams et al., 2024, Haguet et al., 2021]. Por fim, os CHCs também podem provocar alterações no sistema fibrinolítico, responsável pela dissolução de coágulos, embora a importância clínica dessas mudanças ainda não seja totalmente compreendida [Williams et al., 2024]. De modo geral, essas alterações se normalizam entre duas a quatro semanas após a interrupção do uso dos CHCs [Williams et al., 2024]. O tipo de progesterona utilizada também interfere no risco de trombose. Progestinas de terceira geração, como desogestrel, gestodeno e drospirenona, estão associadas a maior resistência à APC e a outros marcadores de hipercoagulabilidade, enquanto progestinas de segunda geração, como o levonorgestrel, apresentam impacto menor nesse aspecto [Williams et al., 2024, Haguet et al., 2021]. A combinação de estrogênio e progesterona influencia a “estrogenicidade” total do contraceptivo [Williams et al., 2024]. A via de administração do contraceptivo também exerce influência. Os CHCs orais passam pelo fígado inicialmente (metabolismo de primeira passagem), o que estimula a produção de proteínas de coagulação [Williams et al., 2024]. Já os métodos não orais, como adesivos transdérmicos e anéis vaginais, não passam pelo fígado nesse primeiro momento, mas ainda assim podem causar alterações na coagulação, provavelmente relacionadas ao tipo de progesterona utilizada [Williams et al., 2024]. Entre os métodos contraceptivos com menor impacto sobre a coagulação destacam-se o dispositivo intrauterino com levonorgestrel (DIU-LNG), as pílulas compostas apenas por progestina (POP), os implantes subdérmicos e a injeção de acetato de medroxiprogesterona (DMPA) [Williams et al., 2024].
-Quadro clínico
O quadro clínico da TVP pode ou não manifestar-se. Os sintomas mais comuns são: edema unilateral, dor localizada, sensação de peso no membro afetado, eritema e aumento da temperatura no local. A piora do quadro pode causar cianose, endurecimento do membro e dilatação das veias superficiais, o que indica debilitação do retorno venoso. A dor costuma piorar com o toque na musculatura e, caso a TVP esteja na perna, durante a dorsiflexão do pé (sinal de Homan) a panturrilha tende a doer.
Uma das maiores complicações da TVP é a embolia pulmonar (EP). Ela acontece em casos nos quais o coágulo, ou parte dele, se liberta da veia profunda e se desloca para a circulação do pulmão, obstruindo uma ou mais artérias. A EP pode causar pressão baixa, dor no tórax, dispnéia súbita, palpitações e parada cardiorrespiratória.
Outra intercorrência pertinente é a síndrome pós-trombótica (SPT), enfermidade consequente do aumento da pressão nas veias e lesão valvular venosa, geradas pela remissão parcial do coágulo (pode demorar meses para se manifestar). Essa condição tem como sintomas dores duradouras, edemas, sensação de peso nos membros e feridas nos vasos. Ademais, caso haja fatores pré-existentes, como o uso de anticoncepcional ou heranças biológicas, existem chances de que haja uma recorrência da TPV.
-Diagnóstico
Exame Físico
O quadro clínico, quando presente, pode consistir de: dor, edema, eritema, cianose, dilatação do sistema venoso superficial, aumento de temperatura, empastamento muscular e dor à palpação.
A avaliação dos principais fatores relacionados ao surgimento da TVP, associado ao quadro de dor e edema, podem ser agrupados em modelos de predição clínica. Nenhuma avaliação clínica isoladamente é suficiente para diagnosticar ou descartar a TVP pois os achados clínicos se relacionam com a doença em apenas 50% dos casos. A literatura existente recomenda a anamnese e o exame físico, combinados com a realização de testes laboratoriais e exames de imagem.
O sistema de predição clínica de TVP mais bem estudado é o escore de Wells. Escore de Wells
É um modelo de predição clínica, baseado em sinais e sintomas, fatores de risco e diagnósticos alternativos, estimando a probabilidade pré-teste para TVP demonstrada na tabela abaixo. Essa classificação tem se mostrado útil na abordagem inicial do paciente com suspeita de TVP [Marques et al., 2021]. Em sua primeira versão, categoriza os pacientes com probabilidade baixa, moderada ou alta de TVP, com uma prevalência de 5% (95% CI, 4%-8%), 17% (95%CI, 13%-23%) e 53% (95% CI, 44%-61%), respectivamente [Marques et al.]. Este escore deve ser usado em combinação com meios diagnósticos adicionais, como o eco Doppler colorido (EDC) associado à compressão de todo trajeto venoso troncular do membro inferior (pacientes com alto escore) e a mensuração do D-dímero (pacientes com baixo escore) [Marques et al., 2021]. A combinação EDC negativa seguida de DD negativo permite descartar com segurança a hipótese da TVP. Metanálise elaborada por Geersing GJ, define que, com escore de Wells ≤ 1 e DD negativo, a probabilidade de existência de TVP é menor que 2%, podendo excluí-la com segurança, em diferentes grupos de pacientes, com exceção de condições como o câncer e TVP recorrente [Marques et al., 2021]. Apresenta melhor resultado na avaliação de pacientes jovens sem comorbidades ou história prévia de tromboembolismo venoso (TEV), que em outros pacientes [Marques et al., 2021]. Para TVP recorrente é recomendado usar o escore de Wells modificado (que inclui pontuação extra para a história prévia de TVP) [Marques et al., 2021].
-Exame laboratorial
Teste D-dímero (DD)
O D-dímero é um dos produtos da degradação da fibrina, está presente em qualquer situação na qual haja formação e degradação de um trombo, não sendo, portanto, um marcador específico de TVP [Marques et al., 2021]. Apresenta alta sensibilidade, mas pouca especificidade para o diagnóstico da TVP [Marques et al., 2021]. Os testes de ELISA e ELFA (testes de enzyme-linked immunofluorescence), juntamente com testes imunoturbidimétricos ou de látex quantitativo, são considerados de alta sensibilidade; o DD de sangue total é considerado de moderada sensibilidade apesar de apresentar a mais alta especificidade [Marques et al., 2021]. Seus resultados geralmente são divididos em grupos: negativo (<350ng/mL),intermediário(351−500ng/mL),e positivo(>500 ng/mL) [Marques et al., 2021]. A dosagem do DD deve ser utilizada apenas em pacientes de baixa probabilidade clínica para TVP, uma vez que não apresentam 100% de sensibilidade. Há fortes evidências de que o uso de DD isolado, ou seja, sem a combinação de escores pré-teste, apresenta um valor preditivo negativo alto em população específica: pacientes ambulatoriais, não recorrentes, adultos (não-idosos) e com curta duração dos sintomas [Marques et al., 2021]. Em pacientes com alta probabilidade pré-teste para TVP ou EP, a utilidade do DD é questionável [Marques et al., 2021].
-Diagnóstico de Imagem
Eco Doppler colorido (EDC)
O EDC venoso é o método diagnóstico mais frequentemente utilizado para o diagnóstico de TVP em pacientes sintomáticos [Marques et al., 2021]. Apresenta menor acurácia em veias distais, em veias de membros superiores, e em pacientes assintomáticos [Marques et al., 2021]. É o exame de escolha para o diagnóstico de TVP, com sensibilidade de 96% e especificidade de 98-100%, em substituição à venografia [Marques et al., 2021]. Utiliza-se a ultrassonografia em tempo real para avaliar a ausência ou presença de compressibilidade das veias e a ecogenicidade intraluminal [Marques et al., 2021]. O EDC avalia a anatomia, a fisiologia e as características do fluxo venoso, combinando imagem em tempo real e a análise espectral [Marques et al., 2021]. A acurácia do EDC para diagnosticar TVP assintomática é menor em relação à TVP sintomática [Marques et al., 2021]. O paciente que tem alta probabilidade de acordo com o escore de Wells, EDC negativo e DD positivo, o EDC deverá ser repetido em três a sete dias [Marques et al., 2021]. Nos casos de TVP recorrente ipsilateral, os critérios utilizados para o diagnóstico pelo EDC são: aumento do diâmetro do mesmo segmento acometido ≥ 4 mm, aumento de 9 cm de extensão do trombo ou em segmento venoso distinto do acometido previamente [Marques et al., 2021].
Venografia / Flebografia
A Venografia com contraste é o exame considerado padrão-ouro para o diagnóstico de TVP, reservado, atualmente, apenas quando os outros testes são incapazes de definir o diagnóstico [Marques et al., 2021]. Porém, devido a várias limitações (custo, reações adversas ao contraste, ser desconfortável para o paciente, contraindicado a pacientes com insuficiência renal), não é o exame de rotina utilizado na suspeita de TVP [Marques et al., 2021]. Tem acurácia limitada nos quadros de TVP recorrente [Marques et al., 2021].
Tomografia Computadorizada (TC)
Como a sensibilidade e especificidade da angiotomografia são similares à do EDC, não há evidência suficiente para recomendá-la como modalidade diagnóstica inicial para TVP [Marques et al., 2021]. Metanálise realizada por Thomas, a sensibilidade encontrada para angiotomografia foi de 96% (95% IC, 93-98), e especificidade de 95% (95% IC, 94-97) para diagnóstico de TVP proximal em pacientes com suspeita de EP [Marques et al., 2021]. Pode ser útil para pacientes com suspeita de TVP, para os quais a EDC não pode ser aplicada devido a limitações técnicas e suspeita de anomalia venosa [Marques et al., 2021].
Ressonância Magnética (RM)
A RM pode ser utilizada para o diagnóstico de TVP em casos onde o EDC oferece resultados inconclusivos [Marques et al., 2021]. Apresenta acurácia similar ao EDC no diagnóstico da TVP do segmento ilíaco-caval [Marques et al., 2021]. RM com imagem direta do trombo, baseada nas propriedades paramagnéticas da metahemoglobina, pode ser o método de escolha para suspeita de recorrência aguda de TVP, distinguindo um evento novo de um antigo [Marques et al., 2021].
-Tratamento
Para que se possa definir o melhor tratamento para pacientes com antecedentes pessoais ou familiares de condições como: trombose venosa profunda (TVP), tromboembolismo venoso (TEV) e mutações do Fator V de Leiden, deve-se avaliar o caso de forma individualizada e em conjunto com a equipe multiprofissional. Considerando, além destas patologias citadas, o estilo de vida e características individuais de cada pessoa, como por exemplo: obesidade, tabagismo, idade e presença de doenças autoimunes. Isto é necessário, visto que a presença ou combinação destes fatores pode torná-lo mais ou menos provável de desenvolver complicações com a utilização de terapias hormonais. Sendo indispensável e essencial para garantir a segurança e eficácia da terapêutica, o acompanhamento contínuo da equipe profissional responsável [Barcellona et al.2023, Lavasseur et al., 2022].
Em pacientes com risco aumentado de trombose, portadores de riscos prévios citados anteriormente, a recomendação é evitar a prescrição de contraceptivos combinados, os quais contêm em sua composição estrogênio e progesterona, em especial os de administração oral, já que estes têm um efeito pró-coagulante no organismo, aumentando assim os riscos de causar efeitos colaterais [Williams et al.2024, Barcellona et al., 2023].
Nestes casos, existem alternativas mais seguras as quais podem ser recomendadas, destacando-se os métodos à base de progesterona isolada, como pílulas isoladas de progestagênio (POPs), implantes subdérmicos e dispositivos intrauterinos com levonorgestrel, os quais apresentam riscos ínfimos de causar trombose [Williams et al.,2024, Barcellona et al., 2023].
Além disso, há evidências científicas promissoras em relação ao uso de contraceptivos combinados de estrogênios naturais, como o valerato de estradiol, com progestagênios de baixo índice trombótico, como o dienogeste, embora tal conduta ainda requer cautela e avaliação minuciosa [Williams et al., 2024].
Em casos de pacientes que utilizam terapias hormonais além da contracepção, como por exemplo na reposição hormonal (TRH) ou afirmação de gênero, a via de administração se torna o fator determinante principal de risco trombótico. Adesivos ou géis de estradiol isolado apresentam menor impacto sobre o sistema de coagulação, quando comparados às formas orais, desta forma são mais indicados em pessoas com risco trombótico moderado a alto [Lavasseur et al.,2022, Barcellona et al.,2023].
Por fim, para pacientes as quais já apresentaram quadros prévios de trombose ou doenças relacionadas, a necessidade de prosseguimento com a terapia hormonal deve ser cuidadosamente avaliada pela equipe multiprofissional responsável pelo caso. Nestas situações, pode ser necessário interromper a terapia ou mantê-la associada à anticoagulantes, dependendo de uma série de fatores, entre eles: a gravidade do quadro, objetivo clínico da terapêutica e preferências pessoais da paciente. Deve ser feita uma avaliação integral do quadro pelo médico, e então apresentada a situação panorâmica à paciente, para que então a decisão seja tomada em conjunto, levando sempre em consideração as vontades individuais e o quadro clínico. Sendo a principal meta alcançar o equilíbrio entre a segurança e os benefícios do tratamento hormonal [Lavasseur et al.,2022, Barcellona et al,2023.].
Conclusão
A relação entre contraceptivos hormonais e a ocorrência de casos de trombose é bem estabelecida pela literatura e pesquisas científicas, especialmente quando esta contracepção está relacionada com o uso de estrogênios orais em combinação com progestagênios. No entanto, os avanços da ciência e tecnologia permitiram o desenvolvimento de formulações anticoncepcionais mais seguras, as quais levam em consideração métodos e compostos com menor impacto na coagulação sanguínea, como por exemplo as terapias baseadas em progestagênio isolado e os sistemas transdérmicos. Tal evolução farmacêutica tem sido fundamental para oferecer alternativas mais seguras, especialmente para mulheres e pessoas com risco trombótico elevado.
É de suma importância ressaltar que nem todos os métodos hormonais de contracepção apresentam o mesmo risco trombogênico, e que uma avaliação multiprofissional de cada caso de forma individualizada é imprescindível, devendo levar-se em conta fatores genéticos, clínicos e comportamentais de cada pessoa. A escolha do método de contracepção ou da terapia hormonal necessária deve se basear em três pilares fundamentais: segurança para a paciente, eficácia terapêutica e preferência pessoal, evitando uma abordagem generalista que exclua fatores particulares determinantes na decisão. A determinação de uma abordagem clínica deve ser discutida de forma integral e ampla com a paciente, visando sanar dúvidas e tranquilizar, fatores que são determinantes na adesão ao tratamento proposto pelos profissionais.
Logo, o uso seguro de hormônios em terapias hormonais e métodos contraceptivos depende intimamente da educação em saúde, aconselhamento adequado por parte da equipe profissional responsável, avaliação de risco rigorosa e ampla, e tomada de decisão compartilhada entre a paciente e a equipe médica. Com base nestas estratégias de abordagem, é possível reduzir significativamente os riscos atrelados à trombose e melhorar a qualidade de vida de quem necessita destas terapias.
-Referências
BARCELLONA, D. et al. Contraceptives and thrombosis: a revolutionary intertwined path. Thrombosis Research, v. 224, p. 1-8, 2023. Disponível em: https://pubmed.ncbi.nlm.nih.gov/36913971/. Acesso em: 19 jun. 2025.
BARCELLONA, D. et al. Hormones and thrombosis: the dark side of the moon. Thrombosis Research, v. 226, p. 112-117, 2023. Disponível em: https://pubmed.ncbi.nlm.nih.gov/37235737/. Acesso em: 19 jun. 2025.
HAGUET, H. et al. Combined oral contraceptives and venous thromboembolism: Review and perspective to mitigate the risk. International Journal of Molecular Sciences, v. 22, n. 24, p. 13248, 2021. Disponível em: https://pubmed.ncbi.nlm.nih.gov/34956081/. Acesso em: 19 jun. 2025.
LAVASSEUR, A. R. et al. Hormonal therapies and venous thrombosis: considerations for prevention and treatment. Journal of Thrombosis and Thrombolysis, v. 54, n. 3, p. 327-340, 2022. Disponível em: https://pubmed.ncbi.nlm.nih.gov/36032216/. Acesso em: 19 jun. 2025.
MARQUES, C. P. et al. Tromboembolismo venoso em mulheres: novos desafios para uma doença antiga. Revista da Associação Médica Brasileira, v. 67, n. 6, p. 917-922, 2021. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC8202191/. Acesso em: 19 jun. 2025.
WILLIAMS, E. et al. Estrogen, progesterone, and beyond: thrombotic risk and contraceptive choices. Journal of Blood Medicine, v. 15, p. 699-715, 2024. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC11665608/. Acesso em: 19 jun. 2025.
WILLIAMS, J. P. et al. Influence of hormonal contraceptives on peripheral vascular function and structure in premenopausal women: a review. American Journal of Physiology-Heart and Circulatory Physiology, v. 319, n. 6, p. H1443-H1454, 2020. Disponível em: https://pubmed.ncbi.nlm.nih.gov/33164574/. Acesso em: 19 jun. 2025.
