REGISTRO DOI: 10.69849/revistaft/cl10202510311918
Mariana Mion Muniz
Orientador: Prof. Me. Raphael Grillo da Silva
RESUMO
O hemangiossarcoma esplênico é uma neoplasia maligna de origem endotelial, comumente observada em cães de meia-idade a idosos, caracterizada por seu comportamento agressivo e alta taxa de metástase. O objetivo deste trabalho é relatar o caso de um cão diagnosticado com hemangiossarcoma esplênico, submetido à esplenectomia para remoção do baço, seguida de tratamento quimioterápico com doxorrubicina e ciclofosfamida. Apesar da abordagem cirúrgica e terapêutica adotada, durante o acompanhamento clínico foi observada metástase em lobo hepático, evidenciando o caráter metastático e prognóstico reservado dessa neoplasia, mesmo diante de tratamento instituído de forma adequada.
Palavras chaves: Baço. Canino. Exames clínicos. Metástase. Tumor.
ABSTRACT
Splenic hemangiosarcoma is a malignant neoplasm of endothelial origin, commonly observed in middle-aged to older dogs, characterized by its aggressive behavior and high metastasis rate. The aim of this study is to report the case of a dog diagnosed with splenic hemangiosarcoma, which underwent splenectomy to remove the spleen, followed by chemotherapy treatment with doxorubicin and cyclophosphamide. Despite the surgical and therapeutic approach adopted, during clinical follow-up metastasis was observed in a hepatic lobe, highlighting the metastatic nature and reserved prognosis of this neoplasm, even with appropriately instituted treatment.
Keywords: Spleen. Canine. Clinical examinations. Metastasis. Tumor
INTRODUÇÃO
O hemangiossarcoma (HSA) é uma neoplasia maligna agressiva de células mesenquimais. Se apresentam de tamanhos distintos, multicêntricos, com crescimento exacerbado com alta capacidade de infiltração, podendo ser visceral ou não visceral (Fossum, 2021). Pode-se iniciar em tecidos vascularizados, no entanto, as maiores incidências são: baço (50-60%), átrio direito (3-25%), tecido subcutâneo (13-17%) e fígado (Nardi, et al, 2023). O hemangiossarcoma é uma neoplasia com altos índices de mortalidade em cães, que se apresentam de coloração cinza-pálida e vermelho-escuro, em aspecto nodular, não aderido, com ou sem áreas cavitárias, ocasionando hemorragias, áreas de necrose e isquemia (Flores, et al 2012). Sua ocorrência é descrita em cães geriátricos com idade de 8 até 10 anos, machos de prevalência racial em: Pastor Belga, Boxer, Golden Retriever, sua casuística em felinos é de menor incidência, sendo uma tipologia tumoral exclusiva em caninos geriátricos (PAIVA et al, 2020).
O diagnóstico precoce, é indispensável para o sucesso do tratamento, visto que a intervenção cirúrgica é o principal método preconizado para a exérese do hemangiossarcoma, necessitando-se de correção completa e com margens cirúrgicas adequadas para minimizar o risco das recidivas (MARTINS, 2019). A quimioterapia é utilizada como terapia adjuvante, sendo recomendada através de protocolos específicos, com o propósito de prolongar a sobrevida dos pacientes acometidos especialmente diante das limitações impostas pela abordagem cirúrgica, especialmente ao que se refere à intervenções complexas e celiotomias viscerais, onde a margem e dose cirúrgica é comprometida, dessa forma, torna-se um componente adicional na terapêutica (Lopes, et al, 2020). O protocolo quimioterápico utilizado em sua grande maioria, envolve o uso da doxorrubicina,que é um agente antraciclínico com potencial de ação citotóxico, a doxorrubicina é administrada a cada 2 semanas, por um total de 4 a 6 ciclos, a depender da resposta e bem estar do animal (PAIVA, F.N.D. et al, 2020). Além da monoterapia à doxorrubicina, também se é empregados protocolos recombinantes em associação, como: a vincristina, e ciclofosfamida), que tem o intuito de potencializar os efeitos medicinais e retardar a resistência tumoral e metronômica. Outra forma salutar terapêutica, é a associação da ciclofosfamida com o piroxicam, onde se utiliza de doses menores, visando inibir a angiogênese tumoral e reduzir a progressão neoplásica (BENTO, 2022)
O objetivo deste trabalho, é relatar o caso de um cão de raça Pastor Belga, macho, com 10 anos, onde foi submetido a exérese tumoral, pelo diagnóstico de hemangiossarcoma esplênico, multimodal a tratamento quimioterápico metronômico com finalidade de longevidade.
REVISÃO DA LITERATURA
ETIOPATOGENIA
O desenvolvimento dos hemangiossarcomas em cães ainda é idiopática, entretanto, diversos fatores predispostos à sua ocorrência, foram identificados (Tamburini, 2009).Certas raças como: Pastor alemão, Golden retriever, Labrador retriever, Boxer, Beagle, Basset hound e Dálmata, apresentam maior disposição ao HSA, sugerindo um componente de causalidade genética, que são frequentemente acometidas por essa neoplasia (GOLDSCHMIDT, 2014). A subsistência de cães entre 8 e 10 anos, são em grande escala afetados pela tipologia tumoral (PEREIRA, M.A; LIMA, A. R; CARVALHO L. M. 2019). A pelagem é algo a se pontuar, visto que em cães com pelagem clara ou curta, como Pitbull, Whippet, Dálmata, Beagle e Boxer, estão mais suscetíveis ao HSA cutâneo devido à exposição prolongada à radiação solar, especialmente em regiões de pele despigmentada (Nardi, A. 2023). Outro fator influenciável propício à multiplicação celular descontrolada, é a ocorrência de traumas e processos inflamatórios em tecidos vasculares que podem favorecer o desenvolvimento de hemangiossarcoma (Freitas et al., 2019).
Embora não sejam comprovados de maneira conclusiva, fatores como exposição a substâncias químicas, fumaças e nicotinas, contribuem para o desenvolvimento deste neoplasma (PEREIRA, M.A; LIMA, A. R; CARVALHO L. M. 2019). De acordo com Lamerato Kozicki (2024), o HSA tem ancestralidade de células endoteliais precursoras da medula óssea, onde há um aumento exacerbado da expressão de proteínas definidoras da stem cell hemangioblasto, em que se atua como marcadores de células-tronco hematopoéticas e progenitoras (CD133), como a glicoproteína e células endoteliais imaturas (CD34), o receptor tirosina-quinase que regula crescimento, sobrevivência e diferenciação celular (c-kit) e um marcador típico de células de origem hematopoética (leucócitos). A expressão dele confirma que a célula tem linhagem hematológica (CD45), atualmente conhecida como Proteína Tirosina Fosfatase Receptora tipo C (PTPRC) que sinaliza processos da célula, como diferenciação, crescimento, transformação oncológica e mitose (Gene, 2019).
Sugeriram que, além da mutação em células teciduais residentes, a origem do hemangiossarcoma pode estar relacionado com células progenitoras circulantes adultas que foram recrutadas dos tecidos hematopoiéticos (baço e fígado).
SINAIS CLÍNICOS
Segundo Pasteur (Edição VII) os sinais clínicos são inespecíficos e geralmente estão relacionados a hemorragias internas intermitentes, decorrentes da ruptura de vasos tumorais. Entre os achados mais comuns destacam-se letargia, anorexia, fraqueza, palidez das mucosas, distensão abdominal, algia abdominal, síncope e colapso súbito. Em casos de hemoperitônio, o animal pode apresentar choque hipovolêmico agudo. A localização tumoral influencia a apresentação clínica: massas esplênicas e hepáticas causam principalmente hemorragia intra-abdominal (Figura 2), enquanto lesões cardíacas podem resultar em tamponamento cardíaco e arritmias. Devido à sua evolução silenciosa, muitos pacientes são diagnosticados apenas após episódios de colapso ou morte súbita (Lamerato-Kozicki et al., 2023; Cohen et al., 2022). O HSA se apresenta como nódulos superficiais (Figura 1) ou múltiplos de cor cinza-pálida e vermelho escuro, suas manifestações clínicas são localizadas e limitadas (Mullin et al, 2020).
Figura 01: Animal portador de hemangiossarcoma – em região inguinal esquerda medindo 7,0 cm x 7,0 cm x 4,0 cm durante atendimento inicial (A). Neoplasia dois meses depois, com alterações superficiais hemorrágicas, (seta) medindo 18,0 cm x 17,0 cm x 10,0 cm (B).
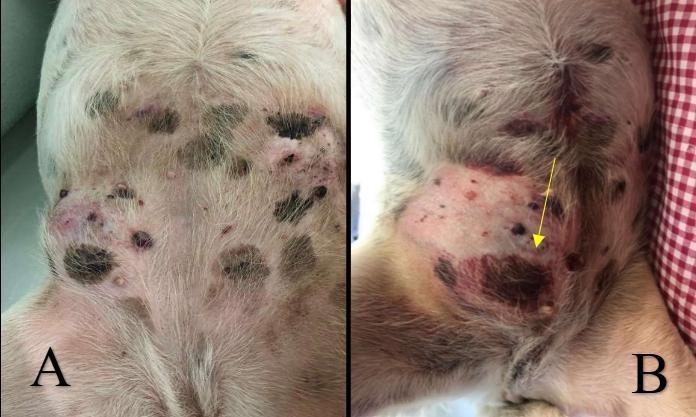
Fonte: (Paiva, et al, 2020).
Os sinais clínicos manifestam-se conforme a localização do tumor e a progressão da doença, sendo mais comuns nos estágios iniciais.
Figura 02: Esplenomegalia após diagnóstico de baço sendo exposto; B e C: nódulos ulcerados no baço; D e E: baço removido; G: síntese após 15 dias para remoção dos pontos.
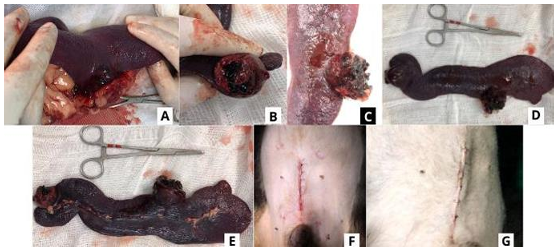
Fonte: Pasteur (Edição VII, revista ciência animal, 2020).
Nos casos de acometimento cardíaco, em específico no átrio direito, são vistos sinais de intolerância à exercícios, síncope, efusão pericárdica e tamponamento cardíaco. A presença de metástase pode agravar o quadro clínico, contribuindo para sinais respiratórios ou neurológicos, conforme o tipo de órgão acometido (Ettinger, 2017). Em tomografia computadorizada, é visualizado como sítio metastático, os lobos pulmonares, (entre 19 % e 52 %), muitas vezes acompanhados por comprometimento hepático (42,4 %), esplênico (33,3 %), muscular (30,3 %) e peritoneal/retroperitoneal (18,2 %) (Hemangio, 2024). Um estudo retrospectivo com 61 cães, revelou que 75,4 % apresentavam múltiplas metástases, sendo locais recorrentes: regiões esplênicas, hepáticas e pulmonares, outros órgãos com menor casuística, mas já descritos com aparecimento metastático, incluem os rins, ossos, linfonodos, e cavidade peritoneal, com sintomatologia de efusões cavitárias (Carloni A et al, 2019). Concluindo-se, foi feito um levantamento epidemiológico no Brasil, onde o estudo retrospectivo com 40 casos, mostrou que os órgãos mais acometidos pelo HSA, independentemente de se tratar de tumores primários, metastáticos ou multicêntricos, foram em ordem decrescente: baço, pulmão, fígado, peritônio, rim, encéfalo, pleura e coração (Flores, et al; 2012).
DIAGNÓSTICO
O diagnóstico do HSA esplênico é realizado por meio de exames de imagem, que auxiliam na investigação clínica e no estadiamento da doença. No entanto, a confirmação definitiva só é possível por meio da análise histopatológica do tumor (Smith, 2003; Batschinski, 2018; Mullin C, 2019; Griffin, 2021). A citologia aspirativa por agulha fina (CAAF) apresenta baixa eficácia na identificação do HSA. Um dos principais desafios desse método é a frequente contaminação por sangue, além do risco de hemorragia e da possível disseminação de células neoplásicas na cavidade abdominal (Smith, 2003; Mullin C, 2019-2020; Griffin, 2021; de Nardi, 2023). Devido a isto, o diagnóstico definitivo do HSA esplênico só pode ser feito por meio de histopatologia, após a remoção cirúrgica do baço (esplenectomia). Durante a cirurgia, recomenda-se o envio do órgão inteiro ao laboratório, pois a massa tumoral frequentemente apresenta áreas de necrose e hematomas, o que pode dificultar a amostragem adequada e gerar resultados falso-negativos (Smith, 2003; de Nardi, 2023).
TRATAMENTO
O tratamento do HSA em cães é desafiador devido à sua natureza agressiva e altos índices metastáticos, e interfere no controle da enfermidade tumoral, melhoramento da qualidade de vida e, quando possível, prorroga a sobrevida. As terapias multimodais envolvem a ressecção cirúrgica do tumor, respeitando a margem de segurança, de dois a três centímetros, por volta de todo o material a ser removido (CHAN et al, 2016). A fim de que contribua para maiores chances de cura (YAMAMOTO et al, 2013). Para ampliar o sucesso do tratamento, a cirurgia deve ser radical principalmente se a neoplasia estiver em regiões cutâneas e subcutâneas (PINTO, 2015). Em caso em que o HSA se encontra em órgão como o baço, recomenda-se esplenectomia total de preferência ou parcial, a depender do caso (FOSSUM, CAPLAN, 2014). No ato da cirurgia de esplenectomia deve-se realizar a exploração minuciosa por toda a região abdominal a fim detectar possíveis massas neoplásicas, como no fígado ou omento, deve ser feito a ressecção parcial dos mesmos.
Os protocolos de quimioterapia para HSA são essenciais para a continuidade do tratamento, podendo ser realizada com doxorrubicina isoladamente ou combinado com inibidores microtúbulos (vincristina) e agentes alquilantes (ciclofosfamida) (Freitas et al, 2019). Além disso, os inibidores seletivos da enzima cicloxigenase-2 (COX-2), conhecidos como coxibes, integram o protocolo terapêutico antineoplásico devido à sua capacidade de atuar na limitação da carcinogênese. Estes fármacos exercem seus efeitos por meio de diversos mecanismos, como a redução do apoptose celular, a inibição da atividade das metaloproteinases, enzimas associadas ao aumento da mitose e à disseminação de células tumorais, além da intensificação do metabolismo de xenobióticos. Complementarmente, o tratamento pode incluir o uso de imunomoduladores e a aplicação da eletroquimioterapia como abordagens terapêuticas adjuvantes (Freitas et al, 2019).
PROGNÓSTICO
O prognóstico do hemangiossarcoma é geralmente reservado a ruim, uma vez que se trata de uma neoplasia maligna altamente agressiva, caracterizada por crescimento rápido, alto potencial metastático e dificuldade de diagnóstico precoce. Mesmo com intervenção cirúrgica e quimioterapia adjuvante, a sobrevida média dos animais acometidos, especialmente cães, é limitada, variando entre 3 a 6 meses após o diagnóstico, porém, vários fatores como grau e tipo histológico, tamanho do tumor, localização, invasão e padrão das margens cirúrgicas, localização primária e idade do paciente contribuem para obtenção deste prognóstico (Stephen J, et al, 2013).
RELATO DE CASO
O presente trabalho apresenta o relato clínico de um cão da raça Pastor Belga, macho, castrado, 10 anos de idade e pesando 47 kg, atendido em um Hospital Veterinário localizado na região de Guarulhos. Em dezembro de 2024, o tutor levou o animal à clínica relatando um episódio de síncope. Segundo o relato, momentos antes da ocorrência, o cão demonstrava sinais clínicos como ataxia e apatia. No exame físico realizado na ocasião, observou-se abdômen distendido, com suspeita de presença de líquido livre, além de mucosas hipocoradas. Foram, então, solicitados exames complementares para triagem diagnóstica, incluindo hemograma completo, dosagens séricas de uréia (URE), creatinina (CRE), Alanina aminotransferase (ALT), Fosfatase alcalina (FA) e albumina (ALB), além de exame ultrassonográfico abdominal. Os resultados laboratoriais indicaram hematócrito de 30% e demais exames dentro da normalidade para a espécie. O exame ultrassonográfico revelou uma massa esplênica medindo entre 8 a 10 cm, altamente vascularizada, associada à presença de grande quantidade de líquido livre na cavidade abdominal.
Diante do quadro, realizou-se abdominocentese para coleta do líquido peritoneal, que foi encaminhado para análise laboratorial. O resultado demonstrou hematócrito de 33% no líquido abdominal, confirmando o diagnóstico de hemoperitônio. Após a confirmação diagnóstica por meio dos exames laboratoriais e de imagem, o animal foi internado no Hospital Veterinário para estabilização clínica e preparo cirúrgico. Realizou-se a canulação venosa para administração de fluidos e início do protocolo medicamentoso. A analgesia foi instituída com dipirona na dose de 25 mg/kg, por via intravenosa, e foi solicitada uma bolsa de concentrado de hemácias para realização de transfusão sanguínea. Diante do quadro clínico, indicou-se a realização de esplenectomia, cuja cirurgia foi devidamente programada. Durante o preparo cirúrgico, o paciente foi posicionado em decúbito dorsal para acesso por abordagem ventral. Em seguida, procedemos à incisão mediana ventral, estendendo-se do processo xifóide até a região púbica. Realizada a incisão da pele e do tecido subcutâneo até a identificação da linha alba, a qual foi aberta cuidadosamente com bisturi e tesoura, permitindo o acesso à cavidade abdominal. Para garantir adequada exposição e visualização do campo operatório, foi utilizado afastadores de Balfour, mantendo compressas estéreis embebidas em solução fisiológica morna sobre o baço, a fim de protegê-lo. Na exploração da cavidade abdominal, verificamos a presença de hemorragia livre inicial e a presença de uma massa esplênica, previamente identificada no exame ultrassonográfico, medindo entre 8 e 10 cm, com áreas ulceradas (Figura 3). Avaliamos também fígado, linfonodos e demais estruturas adjacentes, visto que muitas enfermidades esplênicas podem estar associadas a alterações em outros órgãos. Prosseguimos com a ligadura dos vasos esplênicos.
Figura 3: Retirada do baço após identificação de massa aderida, foi coletada e enviada para realização de histopatológico.
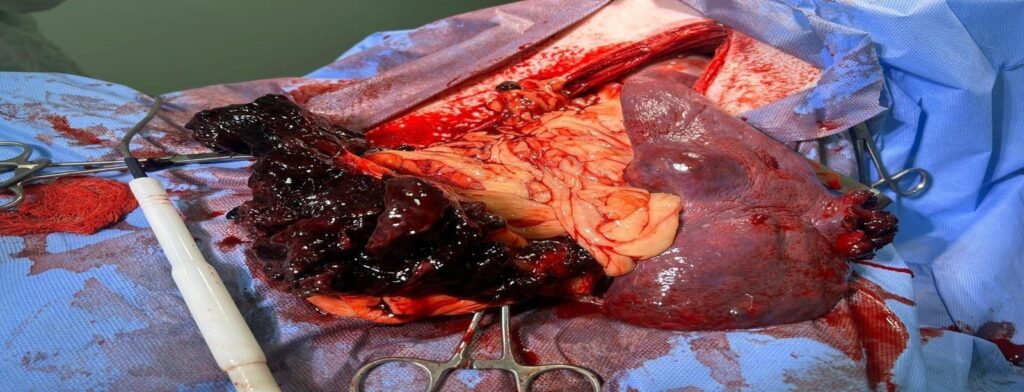
Fonte: Pessoal, 2024.
O baço, irrigado pela artéria esplênica (ramo da artéria celíaca) e drenado pela veia esplênica (tributária da veia porta), teve seu pedículo identificado próximo ao hilo. Realizamos a ligadura dos vasos em pares, sempre respeitando a sequência, primeiramente a artéria e posteriormente a veia, com cautela para não comprometer a irrigação do pâncreas, considerando a presença de ramos curtos que o irrigam a partir da artéria esplênica. Utilizei fios absorvíveis sintéticos de longa duração (PDS 2-0) para a execução das ligaduras, empregando a técnica de tripla ligadura dos vasos de maior calibre. Dessa forma, fomos ligando e seccionando progressivamente os vasos até que o baço estivesse completamente liberado.
Após o controle total do pedículo vascular, foi removido o baço da cavidade abdominal. Durante o procedimento, observei a ocorrência de sangramento na região, razão pela qual realizei revisão minuciosa da hemostasia e, em seguida, lavagem abdominal com solução fisiológica morna. Após confirmar a ausência de hemorragias ativas, iniciei o fechamento da cavidade por planos: sutura da linha alba com fio absorvível sintético (PDS 2-0), em padrão simples contínuo; tecido subcutâneo com fio absorvível (Monocryl 2-0/3-0), em padrão simples contínuo; e pele com nylon monofilamentar 2-0, em padrão simples interrompido, do tipo Donatti.
Decorrida a cirurgia, o animal manteve-se internado e a transfusão foi realizada no transoperatório para o pós-operatório, iniciamos com a diluição do concentrado de hemácias, que deve ser diluído com NaCl a 0,9% aquecido antes do uso (10ml de NaCL a 0,9% para 30 a 40ml de concentrado de hemácias) e na seguinte velocidade: primeiros 15 minutos = 0,25 à 0,5 ml/kg/h, sempre monitorando a reação, se tolerado, aumentar para 5 à 10 ml/kg/h, o volume total sempre deve ser infundido em no máximo 4 horas, devido ao risco de proliferação bacteriana. Depois da transfusão foi autorizado uma recoleta para controle de hemograma, na qual, o hematócrito aumentou para 35% após transfundir, o animal ficou estável na internação, se alimentando espontaneamente, com polidipsia, estava com anúria, devido a isso, foi passado uma sonda uretral para esvaziamento da bexiga e glicemia se manteve em 135 mg/dl. Procedendo a cirurgia e a internação de 24 horas, como o animal ficou estável, foi realizada a alta dele para casa com o seguinte protocolo: agemoxi 20 mg/kg bid durante 7 dias, prednisona 1 mg/kg sid durante 5 dias, tramadol 4mg/kg bid 4 dias e dipirona 25mg/kg bid durante 4 dias.
Logo após, recebemos o resultado da amostra enviada ao laboratório, que confirmou o diagnóstico de hemangiossarcoma esplênico. Foi recomendado o acompanhamento com um oncologista para avaliar as melhores opções de tratamento. O especialista indicou a quimioterapia com doxorrubicina, sendo realizadas duas sessões até o momento, o paciente apresentou bom estado geral durante cerca de dois meses (Janeiro e Fevereiro de 2025). No entanto, em Março do mesmo ano, o tutor retornou relatando que o animal voltou a apresentar prostração. O paciente foi novamente internado para controle medicamentoso, monitoramento clínico e realização de exames de controle. Os exames evidenciaram metástases nos lobos hepáticos, de forma difusa e a presença de líquido livre na cavidade abdominal. Já apresentava prognóstico reservado, com apatia e dispneia. Foi realizada nova drenagem abdominal para remoção do líquido. Contudo, durante a madrugada, houve descompensação clínica e o paciente evoluiu para óbito.
DISCUSSÃO
No presente relato, a raça, sexo e idade do paciente são condizentes com as características descritas na literatura dos animais mais susceptíveis a desenvolver hemangiossarcoma esplênico, sendo mais frequentemente observados em cães de raças de grande porte e de meia-idade a idosos. O comprometimento esplênico observado neste caso está de acordo com estudos prévios que destacam a agressividade e a alta propensão a metástases dessa neoplasia, principalmente para órgãos como fígado e pulmões (NELSON, COUTO, 2015; FREITAS et al., 2019).
De acordo com alguns autores, os sinais clínicos apresentados por cães com hemangiossarcoma esplênico são compatíveis com os observados no paciente relatado, como: aumento abdominal, apatia, hiporexia, perda de peso, síncope, êmese, etc. Os exames laboratoriais, como ureia, creatinina, ALT, fosfatase alcalina e albumina, mostraram alterações condizentes com comprometimento hepático e impacto sistêmico do tumor, corroborando os achados descritos por (Silva et al, 2018).
Como diagnóstico, além do exame físico e dos exames laboratoriais, a ultrassonografia abdominal desempenha um papel fundamental, na qual, neste relato, evidenciou massa esplênica heterogênea, confirmando a importância da somatória de exames de imagem para caracterizar o tumor e identificar possíveis metástases, como demonstrado por (Souza et al, 2017).
O paciente foi submetido à esplenectomia, considerada o tratamento de escolha para hemangiossarcoma esplênico, associada à quimioterapia adjuvante com doxorrubicina e ciclofosfamida, seguindo protocolos descritos na literatura para reduzir a probabilidade de metástase. Apesar da intervenção cirúrgica e do tratamento quimioterápico, durante o acompanhamento clínico foi observada metástase no lobo hepático, evidenciando o caráter altamente metastático dessa neoplasia, conforme relatado por outros autores, na qual, o animal veio a óbito (FOSSUM TW, 2014).
Esse relato reforça que, mesmo com manejo cirúrgico adequado e quimioterapia, o hemangiossarcoma esplênico apresenta prognóstico reservado, destacando a necessidade de acompanhamento clínico rigoroso e abordagem terapêutica precoce (Nascimento, 2020).
CONCLUSÃO
Os hemangiossarcomas representam neoplasias malignas em cães e exigem uma abordagem clínica cuidadosa para seu diagnóstico e manejo. A conduta terapêutica é guiada por uma avaliação clínica completa, que inclui exame físico minucioso, além de exames laboratoriais e de imagem. O diagnóstico precoce, aliado a uma intervenção cirúrgica eficaz e livre de complicações, é essencial para o sucesso do tratamento e melhora do prognóstico do paciente. A confirmação do hemangiossarcoma esplênico por meio de exame histopatológico possibilitou a indicação de quimioterapia adjuvante, que demonstrou eficácia no controle da doença. Essa abordagem terapêutica integrada foi fundamental para um desfecho clínico favorável, contribuindo para a recuperação e manutenção da qualidade de vida do paciente.
REFERÊNCIAS
BATSCHINSKI, K.; NOBRE, A.; VARGAS-MENDEZ, E.; TEDARDI, M. V.; CIRILLO, J.; CASTARI, G.; UBUKATA, R.; DAGLI, M. L. Z. Canine visceral hemangiosarcoma treated with surgery alone or surgery and doxorubicin: 37 cases (2005–2014). Canadian Veterinary Journal, v. 59, p. 967–972, 2018.
BENTO, J. R. N. Hemangiossarcoma em cães e gatos: estudo retrospectivo de 38 casos clínicos [Dissertação]. Lisboa: Faculdade de Medicina Veterinária, Universidade de Lisboa, 2022.
CARLONI, A.; TERRAGNI, R.; MORSELLI-LABATE, A. M.; PANINAROVA, M.; GRAHAM, J.; VALENTI, P.; ALBERTI, M.; ALBARELLO, G.; MILLANTA, F.; VIGNOLI, M. Prevalence, distribution, and clinical characteristics of hemangiosarcoma-associated skeletal muscle metastases in 61 dogs: a whole body computed tomographic study. Journal of Veterinary Internal Medicine, v. 33, n. 2, p. 812–819, mar. 2019. DOI: 10.1111/jvim.15456.
CHAN, C. M.; CASTIER, M. B.; SALGADO, C. G. Papel do ecocardiograma na avaliação de cardiotoxicidade no tratamento do câncer de mama. Revista Brasileira de Cardiologia, v. 24, n. 6, p. 382–386, nov./dez. 2011.
DALECK, C. R.; DE NARDI, A. B. Oncologia em cães e gatos. São Paulo: Grupo GEN – Editora Roca, 2016.
DE NARDI, A. B.; JARK, P. C. Oncologia. In: CRIVELLENTI, L. Z.; BORIN CRIVELLENTI, S. Casos de rotina em medicina veterinária de pequenos animais. 3. ed. São Paulo: MedVet, 2023. p. 1016–1018.
ETTINGER, S. J.; FELDMAN, E. C.; CÔTÉ, E. Tratado de Medicina Interna Veterinária: doenças do cão e do gato. 8. ed. Rio de Janeiro: Elsevier, 2017.
FILHO CANINO. Tratamento e prognóstico do hemangiossarcoma em cães. Filho Canino, 2025. Disponível em: https://filhocanino.com.br/tratamento-eprognostico-do-hemangiossarcoma-em-caes. Acesso em: 1 set. 2025.
FOSSUM TW. Cirurgia do baço. In: FOSSUM TW. Cirurgia de pequenos animais. 4. ed. Rio de Janeiro: Elsevier, 2014; cap. 24, p. 1963-1979.12.FREITAS, YI e FORLANI, 2019. Hemangiossarcoma canino: uma revisão. Pubvet, 2019. Acesso em: 28 out. 2025.
FLORES, M. M.; PANZIERA, W.; KOMMERS, G. D.; IRIGOYEN, L. F.; BARROS, C. S. L.; FIGHERA, R. A. Aspectos epidemiológicos e anatomopatológicos do hemangiossarcoma em cães: 40 casos (1965–2012). Pesquisa Veterinária Brasileira, v. 32, n. 12, p. 1319–1328, 2012. Disponível em: http://www.scielo.br/pdf/pvb/v32n12/v32n12a17.pdf. Acesso em: 15 ago. 2025.
FOSSUM, T. W.; CAPLAN, E. R. Cirurgia do sistema hemolítico. In: FOSSUM, T. W. Cirurgia de pequenos animais. 4. ed. Rio de Janeiro: Elsevier, 2014. p. 685–700.
GOLDSCHMIDT, M. H.; HENDRICK, M. J. Hemangiomas e hemangiossarcomas em cães: estudo retrospectivo de 192 casos (2002–2014). Ciência Animal Brasileira, 2016. Disponível em: https://www.scielo.br/j/cab/a/hcqtgbm5LrTyFTyHb7CtRRj/. Acesso em: 19 out. 2025.
LAMERATO-KOZICKI, A. R.; HELM, K. M.; JUBALA, C. M.; CUTTER, G. C.; MODIANO, J. F. Canine hemangiosarcoma originates from hematopoietic precursors with potential for endothelial differentiation. Experimental Hematology, v. 34, p. 870–878, jul. 2006. Disponível em: https://www.ncbi.nlm.nih.gov/pubmed/16797414. Acesso em: 1 jul. 2025.
LOPES, A. R.; CARVALHO, L. M.; LIMA, A. R. Hemangiossarcoma de terceira pálpebra: caracterização clínica, diagnóstico e abordagens terapêuticas. Filho Canino, 2025. Disponível em: https://filhocanino.com.br/tratamento-eprognostico-do-hemangiossarcoma-em-caes. Acesso em: 1 set. 2025.
MARTINS, K. P. Hemangiossarcoma canino. 2019. 12 f. TCC (Graduação) – União das Faculdades dos Grandes Lagos, São José do Rio Preto, 2019.
MORRISON, W. B. Cancer in dogs and cats: medical and surgical management. Teton NewMedia: Estados Unidos, 2002.
MULLIN, C.; CLIFFORD, C. A. Miscellaneous tumours: hemangiosarcoma. In: WITHROW, S. J.; VAIL, D. M.; PAGE, R. L. (eds.). Withrow and MacEwen’s Small Animal Clinical Oncology. 5. ed. St. Louis, MO: Elsevier Saunders, 2020. p. 773–778.
NARDI, A. Pesquisadores da Unesp participam de primeiro consenso mundial sobre hemangiossarcoma em cães. Jornal da Unesp, 2023. Disponível em: https://jornal.unesp.br/2023/05/03/pesquisadores-da-unesp-participam-deprimeiro-consenso-mundial-sobre-hemangiossarcoma-em-caes. Acesso em: 20 out. 2025.
NELSON RW, COUTO CG. Medicina interna de pequenos animais.5. ed. Rio de Janeiro: Elsevier, 2015. Acesso em: 20 out. 2025.
PAIVA, F. N. D. et al. Terapia multimodal no tratamento de hemangiossarcoma cutâneo canino. Ciência Animal, Seropédica, v. 30, n. 3, p. 155–162, out. 2020.
PEREIRA, M. A.; LIMA, A. R.; CARVALHO, L. M. Hemangiossarcoma canino: revisão. ResearchGate, 2019. Disponível em: https://www.researchgate.net/publication/336223471_Hemangiossarcoma_cani no_revisao. Acesso em: 10 mar. 2025.
WITHROW, S. J.; VAIL, D. M.; PAGE, R. L. Withrow and MacEwen’s Small Animal Clinical Oncology. 5. ed. St. Louis: Elsevier Saunders, 2013.
YAMOTO, S.; HOSHI, K.; HIRAKAWA, A.; CHIMURA, S.; KOBAYASHI, M.; MACHIDA, N. Epidemiological, clinical and pathological features of primary cardiac hemangiosarcoma in dogs: a review of 51 cases. Journal of Veterinary Medical Science, v. 75, n. 11, p. 1433–1441, 2013.
ZEMAN, A. M.; JOHNSON, K. H.; REESE, M. J. Hemangiosarcoma in dogs: clinical features, diagnosis, and treatment strategies. Veterinary Clinics of North America: Small Animal Practice, v. 53, n. 1, p. 101–118, 2023. DOI: https://doi.org/10.1016/j.cvsm.2022.09.003
