ANALYSIS OF THE EFFECTS OF OPEN AND CLOSED KINETIC CHAIN EXERCISES ON ACL INJURY REHABILITATION – A LITERATURE REVIEW
REGISTRO DOI: 10.69849/revistaft/ch10202510120626
Cristhian de Farias Silva*
João Augusto Barbosa da Silva*
Gustavo Henrique Marques Moreno**
RESUMO
A lesão do Ligamento Cruzado Anterior (LCA) é comum em esportes que exigem mudanças rápidas de direção, saltos e impactos, sendo mais prevalente em atletas do sexo masculino. A LCA é responsável por cerca de 85% da contenção do deslizamento anterior da tíbia em relação ao fêmur, além de estabilizar a rotação do joelho. Seu rompimento ocorre, geralmente, por mecanismos de valgo excessivo, rotação do joelho com o pé fixo ou trauma direto na lateral do joelho. O tratamento pode ser cirúrgico, utilizando enxertos do tendão patelar ou dos flexores, ou conservador, indicado em lesões parciais. A reabilitação pós-cirúrgica visa reduzir inflamações, preservar a amplitude de movimento (ADM), manter equilíbrio, propriocepção e prevenir hipotrofia muscular. Este estudo, uma revisão bibliográfica baseada no método PICO, busca comparar os efeitos dos exercícios em cadeia cinética aberta (CCA) e cadeia cinética fechada (CCF) na reabilitação de atletas com LCA. Os resultados preliminares apontam que a CCF oferece menor estresse articular e maior ativação muscular, favorecendo propriocepção, equilíbrio e retorno seguro às atividades. Já a CCA, embora ofereça risco de sobrecarga se utilizada precocemente, mostra-se eficiente nas fases intermediárias e finais para fortalecimento específico, ADM e controle motor. O estudo defende a integração progressiva das duas abordagens, respeitando as fases da cicatrização e as demandas esportivas, proporcionando uma reabilitação eficiente, funcional e segura, além de enfatizar a importância da individualização dos protocolos conforme o perfil do atleta.
Palavras-chave: Cadeia Aberta. Cadeia Cinética Fechada. Lesão do Ligamento Cruzado Anterior. Reabilitação Fisioterapêutica.
ABSTRACT
Anterior Cruciate Ligament (ACL) injury is common in sports that require quick changes of direction, jumps, and impacts, being more prevalent in male athletes. The ACL is responsible for approximately 85% of the restraint of anterior tibial translation relative to the femur, as well as stabilizing knee rotation. Its rupture generally occurs due to excessive valgus mechanisms, knee rotation with the foot fixed, or direct trauma to the lateral side of the knee. Treatment can be surgical, using grafts from the patellar tendon or hamstrings, or conservative, indicated in partial injuries. Post-surgical rehabilitation aims to reduce inflammation, preserve range of motion (ROM), maintain balance, proprioception, and prevent muscle hypotrophy. This study, a bibliographic review based on the PICO method, aims to compare the effects of open kinetic chain (OKC) and closed kinetic chain (CKC) exercises in the rehabilitation of athletes with ACL injuries. Preliminary results indicate that CKC exercises provide less joint stress and greater muscle activation, promoting proprioception, balance, and a safer return to activities. OKC exercises, although posing a risk of overload if used too early, are effective in the intermediate and final phases for specific strengthening, ROM gains, and motor control. The study advocates the progressive integration of both approaches, respecting tissue healing phases and sports demands, providing efficient, functional, and safe rehabilitation. It also emphasizes the importance of individualizing protocols according to the athlete’s profile.
Keywords: Closed Kinetic Chain. Anterior Cruciate Ligament Injury. Physiotherapy Rehabilitation.
1. INTRODUÇÃO
A lesão do Ligamento Cruzado Anterior (LCA) acomete a articulação do joelho e está frequentemente associada a atividades que envolvem impactos diretos de alta intensidade ou mudanças bruscas de direção. O mecanismo de lesão geralmente decorre de trauma direto na face lateral do joelho, resultando em um estresse em valgo excessivo, inclinação ipsilateral do tronco ou impacto na região posterior da tíbia, ocasionando seu deslizamento anterior exagerado, além de rotação do joelho com o pé fixo ao solo (Munhoz et al., 2022).
De acordo com Brandão et al. (2022), o LCA é capaz de suportar forças de até 2500 N, sendo responsável por aproximadamente 85% da contenção contra o deslocamento anterior da tíbia em relação ao fêmur. Ademais, exerce papel estabilizador durante os movimentos de rotação interna e externa do joelho. Nesse contexto, diversos autores têm investigado quais exercícios estariam mais associados à geração desses movimentos rotacionais, capazes de desencadear o deslocamento anterior da tíbia.
A lesão do Ligamento Cruzado Anterior (LCA) é particularmente frequente em esportes de alto rendimento. Um estudo quantitativo estimou a ocorrência de aproximadamente 250.000 casos anuais, sendo que o mecanismo de contato corresponde a cerca de 70% dessas lesões, com maior prevalência em atletas do sexo masculino. Evidências apontam que cerca de 50% dos atletas acometidos apresentam déficits musculares nos grupos anterior e posterior da coxa, condição que aumenta a sobrecarga sobre o LCA e eleva o risco de lesão.
Do ponto de vista epidemiológico, a lesão do LCA configura-se como um problema de saúde pública, tanto por sua elevada incidência quanto pelos custos associados ao tratamento e à reabilitação. Nos Estados Unidos, a estimativa ultrapassa 250.000 casos por ano, sobretudo em modalidades que envolvem movimentos de alta intensidade, como futebol, basquete, vôlei e esqui. No Brasil, embora não haja registros oficiais sistematizados, estudos regionais indicam prevalência semelhante, reforçando a relevância clínica e social dessa condição (Wakefield et al., 2021).
Atletas do sexo feminino apresentam risco de duas a oito vezes maior de sofrer lesões do LCA em comparação aos homens, devido a fatores anatômicos, hormonais e neuromusculares. Esses fatores incluem maior ângulo Q, variações hormonais que afetam a laxidade ligamentar e predominância de ativação do quadríceps em relação aos isquiotibiais (Griffin et al., 2023; Hewett et al., 2021).
Além da elevada prevalência, ressalta-se o impacto funcional dessa lesão, em que atletas acometidos, frequentemente necessitam de afastamento prolongado de suas atividades, variando entre seis e doze meses, a depender da gravidade da lesão e da estratégia terapêutica adotada. Esse afastamento pode comprometer carreiras esportivas, reduzir o desempenho físico e gerar custos significativos tanto para o indivíduo quanto para instituições de saúde públicas e privadas (Griffin et al., 2023).
O tratamento das lesões do Ligamento Cruzado Anterior (LCA) pode ser realizado por meio de intervenção cirúrgica, geralmente envolvendo a substituição do ligamento lesionado. O método mais amplamente utilizado é a reconstrução com enxerto autólogo, obtido a partir de segmentos do tendão patelar ou dos tendões flexores do joelho (Lara et al., 2024).
Uma alternativa, ainda em estudo e aplicada em alguns países, consiste na utilização de enxertos alógenos provenientes de cadáveres; entretanto, essa abordagem apresenta menor adesão clínica devido à qualidade considerada inferior em relação aos enxertos autólogos. Já os enxertos sintéticos foram avaliados em diferentes contextos, mas os resultados obtidos não corresponderam às expectativas regenerativas (Lara et al., 2024).
A reabilitação do atleta submetido à reconstrução do LCA tem início no período pós-operatório imediato, com foco em assegurar a proteção da articulação, o controle do processo inflamatório, a mobilização passiva e a progressiva descarga de peso. Superada essa fase inicial, o fisioterapeuta responsável deve concentrar-se na prevenção da redução da Amplitude de Movimento (ADM), da perda de equilíbrio estático e dinâmico, bem como dos déficits proprioceptivos. Além disso, atenção especial deve ser dada às alterações neuromusculares, como hipotonia e hipotrofia, frequentemente decorrentes da inibição artrogênica induzida pelo trauma cirúrgico (Silva et al., 2020).
A fisioterapia conservadora constitui uma alternativa de tratamento indicada principalmente em casos de lesão parcial do LCA, quando a equipe multidisciplinar opta por não realizar intervenção cirúrgica. O protocolo conservador tem como objetivos a redução do edema, o controle da dor, a proteção das estruturas comprometidas, a recuperação completa da Amplitude de Movimento (ADM), o restabelecimento da função proprioceptiva, a retomada das atividades de vida diária (AVDs) e o fortalecimento dos principais grupos musculares responsáveis pela estabilização do joelho (Trindade et al., 2020).
Entre eles, destacam-se o quadríceps formado pelo reto femoral, vasto lateral, vasto medial e vasto intermédio e os isquiotibiais compostos pelo semitendíneo, semimembranoso e bíceps femoral. O processo de reabilitação visa, por fim, o retorno seguro às práticas esportivas (Trindade et al., 2020).
Após a reconstrução do LCA, a reabilitação deve ser direcionada para assegurar a recuperação funcional do atleta e possibilitar o retorno seguro ao nível esportivo previamente alcançado. Nesse cenário, diversos estudos têm comparado os efeitos dos exercícios realizados em cadeia cinética aberta (CCA) e em cadeia cinética fechada (CCF). A CCA caracteriza-se por exercícios com maior amplitude de movimento, voltados para o fortalecimento de grupos musculares específicos; contudo, por serem mais seletivos, esses exercícios podem impor maior estresse articular ao joelho (Barreto; Silva; Cunha et al., 2023).
Em contrapartida, a CCF envolve extremidades distais fixas em uma superfície, permitindo a execução de movimentos integrados por múltiplas articulações. Esse tipo de exercício promove o recrutamento de um maior número de grupos musculares e tende a reduzir o estresse articular, favorecendo, assim, uma reabilitação mais segura e eficiente para o atleta (Barreto; Silva; Cunha et al., 2023).
A literatura destaca a importância de respeitar as diferentes fases de recuperação do atleta após a lesão do LCA. Na fase aguda, o foco deve estar na redução da dor, no controle do processo inflamatório e na proteção da articulação, utilizando recursos como crioterapia, eletroterapia, laserterapia, ultrassom e técnicas manuais, além do início precoce da mobilização passiva. Na fase subaguda, a prioridade passa a ser a introdução de exercícios concêntricos, associados à progressão de exercícios de mobilidade (De Souza et al., 2022).
Por fim, na fase crônica, o objetivo principal é a realização de exercícios pliométricos, atividades que simulem os gestos esportivos específicos da modalidade praticada pelo atleta, bem como exercícios proprioceptivos, fundamentais para a recuperação funcional e o retorno seguro ao esporte (De Souza et al., 2022).
No contexto da reabilitação, os exercícios em cadeia cinética aberta (CCA) e cadeia cinética fechada (CCF) têm sido amplamente investigados. A CCA é caracterizada por movimentos em que a extremidade distal está livre, permitindo maior isolamento muscular e amplitudes articulares mais amplas. No entanto, esse tipo de exercício pode gerar maior estresse sobre a articulação, especialmente nos ângulos próximos à extensão total, o que levanta preocupações sobre a segurança em fases iniciais da reabilitação.
Por outro lado, os exercícios em cadeia cinética fechada (CCF) caracterizam-se pela fixação da extremidade distal em uma superfície estável, o que promove maior coativação dos grupos musculares e recrutamento simultâneo de múltiplas articulações. Essa modalidade de exercício tende a gerar menor estresse sobre o LCA reconstruído, além de proporcionar estímulos proprioceptivos mais semelhantes às demandas funcionais esportivas. Tais características tornam a CCF uma estratégia relevante na reabilitação de atletas, contribuindo para um retorno mais seguro e eficiente às práticas atléticas (Barreto et al., 2023).
Diante da relevância clínica e epidemiológica das lesões do LCA, dos elevados custos associados ao tratamento e reabilitação, do impacto funcional sobre atletas e da variedade de protocolos fisioterapêuticos disponíveis, torna-se fundamental investigar quais abordagens apresentam melhores resultados.
Nesse contexto, a comparação entre exercícios em cadeia cinética aberta (CCA) e fechada (CCF) mostra-se especialmente relevante, visto que ambas as metodologias oferecem benefícios e apresentam limitações específicas, mas ainda não há consenso definitivo sobre qual delas proporciona maior segurança articular e eficácia no retorno ao esporte.
Deste modo, o presente estudo tem por objetivo, identificar os principais efeitos dos exercícios em cadeia cinética aberta e fechada na recuperação de lesões do ligamento cruzado anterior, em diferentes fases de reabilitação.
2. METODOLOGIA
Trata-se de uma revisão bibliográfica com abordagem qualitativa, utilizando o método PICO, que representa um acrônimo Paciente, Intervenção, Comparação e “Outcomes” (desfecho), para formular a pergunta norteadora e definir os critérios de inclusão e exclusão das publicações. Este modelo permite a construção de uma pergunta clínica estruturada a partir de quatro componentes:
• P (Paciente ou Problema): atletas com lesão de Ligamento Cruzado Anterior (LCA), submetidos à cirurgia de reconstrução ligamentar.
• I (Intervenção): fisioterapia com exercícios de cadeia cinética fechada (CCF).
• C (Comparação): fisioterapia com exercícios de cadeia cinética aberta (CCA).
• O (Desfecho): retorno funcional mais seguro e rápido às atividades esportivas, com menor estresse articular e menor risco de recidiva da lesão.
Em atletas submetidos à reconstrução do Ligamento Cruzado Anterior (P), a reabilitação com exercícios de cadeia cinética fechada (I), quando comparada à cadeia cinética aberta (C), promove melhor recuperação funcional, com menor estresse articular e risco de nova lesão (O).
2.1 Estratégia de busca
A busca dos estudos foi realizada de janeiro de 2020 a agosto de 2025, contemplando os últimos cinco anos, para garantir atualização científica. As bases de dados utilizadas foram: PubMed, Scielo, Lilacs, Science Direct e Google Scholar.
Foram empregados descritores em português e inglês, utilizando combinações com os operadores booleanos AND e OR. Em português: “lesão do Ligamento Cruzado Anterior” AND “reabilitação fisioterapêutica” AND (“cadeia cinética fechada” OR “cadeia cinética aberta”). Em inglês: “anterior cruciate ligament” AND “rehabilitation” AND (“closed kinetic chain” OR “open kinetic chain”). Foi utilizado rayyan como uma ferramenta para triagem dos artigos e exclusão de duplicatas.
2.2 Critérios de inclusão e exclusão
Inclusão: artigos publicados entre 2020 e 2025; estudos com seres humanos (atletas ou praticantes de esporte); trabalhos que compararam intervenções de CCF e CCA na reabilitação do LCA; idiomas português e inglês.
Exclusão: artigos duplicados; revisões sem descrição metodológica clara; estudos com população idosa ou com foco em outras lesões e artigos abaixo do ano de 2020. A seguir visualizados em fluxograma prisma.
2.3 Seleção dos artigos
Dos 78.300 registros inicialmente identificados nas bases de dados, realizou-se a exclusão de duplicatas por meio da ferramenta Rayyan, resultando em 82 artigos únicos. Em seguida, procedeu-se à triagem por título e resumo, etapa na qual 61 artigos foram excluídos por não atenderem aos critérios de inclusão, restando 21 para leitura completa. Após a leitura integral e avaliação metodológica, 10 artigos foram excluídos por não compararem diretamente os exercícios de cadeia cinética aberta (CCA) e cadeia cinética fechada (CCF), ou por apresentarem amostras distintas da população-alvo (atletas com lesão de LCA). Assim, 11 artigos atenderam integralmente aos critérios de elegibilidade e foram incluídos na presente revisão.
• Registros identificados nas bases de dados: (n = 78.300);
• Registros triados por título e resumo (n = 82);
• Registros excluídos por não atender critérios (n = 21).
• Artigos selecionados (n=11)
Fluxograma 1: Registros da seleção de artigos selecionados para o artigo.
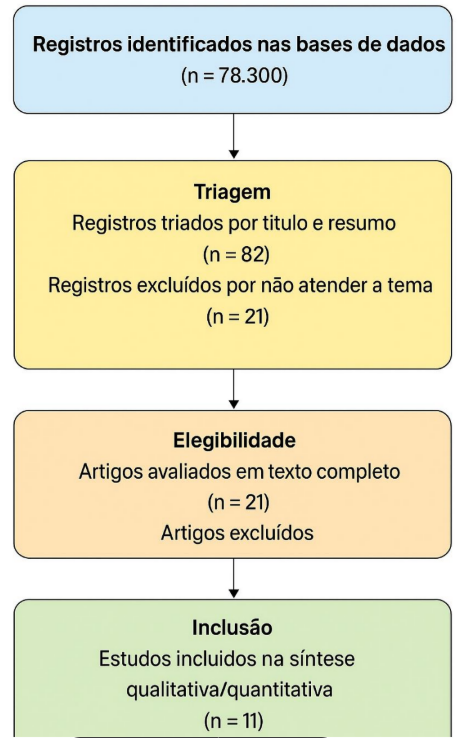
Fonte: imagem criada por IA
2.4 Avaliação crítica dos estudos
Cada artigo incluído foi avaliado quanto à qualidade metodológica e nível de evidência, segundo a hierarquia do Oxford Centre for Evidence-Based Medicine (OCEBM):
• Nível 1: ensaios clínicos randomizados e revisões sistemáticas. • Nível 2: estudos de coorte.
• Nível 3: estudos caso-controle.
• Nível 4: séries de casos.
• Nível 5: opinião de especialistas.
Foram observados os seguintes aspectos:
• Clareza dos objetivos e da amostra.
• Detalhamento das intervenções (tipo, frequência e duração dos exercícios).
• Critérios de progressão e retorno ao esporte.
• Registro de complicações ou efeitos adversos.
2.5 Organização e síntese dos dados
Os dados extraídos foram sistematizados em tabelas comparativas, contendo: autor/ano, população estudada, intervenção (CCA ou CCF), tempo de intervenção, principais achados, conclusões dos autores e pontos divergentes. A análise foi qualitativa, priorizando a interpretação crítica das evidências e suas implicações clínicas na prática fisioterapêutica.
Os dados foram organizados em tabelas comparativas, contemplando: • Autor/ano;
• População estudada;
• Tipo de intervenção (CCA ou CCF);
• Tempo de intervenção;
• Principais achados;
• Conclusões dos autores;
• Divergências metodológicas.
A análise final foi qualitativa e crítica, priorizando a interpretação dos resultados e suas implicações práticas para a fisioterapia esportiva.
3. REFERENCIAL TEÓRICO
3.1 Anatomia e Função do LCA
O joelho é uma articulação sinovial de elevada complexidade, desempenhando papel crucial na locomoção e na manutenção da estabilidade corporal. Avanços recentes em técnicas de imagem, biomecânica computacional e estudos anatômicos
detalhados têm ampliado significativamente o entendimento sobre suas estruturas. A literatura atual destaca que o conhecimento aprofundado da anatomia do joelho é essencial para o diagnóstico preciso, prevenção de lesões e planejamento cirúrgico adequado (Zhang et al., 2020; Hassebrock et al., 2020).
O fêmur, que é o maior osso do corpo humano, articula-se com a tíbia na região do joelho e pesquisas recentes apontam variações na morfologia do côndilo femoral, as quais podem influenciar tanto a distribuição de cargas quanto a estabilidade da articulação (Smith, John et al., 2020).
A tíbia, principal osso da perna, possui os platôs tibiais que recebem os côndilos femorais. Alterações na geometria desses platôs podem aumentar a predisposição a lesões ligamentares, incluindo aquelas do ligamento cruzado anterior (LCA) (Miller et al., 2020).
A patela é um osso sesamoide que potencializa a ação do músculo quadríceps. Estudos morfométricos recentes investigaram parâmetros como a altura patelar e a classificação de Wiberg, a classificação de Wiberg descreve o formato das facetas articulares da patela em três tipos principais: Tipo I, quando as facetas medial e lateral são simétricas e côncavas, Tipo II, quando a faceta medial é menor que a lateral, e Tipo III, quando a faceta medial é bem menor, quase plana ou convexa, predispondo a instabilidades femoropatelares, considerados fundamentais para procedimentos cirúrgicos, incluindo a artroplastia total do joelho (Jones et al., 2020).
A superfície articular do fêmur e da tíbia é revestida por cartilagem hialina, cuja função principal é reduzir o atrito durante os movimentos e permitir o deslizamento eficiente entre os ossos. Entre os côndilos femorais e os platôs tibiais encontram-se os meniscos medial e lateral, estruturas fibrocartilaginosas com múltiplas funções biomecânicas, que aumentam a congruência articular, distribuem cargas compressivas, auxiliam na lubrificação e nutrição da articulação e contribuem para a propriocepção (Santos et at., 2020).
O menisco medial apresenta menor mobilidade em comparação ao lateral, o que o torna mais propenso a rupturas, especialmente na região do corno posterior, fundamental para a estabilidade articular. Em contraste, o menisco lateral, devido à sua maior mobilidade e formato semicircular, sofre menos lesões, mas continua desempenhando papel essencial na distribuição de cargas e na proteção da cartilagem articular. Assim, a integridade meniscal é crucial para o funcionamento biomecânico do joelho e para a prevenção de degenerações articulares ao longo do tempo (Oliveira et al., 2020).
O joelho é envolto por uma cápsula articular fibrosa que se insere ao redor dos limites ósseos e é reforçada por ligamentos intrínsecos e extrínsecos. No interior dessa cápsula, encontra-se a membrana sinovial, cuja principal função é secretar o líquido sinovial, elemento essencial para a lubrificação, nutrição da cartilagem hialina e redução do atrito durante os movimentos articulares (Huang et al., 2020; Kapoor; Maitland; Kippel, 2021).
Além disso, a membrana forma pregas sinoviais e bolsas, entre as quais se destaca a bolsa suprapatelar, que contribui para a dissipação de forças compressivas e a manutenção da homeostase intra-articular. Estudos recentes em anatomia e biomecânica do joelho reforçam a importância dessas estruturas sinoviais para a preservação da integridade da cartilagem e para a prevenção de processos degenerativos (Huang et al., 2020; Kapoor; Maitland; Kippel, 2021).
A estabilidade do joelho é amplamente determinada pela ação de seus ligamentos, classificados em extracapsulares e intracapsulares. Entre os extracapsulares, o ligamento colateral medial (LCM) atua limitando o movimento em valgismo e fornecendo estabilidade à face interna do joelho, enquanto o ligamento colateral lateral (LCL) restringe o varismo e promove estabilidade no compartimento lateral (Moore; Dalley; Agur et al., 2020; Netter et al., 2021).
No interior da articulação, os ligamentos cruzados desempenham papel fundamental no controle do deslocamento tibial. O ligamento cruzado anterior (LCA) impede a translação anterior da tíbia em relação ao fêmur, sendo considerado essencial para o controle cinemático do joelho, especialmente em movimentos de rotação e desaceleração. Já o ligamento cruzado posterior (LCP) atua de forma oposta, prevenindo a translação posterior da tíbia, além de contribuir para a estabilidade rotacional em situações de carga (Kapandji et al., 2020).
Complementando esse sistema, o ligamento patelar e os retináculos patelares desempenham função importante no alinhamento e estabilização da patela, influenciando diretamente a biomecânica femoropatelar. Estudos recentes de revisão anatômica e biomecânica destacam que a compreensão detalhada da morfologia e função dessas estruturas é essencial para estratégias de prevenção de lesões e para o sucesso de procedimentos reconstrutivos (Herzog et al., 2020; Andrade et al., 2022).
No compartimento posterior da coxa, encontram-se os flexores, principalmente os isquiotibiais (bíceps femoral, semitendíneo e semimembranáceo. Esses músculos não apenas realizam a flexão do joelho, mas também contribuem para o controle dinâmico da articulação, auxiliando na estabilidade durante movimentos de alta demanda, como mudanças de direção e desacelerações (Farina et al., 2021)
O músculo poplíteo merece destaque por sua função específica: atua no desbloqueio inicial da extensão, permitindo o início da flexão do joelho. Essa ação é fundamental para a transição entre movimentos estáticos e dinâmicos, além de ter papel estabilizador secundário na região póstero-lateral do joelho (Kapandji et al., 2020; Andrade et al., 2022).
O suprimento arterial do joelho é realizado por meio de um extenso plexo anastomótico periarticular, constituído principalmente pelos ramos geniculares oriundos da artéria poplítea, além de contribuições das artérias femoral e tibiais. Esse arranjo vascular garante irrigação eficiente às estruturas intra e extra-articulares, mesmo durante diferentes graus de flexão, quando a artéria poplítea pode sofrer compressão mecânica (Netter et al., 2021; Tang et al., 2022).
A drenagem venosa segue o trajeto arterial correspondente, sendo realizada pelas veias geniculares, que convergem para a veia poplítea, assegurando retorno venoso adequado e colaborando para a homeostase articular (Moore; Dalley; Agur et al., 2020).
A inervação do joelho é fornecida por ramos articulares dos nervos femoral, obturatório, tibial e fibular comum, em conformidade com a regra de Hilton, a qual os nervos que suprem os músculos atuantes sobre uma articulação também inervam a própria cápsula articular e suas estruturas internas. Esse princípio explica a convergência de informações nociceptivas e proprioceptivas do joelho, tornando-o uma das articulações mais ricamente inervadas e com grande importância clínica em quadros de dor articular e reabilitação (Andrade et al., 2021; Netter et al., 2021).
3.2 Mecanismo de Lesão
Décadas de estudos demonstraram que as funções principais do LCA incluem, sobretudo, resistir à força de cisalhamento anterior da tíbia proximal em relação ao fêmur distal, e, de forma secundária, controlar o torque interno da tíbia e o momento de abdução do joelho. Para entender esses papéis, uma extensa série de pesquisas investigou o comportamento do LCA diante de cenários de carga simples e praticamente estáticos do joelho. Embora esses cenários de carga possam não refletir condições fisiológicas típicas de lesão do LCA, apresentando pouca ou nenhuma força de compressão axial, mínima contribuição muscular trans-articular, cargas quase estáticas, magnitudes pouco realistas e/ou tempos de aplicação não fisiológicos, eles permitem isolar o efeito de cada força ou momento sobre o comportamento do ligamento (Kennedy et al., 1974).
Durante movimentos atléticos, como aterrissagens de salto, a articulação tibiofemoral é submetida a forças de compressão axial significativas. Essas forças resultam principalmente das contrações musculares que atravessam o joelho, especialmente do quadríceps, que atua para resistir ao grande momento de flexão gerado nessas manobras, e também da força de reação do solo transmitida através da articulação, contribuindo adicionalmente para o momento de flexão (Hendrix et al., 2019)
Como diz Markolf et al. (1995), embora essas forças de compressão provoquem os maiores deslocamentos do joelho em ângulos de flexão mais elevados (30–50°), deslocamentos significativos também são observados em ângulos menores (10–30°), faixa em que ocorre a maioria das lesões do LCA sem contato. A força de compressão ao longo do eixo longitudinal da tíbia gera um componente de cisalhamento anterior, promovendo a translação anterior da tíbia devido à inclinação posterior-inferior dos platôs tibiais lateral e medial.
De fato, Wang et al. (2023) observou que a magnitude da translação anterior da tíbia, induzida por uma força de compressão axial no joelho, está positivamente correlacionada com as inclinações medial e lateral do platô tibial: quanto maiores as inclinações, maior a translação tibial. Não é surpreendente, portanto, que exista ampla evidência indicando que a inclinação posterior-inferior do platô tibial, particularmente do platô lateral, seja um fator de risco significativo para lesão do LCA.
Segundo o autor Kiapour et al. (2013), outro mecanismo de carga no plano sagital que afeta o LCA ocorre durante a ativação e o alongamento do quadríceps em manobras atléticas. Por exemplo, quando a força exercida sobre um músculo ativo supera a capacidade de geração de força do próprio músculo, ele é estendido sob carga em uma contração denominada “excêntrica”. Esse alongamento pode aumentar a tensão muscular em até 70% acima do valor isométrico máximo, um fenômeno frequentemente aproveitado por atletas para produzir forças musculares elevadas, como acontece durante o ciclo de alongamento e encurtamento muscular.
Já o autor Hosseini, et al. (2011), diz que quando o quadríceps é alongado sob carga enquanto o joelho apresenta leve flexão durante uma manobra atlética, gera-se uma força muscular considerável. Há consenso de que essa força, transmitida pelo mecanismo patelofemoral, aumenta significativamente a translação anterior da tíbia e a rotação interna tibial, impondo uma sobrecarga importante sobre o LCA. Isso ocorre devido ao ângulo de inserção do quadríceps na tíbia por meio do tendão patelar.
A força de tração gerada pelo quadríceps na inserção tibial tem um componente anterior que produz cisalhamento tibial anterior, além de um componente de compressão axial no joelho, ambos capazes de tensionar o LCA. Quando o joelho está quase totalmente estendido (0–20°), o componente de cisalhamento anterior é maior devido ao ângulo relativamente acentuado de inserção na tíbia. Em ângulos de flexão mais elevados (>20°), o componente de cisalhamento diminui, enquanto o componente de compressão axial se torna predominante. A co-contração dos isquiotibiais pode reduzir a carga sobre o LCA ao gerar uma força de cisalhamento tibial posterior que se opõe ao cisalhamento anterior da tíbia. No entanto, quando o joelho está quase totalmente estendido (~0°), os isquiotibiais apresentam menor eficiência devido ao ângulo de inserção relativamente pequeno na tíbia, produzindo, portanto, forças de cisalhamento posterior relativamente reduzidas (Shultz et al., 2008).
No contato inicial com o solo durante manobras atléticas que envolvem rotação axial como aterrissagem em pivô ou movimentos de apoio e giro a magnitude do torque interno aplicado à articulação do joelho é influenciada pelo coeficiente de atrito entre o calçado do atleta e a superfície de jogo. Valores mais elevados de atrito podem gerar torques maiores no joelho. Por exemplo, superfícies de grama artificial com enchimento de areia/borracha, associadas a chuteiras com travas em lâmina, produzem torques axiais mais elevados na perna em comparação com grama natural e chuteiras com travas do tipo garanhão (Sonnery-Cottet et al., 2021).
Assim, em superfícies de jogo com alto coeficiente de atrito, combinadas com determinados tipos de calçado, é esperado que os atletas desenvolvam maiores torques tibiais internos, o que aumenta o risco de lesões do LCA. (Hirokawa et al., 1991), Segundo (Solomonow, et al., 2020), por exemplo, estudos na NFL identificaram que a incidência de lesões do LCA foi 67% maior em superfícies artificiais (FieldTurf) em comparação com gramados naturais.
É importante destacar, contudo, que nem todas as evidências apontam para um risco aumentado de lesão do LCA em superfícies artificiais. Ainda assim, os princípios biomecânicos indicam que o coeficiente de atrito entre o calçado e o solo exerce papel fundamental na geração do torque tibial interno. A controvérsia observada na literatura reflete, portanto, a complexa interação entre múltiplos fatores que influenciam a magnitude e a direção tridimensional das cargas aplicadas ao joelho e ao LCA (Laprade et al., 2021).
3.3 Abordagens de Tratamento Cirúrgico e Conservador
No estudo realizado por Liu et al. (2020), as lesões dos ligamentos cruzados do joelho constituem um grande desafio para ortopedistas e cirurgiões, sobretudo em indivíduos mais jovens. A técnica cirúrgica mais adequada para a reconstrução do ligamento cruzado anterior (LCA), ainda está em constante aprimoramento, buscando otimizar os resultados em longo prazo e reduzir o risco de complicações.
Existem duas possibilidades de tratamento para esse tipo de lesão: o cirúrgico e o conservador. A intervenção cirúrgica tem como principal objetivo restabelecer a estabilidade articular do joelho e recuperar o máximo possível da função, possibilitando que o paciente retome a prática esportiva em condições semelhantes às que apresentava antes da lesão. Saber lidar com este tipo de lesão e fundamental para que os profissionais possam restabelecer o nível de função física pré-lesão dos pacientes. Cabe aos profissionais da saúde orientar seus pacientes, esclarecendo todas as alternativas de tratamento disponíveis, bem como os benefícios e limitações de cada uma (Trindade et al., 2020).
Essa orientação deve levar em conta fatores individuais e contextuais, como características próprias do paciente, nível de prática esportiva, além de seus objetivos e expectativas quanto ao retorno às atividades. A comunicação clara sobre essas possibilidades faz parte do papel dos fisioterapeutas e de outros profissionais da área da saúde. Se fomos para o caminho do tratamento conservador vamos basear em um protocolo que envolve várias técnicas da fisioterapia e seguir um protocolo seguro para otimizar a volta do atleta o mais rápido possível e com segurança (Liu et al., (2020).
Segundo Ciechanowicz et al. (2020), o uso da eletroterapia por meio da High Tone Power Therapy (HiToP) apresenta efeitos positivos na função muscular, na redução do derrame articular, no aumento da massa muscular e na melhora da função articular. A reabilitação aquática também é uma estratégia indicada, incluindo exercícios como a caminhada em meio aquático, que contribui para o fortalecimento dos músculos extensores do joelho, além de promover melhora da propriocepção e do desempenho funcional da articulação, apresentando resultados superiores em comparação ao treinamento de caminhada em solo (Li et al., 2021).
Para que os pacientes obtenham um controle adequado da articulação, o treinamento neuromuscular após a lesão é fundamental, pois contribui significativamente para a redução da dor, melhora da função, aumento da força, do desempenho e, consequentemente, da qualidade de vida (Khalid et al., 2022).
Se for necessário o atleta passar por procedimento cirúrgico, o objetivo da reconstrução cirúrgica é restabelecer a estabilidade do joelho e otimizar a capacidade funcional, possibilitando que o indivíduo retorne às atividades esportivas no mesmo nível em que se encontrava antes da lesão (Carter et al., 2017). Nos estudos de Amatuzzi et al. (2004), esse tipo de intervenção é indicada principalmente para pacientes que apresentam elevado risco de instabilidade ou que relatam episódios frequentes de falseio articular.
O estudo do Mota et al. (2024), fez uma revisão sistemática sobre o retorno ao esporte em atletas profissionais, revelando que 82% dos pacientes conseguiram retomar alguma prática esportiva após a reconstrução do LCA. No entanto, apenas 63% retornaram ao nível de desempenho esportivo pré-lesão, e somente 44% conseguiram voltar às competições.
A reconstrução cirúrgica do LCA é considerada o padrão-ouro no tratamento de lesões completas em pacientes ativos. Entre as técnicas mais utilizadas estão a reconstrução com enxerto autólogo do tendão patelar, dos isquiotibiais ou do tendão do quadríceps (Webster et al., 2018). Pesquisas indicam que essas abordagens promovem uma restauração eficaz da estabilidade do joelho, permitindo que mais de 80% dos pacientes retornem ao nível de atividade que apresentavam antes da lesão.
Os principais benefícios da cirurgia incluem a diminuição do risco de novas lesões, a melhora da função articular e a prevenção de danos adicionais ao menisco e à cartilagem. A escolha da técnica ideal depende de fatores como idade, nível de atividade e preferência do cirurgião, sendo que cada abordagem apresenta vantagens específicas (Almeida et al., 2010).
No estudo conduzido por Kopka et al. (2024), foi realizada uma análise comparativa entre duas técnicas distintas de reconstrução do ligamento cruzado anterior (LCA). A primeira abordagem envolve a preservação parcial dos remanescentes do ligamento durante a cirurgia, enquanto a segunda consiste na reconstrução anatômica de único feixe, que normalmente remove completamente o ligamento lesionado. Na técnica de preservação parcial, uma porção do ligamento original é mantida e integrada ao enxerto durante o procedimento. Em contraste, na reconstrução anatômica de único feixe, o ligamento comprometido é totalmente removido antes da reconstrução propriamente dita.
O acompanhamento criterioso de cada fase do retorno ao esporte é essencial para reduzir o risco de novas lesões e garantir que o atleta recupere tanto a função física quanto a confiança psicológica. Programas de reabilitação progressiva, aliados a avaliações contínuas de força, estabilidade e desempenho funcional, ajudam a determinar o momento adequado para avançar de uma etapa para a seguinte, assegurando um retorno seguro e eficaz às atividades esportivas (Ardern et al., 2010).
Segundo Forsdyke et al. (2016), fatores emocionais e de confiança são amplamente reconhecidos na literatura como preditores importantes do retorno ao esporte após a reconstrução do LCA. Reações psicológicas positivas aumentam de forma significativa as chances de o atleta retomar a prática esportiva no mesmo nível apresentado antes da lesão. Muitos atletas sentem que lesões ligamentares no joelho são um bom motivo para parar com o nível competitivo e focar seu tempo em uma vida social e familiar. Outros apresentam um obstáculo psicológico, que limita a função em troca de proteção contra uma possível re-lesão (Astur et al., 2016).
Na literatura, não há consenso de que a intervenção cirúrgica seja superior ao tratamento conservador. Observa-se que a taxa de retorno ao esporte é semelhante entre os dois grupos, variando de 8% a 82% nos pacientes submetidos à reconstrução cirúrgica e de 19% a 82% naqueles que não passaram pelo procedimento (Almeida et al., 2010).
3.4 Cadeia Cinética Aberta
Nos exercícios em CCA, o segmento distal (pé) é livre para se mover, permitindo a mobilidade da perna sem contato fixo com uma superfície estável. Exemplos clássicos são a extensão de joelho em máquina, flexão de joelho em mesa flexora e a elevação de perna estendida (Fitzgerald et al., 1997).
Estudos apontam que a CCA promove maior ganho de força isocinética e resistência dos músculos extensores do joelho em comparação com a CCF (Tagesson et al., 2008). Essa característica é fundamental, visto que o fortalecimento do quadríceps é essencial para a recuperação funcional após a reconstrução do LCA (Williams et al., 2005).
Entretanto, uma desvantagem importante é o aumento da força de cisalhamento anterior da tíbia, especialmente nos últimos 30° de extensão do joelho. Essa sobrecarga pode gerar tensão adicional sobre o enxerto do LCA, aumentando o risco de instabilidade secundária (Torzilli; Deng; Warren et al., 1994). Por essa razão, exercícios em CCA foram historicamente considerados menos seguros, sobretudo nas fases iniciais da reabilitação (Bynum; Barrack; Alexander et al., 1995).
3.5 Cadeia Cinética Fechada
Nos exercícios em CCF, o pé permanece fixo contra uma superfície, e o movimento ocorre nos segmentos proximais, como quadril e joelho. São exemplos comuns: agachamento, leg press e avanço (lunge) (Fitzgerald et al., 1997).
Entre suas principais vantagens, destaca-se a redução da força de cisalhamento anterior da tíbia, o que contribui para proteger o enxerto do LCA (Fleming; Oksendahl; Beynnon et al., 2005). Além disso, os exercícios em CCF estimulam a co-contração entre extensores e flexores do joelho, aumentam a compressão tibiofemoral e reduzem complicações patelofemorais (Glass; Waddell;
Hoogenboom et al., 2010). Por essas razões, a literatura tradicionalmente recomenda a CCF como abordagem inicial mais segura após a reconstrução do LCA (Mikkelsen; Werner; Erickson et al., 2000).
Contudo, a ativação isolada do quadríceps é menor do que na CCA, o que pode limitar os ganhos de força específicos desse músculo. Dessa forma, pacientes podem apresentar uma recuperação mais lenta da força do quadríceps quando submetidos apenas a programas de CCF (Ross; Denegar; Winzenried et al., 2001).
3.6 Evidências Comparativas
A reabilitação do ligamento cruzado anterior (LCA) continua sendo um dos maiores desafios da fisioterapia esportiva, em especial pela necessidade de equilibrar proteção do enxerto reconstruído e ganho rápido de força e função muscular. Nos últimos anos, estudos têm se concentrado em comparar os efeitos dos exercícios em cadeia cinética aberta (CCA) e cadeia cinética fechada (CCF), buscando determinar a melhor abordagem ou combinação entre ambos (Brinlee et al., (2022).
Os exercícios em cadeia cinética aberta caracterizam-se pela movimentação livre do segmento distal, como o pé, permitindo isolar grupos musculares específicos, principalmente o quadríceps. Essa característica faz com que sejam altamente eficazes para o ganho de força isocinética. Em uma revisão sistemática com meta análise, Pamboris et al. (2024), demonstraram que pacientes submetidos a programas que incluíram CCA obtiveram maior incremento de força do quadríceps nos meses 3 e 4 após a lesão ou reconstrução do LCA, quando comparados a programas compostos apenas por CCF. Além disso, o mesmo estudo identificou que a CCA, quando realizada com cargas baixas, não aumentou a frouxidão anterior da tíbia, e em alguns casos até contribuiu para a redução da laxidade articular em joelhos com deficiência do LCA.
Outro aspecto relevante investigado é a introdução precoce da CCA. Tradicionalmente, havia resistência em utilizá-la nos estágios iniciais da reabilitação, devido ao receio de sobrecarga no enxerto. Entretanto, uma revisão sistemática conduzida por Fontanier et al. (2025), analisou ensaios clínicos recentes e concluiu que a introdução de exercícios em CCA a partir da 4ª semana pós-cirurgia, sempre após um período inicial com CCF, promoveu melhorias significativas na dor, força muscular, função e retorno ao esporte, sem evidências de efeitos adversos. Esse achado reforça a tendência atual de não excluir a CCA dos protocolos iniciais, mas sim inseri-la de maneira controlada e progressiva.
Complementando essas evidências, um estudo de coorte realizado em 2023 avaliou pacientes submetidos à reconstrução do LCA divididos em dois grupos: um que realizou apenas CCF e outro que combinou CCF com a inclusão progressiva de CCA a partir da 4ª semana. Os resultados mostraram que o grupo combinado apresentou maior força de quadríceps e isquiotibiais aos 3 e 6 meses, sem aumento na laxidade do enxerto, indicando que a CCA pode ser utilizada com segurança quando criteriosamente aplicada (Forelli et al., (2023).
Do ponto de vista biomecânico, Wang et al. (2023), realizaram uma análise in vivo da deformação do enxerto durante a execução de exercícios. Os autores observaram que os exercícios em CCA com carga aumentam o alongamento do LCA mais do que os em CCF, confirmando a necessidade de cuidado na prescrição precoce de CCA sob resistência. No entanto, também demonstraram que os exercícios em CCA sem carga não aumentaram a tensão no enxerto, o que os torna viáveis e seguros nas fases iniciais da reabilitação.
Já os exercícios em cadeia cinética fechada permanecem como a base inicial da reabilitação. Por fixarem o segmento distal, eles reduzem a translação anterior da tíbia e promovem co-contração entre quadríceps e isquiotibiais, o que aumenta a estabilidade articular e protege o enxerto em cicatrização. Esse padrão de ativação também contribui para uma melhor distribuição das forças compressivas na articulação femorotibial, diminuindo o estresse patelofemoral. Por isso, a CCF é considerada a estratégia mais segura nas primeiras semanas após a reconstrução. Contudo, diversos estudos apontam que programas exclusivos de CCF podem resultar em déficit persistente de força do quadríceps, prejudicando o desempenho funcional a médio e longo prazo (Pamboris et al., 2024; Fontanier et al., 2025).
Portanto, a literatura atual converge para um modelo integrado: iniciar a reabilitação com predominância de CCF, visando estabilidade e proteção do enxerto, e introduzir gradualmente a CCA a partir da 4ª semana, em amplitude segura (geralmente entre 90° e 45° de flexão do joelho), progredindo conforme a evolução clínica do paciente. Essa estratégia parece ser a que melhor equilibra segurança biomecânica e ganho funcional, além de acelerar o retorno às atividades esportivas. (Fontanier et al., 2025)
4. RESULTADOS
Os estudos selecionados foram sintetizados em formato de quadro comparativo (Quardro 1), contemplando autor/ano, população estudada, tipo de intervenção (cadeia cinética aberta ou fechada), tempo de intervenção, principais achados, conclusões dos autores e pontos divergentes. Essa apresentação possibilita visualizar de maneira organizada as evidências disponíveis e as diferenças metodológicas e conceituais entre os estudos.
Quadro 1: Compilado de artigos selecionados para a revisão de literatura.
| Autor / Ano | População Estudada | Intervenção (CCA ou CCF) | Tempo de Intervenção | Principais Achados | Conclusões dos Autores | Pontos Divergentes |
| Fontanier et al., 2025 | Pacientes submetidos à reconstrução do LCA (meta análise). | OKC (CCA) vs CKC (CCF). | Primeiras semanas; benefícios mais evidentes após 4 semanas e/ou após CKC. | OKC melhora força e PROMs sem prejuízo claro da estabilidade. | OKC pode ser incluído de forma criteriosa sem efeitos adversos significativos. | Divergência sobre quando iniciar OKC: alguns apontam riscos na fase inicial, outros defendem introdução precoce controlada. |
| Badawy et al., 2022 | Atletas pós ACLR (revisão/guia). | Discute CKC e OKC em protocolos. | Baseado em fases da cicatrização; tempo varia conforme critérios. | Reforça importância da progressão por critérios funcionais. | Protocolos devem considerar milestones, não apenas tempo. | Diverge de protocolos tradicionais baseados apenas em semanas; defende abordagem individualizada |
| Brinlee et al., 2022 | Atletas com ACLR (guia de retorno ao esporte). | Protocolos com CKC e OKC na progressão. | Não fixa duração; depende de marcos funcionais. | Progressão deve se basear em testes (força, hop tests). | OKC e CKC têm papéis complementa res. | Divergência com abordagens lineares de tempo; prioriza critérios objetivos. |
| Forelli et al., 2023 | Coorte de pacientes pós ACLR. | OKC precoce vs CCF. | Primeiras semanas (fase inicial). | OKC precoce melhorou força sem aumento consistente da laxidade. | OKC pode ser seguro se bem monitorado. | Divergência entre achados clínicos (sem instabilidade) e estudos biomecânicos (risco de estresse no enxerto). |
| Wang et al., 2023 | 18 voluntários saudáveis (estudo biomecânico). | Testes OKC vs CCF. | Testes agudos em laboratório | OKC alongou mais o LCA que CKC. | Base teórica para cautela no OKC precoce. | Diverge de estudos clínicos que não observaram instabilidade; mostra discrepância entre biomecânica e prática. |
| Elabd & Elabd, 2023 | Atletas amadores pós ACLR (RCT). | Critérios funcionais (OKC + CCF). | Semanas/me ses. | Grupo baseado em critérios teve melhores resultados funcionais. | Protocolos baseados em milestones são superiores. | Diverge de protocolos fixos por tempo. |
| Pamboris et al., 2024 | Pacientes pós- ACLR (meta-análise). | OKC vs CCF. | Meses 3–4 após cirurgia. | OKC aumentou força do quadríceps sem aumento da frouxidão. | OKC seguro quando aplicado após estabilização inicial. | Divergência sobre impacto no início precoce. |
| De Souza et al., 2022 | Pacientes em fases distintas de reabilitação pós-LCA. | CCF na fase aguda; CCA nas fases intermediária e crônica. | Fase aguda, subaguda e crônica. | CCF inicial favoreceu estabilidade; CCA posterior melhorou força e propriocepção | Protocolos devem respeitar fases da cicatrização. | Divergência sobre início precoce da CCA. |
| Barreto; Silva; Cunha, 2023 | Atletas de elite em reabilitação. | Comparação CCA e CCF. | Protocolos clínicos variáveis. | CCA impõe mais estresse em extensão terminal; CCF reduz carga articular e aumenta estabilidade. | CCF indicada na fase inicial; CCA importante para força específica em fases intermediária s. | Divergência quanto à segurança da CCA em extensão terminal. |
| Trindade et al., 2020 | Atletas com lesão parcial de LCA (tratamento conservador). | Protocolos mistos de CCF e CCA. | Conforme evolução clínica. | Redução do edema, recuperação da ADM e fortaleciment o com associação progressiva. | Integração de CCF e CCA promove retorno funcional seguro. | Divergência quanto à eficácia do conservador vs cirúrgico. |
| Silva et al., 2020 | Pacientes pós cirurgia de LCA. | Foco em prevenção de déficits neuromuscul ares. | Pós operatório imediato. | Inibição artrogênica afeta força e controle motor. | Exercícios progressivos essenciais para restaurar função neuromuscul ar. | Divergência sobre tempo ideal para iniciar carga e mobilização. |
Legendas: LCA – Ligamento Cruzado Anterior; ACLR – Anterior Cruciate Ligament Reconstruction (Reconstrução do Ligamento Cruzado Anterior); OKC – Open Kinetic Chain (Cadeia Cinética Aberta); CCF – Cadeia Cinética Fechada; CCA – Cadeia Cinética Aberta; RCT – Randomized Clinical Trial (Ensaio Clínico Randomizado); PROMs – Patient-Reported Outcome Measures (Medidas de Resultados Relatados pelos Pacientes).
Fonte: os autores, 2025.
5. DISCUSSÃO
A utilização de exercícios em cadeia cinética aberta (CCA) no processo de reabilitação após reconstrução do ligamento cruzado anterior (LCA) tem sido alvo de intensos debates na literatura, principalmente quanto à segurança em relação ao enxerto e ao impacto sobre a força muscular do quadríceps. Estudos recentes apontam para uma mudança de paradigma, indicando que a CCA, quando aplicada de forma progressiva e com controle de carga e amplitude, não apenas é segura, mas também desempenha papel essencial no restabelecimento funcional do joelho (Badawy et al., 2022)
Uma revisão sistemática e meta-análise conduzida por Fontanier et al., (2025) evidenciou que a introdução precoce de exercícios em CCA não resulta em aumento da frouxidão ligamentar, o que contraria receios anteriores sobre possível estresse excessivo no enxerto. Além disso, os autores verificaram ganhos mais expressivos na força do quadríceps quando comparados a protocolos baseados exclusivamente em cadeia fechada, reforçando a relevância desse tipo de exercício no processo de reabilitação.
Nesse mesmo sentido, Forelli et al., (2023), em um estudo de coorte, analisaram pacientes submetidos a exercícios precoces em CCA e constataram que, além da melhora significativa da força muscular, não houve diferenças na estabilidade do enxerto entre aqueles que realizaram CCA e os que não realizaram. Esses achados corroboram a segurança da introdução gradual desse recurso, desde que respeitados critérios clínicos e biomecânicos.
Outro ponto relevante é destacado por Brinlee et al., (2022), que ressaltam a limitação dos exercícios em cadeia cinética fechada (CCF) quando utilizados isoladamente, uma vez que eles não são suficientes para restaurar plenamente a força do quadríceps. Os autores defendem a combinação estratégica de CCF e CCA como abordagem mais eficaz para otimizar o processo de reabilitação e favorecer o retorno seguro ao esporte. Essa perspectiva é reforçada pelo ensaio clínico randomizado de Elabd e Elabd et al, (2023), no qual a inclusão progressiva da CCA em um protocolo baseado em critérios resultou em melhores desfechos funcionais e maior confiança dos pacientes para retomar suas atividades esportivas.
Por outro lado, Wang et al., (2023), em uma avaliação in vivo, observaram que os exercícios em CCA provocam maior alongamento do LCA em comparação à CCF, o que sugere a necessidade de cautela, sobretudo nas fases iniciais de reabilitação. Esse achado não desqualifica o uso da CCA, mas indica que parâmetros como amplitude e carga devem ser cuidadosamente monitorados para evitar sobrecarga. Nesse contexto, Badawy et al., (2022) recomendam que, nas fases iniciais, a amplitude de movimento em CCA seja restrita preferencialmente entre 90° e 40°, evitando a extensão terminal (0°–30°), considerada mais crítica para o estresse sobre o enxerto.
De forma integrada, a literatura converge para a compreensão de que a CCA não deve ser negligenciada nos protocolos de reabilitação do LCA. Pelo contrário, sua aplicação adequada promove benefícios essenciais, como a restauração da força do quadríceps e o aprimoramento da função global do joelho, sem comprometer a integridade do enxerto. Dessa forma, o debate atual não se concentra mais em excluir ou incluir a CCA, mas em como, quando e em quais parâmetros ela deve ser inserida no processo de reabilitação (Fontanier et al., 2025).
Assim, os achados reforçam a ideia de que a reabilitação deve seguir uma lógica baseada em evidências e critérios clínicos, em que a CCA desempenha papel determinante. A integração deste recurso, em conjunto com a CCF, favorece não apenas o equilíbrio entre segurança e eficácia, mas também potencializa o retorno do paciente ao nível funcional desejado, especialmente no contexto esportivo (Fontanier et al., 2025; Forelli et al., 2023; Brinlee et al., 2022; Elabd & Elabd, 2023; Wang et al., 2023; Badawy et al., 2022).
Os exercícios em cadeia cinética fechada (CCF) são amplamente reconhecidos como a base do processo de reabilitação inicial após a reconstrução do ligamento cruzado anterior (LCA). A literatura clássica e contemporânea aponta essa modalidade como a mais segura durante as fases precoces, sobretudo por favorecer um ambiente biomecânico que promove maior estabilidade articular. De acordo com Fontanier et al., (2025), os exercícios em CCF configuram-se como o “padrão-ouro” no pós-operatório imediato, uma vez que mantêm o segmento distal fixo e distribuem as cargas de forma integrada através das estruturas do joelho, reduzindo significativamente o estresse de translação anterior da tíbia sobre o enxerto. Esse aspecto é de fundamental importância, considerando que a principal preocupação nas fases iniciais de reabilitação é assegurar a proteção e integridade do ligamento recém reconstruído, evitando sobrecargas que possam comprometer o sucesso cirúrgico.
A co-contração muscular promovida pela cadeia cinética fechada (CCF) representa outro aspecto de grande relevância clínica e funcional. Conforme salientado por Brinlee et al. (2022), essa modalidade de exercício induz a ativação simultânea dos músculos quadríceps e isquiotibiais, favorecendo a compressão tibiofemoral e garantindo maior controle dinâmico da articulação. Esse mecanismo contribui não apenas para a diminuição do estresse direto sobre o enxerto, mas também para o aprimoramento do controle neuromuscular, elemento considerado determinante na prevenção de falhas na reconstrução ligamentar e na redução do risco de novas lesões.
Além disso, ao promover estabilidade articular por meio da coativação, os exercícios em CCF favorecem a integração entre força, propriocepção e coordenação motora, aspectos fundamentais para a reabilitação esportiva. Assim, essa abordagem não se limita ao fortalecimento dos grupos musculares envolvidos, mas atua de maneira mais abrangente na otimização do padrão motor funcional, preparando o atleta para as demandas específicas do retorno às atividades esportivas (Brinlee et al., 2022).
Ademais, evidências comparativas indicam que os exercícios em cadeia cinética fechada (CCF) impõem menor solicitação mecânica ao enxerto quando comparados à cadeia cinética aberta (CCA). Wang et al., (2023), em uma avaliação in vivo, demonstraram que a execução de exercícios em CCA, sobretudo quando associada ao uso de cargas adicionais, promove maior alongamento do ligamento cruzado anterior reconstruído em relação aos exercícios em CCF.
Esse achado biomecânico fortalece a compreensão de que a CCF representa uma escolha mais segura nas fases iniciais da reabilitação, pois proporciona um ambiente de menor risco para a integridade do enxerto em processo de cicatrização. Dessa forma, a literatura sustenta que a progressão ideal deve priorizar, inicialmente, a aplicação de exercícios em CCF, com a introdução gradual da CCA apenas em estágios mais avançados, quando a maturação e a consolidação do enxerto já estão mais bem estabelecidas (De Souza et al., 2022).
Outro aspecto de grande relevância é a transferência funcional proporcionada pelos exercícios em cadeia cinética fechada (CCF). Badawy et al., (2022) ressaltam que, por reproduzirem gestos motores similares às demandas específicas do esporte, como agachamentos, avanços, aterrissagens e saltos, esses exercícios oferecem um treinamento mais direcionado para o retorno às atividades atléticas.
Dessa forma, a CCF não se limita apenas a promover estabilidade articular e segurança biomecânica, mas também desempenha papel essencial na readaptação funcional do atleta. Essa característica garante que o processo de reabilitação seja mais integrado às exigências reais do gesto esportivo, preparando o indivíduo de forma progressiva para enfrentar movimentos de maior complexidade e intensidade no contexto competitivo (Elabd & Elabd., 2023).
No entanto, embora a CCF seja reconhecida como a base inicial da reabilitação, não se deve negligenciar o papel complementar dos exercícios em cadeia cinética aberta (CCA) dentro de protocolos bem estruturados. Fontanier et al., (2025) destacam que programas que se iniciam com CCF e passam a incluir a CCA a partir de aproximadamente quatro semanas de pós-operatório apresentam resultados superiores, sobretudo no que se refere ao ganho de força do quadríceps, sem prejuízo à estabilidade articular.
Tal evidência indica que a CCF atua como um alicerce seguro, garantindo proteção ao enxerto e restabelecimento da função básica do joelho, sobre o qual a CCA pode ser gradualmente incorporada. Essa associação equilibrada entre ambas as modalidades potencializa os ganhos funcionais do paciente, otimizando não apenas a recuperação muscular, mas também a preparação para as demandas esportivas de maior intensidade (Forelli et al., 2023).
Os autores Forelli et al., (2023) reforçam esse ponto ao observar que a introdução precoce de exercícios em CCA pode ser realizada sem prejuízo clínico, desde que o paciente já tenha passado por um período inicial de adaptação com CCF. Ou seja, o risco não está intrinsecamente associado à CCA, mas sim ao momento da sua inserção no protocolo. Dessa forma, a lógica de sequenciamento mostra-se determinante para o sucesso da reabilitação: inicia-se com CCF, garantindo estabilidade articular, coativação muscular e proteção ao enxerto, e posteriormente evolui-se para CCA, com carga e amplitude criteriosamente controladas, a fim de promover ganhos mais específicos de força e ativação do quadríceps. Essa progressão planejada contribui não apenas para otimizar o desempenho funcional, mas também para reduzir o risco de falhas na reconstrução e favorecer um retorno esportivo mais seguro.
Portanto, ao analisar o papel da cadeia cinética fechada (CCF) na reabilitação pós-LCA, é possível destacar três benefícios centrais: segurança biomecânica para o enxerto, aprimoramento do controle neuromuscular e transferência funcional para gestos específicos do esporte. Contudo, a literatura mais recente enfatiza que os melhores resultados são obtidos quando a CCF não é utilizada de forma isolada até o término do processo de reabilitação, mas sim como base para a introdução progressiva da cadeia cinética aberta (CCA) em fases mais avançadas (Pamboris et al., 2024).
Dessa forma, a discussão contemporânea sobre protocolos de reabilitação não se restringe à escolha entre CCF ou CCA, mas sim à compreensão do momento ideal e da forma adequada de integrar ambas as modalidades, maximizando ganhos funcionais e garantindo um retorno seguro e eficiente às atividades esportivas (Forelli et al., 2023).
A literatura atual sobre reabilitação após reconstrução do ligamento cruzado anterior apresenta algumas limitações relevantes. A primeira diz respeito à heterogeneidade metodológica entre os estudos, já que há grande variação nos tipos de enxertos utilizados, técnicas cirúrgicas empregadas, tempos de avaliação e até nos protocolos de exercícios de cadeia cinética aberta (CCA) e cadeia cinética fechada (CCF) (Kopka et al., 2024).
Essa diversidade dificulta a comparação direta e reduz a força das conclusões. Outro ponto é a qualidade metodológica: nem todos os trabalhos são ensaios clínicos randomizados, e em muitos deles o cegamento dos avaliadores e a padronização da carga ou da amplitude de movimento não ficam claros, o que pode introduzir vieses.
Além disso, muitos estudos privilegiam desfechos de curto prazo, como força e estabilidade articular, deixando de avaliar de forma consistente os resultados funcionais e o retorno ao esporte em médio e longo prazo. Observa-se também que parte das evidências biomecânicas é baseada em estudos in vivo em joelhos íntegros ou em condições que não refletem exatamente a situação pós-operatória de um enxerto em cicatrização, limitando a aplicação direta desses achados na clínica. Outro fator limitante é a ausência de consenso nos critérios de progressão entre fases da reabilitação, já que diferentes autores utilizam pontos de corte variados para força, testes de salto ou questionários subjetivos. Por fim, muitas pesquisas contam com amostras pequenas ou restritas a atletas recreacionais, dificultando a extrapolação para atletas de alto rendimento ou populações específicas, como mulheres ou indivíduos com lesões associadas (Astur et al., 2016).
Apesar das limitações metodológicas encontradas em alguns estudos, algumas implicações práticas podem ser destacadas. Os exercícios em cadeia cinética aberta (CCA) podem ser incorporados desde as fases iniciais da reabilitação, desde que respeitados parâmetros seguros, como amplitudes de flexão entre 40° e 90° e cargas baixas a moderadas, evitando resistência em extensão terminal (0–30°) nas primeiras semanas, especialmente quando o enxerto utilizado for o tendão patelar ou o semitendíneo-grácil. A inclusão criteriosa da CCA contribui para uma recuperação mais rápida da força do quadríceps sem aumento significativo da frouxidão articular (Pamboris et al., 2024).
Outro ponto central é adotar um modelo de progressão baseado em critérios objetivos, e não apenas no tempo decorrido desde a cirurgia. Elementos como amplitude de movimento completa, ausência de derrame articular, simetria de força em relação ao lado contralateral e execução adequada de exercícios funcionais devem nortear a evolução das fases de reabilitação. A combinação de CCF e CCA ao longo do processo mostra-se indicada: os exercícios em CCF promovem coativação muscular e maior estabilidade articular, enquanto os em CCA favorecem ganhos mais específicos de força do quadríceps (Trindade et al., 2020).
Além disso, a individualização do tratamento é fundamental, considerando o tipo de enxerto utilizado e a presença de lesões associadas, como reparos meniscais ou condropatias, pois tais condições podem alterar o ritmo de progressão, principalmente em relação ao ganho de amplitude de movimento e à introdução de exercícios de impacto. Dessa forma, mesmo diante de limitações metodológicas, a literatura evidencia que a reabilitação deve ser estruturada, baseada em critérios objetivos e adaptada às características de cada paciente, garantindo um retorno ao esporte seguro e eficaz (Silva et al., 2020).
5.1 Protocolo de recuperação do LCA
Baseado em nossos estudos e baseado na literatura atual a reabilitação após a reconstrução do ligamento cruzado anterior (LCA) pode ser estruturada em três fases principais: inicial, intermediária e final. Embora os períodos sejam comumente utilizados como referência, a progressão entre as fases deve ser orientada por critérios funcionais objetivos, e não apenas pelo tempo decorrido desde a cirurgia.
Na fase inicial (0–6 semanas), os objetivos centrais incluem o controle da dor e do edema, a recuperação da extensão completa do joelho, o início do ganho gradual de flexão, a restauração do padrão de marcha e a ativação do quadríceps. Durante este período, são indicados exercícios de mobilidade suave, fortalecimento isométrico, elevação de perna estendida sem déficit de extensão e exercícios em cadeia cinética fechada (CCF), como mini-agachamentos e leg press em amplitude reduzida. A cadeia cinética aberta (CCA) pode ser introduzida de forma controlada, especialmente em exercícios de extensão de joelho entre 40° e 90°, evitando resistência próxima da extensão completa. Os critérios para progressão incluem amplitude total de extensão, flexão próxima de 110°–120°, marcha sem claudicação e ausência significativa de derrame articular (Silva et al., 2020).
Na fase intermediária (6–12/16 semanas), o foco passa a ser o ganho de força muscular, principalmente do quadríceps, o aprimoramento do controle neuromuscular e a introdução gradual de tarefas unipodais e de baixo impacto. A CCA é progressivamente incorporada com maior sobrecarga, respeitando ângulos seguros, enquanto os exercícios em CCF, como agachamentos profundos, avanço e levantamento terra romeno, têm intensidade aumentada de forma gradual. Também são incluídos saltos bipodais de baixo impacto e treinamento de equilíbrio dinâmico. Para iniciar a corrida leve, recomenda-se que o paciente apresente força do quadríceps com pelo menos 70–80% de simetria em relação ao lado contralateral, boa qualidade de movimento e ausência de dor ou derrame. A transição para a fase final requer força mínima de 80–85% de simetria e execução adequada de saltos lineares sem compensações (Brinlee et al., 2022).
Na fase final (12/16 semanas até 9 meses ou mais), o objetivo principal é o desenvolvimento máximo de força e potência muscular, exercícios pliométricos e habilidades específicas do esporte. São aplicados exercícios de alta intensidade, saltos unipodais multidirecionais, treinos de aceleração e mudança de direção, além de atividades técnico-táticas progressivas. Os critérios para o retorno seguro ao esporte incluem índice de simetria ≥ 90% (idealmente 95%) na força dos extensores e flexores, testes funcionais de salto com simetria ≥ 90%, execução de movimentos sem valgo dinâmico, escores elevados em questionários subjetivos de função e confiança, e ausência de dor ou derrame articular (Fontanier et al., 2025).
6. CONCLUSÃO
Os exercícios em cadeia cinética aberta (CCA) e cadeia cinética fechada (CCF) desempenham papéis distintos, porém complementares, na recuperação de lesões do Ligamento Cruzado Anterior (LCA). Estudos recentes indicam que os exercícios em cadeia aberta são particularmente eficazes no fortalecimento específico do quadríceps, especialmente entre três e quatro meses após a reconstrução ou lesão, favorecendo a simetria muscular e acelerando a recuperação da força.
Além disso, há evidências de que a introdução precoce da CCA pode reduzir dor e desconforto, sem comprometer a estabilidade do enxerto, desde que respeitados critérios clínicos rigorosos e controle adequado de carga e amplitude, limitando, por exemplo, o movimento entre 90° e 45° de flexão. Quanto à laxidade articular, tanto os exercícios em cadeia aberta quanto em cadeia fechada apresentaram eficácia semelhante, com alguns estudos sugerindo que a CCA pode, inclusive, reduzir a frouxidão ligamentar em determinadas fases da reabilitação.
Por outro lado, os exercícios em cadeia cinética fechada (CCF) oferecem vantagens importantes nas fases iniciais da reabilitação, sendo biomecanicamente mais seguros, promovendo menor estresse direto sobre o enxerto e favorecendo o controle neuromuscular e funcional do joelho. Pacientes submetidos prioritariamente a protocolos baseados em CCF demonstraram melhores resultados quanto à função do joelho, amplitude de flexão e redução da dor nos primeiros meses pós-operatórios, indicando que esses exercícios são mais indicados nos estágios iniciais, quando a proteção do enxerto e a estabilidade global da articulação são prioritárias.
Dessa forma, não se pode afirmar que uma abordagem isolada seja universalmente superior. A literatura mais recente converge para a ideia de que a associação progressiva de ambos os métodos é a estratégia mais eficaz. O protocolo mais recomendado consiste em iniciar a reabilitação com exercícios em CCF, devido à segurança e funcionalidade que oferecem, e introduzir gradualmente os exercícios em CCA após aproximadamente quatro semanas, de forma controlada, para otimizar o fortalecimento do quadríceps e garantir uma recuperação mais completa. Essa combinação equilibra ganhos de força, manutenção da estabilidade do enxerto e melhora funcional, favorecendo o retorno às atividades esportivas e às demandas do cotidiano com maior segurança.
Do ponto de vista clínico, a aplicabilidade desse modelo combinado é evidente: os exercícios em CCF devem ser priorizados na fase inicial, garantindo estabilidade articular e ativação muscular global, enquanto os exercícios em CCA, introduzidos de forma gradual, potencializam a recuperação do quadríceps e reduzem déficits que poderiam comprometer o retorno ao esporte ou aumentar o risco de nova lesão. Essa abordagem integrada atende tanto às necessidades de proteção do enxerto nas fases precoces quanto ao objetivo de força e funcionalidade nas fases intermediárias e finais.
Apesar dos avanços, ainda existem limitações importantes na literatura. Muitos estudos apresentam heterogeneidade metodológica, amostras pequenas, diferentes tempos de intervenção e falta de padronização quanto à carga, amplitude de movimento e critérios clínicos para a introdução dos exercícios. Essas limitações dificultam a definição de protocolos universais e reduzem a força das evidências disponíveis.
Portanto, reforça-se a necessidade de ensaios clínicos randomizados, com amostras mais robustas e seguimento a longo prazo, capazes de comparar protocolos isolados e combinados, avaliar o impacto funcional real, a taxa de retorno ao esporte, a prevenção de recidivas e até mesmo o desenvolvimento de artrose precoce. Também é fundamental padronizar critérios para a introdução dos exercícios em CCA, incluindo parâmetros de carga, tempo pós-operatório e amplitude segura, de modo a orientar a prática clínica com maior segurança.
Em conclusão, os exercícios em cadeia aberta e fechada exercem efeitos benéficos e complementares na recuperação de lesões do LCA. Enquanto a CCF se destaca na segurança inicial e no ganho funcional precoce, a CCA é essencial para o fortalecimento do quadríceps e restauração da simetria muscular. A abordagem combinada, respeitando o tempo pós-operatório e critérios clínicos individualizados, apresenta-se como a mais eficaz e aplicável para a reabilitação. Ainda assim, a necessidade de estudos futuros, bem estruturados e de alta qualidade metodológica, é evidente para que se estabeleçam protocolos clínicos mais claros e universais, capazes de otimizar o processo de recuperação e reduzir riscos de complicações a longo prazo.
7. REFERÊNCIAS
ALMEIDA, G. P. L. et al. Tratamento conservador e cirúrgico da lesão do ligamento cruzado anterior: revisão sistemática. Revista Brasileira de Ortopedia, v. 45, n. 3, p. 247–255, 2010.
AMATUZZI, M. M. et al. Reconstrução do ligamento cruzado anterior: indicações e resultados. Acta Ortopédica Brasileira, v. 12, n. 3, p. 155–160, 2004.
ANDRADE, R. et al. Morphological and biomechanical analysis of the knee: implications for ligament injury and reconstruction. Journal of Anatomy, v. 240, n. 1, p. 45–57, 2022.
ANDRADE, R. et al. Neural innervation of the human knee joint: anatomical and clinical aspects. Clinical Anatomy, v. 34, n. 4, p. 556–565, 2021.
ARDERN, C. L. et al. Return to sport following anterior cruciate ligament reconstruction surgery: a systematic review and meta-analysis of the state of play. British Journal of Sports Medicine, v. 45, n. 7, p. 596–606, 2011.
ASTUR, D. C. et al. Psychological factors associated with return to sport after ACL reconstruction. Revista Brasileira de Ortopedia, v. 51, n. 6, p. 647–652, 2016.
BADAWY, W. et al. Rehabilitation following anterior cruciate ligament reconstruction: evidence-based guidelines. Journal of Orthopaedic & Sports Physical Therapy, v. 52, n. 3, p. 164–176, 2022.
BARRETO, R.; SILVA, C.; CUNHA, L. Exercícios em cadeia cinética aberta e fechada na reabilitação do LCA: uma revisão atual. Revista Brasileira de Fisioterapia Esportiva, v. 27, n. 2, p. 112–120, 2023.
BRINLEE, A. W. et al. Return-to-sport criteria after ACL reconstruction: clinical practice guidelines. International Journal of Sports Physical Therapy, v. 17, n. 4, p. 650–661, 2022.
CARTER, T. R. et al. Surgical techniques in ACL reconstruction: outcomes and challenges. Orthopaedic Journal of Sports Medicine, v. 5, n. 2, p. 45–53, 2017.
DE SOUZA, R. A. et al. Protocolos de reabilitação fisioterapêutica pós-lesão do ligamento cruzado anterior: revisão narrativa. Fisioterapia em Movimento, v. 35, e35110, 2022.
ELABD, A.; ELABD, O. Functional rehabilitation after ACL reconstruction: randomized controlled trial. Clinical Rehabilitation, v. 37, n. 1, p. 88–97, 2023.
FITZGERALD, G. K. et al. Open versus closed kinetic chain exercises: implications for ACL rehabilitation. American Journal of Sports Medicine, v. 25, n. 6, p. 823–829, 1997.
FORELLI, L. et al. Early open kinetic chain exercises after ACL reconstruction: a cohort study. Knee Surgery, Sports Traumatology, Arthroscopy, v. 31, n. 2, p. 450–458, 2023.
FORSYKE, D. et al. Psychological readiness to return to sport following ACL reconstruction. British Journal of Sports Medicine, v. 50, n. 13, p. 808–814, 2016.
GLASS, R.; WADDELL, D.; HOOGENBOOM, B. Closed kinetic chain exercises in rehabilitation after ACL reconstruction. North American Journal of Sports Physical Therapy, v. 5, n. 3, p. 125–132, 2010.
GRIFFIN, L. Y. et al. Sex differences in ACL injury: epidemiology and risk factors. Journal of Bone and Joint Surgery, v. 105, n. 4, p. 321–330, 2023.
HASSEBROCK, J. D. et al. Advances in knee joint anatomy and biomechanics. Journal of Orthopaedic Research, v. 38, n. 8, p. 1765–1773, 2020.
HEWETT, T. E. et al. Neuromuscular risk factors for ACL injury in female athletes. American Journal of Sports Medicine, v. 49, n. 9, p. 2451–2460, 2021.
JONES, D. et al. Patellar morphology and Wiberg classification: clinical relevance in knee surgery. Journal of Arthroplasty, v. 35, n. 7, p. 1820–1826, 2020.
KAPANDJI, I. A. Fisiologia articular: esquemas comentados de mecânica humana. 6. ed. Rio de Janeiro: Guanabara Koogan, 2020.
KAPOOR, M.; MAITLAND, M.; KIPPEL, J. Synovial structures of the knee joint: anatomy and clinical aspects. Clinical Anatomy, v. 34, n. 3, p. 355–362, 2021.
KHALID, M. et al. Neuromuscular training for ACL injury: systematic review. Sports Health, v. 14, n. 1, p. 36–45, 2022.
KOPKA, M. et al. Partial remnant preservation versus single-bundle ACL reconstruction: outcomes. Knee Surgery, Sports Traumatology, Arthroscopy, v. 32, n. 1, p. 22–33, 2024.
LAPRADE, R. F. et al. Playing surfaces and ACL injury risk: biomechanical analysis. American Journal of Sports Medicine, v. 49, n. 5, p. 1155–1163, 2021.
LARA, P. H. et al. Advances in ACL reconstruction techniques: autografts, allografts and synthetics. Journal of Experimental Orthopaedics, v. 11, n. 1, p. 78–89, 2024.
LI, Z. et al. Aquatic therapy in ACL rehabilitation: randomized controlled trial. Journal of Physical Therapy Science, v. 33, n. 12, p. 1005–1011, 2021.
LIU, J. et al. Surgical and conservative management of ACL injuries: current perspectives. Journal of Clinical Orthopaedics and Trauma, v. 11, n. 5, p. 789–795, 2020.
MIKKELSEN, C.; WERNER, S.; ERICKSON, B. Closed kinetic chain exercises in ACL rehabilitation: clinical benefits. Scandinavian Journal of Medicine & Science in Sports, v. 10, n. 1, p. 30–35, 2000.
MILLER, R. M. et al. Tibial plateau morphology and ACL injury risk. Journal of Bone and Joint Surgery, v. 102, n. 9, p. 812–819, 2020.
MOTA, R. C. et al. Return to sport after ACL reconstruction: systematic review. Knee Surgery, Sports Traumatology, Arthroscopy, v. 32, n. 4, p. 895–905, 2024.
MUNHOZ, F. B. et al. Mecanismos de lesão do LCA: revisão narrativa. Revista Brasileira de Ortopedia, v. 57, n. 2, p. 123–130, 2022.
NETTER, F. H. et al. Atlas de anatomia humana. 8. ed. Rio de Janeiro: Elsevier, 2021.
OLIVEIRA, R. C. et al. Meniscal injuries: anatomy and biomechanics. Revista Brasileira de Ortopedia, v. 55, n. 1, p. 45–52, 2020.
PAMBORIS, E. et al. Open versus closed kinetic chain exercises after ACL reconstruction: systematic review and meta-analysis. Sports Medicine, v. 54, n. 2, p. 225–238, 2024.
ROSS, M. D.; DENEGAR, C. R.; WINZENRIED, S. J. Quadriceps recovery following ACL reconstruction: comparison of OKC and CKC training. Journal of Orthopaedic & Sports Physical Therapy, v. 31, n. 9, p. 482–488, 2001.
SANTOS, A. et al. Meniscal function and injury: a biomechanical review. Revista Brasileira de Ortopedia, v. 55, n. 6, p. 635–642, 2020.
SHULTZ, S. J. et al. Quadriceps-hamstring coactivation and ACL loading. Journal of Athletic Training, v. 43, n. 4, p. 356–362, 2008.
SILVA, G. A. et al. Reabilitação precoce após reconstrução do LCA: aspectos neuromusculares. Fisioterapia em Movimento, v. 33, e33304, 2020.
SMITH, J. D. et al. Femoral condyle morphology and implications for ACL injury. Clinical Orthopaedics and Related Research, v. 478, n. 2, p. 345–353, 2020.
SONNERY-COTTET, B. et al. Playing surface and ACL injuries: NFL data. American Journal of Sports Medicine, v. 49, n. 11, p. 3015–3023, 2021.
TANG, X. et al. Vascular supply of the knee joint: anatomical and clinical relevance. Anatomical Science International, v. 97, n. 2, p. 185–193, 2022.
TAGESSON, S. et al. Strength recovery in ACL rehab: OKC versus CKC training. Scandinavian Journal of Medicine & Science in Sports, v. 18, n. 1, p. 20–27, 2008.
TORZILLI, P. A.; DENG, X.; WARREN, R. F. Biomechanical basis of ACL rehabilitation: shear forces in open chain exercises. American Journal of Sports Medicine, v. 22, n. 1, p. 67–72, 1994.
TRINDADE, R. C. et al. Reabilitação conservadora do LCA: revisão narrativa. Revista Brasileira de Ortopedia, v. 55, n. 3, p. 234–241, 2020.
WAKEFIELD, J. R. et al. ACL injury epidemiology: global perspective. Sports Medicine and Arthroscopy Review, v. 29, n. 4, p. 235–243, 2021.
WANG, H. et al. In vivo analysis of ACL graft deformation during rehabilitation exercises. Knee Surgery, Sports Traumatology, Arthroscopy, v. 31, n. 6, p. 2103–2112, 2023.
WEBSTER, K. E. et al. Outcomes of ACL reconstruction: systematic review. Sports Medicine, v. 48, n. 2, p. 181–192, 2018.
ZHANG, J. et al. Advances in imaging and anatomy of the knee joint. Journal of Orthopaedic Surgery and Research, v. 15, n. 1, p. 320–329, 2020.
Acadêmicos do curso de Fisioterapia – UniCV*
Mestre e docente do curso de Fisioterapia – UniCV**. E-mail: prof_gustavomoreno@unicv.edu.br
