OSTEONECROSE DOS MAXILARES EM PACIENTES SUBMETIDOS A TERAPIA COM BIFOSFONATOS: REVISÃO DE LITERATURA
REGISTRO DOI: 10.69849/revistaft/cs10202502241420
Beatriz Kely Pereira Gomes1; Larissa Francielly Andrade Mateus da Silva2; Darlan Kelton Ferreira Cavalcante3; João Vitor Palma Wilke4; Nicole Machado Grisa5; Fernando Becklin da Silva6; Emerson Gonçalves de Arandas Viana dos Santos7; Isabelly Barcellos Daleprane8; Emanoel Felipe Albuquerque de Andrade9; Clebeson André da Silva10
RESUMO
Introdução: Os bifosfonatos são uma classe de medicamentos amplamente administrados a pacientes portadores de metástase óssea de tumores sólidos, osteoporose, osteopenia, dentre outras lesões ósseas. Essas drogas agem alterando a dinâmica de reabsorção óssea, por induzir apoptose dos osteoclastos, interferindo na redução da porosidade e vascularização óssea, podendo potencializar uma necrose avascular óssea, mas comumente denominada osteonecrose. Objetivo: O presente estudo visa desenvolver uma revisão de literatura a respeito da identificação, prevenção e tratamento da osteonecrose dos maxilares em pacientes que recebem terapia com fármacos da classe dos bifosfonatos. Metodologia: Para isso, foi desenvolvida uma estratégia de busca aplicada nas bases de dados: PubMed, SciELO e LILACS, nas línguas portuguesa e inglesa entre o período abrangido pela pesquisa de 2008 a 2024. Foram incluídas revisões sistemáticas, relatos de casos, estudos observacionais, bem como, ensaios clínicos. Como critérios de exclusão encontram-se trabalhos fora do período abrangido pela pesquisa, bem como, artigos que não se propusessem a explanar as informações requeridas. Resultados e Discussão: Os autores sustentam que não há um padrão ouro para tratamento da osteonecrose, e que as opções são descritas de acordo com o estadiamento da AAOMS, dentre elas destaca-se o controle da dor, desbridamento cirúrgico ou ressecção e laser de baixa intensidade, bem como, a utilização do ozônio em combinação com antibioticoterapia associada ao tratamento cirúrgico. Diante disso, maximizar a qualidade de vida dos pacientes deve ser característica fundamental e imprescindível de todo protocolo que exija tratamento para BRONJ, e que a abordagem adjuvante das modalidades de tratamento citadas é a alternativa mais viável. Conclusão: Conclui-se que, a BRONJ apresenta-se como uma complicação relativamente rara, entretanto nociva, primordialmente quando administrado por via endovenosa. Assim sendo, o cirurgião dentista mostra-se como profissional essencial contíguo à equipe multidisciplinar, abordando educação em saúde, bem como eliminando possíveis focos infecciosos ou potencialmente irritativos.
Palavras-Chaves: Osteonecrose dos Maxilares, Terapia com Bifosfonatos, Osteonecrose induzida por drogas.
ABSTRACT
Introduction: Bisphosphonates are a class of drugs widely administered to patients with bone metastases from solid tumors, osteoporosis, osteopenia, among other bone lesions. These drugs act by altering the dynamics of bone resorption by inducing osteoclast apoptosis, interfering in the reduction of bone porosity and vascularization, and may potentiate avascular bone necrosis, commonly called osteonecrosis. Objective: The present study aims to develop a literature review on the identification, prevention, and treatment of osteonecrosis of the jaw in patients receiving therapy with drugs from the bisphosphonate class. Methodology: For this purpose, a search strategy was developed applied to the databases: PubMed, SciELO, and LILACS, in Portuguese and English between the period covered by the research from 2008 to 2024. Systematic reviews, case reports, observational studies, as well as clinical trials were included. Exclusion criteria were studies outside the period covered by the research, as well as articles that did not intend to explain the required information. Results and Discussion: The authors argue that there is no gold standard for the treatment of osteonecrosis, and that the options are described according to the AAOMS staging, among which are pain control, surgical debridement or resection and low-intensity laser, as well as the use of ozone in combination with antibiotic therapy associated with surgical treatment. Therefore, maximizing the quality of life of patients should be a fundamental and essential characteristic of any protocol that requires treatment for BRONJ, and that the adjuvant approach of the aforementioned treatment modalities is the most viable alternative. Conclusion: It is concluded that BRONJ presents itself as a relatively rare complication, however harmful, primarily when administered intravenously. Therefore, the dentist is an essential professional in the multidisciplinary team, addressing health education, as well as eliminating possible infectious or potentially irritating foci.
Keywords: Osteonecrosis of the Jaw, Bisphosphonate Therapy, Drug-induced Osteonecrosis.
1. Introdução
Os bifosfonatos são uma classe de medicamentos amplamente administrados a pacientes portadores de metástase óssea de tumores sólidos, osteoporose, osteopenia, doença de paget, mieloma múltiplo, dentre outras lesões ósseas (Rajeshwaree et al., 2023). Esses medicamentos são comumente prescritos para prevenção e tratamento de uma variedade de outras condições esqueléticas, como baixa densidade óssea e osteogênese imperfeita (Drake et al., 2008). Também denominadas de anti-reabsortivos ósseos, eles contêm uma estrutura semelhante ao pirofosfato nativo e dividem-se em dois grupos: bifosfonatos contendo e não contendo nitrogênio (Kim et al., 2020).
Há uma ampla variedade de drogas a base de bifosfonatos, sendo alguns administrados por via intravenosa (IV) (pamidronato, ácido zoledrônico, clodronato) e alguns administrados por via oral (alendronato, etidronato, risedronato, tiludronato, ibandronato). Suas indicações geralmente sobressaem ao tipo de condição clínica a ser tratada (Kim et al., 2020).
No entanto, essa classe de medicamentos age alterando a dinâmica de reabsorção óssea, por induzir apoptose dos osteoclastos (Jaeger, Menezes 2022). Os bifosfonatos mostram-se potentes inibidores da atividade osteoclástica, motivo pelo qual são geralmente prescritos. Dependendo da duração do tratamento e do tipo específico de bifosfonato prescrito, a substância pode permanecer no corpo por anos (Rodrigues, Sanchez 2016). Todavia, os osteoblastos e os osteócitos irão continuar sintetizando matriz óssea reduzindo a porosidade e a vascularização da periferia óssea, podendo potencializar uma necrose avascular óssea, mas comumente denominada de osteonecrose (Ruocco et al., 2023).
Atualmente, é reconhecido que os procedimentos odontológicos mais invasivos estão intimamente ligados à prevalência da osteonecrose dos maxilares, sendo a exodontia o principal procedimento associado ao surgimento dessa patologia. Desse modo, a prevenção da osteonecrose dos maxilares emerge como uma prioridade no cuidado de pacientes que estão prestes a iniciar, estão em andamento ou concluíram a terapia com medicamentos antirreabsortivos ósseos (Ruggieiro, 2022). Assim sendo, este trabalho tem por objetivo realizar uma revisão de literatura para compreender as complicações causadas pelo uso desses fármacos, associado à realização de procedimentos invasivos em pacientes odontológicos.
2. Objetivos
2.1 Objetivo Geral
Compreender a incidência de osteonecrose em pacientes que fazem uso de bifosfonatos, e que necessitam de procedimentos odontológicos invasivos; bem como as possíveis abordagens preventivas a essa complicação.
2.2 Objetivos Específicos
• Relatar o mecanismo de ação dos fármacos da classe dos bifosfonatos e suas indicações terapêuticas;
• Identificar as reações adversas de interesse para odontologia em pacientes que fazem uso de bifosfonatos;
• Estimar a importância da anamnese suscinta, e abordagem multidisciplinar a fim de executar o manejo preventivo na abordagem de procedimentos odontológicos em pacientes de risco para osteonecrose por bifosfonatos;
• Avaliar os riscos e benefícios da realização de procedimentos invasivos em pacientes que fazem uso de bifosfonatos e o tratamento empregado em caso de osteonecrose.
3. Metodologia
O presente estudo trata-se de uma revisão narrativa da literatura. Para isso, foi realizada uma estratégia de busca de artigos, nas seguintes bases de dados eletrônicas: Scientific Electronic Library Online (SciELO), US National Library of Medicine (Pubmed) e LILACS.
Para a estratégia de busca foram utilizados os descritores “osteonecrose dos maxilares “, “terapia com bifosfonatos” e “osteonecrose induzida por medicamento”, e seus sinônimos, combinados com os operadores booleanos “AND” e/ou “OR”.
Como critérios de inclusão, foram selecionados artigos, sem restrição de idiomas, publicados entre os anos de 2008 e 2024; que trouxessem evidências científicas a respeito dos bifosfonatos, incluindo suas indicações, efeitos adversos, manejos preventivos e/ou tratamentos empregados quando necessário. Foram incluídas revisões sistemáticas, relatos de casos, estudos observacionais e ensaios clínicos.
Foram excluídos artigos e trabalhos publicados fora do período proposto, trabalhos onde apenas houvesse informações a respeito de osteonecrose causada por outros meios que não associada ao uso de bifosfonatos (não relevantes para a pesquisa), bem como artigos que não se propusessem a explanar as informações requeridas, como comentários, resumos expandidos, anais de congressos, cartas ao editor e artigos em duplicata.
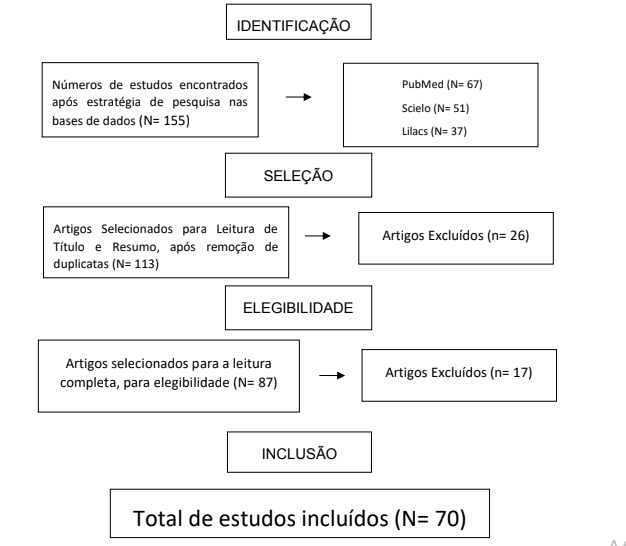
Após leitura dos títulos e resumos, conforme os critérios de inclusão e exclusão, os artigos elegíveis foram selecionados para leitura na íntegra, por dois pesquisadores independentes. Em caso de não concordância, reunião com um terceiro pesquisador independente foi utilizada para fechar a seleção dos artigos elegíveis. Os dados foram sumarizados na tabela de Excel com os principais achados dos artigos. O fluxograma dos artigos selecionados está anexado na figura 1 deste trabalho.
Figura 1 – Fluxograma dos estudos contemplados na amostra da pesquisa.
4. Fundamentação Teórica
4.1 Bifosfonatos
Desde sua introdução na prática clínica há mais de 4 décadas, os bifosfonatos têm sido cada vez mais utilizados para uma série de alterações esqueléticas. São atualmente utilizados para tratar condições tão variadas como distúrbios esqueléticos hereditários em crianças (GIO), bem como, metástases ósseas em pacientes com neoplasias (Drake et al., 2008).
Agentes antirreabsortivos como os bifosfonatos (BP) são pirofosfatos inorgânicos que diminuem o turnover ósseo e são usados para reduzir ou retardar eventos relacionados ao esqueleto, como fraturas em pacientes com lesões líticas metastáticas, hipercalcemia de malignidade, mieloma múltiplo (MM), doença de Paget, osteopenia e osteoporose (Bansal H, 2022).
Os bifosfonatos mostram-se potentes inibidores da atividade osteoclástica, motivo pelo qual são geralmente prescritos. Dependendo da duração do tratamento e do tipo específico de bifosfonato, a substância pode permanecer no corpo por anos (Lozano, Sanchez 2016).
Todavia, quando o osso que contém fármaco à base de bifosfonato reabsorve, uma parte da medicação é liberada e recirculada localmente e sistemicamente, fixando-se novamente a outras superfícies e inibindo a reabsorção óssea. Essa retenção de bifosfonato no tecido ósseo explica a lenta perda óssea após a descontinuação da terapia, pois a droga pode ficar retida por até 10 anos na matriz óssea (Madeira et al., 2020). Julgar necessário que a suspensão da medicação por um determinado período, a fim de evitar complicações pós cirúrgicas não é totalmente eficaz.
O uso prolongado de terapia antirreabsortiva chamou a atenção para dois eventos adversos extremamente raros, embora graves. Sendo eles, fratura atípica do fêmur e osteonecrose da mandíbula relacionada a medicamentos, que são mais comuns em pacientes com altas doses cumulativas e maior duração da terapia (Gehrke et al., 2024).
Os bifosfonatos podem ser tomados por via intravenosa (IV) ou oral. Podendo ser classificados como não nitrogenados, mas comumente os clodronato, etidronato e o tiludronato de (1 geração) e os nitrogenados sendo eles, alendronato, incandronato, ibandronato e pamidronato de (2 geração), bem como, risedronato e ácido zoledrônico de (3 geração). Vale ressaltar que os bifosfonatos nitrogenados possuem maior potência terapêutica, devido ao nitrogênio não ser metabolizado, permitindo assim uma maior retenção ao tecido ósseo. O desenvolvimento de MRONJ pode ocorrer durante ou após o tratamento com fármacos da classe dos bifosfonatos (Lo JC, et al., 2010).
4.2 Osteonecrose
A osteonecrose pode ser um efeito colateral medicamentoso do tratamento de doenças ósseas malignas e benignas com bifosfonatos (Bp), bevacizumabe e denosumabe (Dmab) como terapia antirreabsortiva. A incidência da osteonecrose dos maxilares é maior na população de pacientes oncológicos (variação de 1-15%), onde altas doses desses medicamentos são usadas em intervalos frequentes. Na população de pacientes com osteoporose, a incidência de ONMS é estimada em 0,001-0,01%, marginalmente maior do que a incidência na população geral (<0,001%). Outros fatores de risco para o desenvolvimento da osteonecrose incluem uso de glicocorticoides, cirurgia óssea maxilar ou mandibular, higiene oral deficiente, inflamação crônica, diabetes mellitus, próteses mal adaptadas, bem como outras drogas, incluindo agentes antiangiogênicos (Svejda et al., 2016).
Curiosamente, a ONMB é primariamente limitada à região maxilofacial. Ao contrário de outros ossos esqueléticos, os ossos da mandíbula (processo alveolar e periodonto) possuem vascularização, turnover ósseo e remodelação relativamente altos devido ao estresse mecânico contínuo, o que pode torná-los vulneráveis aos efeitos adversos das drogas (Ruggiero, 2014).
Diversas são as características que fazem da cavidade oral um ambiente propício ao desenvolvimento desta condição. Uma fina camada de periósteo recobre o osso alveolar tanto na mandíbula quanto na maxila com uma camada atenuada de tecido conjuntivo. A mandíbula é uma área de alto turnover ósseo, devido à presença de dentes e ao remodelamento diário ao redor do ligamento periodontal, as estruturas bucais estão sujeitas a vários estresses. Estes são fisiológicos na forma de mastigação, iatrogênicos na forma de vários procedimentos dentários, ou inflamatórios na forma de doenças periodontais. Esses fatores levam a trauma da mucosa, exposição óssea e aumento da remodelação óssea (Aghaloo T, 2015).
Além disso, uma complexa flora microbiana patogênica coloniza a cavidade oral e os dentes. O microtrauma durante a mastigação leva a um possível portal de entrada para a flora microbiana patogênica e outros produtos inflamatórios no osso subjacente (Guarneri et al., 2010).
De acordo com a definição de caso fornecida pela Sociedade Americana de Pesquisa Mineral e Óssea e pela Associação Americana de Cirurgiões Bucomaxilofaciais, os indivíduos podem ser considerados portadores de ONMB se todas as seguintes características estiverem presentes: (i) tratamento atual ou prévio com agentes antirreabsortivos ou antiangiogênicos, (ii) osso exposto ou necrótico na região maxilofacial que não cicatrizou (por intenção primária ou secundária) dentro de oito semanas após a identificação por um serviço de saúde, (iii) nenhuma história de radioterapia para os maxilares e (iv) nenhuma evidência de doença metastática para os maxilares (Sigua et al., 2014).
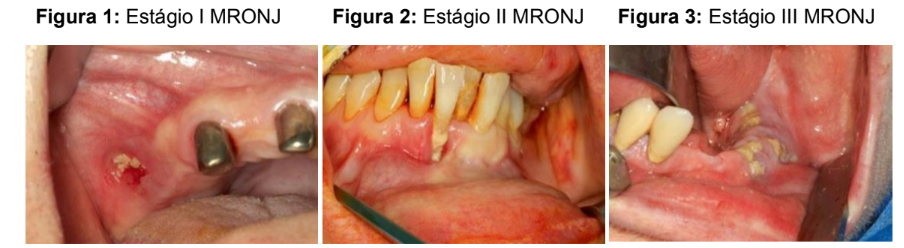
A ONMB foi dividida em quatro estágios (Tabela 1) com base nos sintomas clínicos, além disso, os pacientes são classificados de risco quando não houver osso necrótico exposto aparente em pacientes que foram tratados com antirreabsortivos IV ou VO, entretanto esses pacientes devem ser informados sobre o risco de desenvolver ONMB e sobre os sinais e sintomas desse processo patológico. O estágio 0 descreve indivíduos com doença prodrômica (variante não exposta). A exposição óssea é comum em indivíduos com ONM estágio 1 a 3 (Figuras 1, 2 3) sendo, assintomáticos e sem evidência de infecção (estágio 1), sintomático e com evidência de infecção (estágio 2), ou com infecção, bem como fratura patológica ou fístula e evidência de osteólise estendendo-se para a borda inferior da mandíbula ou assoalho do seio (estágio 3) (Ruggiero 2014; Sigua-Rodriguez 2014; Vescovi 2012).
Diante disso, a ONMB consiste em osso necrótico cronicamente exposto, em região oral e maxilo facial, que persiste por mais de 08 semanas, que em geral costuma ser dolorosa e infectada. Os sinais objetivos além da dor na mandíbula e cavidade oral são dentes soltos, inchaço gengival, ulceração e parestesia no território dos ramos do nervo trigêmeo (Sharma et al., 2023).
Tabela 1 – Estadiamento da Osteonecrose dos Maxilares Relacionada a Bisfosfonatos. Baseado nas recomendações da American Association of Oral & Maxillofacial Surgeons.
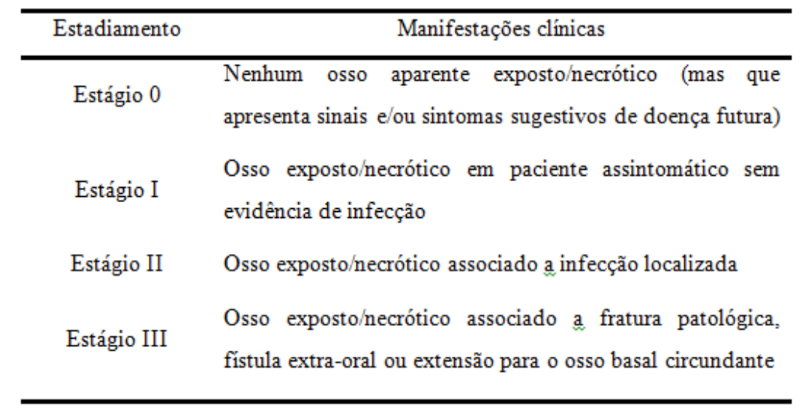
Os fatores de risco clínicos para o desenvolvimento da ONMB abrangem uma variedade de características relacionadas ao paciente e ao tratamento. Entre os fatores de risco odontológicos, a extração dentária foi considerada o risco mais proeminente, seguida pela doença periodontal (McGowan et al., 2018). Condições infecciosas ou inflamatórias orais pré-existentes, incluindo infecções periapicais, também elevam o risco de ONMB (Chun Lei et al., 2016).
Desse modo, a exposição de osso necrótico pode ocorrer de forma espontânea ou mais comumente após procedimentos odontológicos invasivos, geralmente os pacientes queixam-se de halitose e dificuldade para se alimentar e falar. As lesões são persistentes e não respondem a modalidades convencionais de tratamento como desbridamento, terapia antibiótica ou terapia por HBO (Sharma et al., 2023).
4.3 Medidas Preventivas
Embora inúmeros estudos sobre a patologia venham sendo realizados, em levantamento da literatura, foi constatado a falta de conhecimento dela por cirurgiões dentistas, médicos e pacientes (Senturk et al., 2016).
Segundo Senturk et al. (2016) o grande desafio é que oncologistas e dentistas não costumam trabalhar em parceria quando o diagnóstico do paciente é relacionado à osteonecrose induzida por medicação (MRONJ). Os autores consideraram importante aumentar a conscientização dos oncologistas sobre a doença, pois, é primordial que seja realizada uma abordagem multidisciplinar para o sucesso do tratamento.
A abordagem multidisciplinar de conscientização levaria a prevenção de complicações e melhoria da qualidade de vida, partindo pelo pressuposto de que o segredo não está relacionado ao tratamento, mas sim identificar o paciente que faz uso da medicação e atuar de maneira preventiva (Jaeger , Menezes 2023).
A osteonecrose é uma complicação relativamente rara, entretanto nociva e medidas terapêuticas consistentes eficazes ainda não foram identificadas, entretanto, isso representa um dilema tanto para o paciente quanto para o cirurgião-dentista. A prevenção dessa condição é, portanto, fundamental para esses pacientes, de modo que possam receber as terapias antineoplásicas de que necessitam (Ruggiero, 2014).
No entanto, dentistas bem-informados são essenciais para identificar riscos, tomar decisões clínicas apropriadas e educar os pacientes sobre as precauções necessárias, o que não apenas melhora o atendimento odontológico, mas também contribui para a saúde geral dos pacientes, evitando complicações indesejadas (Rocha et al., 2024).
Medidas preventivas devem ser consideradas e incluem educação do paciente, boa higiene oral, exame odontológico clínico de rotina a cada três ou quatro meses, avaliação visual concisa da cavidade oral em cada consulta de acompanhamento e uma radiografia panorâmica para detectar possíveis doenças dentárias e periodontais. Além das medidas preventivas conservadoras antes de iniciar o tratamento, qualquer procedimento odontológico ou cirúrgico eletivo que comprometa as superfícies mucosas ou a exposição óssea que não possa se recuperar totalmente antes de iniciar a terapia com bifosfonatos deve ser evitado. Entretanto, se a terapia com fármacos anti-reabsortivos ósseos puderem ser adiados brevemente sem risco, nesse caso, dentes com prognóstico ruim ou que precisam de extração devem ser extraídos, cirurgias odontológicas adicionais devem ser concluídas e os tecidos devem ser deixados cicatrizar completamente antes de iniciar o tratamento com bifosfonatos (Wan et al., 2020).
Em circunstâncias clínicas, ao postergar o uso de bifosfonatos, os riscos ou benefícios da terapia ainda precisam ser avaliados sistemicamente. Assim, o oncologista assistente deve decidir adiar o tratamento com bifosfonatos em consulta com um especialista em odontologia. O Cirurgião-Dentista deve verificar cuidadosamente as próteses removíveis quanto ao seu potencial para causar lesões nos tecidos moles, particularmente o tecido que sobrepõe o osso, e ajustar se necessário. A terapia endodôntica é preferível às extrações para eliminar amputações coronais, seguida de tratamento de canal nas raízes retidas para evitar a extração dentária e o potencial desenvolvimento de osteonecrose (Wan et al., 2020).
4.4 Tratamento da Osteonecrose Mediada por Bifosfonatos
Apesar das evidências crescentes dos riscos da realização de procedimentos odontológicos que englobem a realização de manipulação óssea em pacientes submetidos à terapia com bifosfonatos, porventura surge a necessidade da realização de tais procedimentos. Portanto, a necessidade de identificar protocolos de tratamento que possam reduzir a incidência dessa síndrome oral “recém-reconhecida” é cada vez mais pertinente (Mozzati et al., 2012).
Consequentemente, protocolos cirúrgicos que favoreçam os processos de cicatrização óssea e mucosa e, ao mesmo tempo, limitem o dano cirúrgico a níveis mínimos, devem ser pesquisados e adotados para pacientes sobre terapia com bifosfonatos. Entretanto, a eficácia de um tratamento depende da via de administração, da concentração, do tratamento e da frequência de uso do medicamento (Boff et al., 2014).
Segundo Gil et al. (2019) existem algumas possibilidades de tratamentos tais como; terapia conservadora, cirurgia minimamente invasiva, tratamento médico + cirurgia minimamente invasiva, cirurgia de grande porte (ressecção), terapia fotodinâmica, fatores de crescimento (PRGF ou proteína morfogenética óssea), e tratamento com ozônioterapia. No entanto, não há evidências científicas claras que estabeleçam qual tratamento usar, dependendo do tamanho da lesão, localização, tipo de bifosfonato (oral ou intravenovo) e/ou outras patologias associadas.
4.4.1 Terapia Conservadora
O manejo da terapia conservadora da BRONJ visa melhorar o estágio da doença e evitar sua progressão, vale ressaltar que o controle da dor é o objetivo principal. As opções não cirúrgicas incluem o uso de enxaguatórios bucais antimicrobianos (bochechos com digluconato de clorexidina 0,12%), desinfecção/limpeza local de ossos e fístulas expostas, controle da dor e administração de antibióticos, além do suporte nutricional quando necessário. Na presença de osso exposto, o desbridamento superficial pode ser útil para reduzir as bordas afiadas e aliviar a irritação dos tecidos moles. Mesmo quando o tratamento cirúrgico é indicado, o manejo não cirúrgico antes e depois da cirurgia (ou seja, durante o período perioperatório) é fundamental para ser realizado (Kishimoto et al.,2019).
Ruggiero et al. (2009), propuseram terapêuticas distintas baseadas nos estágios de evolução das MRONJ, sendo o primeiro e segundo estágio tratados com abordagens conservadoras. Os autores preconizaram que no primeiro estágio fossem realizados bochechos antimicrobianos de clorexidina 0,12%, e instruções de higiene bucal, o segundo estágio representa a maioria dos casos relatados em cerca de (67%) e dentro desse número de pacientes cerca de 75% apresentaram estabilidade ao utilizar a clorexidina associada a antibioticoterapia, determinada tanto pela cultura do osso quanto pelo exsudato. Em casos resistentes podem requerer administrações maiores do antibiótico ou antibioticoterapia endovenosa. Além disso, deve ser realizada a remoção de quaisquer fragmentos ósseos soltos e o desbridamento da área afetada para promover cicatrização adequada.
Segundo Ristow et al. (2019), em seu estudo retrospectivo foi analisada a eficiência do tratamento conservador não cirúrgico em lesões de MRONJ estágio 1 após terapia com bifosfonatos. Setenta e cinco pacientes com 92 lados lesionados foram avaliados e tratados com solução de digluconato de clorexidina 0,12% e aplicação tópica diária de gel de clorexidina 1%. Para controle da limpeza manual da área afetada, consultas de acompanhamento foram realizadas a cada 4 semanas. A integridade da mucosa foi apresentada em apenas 8 das 92 (8,7) lesões sem sinais de infecção residual durante o período de acompanhamento, ao passo que 84 das 92 lesões (91,3%) prosseguiram com o maxilar exposto. O estágio de piora ocorreu em 79,8% das lesões sem integridade da mucosa, evoluindo para indicação de procedimentos mais invasivos em 57 lesões.
No entanto, o tratamento conservador pode proporcionar alívio temporário, minimizando os sintomas e as infecções, mas não implica na resolução definitiva da osteonecrose (Coropciuc et al., 2017). Para controle dos sintomas, a terapia conservadora não cirúrgica no tratamento das lesões de ONMB deve ser restrita a pacientes que não desejam se submeter à cirurgia ou cujo estado geral não permite intervenção cirúrgica (Ristow et al., 2019).
4.4.2 Terapia Cirúrgica
Segundo a AAOMS, o estadiamento da MRONJ conforme o quadro 1 representado pelo estágio 3 da doença, beneficia-se da terapia cirúrgica. Além da utilização do antibacteriano, enxaguatório bucal, antibioticoterapia e controle da dor, o desbridamento cirúrgico ou ressecção têm se mostrado eficazes.
Entretanto, independentemente do estágio da doença, o sequestro ósseo móvel deve ser removido para facilitar a cicatrização dos tecidos moles. A extração de dentes sintomáticos dentro do osso necrótico exposto deve ser considerada, pois é improvável que a extração exacerba o processo necrótico estabelecido (Ruggiero et al., 2014).
De acordo com Carlson e Basile (2009), os pacientes com MRONJ tratados através de intervenções cirúrgicas, demonstraram taxa de sucesso de 90%, com manutenção estável do fechamento da mucosa.
No entanto, a remoção do osso necrótico se torna uma abordagem fundamental no tratamento da MRONJ, porém as ressecções cirúrgicas são procedimentos altamente invasivos, e pacientes com a doença avançada, sobretudo estágio 3 podem não tolerar essas operações (Sahin, 2022).
Segundo Pavlíková et al. (2011), uma alternativa potencial seria a utilização da cirurgia piezoelétrica ultrassônica com enxaguatórios bucais para auxiliar na remoção do osso necrótico. A Piezocirurgia possibilita a remoção do osso necrótico com trauma minimizado, o que pode favorecer a eliminação da necessidade de procedimentos invasivos de ressecção com serras e instrumentos rotatórios. Além disso, a piezocirurgia permite manter a continuidade do osso vital, o que pode ser benéfico para o sucesso do tratamento da osteonecrose, bem como, pela presença de efeitos bactericidas.
Sahin et al. (2022), propôs a abordagem de tratamento em estágios avançados da osteonecrose, onde foi realizado a exposição da área necrótica através de incisões na crista óssea estendendo-se em ambos os lados da lesão, as fístulas e a deiscência da mucosa também foram incluídas na linha de incisão. Os limites do desbridamento foram determinados pela exposição de sangramento do osso saudável. O osso necrótico foi então removido por meio de cirurgia óssea piezoelétrica ultrassônica, seguidas pela remoção de bordas ósseas afiadas. Diante disso, o tratamento cirúrgico em pacientes com osteonecrose da mandíbula relacionada a medicamentos em estágios avançados tem-se apresentado resultados positivos, principalmente após remoção cirúrgica da área necrótica e aplicação de material de regeneração óssea e de tecidos moles (Seluki et al., 2023).
4.4.3 Fotobiomodulação
Segundo Moreira (2020), a terapia de fotobiomodulação (laserterapia de baixa potência) nada mais é que o uso terapêutico da luz (laser ou led) absorvida pela célula, desencadeando reações não-térmicas, não citotóxicas e biológicas por meio de eventos fotoquímicos ou fotofísicos, levando a modulação da inflamação, reparação tecidual, angiogênese, analgesia e redução antimicrobiana.
Apesar de ser muito utilizado Mobaddere et al. (2023) e Nica et al. (2021) afirmam que o tratamento por meio da fotobiomodulação (FBM) tem seu mecanismo de ação ainda um tanto obscuro. Porém presume-se que ocorre uma absorção da luz por cromóforos específicos da célula, gerando estímulos.
Pontes (2022) afirma que, a fotobiomodulação utiliza uma luz através de lasers de baixa potência em comprimento de onda com intuito de estimular respostas celulares. Essa irradiação de luz tem capacidade de interagir com as células, de maneira que não cause danos, promovendo reparo tecidual, diminuindo a inflamação, e até mesmo estimulando a analgesia.
De acordo com Ribeiro et al. (2018), a laserterapia de baixa potência tem-se apresentado resultados positivos ao manejo da osteonecrose, entretanto, tem-se maior eficácia quando associada a outras modalidades de tratamento como plasma rico em plaquetas, antibioticoterapia, e até mesmo o desbridamento cirúrgico.
4.4.4 Terapia Fotodinâmica
A terapia fotodinâmica antimicrobiana (aPDT) é baseada em uma aplicação tópica de veículo corante que seja fotossensibilizador, e em seguida aplicado uma luz, em um comprimento de onda de 630-880nm. A luz por sua vez, gera estímulo ao agente fotossensibilizador que absorve e consequentemente gera as espécies reativas de oxigênio (ROS). Essas espécies possuem citotoxidade elevada aos micro organismos corados pelo fotossensibilizador. Comumente é utilizado o azul de metileno como corante na aPDT, mas também pode ser utilizado azul de toluidina, ambos possuem características físico-químicas semelhantes (Poli et al., 2018; Evorlino et al.,2019; Poli et al., 2019).
A aPDT, vem sendo uma terapêutica alternativa para tratamento da osteonecrose, obtendo-se como vantagem a aplicação de maneira menos invasiva, tendo capacidade de provocar a morte dos micro-organismos sem gerar resistência microbiana e sem gerar efeitos colaterais (Ribeiro et al., 2018; Tartaroti et al., 2020).
Além disso, possuem atividade não apenas nas bactérias gram-negativas como também nas gram-positivas, bem como vírus, parasitas e fungos (Poli et al., 2019). É evidenciado melhores resultados quando realizados várias aplicações de aPDT (Tartaroti et al., 2020), além de favorecer o reparo do processo alveolar (Ervolino et al., 2019). Como também, pode servir como alternativa de prevenção para reduzir os riscos de desencadeamento da necrose avascular óssea (Ervolino et al., 2019; Poli et al.,2018).
Ervolino et al. (2019), realizou um estudo com 28 ratos, onde foi avaliado a terapia fotodinâmica como prevenção de osteonecrose. Os ratos foram submetidos a administração da medicação, mas precisamente o ácido zoledrônico (zometa) a cada três dias, durante sete semanas. As mesmas foram então submetidas a três sessões de aPDT após realização de remoção dos elementos dentários. Os autores concluíram que em três sessões de aPDT (dias 0, 2 e 4 pós exodontia) houve resultados positivos no processo de reparo alveolar como também prevenir o desenvolvimento da osteonecrose.
Tartaroti et al. (2020), avaliaram 17 pacientes já diagnosticados com osteonecrose, onde foram submetidos a terapia com antibiótico por um período de sete dias. Como medidas para prevenir osteonecrose, antes do procedimento de exodontia, o paciente recebia terapia fotodinâmica. Como forma de tratamento, o paciente recebeu aPDT no pré-operatório, e até que os sinais e sintomas de infecção fossem minimizados. Então, após retirada do tecido ósseo necrótico, foi aplicado a aPDT 01 vez por semana, até presença de sinais de cicatrização. Os autores observaram que 16 (94%) dos pacientes diagnosticados com a patologia e que foram submetidos ao protocolo de aPDT e fotobiomodulação demonstraram regressão total das lesões. Também foi revelado que houve alívio da dor e redução da halitose, já nas primeiras sessões de aPDT.
4.4.5 Plasma Rico em Plaquetas (L- PRF)
O L-PRF é uma matriz cicatricial autóloga e foi considerada um aglomerado de plaquetas de segunda geração, devido sua técnica não necessitar do uso de anticoagulantes ou trombinas (ou outro agente de geilificação) como também apresentar capacidade de estimular a proliferação celular, remodelação da matriz e angiogênese (Costa et al., 2018).
O L-PRF é o novo conceito de cicatrização do tecido fisiológico, trata-se de um biomaterial autólogo derivado de uma amostra do sangue do próprio paciente em um volume de aproximadamente 10 mL, sem adicionar nenhum componente que acelere a cicatrização, remodelação e a cura de tecidos moles ou duro. A ausência de aditivos para a não coagulação do sangue torna o processo mais rápido, o que promove a ativação plaquetária e o processo quase que de forma imediata da formação da cascata de coagulação (Viana et al., 2019).
De acordo com Viana et al. (2019), a amostra de sangue é colocada em uma centrífuga de imediato após a coleta, podendo permanecer por 10 minutos em 3000rpm ou por 12 minutos em 2700rpm. No tubo onde foi armazenado a amostra, é possível observar a coagulação em camadas, no fundo se localiza o plasma acelulado, no meio uma camada com coágulo de fibrina ou fibrinogênio e em cima glóbulos vermelhos.
A membrana está se tornando cada vez mais popular no âmbito odontológico, estando presente em cirurgias de diversas especialidades, na implantodontia como relata Sousa et al (2017), tem sido utilizada no tratamento de casos de peri-implantite, gerando a regeneração e estimulando crescimento ósseo ao redor do implante. Como também para o fechamento de comunicações buco-sinusais ou até mesmo na estimulação do crescimento de tecido ósseo em enucleação de cistos ou atrofias de mandíbula e maxila.
Szentpeteri et al. (2020), relataram a utilização de PRF como medida terapêutica para pacientes com ONMB desencadeada pela administração de bifosfonatos. No estudo foram incluídos 101 pacientes diagnosticados em estágio 2-3 e separados em 2 grupos controles de acordo com o plano de tratamento, incluindo o uso ou não de PRF. Os dois protocolos cirúrgicos foram então avaliados e comparados a recuperação do paciente, a melhora do quadro e a recorrência. A proservação dos casos durou cerca de um ano. De acordo com os resultados obtidos no estudo houve diferença significativa nos grupos que utilizou o PRF- obtendo melhor cicatrização das lesões de MRONJ (P= 0,022), estadiamento mais bem-sucedido (P=0,005) e menores taxas de recidiva (P< 0,001) em comparação com o grupo controle.
4.4.6 Ozônioterapia
O alemão Dr, Christian Friedrich Schonbein, na década de 40 realizou um experimento com eletrólise de água, onde foi implementado a introdução do ozônio, “ozein” também denominado por ele. Descreveu como uma substância de odor característico. E assim o ozônio foi considerado como um potente oxidante por suas propriedades desinfetantes (Sguglia, 2019).
Dentre as vias de administração estão a intravenosa, retal, intramuscular, e/ou intradérmica, podendo ser na forma aquosa ou oleosa (Jaramilho et al., 2020; Palumbo et al., 2019).
Tasdoven e colaboradores (2017), afirmaram que o ozônio aumenta a distribuição de oxigênio, glicose e trifosfato de adenosina (ATP) para os tecidos isquêmicos em sua totalidade, produzindo derivados reativos de oxigênio, gerando efeitos diretos ou indiretos na vasodilatação, na elevação de oferta de óxido nítrico (NO), na angiogênese e na imunomodulação. Considerado um pró-fármaco seus efeitos são ligados a uma melhor disponibilidade de oxigênio, à modulação de sistema imune, à liberação de fatores de crescimento, à regulação de enzimas antioxidantes, como também está ligado a redução de dor e inflamação, impedindo o excesso de tecido fibrótico e estimulando o reparo ósseo (Anzolin; Bertol, 2018). O ozônio tem sido experimentado para várias modalidades na odontologia há mais de 100 anos, e atualmente é utilizada como auxílio na cicatrização de feridas, bem como, cárie dentária, líquen plano, gengivite, periodontite, halitose, osteonecrose da mandíbula, dor pós-cirúrgica, hipersensibilidade dentinária e distúrbios da articulação temporomandibular (Suh, Yiji et al., 2019).
No entanto, segundo Re Kaitlyn et al. (2023), existem possíveis contraindicações na utilização da ozônioterapia, com capacidade de induzir efeitos sistêmicos, dentre elas, destaca-se infarto agudo do miocárdio, hipertireoidismo, intoxicação alcoólica aguda, anemia grave, trombocitopenia, hemorragia ativa e pacientes em períodos gestacionais.
Todavia, segundo o Comitê Científico Internacional de Ozônioterapia, quando esta for manuseada com precaução os efeitos colaterais são reduzidos significativamente, proporcionando terapia com ozônio livre de toxicidade, com auxílio da tecnologia moderna disponível de acordo com as instruções do fabricante e as diretrizes das recomendações atuais.
Partindo por esse pressuposto, Ripamonti et al. (2012) afirmam que, a administração da ozônioterapia mostrou-se como um método eficaz para condução do tratamento da osteonecrose no pós-operatório, primordialmente em pacientes cuja lesão apresentavam-se maiores que 2,5cm.
Raimondi et al. (2020), propuseram a abordagem de tratamento com a utilização de 10 ciclos de ozônioterapia (administrados duas vezes por semana, durante cinco semanas consecutivas), seguida por remoção cirúrgica de osso necrótico e desvascularizado até evidência de osso aparentemente vital, onde obteve resolução completa de osteonecrose estágios 2 e 3.
5. Discussão
De acordo com os dados obtidos no último censo do IBGE, a população idosa no Brasil tem crescido significativamente. Em 2023, 15,6% da população brasileira tinha 60 anos ou mais, superando pela primeira vez a faixa etária de 15 a 24 anos, onde representa cerca de 14,8% (IBGE 2023).
Partindo pelo pressuposto que os fármacos da classe dos bifosfonatos têm se mostrado eficazes e comumente prescritos para tratamentos de uma variedade de condições esqueléticas, por vezes, advindas da população acima citada. Desse modo, desencadeando complicações sendo as mais comuns mialgia e esofagite, e a mais grave a osteonecrose (Eguia et al., 2020; Otto et al., 2018).
Os autores desta revisão concordam que a ingestão crônica de fármacos da classe dos bifosfonatos, bem como sua posologia, via de administração, potência, uso concomitante de corticosteroides ou presença de patologias sistêmicas associadas elevam o risco do desenvolvimento da ONMB. Além disso, quando administrados por via endovenosa intensificam o risco para desenvolvimento da patologia (Hamadeh et al., 2015). Os estudos atuais afirmam que os fatores de risco podem ser; a) fatores relacionados às drogas; b) fatores locais e c) fatores sistêmicos (Carvalho et al., 2018). Os fármacos antiangiogênicos/inibidores de tirosina quinase também são drogas que apresentam fatores de riscos para osteonecrose, além dos bifosfonatos e denosumabe. Isto leva os autores a acreditarem que a porcentagem de pacientes acometidos por essa patologia tem-se elevado significativamente (Kawahara et al.,2021; Govaerts et al., 2020).
No entanto, os autores concordam que é de suma importância a realização de procedimentos preventivos, previamente a iniciar terapia com os bifosfonatos, com a finalidade de eliminar focos de infecção, realização de terapia periodontal, extrações e próteses mal adaptadas. Para que então o paciente possa iniciar a terapia com bifosfonatos com redução dos riscos para desencadeamento da osteonecrose. Entretanto, os pacientes que já apresentarem sobre terapia é primordial o acompanhamento e monitoramento da higiene bucal e demais fatores de risco (Ribeiro et al.,2018).
Por este viés, Ruggiero et al. (2022), abordam a promoção e educação na conscientização dos pacientes como forma de tratamento, cuidados de rotina com a higiene da cavidade oral, bem como, retornos periódicos ao cirurgião dentista e por vezes eliminação de hábitos deletérios como tabagismo e ingestão de álcool. Carvalho et al. (2018) reforçam que os objetivos do tratamento desta complicação visam erradicar a dor, controlar a infecção e reduzir a evolução do sequestro ósseo. Embora diferentes tratamentos (terapêuticos ou paliativos) tenham sido descritos para o tratamento de MRONJ, ainda se torna uma questão de controvérsia nas comunidades oral e maxilofacial e que um padrão ouro ainda não foi totalmente elucidado (Ristow et al., 2019).
Assim sendo, Fliefel R et al. (2015) sustentam que não há um padrão ouro para tratamento da osteonecrose, e que as opções são descritas de acordo com o estadiamento da AAOMS, dentre elas destaca-se o controle da dor, desbridamento cirúrgico ou ressecção e laser de baixa intensidade, bem como, a utilização do ozônio em combinação com antibioticoterapia associada ao tratamento cirúrgico onde resultou em resolução da dor, secreção e halitose. Presume-se que a terapia adjuvante tem demonstrado resultados satisfatórios.
Do mesmo modo, segundo Sahin et al. (2022), além do desbridamento cirúrgico com a utilização do piezo, em seu estudo os autores preconizaram a associação com concentrado de fibrina rica em plaquetas e leucócitos, laserterapia e retalho pediculado de coxim adiposo bucal para fechamento da ferida. Neste estudo, o sucesso foi definido pela cicatrização completa da mucosa, cobertura óssea e ausência dos sintomas após o tratamento cirúrgico.
Em suma, segundo Agrillo et al. (2012); Kin et al. (2014); Rodriguez L e Onate S (2016) a associação do tratamento conservador com tratamentos adjuvantes, como oxigênio hiperbárico, ozonioterapia ou laserterapia de baixa intensidade, podem resultar em uma maior taxa de sucesso com resultados significativos no manejo de tratamento da osteonecrose mediada por bifosfonatos.
De acordo com o relato de caso de Ozalp et al. (2021), a associação do tratamento cirúrgico adjuvante com o L-PRF mostrou-se resultados promissores ao tratamento da BRONJ, devido suas propriedades de reparo tecidual, cicatrização de feridas, bem como ativação de fatores de crescimento. No estudo descrito pelo autor, foi realizado abordagem cirúrgica com ressecção marginal/sequestrectomia com ostectomia periférica (SPO), até que osso aparentemente saudável e sangrante fosse observado, seguida por irrigação abundante com solução salina estéril e aplicação de L-PRF complementando com fechamento primário da ferida.
Em contrapartida, Alrmali et al. (2023), em seu estudo retrospectivo avaliaram a eficácia da utilização do L-PRF associado ao tratamento cirúrgico para BRONJ, onde foi realizado remoção do osso necrótico através de desbridamento cirúrgico até identificação de osso saudável sobre irrigação abundante, os autores optaram por colocar o PRF diretamente sobre o osso perfurado seguido por fechamento primário da ferida. Prescrição medicamentosa e orientações pós-operatórias foram realizadas, bem como acompanhamento durante os primeiros meses até completa cicatrização. Ao total 13 pacientes foram incluídos no estudo, obtendo resultados satisfatórios em todos os pacientes, exceto por um onde foi apresentado deiscência de sutura. Os autores concluíram que a terapia adjuvante do PRF representa um complemento valioso no tratamento e prevenção da osteonecrose dos maxilares.
Com base em todas as considerações descritas, os autores desta revisão sustentam que maximizar a qualidade de vida dos pacientes deve ser característica fundamental e imprescindível de todo protocolo que exija tratamento para MRONJ, e que a abordagem adjuvante das modalidades de tratamentos citadas é a alternativa mais viável.
6. Considerações Finais
Diante do que foi abordado conclui-se que, a osteonecrose dos maxilares associada ao uso dos bifosfonatos apresenta-se como uma complicação relativamente rara, entretanto nociva, primordialmente quando esses fármacos são administrados por via endovenosa. Esse problema é de difícil condução e leva a quadros de dor e desconforto aos pacientes acometidos.
Constatamos através da literatura especializada que não há um tratamento padrão ouro para tal condição que garanta o melhor desfecho ao tratamento, e que as medidas terapêuticas adjuvantes podem apresentar alto índice de sucesso, bem como, melhoria na qualidade de vida dos pacientes acometidos.
Acredita-se que os pacientes sobre terapia com os BF´s, devem ter um acompanhamento periódico regular, principalmente quando estiverem prestes a iniciar terapia com tais medicamentos, no intuito de prevenir complicações durante e após o tratamento. Assim, a prioridade se deve, sem dúvida, à prevenção de sua ocorrência, através de tratamento prévio das condições odontológicas que possam acarretar déficit de cicatrização ou exposição de tecido ósseo, antes da terapia com os bifosfonatos. Assim sendo, o cirurgião dentista mostra-se como profissional essencial contíguo a equipe multidisciplinar, abordando educação em saúde por meio de orientação quanto à higiene bucal e eliminação de possíveis focos infecciosos ou potencialmente irritativos.
Referências Bibliográficas:
1-AGHALOO, T.; HAZBOUN, R.; ETRADIS S. : Fisiopatologia da osteonecrose dos maxilares. 2015, 27:489-96. 10.1016/j.coms.2015.06.001
2-AGRILLO, A.; FILIACI, F.; RAMIERI, V. et al. Osteonecrose da mandíbula relacionada ao bifosfonato (BRONJ): 5 anos de experiência no tratamento de 131 casos com ozonioterapia. Eur Rev Med Pharmacol Sci. 2012 novembro; 16(12):1741-7. [Medline: 23161050]
3-ALDHALAAN, NA.; BAQAIS, A.; Al-OMAR, A. Medication relatedOsteonecrosis of the Jaw: A Review. Cureus. 2020 Feb 10;
4-ALRMALI, A.; SALEH, M. H. A.; KURDI, S. M. et al. Prevenção e tratamento da osteonecrose induzida por drogas dos maxilares usando fibrina rica em plaquetas: um estudo de viabilidade clínica. Clin Exp Dent Res. 2023 outubro; 9(5):791-798. DOI: 10.1002/CRE2.775. Epub 2023 21 de agosto. PMID: 37605488; PMCID: PMC10582237.
5-ANZOLIN, A. P.; BERTOL, C. D. Ozonioterapia como terapêutica integradora no tratamento da osteoartrose: uma revisão sistemática. Brazilian Journal of Pain, São Paulo, v. 1, n. 2, p. 171-175, jun. 2018. Disponível em: https://brjp.org.br/article/10.5935/2595-0118.20180033/pdf/brjp-1-2-171- trans1.pdf.
6-BAL, R.; AMBADE, R.; SINGH, N. et al. Bifosfonatos e fraturas atípicas do fêmur: a relação é causal ou casual?. Cureus. 2023; 15(11):e48141. Publicado em 2023 de novembro de 2. DOI:10.7759/cureus.48141
7-BANSALl, H. Osteonecrose da mandíbula relacionada a medicamentos: uma atualização. 2022,13:5-10. 10.4103/njms.NJMS_236_20
8-BOFF, R. C.; SALUM, F. G.; FIGUEIREDO, M. A. et al. Aspectos importantes sobre o papel dos microrganismos na osteonecrose dos maxilares relacionada ao bifosfonato. (2014) Arquivos de biologia oral, 59(8), 790–799. https://doi.org/10.1016/j.archoralbio.2014.05.002
9-CARLSON, E. R.; BASILE, J. D. O papel da ressecção cirúrgica no tratamento da osteonecrose dos maxilares relacionada ao bifosfonato. Jornal de Cirurgia Oral e Maxillofacial, Volume 67, Edição 5, 85-9 Maio 2009; [Medline: 19371819] [doi:10.1016/j.joms.2009.01.006]
10-Carvalho, L. N. V.; Duarte, N. T.; Figueiredo, M. A. et al. Osteonecrose dos maxilares relacionada ao uso de medicações: Diagnóstico, tratamento e prevenção. Revista CES Odontologia, Medellin, 31(2)48-63, 2018.
11-CHUN LEI, L.; LU, W. W.; OLIVEIRA, C. J. et al. Papel da doença periodontal na osteonecrose relacionada ao bifosfonato dos maxilares em ratos ovariectomizados. Clin. Implante Oral. Res. 2016, 27, 1–6
12-Comitê Científico Internacional de Ozonioterapia-ISCO3: Instruções de metodologia de aprendizagem e aperfeiçoamento em ozonioterapia para médicos, 2015. Disponível online em: https://isco3.org/wp content/uploads/2015/09/ISCO3-HUM-00-01.pdf.
13-COROPCIUC, R. G.; GRISAR, K.; AERDEN, T. et al. Osteonecrose da mandíbula relacionada a medicamentos em pacientes oncológicos com metástases esqueléticas: o tratamento conservador é eficaz até o estágio 2. Br J Oral Maxillofac Surg, 55 (2017), pp. 787-792 https://doi.org/10.1016/j.bjoms.2017.06.014
14-COSTA, D. S.; RESENDE, L. D. O.; ASSIS L. J. et al. Enucleação de cisto periapical e preenchimento com biomaterial e L-PRF: relato de caso. Cent Un Anápolis. Unievangélica. 2018.
15-DRAKE, M.T.; CLARKE, B. L.; KHOSLA, S. Bifosfonatos: mecanismo de ação e papel na prática clínica. Mayo Clin Proc. 2008 Set; 83(9):1021-45. DOI: 10.4065/83.9.1032. PMID:18775204; PMCID: PMC2667901.
16-EGUIA, A.; BAGAN, L.; CARDONA, F. Review and update on drugs related to the development of osteonecrosis of the jaw. Medicina oral, patologia oral y cirugia bucal, v. 25, n. 1, p. e71, 2020. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6982985/.
17-ERGUN, T. G.; DERIN, A. T.; YAPRAK, N. et al. The place of hyperbaric oxygen therapy and ozone therapy in sudden hearing loss. Braz J Otorhinolaryngol. 2017;83:457-63. Disponível em: http://dx.doi.org/10.1016/j.bjorl.2016.06.002
18-ERVOLINO, E.; STATKIEVICZ, C.; TORO, L. F. et al. Antimicrobial photodynamic therapy improves the alveolar repair process and prevents the occurrence of osteonecrosis of the jaws after tooth extraction in senile rats treated with zoledronate. Bone. 2019;120:101-13. doi: 10.1016/j.bone.2018.10.014.
19-FLIEFEL, R.; TROLTZSCH, M.; KUHNISCH, J. et al. Estratégias de tratamento e resultados da osteonecrose da mandíbula relacionada ao bifosfonato (BRONJ) com caracterização de pacientes: uma revisão sistemática. Int J Oral Maxillofac Surg. 2015 Maio; 44(5):568-85. DOI: 10.1016/j.ijom.2015.01.026.
20-GARCÍA, I. G.; MOLINA, B. P.; TRAPOTE, S. M. Et al. Tratamento da osteonecrose da mandíbula relacionada ao bisfosfonato com plasma rico em fatores de crescimento após cirurgia de implante dentário: relato de caso. J Implantol Oral (2019) 45 (4): 289-296 https://doi.org/10.1563/aaid-joi-D-18-00254
21-GEHRKE, B.; COELHO, M. C. A.; D’ALVA, C. B. et al. Consequências a longo prazo da terapia da osteoporose com bisfosfonatos. Arco Endocrinol. Metab., v. 68, e220334, jan. 2024.
22-GIL, I. G.; PONTE, B. M.; MATEO, S. T. et al. Tratamento da osteonecrose da mandíbula relacionada ao bifosfonato com plasma rico em fatores de crescimento após cirurgia de implante dentário: relato de caso. O Jornal de implantologia oral, 45(4), 289–296, 2019. https://doi.org/10.1563/aaid-joi-D18-00254
23-GOVAERTS, D. et al. Adjuvant therapies for MRONJ: A systematic review. Bone, v. 141, p. 115676, 2020. Disponível em: https://pubmed.ncbi.nlm.nih.gov/33022455/.
24-GUARNERI, V.; MILES, D.; ROBERT, N. et al. Bevacizumabe e osteonecrose da mandíbula: incidência e associação com terapia com bisfosfonatos em três grandes estudos prospectivos em câncer de mama avançado. Câncer de mama ResTreat. 2010, 122: 181-8. 10,1007/s10549-010-0866-3
25-HAMADEH, I.S.; NGWA B.A.; GONG Y. Drug induced osteonecrosis of the jaw. Cancer Treat Rev 2015;41(5):455-464.
26-HUPP, James; TUCKER, Myron; ELLIS, Edwad. Cirurgia Oral e Maxilofacialcontemporanea. 7 Ed. Barueri: GEN Guanabara Koogan, 2021.
27-JAEGER, Filipe; MENEZES, Gustavo. Guia Prático de Farmacologia e Terapêutica Medicamentosa Aplicada à Odontologia. 1 Ed. Belo Horizonte: Editora MFT Academy, 2022.
28-JAEGER, Filipe; MENEZES, Gustavo. Guia Prático de Cirurgia Oral- O Blackbook da Cirurgia Odontológica. 1 Ed. Belo Horizonte: Editora MFT Academy, 2023.
29-JARAMILHO, F. M.; VENDRUSCULO, C. P.; FULBER J. et al. Effects of transrectal medicinal ozone in horses: clinical and laboratory aspects. Arquivo Brasileiro de Medicina Veterinária e Zootecnia, v. 72, n. 1, p. 56-64, 2020 Tradução . Disponível em: https://doi.org/10.1590/1678-4162-11155. Acesso em: 10 set. 2024.
30-KAWAHARA, M.; KUROSHIMA, S.; SAWASE, T. Clinicalconsiderations for medication-relatedosteonecrosis of the jaw: a comprehensiveliterature review. International Journal of ImplantDentistry [Internet]. 2021 May 14;7(1):47. Available from: https://pubmed.ncbi.nlm.nih.gov/33987769/
31-KIM, J.; LEE, D. H.; DZIAK, R. et al. Bisphosphonate-relatedosteonecrosis of the jaw: Currentclinicalsignificance and treatmentstrategy review. American Journal of Dentistry [Internet]. 2020 Jun 1;33(3):115–28. Available from: https://pubmed.ncbi.nlm.nih.gov/32470236
32-KISHIMOTO, H.; NOGUCHI, K.; TAKAOKA, K. Novo insight sobre o tratamento da osteonecrose da mandíbula relacionada ao bifosfonato (BRONJ) Dente japonês. Sci. Rev., 55(1) (2019), pp. 95-102 https://doi.org/10.1016/j.joms.2014.04.031
33-LOBEKK, O.K.; DIJKSTRA, W.; PEDERSEN, T.O. Tratamento cirúrgico versus conservador da osteonecrose da mandíbula relacionada a medicamentos: uma complexa revisão sistemática e metanálise. Oral Surg Oral Med Oral Pathol Oral Radiol. 2021; 132(6):671-679. DOI:10.1016/j.oooo.2021.09.009
34-LO, J.C.; O´RYAN, F.S.; GORDON, N.P. et al. Prevalência de osteonecrose da mandíbula em pacientes com exposição oral ao bisfosfonatos. 2010, 68:243-53. 10.1016/j.joms.2009.03.050
35-MADEIRA, M.; ROCHA, A. C.; MOREIRA, C. A. et al. Prevenção e tratamento dos efeitos adversos orais e medicamentos antirreabsortivos para osteoporose– Posicionamento da Sociedade Brasileira de Endocrinologia e Metabologia (SBEM), Sociedade Brasileira de Estomatologia e Patologia Oral (Sobep) e Associação Brasileira de Avaliação Óssea e Csteometabolismo (Abrasso). Maio de 2021; 64(6):664-672. DOI: 10.20945/2359- 3997000000301. PMID: 34033275; PMCID: PMC10528626
36-MCGOWAN, K.; MCGOWAN, T.; IVANOVSKI, S. Fatores de risco para osteonecrose dos maxilares relacionada a medicamentos: uma revisão sistemática. Doenças bucais. 2018, 24(4), 527–536. https://doi.org/10.1111/odi.12708
37- MIGLIORATI, C.A.; BRENNAN, M.T.; PETERSON, D.E. Medication RelatedOsteonecrosis of the Jaws. JNCI Monographs. 2019 Aug 1;2019
38-MOBADDER, M.; GRZECH, L. Z.; El MOBADDER, W. et al. Management of Medication-Related Osteonecrosis of the Jaw with Photobiomodulation and Minimal Surgical Intervention. Dent J (Basel). 2023 May 8;11(5):127. doi: 10.3390/dj11050127. PMID: 37232778; PMCID: PMC10216921.
39-MOREIRA, F. C. L. Manual prático para uso dos lasers na odontologia. 1. ed. Goiânia: Cegraf UFG, 2020, 43 p.
40-MOZZATI, M.; ARATA, V.; GALLESIO, G. Extração dentária em pacientes em terapia com ácido zoledrônico. Oncologia oral. 2012, 48(9), 817–821. https://doi.org/10.1016/j.oraloncology.2012.03.009
41-NICA, D.F.; RIVIS, M.; ROI, C.L. et al. Complementarity of Photo Biomodulation, Surgical Treatment, and Antibiotherapy for Medication Related Osteonecrosis of the Jaws (MRONJ). Medicina. 2021; 57(2):145. https://doi.org/10.3390/medicina57020145
42-ONUR, S.; ENDER, A.; BIRKAN, T. et al. Abordagem combinada para o tratamento de estágios avançados de osteonecrose relacionada a medicamentos de pacientes maxilares. Revista Brasileira de Otorrinolaringologia Volume 88, Edição 4, Julho–Agosto de 2022, Páginas 613-620 https://doi.org/10.1016/j.bjorl.2021.04.004]
43-OTTO, S. et al. Medication-related osteonecrosis of the jaw: Prevention, diagnosis and management in patients with cancer and bone metastases. Cancer Treatment Reviews, v. 69, p. 177-187, 2018. Disponível em: https://www.sciencedirect.com/science/article/pii/S0305737218301014. Acesso em 28 out. 2024.
44-OZALP, O.; YILDIRIMYAN, N.; ÖZTURK, C. et al. Resultados promissores do tratamento cirúrgico da osteonecrose dos maxilares relacionada a medicamentos avançados usando leucócitos adjuvantes e fibrina rica em plaquetas. BMC Saúde Bucal. 1º de dezembro de 2021; 21(1):613. DOI: 10.1186/s12903-021-01965-7.
45-PAGEAU, S.C. Denosumabe. MAbs2009; 1(3):210-5.
46-PALUMBO, C.; NEGRI, A.; ZANCHETTA, M. B. Osteoactivos en insuficiencia renal crónica avanzada: a propósito de um caso. Actualizaciones en Osteología, v. 15, n. 2, p. 94-102, mayo/ago. 2019. Disponível em: http://aaomm.org.ar/wp-content/uploads/2020/09/Casos11.pdf.
47-PAVLÍKOVÁ, G.; FOLTÁN, R.; HORKÁ, M. et al. Piezocirurgia em cirurgia bucomaxilofacial. Int J Oral Maxillofac Surg, 40 (2011), pp. 451-457
48-POLI, P. P.; SOUZA, F. A.; MAIORANA, C. Adjunctive use of antimicrobial photodynamictherapy in the treatment of medication-related osteonecrosis of the jaws: A case report. PhotodiagnosisPhotodyn Ther, v. 23, p. 99-101, 2018.
49-PONTES, J. C. X. Avaliação da imunomodulação e eficácia da fotobiomodulação no tratamento da osteonecrose dos maxilares induzida por bisfosfonatos em modelo murino. 2022. Dissertação (Mestrado em Odontologia) –Programa de Pós-graduação em Odontologia, Universidade Federal da Paraíba, João Pessoa, 2022. Disponível em: https://repositorio.ufpb.br/jspui/handle/123456789/27136.
50-RAIMONDI, A.; SIMEONE, N.; GUZZO M. et al. Redesafio de denosumabe na osteonecrose da mandíbula de pacientes com tumor ósseo de células gigantes irressecável: uma análise de série de casos e revisão da literatura. ESMO Open. Julho de 2020; 5(4):e000663. DOI: 10.1136/esmoopen-2019-000663.
51-RE, K.; GANDH, J.; LIANG, R. Utilidade clínica da ozonioterapia e oxigenoterapia hiperbárica na doença degenerativa do disco. Pesquisa de gases medicinais. 2023, 13(1), 1–6. https://doi.org/10.4103/2045- 9912.351890
52-RIBEIRO, G.H.; MINAMISAKO, M. C.; RATH, I.B.S. et al. Osteoradionecrosis of the jaws: case series treated with adjuvant low-level laser therapy and antimicrobial photodynamic therapy. J Appl Oral Sci, v. 26, p. e20170172, 2018. http://dx.doi.org/10.1590/1678-7757-2017-0172.
53-RISTOW, O.; RUCKSCHLO, T.; MULLER M. et al. O tratamento conservador não cirúrgico da osteonecrose da mandíbula relacionada a medicamentos é uma opção de tratamento apropriada para os estágios iniciais? Um estudo de coorte de longo prazo de centro único. J Craniomaxilofaque Surg. 2019 março; 47(3):491-499. [Medline: 30642734] [doi: 10.1016/j.jcms.2018.12.014
54-RIPAMONTI, C. I.; MANIEZZO, M.; PESSI, M. A. et al. Tratamento da osteonecrose da mandíbula (ONJ) por insuflação médica de gás ozônio. Um relato de caso Tumori. 2012; 98:72e-75e
55-ROCHA, C. T. A. V.; RIBEIRO, P. M.; ANDREA, L. M. A I. et al. Avaliando a compreensão dos cirurgiões-dentistas sobre os bifosfonatos: implicações para a saúde do paciente em cirurgia oral. A revista odontológica saudita. 2024, 36(1), 180–186. https://doi.org/10.1016/j.sdentj.2023.09.011
56-RODRIGUEZ, L. F. J.; ONATE, S. R. E. Tratamento da osteonecrose da mandíbula relacionada a bifosfonatos e outros agentes antirreabsortivos. Med Oral Patol Oral Cir Bucal. 1º de setembro de 2016; 21(5):e595-600. [Medline: 27475683] [artigo livre PMC: 5005097] [doi: 10.4317/medoral.20980]
57-RUGGIERO, S. L.; DODSON, T. B.; ASSAEL, L. A. et al. American Association of Oral and Maxillofacial Surgeons. American Association of Oral and Maxillofacial Surgeons position paper on bisphosphonate-related osteonecrosis of the jaws—2009 update J Oral Maxillofac Surg. 2009 ; 67(5 Suppl): 2-12.
58-RUGGIERO, S. L.; DODSON, T. B.; FANTASIA, J. et al. American Association of Oral and Maxillofacial Surgeons Position Paper on Medication-Related Osteonecrosis of the Jaw—2014 Update. Revista de Cirurgia Bucomaxilofacial2014; 72(10):1938-56. [PMID: 25683041]
59-RUGGIERO, S.L.; DODSON, T.B.; AGHALOO, T. et al. American Association of Oral and MaxillofacialSurgeons’ PositionPaper on Medication-RelatedOsteonecrosis of the Jaws—2022 Update. Journal of Oral and MaxillofacialSurgery. 2022 May;80(5):920–4
60-RUOCCO, V. V.; BERGANTIM, M.; CASTELO, B. L. et al . Bifosfonatos: tipos, mecanismos de ação e efeitos colaterais. Revisão da literatura para orientação de profissionais e estudantes das áreas médica e odontológica. Revista Brasileira Multidisciplinar, [S. l.], v. 26, n. 1, p. 94-120, 2023. DOI: 10.25061/2527-2675/ReBraM/2022.v25i3.1682. Disponível em: https://revistarebram.com/index.php/revistauniara/article/view/1682. Acesso em: 16 setembro. 2024.
61-SELUKI, R.; SELUKI, M.; VAITKEVICIENE, I. et al. Comparação da eficácia do tratamento conservador e cirúrgico da osteonecrose da mandíbula relacionada a medicamentos: uma revisão sistemática. J Maxilofac Oral Res 2023; 14(4):e1 DOI:10.5037/jomr.2023.14401
62-SENTURK, F. M.; CIMEN, E.; ONCUL, T. M. A. et al. Conscientização dos oncologistas sobre a osteonecrose dos maxilares relacionada ao bifosfonato. JPMA. O Jornal da Associação Médica do Paquistão. 2016, 66(7), 880–883.
63-SHARMA, S.; SHANKAR, R.;, RAVI K. B. et al .Uma revisão narrativa da osteonecrose da mandíbula: o que um clínico deve saber. Dezembro 2023, 15(120: e51183. DOI:10.7759/cureus.51183
64-SGUGLIA, S. A. Uso de bifosfonatos em pacientes com osteopenia. Evidencia, Actualizacion en la Práctica Ambulatoria, Buenos Aires, v. 22, n. 2, sep. 2019. Disponível em: http://www.evidencia.org/index.php/Evidencia/article/view/4239
65-SIGUA, R. E. A.; COSTA, R.R.; BRITO, A.C. et al. Revista Internacional de Odontologia 2014; 2014:192320. [PMID: 24868206]
66-SOUSA, E.O.; BOTELHO, A.C.L.; DUARTE, B.T. et al. Braz J Periodontol. 2017 dez; 27(4): 91-98.
67-SUH, Y.; PATEL, S.; KAITLYN, R. et al. Utilidade clínica da ozonioterapia na medicina dentária e oral. Med Gas Res. 2019 julho-setembro; 9(3):163-167. DOI: 10.4103/2045-9912.266997.
68- SVEJDA, B.; MUSUSCHITZ, C.; GRUBER, R.; et al. WIEN Med Wochenschr. 2016 Fev; 166(1-2):68-74. Alemão. DOI: 10.1007/s10354-016-0437-2.
69-SZENTPETERI, S.; SCHMIDT, L.; RESTAR, L. et al. O efeito da membrana de fibrina rica em plaquetas na terapia cirúrgica da osteonecrose da mandíbula relacionada a medicamentos. J Oral Maxillofac Surg. 2020 maio; 78(5):738-748. [Medline: 31945309] [doi: 10.1016/j.joms.2019.12.008]
70-TARTAROTI, N. C.; MARQUES, M. M.; NACLÉRIO, H. M. G. et al. Terapias adjuvantes fotodinâmicas e fotobiomoduladoras antimicrobianas para prevenção e tratamento da osteonecrose dos maxilares relacionada a medicamentos: série de casos e acompanhamento a longo prazo. Fotodiagnóstico e terapia fotodinâmica. 2020; 29, 101651. https://doi.org/10.1016/j.pdpdt.2020.101651
71-VESCOVI, P. Bifosfonatos e osteonecrose: uma questão aberta. Casos Clínicos em Metabolismo Mineral e Ósseo 2012; 9(3):142-4. [PMID: 23289026]
72-VIANA, M.V.G.; CARVALHO, M.M.M.; FIALHO, P.V. et al. Considerações clinicas sobre o uso do L- PRF na terapêutica de osteonecrose medicamentosa dos maxilares: relato de caso. Braz. J. Hea. Rev. 2019 jul/aug.;2(4): 3318-3327
73-WAN, J.T.; SHEELEY, D.M.; SOMERMAN, M.J. et al. Mitigando a osteonecrose da mandíbula (ONM) através de cuidados dentários preventivos e compreensão dos fatores de risco. Osso Res.2020, 8:14. 10.1038/s41413-020-0088-1
1E-mail: drabeatrizkely@outlook.com
2E-mail: larissandradems@outlook.com
3E-mail: darlankelton@gmail.com
4E-mail: palmawilke225@gmail.com
5E-mail: nicolemgrisa@gmail.com
6E-mail: fernandobecklin@gmail.com
7E-mail: vianaemerson21@gmail.com
8E-mail: isabellydaleprane@hotmail.com
9Email: Felipealbuquerque.1987@gmail.com
10E-mail: clebesonandre@gmail.com
