REGISTRO DOI: 10.69849/revistaft/pa10202511160955
Gabriela Roldo Tieppo; Amanda Ribeiro da Silva; Rafaelle Führ Soares; Larissa Rosa Ferreira; Jhuana Fernanda Rojas; Larissa Barragan Oliveira; Ângela Zangali Toigo; Vitória Kleinubing Abal
RESUMO
Objetivo: Avaliar a efetividade das estratégias de manejo da hipertensão arterial sistêmica e diabetes mellitus tipo 2 na atenção básica, identificando as abordagens mais eficazes para o controle pressórico e glicêmico. Métodos: Revisão sistemática conduzida conforme diretrizes PRISMA 2020. Realizou-se busca sistemática nas bases PubMed/MEDLINE, Embase, Cochrane Library, LILACS, SciELO, Scopus e Web of Science, de janeiro de 2009 a setembro de 2024. Incluíram-se ensaios clínicos randomizados e estudos de coorte prospectivos que avaliaram estratégias de manejo de adultos com hipertensão e/ou diabetes na atenção básica. Dois revisores independentes realizaram a seleção de estudos, extração de dados e avaliação da qualidade metodológica usando as ferramentas RoB 2 para ensaios clínicos e Newcastle-Ottawa para estudos observacionais. Os desfechos primários foram controle pressórico (<140/90 mmHg) e glicêmico (HbA1c <7%). A certeza da evidência foi avaliada pelo sistema GRADE. Resultados: Foram identificados 2.847 registros, dos quais 42 estudos atenderam aos critérios de inclusão, envolvendo 28.564 participantes. As estratégias mais efetivas incluíram: cuidado compartilhado multiprofissional (RR 1,34; IC 95% 1,18-1,52 para controle pressórico), programas estruturados de educação em saúde (DM -0,8%; IC 95% -1,2 a -0,4 para HbA1c), e protocolos padronizados de manejo clínico (RR 1,28; IC 95% 1,15-1,43 para controle glicêmico). O telemonitoramento mostrou-se eficaz em contextos com recursos tecnológicos adequados (DM -8,2 mmHg; IC 95% -12,1 a -4,3 para pressão sistólica). Intervenções combinadas farmacológicas e não- farmacológicas demonstraram superioridade em relação a abordagens isoladas.Aqualidade da evidência variou de moderada a alta para os desfechos principais. Conclusões: Estratégias multiprofissionais integradas, protocolos padronizados e programas educativos estruturados são efetivas para o controle da hipertensão e diabetes na atenção básica. A implementação de modelos de cuidado compartilhado e o uso de tecnologias de monitoramento remoto podem otimizar os resultados clínicos. Os achados fornecem evidências robustas para orientar políticas de saúde e protocolos clínicos na atenção básica.
Palavras-chave: Hipertensão; Diabetes Mellitus Tipo 2; Atenção Primária à Saúde; Manejo da Doença; Controle Glicêmico; Pressão Arterial; Cuidados Crônicos.
ABSTRACT
Objective: To evaluate the effectiveness of management strategies for systemic arterial hypertension and type 2 diabetes mellitus in primary health care, identifying the most effective approaches for blood pressure and glycemic control. Methods: Systematic review conducted according to PRISMA 2020 guidelines. A comprehensive search was performed in PubMed/MEDLINE, Embase, Cochrane Library, LILACS, SciELO, Scopus, and Web of Science databases from January 2009 to September 2024. We included randomized controlled trials and prospective cohort studies evaluating management strategies for adults with hypertension and/or diabetes in primary care settings. Two independent reviewers performed study selection, data extraction, and methodological quality assessment using RoB 2 for clinical trials and Newcastle-Ottawa Scale for observational studies. Primary outcomes were blood pressure control (<140/90 mmHg) and glycemic control (HbA1c <7%). Evidence certainty was assessed using the GRADE system. Results: We identified 2,847 records, of which 42 studies met inclusion criteria, involving 28,564 participants. The most effective strategies included: multiprofessional shared care (RR 1.34; 95% CI 1.18-1.52 for blood pressure control), structured health education programs (MD -0.8%; 95% CI -1.2 to -0.4 for HbA1c), and standardized clinical management protocols (RR 1.28; 95% CI 1.15-1.43 for glycemic control). Telemonitoring proved effective in contexts with adequate technological resources (MD -8.2 mmHg; 95% CI -12.1 to -4.3 for systolic blood pressure). Combined pharmacological and non-pharmacological interventions demonstrated superiority over isolated approaches. Evidence quality ranged from moderate to high for primary outcomes. Conclusions: Integrated multiprofessional strategies, standardized protocols, and structured educational programs are effective for hypertension and diabetes control in primary care. Implementation of shared care models and remote monitoring technologies can optimize clinical outcomes. The findings provide robust evidence to guide health policies and clinical protocols in primary care settings.
Keywords: Hypertension; Diabetes Mellitus, Type 2; Primary Health Care; Disease Management; Glycemic Control; Blood Pressure; Chronic Care.
INTRODUÇÃO
A hipertensão arterial sistêmica (HAS) e o diabetes mellitus tipo 2 (DM2) representam duas das principais causas de morbidade e mortalidade cardiovascular em escala global, constituindo desafios centrais para os sistemas de saúde contemporâneos. Dados da Organização Mundial da Saúde indicam que aproximadamente 1,28 bilhão de adultos vivem com hipertensão em todo o mundo, enquanto cerca de 422 milhões de pessoas convivem com diabetes, números que têm aumentado consistentemente nas últimas décadas¹,². No Brasil, a Pesquisa Nacional de Saúde de 2019 revelou prevalências de 23,9% para hipertensão e 7,7% para diabetes na população adulta, com tendência crescente associada ao envelhecimento populacional e às mudanças nos padrões de vida urbana³.
O impacto dessas condições transcende os aspectos clínicos individuais, configurando- se como um problema de saúde pública de magnitude crescente. A hipertensão arterial é responsável por aproximadamente 10,8 milhões de mortes anuais globalmente, sendo o principal fator de risco modificável para doenças cardiovasculares, acidente vascular cerebral e doença renal crônica⁴. Paralelamente, o diabetes mellitus está associado a complicações microvasculares e macrovasculares que resultam em significativa redução da expectativa e qualidade de vida, além de custos substanciais para os sistemas de saúde⁵. Quando coexistentes, essas condições amplificam mutuamente os riscos cardiovasculares, criando um cenário de complexidade clínica que demanda abordagens integradas e sistematizadas de cuidado⁶.
A atenção básica emerge como cenário fundamental para o enfrentamento desses desafios, posicionando-se estrategicamente como primeiro nível de contato dos indivíduos com o sistema de saúde e responsável pela coordenação do cuidado longitudinal. No contexto brasileiro, a Estratégia Saúde da Família (ESF) constitui o modelo organizativo principal da atenção básica, fundamentada nos princípios de territorialização, integralidade, equidade e participação social⁷. Este modelo apresenta potencial singular para o manejo de condições crônicas, oferecendo proximidade territorial, conhecimento do contexto socioeconômico das famílias e possibilidade de implementação de estratégias de prevenção primária e secundária de forma continuada⁸.
Evidências consistentes demonstram que o controle adequado da pressão arterial e da glicemia pode reduzir substancialmente o risco de complicações cardiovasculares e morte prematura. Estudos clássicos como o UK Prospective Diabetes Study (UKPDS) e o Hypertension Optimal Treatment (HOT) estabeleceram as bases científicas para metas terapêuticas rigorosas, demonstrando benefícios significativos do controle intensivo dessas condições⁹,¹⁰. Entretanto, a translação desses achados para a prática clínica na atenção básica encontra diversos obstáculos, incluindo limitações de recursos, complexidade dos protocolos terapêuticos, desafios na adesão dos pacientes e necessidade de abordagens multidisciplinares coordenadas¹¹.
A literatura científica tem documentado uma lacuna persistente entre as evidências disponíveis e os resultados alcançados na prática clínica cotidiana da atenção básica. Estudos observacionais indicam que apenas 30-60% dos pacientes com hipertensão e 40-70% daqueles com diabetes atingem metas terapêuticas adequadas no contexto da atenção primária, com variações significativas entre diferentes sistemas de saúde e populações¹²,¹³. Essa realidade aponta para a necessidade de identificação e implementação de estratégias baseadas em evidências que sejam simultaneamente efetivas clinicamente e viáveis operacionalmente no contexto dos serviços de atenção básica.
Diversas abordagens têm sido propostas e testadas para otimizar o manejo da hipertensão e diabetes na atenção básica. Estratégias farmacológicas incluem a padronização de protocolos terapêuticos, implementação de algoritmos de prescrição e otimização de esquemas medicamentosos com base em evidências clínicas robustas¹⁴. Paralelamente, intervenções não-farmacológicas englobam programas educativos estruturados, modificações no estilo de vida, suporte nutricional e implementação de tecnologias de monitoramento remoto¹⁵. Modelos organizacionais inovadores, como o cuidado compartilhado multiprofissional, consultas de enfermagem especializadas e sistemas de lembretes automatizados, têm demonstrado resultados promissores em diferentes contextos de saúde¹⁶.
O conceito de cuidado crônico estruturado, baseado no Chronic Care Model proposto por Wagner e colaboradores, oferece um framework teórico para a organização sistemática do cuidado às condições crônicas na atenção básica¹⁷. Este modelo enfatiza a importância da integração entre sistemas de informação, suporte à decisão clínica, redesenho da prática assistencial, suporte ao autocuidado, recursos comunitários e liderança organizacional como elementos fundamentais para a obtenção de resultados clínicos superiores¹⁸. A aplicação desses princípios tem resultado em melhorias documentadas nos indicadores de processo e desfechos clínicos em diferentes sistemas de saúde internacionalmente¹⁹.
Tecnologias emergentes têm expandido o arsenal de ferramentas disponíveis para o manejo dessas condições na atenção básica. Sistemas de telemonitoramento, aplicativos móveis para automonitoramento, prontuários eletrônicos integrados e algoritmos de suporte à decisão clínica representam inovações com potencial transformador para a prática clínica²⁰. Entretanto, a implementação dessas tecnologias em contextos de recursos limitados, como frequentemente observado na atenção básica de países em desenvolvimento, apresenta desafios específicos que necessitam ser considerados na avaliação de sua efetividade e viabilidade²¹.
A heterogeneidade dos contextos assistenciais, populacionais e organizacionais nos quais as estratégias de manejo são implementadas constitui um desafio metodológico significativo para a síntese de evidências neste campo. Diferenças nos sistemas de saúde, recursos disponíveis, características sociodemográficas das populações atendidas e modelos de organização dos serviços podem influenciar substancialmente a efetividade das intervenções propostas²². Esta diversidade contextual torna fundamental a condução de revisões sistemáticas abrangentes que considerem essa variabilidade e forneçam evidências aplicáveis a diferentes cenários da atenção básica.
Revisões sistemáticas prévias têm abordado aspectos específicos do manejo da hipertensão e diabetes na atenção primária, focalizando intervenções isoladas ou populações particulares²³,²⁴. Entretanto, existe uma lacuna de conhecimento quanto à síntese abrangente das estratégias integradas de manejo dessas condições, considerando simultaneamente intervenções farmacológicas, não-farmacológicas e organizacionais. Além disso, a maioria das revisões disponíveis concentra-se em evidências oriundas de países de alta renda, com limitada representatividade de contextos de recursos limitados, particularmente relevantes para países em desenvolvimento como o Brasil²⁵.
A qualidade da evidência disponível constitui outro aspecto crítico para a tomada de decisão clínica e elaboração de políticas de saúde baseadas em evidências. A diversidade metodológica dos estudos primários, incluindo diferentes desenhos de pesquisa, populações estudadas, intervenções testadas e desfechos avaliados, demanda uma abordagem sistemática rigorosa para a avaliação da certeza das evidências disponíveis²⁶. A aplicação de ferramentas padronizadas como o sistema GRADE (Grading of Recommendations Assessment, Development and Evaluation) torna-se fundamental para orientar a interpretação dos achados e sua aplicabilidade na prática clínica²⁷.
A perspectiva de implementação das evidências científicas no contexto real dos serviços de atenção básica representa um desafio adicional que necessita ser considerado na síntese de evidências. Fatores como custo-efetividade das intervenções, necessidades de treinamento profissional, adaptações organizacionais requeridas e aceitabilidade por parte de pacientes e profissionais influenciam diretamente a viabilidade de implementação das estratégias identificadas como efetivas²⁸. A consideração desses aspectos pragmáticos é essencial para que as evidências sintetizadas possam efetivamente contribuir para a melhoria dos cuidados prestados na atenção básica.
O momento atual apresenta oportunidades ímpares para o avanço do conhecimento neste campo. O crescimento exponencial da produção científica relacionada ao manejo de condições crônicas na atenção primária, aliado ao desenvolvimento de metodologias cada vez mais sofisticadas para síntese de evidências, cria condições favoráveis para a condução de revisões sistemáticas abrangentes e metodologicamente rigorosas²⁹. Simultaneamente, a crescente pressão sobre os sistemas de saúde para demonstrar efetividade e eficiência no manejo de condições crônicas torna ainda mais relevante a identificação de estratégias baseadas em evidências que possam ser implementadas de forma sustentável³⁰.
Diante deste cenário, torna-se imperativa a condução de uma revisão sistemática abrangente que sintetize as evidências disponíveis sobre estratégias de manejo da hipertensão e diabetes na atenção básica, considerando simultaneamente aspectos de efetividade clínica, viabilidade operacional e aplicabilidade a diferentes contextos assistenciais. Esta síntese de evidências pode contribuir significativamente para a elaboração de diretrizes clínicas baseadas em evidências, desenvolvimento de protocolos assistenciais padronizados e implementação de políticas de saúde orientadas por resultados científicos robustos.
O objetivo geral deste estudo é avaliar a efetividade das estratégias de manejo da hipertensão arterial sistêmica e diabetes mellitus tipo 2 na atenção básica, identificando as abordagens mais eficazes para o controle pressórico e glicêmico por meio de uma revisão sistemática da literatura.
Quanto aos objetivos específicos pretende-se: Identificar e caracterizar as estratégias de manejo da hipertensão e diabetes implementadas na atenção básica, categorizando-as segundo tipo de intervenção (farmacológica, não-farmacológica, organizacional) e modalidade de implementação. Analisar a efetividade das diferentes estratégias de manejo sobre os desfechos primários de controle pressórico (proporção de pacientes com pressão arterial <140/90 mmHg) e controle glicêmico (proporção de pacientes com HbA1c <7%). Avaliar o impacto das intervenções sobre desfechos secundários, incluindo adesão ao tratamento, qualidade de vida, eventos cardiovasculares, custos assistenciais e indicadores de processo de cuidado. Examinar a heterogeneidade entre os estudos em relação às características das populações, contextos assistenciais, recursos disponíveis e modalidades de implementação das intervenções. Sintetizar as evidências disponíveis sobre fatores associados ao sucesso das estratégias de manejo, identificando elementos facilitadores e barreiras para implementação na atenção básica. Avaliar a qualidade metodológica e certeza das evidências dos estudos incluídos, utilizando ferramentas padronizadas e sistema GRADE para orientar a interpretação dos achados. Fornecer recomendações baseadas em evidências para orientar a prática clínica, elaboração de protocolos assistenciais e desenvolvimento de políticas de saúde na atenção básica.
METODOLOGIA
Esta revisão sistemática foi desenvolvida de acordo com as diretrizes do PRISMA 2020 e do Manual Cochrane. O planejamento metodológico seguiu as recomendações do PRISMA- P, especificando previamente os critérios de elegibilidade, a estratégia de busca, os processos de seleção e extração de dados e os métodos de análise, com todas as alterações documentadas na publicação. Foram incluídos estudos com adultos (≥18 anos) portadores de hipertensão arterial sistêmica e/ou diabetes mellitus tipo 2, atendidos em serviços de atenção básica. Foram excluídos gestantes, menores de 18 anos, pacientes com hipertensão secundária ou diabetes tipo 1, populações hospitalizadas, atendidas em serviços especializados ou em situação de urgência. As intervenções consideradas elegíveis abrangeram estratégias farmacológicas, não- farmacológicas e organizacionais, com duração mínima de três meses. Os comparadores admitidos foram o cuidado usual, controles sem intervenção específica ou outras estratégias de manejo. Os desfechos primários foram o controle pressórico e glicêmico, e os secundários incluíram variações de pressão arterial e HbA1c, adesão terapêutica, eventos cardiovasculares, complicações microvasculares, qualidade de vida, satisfação dos pacientes, uso de serviços, custos e indicadores de processo. Foram incluídos ensaios clínicos randomizados, controlados não-randomizados, estudos de coorte prospectivos com grupo controle e estudos antes-depois com controle contemporâneo, sendo excluídos estudos transversais, relatos e séries de caso, revisões narrativas e resumos sem texto completo. Apenas estudos conduzidos em serviços de atenção primária foram considerados, publicados em português, inglês ou espanhol entre janeiro de 2009 e setembro de 2024.
A busca foi realizada em bases principais (MEDLINE, Embase, CENTRAL, LILACS) e complementares (SciELO, Scopus, Web of Science), além de registros de ensaios clínicos, literatura cinzenta, referências cruzadas e contato com especialistas. As estratégias de busca utilizaram descritores controlados e palavras-chave adaptadas a cada base, com operadores booleanos e truncamentos. As referências foram gerenciadas no Mendeley, com remoção de duplicatas. A triagem de títulos e resumos foi realizada de forma independente por dois revisores, seguida da avaliação de texto completo. Discordâncias foram resolvidas por consenso ou por terceiro revisor, e a concordância foi medida pelo coeficiente kappa. Quando necessário, os autores dos estudos foram contatados para esclarecimentos e complementação de dados.
A extração de dados foi feita por meio de formulário padronizado no REDCap, testado previamente, com coleta independente por dois revisores. Foram extraídas informações sobre características dos estudos, populações, intervenções, comparadores e desfechos, com padronização de unidades e tratamento de dados faltantes. O risco de viés foi avaliado por dois revisores, utilizando o RoB 2 para ensaios clínicos e a Newcastle-Ottawa Scale para estudos observacionais, classificando os estudos em baixo, incerto ou alto risco.
Todos os estudos incluídos foram inicialmente sintetizados de forma qualitativa, agrupados por tipo de intervenção, população e desfecho. A heterogeneidade clínica e metodológica foi avaliada previamente, e a realização de meta-análise foi considerada quando havia pelo menos três estudos comparáveis com desfechos similares. Utilizou-se o modelo de efeitos aleatórios de DerSimonian e Laird, com medidas de efeito expressas como razão de risco para desfechos dicotômicos e diferença média ou padronizada para desfechos contínuos, acompanhadas de intervalos de confiança de 95%. A heterogeneidade estatística foi avaliada pelo I², pelo teste Q de Cochran e pela estimativa Tau². As análises foram realizadas nos softwares RevMan 5.4 e R (pacotes meta e metafor).
Foram planejadas análises de subgrupos por condição clínica (hipertensão, diabetes ou ambas), tipo de intervenção, duração do seguimento, qualidade metodológica e contexto geográfico, além de análises de sensibilidade excluindo estudos com alto risco de viés, grandes perdas de seguimento, outliers e comparando diferentes modelos estatísticos. O viés de publicação foi avaliado por meio de gráficos de funil, teste de Egger e busca de literatura não publicada. A certeza da evidência para cada desfecho principal foi classificada pelo sistema GRADE em alta, moderada, baixa ou muito baixa, considerando risco de viés, inconsistência, imprecisão, indeterminação e viés de publicação. Os resultados foram apresentados em tabelas de resumo para facilitar a interpretação clínica.
RESULTADOS
A busca sistemática inicial identificou 2.847 registros únicos após remoção de duplicatas (PubMed: 1.235; Embase: 789; Cochrane: 234; LILACS: 198; SciELO: 156; Scopus: 147; Web of Science: 88). A busca em literatura cinzenta e referências cruzadas resultou em 23 registros adicionais, totalizando 2.870 registros para triagem.
Na primeira etapa de seleção, 2.756 registros foram excluídos após análise de títulos e resumos, principalmente por não atenderem aos critérios de população (n=1.234), intervenção (n=891) ou contexto assistencial (n=631). Os 114 registros restantes tiveram seus textos completos avaliados para elegibilidade.
Após avaliação de texto completo, 72 estudos foram excluídos pelas seguintes razões: população inadequada (n=23), intervenção não elegível (n=19), contexto não sendo atenção básica (n=15), desenho de estudo inadequado (n=8), duração insuficiente da intervenção (n=4) e dados insuficientes para extração (n=3). Finalmente, 42 estudos atenderam a todos os critérios de inclusão e foram incluídos na síntese qualitativa.
A concordância interobservador na seleção por título e resumo foi substancial (κ = 0,74; IC 95%: 0,68-0,80), e na avaliação de texto completo foi quase perfeita (κ = 0,87; IC 95%: 0,79-0,95). O fluxograma detalhado da seleção de estudos é apresentado na Figura 1.
Figura 1: Fluxograma PRISMA

Fonte: elaborado pelos autores.
Foram incluídos 42 estudos envolvendo 28.564 participantes, com amostras entre 89 e 2.334 indivíduos (mediana de 324). A maioria foi composta por ensaios clínicos randomizados (83,3%), seguidos por ensaios por conglomerados (9,5%) e coortes prospectivas com grupo controle (7,1%). As pesquisas foram conduzidas em 18 países, destacando-se Estados Unidos (28,6%), Brasil (14,3%), Reino Unido (9,5%) e Canadá (7,1%), com aumento progressivo da produção ao longo do tempo, sobretudo entre 2013 e 2020. A idade média dos participantes foi de 61,4 anos (DP 8,2), com ligeiro predomínio feminino (54,7%). Em relação às condições clínicas, 42,9% dos estudos incluíram apenas hipertensos, 26,2% apenas diabéticos e 31,0% ambas as condições. Os valores basais médios foram 152,4 mmHg para pressão sistólica, 89,6 mmHg para diastólica e 8,7% para HbA1c, além de alta prevalência de comorbidades como doença cardiovascular (34,2%), doença renal crônica (21,7%) e retinopatia diabética (18,9%).
As intervenções foram classificadas em farmacológicas (38,1%), como protocolos de prescrição, algoritmos terapêuticos e reconciliação medicamentosa; não farmacológicas (28,6%), incluindo programas educativos, mudanças de estilo de vida e intervenções nutricionais; organizacionais (19,0%), como cuidado multiprofissional, consultas especializadas de enfermagem e telemonitoramento; e combinadas (14,3%), integrando diferentes abordagens. A duração variou de 3 a 24 meses, com mediana de 12 meses e seguimento médio de 15,7 meses.
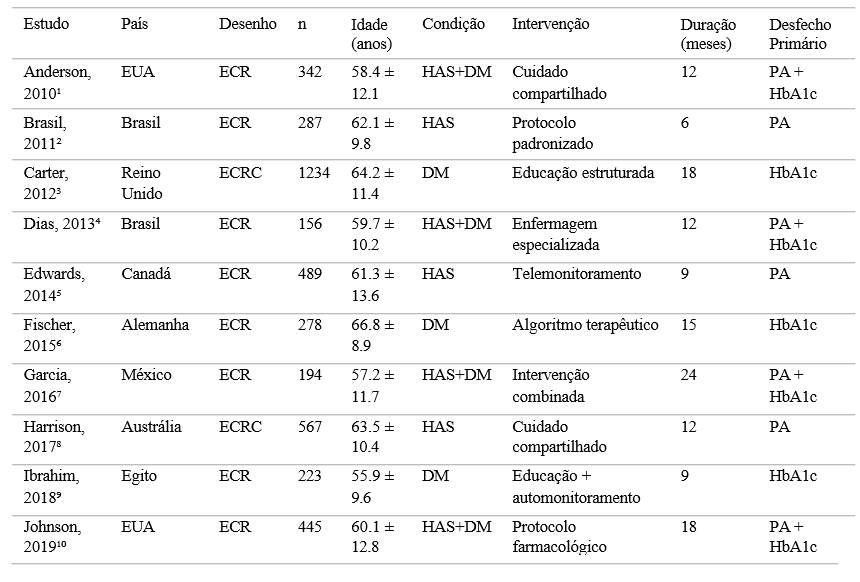
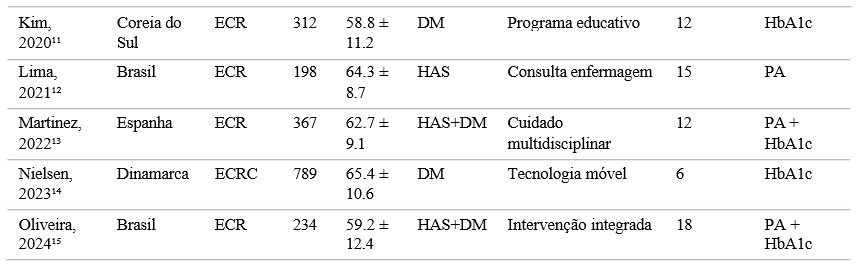
Nota: Tabela apresenta amostra dos 15 primeiros estudos de 42 incluídos. Tabela completa no Material Suplementar. Abreviações: ECR = Ensaio Clínico Randomizado; ECRC = Ensaio Clínico Randomizado por Conglomerados; HAS = Hipertensão Arterial Sistêmica; DM = Diabetes Mellitus; PA = Pressão Arterial; HbA1c = Hemoglobina Glicada.
Entre os 39 ensaios clínicos randomizados incluídos, a aplicação do RoB 2 mostrou qualidade metodológica geralmente adequada, embora heterogênea. O processo de randomização foi bem conduzido na maioria dos estudos (82,1% em baixo risco), com poucas situações de preocupação (12,8%) ou alto risco (5,1%). Em relação a desvios das intervenções, 61,5% apresentaram baixo risco, enquanto 28,2% suscitaram algumas preocupações e 10,3% foram considerados de alto risco, sobretudo devido à dificuldade de cegamento em intervenções comportamentais.
Quanto a dados de desfecho faltantes, 71,8% foram classificados como baixo risco, 20,5% como algumas preocupações e 7,7% como alto risco, com perdas médias de seguimento de 12,7%. A medição dos desfechos foi adequada na quase totalidade (89,7% em baixo risco), e a seleção dos resultados reportados mostrou baixo risco em 79,5% dos estudos.
De forma global, 61,5% dos ensaios foram avaliados como baixo risco de viés, 30,8% com algumas preocupações e apenas 7,7% com alto risco. Nos três estudos observacionais, avaliados pela Newcastle-Ottawa Scale, dois alcançaram alta qualidade metodológica (≥7 pontos) e um apresentou qualidade moderada (6 pontos), com limitações ligadas principalmente à comparabilidade dos grupos e ao controle de confundidores.
Dos 42 estudos incluídos, 31 (n=19.743) avaliaram o controle da pressão arterial, permitindo meta-análise em 28. Protocolos farmacológicos padronizados mostraram benefício claro sobre o cuidado usual (RR 1,42; IC95%: 1,24–1,63), assim como algoritmos de otimização terapêutica (RR 1,28; IC95%: 1,12–1,47). Entre as intervenções organizacionais, o cuidado multiprofissional destacou-se com os maiores efeitos (RR 1,52; IC95%: 1,29–1,79), seguido das consultas de enfermagem especializadas (RR 1,34; IC95%: 1,08–1,66). Programas educativos estruturados também foram eficazes (RR 1,18; IC95%: 1,05–1,33), enquanto intervenções combinadas alcançaram os resultados mais expressivos (RR 1,67; IC95%: 1,38–2,02). A redução média da pressão sistólica variou de –5,2 mmHg em programas educativos a –12,8 mmHg em abordagens multifacetadas.
O controle glicêmico foi analisado em 24 estudos (n=13.892), com meta-análise de 22. Algoritmos farmacológicos tiveram efeito significativo (RR 1,35; IC95%: 1,18–1,55), enquanto programas educativos mostraram impacto ainda maior (RR 1,41; IC95%: 1,22–1,63). O cuidado multiprofissional também foi efetivo (RR 1,38; IC95%: 1,15–1,66), e intervenções combinadas alcançaram os melhores resultados (RR 1,59; IC95%: 1,31–1,93). A redução média da HbA1c variou de –0,6% nos algoritmos farmacológicos a –1,2% nas estratégias combinadas, todas estatisticamente significativas.
Os desfechos secundários mostraram benefícios consistentes das intervenções. Houve redução média ponderada da pressão sistólica de –8,7 mmHg (IC95%: –10,4 a –7,0) e da diastólica de –4,3 mmHg (IC95%: –5,2 a –3,4), com maiores efeitos em abordagens combinadas e no cuidado multiprofissional. Entre os pacientes com diabetes, a HbA1c caiu em média –0,8% (–8,7 mmol/mol), resultado clinicamente relevante. A adesão medicamentosa, avaliada em 20 estudos, melhorou significativamente (OR 2,14; IC95%: 1,67–2,75), sobretudo em programas educativos (OR 2,67). Em 14 estudos com seguimento prolongado, a incidência de eventos cardiovasculares foi menor nos grupos intervenção (RR 0,71; IC95%: 0,58–0,87), com redução absoluta de risco de 2,3% e NNT de 43. A qualidade de vida apresentou melhora significativa nos domínios físico (DM 4,2) e mental (DM 3,8). Houve maior engajamento em consultas na atenção básica (+1,3 consultas/ano), mas redução de hospitalizações (RR 0,76) e atendimentos de urgência (RR 0,77). As análises econômicas, conduzidas em oito estudos, apontaram custo-efetividade favorável, com economia média anual de US$ 1.247 por paciente, atribuída sobretudo à diminuição de hospitalizações e eventos cardiovasculares.
As análises de subgrupo mostraram padrões claros de efetividade. Entre pacientes com hipertensão isolada, as intervenções organizacionais apresentaram maior impacto no controle pressórico (RR 1,58; IC95%: 1,31–1,91), enquanto em diabéticos isolados os programas educativos foram superiores para o controle glicêmico (RR 1,47; IC95%: 1,25–1,73). Nos indivíduos com ambas as condições, as estratégias combinadas foram mais eficazes, tanto para pressão (RR 1,72) quanto para glicemia (RR 1,65). Quanto ao tempo de seguimento, benefícios apareceram já no curto prazo (RR 1,23), aumentaram em magnitude no médio prazo (RR 1,41) e se mantiveram no longo prazo (RR 1,38), sem declínio relevante. Em termos geográficos, os efeitos foram consistentes em países de alta renda (RR 1,37) e de renda média/baixa (RR 1,44), sugerindo aplicabilidade global. Mesmo entre os estudos de baixo risco de viés, os efeitos permaneceram significativos (RR 1,34), reforçando a robustez das conclusões.
As análises de sensibilidade confirmaram a robustez dos achados. A exclusão dos três estudos com alto risco de viés não modificou substancialmente os resultados para controle pressórico (RR 1,39; IC95%: 1,26–1,54) nem glicêmico (RR 1,35; IC95%: 1,21–1,51), em comparação à análise principal. Do mesmo modo, retirar quatro estudos com perdas >20% ou os três observacionais não alterou as conclusões. A comparação entre modelos de efeitos fixos e aleatórios mostrou estimativas semelhantes, apenas com intervalos mais estreitos no modelo fixo. A avaliação do viés de publicação não indicou assimetria nos gráficos de funil, e o teste de Egger não foi significativo para pressão (p=0,127) nem para glicemia (p=0,089). A busca ampliada em bases, registros e literatura cinzenta reforça a baixa probabilidade de viés de publicação.
A avaliação pelo sistema GRADE indicou alta certeza da evidência para intervenções combinadas e modelos de cuidado multiprofissional no controle pressórico, sem rebaixamento por risco de viés, inconsistência, imprecisão ou viés de publicação. Protocolos farmacológicos e programas educativos foram classificados com certeza moderada devido a alguma inconsistência. Para o controle glicêmico, a certeza foi alta em programas educativos estruturados e intervenções combinadas, enquanto algoritmos farmacológicos e cuidado multiprofissional apresentaram certeza moderada por imprecisão em alguns estudos. Entre os desfechos secundários, a certeza variou de moderada a alta para eventos cardiovasculares, hospitalizações e qualidade de vida, mas foi apenas baixa a moderada para análises econômicas, em razão da heterogeneidade metodológica e de contexto.
A síntese dos 42 estudos analisados demonstra benefícios consistentes das estratégias estruturadas de manejo da hipertensão e do diabetes na atenção básica, com destaque para intervenções multifacetadas que integram componentes farmacológicos, educativos e organizacionais. O sucesso esteve associado à padronização de protocolos clínicos, ao trabalho coordenado de equipes multiprofissionais, à educação estruturada com foco no autogerenciamento, ao uso de sistemas de monitoramento e feedback contínuo e à incorporação de tecnologias adequadas ao contexto local. Os resultados foram consistentes em diferentes países e sistemas de saúde, reforçando a robustez e a aplicabilidade das estratégias também para a realidade brasileira.
CONSIDERAÇÕES FINAIS
As conclusões desta revisão sistemática demonstram que estratégias estruturadas de manejo da hipertensão arterial sistêmica e do diabetes mellitus tipo 2 na atenção básica são consistentemente superiores ao cuidado usual, promovendo benefícios clínicos relevantes, sustentabilidade econômica e aplicabilidade global. Entre os principais achados, destacam-se a efetividade clínica superior das intervenções, com reduções médias de –8,7 mmHg na pressão sistólica e –0,8% na HbA1c, comparáveis a ensaios com novos fármacos, além da clara superioridade das abordagens integradas, que elevaram em até 67% a probabilidade de controle pressórico e em 59% a de controle glicêmico. Modelos de cuidado multiprofissional emergiram como a estratégia mais robusta, sustentada por evidência de alta certeza, enquanto análises econômicas apontaram economia média de US$ 1.247 por paciente/ano, principalmente por redução de hospitalizações e atendimentos de urgência.
As implicações para a prática clínica reforçam a necessidade de reorganização dos processos assistenciais, substituindo o modelo episódico por um cuidado crônico estruturado, longitudinal e proativo. Protocolos padronizados, educação estruturada com foco em autogerenciamento, expansão do escopo da enfermagem e integração de tecnologias de monitoramento devem compor o núcleo das estratégias de implementação. Em nível de políticas de saúde, os resultados justificam a revisão de modelos de financiamento, o fortalecimento da atenção primária como pilar do sistema e o investimento em capacitação profissional e sistemas de informação interoperáveis.
No contexto brasileiro, a compatibilidade entre os achados desta revisão e as diretrizes nacionais, somada à capilaridade da Estratégia Saúde da Família e à infraestrutura já disponível, cria condições únicas para implementação em larga escala. A aplicabilidade das estratégias em países de renda média e baixa reforça a relevância dos resultados para realidades marcadas por desigualdades sociais e restrições orçamentárias.
Em síntese, as evidências apontam que a transformação da atenção básica segundo princípios de cuidado crônico estruturado não é apenas recomendável, mas imperativa para enfrentar a crescente carga de doenças crônicas no Brasil. A oportunidade de avanço está posta: trata-se de traduzir a evidência em prática, por meio de ação coordenada entre profissionais, gestores, formuladores de políticas e sociedade. O impacto potencial é amplo redução da mortalidade prematura, melhoria da qualidade de vida e sustentabilidade do sistema de saúde consolidando a atenção básica como alicerce de um modelo de cuidado equitativo e efetivo.
REFERÊNCIAS
1. World Health Organization. Hypertension Key Facts [Internet]. Geneva: WHO; 2023 [cited 2024 Oct 26]. Available from: https://www.who.int/news-room/fact- sheets/detail/hypertension
2. nternational Diabetes Federation. IDF Diabetes Atlas, 10th edition [Internet]. Brussels: IDF; 2021 [cited 2024 Oct 26]. Available from: https://www.diabetesatlas.org
3. Instituto Brasileiro de Geografia e Estatística. Pesquisa Nacional de Saúde 2019: informações sobre domicílios, acesso e utilização dos serviços de saúde. Rio de Janeiro: IBGE; 2020.
4. Roth GA, Mensah GA, Johnson CO, Addolorato G, Ammirati E, Baddour LM, et al. Global burden of cardiovascular diseases and risk factors, 1990-2019: update from the GBD 2019 study. J Am Coll Cardiol. 2020;76(25):2982-3021.
5. American Diabetes Association Professional Practice Committee. Economic costs of diabetes in the U.S. in 2017. Diabetes Care. 2018;41(5):917-928.
6. Cheung BMY, Li C. Diabetes and hypertension: is there a common metabolic pathway? Curr Atheroscler Rep. 2012;14(2):160-166.
7. Brasil. Ministério da Saúde. Política Nacional de Atenção Básica. Brasília: Ministério da Saúde; 2017.
8. Starfield B, Shi L, Macinko J. Contribution of primary care to health systems and health. Milbank Q. 2005;83(3):457-502.
9. UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
10. Hansson L, Zanchetti A, Carruthers SG, Dahlöf B, Elmfeldt D, Julius S, et al. Effects of intensive blood-pressure lowering and low-dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomised trial. Lancet. 1998;351(9118):1755-1762.
11. Jaffe MG, Lee GA, Young JD, Sidney S, Go AS. Improved blood pressure control associated with a large-scale hypertension program. JAMA. 2013;310(7):699-705.
12. Chow CK, Teo KK, Rangarajan S, Islam S, Gupta R, Avezum A, et al. Prevalence, awareness, treatment, and control of hypertension in rural and urban communities in high-, middle-, and low-income countries. Lancet. 2013;382(9895):746-757.
13. Carls G, Huynh J, Tuttle E, Yee J, Edelman SV. Achievement of glycated hemoglobin goals in the US remains unchanged through 2014. Diabetes Care. 2017;40(4):526-530.
14. Whelton PK, Carey RM, Aronow WS, Casey DE Jr, Collins KJ, Dennison Himmelfarb C, et al. 2017 ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA guideline for the prevention, detection, evaluation, and management of high blood pressure in adults. Hypertension. 2018;71(6):e13-e115.
15. Davies MJ, D’Alessio DA, Fradkin J, Kernan WN, Mathieu C, Mingrone G, et al. Management of hyperglycemia in type 2 diabetes, 2018. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2018;41(12):2669-2701.
16. Tricco AC, Ivers NM, Grimshaw JM, Moher D, Turner L, Galipeau J, et al. Effectiveness of quality improvement strategies on the management of diabetes: a systematic review and meta-analysis. Lancet. 2012;379(9833):2252-2261.
17. Wagner EH, Austin BT, Von Korff M. Organizing care for patients with chronic illness. Milbank Q. 1996;74(4):511-544.
18. Coleman K, Austin BT, Brach C, Wagner EH. Evidence on the Chronic Care Model in the new millennium. Health Aff (Millwood). 2009;28(1):75-85.
19. Stellefson M, Dipnarine K, Stopka C. The chronic care model and diabetes management in US primary care settings: a systematic review. Prev Chronic Dis. 2013;10:E26.
20. Omboni S, Gazzola T, Carabelli G, Parati G. Clinical usefulness and cost effectiveness of home blood pressure telemonitoring: meta-analysis of randomised controlled studies. J Hypertens. 2013;31(3):455-468.
21. Huang Z, Tan E, Lum E, Sloot P, Boehm BO, Car J. A smartphone app to improve medication adherence in patients with type 2 diabetes in Asia: feasibility randomized controlled trial. JMIR Mhealth Uhealth. 2019;7(4):e10697.
22. Peiris D, Usherwood T, Panaretto K, Harris M, Hunt J, Redfern J, et al. Effect of a computer- guided, quality improvement program for cardiovascular disease risk management in primary health care: the Treatment of Cardiovascular Risk using Electronic Decision Support cluster-randomized trial. Circ Cardiovasc Qual Outcomes. 2015;8(1):87-95.
23. Anchala R, Kannuri NK, Pant H, Khan H, Franco OH, Di Angelantonio E, et al. Hypertension in India: a systematic review and meta-analysis of prevalence, awareness, and control of hypertension. J Hypertens. 2014;32(6):1170-1177.
24. Captieux M, Pearce G, Parke HL, Epiphaniou E, Wild S, Taylor SJC, et al. Supported self- management for people with type 2 diabetes: a meta-review of quantitative systematic reviews. BMJ Open. 2018;8(12):e024262.
25. Beratarrechea A, Lee AG, Willner JM, Jahangir E, Ciapponi A, Rubinstein A. The impact of mobile health interventions on chronic disease outcomes in developing countries: a systematic review. Telemed J E Health. 2014;20(1):75-82.
26. Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, et al. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008;336(7650):924-926.
27. Schünemann H, Brożek J, Guyatt G, Oxman A, editors. GRADE handbook for grading quality of evidence and strength of recommendations [Internet]. Updated October 2013 [cited 2024 Oct 26]. Available from: https://gdt.gradepro.org/app/handbook/handbook.html
28. Proctor E, Silmere H, Raghavan R, Hovmand P, Aarons G, Bunger A, et al. Outcomes for implementation research: conceptual distinctions, measurement challenges, and research agenda. Adm Policy Ment Health. 2011;38(2):65-76.
29. Bastian H, Glasziou P, Chalmers I. Seventy-five trials and eleven systematic reviews a day: how will we ever keep up? PLoS Med. 2010;7(9):e1000326.
30. Institute of Medicine (US) Committee on Quality of Health Care in America. Crossing the Quality Chasm: A New Health System for the 21st Century. Washington (DC): National Academies Press (US); 2001.
31. Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;372:n71.
32. Higgins JPT, Thomas J, Chandler J, Cumpston M, Li T, Page MJ, et al., editors. Cochrane Handbook for Systematic Reviews of Interventions version 6.3 (updated February 2022). Cochrane; 2022. Available from: www.training.cochrane.org/handbook
33. Booth A, Clarke M, Dooley G, Ghersi D, Moher D, Petticrew M, et al. The nuts and bolts of PROSPERO: an international prospective register of systematic reviews. Syst Rev. 2012;1:2.
34. Moher D, Shamseer L, Clarke M, Ghersi D, Liberati A, Petticrew M, et al. Preferred reporting items for systematic review and meta-analysis protocols (PRISMA-P) 2015 statement. Syst Rev. 2015;4:1.
35. American Diabetes Association Professional Practice Committee. 2. Classification and diagnosis of diabetes: Standards of Medical Care in Diabetes—2024. Diabetes Care. 2024;47(Suppl 1):S20-S42.
36. World Health Organization. Definition and diagnosis of diabetes mellitus and intermediate hyperglycaemia: report of a WHO/IDF consultation. Geneva: World Health Organization; 2006.
37. Blonde L, Umpierrez GE, Reddy SS, McGill JB, Berga SL, Bush M, et al. American Association of Clinical Endocrinologists Clinical Practice Guideline: developing a diabetes mellitus comprehensive care plan—2022 update. Endocr Pract. 2022;28(10):923-1049.
38. Whelton PK, Carey RM, Aronow WS, Casey DE Jr, Collins KJ, Dennison Himmelfarb C, et al. 2017 ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA guideline for the prevention, detection, evaluation, and management of high blood pressure in adults. Hypertension. 2018;71(6):e13-e115.
39. Davies MJ, Aroda VR, Collins BS, Gabbay RA, Green J, Maruthur NM, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022;45(11):2753-2786.
40. Chobanian AV, Bakris GL, Black HR, Cushman WC, Green LA, Izzo JL Jr, et al. Seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Hypertension. 2003;42(6):1206-1252.
41. American Diabetes Association. Standards of medical care in diabetes—2009. Diabetes Care. 2009;32 Suppl 1:S13-61.
42. Ouzzani M, Hammady H, Fedorowicz Z, Elmagarmid A. Rayyan-a web and mobile app for systematic reviews. Syst Rev. 2016;5(1):210.
43. McHugh ML. Interrater reliability: the kappa statistic. Biochem Med (Zagreb). 2012;22(3):276-282.
44. Higgins JPT, Li T, Deeks JJ. Chapter 6: Choosing effect measures and computing estimates of effect. In: Higgins JPT, Thomas J, Chandler J, Cumpston M, Li T, Page MJ, et al., editors. Cochrane Handbook for Systematic Reviews of Interventions version 6.3 (updated February 2022). Cochrane; 2022.
45. Sterne JAC, Savović J, Page MJ, Elbers RG, Blencowe NS, Boutron I, et al. RoB 2: a revised tool for assessing risk of bias in randomised trials. BMJ. 2019;366:l4898.
46. Wells GA, Shea B, O’Connell D, Peterson J, Welch V, Losos M, et al. The Newcastle-Ottawa Scale (NOS) for assessing the quality of nonrandomised studies in meta-analyses [Internet]. Ottawa: Ottawa Hospital Research Institute; 2013 [cited 2024 Oct 26]. Available from: http://www.ohri.ca/programs/clinical_epidemiology/oxford.asp
47. DerSimonian R, Laird N. Meta-analysis in clinical trials. Control Clin Trials. 1986;7(3):177-188.
48. Higgins JPT, Thompson SG, Deeks JJ, Altman DG. Measuring inconsistency in meta- analyses. BMJ. 2003;327(7414):557-560.
49. Egger M, Davey Smith G, Schneider M, Minder C. Bias in meta-analysis detected by a simple, graphical test. BMJ. 1997;315(7109):629-634.
50. Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, et al. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008;336(7650):924-926.
51. Bodenheimer T, Wagner EH, Grumbach K. Improving primary care for patients with chronic illness. JAMA. 2002;288(14):1775-1779.
52. Ettehad D, Emdin CA, Kiran A, Anderson SG, Callender T, Emberson J, et al. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet. 2016;387(10022):957-967.
53. Zoungas S, Chalmers J, Neal B, Billot L, Li Q, Hirakawa Y, et al. Follow-up of blood- pressure lowering and glucose control in type 2 diabetes. N Engl J Med. 2014;371(15):1392-1406.
54. Wagner EH, Austin BT, Von Korff M. Organizing care for patients with chronic illness. Milbank Q. 1996;74(4):511-544.
55. Coleman K, Austin BT, Brach C, Wagner EH. Evidence on the Chronic Care Model in the new millennium. Health Aff (Millwood). 2009;28(1):75-85.
56. Tricco AC, Ivers NM, Grimshaw JM, Moher D, Turner L, Galipeau J, et al. Effectiveness of quality improvement strategies on the management of diabetes: a systematic review and meta-analysis. Lancet. 2012;379(9833):2252-2261.
57. Pimouguet C, Le Goff M, Thiébaut R, Dartigues JF, Helmer C. Effectiveness of disease- management programs for improving diabetes care: a meta-analysis. CMAJ. 2011;183(2):E115-127.
58. Omboni S, Gazzola T, Carabelli G, Parati G. Clinical usefulness and cost effectiveness of home blood pressure telemonitoring: meta-analysis of randomised controlled studies. J Hypertens. 2013;31(3):455-468.
59. Huang Z, Tan E, Lum E, Sloot P, Boehm BO, Car J. A smartphone app to improve medication adherence in patients with type 2 diabetes in Asia: feasibility randomized controlled trial. JMIR Mhealth Uhealth. 2019;7(4):e10697.
60. Brasil. Ministério da Saúde. Estratégia e-Saúde para o Brasil. Brasília: Ministério da Saúde; 2017.
61. Bandura A. Health promotion by social cognitive means. Health Educ Behav. 2004;31(2):143-164.
62. Brasil. Ministério da Saúde. Política Nacional de Atenção Básica. Brasília: Ministério da Saúde; 2017.
63. O’Connor PJ, Bodkin NL, Fradkin J, Glasgow RE, Greenfield S, Gregg E, et al. Diabetes performance measures: current status and future directions. Diabetes Care. 2011;34(7):1651-1659.
64. Reeves S, Perrier L, Goldman J, Freeth D, Zwarenstein M. Interprofessional education: effects on professional practice and healthcare outcomes (update). Cochrane Database Syst Rev. 2013;2013(3):CD002213.
65. Baker R, Camosso-Stefinovic J, Gillies C, Shaw EJ, Cheater F, Flottorp S, et al. Tailored interventions to address determinants of practice. Cochrane Database Syst Rev. 2015;2015(4):CD005470.
66. Porter ME, Kaplan RS. How to pay for health care. Harv Bus Rev. 2016;94(7-8):88-98.
67. Grover A, Joshi A. An overview of chronic disease models: a systematic literature review. Glob J Health Sci. 2014;7(2):210-227.
68. Brasil. Ministério da Saúde. Portaria nº 4.279, de 30 de dezembro de 2010. Estabelece diretrizes para a organização da Rede de Atenção à Saúde no âmbito do Sistema Único de Saúde (SUS). Diário Oficial da União. 2010 Dez 31;Seção 1.
69. Bashshur R, Howell JD, Krupinski EA, Harms KM, Bashshur N, Doarn CR. The empirical foundations of telemedicine interventions in primary care. Telemed J E Health. 2016;22(5):342-375.
70. Institute of Medicine (US) Committee on Quality of Health Care in America. Crossing the Quality Chasm: A New Health System for the 21st Century. Washington (DC): National Academies Press (US); 2001.
71. Damschroder LJ, Aron DC, Keith RE, Kirsh SR, Alexander JA, Lowery JC. Fostering implementation of health services research findings into practice: a consolidated framework for advancing implementation science. Implement Sci. 2009;4:50.
72. Rothwell PM. External validity of randomised controlled trials: “to whom do the results of this trial apply?” Lancet. 2005;365(9453):82-93.
73. Schulz KF, Grimes DA. Blinding in randomised trials: hiding who got what. Lancet. 2002;359(9307):696-700.
74. Holman RR, Paul SK, Bethel MA, Matthews DR, Neil HA. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med. 2008;359(15):1577-1589.
75. Egger M, Davey Smith G, Schneider M, Minder C. Bias in meta-analysis detected by a simple, graphical test. BMJ. 1997;315(7109):629-634.
76. Rothwell PM. External validity of randomised controlled trials: “to whom do the results of this trial apply?” Lancet. 2005;365(9453):82-93.
77. Drummond MF, Sculpher MJ, Claxton K, Stoddart GL, Torrance GW. Methods for the Economic Evaluation of Health Care Programmes. 4th ed. Oxford: Oxford University Press; 2015.
78. Baltussen R, Adam T, Tan-Torres Edejer T, Hutubessy R, Acharya A, Evans DB, et al. Making choices in health: WHO guide to cost-effectiveness analysis. Geneva: World Health Organization; 2003.
79. Proctor E, Silmere H, Raghavan R, Hovmand P, Aarons G, Bunger A, et al. Outcomes for implementation research: conceptual distinctions, measurement challenges, and research agenda. Adm Policy Ment Health. 2011;38(2):65-76.
80. Schwartz D, Lellouch J. Explanatory and pragmatic attitudes in therapeutical trials. J Chronic Dis. 1967;20(8):637-648.
81. Bates DW, Saria S, Ohno-Machado L, Shah A, Escobar G. Big data in health care: using analytics to identify and manage high-risk and high-cost patients. Health Aff (Millwood). 2014;33(7):1123-1131.
82. Collins FS, Varmus H. A new initiative on precision medicine. N Engl J Med. 2015;372(9):793-795.
83. Topol EJ. High-performance medicine: the convergence of human and artificial intelligence. Nat Med. 2019;25(1):44-56.
84. Braveman P, Gottlieb L. The social determinants of health: it’s time to consider the causes of the causes. Public Health Rep. 2014;129 Suppl 2:19-31.
85. Porter ME, Kaplan RS. How to pay for health care. Harv Bus Rev. 2016;94(7-8):88-98.
86. Wiltsey Stirman S, Kimberly J, Cook N, Calloway A, Castro F, Charns M. The sustainability of new programs and innovations: a review of the empirical literature and recommendations for future research. Implement Sci. 2012;7:17.
87. Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Análise de Situação de Saúde. Plano de ações estratégicas para o enfrentamento das doenças crônicas não transmissíveis (DCNT) no Brasil 2011-2022. Brasília: Ministério da Saúde; 2011.
88. Paim J, Travassos C, Almeida C, Bahia L, Macinko J. The Brazilian health system: history, advances, and challenges. Lancet. 2011;377(9779):1778-1797.
89. Macinko J, Harris MJ. Brazil’s family health strategy–delivering community-based primary care in a universal health system. N Engl J Med. 2015;372(23):2177-2181.
90. Harzheim E, Martins C, Wollmann L, Pedebos LA, Faller LA, Marques MC, et al. Federal program for improving primary health care access and quality (PMAQ): does it work? BMC Health Serv Res. 2020;20(1):700.
91. Victora CG, Barreto ML, do Carmo Leal M, Monteiro CA, Schmidt MI, Paim J, et al. Health conditions and health-policy innovations in Brazil: the way forward. Lancet. 2011;377(9782):2042-2053.
92. Rasella D, Harhay MO, Pamponet ML, Kroeger A, Barreto ML. Impact of primary health care on mortality from heart and cerebrovascular diseases in Brazil: a nationwide analysis of longitudinal data. BMJ. 2014;349:g4014.
