REGISTRO DOI: 10.69849/revistaft/ni10202511231528
Gabriella Da Silva Rodrigues
Léo Vitor Alves De Abreu
Mariana Guedes De Sousa Cruz
Orientadora: Dra. Caroline Castro de Araújo
RESUMO
A Síndrome do Intestino Irritável (SII) é um distúrbio gastrointestinal funcional caracterizado por dor abdominal recorrente e alterações do hábito intestinal, afetando negativamente a qualidade de vida. Este estudo teve como objetivo analisar, por meio de revisão integrativa, as principais intervenções dietéticas utilizadas no manejo dos sintomas da SII. A busca foi realizada nas bases PubMed e SciELO, em artigos publicados nos últimos dez anos, utilizando descritores relacionados à síndrome, microbiota intestinal, fibras, prebióticos, probióticos e dietas específicas. Foram incluídos estudos clínicos e de coorte, enquanto revisões, relatos de caso e artigos envolvendo outras doenças gastrointestinais foram excluídos. Ao final da seleção, 9 estudos compuseram a amostra. Os resultados demonstraram que a dieta com baixo teor de FODMAPs é eficaz na redução de dor, na distensão abdominal e em irregularidades intestinais, porém pode reduzir a ingestão de fibras e micronutrientes. A dieta com redução de amido e sacarose (SSRD) mostrou eficácia semelhante, com melhor equilíbrio nutricional. O uso de fibras solúveis, como psyllium, e a suplementação de probióticos e prebióticos também apresentaram benefícios, especialmente quando personalizados ao subtipo da SII. Conclui-se que o manejo dietético deve ser individualizado, com acompanhamento profissional contínuo.
Palavras-chave: Síndrome do intestino irritável; FODMAP; fibras alimentares; microbiota intestinal; probióticos.
ABSTRACT
Irritable Bowel Syndrome (IBS) is a functional gastrointestinal disorder characterized by recurrent abdominal pain and changes in bowel habits, which negatively affect quality of life. This study aimed to analyze, through an integrative literature review, the main dietary interventions used to manage IBS symptoms. The search was conducted in the PubMed and SciELO databases, including articles published in the last ten years and using descriptors related to IBS, intestinal microbiota, fibers, prebiotics, probiotics, and dietary approaches. Clinical and cohort studies were included, while reviews, case reports, and studies involving other gastrointestinal diseases were excluded. A total of 9 studies were selected. The results demonstrated that the low-FODMAP diet effectively reduces abdominal pain, bloating, and bowel irregularities, although it may reduce fiber and micronutrient intake. The starch- and sucrose-restricted diet (SSRD) showed similar efficacy, with better nutritional balance. The use of soluble fibers, such as psyllium, as well as probiotic and prebiotic supplementation, also showed benefits, especially when tailored to the IBS subtype. It is concluded that dietary management should be individualized, with continuous professional monitoring.
Keywords: Irritable bowel syndrome; FODMAP; dietary fiber; intestinal microbiota; probiotics
1 INTRODUÇÃO
A Síndrome do Intestino Irritável (SII) é um distúrbio funcional gastrointestinal caracterizado por dor abdominal recorrente associada a alterações nos hábitos intestinais, sem evidência de anormalidades estruturais ou bioquímicas detectáveis. Estima-se que a SII afeta entre 10% e 20% da população mundial, impactando significativamente a qualidade de vida dos indivíduos acometidos (SHAMS et al., 2024).
Embora possa acometer qualquer pessoa, estudos apontam que a SII é mais frequente em mulheres, com uma proporção de até duas para cada homem diagnosticado, principalmente em países ocidentais (CHEY et al., 2015; FAKUDO et al.,2023). Além disso, as manifestações da síndrome também variam de acordo com o sexo, as mulheres costumam apresentar constipação, enquanto os homens têm episódios mais frequentes de diarreia (SHIN et al., 2018). As questões hormonais, como as oscilações de estrogênio e progesterona ao longo do ciclo menstrual, parecem agravar os sintomas em muitas mulheres, especialmente durante a menstruação. Adicionalmente, fatores emocionais, como ansiedade e depressão, que também são mais comuns nesse grupo, podem intensificar ainda mais o desconforto (FUKUDO et al., 2023).
A etiologia da SII é multifatorial, envolvendo interações complexas entre o eixo cérebro-intestino, motilidade gastrointestinal, hipersensibilidade visceral, alterações na microbiota intestinal e fatores psicossociais (STAUDACHER; WHELAN, 2016). Entre os principais fatores moduladores dos sintomas, destaca-se a alimentação, visto que muitos pacientes relatam agravamento dos sintomas após a ingestão de determinados alimentos (VAN LANEM; DE BREE; GREYLING, 2021).
Neste contexto, diversas intervenções dietéticas vêm sendo estudadas. A dieta com baixo teor de FODMAPs tem mostrado eficácia na redução dos sintomas da SII, sendo recomendada como abordagem inicial em protocolos clínicos (VAN LANEN; DE BREE; GREYLING, 2021). Além disso, a suplementação de fibras, prebióticos e probióticos também se mostra promissora, contribuindo para a modulação da microbiota intestinal e para a diminuição da hipersensibilidade visceral (WANG et al., 2020).
A atuação da microbiota intestinal na SII tem sido amplamente estudada, sugerindo que o desequilíbrio na composição microbiana intestinal pode estar associado à alteração e aumento dos sintomas, o que reforça a importância de estratégias que promovam o seu reequilíbrio (STAUDACHER; WHELAN, 2016). Diante da relevância clínica e do impacto na qualidade de vida dos pacientes com SII, o presente trabalho tem como objetivo analisar por meio da literatura científica recente, como fibras, prebióticos, probióticos, medicamentos, dieta low FODMAP e a microbiota intestinal influenciam no manejo dos sintomas da SII.
2 REFERENCIAL TEÓRICO
2.1 Fisiopatologia das DII
A Síndrome do Intestino Irritável (SII) caracteriza-se como um grupo heterogêneo de enfermidades que envolvem inflamação crônica e recorrente do trato gastrointestinal, cuja etiologia e patogênese permanecem incompletamente elucidadas. De acordo com a revisão integrativa, a etiologia da DII está associada a múltiplos fatores de risco, incluindo disfunções no sistema imunológico do hospedeiro, predisposição genética e influências ambientais (SAEZ et al., 2023).
O desenvolvimento da DII ocorre em indivíduos geneticamente suscetíveis, nos quais uma resposta imune desregulada, tanto inata quanto adaptativa, contribui para o processo inflamatório crônico. Esse desequilíbrio imunológico pode estar implicado na manifestação de outras condições gastrointestinais funcionais, como a Síndrome do Intestino Irritável (SII), embora a relação entre essas patologias ainda não esteja totalmente compreendida. A desregulação do sistema imune inato está diretamente associada à progressão da DII (SAEZ et al., 2023).
Estima-se que a SII afete entre 5% e 10% da população ao longo da vida, com períodos de melhora intercalados por recaídas. Essa condição é mais comum em mulheres jovens e em pessoas que enfrentam transtornos psicológicos, como ansiedade e depressão. Embora sua causa exata ainda não seja completamente compreendida, sabe-se que a SII está relacionada a um desequilíbrio na comunicação entre o intestino e o cérebro, levando a mudanças na motilidade intestinal, aumento da sensibilidade visceral e um processamento diferenciado dos estímulos pelo sistema nervoso central. Além disso, fatores como infecções intestinais, microbiota alterada e predisposição genética também podem contribuir para o seu desenvolvimento (OKA et al., 2020).
Atualmente, os critérios de Roma IV, amplamente utilizados para o diagnóstico da Síndrome do Intestino Irritável (SII), reconhecem que os distúrbios gastrointestinais funcionais (FGIDs) não se apresentam como doenças isoladas, mas sim como condições que ocorrem em um espectro contínuo de manifestações clínicas. Essa compreensão mais abrangente considera que a sobreposição de sintomas entre diferentes regiões do trato gastrointestinal é um fenômeno comum e natural.
Um estudo com 54.127 adultos, distribuídos por 26 países, demonstrou que 68,3% apresentavam sintomas sobrepostos entre diferentes regiões gastrointestinais, e 2,3% relataram sintomas simultâneos nas regiões esofágica, gastroduodenal, intestinal e anorretal. Esses achados reforçam a ideia de que os FGIDs frequentemente coexistem e compartilham características clínicas, especialmente sintomas associados a fatores emocionais, como ansiedade e depressão. Esses fatores, por sua vez, corroboram a importância do eixo cérebro-intestino e do sistema nervoso central na fisiopatologia dessas condições (LIU et al., 2023)
Parte do diagnóstico pode ser feito com base em histórico clínico do paciente, porém com uso limitado e criterioso de investigação, a menos que o indivíduo já apresente ou haja algum histórico família de doença inflamatória intestinal (DII) sendo considerado sintomas de alarme temos, perda de peso, sangramento retal, distensão abdominal, sensação de evacuação incompleta ou situação de urgência por. Uma vez feito o diagnostico, deve-se adotar uma abordagem empática é fundamental para uma melhora da qualidade de vida e uma diminuição dos sintomas, reduzindo assim os gastos com assistência médica e medicamentos (Ford et al., 2020).
2.2 Fatores causais
A síndrome do intestino irritável é um distúrbio gastrointestinal funcional, e uma das doenças mais comuns no trato gastrointestinal. Os sintomas que incluem dores abdominais e distúrbios do movimento intestinal associada a uma mudança na forma ou frequência das fezes. Por esse motivo, as principais formas de SII com constipação predominante (SII-C) e diarreia (SII-D) ou mista (SII-M), foram distinguidas. Esses sintomas não são permanentes, a síndrome do intestino irritável também é mais comum em pessoas com comorbidade psicológica e em mulheres adultas jovens do que no resto da população em geral. (KACZKA et al., 2025)
Pacientes com SII-C também podem apresentar sintomas abdominais como inchaço, desconforto, cólicas e plenitude. Os sintomas de dor abdominal e inchaço têm sido associados à hipersensibilidade visceral, que é uma sensação aumentada (BRENNER et al., 2024) em resposta a estímulos fisiológicos e ativação de nervos sensoriais viscerais aferentes. Além disso, a exacerbação da dor abdominal também tem sido associada ao aumento da permeabilidade intestinal, potencialmente permitindo maior infiltração de macromoléculas do lúmen intestinal para as camadas mais profundas do intestino (ou seja, submucosa). Os sintomas abdominais associados à SII-C podem resultar em maior uso de recursos de saúde, diminuição da produtividade no trabalho e redução da qualidade de vida relacionada à saúde. Embora os medicamentos de venda livre possam melhorar a consistência e a frequência das fezes, esses tratamentos têm como alvo principal os sintomas intestinais subjacentes da SII (ou seja, constipação e/ou diarreia) e podem não tratar os sintomas abdominais.
A síndrome do intestino irritável com diarreia (SII-D), apesar de sua alta prevalência, a SII-D está associada a grande incerteza, especialmente em relação ao seu diagnóstico e tratamento ideais. (SAVARINO et al., 2022). Indivíduos com SII-D apresentaram maior consumo de alimentos vegetais saudáveis, como grãos integrais, frutas, vegetais e leguminosas, além de maiores níveis de magnésio e ferro, enquanto ingeriam menos maltose e lactose, substâncias frequentemente associadas a sintomas como inchaço e diarreia. SII-D mostrou uma redução de bactérias anaeróbicas benéficas, produtoras de butirato, como Faecalibacterium prausnitzii, resultando em menor diversidade microbiana. Apesar do impacto de outros fatores, como idade, sexo e dieta, a composição da microbiota intestinal e suas funções metabólicas se destacaram como marcadores independentes, diferenciando indivíduos com SII-D.
Diversos estudos sugerem que fatores emocionais, como o estresse, a ansiedade e a depressão, desempenham um papel significativo na manifestação e na gravidade dessa condição. O impacto de fatores emocionais na SII está associado à interação entre o sistema nervoso e o trato gastrointestinal, com ênfase na conexão entre o cérebro e o intestino, conhecida como o eixo cérebro-intestino. Estudos demonstram que o estresse psicológico é um fator importante na ativação e exacerbação dos sintomas da SII (MAYER, 2011; CHANG et al., 2021).
O estresse pode alterar a motilidade gastrointestinal, aumentar a percepção da dor abdominal e modificar a microbiota intestinal. A ansiedade e a depressão também têm sido associadas a uma piora nos sintomas da SII, devido à influência no sistema nervoso autônomo e à liberação de substâncias inflamatórias que afetam a função gastrointestinal (FELDMAN et al., 2022). Os estressores desempenham um papel crítico na progressão da síndrome do intestino irritável (SII). (LÓPEZ-ÁLVAREZ et al., 2023). O estresse físico ou psicológico pode alterar a comunicação entre o cérebro e o intestino, levando a distúrbios na motilidade intestinal e no aumento da dor abdominal. Ansiedade e Depressão tem um impacto negativo sobre o controle das funções intestinais, o que pode intensificar os sintomas da SII. (PÉREZ-LÓPEZ., et al 2022). Estudos indicam que o tratamento adequado de fatores emocionais, como por meio de terapias cognitivas ou medicamentos ansiolíticos, pode ajudar a controlar os sintomas da SII.
O estresse heterogêneo causa alterações em nossos movimentos intestinais, o que pode causar ainda mais ansiedade e sintomas semelhantes aos da depressão, diminuindo a capacidade de indivíduos em todo o mundo de funcionar em ambientes sociais, acadêmicos e de emprego. (SHARMA et al., 2024) investigaram a eficácia do óleo de semente de Nigella sativa no tratamento de síndrome do intestino irritável e sintomas de ansiedade em ratos Wistar. (WU et al., 2024) A considerável carga de doença da síndrome do intestino irritável (SII) coincidiu com o aumento do consumo de alimentos ultraprocessados (AUP) nas últimas décadas. Participantes que completaram recordatórios alimentares de 24 horas durante 2009 a 2012 do UK Biobank, e livres de SII, doença celíaca, doença inflamatória intestinal e qualquer câncer no início do estudo, foram incluídos (N = 178.711; 53,1% mulheres). O consumo de UPF foi definido de acordo com o sistema de classificação de alimentos NOVA, expresso como uma porcentagem do conteúdo de UPF na ingestão total da dieta (em gramas por dia).
As principais causas que foram observadas nesta análise, foram síndrome do intestino irritável com constipação predominante (SII-C) e diarreia (SII-D) ou mista (SII-M). Estudos comprovam que fatores emocionais, influenciam na síndrome do intestino irritável como o estresse, a ansiedade e a depressão, têm um papel significativo na manifestação e na gravidade dessa condição, pois está associado à interação entre o sistema nervoso e o trato gastrointestinal.
2.2.1 Microbiota intestinal
A SII é um distúrbio complexo caracterizado por interações alteradas entre o intestino e o cérebro, com a microbiota gastrointestinal e a desregulação metabólica desempenhando papéis importantes em sua fisiopatologia. Identificar alterações metabólicas específicas na mucosa colônica pode melhorar nossa compreensão da SII e contribuir para melhores abordagens diagnósticas e terapêuticas (KRYNICKA et al., 2025). É cada vez mais percebido que as interações hospedeiro-microbiano do intestino são elementos importantes na patogênese de distúrbios gastrointestinais funcionais (FGID). A evidência mais convincente até o momento é a descoberta de que a dispepsia funcional e a síndrome do intestino irritável (SII) podem se desenvolver em indivíduos predispostos após um surto de gastroenterite infecciosa. Os resultados da abordagem demonstram mudanças quantitativas e qualitativas da microbiota intestinal mucosa e fecal, particularmente na SII.
Os pesquisadores também estão começando a medir as interações hospedeiro-microbiano na SII. Os ensaios controlados existentes de manipulação dietética, prebióticos, probióticos, simbióticos e antibióticos não absorvíveis são promissores, embora a maioria seja limitada pelo design subótimo e pequeno tamanho da amostra. A hipótese de trabalho atual é que a microbiota anormal ativa respostas imunes inatas da mucosa que aumentam a permeabilidade epitelial, ativam vias sensoriais nociceptivas e desregulam o sistema nervoso entérico, a microbiota já é um alvo terapêutico. Uma relação, frequentemente denominada simbiose, desenvolveu-se entre o hospedeiro e a microbiota intestinal ao longo de milhões de anos. Fatores genéticos e imunológicos do hospedeiro, bem como ambientais, influenciam a composição da microbiota intestinal que, por sua vez, molda a imunidade e a fisiologia do hospedeiro dentro e além do intestino (SIMREŃ et al., 2013).
Com o aprofundamento da compreensão do papel da microbiota intestinal na saúde e doença humana, o transplante de microbiota fecal ganhou ampla atenção como uma abordagem terapêutica emergente nos últimos anos. Esta técnica envolve o transplante de comunidades microbianas das fezes de doadores saudáveis em pacientes para reconstruir ou melhorar a estrutura da microbiota intestinal, alcançando assim objetivos terapêuticos.
O transplante de microbiota fecal se tornou um método eficaz para tratar infecções recorrentes ou refratárias por Clostridium difficile e demonstrou bons efeitos terapêuticos e segurança em ensaios clínicos para várias doenças gastrointestinais, incluindo doença inflamatória intestinal, síndrome do intestino irritável, constipação de trânsito lento e diarreia crônica. Os probióticos inibem a adesão de patógenos às células epiteliais intestinais regulando competitivamente a produção de bacteriocinas, ácidos graxos de cadeia curta e biossurfactantes pela microbiota intestinal (GAO et al., 2025; SIMREŃ et al., 2013).
Além disso, eles podem melhorar a função da barreira intestinal regulando negativamente a resposta imune leve da mucosa, melhorando a barreira do muco e estimulando a síntese de proteínas de junção estreita, ao mesmo tempo em que melhoram a imunidade intestinal inibindo citocinas pró-inflamatórias. Até agora, a pesquisa mostrou que os pacientes com SII apresentam diversidade reduzida da microbiota intestinal, especialmente em termos de diminuição de Firmicutes e aumento de Bacteroidetes em comparação com indivíduos saudáveis.
2.2.2 Tratamentos para a síndrome do intestino irritável
A síndrome do intestino irritável apresenta diferentes formas que se associam aos distúrbios causados ao sistema intestinal sendo comum casos de SII com constipação predominante (SII-C), SII com diarreia conhecida como (SII-D) ou mista (SII-M) por (CHEY et al., 2022).
Sendo assim de acordo com ensaios clínicos realizados por The American College of Gastroenterology (2021), um estudo realizado com Tenapanor que é um inibidor de moléculas pequenas, de primeira classe e de absorção mínima, sendo um trocador de sódio/hidrogênio isoforma 3 gastrointestinal. Neste estudo de fase 3 foi avaliado a eficácia e a segurança de pacientes fazerem o tratamento do tenapanor 50 mg bid a longo prazo para melhor da síndrome do intestino irritável com constipação (SII-C). Nos estudos realizados em formato de randomizado duplo-cego foi observado que em animais o tenapanor tinha feito de inibir o NHE3 é o NHE (que são dominante responsáveis pela absorção transepetelial de sódio), reduzindo assim a absorção de sódio e aumentando a excreção de sódio fazendo com que as fazes saiam de forma fluida aonde uma grande parte dos pacientes avaliados no estudo relataram melhora do quadro intestinal e apresentaram um boa tolerância ao tratamento, tendo como evento adverso a diarreia (CHEY et al., 2021).
O tratamento farmacológico da SII com diarreia (SII-D) apresentado pela American Gastroenterology Association como objetivo de suporte aos profissionais em decisões sobre medicamentos e é também uma atualização de uma revista técnica a diretrizes anteriores, a estrutura da avaliação de classificações de recomendações foi usada para avaliar evidências e fazer recomendações de acordo com a revisão técnica e questões clínicas apresentaram os seguintes medicamentos como agentes: eluxadolina, rifaximina, aldosterona, loperamida, antidepressivos tricíclicos, inibidores seletivos de recaptação de serotonina e antiespasmódicos. Todavia nem todas as recomendações apresentam resultados favoráveis para a melhora do quadro diarreico, porém em uma pesquisa sistemática foi relatado que todas as oito recomendações são seguras mesmo que com baixa eficácia para o tratamento síndrome do intestino irritável na Diarreia (SII-D) por (LEMBO et al., 2022).
A maioria dos pacientes são tratados com os tratamentos de cuidados primários, mas em contrapartida quando os tratamentos de primeira linha são ineficazes para o tratamento da SII. A partir dessa necessidade, surgem os novos tratamentos como o proposto pela Diretriz do Instituto Nacional de Saúde e Excelência em Cuidados do Reino Unido que sugere considerar antidepressivos tricíclicos em uma baixa dosagem como o tratamento de segunda linha, mas a sua eficácia como forma de tratamento em cuidados primários segue desconhecida (FORD et al., 2023).
Estes são raramente prescritos para este cenário. Ainda em uma análise do estudo randomizado, duplo-cego e controlado por placebo (amitriptilina em baixa dose e titulado para síndrome do cólon irritável), para serem elegíveis para o estudo os participantes tinham que ter 18 anos ou mais, com a SII, de qualquer subtipo e sintomas contínuos e que tenham passado por outras formas de tratamento como mudanças de dieta e terapias de primeira linha, e apresentando exames como hemograma completo e proteína C-reativa normais, sorologia celíaca negativa e nenhuma evidência de ideação suicida. A até a atual vivencia esse é o maior estudo de um antidepressivo tricíclico como forma de tratamento para a SII já conduzido, apresentando um resultado produtivo e superior ao uso de amitriptilina em baixa dosagem ao uso de placebo como tratamento de segunda linha (FORD et al., 2023).
Uma revisão recente da AGA destacou a dieta pobre em carboidratos fermentáveis, como oligossacarídeos, dissacarídeos, monossacarídeos e polióis (FODMAPs) como uma das abordagens dietéticas mais eficazes, especialmente quando acompanhada por um profissional capacitado. Com isso, a combinação de mudanças alimentares personalizadas e o uso adequado de medicamentos tem se mostrado a forma mais eficiente e segura de aliviar os sintomas e melhorar a qualidade de vida dos pacientes com SII-D por (CHEY et al., 2022).
2.3 Tratamento dietético
As abordagens terapêuticas que envolvem ajustes na alimentação e uso de microrganismos benéficos geram grande interesse em indivíduos com síndrome do intestino irritável (SII), devido a sua segurança e boa aceitação. A intervenção nutricional tradicional envolve a inclusão de fibras na dieta, além da adoção de um plano alimentar com quantidades reduzidas de FODMAPs, sendo também uma alimentação isenta de glúten (FORD et al.,2020).
A ingestão de fibras tem múltiplos impactos no sistema gastrointestinal, embora ainda não compreendidos. Elas influenciam a microbiota intestinal, o metabolismo, o tempo que leva para os alimentos percorrerem o trato digestivo, textura das fezes e a absorção de ácidos biliares. Em pacientes com SII, especialmente aqueles com constipação predominante, o consumo de fibras pode ser indicado para aliviar os sintomas (LACY et al., 2021).
No entanto, certos tipos de fibras ajudam a estimular o funcionamento intestinal ao reter água nas fezes e evitar a fermentação excessiva no cólon. Em contrapartida, aquelas que sofrem fermentação no intestino grosso podem perder essa capacidade de retenção de líquidos e gerar gases, o que pode intensificar sintomas como inchaço e flatulência (LACY et al.,2021).
Um estudo controlado randomizado concluiu que o uso de psyllium diminuiu a formação de gases provocados pela inulina (prebióticos) em indivíduos com SII, embora não tenha atuado diretamente na inibição do processo fermentativo. Além disso, o estudo indica que o consumo de fibras viscosas e de baixa fermentação, como o psyllium, junto com alimentos ricos em FODMAPs, pode reduzir a produção de gases no cólon de forma semelhante ao comparar com dieta pobre em FODMAPs. Sendo assim podendo minimizar sintomas sem comprometer a composição da microbiota intestinal ou exigir restrições alimentares. (GUNN et al., 2022).
A restrição de oligossacarídeos, dissacarídeos, monossacarídeos e polióis fermentáveis da alimentação, conhecidos como FODMAPs, tornou-se uma abordagem bastante popular e amplamente aplicada para o manejo da SII. Os FODMAPs podem causar um aumento da coordenação de fluidos no trato gastrointestinal e fermentação colônica, resultando na produção de ácidos graxos de cadeia curta e gases. Esse processo pode levar à distensão do lúmen e surgimento de sintomas gastrointestinais desencadeados pela ingestão alimentar em indivíduos com SII. (LACY et al., 2021).
Foi analisado em um ensaio clínico randomizado, pacientes com SII que foram atendidos na atenção primária, a adoção de uma alimentação com menor teor de FODMAP demonstrou maior eficácia na redução de sintomas em comparação ao uso de espasmolíticos (CARBONE et al., 2022). Em outro estudo clínico foi realizado uma reintrodução randomizada, mostrou que os pacientes apresentaram melhora nos sintomas da SII após seis semanas seguindo uma dieta com baixo teor de FODMAPs, onde foi caracterizada por uma redução na pontuação IBS-SSS, (Irritable Bowel Syndrome – Symptom Severity Scale), instrumento amplamente utilizado para mensurar a intensidade e o impacto clínico da doença, em relação ao começo do tratamento, logo depois foi avançado para uma reintrodução com duração de nove semanas. Durante esse período, receberam um dos seis compostos de FODMAP (frutanos, frutose, gacto-oligossacarídeos, lactose, manitol ou sorbitol) ou um controle contendo glicose. Um aumento de pelo menos 50 pontos no IBS-SSS foi utilizado para identificar FODMAPs pontos de gatilho (VAN DEN HOUTE et al., 2024).
Apesar de ganhar uma aceitação para o tratamento da síndrome do intestino irritável, uma dieta baixa em FODMAP tem sido questionada sobre suas implicações nutricionais incertas. Em um ensaio clínico com pacientes diagnosticados com SII diarreica, foi imposto duas abordagens dietéticas, à dieta com baixa ingestão de FODMAPs e à intervenção dietética mNICE. A análise descreve que ambas as abordagens resultaram em redução de consumo energético e de carboidratos, porém o grupo que recebeu a dieta low-FODMAP, apresentou uma diminuição na ingestão de riboflavina e outros micronutrientes em comparação ao grupo mNICE (ESWARAN, 2020).
O uso de probióticos pode ser contemplado como estratégias não farmacêuticos que são incorporadas a diferentes protocolos, pois há evidências consideradas significativas que mostram sua eficácia no alívio dos sintomas da SII (GALICA et al., 2022). Um estudo clínico recente concluiu após a implementação de suplementos personalizados de prebióticos e probióticos, feitos para cada tipo de microbiota intestinal de cada tipo de paciente que foi envolvido no estudo, por quatro semanas. O resultado mostrou uma diminuição significativa da gravidade dos sintomas em pacientes com SII-D e SII-C(MATSUURA et al., 2024). Sendo assim, levantando uma discussão para que o tratamento dietético pra pacientes diagnosticados com SII, a importância de um tratamento individual e personalizado.
As diretrizes atuais reconhecem, ainda que com ressalvas, a utilização de probióticos como parte do manejo da síndrome do intestino irritável. É importante que o uso de cepas de probióticos sejam específicas e bem estudadas, as cepas de Lactobacillus e Bifidobacterium têm mostrado eficácia (BÁRBARA et al., 2023). Os mecanismos de probióticos como Lactiplantibacilus plantarum atuam na SII-D, foram estudados em um ensaio clínico que mostra uma modulação da microbiota intestinal, propriedades anti-inflamatórias, melhora na permeabilidade intestinal e promoção de compostos benéficos (MARTONI et al., 2023)
Um estudo observacional analisou prebióticos e probióticos específicos para a melhoria da qualidade de vida de pacientes com SII crônico, mostrando que os probióticos como Lactobacillus rhamnosus que são uma das cepas mais utilizadas, ajudam no equilíbrio da microbiota intestinal, Bifidobacterium é essencial para saúde intestinal é encontrado em suplementos usados no tratamento, Saccharomyces boulardii uma levedura que pode ajudar a tratar diarreias, Streptococcus thermophilus auxilia na digestão da lactose e melhora a saúde intestinal. Os prebióticos observados como a inulina ajuda a melhora da saúde digestiva, os frutooligossacarídeos (FOS) ajuda a estimular o crescimento de bactérias benéficas no intestino, e galactooligossacarídeos (GOS) encontrado no leite materno, contribui também para a saúde intestinal (BERTANI et al., 2024).
2.3.1 Uso de fibras solúveis e insolúveis
A síndrome do intestino irritável tem três subtipos clínicos: constipação, diarreia e mista (CAMACHO-DÍAZ et al., 2023). O tratamento que usa a fibra alimentar leva em consideração, tanto a composição química da fibra quanto os subtipos clínicos. Embora não haja tratamento adequado para a síndrome do intestino irritável com sintomas mais predominantes de constipação (SSI-C), fibras prebióticas e compostos probióticos têm sido usados para o alívio de queixas de SII-C (JANSSENDUIJGHUIJSEN et al., 2024).
A adoção de uma dieta baixa FODMAPs em pacientes diagnosticados com SII, pode ter em consequência uma ingestão inadequada de fibras. Em um estudo clínico foi realizado a introdução de dietas de baixo FODMAP, que se diferem no conteúdo final de fibras 23 g/d; bagaço de cana, 33 g/d; ou combinação de fibras (bagaço de cana com amido resistente), 45 g/d. Em conclusão, a suplementação de fibras no início de uma dieta low-FODMAP, foi capaz de mostrar que houve aumento no volume das fezes e normalizou o baixo teor de água nas fezes e o aumentou a motilidade intestinal. Sendo assim eficaz em pacientes com SSI-C (SO et al., 2022).
As fibras solúveis estão presentes em alimentos como psyllium, casca de ispagula, fibra de milho, policarbofilo, metilcelulose, farelo de aveia e na polpa de frutas e vegetais. Já a fibra insolúvel é mais comum no farelo de trigo, grãos integrais, cascas e sementes de frutas e vegetais (CHEY et al., 2022). Segundo as Diretrizes do American College of Gastroenterology (2021), o uso de fibra solúvel é fortemente recomendado para pacientes com SII, principalmente para aquelas que têm predominância em constipação, podendo aliviar os sintomas. Em contrapartida, a fibra insolúvel não demonstrou o mesmo benefício.
Em um ensaio randomizado duplo-cego, que teve o objetivo de analisar o uso e efeito do Fibre-fix, um suplemento contendo mistura de fibras alimentares, na microbiota intestinal, a capacidade fermentativa dessas fibras, qualidade do sono e de vida dos pacientes com SII, que já passaram por uma dieta low-FODMAP. Foi discutido a possibilidade dessas fibras evitar a fermentação intestinal, aumentando a biossíntese e metabolismo dos neurotransmissores que podem consequentemente melhorando a qualidade do sono e de vida dos pacientes com a síndrome do intestino irritável (YAN et al., 2020).
Uma possibilidade encontrada na literatura para o manejo do alívio a curto prazo dos sintomas da síndrome do intestino irritável, foi realizada em um ensaio clínico randomizado que utilizou uma suplementação da fibra de nopal (Opuntia ficusindica), uma fibra de planta de cacto, que tem em sua composição tanto fibras solúveis quanto insolúveis. Neste estudo o uso dessa fibra de nopal em doses de 20 e 30g/dia, mostrou uma melhora a curto prazo dos sintomas da SII, como a dor abdominal por exemplo (REMES-TROCHE et al., 2021). Porém, a adoção de intervenções terapêuticas nutricionais específicas, devem ser testadas por períodos de tempo determinados, caso não houver resposta clínica a intervenção dietética deve ser interrompida, e outra busca de alternativa deve ser analisada, seja por dietas diferentes, mediações ou outra forma de terapia (CHEY et al., 2022).
2.3.2 Uso de prebióticos e probióticos
Em pesquisas recentes é mostrado que as células do sistema imunológico e do epitélio intestinal conseguem diferenciar os tipos de microrganismos. Sendo assim, facilitou o entendimento de como os probióticos atuam no organismo, e como essas bactérias benéficas influenciam na resposta imunológica e saúde da mucosa intestinal (FEDORAK; MADSEN, 2004).
É relatado que o uso de prebióticos e probióticos usados em pacientes diagnosticados com SII, mostram eficácia na melhora dos sintomas da doença. Contudo, os efeitos dos prebióticos e probióticos pode mudar de acordo com os subtipos de SII, como os tipo constipação (SSI-C), tipo diarreia (SII-D) e mista (SSIM) (CAMACHO-DÍAZ et al., 2023).
Foi realizado em um estudo a suplementação durante 4 semanas com base na microbiota intestinal de cada paciente, prebióticos e probióticos. Os prebióticos oferecidos aos pacientes na forma de pó (7500 mg de fibras alimentares arabinogalactanas, goma guar parcialmente hidrolisada, pectina, farelo de arroz desengordurante, inulina, amido de milho e psyllium), e os probióticos que representam uma mistura de Bifidobacterium e Lactobacillus. Foi observado uma redução nas pontuações do SII-SSS nos pacientes com os subtipos diarreico (SII-D) e com constipação (SII-C), contudo não foi observado uma melhora nos indivíduos com o subtipo misto (SII-M). É analisada também a diminuição dos sintomas de dor abdominal e distensão abdominal, principalmente nos grupos SII-D e SII-C. Além de pacientes com SII-C apresentarem um maior número de evacuações. (SOMMERMEYER et al., 2024).
Como já visto, o uso de fibras que alimentam as bactérias boas do intestino (prebióticos), ajudam na constipação. Em um ensaio clínico foi usada a inulina chicória, por quatro semanas em idosos com constipação, essa fibra ajudou a aumentar a presença de Bifidobacterium, que melhorou a frequência de evacuações. Além disso também foi usado grânulos de estaquiose (DSGs), que ajudam a equilibrar a microbiota intestinal, consequentemente aumentando o número de bactérias benéficas e reduzindo as prejudiciais, facilitando então a evacuação, tornando as fezes mais macias. De modo geral, os prebióticos são considerados seguros e eficazes, trazendo um efeito positivo por estar ligado à forma como modulam o microbioma intestinal (RAU et al., 2024).
3 OBJETIVOS
3.1 Objetivo geral
Investigar se os padrões alimentares podem contribuir para o tratamento da síndrome do intestino irritável.
3.2 Objetivos específicos
- Caracterizar a fisiopatologia e o tratamento da síndrome do intestino irritável;
- Analisar os efeitos da alimentação nos sintomas da SII;
- Descrever a contribuição das fibras alimentares no manejo da SII;
- Avaliar, por meio da literatura científica, os efeitos do uso de probióticos e prebióticos na modulação da microbiota intestinal.
4 METODOLOGIA
O presente trabalho será uma revisão integrativa da literatura, composta por artigos nos idiomas inglês e português publicados nos últimos dez anos na base de dados U.S National Library of Medicine (PubMed) e SciELO. A partir de buscas realizadas nos descritores de busca MeSH terms da National Center of Biotechnology Information (NCBI) e Descritores em Ciências da Saúde (DeCS), as palavras chaves que melhor descrevem o tema e serão utilizadas como estratégias de busca são “low fodmaps”, “intestinal hypersensitivity”, “intestinal microbiota”, “constipation”, “diarrhea”, “irritable bowel syndrome”, “food intake”, “dietary fiber”,”probiotics and prebiotics”, “mediterranean diet”,em inglês e “baixos fodmaps”, “hipersensibilidade intestinal”, “microbiota intestinal”, “constipação”, “diarreia”, “síndrome do intestino irritável”, “ingestão alimentar”, “fibras alimentares”, “probióticos e prebióticos”, “dieta mediterrânea”, em português, combinados pelos operadores booleanos AND e OR.
Os critérios de inclusão para a seleção de artigos serão estudos do tipo coorte, caso-controle e ensaio clínico que apresentem associação entre padrões alimentares que podem contribuir para o tratamento da síndrome do intestino irritável. Artigos que não contenham a seleção de dados originais, como revisões de literatura, relatos de casos, nota técnica, editorial e estudos que correlacionam com doença de Crohn, retocolite ulcerativa, câncer de cólon, intolerâncias e alergias alimentares, serão excluídos durante a busca bibliográfica.
Inicialmente, a seleção de artigos se deu a partir da aplicação de filtros anteriormente descritos, resultando em um total de 521 artigos encontrados. A partir da leitura do título e exclusão de duplicatas,15 artigos surgiram no processo de seleção de resultados. Desse total, 6 artigos foram excluídos após a leitura da conclusão e resumo por não corresponderem aos critérios de inclusão, totalizando 9 artigos internacionais incluídos na revisão da literatura. A figura 1 ilustra as etapas de seleção de artigos.
Figura 1. Etapa de seleção dos artigos incluídos na revisão integrativa.
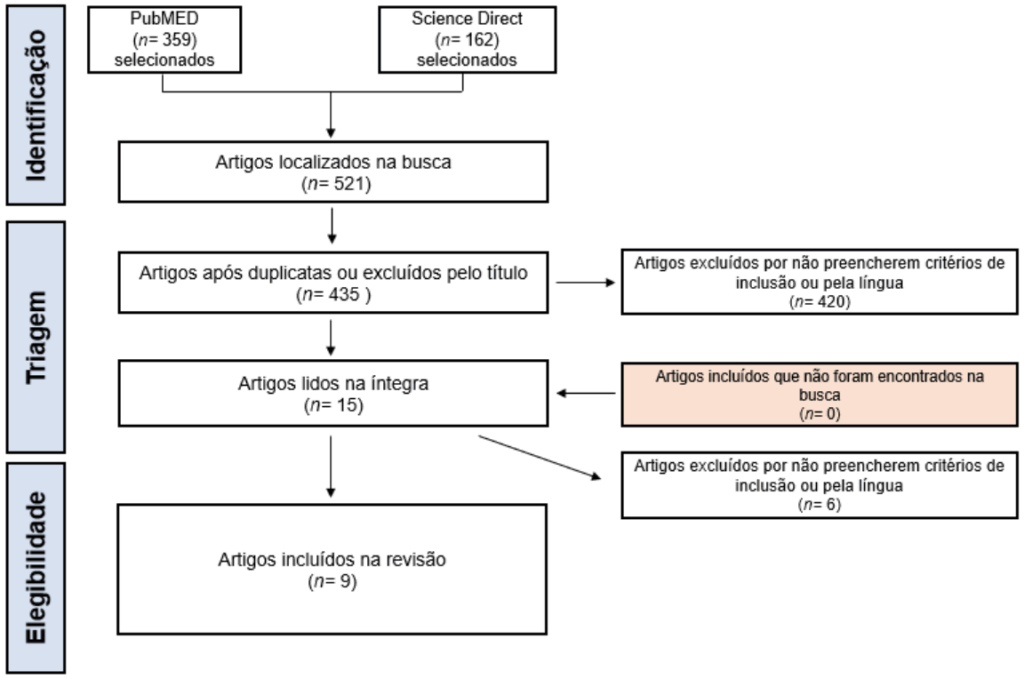
5 RESULTADOS E DISCUSSÃO
A partir da busca de resultados foram encontrados 9 artigos satisfatórios, dos quais, 6 foram estudos duplos-cegos e cruzados, 1 estudo aberto e unicêntrico, 1 estudo em duas fases com reintrodução cega e 1 estudo controlado, duplo-cego e cruzado. Esses delineamentos evidenciam o predomínio de abordagens experimentais voltadas à avaliação de efeitos de dietas low foodmaps e inclusão de fibras alimentares em pacientes com SII. Os principais pontos apresentados na tabela de resultados abrangem os autores e locais dos estudos, o público participante, a metodologia empregada e os principais achados obtidos em cada pesquisa.
A Síndrome do Intestino Irritável (SII) é um distúrbio gastrointestinal comum que afeta cerca de 15% da população mundial. Caracteriza-se por dor abdominal recorrente associada à defecação ou alterações nos hábitos intestinais, sendo classificada, conforme a Escala de Fezes de Bristol, em três subtipos: SII-D (diarreia predominante), SII-C (constipação predominante) e SII-M (misto)(Bjørkevoll et al., 2025). Diante dessa classificação, é possível adaptar estratégias para gerenciar as necessidades específicas de cada subgrupo da doença.
Um estudo de intervenção dietética aberta realizado em pacientes diagnosticados com SII-D e SII- M moderadas ou graves, em que 49 indivíduos foram inscritos em dieta LFD durante um período de 12 semanas. Inicialmente foram feitas consultas com nutricionista registrado, e questionários que avaliam os níveis de sintomas, como a fadiga, ansiedade e depressão. Após o período das 12 semanas houve uma resposta clínica de melhora dos quadros de fadiga, ansiedade e depressão, além da melhora de desempenho durante um teste computadorizado de atenção. (BJORKEVOLL et al., 2025).
Em contrapartida, um estudo randomizado determinou quais FODMAPS tem mais probabilidade para desencadear sintomas em pacientes diagnosticados com SII que já melhoraram com a restrição dos FODMAPS. Neste estudo foi analisados 45 pacientes, tendo que 25 apresentaram melhora com a dieta baixa em FODMAPs e 21 seguiram para a fase de reintrodução. A ingestão de frutanos e galacto-oligossacarídeos (GOS) esteve associada ao aumento da dor abdominal, e 21 os GOS também contribuíram para uma maior distensão abdominal. Ao longo do estudo, dor e
Tabela 1 – Consolidado de estudos internacionais selecionados (n= 9).
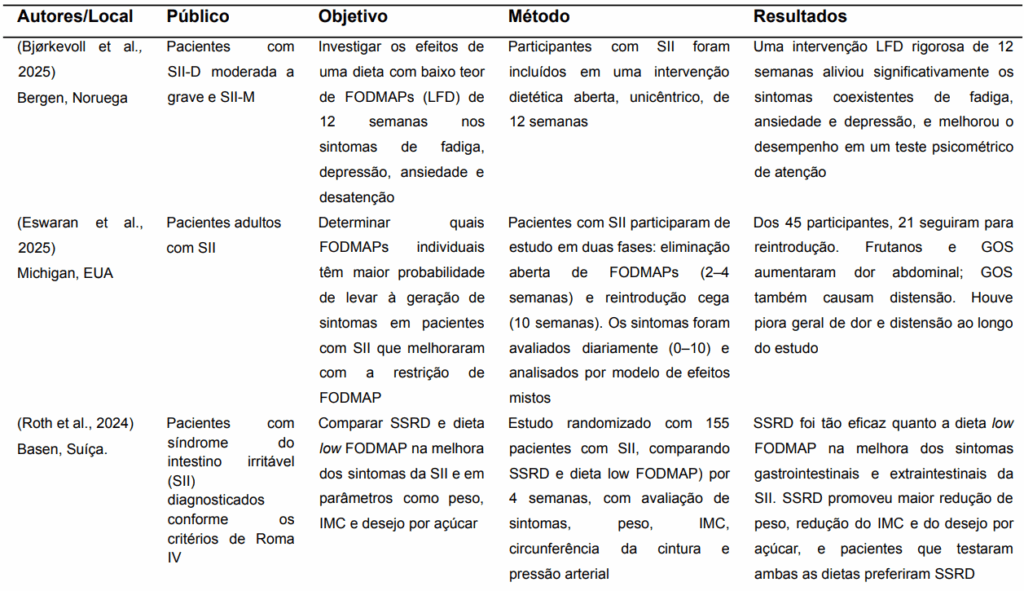


↓ = redução / ↑ = aumento
SII – Síndrome do Intestino Irritável; FODMAPs – do inglês, fermentable oligosaccharides, disaccharides, monosaccharides and polyols, tradução livre, oligossacarídeos, dissacarídeos, monossacarídeos e polióis fermentáveis; SSRD – do inglês, starch-sucrose restricted diet, tradução livre, dieta de amido e sacarose reduzidos; LFD – do inglês, low FODMAP, tradução livre, baixo em FODMAP; AGCC – ácidos graxos de cadeia curta; IMC – índice de massa corporal.
Fonte: elaborado pelos autores (2025).
O inchaço abdominal se intensificou independentemente da reintrodução dos FODMAPs. Esses achados sugerem que a reintrodução de determinados FODMAPs pode desencadear sintomas em pacientes com SII que respondem à dieta restritiva, reforçando a necessidade de estudos futuros comparando dietas baixas em FODMAP restritivas e padrões (ESWARAN et al., 2025).
Outro padrão alimentar além de uma restrição de FODMAP também foi analisado em um estudo randomizado de não inferioridade, compara uma dieta com baixo teor de amido e sacarose, a dieta LFD no tratamento dietético da SII. A intervenção durou 4 semanas, seguida de reintrodução gradual para o grupo FODMAP. Avaliações incluíram questionários de sintomas (IBS-SSS, VAS-IBS, Roma IV), diário alimentar e medidas antropométricas. SSRD focou em reduzir amido e sacarose; FODMAP restringiu frutanos, GOS, lactose, frutose e polióis. Ambos os grupos receberam receitas, orientações e acompanhamento remoto. Em resumo, a dieta SSRD por 4 semanas mostrou eficácia similar à dieta baixa em FODMAP para aliviar sintomas gastrointestinais da SII. Ambos os grupos apresentaram melhora nos sintomas extra intestinais, mas a SSRD levou a reduções maiores de peso, IMC e desejo por açúcar. Além disso, os participantes que experimentaram ambas as dietas preferiram a SSRD por ser mais fácil de seguir. (ROTH et al., 2024).
Além do estudo mencionado, outro trabalho conduzido por AL-SHIBLAWI et al., (2025) teve como objetivo comparar os efeitos de uma dieta com redução de amido e sacarose (SSRD) com a dieta pobre em FODMAPs em pacientes com síndrome do intestino irritável (SII). Trata-se de um ensaio clínico randomizado e aberto, com duração de quatro semanas e acompanhamento de seis meses, que avaliou 155 pacientes diagnosticados conforme os critérios de Roma IV.
Ambas as dietas promoveram redução dos sintomas gastrointestinais, perda de peso e diminuição da ingestão calórica e de carboidratos. No entanto, a dieta SSRD apresentou vantagens nutricionais superiores, incluindo redução mais acentuada de amido, sacarose, dissacarídeos e açúcares adicionados, além de aumento no consumo de proteínas, gorduras, vitaminas e minerais essenciais, como vitamina E, folato, vitamina B12, magnésio, fósforo, selênio e iodo. Por outro lado, a dieta low FODMAP foi associada à diminuição da ingestão de fibras, tiamina, riboflavina, ferro e potássio.
Os autores concluíram que a SSRD é uma alternativa eficaz para o manejo da SII, promovendo não apenas o alívio sintomático, mas também uma melhoria do perfil nutricional geral, com maior densidade de nutrientes e menor risco de deficiência vitamínica. Esses resultados indicam que a substituição de alimentos ricos em amido e sacarose por frutas, vegetais, ovos e laticínios pode favorecer o equilíbrio nutricional e contribuir para a saúde metabólica de pacientes com SII, tornando a SSRD uma abordagem potencialmente mais sustentável a longo prazo (AL-SHIBLAWI et al.,2025).
Outro estudo avaliou as respostas diferenciais à exposição de FODMAPs e glúten em indivíduos com SII por meio de um ensaio clínico randomizado, duplo-cego e cruzado. Participaram 110 indivíduos diagnosticados com SII moderada a grave, dos quais 74 completaram todas as etapas experimentais. Realizado de forma que os participantes foram submetidos a três fases de intervenção (FODMAPs, Glúten e Placebo), intercalados por períodos de pausa ou washout, além de um teste de provocação rápida contendo ambos os componentes. As respostas clínicas foram analisadas pelo questionário IBS-SSS e associadas a dados moleculares de microbiota fecal, ácidos graxos de cadeia curta e metabolômica plasmática. Obtendo-se resultados que mostraram que a ingestão de FODMAPs promoveu aumento significativo nos escores de sintomas quando comparada ao placebo, enquanto o glúten não apresentou diferença estatística.
Embora o FODMAP tenha ocasionado alterações metabólicas e microbianas detectáveis como elevação de bactérias sacarolíticas, metabólitos fenólicos e 3-índole propionato, essas mudanças não se correlacionaram de forma robusta com a gravidade dos sintomas relatados. As análises de regressão e classificação por aprendizado de máquina apresentaram baixo poder preditivo, e os modelos de agrupamento não conseguiram identificar metabólitos clinicamente relevantes. Além disso, a análise de componentes paralelos (PARAFAC) mostrou que as respostas metabólicas imediatas à provocação com FODMAPs e glúten não se relacionaram significativamente à intensidade dos sintomas gastrointestinais (NORDIN et al.2024).
Os resultados indicam que a resposta à dieta em pacientes com SII é multifatorial, envolvendo não apenas os componentes alimentares, mas também fatores psicológicos e comportamentais não avaliados no estudo. A falta de correlação entre microbiota, metabólitos e sintomas sugere que outros elementos podem estar relacionados à sensibilidade intestinal. A alta variabilidade individual e o possível efeito placebo também podem ter influenciado os achados. Apesar disso, o estudo se destaca pela robustez metodológica e reforça que ainda não existem evidências suficientes para sustentar respostas diferenciais entre FODMAPs e glúten. Assim, a personalização dietética na SII permanece dependente de novas pesquisas que integrem aspectos metabólicos e psicológicos. (Nordin et al,2024).
Em contrapartida, um experimento do estilo ensaio clínico randomizado, duplo-cego, cruzado. Observou- se uma dieta baixa em FODMAPs reduziu sintomas gastrointestinais, dor abdominal e melhora significativa dos hábitos intestinais. E os resultados corroboram achados prévios que apontam a eficácia dessa dieta na melhora dos sintomas da síndrome do intestino irritável, ainda que as taxas de resposta tenham sido menores em relação a outros estudos. Essa diferença pode estar relacionada ao curto período de intervenção e às variações metodológicas entre pesquisas. O delineamento duplo-cego e o controle rigoroso das refeições reforçam a validade dos resultados, minimizando vieses associadas ao efeito placebo e nocebo. Além disso, o estudo confirma que a redução dos FODMAPs influencia diretamente a consistência e frequência das evacuações, o que pode beneficiar especialmente pacientes com diarreia predominante. (Algera et al., 2022)
Demostrando que a dieta com baixo teor de FODMAPs é eficaz na redução dos sintomas gastrointestinais e na modulação dos hábitos intestinais em indivíduos com síndrome do intestino irritável, quando comparada à dieta com quantidade moderada desses compostos. A avaliação prévia da gravidade dos sintomas pode auxiliar o profissional na decisão de adotar a dieta como estratégia terapêutica, contribuindo para um manejo mais direcionado da SII. (ALGERA et al., 2022).
Em favorecimento ao estudo supracitado, um estudo de estilo randomizado de 3 semanas com análises de microbiota e AGCC demonstrou grande relevância ao comparar uma alimentação LFD (Low fodMaps Diet) e TDA (Traditional Diet Approach), Entre os 100 pacientes que concluíram o estudo, o desfecho primário foi alcançado em um número semelhante de pacientes LFD (30 de 51, 59%) e TDA (26 de 49, 53%) (∆6%; IC 95%: −13%, 24%). Os pacientes no grupo LFD obtiveram melhora sintomática mais precoce na frequência das fezes e gases excessivos do que aqueles que seguiram a alimentação TDA. O LFD reduziu as bactérias fermentadoras de carboidratos, como Bifidobacterium e Bacteroides, e diminuiu a atividade da fermentação sacarolítica. Isso foi associado à melhora sintomática nos respondedores. A alta atividade de fermentação sacarolítica no início do estudo foi associada a uma maior carga de sintomas (p= 0,01) e a uma resposta terapêutica favorável ao LFD (log OR: 4,9; IC 95%: −0,1, 9,9; p= 0,05). Em conclusão, tanto a LFD quanto a TDA reduziram os sintomas em pacientes chineses com SII-D; no entanto, a LFD proporcionou melhoras sintomáticas mais precoces na frequência das fezes e gases excessivos. O efeito terapêutico da LFD foi associado a alterações na microbiota fecal e no índice de fermentação fecal, melhorando consideravelmente a qualidade de vida dos pacientes (ZHANGet al.,2021).
A dieta é um modulador da microbiota gastrointestinal e uma terapia importante na síndrome do intestino irritável (SII) (WHELAN et al., 2021). O estudo teve como objetivos identificar associações entre dieta e microbiota em adultos com SII que consomem dieta habitual, avaliar o impacto de intervenções nutricionais na microbiota e determinar se a microbiota basal pode prever a resposta clínica à dieta ou à intervenção probiótica (WHELAN et al., 2021).
Foram analisados dados de 95 indivíduos que participaram de um ensaio clínico randomizado, controlado, com delineamento fatorial 2×2, com duração de quatro semanas, no qual se investigou o efeito da dieta com baixo teor de FODMAPs e a coadministração de um probiótico. A microbiota foi caracterizada utilizando sequenciamento parcial do gene 16S rRNA (WHELAN et al., 2021).
Os resultados mostraram alterações na abundância de Bifidobacterium, Bacteroides, Lactobacillus e Streptococcus, e o tratamento probiótico modulou parcialmente os efeitos da dieta sobre a microbiota (WHELAN et al., 2021). Apesar dessas modificações, a análise de correlação bivariada forneceu explicação limitada sobre as interações entre dieta e bactérias intestinais individuais na SII (WHELAN et al., 2021). Além disso, a composição microbiana basal não apresentou capacidade preditiva consistente para a resposta clínica à dieta ou à suplementação probiótica. O estudo evidencia a complexidade das interações dieta-microbiota na SII e a necessidade de abordagens mais integrativas para compreender a modulação microbiana por fatores dietéticos e terapêuticos (WHELAN et al., 2021).
A implementação de uma dieta com baixo teor de oligossacarídeos, dissacarídeos, monossacarídeos e polióis fermentáveis (FODMAPs) em pacientes com SII pode levar à ingestão inadequada de fibras (DANIEL et al., 2022). O presente estudo teve como objetivo investigar os efeitos da suplementação de fibras específicas concomitantemente a uma dieta pobre em FODMAPs sobre índices clínicos e fisiológicos relevantes em pacientes sintomáticos com SII. Foi conduzido um ensaio clínico duplo-cego cruzado com 26 pacientes com SII, que foram aleatoriamente designados para uma das três dietas com baixo teor de FODMAPs, diferindo apenas no teor total de fibras: controle (23 g/d), bagaço de cana (33 g/d) ou combinação de fibras (bagaço de cana com amido resistente, 45 g/d). Cada dieta durou 14 dias, com fornecimento da maior parte dos alimentos, e intervalo de ≥ 21 dias entre elas. Os desfechos foram avaliados durante o período basal e as intervenções dietéticas (DANIEL et al., 2022). Colaboradores demonstram que a suplementação concomitante de fibras durante o início de uma dieta com baixo teor de FODMAPs aumenta a produção de fezes e normaliza parâmetros fisiológicos sem reduzir a eficácia clínica na diminuição dos sintomas de SII.
Os resultados mostraram que todas as dietas reduziram as pontuações medianas do sistema de pontuação de gravidade da SII em mais de 50%, sem diferenças significativas nas taxas de resposta sintomática entre os grupos: controle (57%), bagaço de cana (67%) e combinação de fibras (48%; p = 0,459). A suplementação com fibras aumentou em aproximadamente 50% a produção de fezes em comparação à dieta controle (p < 0,001). Embora não haja diferenças gerais nas características das fezes, o bagaço de cana isoladamente normalizou o baixo teor de água nas fezes e o trânsito colônico lento observado durante a dieta controle. O amido resistente não apresentou benefícios sintomáticos adicionais em comparação ao bagaço de cana isoladamente (DANIEL et al., 2022).
Este estudo apresenta algumas limitações. Por se tratar de uma revisão integrativa, os resultados dependem das informações já publicadas na literatura, o que impede controle direto sobre os métodos aplicados em cada pesquisa. Além disso, muitos dos estudos analisados possuem amostras reduzidas e tempo de intervenção curto, o que limita a avaliação dos efeitos em longo prazo das intervenções dietéticas, como a dieta low FODMAP e o uso de fibras.
Outro ponto importante é que há variação significativa entre os protocolos utilizados, especialmente no tipo e quantidade de fibras e probióticos empregados, bem como no modo de reintrodução dos FODMAPs, o que dificulta comparações diretas entre os resultados. Além disso, a resposta aos tratamentos pode diferir entre os subtipos da SII, reforçando a necessidade de planejamentos alimentares individualizados.
Diante das limitações observadas, estudos futuros devem incluir amostras maiores, tempo de acompanhamento prolongado e maior padronização das intervenções, de modo a aprimorar a consistência dos resultados. Também se destaca a importância de investigações que avaliem estratégias personalizadas, considerando a composição da microbiota e o subtipo clínico da SII, já que a resposta pode variar entre indivíduos. Além disso, pesquisas comparando diferentes abordagens nutricionais, como dieta low FODMAP, dieta com redução de amido e sacarose e uso combinado de fibras, prebióticos e probióticos, podem ajudar a identificar intervenções mais eficazes e sustentáveis a longo prazo.
6 CONSIDERAÇÕES FINAIS
O presente trabalho, desenvolvido por meio de uma revisão integrativa da literatura, analisou as principais intervenções dietéticas utilizadas no manejo dos sintomas da Síndrome do Intestino Irritável (SII). Os estudos incluídos evidenciaram que diferentes padrões alimentares e estratégias nutricionais podem auxiliar no controle dos sintomas, variando conforme o subtipo da doença e as particularidades individuais dos pacientes.
A dieta com baixo teor de FODMAPs destacou-se como uma das abordagens mais eficazes na redução de sintomas gastrointestinais, como dor abdominal, distensão e alterações do trânsito intestinal, especialmente em pacientes com SII-D e SII-M. A exclusão temporária desses carboidratos, seguida de reintrodução gradual, demonstrou melhora significativa, embora exija acompanhamento profissional devido ao risco de deficiências nutricionais e à necessidade de adaptação individual.
A dieta SSRD apresentou resultados semelhantes à Low FODMAP na redução dos sintomas e na melhora do bem-estar geral, diferenciando-se por oferecer melhor equilíbrio nutricional, maior variedade de nutrientes e maior facilidade de adesão, configurando-se como alternativa viável para indivíduos com dificuldade de seguir a dieta Low FODMAP.
A revisão também abordou o papel de prebióticos e probióticos como estratégias complementares, destacando seus mecanismos de ação na modulação da microbiota intestinal, na integridade da barreira epitelial e na resposta inflamatória. Esses compostos demonstraram potencial para reduzir sintomas como dor abdominal, distensão, diarreia e constipação, especialmente quando sua suplementação é personalizada conforme o subtipo da SII e o perfil microbiano individual. Contudo, a eficácia desses recursos varia em função da cepa utilizada, tipo de fibra, dose, tempo de uso e características da microbiota, além de limitações metodológicas dos estudos, reforçando a necessidade de novos ensaios clínicos mais padronizados.
Os achados também evidenciaram o papel relevante das fibras alimentares no manejo da SII. As fibras solúveis, como o psyllium, mostraram melhor desempenho clínico por melhorar o trânsito intestinal, aumentar o volume fecal e reduzir dor abdominal e distensão, sem elevar a produção de gases. Em contraste, as fibras insolúveis não apresentaram os mesmos benefícios e, em alguns casos, podem intensificar desconfortos. A suplementação de fibras associada à dieta Low FODMAP contribuiu para a normalização da consistência das fezes e melhora da motilidade. Esses ensaios clínicos relataram ainda benefícios do uso combinado de diferentes tipos de fibras, especialmente na constipação predominante. No entanto, a resposta às fibras é variável, e dietas restritivas podem reduzir sua ingestão total, exigindo monitoramento especializado.
Conclui-se que a alimentação representa um componente central no manejo da SII, e que dietas específicas, fibras, prebióticos e probióticos apresentam potencial terapêutico significativo. O sucesso dessas intervenções depende da individualização das condutas e do acompanhamento profissional contínuo.
REFERÊNCIAS
SAEZ et al. Pathophysiology of Inflammatory Bowel Disease: Innate Immune System. International journal of molecular sciences, 24(2), 1526. (Janeiro,2023)
OKA, Patricia; PARR, Hayley; SINGH, Saurabh; et al. irritable bowel syndrome. The Lancet, [S. l.], v. 396, n. 10263, p. 1675-1688, (setembro,2020).
FORD et AL. ATLANTIS trialists. Amitriptyline at Low-Dose and Titrated for Irritable Bowel Syndrome as Second-Line Treatment in primary care (ATLANTIS): a randomized, double-blind, placebo-controlled, phase 3 trial. Lancet(London, England), 402(10414), 1773–1785. (Novembro, 2023).
CHEY et AL. Efficacy of Tenapanor in Treating Patients With Irritable Bowel Syndrome With Constipation: A 26-Week, Placebo-Controlled Phase 3 Trial (T3MPO-2). The American journal of gastroenterology, 116(6), 1294–1303. (Junho, 2021).
AGA Clinical Practice Update on the Role of Diet in Irritable Bowel Syndrome: Expert Review (Maio, 2022) Gastroenterology, Volume 162, Issue 6, 1737 – 1745.e5
KACZKA, A. et al. Periodic Changes in the Gut Microbiome in Women with the Mixed Type of Irritable Bowel Syndrome. *Biomedicines*, v. 13, n. 3, p. 652, 7 mar. 2025.
BRENNER, D. M. et al. Tenapanor Improves Abdominal Symptoms Irrespective of Changes in Complete Spontaneous Bowel Movement Frequency in Adults with Irritable Bowel Syndrome with Constipation. Digestive Diseases, v. 43, n. 2, p. 146-157, 2025
SAVARINO, E. et al. Functional bowel disorders with diarrhoea: Clinical guidelines of the United European Gastroenterology and European Society for Neurogastroenterology and Motility. United European Gastroenterology Journal, v. 10, n. 6, p. 556-584, jul. 2022.
WU, S. et al. Ultra-Processed Food Consumption and Long-Term Risk of Irritable Bowel Syndrome: A Large-Scale Prospective Cohort Study. Clinical Gastroenterology and Hepatology, v. 22, n. 7, p. 1497-1507.e5, jul. 2024.
FELDMAN, M., & CRYER, B. Emotional stress and the gastrointestinal tract: implications for the syndrome of irritable bowel. Journal of Gastroenterology, v. 33, n. 8, p. 1453-1457, 2022.
LÓPEZ-ÁLVAREZ, M. A., et al. Anxiety, depression, and irritable bowel syndrome: a biopsychosocial perspective. Revista Brasileira de Terapias CognitivoComportamentais, v. 21, n. 2, p. 132-142, 2023.
PÉREZ-LÓPEZ, F. R., et al. Stress, psychological factors and gastrointestinal function in irritable bowel syndrome: a review. International Journal of Gastroenterology, v. 48, n. 3, p. 150-158, 2022.
SHARMA, M.; RANA, S.; AGGARWAL, S.; AHSAN, A. U. et al. Efficacy of Nigella sativa seed oil against psychophysical stress induced irritable bowel syndrome and anxietylike symptoms in Wistar rats. Psychopharmacology (Berl), v. 241, n. 12, p. 26092626, dez. 2024.
KRYNICKA, P. et al. Untargeted Metabolomic Profiling of Colonic Mucosa in Individuals with Irritable Bowel Syndrome. Biomedicines, v. 13, n. 3, p. 629, 5 mar. 2025.
SIMRÉN, M. et al. Intestinal microbiota in functional bowel disorders: a Rome foundation report. *Gut*, v. 62, n. 1, p. 159-176, jan. 2013.
CAMMAROTA G , IANIRO G , TILG H , et al. Consenso da conferência europeia sobre transplante de microbiota fecal na prática clínica[J]. Intestino,2017.
GAO, Y. et al. Complex Probiotics Ameliorate Fecal Microbiota TransplantationInduced IBS in Mice via Gut Microbiota and Metabolite Modulation. Nutrients, v. 17, n. 5, p. 801, 26 fev. 2025.
CHEY et AL. AGA Clinical Practice Update on the Role of Diet in Irritable Bowel Syndrome: Expert Review. Gastroenterology, 162(6), 1737–1745.e5. (Maio,2022) LEMBO et AL. AGA Clinical Practice Guideline on the Pharmacological Management of Irritable Bowel Syndrome With Diarrhea. Gastroenterology, 163(1), 137–151. (Julho,2022).
MARSTON et AL. Multiplexed GTPase and GEF biosensor imaging enables network connectivity analysis. Nature chemical biology, 16(8), 826–833. (Maio,2020)
FORD et al. irritable bowel syndrome. Lancet (London, England), 396(10263), 1675– 1688. (Novembro, 2020)
FORD, ALEXANDER C et al. irritable bowel syndrome. The Lacent, v.396, p. 16751688, 21 nov. 2020.
LACY, B. E. et al. ACG Clinical Guideline: Management of Irritable Bowel Syndrome. American Journal of Gastroenterology, v. 116, n. 1, p. 17–44, 1 jan. 2021.
GUNN, D. et al. Psyllium reduces inulin-induced colonic gas production in IBS: MRI and in vitro fermentation studies. Gut, v. 71, n. 5, p. 919–927, 1 maio 2022.
CARBONE, F. et al. Diet or medication in primary care patients with IBS: the DOMINO study – a randomised trial supported by the Belgian Health Care Knowledge Centre (KCE Trials Programme) and the Rome Foundation Research Institute. Gut, v. 71, n. 11, p. 2226–2232, 28 abr. 2022.
VAN DEN HOUTE, K. et al. Efficacy and Findings of a Blinded Randomized Reintroduction Phase for the Low FODMAP Diet in Irritable Bowel Syndrome. Gastroenterology, v. 167, n. 2, p. 333–342, 1 jul. 2024.
ESWARAN, Shanti et al. The impact of a 4-week low-FODMAP and mNICE diet on nutrient intake in a sample of US adults with irritable bowel syndrome with diarrhea. Journal of the Academy of Nutrition and Dietetics, v. 120, n. 4, p. 641-649, abr. 2020.
GALICA, A. N.; GALICA, R.; DUMITRAȘCU, D. L. Diet, fibers, and probiotics for irritable bowel syndrome. Journal of Medicine and Life. Carol Davila University Press, 2022.
MATSUURA, N. et al. Effect of Personalized Prebiotic and Probiotic Supplements on the Symptoms of Irritable Bowel Syndrome: An Open-Label, Single-Arm, Multicenter Clinical Trial. Nutrients, v. 16, n. 19, 1 out. 2024.
BARBARA, Giovanni et al. Diretrizes italianas para o tratamento da síndrome do intestino irritável. Doenças Digestivas e Hepáticas, v. 55, n. 2, p. 187-207, fevereiro. 2023.
MARTONI, C. J. et al. Efficacy and dose response of Lactiplantibacillus plantarum in diarrhea-predominant irritable bowel syndrome. World Journal of Gastroenterology, v. 29, n. 28, p. 4451–4465, 2023.
BERTANI, L. et al. Specific probiotics and prebiotics to improve the quality of life of patients with chronic irritable bowel syndrome. Minerva Gastroenterologia, v. 70, n. 4, p. 413–421, dezembro, 2024.
CAMACHO-DÍAZ, B. H. et al. The Effects of Agave Fructans in a Functional Food Consumed by Patients with Irritable Bowel Syndrome with Constipation: A Randomized, Double-Blind, Placebo-Controlled Trial. Nutrients, v. 15, n. 16, 1 ago. 2023.
JANSSENDUIJGHUIJSEN, L. et al. Acacia fiber or probiotic supplements to relieve gastrointestinal complaints in patients with constipation-predominant IBS: a 4-week randomized double-blinded placebo-controlled intervention trial. European Journal of Nutrition, v. 63, n. 5, p. 1983–1994, 1 ago. 2024.
SO, D. et al. Supplementing Dietary Fibers With a Low FODMAP Diet in Irritable Bowel Syndrome: A Randomized Controlled Crossover Trial. Clinical Gastroenterology and Hepatology, v. 20, n. 9, p. 2112- 2120.e7, 1 set. 2022.
CHEY, W. D. et al. AGA Clinical Practice Update on the Role of Diet in Irritable Bowel Syndrome: Expert Review. Gastroenterology, v. 162, n. 6, p. 1737- 1745.e5, 1 maio 2022.
YAN, R. et al. Does Fibre-fix provided to people with irritable bowel syndrome who are consuming a low FODMAP diet improve their gut health, gut microbiome, sleep and mental health? A double-blinded, randomised controlled trial. BMJ Open Gastroenterology, v. 7, n. 1, 17 ago. 2020.
REMES-TROCHE, J. M. et al. Nopal fiber (Opuntia ficus-indica) improves symptoms in irritable bowel syndrome in the short term: a randomized controlled trial. Neurogastroenterology and Motility, [S. l.], maio, 2021.
FEDORAK, R. N.; MADSEN, K. L. Probiotics and prebiotics in gastrointestinal disorders. Current Opinion in Gastroenterology, v. 20, n. 2, p. 146–155, 2004
SOMMERMEYER, H. et al. Effectiveness of a Balanced Nine-Strain Synbiotic in Primary-Care Irritable Bowel Syndrome Patients-A Multi-Center, Randomized, DoubleBlind, Placebo-Controlled Trial. Nutrients, v. 16, n. 10, 16 maio 2024.
RAU, S. et al. Prebiotics and Probiotics for Gastrointestinal Disorders. Nutrients. Multidisciplinary Digital Publishing Institute (MDPI), 1 mar. 2024.
SHAMS, M. et al. Dietary interventions in irritable bowel syndrome: a systematic review of clinical outcomes, microbiota changes, and inflammatory markers. Cureus, v. 16, n. 9, e70568, 2024.
STAUDACHER, H. M.; WHELAN, K. Altered gastrointestinal microbiota in irritable bowel syndrome and its modification by diet: probiotics, prebiotics and the low FODMAP diet. Proceedings of the Nutrition Society, v. 75, n. 3, p. 306–318, 2016.
VAN LANEN, A.-S.; DE BREE, A.; GREYLING, A. Efficacy of a low-FODMAP diet in adult irritable bowel syndrome: a systematic review and meta-analysis. European Journal of Nutrition, v. 60, n. 6, p. 3505–3522, 2021.
WANG, Y. et al. Efficacy and safety of probiotics, prebiotics and synbiotics in the treatment of irritable bowel syndrome: a systematic review and meta-analysis. Sultan Qaboos University Medical Journal, v. 20, n. 3, p. e323–e331, 2020.
CHEY, W. D. et al. Irritable bowel syndrome: a clinical review. JAMA, v. 313, n. 9, p. 949–958, 2015.
FUKUDO, S. et al. Gender differences in patients with irritable bowel syndrome. Neurogastroenterology & Motility, v. 35, n. 1, e14499, 2023.
MOLLOY, M. et al. Sex and gender differences in irritable bowel syndrome: implications for treatment and management. Therapeutic Advances in Gastroenterology, v. 14, p. 1–14, 2021.
SHIN, A. et al. Gender differences in irritable bowel syndrome: a meta-analysis. World Journal of Gastroenterology, v. 24, n. 42, p. 4759–4768, 2018.
MAYER, E. A. Gut feelings: the emerging biology of gut–brain communication. Nature Reviews Neuroscience, London, v. 12, n. 8, p. 453–466, 2011.
CHANG, L. et al. Brain–gut interactions in irritable bowel syndrome: a review of neuroimaging studies. Gastroenterology Clinics of North America, Philadelphia, v. 50, n. 3, p. 459–472, 2021.
LIU, Yingying et al. Functional gastrointestinal disorders: advances in overlap and pathogenesis research. Frontiers in Neuroscience, Lausanne, v. 17, 2023
BJØRKEVOLL, s. M. G. et al. A 12-week strict low FODMAP diet reduces the severity levels of fatigue, depression, anxiety, and inattention in patients with irritable bowel syndrome. Current Developments in Nutrition, v. 9, n. 7, p. 107483, 2025.
ESWARAN, S. All FODMAPs aren’t created equal: results of a randomized controlled trial. Clinical Gastroenterology and Hepatology, [S.l.], v. 23, n. 4, p. 813-822, 2025.
ROTH, Bodil; et al. A starch- and sucrose-reduced diet has similar efficiency as low FODMAP in IBS—A randomized non-inferiority study. Nutrients, [S.l.], v. 16, n. 17, art. 3039, 2024.
ZHANG, et al. Low fermentable oligosaccharides, disaccharides, monosaccharides, and polyols diet compared with traditional dietary advice for diarrhea-predominant irritable bowel syndrome: a parallel-group, randomized controlled trial with analysis of clinical and microbiological factors associated with patient outcomes. American Journal of Clinical Nutrition, v. 113, n. 6, p. 1531-1545, (01 jun. 2021).
ALGERA, et al. Low FODMAP diet reduces gastrointestinal symptoms in irritable bowel syndrome and clinical response could be predicted by symptom severity: a randomized crossover trial. Clinical Nutrition, v. 41, n. 12, p. 2792-2800, dez. 2022.
NORDIN, et al. Exploration of differential responses to FODMAPs and gluten in people with irritable bowel syndrome a double-blind randomized cross-over challenge study. Metabolomics, v. 20, n. 2, p.(21, fev. 2024).
WHELAN, et al. Dietary modulation of gut microbiota in irritable bowel syndrome: impact of low-FODMAP diet and probiotics. [s.l.]: [s.n.], 2021. ISRCTN02275221.
Daniel, et al. Effects of specific fiber supplementation during low-FODMAP diet in irritable bowel syndrome patients. [s.l.]: [s.n.], 2022. ACTRN12619000691145.
AL-SHIBLAWI, Noor et al. A starch- and sucrose-reduced diet leads to a more favorable nutrient profile than low FODMAP in patients with irritable bowel syndrome: A randomized clinical trial. Human Nutrition & Metabolism, v. 42, p. 200337, 2025.
