IMPACT OF PHARMACEUTICAL INTERVENTION ON THE PREVENTION OF DRUG INTERACTIONS IN CKD
REGISTRO DOI: 10.69849/revistaft/ni10202509071425
Jhenifer de Andrade Marques
Maria Beatriz Andrade Assis
Profª. Tatiana Cristina Santos Lagoa
Resumo
Este estudo teve como objetivo analisar o impacto da atuação do farmacêutico clínico na prevenção de interações medicamentosas (IM) em pacientes com Doença Renal Crônica (DRC). Trata-se de uma pesquisa bibliográfica, exploratória e descritiva, baseada em literatura científica nacional e internacional, diretrizes oficiais e revisões sistemáticas publicadas entre 2010 e 2025. A busca foi realizada em bases como SciELO, PubMed, LILACS e Google Scholar, além de documentos de órgãos como o Ministério da Saúde, ANVISA e Sociedade Brasileira de Nefrologia (SBN). Os resultados evidenciaram que pacientes com DRC apresentam elevada frequência de IM, principalmente em estágios avançados, em razão da polifarmácia e das alterações farmacocinéticas e farmacodinâmicas da insuficiência renal. Mais de 70% das prescrições avaliadas apresentaram potenciais interações, majoritariamente de gravidade moderada ou grave. Nesse cenário, a atuação do farmacêutico clínico mostrou-se essencial para a identificação precoce, prevenção e resolução de IM, contribuindo para maior segurança terapêutica, redução de eventos adversos e otimização da farmacoterapia. Também foi observada boa aceitação das intervenções farmacêuticas pela equipe multiprofissional. Conclui-se que o farmacêutico clínico exerce papel estratégico no cuidado de pacientes renais crônicos, promovendo segurança, racionalização do uso de medicamentos e melhoria da qualidade de vida. Recomenda-se sua institucionalização em todos os níveis de atenção, além da criação de protocolos clínicos e ampliação da capacitação profissional.
Palavras-chave: Doença Renal Crônica. Interações Medicamentosas. Farmacêutico Clínico. Segurança do Paciente. Farmacoterapia.
1 INTRODUÇÃO
1.1. O QUE É DRC E PORQUE É RELEVANTE
A doença renal crônica, segundo a Sociedade Brasileira de Nefrologia, pode ser definida como a presença de lesão renal, geralmente associada à perda progressiva e irreversível da função dos rins (glomerular, tubular e endócrina). Em estágios mais avançados, a doença pode levar à insuficiência renal crônica e, posteriormente, à insuficiência renal crônica terminal, na qual o paciente requer o emprego de alguma terapia de substituição renal para que a normalidade do meio interno seja mantida. Portanto, observa-se que é uma lesão presente por um período igual ou superior a três meses, caracterizada por anormalidades estruturais ou funcionais do rim, com ou sem diminuição da TFG (um indicador da função renal que avalia a capacidade dos rins de filtrar o sangue), evidenciada por anormalidades histopatológicas ou de marcadores de lesão renal, incluindo alterações sanguíneas ou urinárias, ou ainda de exames de imagem (BARBOSA, 2005).
Observa-se que é altamente relevante porque representa um dos maiores problemas de saúde pública mundial. Sua importância está relacionada à alta prevalência, principalmente em decorrência do aumento de fatores de risco como diabetes mellitus, hipertensão arterial e envelhecimento populacional. Nesse contexto, compreender sua relevância é fundamental para subsidiar estratégias de prevenção, diagnóstico precoce, acompanhamento farmacoterapêutico e manejo clínico adequado. No âmbito da Farmácia, possui uma demanda de acompanhamento contínuo da farmacoterapia, prevenção de complicações e individualização dos tratamentos (BARBOSA, 2005).
O farmacêutico desempenha papel fundamental na orientação quanto ao uso seguro e racional de medicamentos, no ajuste de doses em função da taxa de filtração glomerular e na adesão do paciente ao tratamento, contribuindo para a melhora da qualidade de vida e redução de custos em saúde pública. Dessa forma, estudar a DRC sob a perspectiva farmacêutica é essencial para promover um cuidado integral e eficaz (BARBOSA, 2005).
Interações medicamentosas (IMS) são frequentes na prática clínica e estão diretamente relacionadas a fatores como polifarmácia, idade avançada e deficiência na metabolização e excreção de fármacos. Indivíduos com doença renal crônica (DRC) comumente utilizam diversas classes de medicamentos, constituindo um importante grupo de risco para IMS. O uso frequente de múltiplos medicamentos por pacientes renais crônicos é uma característica muito comum, e recebe o nome de polifarmácia. Isso acontece porque a Doença Renal Crônica (DRC), além de comprometer a função dos rins, geralmente está associada a diversas comorbidades que precisam de tratamento simultâneo. (BARBOSA, 2005). Podemos observar os principais pontos:
Causas da polifarmácia na DRC
– Controle da pressão arterial (anti-hipertensivos, diuréticos).
– Manejo do diabetes mellitus (antidiabéticos orais, insulina).
– Tratamento de anemia (eritropoetina, ferro).
– Distúrbios minerais e ósseos (quelantes de fósforo, vitamina D, cálcio).
– Risco cardiovascular aumentado (estatinas, aspirina, anticoagulantes).
– Sintomas associados (analgésicos, antieméticos, laxantes, etc.).
Riscos associados
– Interações medicamentosas (um fármaco afetando a ação ou toxicidade de outro).
– Efeitos adversos aumentados, já que a eliminação dos medicamentos pode estar comprometida devido à redução da função renal
– Erros de adesão (dificuldade em seguir corretamente esquemas complexos).
– Maior custo do tratamento (BARBOSA, 2005).
Importância do acompanhamento
– Avaliação frequente por farmacêuticos clínicos e nefrologistas.
– Ajuste de doses conforme a taxa de filtração glomerular (TFG).
– Revisão periódica da prescrição para evitar medicamentos desnecessários.
– Educação do paciente sobre a importância do uso correto (BARBOSA, 2005).
1.2. MORTALIDADE POR SEPSE EM PACIENTES COM DOENÇA RENAL TERMINAL
As doenças infecciosas constituem uma complicação recorrente em indivíduos com doença renal crônica em fase terminal que dependem da terapia dialítica contínua, sendo reconhecidas como uma das principais causas de adoecimento e morte nesse grupo. Pesquisas indicam que as infecções aparecem logo após os eventos cardiovasculares como um dos maiores determinantes de mortalidade. Essa fragilidade clínica decorre de múltiplos fatores, entre eles a disfunção do sistema imunológico — com destaque para a redução da atividade fagocítica dos granulócitos —, a elevada prevalência de diabetes mellitus (DM) e o envelhecimento característico da população em diálise. Além disso, a exposição constante a potenciais fontes de contaminação durante o tratamento hemodialítico ou peritoneal aumenta de forma considerável a probabilidade de episódios infecciosos (BRAGA; BREGMAN; KIRSZTAJN, 2010).
Estudos longitudinais com pacientes que iniciam terapia renal substitutiva demonstram que tanto o avanço da idade quanto a presença de DM figuram entre os principais determinantes para o aparecimento de septicemia, independentemente da técnica dialítica utilizada. Esses achados reforçam a relevância das comorbidades como fatores agravantes da evolução clínica (BRAGA; BREGMAN; KIRSZTAJN, 2010).
Quando comparados à população geral, indivíduos em diálise apresentam risco significativamente mais elevado de óbito por sepse, alcançando índices centenas de vezes maiores mesmo após ajuste por faixa etária. A própria condição de insuficiência renal crônica constitui-se como fator de risco autônomo, sobrepondo-se a variáveis demográficas como sexo e etnia e evidenciando a gravidade do quadro urêmico (BRAGA; BREGMAN; KIRSZTAJN, 2010).
Apesar disso, as diferenças observadas nas taxas de mortalidade não podem ser atribuídas exclusivamente às infecções relacionadas ao acesso vascular ou peritoneal. Apenas cerca de 11% de pacientes em hemodiálise e 35% em diálise peritonial estão associados a óbitos por sepse. Outros elementos, como o impacto sistêmico da síndrome urêmica, o envelhecimento, a presença de DM e fatores específicos do processo dialítico — incluindo a biocompatibilidade das membranas utilizadas e a sobrecarga de ferro —, também exercem papel fundamental no aumento da suscetibilidade a infecções bacterianas (BRAGA; BREGMAN; KIRSZTAJN, 2010).
1.3. OBJETIVOS
1.3.1. Objetivo Geral
Analisar o impacto da atuação do farmacêutico clínico na prevenção de interações medicamentosas em pacientes com DRC.
1.3.2. Objetivos específicos
– Identificar os principais medicamentos utilizados por pacientes com Doença Renal Crônica (DRC) em acompanhamento clínico.
– Verificar a frequência e a gravidade das interações medicamentosas potenciais e reais nesses pacientes.
– Avaliar intervenções clínicas realizadas pelo farmacêutico clínico na prevenção ou resolução de interações medicamentosas.
– Classificar as interações medicamentosas quanto ao mecanismo (farmacocinético ou farmacodinâmico) e ao risco clínico envolvido.
– Analisar o perfil clínico e laboratorial dos pacientes com DRC para verificar fatores que potencializam o risco de interações medicamentosas.
– Mensurar o impacto das intervenções farmacêuticas na segurança e eficácia da farmacoterapia dos pacientes com DRC.
– Avaliar a aceitação das intervenções farmacêuticas pela equipe multiprofissional.
– Sugerir estratégias para aprimorar a atuação do farmacêutico clínico na prevenção de interações medicamentosas em serviços de atenção à saúde de pacientes renais.
1.4. JUSTIFICATIVA
O cuidado farmacêutico se dá, tanto para o paciente quanto para a sociedade, por meio de serviços clínicos bem estruturados. Esses serviços, como a conciliação de medicamentos, a monitorização do tratamento com medicamentos, a revisão do uso de medicamentos, o acompanhamento do tratamento com medicamentos e a gestão de condições de saúde, mostram a expertise do farmacêutico na identificação, prevenção e resolução de problemas relacionados ao uso de medicamentos (CFF, 2013).
A realização desses serviços deve basear-se nas Boas Práticas Farmacêuticas (BPF), que são um conjunto de normas e ações que garantem a qualidade e a segurança dos produtos e serviços farmacêuticos. Essa alinhamento é fundamental para assegurar um cuidado terapêutico completo, promover o uso racional de medicamentos, evitar complicações, contribuir para a promoção e recuperação da saúde e, por consequência, melhorar a qualidade de vida da população (CFF, 2016).
Os serviços de farmácia clínica têm grande potencial de impacto na atuação entre profissionais de diferentes áreas, favorecendo a oferta de cuidados seguros, eficazes e econômicos (McBane et al., 2015). Nesse contexto, médicos, enfermeiros, nutricionistas e farmacêuticos clínicos trabalham juntos na gestão das doenças associadas à doença renal crônica. (Stemer; Lemmens-Gruber, 2011).
A atuação do farmacêutico no cuidado do paciente com DRC foi organizada por Mason e Bakus (2010), que descreveram funções específicas, como o controle da anemia, da doença óssea renal e da hipertensão arterial, além da seleção e revisão do uso de medicamentos em um sentido mais geral. Por meio dessa atuação, é possível prevenir erros na medicação e reações adversas, aumentando a segurança dos tratamentos (Pehlivanli et al., 2023). Uma revisão sistemática com 20 estudos mostrou que a frequência de problemas do uso de medicamentos (PRMs) em pacientes com DRC varia entre 12% e 87%, mostrando a grande relevância dessa questão clínica (Alruqayb et al., 2021).
Dada essa frequência, é essencial identificar esses problemas precocemente e intervir de forma direcionada para reduzir os efeitos negativos. Nesse sentido, espera-se que a identificação e a intervenção sobre PRMs tornem o uso de medicamentos mais racional, levando a melhores resultados em saúde para essa população (Song et al., 2021).
2 FUNDAMENTAÇÃOTEÓRICA
2.1. DOENÇA RENAL CRÔNICA
2.1.1. Definição
A Doença Renal Crônica (DRC) é caracterizada por lesão do parênquima renal — mesmo com função renal preservada — e/ou por redução da função renal, persistentes por um período igual ou superior a três meses. A Sociedade Brasileira de Nefrologia (SBN) incorporou, de forma mais recente, a definição proposta pela National Kidney Foundation (NKF), dos Estados Unidos, a qual estabelece os critérios diagnósticos da Doença Renal Crônica (DRC):
– Presença de lesão renal por um período igual ou superior a três meses, identificada por anormalidades estruturais ou funcionais nos rins, com ou sem diminuição da taxa de filtração glomerular (TFG), evidenciadas por alterações histopatológicas, marcadores de lesão renal no sangue ou na urina, ou ainda por exames de imagem;
– TFG inferior a 60 mL/min/1,73 m² por três meses ou mais, com ou sem presença de lesão renal (SOCIEDADE BRASILEIRA DE NEFROLOGIA,2010).
Dessa forma, considera-se DRC toda condição em que há lesão renal e/ou diminuição funcional dos rins, mantida por um período mínimo de três meses. (SOCIEDADE BRASILEIRA DE NEFROLOGIA,2010)
Na maioria dos casos, a perda progressiva da função renal decorre de quadros de nefropatia crônica, como a insuficiência renal crônica (IRC). A IRC consiste em uma perda progressiva e irreversível das funções renais que pode se iniciar com um quadro agudo ou de maneira lenta e progressiva (TRENTINI et al., 2004).
2.1.2. Epidemiologia
A Doença Renal Crônica (DRC) é considerada um grave problema de saúde pública global, com crescente prevalência nos últimos anos. Estima-se que cerca de 10% a 15% da população adulta mundial apresente algum grau de comprometimento da função renal, sendo a hipertensão arterial e o diabetes mellitus os principais fatores de risco associados. No Brasil, dados do censo da Sociedade Brasileira de Nefrologia indicam um aumento progressivo no número de pacientes em terapia renal substitutiva, refletindo a crescente incidência da DRC, especialmente entre idosos e populações mais vulneráveis (SOCIEDADE BRASILEIRA DE NEFROLOGIA, 2020).
A Doença Renal Crônica (DRC) é considerada um relevante problema de saúde pública, com alta prevalência mundial e crescente impacto nos sistemas de saúde. Estima-se que entre 10% e 15% da população adulta global apresente algum grau de comprometimento da função renal, sendo o envelhecimento populacional, o diabetes mellitus, a hipertensão arterial e a obesidade os principais fatores de risco associados. No Brasil, a prevalência da DRC gira em torno de 10% da população adulta, o que representa mais de 20 milhões de pessoas. Dados da Pesquisa Nacional de Saúde (PNS 2019) indicam prevalência autorreferida de 1,4%, com valores mais elevados entre indivíduos com hipertensão (3,3%) e diabetes (4,1%). Além disso, entre 2019 e 2023, houve um aumento de mais de 150% nos atendimentos em atenção primária relacionados à DRC no Sistema Único de Saúde (SUS), com predominância de casos nas regiões Sudeste e Sul e em pacientes com idade entre 50 e 79 anos. Tais dados refletem não apenas o aumento da detecção da doença, mas também a sobrecarga progressiva sobre os serviços de saúde, exigindo estratégias de prevenção e monitoramento mais eficazes (MINISTÉRIO DA SAÚDE, 2024; SOCIEDADE BRASILEIRA DE NEFROLOGIA, 2024; SOUSA et al., 2023).
O resultado da análise univariada indicou que os indivíduos mais velhos (≥ 65anos; OR = 8,55; IC95% 6,01 – 12,16), com planos privados relacionados à saúde (OR = 1,20; IC95% 1,04 – 1,38), obesidade declarada (OR = 1,26; IC95% 1,02 – 1,54), que referiram estado de saúde ruim/muito ruim (OR = 7,07; IC95% 5,81 – 8,60), fumantes (OR = 1,85; IC95% 1,55 – 2,20) e ex-fumantes (OR = 2,20; IC95% 1,88 – 2,58) e portadores de doenças crônicas, tais como hipertensão (OR = 2,81; IC95% 2,45 – 3,22), diabetes (OR = 2,78; IC95% 2,30 – 3,36) e hipercolesterolemia (OR = 3,07; IC95% 2,65 – 3,56), apresentaram alta probabilidade de diagnóstico de DRC. Verificou-se que a raça /cor e o nível de escolaridade foram fatores protetores de DRC. Os indivíduos com a cor da pele autorreferida parda (OR = 0,77; IC95% 0,67 – 0,89), ensino médio completo (OR = 0,45; IC95% 0,38 – 0,53) e superior completo (OR = 0,46; IC95% 0,36 – 0,59 apresentaram menor probabilidade de diagnóstico da DRC. Verificou-se, também, que o consumo de álcool abusivo (OR = 0,59; IC95% 0,41 – 0,85) e a realização de exercício no tempo livre (OR = 0,67; IC95% 0,56 – 0,81) reduziram a chance da Doença Renal Crônica (REVISTA BRASILEIRA DE EPIDEMIOLOGIA, 2020).
2.1.3. Estágios
A Taxa de Filtração Glomerular (TFG) é um parâmetro essencial para avaliar a função renal, representando o volume de sangue filtrado pelos glomérulos dos rins por minuto. Ela é influenciada por fatores como pressão de filtração, pressão hidrostática na cápsula de Bowman e o coeficiente de filtração glomerular, além da regulação do fluxo sanguíneo nas arteríolas glomerulares. Em condições normais, a TFG média é de aproximadamente 125 mL/min. Valores abaixo de 60 mL/min/1,73 m² por pelo menos três meses consecutivos são indicativos de doença renal crônica (JUNIOR et.al, 2024).
Para estimar a TFG na prática clínica, utiliza-se a equação CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration), que considera fatores como idade, sexo, raça e níveis de creatinina sérica. Essa equação é preferida por apresentar maior precisão em comparação com outras fórmulas, como a MDRD-4, especialmente em estágios iniciais da DRC. Contudo, é importante notar que a inclusão de parâmetros raciais na equação pode levar a superestimações da TFG, especialmente em populações negras, devido à definição social da raça e não necessariamente a diferenças genotípicas ou metabólicas (JUNIOR et.al, 2024).
Além disso, a TFG tende a diminuir com o envelhecimento, cerca de 1 mL/min por ano, e pode ser influenciada por condições como gravidez, que pode aumentar a TFG devido ao aumento do fluxo sanguíneo renal. De forma sintetizada, a TFG é um indicador essencial da função renal, sendo imprescindível para diagnosticar e acompanhar a DRC. Sua estimativa precisa é essencial para a estratificação de risco e definição de estratégias terapêuticas adequadas (JUNIOR et.al, 2024).
Os estágios da doença renal crônica (DRC) são classificados de acordo com a taxa de filtração glomerular (TFG) em: G1 (≥90 mL/min/1,73 m²), G2 (60–89 mL/min/1,73 m²), G3a (45–59 mL/min/1,73 m²), G3b (30–44 mL/min/1,73 m²), G4 (15–29 mL/min/1,73 m²), G5 (<15 mL/min/1,73 m²) e G5D (diálise). Considera-se DRC em estágios G1 e G2 quando há evidência de lesão renal, geralmente caracterizada pela presença de albuminúria (>30 mg/g ou >3 mg/mmol), mesmo com TFG >60 mL/min/1,73 m². Já os estágios G3 a G5 expressam reduções da TFG. O manejo terapêutico é conservador em sua maioria nos estágios G1 a G4, enquanto no estágio G5 torna-se é necessário iniciar a terapia renal substitutiva (JUNIOR et.al, 2024).
2.1.4. Complicações associadas
A nefropatia diabética configura-se como uma das complicações mais frequentes da doença renal crônica (DRC), caracterizando-se pela lesão progressiva dos pequenos vasos sanguíneos renais. Esse processo desencadeia alterações estruturais em glomérulos e túbulos, frequentemente associadas a proteinúria, hipertensão arterial e maior risco de insuficiência renal e eventos cardiovasculares, o que evidencia a necessidade de monitoramento contínuo e de terapias adequadas (National Kidney Foundation, 2020).
Além disso, distúrbios ósseos e minerais são comuns em fases avançadas da DRC, diretamente relacionados a alterações no metabolismo mineral e ósseo, exacerbadas pela deficiência de vitamina D ativa e pela hiperfosfatemia. Essas disfunções resultam em osteodistrofia renal, calcificações vasculares e fraturas, impactando a qualidade de vida e aumentando a morbimortalidade cardiovascular (National Kidney Foundation, 2023).
Além disso, destaca-se a anemia como uma complicação muito comum da DRC, resultante da redução na produção renal de eritropoietina. Os pacientes apresentam fadiga, fraqueza e dispneia, e, além de comprometer a qualidade de vida, essa condição associa-se a maior risco cardiovascular, demandando intervenções específicas (KDIGO, 2021).
Complicações metabólicas também são frequentes, como a acidose metabólica, que surge da incapacidade renal de eliminar ácidos, levando a anorexia, náuseas, distúrbios neurológicos e maior risco de doença óssea. A correção desse distúrbio é essencial para prevenir consequências adicionais. Outras manifestações menos comuns, porém graves, incluem a pericardite urêmica — caracterizada por inflamação do pericárdio devido ao acúmulo de ureia — que pode evoluir para tamponamento cardíaco, configurando risco de morte (SENA et al., 2021).
Entre as complicações neurológicas, destaca-se a neuropatia periférica, resultante do acúmulo de toxinas urêmicas, que provoca dor, parestesias, fraqueza muscular e disfunções autonômicas, comprometendo a autonomia do paciente (KDIGO, 2021).
No trato gastrointestinal, a gastrite urêmica (devido acúmulo de uremia) é caracterizada por irritação da mucosa gástrica devido às toxinas, causando náuseas, anorexia, úlceras e hemorragias, o que consequentemente piora o estado nutricional. Já a pneumonite urêmica, embora rara, constitui uma complicação pulmonar grave, caracterizada por inflamação e infiltrados pulmonares que podem evoluir para insuficiência respiratória aguda (National Kidney Foundation, 2020).
No Brasil, o diabetes mellitus e a hipertensão arterial são as principais causas da DRC, reforçando a importância de estratégias de prevenção e controle dessas condições (Lugon, 2009). Nas fases iniciais, os sintomas da DRC são inespecíficos — como fadiga, inapetência e alterações urinárias —, tornando o diagnóstico precoce um desafio (Sesso e Gordan, 2007). À medida que a doença progride, complicações mais severas surgem, incluindo anemia, distúrbios ósseos, hipercalemia e acidose metabólica, o que ressalta a necessidade de rastreamento laboratorial contínuo por meio de exames como creatinina sérica, ureia, eletrólitos, urina e ultrassonografia (Porto et al., 2017).
As medidas terapêuticas abrangem controle da pressão arterial e controle glicêmico em diabéticos, restrição de sódio, proteínas e fósforo, uso de anti-hipertensivos e, diante de estágios mais avançados, diálise ou transplante renal (KDIGO, 2013). Dessa forma, a identificação e o tratamento precoce das causas subjacentes, aliados a estratégias preventivas, são fundamentais para retardar a progressão da doença e melhorar a qualidade de vida dos pacientes (Porto et al., 2017).
2.1.5. Tratamentos (clínico, diálise, transplante)
A insuficiência renal aguda (IRA) refere-se à perda súbita e temporária da função dos rins, ocorrendo em questão de horas ou poucos dias. Essa condição é caracterizada pela redução abrupta da taxa de filtração glomerular (TFG), geralmente acompanhada de distúrbios hidroeletrolíticos e ácido-básicos. Entre as possíveis causas estão eventos como desidratação severa, sepse, obstrução urinária ou uso de substâncias nefrotóxicas. Em muitos casos, pode ser necessário o suporte dialítico temporário até que a função renal seja restaurada, o que pode levar semanas, dependendo da etiologia e da resposta terapêutica (ABENSUR, 2001).
Por outro lado, a doença renal crônica (DRC) — ou insuficiência renal crônica (IRC) — caracteriza-se pela perda progressiva, lenta e geralmente irreversível da função renal. Trata-se de uma síndrome clínica cuja principal característica é a redução persistente da TFG ao longo do tempo (RIBEIRO et al., 2008). Durante as fases iniciais, mecanismos compensatórios permitem que o paciente permaneça assintomático. Contudo, à medida que a função renal residual cai para níveis inferiores a 10–12% do normal, torna-se imprescindível o manejo clínico rigoroso, com uso de medicamentos específicos e dieta controlada. Nos estágios finais da doença, o tratamento conservador não é mais suficiente, sendo necessária a introdução de terapias renais substitutivas, como a diálise ou o transplante renal (SBN, 2012).
Manejo Clínico Conservador
O tratamento clínico da DRC visa retardar a progressão da doença e prevenir complicações. De acordo com revisões sistemáticas de ensaios clínicos randomizados, iniciadas na década de 1990, o uso de inibidores do sistema renina-angiotensina-aldosterona (RAAS), como os inibidores da enzima conversora de angiotensina (IECA) e os bloqueadores dos receptores de angiotensina (BRA), mostrou-se eficaz em retardar a deterioração da função renal.
Mais recentemente, os inibidores do cotransportador sódio-glicose tipo 2 (SGLT2) — como canagliflozina e dapagliflozina — ganharam destaque. Esses fármacos, além do efeito hipoglicemiante, demonstraram reduzir o risco de progressão para falência renal e mortalidade em pacientes com ou sem diabetes, especialmente quando utilizados em conjunto com a terapia baseada em RAAS (SANCHEZ, 2021).
Outras medidas conservadoras fundamentais incluem: controle rigoroso da pressão arterial, manejo adequado da glicemia, restrição dietética de proteína e sódio, correção da acidose metabólica, controle de anemia e dislipidemias, além do manejo da hiperfosfatemia.
Terapia Renal Substitutiva: Diálise
Quando o tratamento clínico não é mais suficiente para manter a qualidade de vida e surgem sintomas urêmicos significativos, a diálise torna-se necessária. A diálise é um procedimento terapêutico que substitui parcialmente as funções renais, promovendo a remoção de toxinas, excesso de líquidos e eletrólitos do organismo. Existem duas modalidades principais: hemodiálise e diálise peritoneal (SBN, 2012).
Hemodiálise
A hemodiálise é realizada em ambiente hospitalar ou clínicas especializadas e requer o uso de um equipamento chamado dialisador. O sangue do paciente é retirado por meio de uma fístula arteriovenosa (ou cateter venoso de grande calibre), filtrado no dialisador e retornado ao corpo. Esse processo, geralmente realizado três vezes por semana, dura de três a quatro horas por sessão (SAÚDE BIAZI, 2012).
Apesar da eficácia, a hemodiálise está associada a efeitos colaterais, como hipotensão (que pode causar tontura, fraqueza e náuseas) e cãibras musculares. Além disso, pode comprometer significativamente a qualidade de vida, impondo limitações físicas, emocionais e sociais (HOSPITAL ALBERT EINSTEIN, 2012).
Diálise Peritoneal
A diálise peritoneal (DP), por sua vez, é uma alternativa domiciliar que utiliza o peritônio como membrana semipermeável para a troca de substâncias. A solução dialítica é infundida na cavidade abdominal por meio de um cateter, onde permanece por algumas horas antes de ser drenada e substituída.
As principais modalidades de DP são:
Diálise Peritoneal Ambulatorial Contínua (DPAC): método manual realizado várias vezes ao dia, sem uso de máquina, adequado para pacientes com limitação ao acesso vascular, crianças, idosos e pessoas com alta permeabilidade peritoneal (RIELLA, 2003).
Diálise Peritoneal Automatizada (DPA) ou Contínua Cíclica (DPCC): feita com auxílio de uma máquina (cicladora), geralmente durante o sono, permitindo mais liberdade durante o dia. Apresenta menor risco de infecção e melhor controle da ultrafiltração, embora seu uso no Brasil ainda seja limitado pelo alto custo (PROENÇA, 1999).
Diálise Peritoneal Intermitente (DPI): realizada em ambiente hospitalar, indicada a pacientes com função renal residual importante e alta permeabilidade da membrana peritoneal. Utiliza grande volume de solução em sessões longas, duas vezes por semana (RIELLA, 2003).
A complicação mais comum da DP é a peritonite, uma infecção grave do peritônio, frequentemente relacionada à má assepsia na manipulação do cateter. A presença de lesões peritoneais ou doenças malignas constitui contraindicação à técnica (SAÚDE BIAZI, 2012).
Transplante Renal
O transplante renal é amplamente considerado o tratamento de escolha para pacientes com DRC em estágio terminal. Além de restaurar a função renal, o procedimento promove significativa melhora na qualidade de vida, maior liberdade em relação às terapias dialíticas e redução de complicações associadas à uremia, como doenças cardiovasculares e distúrbios metabólicos (SBN, 2022).
O transplante pode ser realizado com rim proveniente de doador vivo ou falecido. No entanto, há desafios importantes, como a escassez de órgãos e o risco de rejeição imunológica. Para evitar essa rejeição, é necessário o uso contínuo de imunossupressores, os quais, por sua vez, aumentam o risco de infecções e neoplasias (SBN, 2022).
Estudos demonstram que a presença de anticorpos anti-HLA (DSA) aumenta significativamente o risco de rejeição do enxerto, tanto em fases agudas quanto crônicas. Além disso, pesquisas mostram que pacientes acompanhados por equipes multidisciplinares, incluindo transplantados e pré-dialíticos, apresentam desfechos clínicos similares, como sobrevida e manutenção da TFG (SBN, 2022).
A experiência subjetiva do transplante também tem sido investigada. Um estudo de Lazzaretti e Rasia (2003) apontou que a qualidade de vida melhora consideravelmente após o transplante. Já uma revisão integrativa realizada por Zanetti (2018) evidenciou o impacto emocional positivo do procedimento, sendo frequentemente descrito pelos pacientes como uma verdadeira “carta de alforria” frente às limitações da hemodiálise (SBN, 2022).
2.2.SISTEMA RENINA-ANGIOTENSINA-ALDOSTERONA (SRAA)
O sistema renina-angiotensina-aldosterona (SRAA) é formado por diferentes componentes: renina, angiotensinogênio, angiotensina I, angiotensina II, angiotensina III, enzima conversora da angiotensina (ECA), angiotensinases e aldosterona. A renina, uma enzima proteolítica glicoprotéica presente no plasma sanguíneo, é sintetizada, armazenada e secretada principalmente pelos rins, por meio do aparelho justaglomerular (SPINOSA et al., 1999).
Sua principal função é hidrolisar o angiotensinogênio em angiotensina I, um decapeptídeo. Esta, ao circular no sangue, é rapidamente convertida em angiotensina II pela ação da ECA, uma dipeptidilpeptidase, resultando em um octapeptídeo com potente efeito vasoconstritor. A angiotensina IIestimula a produção e liberação de aldosterona, regula de forma indireta a liberação de renina, permite a reabsorção de sódio e possibilita o equilíbrio hídrico e pressórico. Além disso, exerce influência sobre o crescimento de células endoteliais e aumenta a liberação de noradrenalina pelas terminações nervosas simpáticas (SPINOSA et al., 1999).
A angiotensina II pode ser degradada pela ação das angiotensinases, formando metabólitos como a angiotensina III, que atua no córtex adrenal estimulando a secreção de aldosterona, além de participar da regulação do mecanismo da sede. Dessa forma, a angiotensina II é considerada o principal mediador fisiológico do SRAA, sobretudo no sistema nervoso central. A aldosterona, por sua vez, aumenta a reabsorção de sódio e cloreto e estimula a secreção de potássio e íons hidrogênio nos túbulos coletores, favorecendo a retenção de água e, consequentemente, o aumento do volume sanguíneo (NELSON; 2006).
O SRAA pode ser modulado por diferentes fármacos que atuam na síntese ou na ação da angiotensina II. Entre eles, destacam-se os inibidores da renina e, principalmente, os inibidores da ECA, que impedem a conversão da angiotensina I em angiotensina II. Os inibidores da ECA são divididos em três grupos: agentes quelantes, inibidores não peptídicos e inibidores peptídicos. O primeiro fármaco desenvolvido foi o captopril, um inibidor competitivo ativo por via oral. Posteriormente, buscou-se novas drogas com maior potência e menor incidência de efeitos adversos, surgindo o enalapril, com ação mais prolongada (SPINOSA et al., 1999).
As células justaglomerulares, localizadas nas arteríolas aferentes renais, armazenam prorrenina, a qual é convertida em renina pela ação de enzimas como a proconvertase 1 e a catepsina B. A renina madura permanece em grânulos nessas células e é liberada na circulação diante de quatro estímulos principais:
– Alterações da perfusão renal, percebidas por mecanorreceptores da parede arteriolar aferente;
– Redução da concentração de sódio e cloro no túbulo contorcido distal, detectada pela mácula densa;
– Ativação do sistema nervoso simpático, especialmente por estímulo beta-adrenérgico (receptores β1), mais evidente na postura ereta;
– Feedback de fatores humorais, como angiotensina I, potássio (a liberação aumenta na hipocalemia e reduz na hipercalemia) e peptídeo natriurético atrial.
Assim, condições associadas à queda da perfusão renal ou à diminuição da carga tubular de sódio estimulam a secreção de renina na corrente sanguínea.Os efeitos fisiológicos da angiotensina II sobre o volume extracelular e a pressão arterial ocorrem por cinco mecanismos principais:
– Vasoconstrição pela contração do músculo liso arteriolar;
– Estímulo à secreção de aldosterona pela zona glomerulosa do córtex adrenal, via indução do gene CYP11B2 (aldosterona sintase);
– Aumento da reabsorção de sódio no túbulo contorcido proximal, por ativação do antiporte Na⁺/H⁺;
– Intensificação do tônus simpático central;
– Liberação de vasopressina pelo hipotálamo.
Além dos efeitos fisiológicos, a angiotensina II está relacionada a processos patológicos, como estresse oxidativo, fibrose, disfunção endotelial, hipertrofia celular, inibição da apoptose e estímulo à proliferação. Esses mecanismos participam da fisiopatologia da hipertensão, aterosclerose, insuficiência cardíaca e doença renal. Tais ações são mediadas principalmente por dois receptores: AT1-R e AT2-R. (LAPPIN,2023).
O receptor AT1 (AT1-R), acoplado à proteína G, é expresso de forma abundante em tecidos como coração, rins, glândulas suprarrenais, hipófise, sistema nervoso central e vasos sanguíneos. Ele medeia os efeitos de vasoconstrição, retenção de sódio e água. Em condições patológicas, sua ativação promove inflamação, estresse oxidativo, remodelamento tecidual e aumento da pressão arterial, sendo central na gênese de doenças cardiovasculares e renais (LAPPIN,2023).
Já o receptor AT2 (AT2-R), também acoplado à proteína G, predomina em tecidos fetais e apresenta expressão reduzida na vida adulta, embora ainda esteja presente no coração, rins, cérebro e suprarrenais. Sua ativação desencadeia efeitos opostos ao AT1-R, como vasodilatação, natriurese, inibição da fibrose, da inflamação e do tônus simpático central (LAPPIN,2023).
A aldosterona, cuja síntese é regulada principalmente pela angiotensina II, pelo ACTH (Hormônio Adrenocorticotrófico: um hormônio produzido pela hipófise que estimula as glândulas suprarrenais a produzir cortisol e outros esteróides) e pela concentração plasmática de potássio, possui meia-vida inferior a 20 minutos. Ela atua por meio de receptores mineralocorticoides citoplasmáticos nas células principais do ducto coletor cortical. Esse mecanismo aumenta a expressão dos canais de sódio epiteliais na membrana apical e estimula a Na⁺/K⁺-ATPase na membrana basolateral, promovendo maior reabsorção de sódio e secreção de potássio. Além do controle renal, a aldosterona influencia a sede e o apetite por sal, modulando receptores mineralocorticoides no sistema nervoso central (LAPPIN,2023).
A superativação do sistema renina-angiotensina-aldosterona (SRAA) é reconhecida como fator determinante no desenvolvimento de hipertensão primária e secundária, além de estar associada a morbidade e mortalidade cardiovascular e renal. No hiperaldosteronismo primário, geralmente causado por adenoma adrenal (síndrome de Conn) ou hiperplasia adrenal bilateral, observa-se produção excessiva de aldosterona com renina suprimida, hipocalemia e maior risco de complicações cardiovasculares e renais (LAPPIN,2023).
Diversos fármacos atuam sobre o SRAA, entre eles:
– Inibidores diretos da renina (ex.: aliscireno), sem benefícios clínicos consistentes em estudos de longo prazo;
– Inibidores da Enzima Conversora da Angiotensina (IECA) (ex.: captopril, enalapril, ramipril, lisinopril), eficazes na redução da hipertensão, hospitalizações por insuficiência cardíaca e progressão da doença renal;
– Bloqueadores do Receptor de Angiotensina (BRA) (ex.: losartana, valsartana, candesartana), que apresentam benefícios cardiovasculares e renais semelhantes aos IECA;
– Antagonistas dos Receptores Mineralocorticoides (ex.: espironolactona, eplerenona, finerenona), que reduzem hospitalizações e mortalidade em insuficiência cardíaca e melhoram desfechos renais, especialmente na doença renal diabética;
– Inibidores da aldosterona sintase (ex.: baxdrostat), atualmente em avaliação, com resultados promissores em hipertensão resistente;
– Bloqueadores dos canais de sódio epiteliais (ex.: amilorida, triantereno), que reduzem a reabsorção de sódio independentemente da ação mineralocorticoide.
O bloqueio farmacológico do SRAA contribui para a redução da vasoconstrição, melhora da perfusão renal, diminuição da inflamação, da fibrose e da remodelação cardíaca e renal, configurando um dos pilares do tratamento de doenças cardiovasculares e renais.
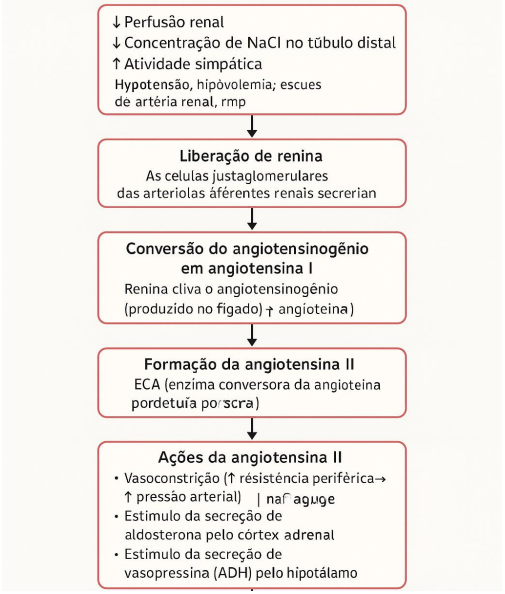
Em suma, a ativação é na seguinte ordem: Hipotensão/hipovolemia → Renina →
Angiotensina I → (ECA) → Angiotensina II → Vasoconstrição + Aldosterona + ADH → Retenção de Na⁺ e H₂O → ↑ Pressão arterial. O ciclo pode ser sistematizado conforme abaixo:
Figura 1: Sistema Renina-Angiotensina-Aldosterona
2.3. HIPERTENSÃO COMO CAUSA E CONSEQUÊNCIA DA DRC
A hipertensão arterial (HA) apresenta elevada prevalência e está associada a lesões em órgãos-alvo, como coração, vasos sanguíneos, cérebro e rins. A presença de HA entre portadores de DRC é bastante frequente, configurando-se como o principal fator de risco para o desenvolvimento e progressão da doença renal no país. Essa relação caracteriza-se por um ciclo de causa e consequência, em que a hipertensão agrava a lesão renal e esta, por sua vez, intensifica o quadro hipertensivo, culminando em pior prognóstico clínico (JORNAL BRASILEIRO DE NEFROLOGIA, 2024).
Entre os principais mecanismos fisiopatológicos envolvidos na HA associada à DRC destacam-se a retenção de sódio, a hiperatividade simpática e a ativação exacerbada do sistema renina-angiotensina-aldosterona. Tais alterações contribuem para modificações no comportamento da PA (pressão arterial) e em seu padrão circadiano. Assim, o controle adequado da PA torna-se fundamental, pois reduz o dano estrutural e funcional dos néfrons, além de impactar positivamente na expectativa de vida do paciente renal crônico (JORNAL BRASILEIRO DE NEFROLOGIA, 2024).
Para o manejo clínico, é indispensável a correta classificação da HA em normotensão, hipertensão verdadeira, hipertensão do avental branco ou hipertensão mascarada. A monitorização ambulatorial da pressão arterial (MAPA) é considerada a ferramenta mais eficaz para a avaliação da PA em 24 horas na prática clínica. Indivíduos com DRC frequentemente apresentam alterações características nesse exame, como a atenuação do descenso noturno ou até mesmo elevação da PA durante o sono. Apesar disso, estudos que investigam tais padrões ainda são limitados. Uma metanálise identificou apenas seis trabalhos que avaliaram a prevalência de hipertensão do avental branco e mascarada em pacientes renais crônicos. Embora esses estudos apontem altas prevalências dessas condições, o mais abrangente deles incluiu apenas 290 indivíduos. Além disso, a maioria não considerou potenciais variáveis de confusão, e não há trabalhos que analisem de forma específica as alterações de MAPA em cada estágio da DRC (JORNAL BRASILEIRO DE NEFROLOGIA, 2024).
A hipertensão arterial é frequentemente observada em pacientes com DRC, contribuindo para maior probabilidade de eventos cardiovasculares, progressão da própria doença renal e aumento da mortalidade. O estudo Systolic Blood Pressure Intervention Trial (SPRINT) demonstrou que manter a pressão arterial sistólica abaixo de 120 mmHg em adultos não diabéticos, mas com elevado risco cardiovascular — incluindo um número expressivo de indivíduos com DRC — reduziu de forma significativa tanto a incidência de doenças cardiovasculares quanto a mortalidade. Contudo, não foi evidenciado impacto relevante sobre a desaceleração da progressão da DRC. É importante destacar que, nesse ensaio, as medidas pressóricas foram realizadas por meio de aparelhos automatizados e, em grande parte, sem acompanhamento direto, o que tende a gerar valores inferiores aos obtidos em consultas clínicas convencionais. Além disso, sugere-se que a redução absoluta do risco seja potencialmente maior em pacientes com albuminúria, considerando a forte correlação dessa condição com complicações cardiovasculares e renais, embora os benefícios da redução intensiva ainda careçam de elucidação completa sobre o risco de DCV parecem ser similares pelo nível de albuminúria (DIRETRIZES BRASILEIRA DE HIPERTENSÃO ARTERIAL, 2020).
As evidências atuais recomendam que pacientes com DRC mantenham a pressão arterial abaixo de 130/80 mmHg, independentemente da presença de diabetes mellitus. Nos casos de DRC em estágio terminal, entretanto, os potenciais benefícios do controle mais rigoroso da pressão arterial permanecem incertos, visto que os estudos disponíveis possuem curta duração e os efeitos hemodinâmicos associados podem ocasionar redução adicional da taxa de filtração glomerular. De todo modo, qualquer estratégia de redução pressórica em indivíduos com DRC deve ser conduzida com cautela, assegurando a aferição adequada da pressão arterial e o acompanhamento contínuo de possíveis eventos adversos, em especial distúrbios eletrolíticos e queda do RFG (DIRETRIZES BRASILEIRAS DE HIPERTENSÃO ARTERIAL, 2020).
2.4. SEGURANÇA DO PACIENTE
A segurança do paciente refere-se ao direito fundamental de receber assistência em saúde sem exposição a danos que poderiam ser evitados. Para isso, os serviços devem estar estruturados de modo a minimizar falhas, identificar possíveis riscos de forma precoce e implementar intervenções eficazes para solucioná-los. O propósito central é assegurar que o cuidado prestado seja pautado na qualidade, no respeito e na proteção integral do paciente em todas as etapas de sua trajetória no sistema de saúde (BRASIL, 2014).
Eventos adversos, definidos como situações inesperadas que comprometem a segurança do cuidado, representam uma preocupação constante. Entre os exemplos mais frequentes estão erros relacionados ao uso de medicamentos, infecções que poderiam ser prevenidas e falhas na comunicação entre os profissionais de saúde. Essas ocorrências, além de impactarem negativamente o estado clínico, podem prolongar a hospitalização e aumentar os custos assistenciais. Dessa forma, a prevenção de riscos é uma estratégia indispensável para garantir o bem-estar e a preservação da vida dos pacientes (BRASIL, 2014).
A relevância do tema ganhou maior visibilidade internacional a partir da publicação do relatório To Err is Human, em 1999, o qual evidenciou que falhas na assistência em saúde eram responsáveis por milhares de óbitos anualmente. Desde então, a Organização Mundial da Saúde (OMS) passou a reconhecer a segurança do paciente como um desafio prioritário em nível global. No Brasil, a criação do Programa Nacional de Segurança do Paciente (PNSP) representou um marco nesse processo, pois visa orientar e apoiar as instituições de saúde na adoção de práticas mais seguras. Além disso, o programa incentiva o protagonismo do paciente e de seus familiares, estimulando-os a participar ativamente do cuidado por meio de perguntas, esclarecimentos e colaboração com a equipe multiprofissional. Essa participação contribui não apenas para a redução de riscos, mas também para um cuidado mais humanizado e centrado na pessoa (BRASIL, 2014).O PNSP tem como princípios e diretrizes:
– Fomento à cultura organizacional voltada para a segurança do paciente, incorporando princípios de vigilância, responsabilização e aprendizado contínuo em todos os níveis de atenção;
– Estruturação e implementação de sistemas formais e padronizados de gerenciamento de riscos assistenciais, com foco na identificação, análise, mitigação e monitoramento de eventos adversos;
– Estabelecimento de políticas institucionais que assegurem a transparência, incentivem a notificação voluntária e compulsória de incidentes críticos e promovam a análise sistemática dos eventos para subsidiar ações de melhoria;
– Valorização da autonomia do paciente e estímulo à sua participação ativa — e de seus familiares — nos processos de cuidado, por meio de estratégias educativas e comunicação efetiva;
– Integração dos princípios e práticas de segurança do paciente aos macroprocessos e fluxos operacionais das organizações de saúde, garantindo transversalidade e sustentabilidade das ações;
– Investimento contínuo na formação e capacitação multiprofissional, assegurando competências técnicas, gerenciais e éticas relacionadas à segurança assistencial e à gestão de riscos (BRASIL, 2014).
A adesão dos serviços de saúde ao Programa Nacional de Segurança do Paciente (PNSP) pode ser efetivada por meio da implementação das seguintes ações estratégicas:
– Estruturação e fortalecimento dos Núcleos de Segurança do Paciente (NSP), unidades responsáveis pela coordenação e execução das ações voltadas à segurança assistencial;
– Adoção de protocolos clínicos, diretrizes operacionais e boas práticas assistenciais alinhadas às recomendações do PNSP;
– Promoção da qualificação contínua e do engajamento dos profissionais de saúde na consolidação de uma cultura organizacional voltada à segurança do paciente;
– Estímulo à notificação sistemática de incidentes e eventos adversos, acompanhada da análise crítica e da implementação de ações corretivas e preventivas (BRASIL, 2014).
A Resolução da Diretoria Colegiada (RDC) nº 36/2013 institui ações obrigatórias para a promoção da segurança do paciente e a melhoria da qualidade dos serviços de saúde públicos e privados em todo o país, com exceção de consultórios individualizados, laboratórios clínicos, serviços móveis e de atenção domiciliar.
Visa estabelecer requisitos mínimos para a gestão de riscos e prevenção de eventos adversos relacionados à assistência à saúde. Aplica-se a estabelecimentos de qualquer natureza e complexidade, inclusive aqueles vinculados ao ensino e à pesquisa (RDC nº 36/2013).
Define termos essenciais como:
Segurança do paciente: redução do risco de dano desnecessário durante o cuidado;
– Evento adverso: incidente que resulta em dano à saúde;
– Gestão de risco: conjunto de ações contínuas para identificar, avaliar e controlar riscos assistenciais;
– Núcleo de Segurança do Paciente (NSP): instância interna do serviço responsável por coordenar e implementar ações de segurança;
– Plano de Segurança do Paciente (PSP): documento técnico que estrutura ações para prevenir e mitigar riscos ao longo da jornada do paciente (RDC nº 36/2013).
Criação e Funcionamento do NSP
Todos os serviços de saúde abrangidos devem criar e estruturar um NSP, com equipe nomeada e recursos garantidos pela direção. Esse núcleo deve:
– Elaborar e acompanhar o PSP;
– Implementar protocolos nacionais de segurança do paciente;
– Monitorar indicadores;
– Estabelecer barreiras para prevenção de incidentes;
– Capacitar profissionais;
– Analisar e notificar eventos adversos (RDC nº 36/2013).
Plano de Segurança do Paciente (PSP)
– Gerenciamento de riscos;
– Identificação correta do paciente;
– Higienização das mãos;
– Segurança em procedimentos (cirúrgicos, medicamentoso, hemoterápico, nutricional, uso de equipamentos etc.);
– Prevenção de quedas, úlceras por pressão e infecções relacionadas à assistência;
– Comunicação efetiva entre profissionais; l Envolvimento do paciente e família no cuidado;
– Promoção de ambiente seguro (RDC nº 36/2013).
Notificação e Monitoramento
– Notificação mensal obrigatória dos eventos adversos por meio eletrônico, até o 15º dia útil de cada mês;
– Notificação de eventos com óbito em até 72 horas;
– Análise e divulgação interna dos dados;
– Guarda e disponibilização das notificações à autoridade sanitária (RDC nº 36/2013).
A Anvisa, junto ao Sistema Nacional de Vigilância Sanitária, é responsável por:
– Monitorar as notificações;
– Publicar relatórios anuais;
– Apoiar investigações locais, especialmente em casos com óbito (RDC nº 36/2013).
Os serviços têm 120 dias para estruturar o NSP e elaborar o PSP, e 150 dias para iniciar as notificações mensais, contados a partir da publicação da norma. O descumprimento da RDC configura infração sanitária, passível de sanções conforme a Lei nº 6.437/1977 (RDC nº 36/2013). No presente trabalho há foco para a meta 3 internacional do NSP: Segurança na Prescrição, Uso e Administração de Medicamentos. Para cumprir a meta nas instituições de saúde é necessário seguir alguns requisitos:
– Identificação e manejo de medicamentos de alto risco:
– Deve-se dar atenção prioritária a medicamentos que apresentam potencial elevado para causar danos graves em caso de uso inadequado, tais como insulina, anticoagulantes e sedativos.
– Rotulagem adequada:
– Todos os medicamentos devem ser armazenados e identificados de forma correta, com etiquetagem clara, a fim de prevenir erros por confusão ou troca.
– Evitar abreviações e siglas:
– Recomenda-se o uso dos nomes completos dos medicamentos, evitando abreviações que possam gerar ambiguidades e comprometer a segurança do paciente.
– Verificação rigorosa pré-administrativa:
Antes da administração de qualquer medicamento, deve-se assegurar a conformidade dos seguintes parâmetros:
Paciente correto;Medicamento correto;Dose correta;Via de administração correta;Horário correto;Registro preciso e tempestivo no prontuário, Educação do paciente e familiares.
Os profissionais de saúde devem orientar o paciente e seus familiares quanto aos medicamentos prescritos, explicando a finalidade, modo correto de uso e possíveis efeitos adversos.
Revisão farmacoterapêutica no momento da alta hospitalar:
Deve ser realizada avaliação criteriosa dos medicamentos em uso pelo paciente, garantindo que as orientações terapêuticas estejam claras para continuidade do tratamento domiciliar (BRASIL, 2014).
Por fim, dentro da meta 3 que engloba a segurança medicamento é necessário aplicar o procedimento seguro de administração de medicamentos – Prática dos “13 Certos” (MINISTÉRIO DA SAÚDE, 2013).
Durante o processo de administração medicamentosa, o profissional de saúde deve seguir uma conduta técnica padronizada que assegure a precisão, rastreabilidade e segurança da terapia. Antes da administração, é indispensável verificar:
– Identificação do paciente (nome completo, pulseira de identificação, leito e prontuário);
– Nome do medicamento, dose prescrita, apresentação farmacêutica, via, horário, posologia, preparo e tempo de infusão;
– Resposta terapêutica esperada e observação de reações adversas.
– Após a administração, deve-se realizar checagem e registro no prontuário físico e eletrônico (SMPEP), incluindo anotações de enfermagem pertinentes.
Boas práticas na administração medicamentosa – Os 13 Certos:
– Paciente certo: Confirmar a identidade verbalmente com o paciente (nome completo), e cruzar com a pulseira de identificação, leito e prontuário/prescrição médica.
– Medicamento certo: Verificar nome, diluição, aprazamento e tempo de infusão conforme prescrição. Avaliar histórico de alergias.
– Dose certa: Validar a dose prescrita. Atenção especial para valores com uso de zeros à esquerda/direita, vírgulas ou pontos.Aspecto físico correto da medicação: Avaliar integridade, cor, precipitação e presença de corpos estranhos. Não administrar em caso de alterações.
– Validade certa: Conferir o prazo de validade de cada fármaco antes da administração.
– Via de administração correta: Confirmar se a via prescrita (oral, intravenosa, intramuscular etc.) é adequada para o tipo de medicamento.
– Horário certo: Preparar e administrar no horário prescrito. Observar indicações como “se necessário”, “agora”, ou “antes da próxima medicação”, “(ACM)”, sempre acompanhadas de posologia e justificativa clínica.
– Compatibilidade medicamentosa certa: Avaliar interações medicamentosas e/ou alimentares entre os fármacos administrados.
– Orientação correta ao paciente: Informar o paciente (ou familiar responsável) sobre o nome do medicamento, indicação, efeitos esperados e potenciais reações adversas.
– Direito de recusa: O paciente possui direito legal de recusar a medicação, devendo tal decisão ser respeitada, registrada e comunicada à equipe multiprofissional.
– Registro correto: Documentar rigorosamente no prontuário o horário de administração, fármaco utilizado, efeitos clínicos, intercorrências, recusas, omissões justificadas ou eventos adversos.
– Forma de apresentação correta: Verificar se a forma farmacêutica (comprimido, solução, suspensão etc.) está adequada para o paciente e condiz com a prescrição.
– Tempo de administração correto: Observar o tempo recomendado para infusão ou ingestão, evitando administrações muito rápidas ou lentas que comprometam a eficácia ou segurança do fármaco (MINISTÉRIO DA SAÚDE, 2013).
A Portaria MS/GM nº 529/2013 determina a elaboração e implementação de um conjunto de protocolos básicos de segurança, alinhados às diretrizes da Organização Mundial da Saúde (OMS). Entre esses protocolos, destacam-se: a prática da higienização das mãos nos serviços de saúde; a realização de cirurgias seguras; a segurança na prescrição, no uso e na administração de medicamentos; a correta identificação dos pacientes; a comunicação eficaz dentro das unidades de saúde; a prevenção de quedas; o cuidado com úlceras por pressão; a transferência segura de pacientes entre diferentes níveis de atenção; e o uso apropriado de equipamentos e materiais (MINISTÉRIO DA SAÚDE, 2014).
Esses protocolos correspondem tanto aos desafios globais de segurança do paciente propostos pela OMS — como a higiene das mãos e a cirurgia segura — quanto às chamadas soluções práticas para problemas recorrentes, incluindo: o risco relacionado a medicamentos com nomes e embalagens semelhantes; o controle rigoroso de soluções eletrolíticas concentradas; a garantia da medicação correta durante as transições do cuidado (por meio da conciliação medicamentosa); a correta identificação do paciente; e a comunicação clara e precisa durante a passagem de informações clínicas. (MINISTÉRIO DA SAÚDE, 2014)
Os Núcleos de Segurança do Paciente (NSPs), instituídos pela Portaria MS/GM nº 529/2013 e pela RDC nº 36/2013 da Anvisa, devem ser estabelecidos nos serviços de saúde com o objetivo de promover e apoiar a implementação de ações voltadas à segurança do paciente. A estrutura e organização dos NSPs variam conforme o tipo de estabelecimento: nos hospitais, sua conformação é distinta da aplicada a serviços não hospitalares. Em unidades de Atenção Básica situadas em uma mesma região de saúde, por exemplo, é possível que um único NSP atenda a todas elas, desde que definido pelo gestor local (MINISTÉRIO DA SAÚDE, 2014).
Nos hospitais, os NSPs devem estar vinculados diretamente à direção da instituição e manter uma agenda regular de reuniões com a direção geral, a direção técnica ou médica e a coordenação de enfermagem. Além disso, é fundamental que participem de reuniões com outras instâncias responsáveis pela gestão da qualidade, regulamentadas por normativas específicas, como a Comissão de Controle de Infecção Hospitalar, Comissão de Revisão de Óbito, Comissão de Análise de Prontuário, Comissão de Farmácia e Terapêutica, Gerência de Risco, Gerência de Resíduos, Núcleo de Saúde do Trabalhador, entre outras (MINISTÉRIO DA SAÚDE, 2014).
A principal função dos NSPs é atuar como articuladores e catalisadores das demais instâncias que gerenciam riscos e promovem ações de qualidade dentro da instituição, favorecendo a complementaridade e a integração entre essas áreas. Hospitais que já disponham de uma estrutura voltada à gestão da qualidade, como comissões ou comitês específicos, devem adequar essas estruturas às diretrizes estabelecidas pela Portaria MS/GM nº 529/2013 e pela RDC nº 36/2013 da Anvisa (MINISTÉRIO DA SAÚDE, 2014).
Cabe ainda aos NSPs a responsabilidade pela elaboração do Plano de Segurança do Paciente, documento que deve identificar e detalhar as estratégias e ações definidas pelo serviço de saúde para promover, proteger e mitigar riscos relacionados à assistência, abrangendo todo o ciclo do cuidado — desde a admissão do paciente até sua transferência, alta ou óbito (MINISTÉRIO DA SAÚDE, 2014).
É importante destacar que os eventos adversos representam complicações decorrentes de determinados cuidados prestados aos pacientes, sendo frequentemente associados a erros que poderiam ser evitados. Estima-se que entre 50% e 60% desses eventos são passíveis de prevenção. Em geral, não resultam em danos permanentes, no entanto, a falta de preparo dos profissionais e a condição de vulnerabilidade dos pacientes com doença renal crônica (DRC) em hemodiálise podem favorecer o surgimento de complicações graves, inclusive o óbito. Um exemplo dessa realidade é apresentado em um estudo realizado nos Estados Unidos, o qual revelou que, dentre aproximadamente um milhão de casos de eventos adversos registrados anualmente, cerca de noventa e oito mil culminam em morte. (SOUSA, 2017)
A doença renal crônica, por sua vez, apresenta elevadas taxas de morbidade e está intimamente relacionada à mortalidade, além de gerar altos custos tanto sociais quanto individuais. Isso ocorre porque os pacientes acometidos demandam maior atenção no que se refere ao autocuidado, além de dependerem do uso contínuo de equipamentos médicos, esquemas terapêuticos complexos e planos alimentares específicos (CANAUD et al., 2019).
2.4.1. Medicamentos comumente utilizados em DRC
Em suma, para o tratamento da DRC são utilizados os seguintes medicamentos, sendo divididos em agentes anti-hipertensivos/ cardiovasculares, analgésicos, antibióticos, antifúngicos, hipoglicemiantes, lipolipemiantes, quimioterápicos, anticoagulantes e meios de contraste iodado, sendo apresentados na tabela a seguir com o monitoramento da TGF:
Tabela 1- Ajustes e recomendações específicas para uso de fármacos em pacientes com doença renal crônica
| Agente terapêutico | Cuidados específicos em DRC |
| Farmácos cardiovasculares | |
| IECA/BRA, antagonistas da aldosterona, inibidores diretos da renina | Evitar em suspeita de estenose de artéria renal. Iniciar com doses reduzidas em TFG < 45 mL/min. Monitorar TFG e potássio sérico em até 1-2 semanas. Suspender temporariamente em exames contrastados e grandes cirurgias. Não suspender rotineiramente em TFG < 30 mL/min. |
| Betabloqueadores | Reduzir dose em 50% quando TFG < 30 mL/min. |
| Digoxina | Ajuste conforme níveis séricos. |
| Análgesicos | |
| AINEs | Contraindicados em TFG < 30 mL/min. Evitar uso prolongado se TFG < 60 mL/min. Não associar a lítio, IECA ou BRA. |
| Opioides | Reduzir dose se TFG < 60 mL/min; usar com cautela em TFG < 15 mL/min. |
| Antibióticos | |
| Penicilinas | Risco de cristalúria e neurotoxicidade em altas doses se TFG < 15 mL/min. |
| Aminonoglicosídeos | Reduzir dose ou ampliar intervalo se TFG < 60 mL/min; monitorar níveis séricos; evitar uso concomitante com furosemida. |
| Macrolídeos | Reduzir dose em 50% se TFG < 30 mL/min. |
| Fluoroquinolonas | Reduzir dose em 50% se TFG < 15 mL/min. |
| Tetraciclinas | Reduzir dose se TFG < 45 mL/min. |
| Antifúngicos | |
| Anfotericina | Evitar quando TFG < 60 mL/min, salvo ausência de alternativas. |
| Fluconazol | Reduzir manutenção em 50% se TFG < 50 mL/min. |
| Hipoglicemiantes | |
| Sulfonilureias | Evitar glibenclamida em TFG < 30 mL/min; reduzir glicazida em 50% se TFG < 30 mL/min. |
| Insulina | Possível necessidade de redução em TFG < 30 mL/min. |
| Metformina | Contraindicada em TFG < 30 mL/min; reavaliar uso se TFG < 45 mL/min. |
| Hipolipemiantes | |
| Estatinas | Não exigem ajuste de dose. |
| Fenofibrato | Pode elevar creatinina; cautela em TFG < 30 mL/min. |
| Quimioterápicos | |
| Cisplatina | |
| Melfalan | Reduzir dose se TFG < 60 mL/min. |
| Metotrexato | Reduzir dose se TFG < 60 mL/min; evitar se TFG < 15 mL/min. |
| Anticoagulantes | Reduzir dose em TFG < 60 mL/min; evitar em TFG < 30 mL/min. |
| Heparina de baixo peso molecular | Preferir heparina não fracionada se TFG < 30 mL/min. |
| Varfarina | Maior risco de sangramento em TFG < 30 mL/min; utilizar menores doses e monitorar. |
| Meios de contraste iodado | Pacientes com TFG < 60 mL/min devem: evitar agentes de alta osmolaridade; empregar menores doses; suspender fármacos nefrotóxicos prévios; garantir hidratação adequada antes e após; monitorar TFG após exposição. |
Fonte: Adaptada de Diretrizes clínicas para o cuidado ao paciente com doença renal crônica – DRC no sistema único de saúde. Brasília: Ministério da Saúde, 2014; KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. USA: Kidney International Supplements, 2013.
De acordo com os estágios da DRC, são utilizados os seguintes esquemas terapêuticos:
– Estágio 1 (TFG ≥ 90 mL/min/1,73 m² com lesão renal)
Objetivos terapêuticos: prevenção da progressão da doença e controle de comorbidades.
1. Anti-hipertensivos: IECA ou BRA: indicados em pacientes com albuminúria (RAC ≥ 30 mg/g) ou diabetes, mesmo com função renal preservada.
2. Antidiabéticos: Manter HbA1c ≈ 7% com uso de metformina (sem restrição nesse estágio).
3. Hipolipemiantes:
4. Uso de estatinas conforme avaliação do risco cardiovascular.
5. Imunizações: Atualizar calendário vacinal, inclusive hepatite B, para prevenir infecções futuras (KDIGO, 2024).
– Estágio 2 (TFG 60–89 mL/min/1,73 m² com evidência de lesão renal) Foco terapêutico: manter controle glicêmico, pressórico e lipídico.
1. Anti-hipertensivos: IECA ou BRA: mantidos se proteinúria ou diabetes. Alvo pressórico: < 140/90 mmHg (não diabéticos e RAC < 30) e ≤ 130/80 mmHg (diabéticos ou RAC ≥ 30)
2. Antidiabéticos: Manter HbA1c em torno de 7%; metformina ainda segura.
3. Ajustes medicamentosos: Ainda não requerem modificações específicas para TFG (KDIGO, 2024).
– Estágio 3A (TFG 45–59 mL/min/1,73 m²)
Início de intervenções com base na função renal reduzida.
1. Anti-hipertensivos: IECA/BRA: continuar se indicado; monitorar potássio e TFG após início ou titulação. Alvo pressórico permanece conforme estágio anterior.
2. Antidiabéticos:Considerar ajuste da dose de metformina com TFG < 45 mL/min.
3. Antibióticos / Antivirais: Início do ajuste de dose baseado na TFG, principalmente para aminoglicosídeos, penicilinas, antivirais e antivirais de uso prolongado.
4. Fármacos com risco de hipercalemia: Monitorar com uso concomitante de IECA/BRA.
5. Suplementações e vigilância: Monitoramento de PTH, fósforo e cálcio para avaliação de distúrbios do metabolismo mineral ósseo (KDIGO, 2024).
– Estágio 3B (TFG 30–44 mL/min/1,73 m²)
Maior necessidade de ajustes e vigilância terapêutica.
1. Anti-hipertensivos: Manter IECA/BRA com monitoramento regular de potássio e função renal.
2. Antidiabéticos: Redução ou suspensão de metformina se TFG<30 mL/min. Avaliação de insulina e outros antidiabéticos de eliminação renal.
3. Correção de doses: Reavaliação de posologia para antibióticos, antivirais, analgésicos e medicamentos renotóxicos.
4. Estatinas e fibratos: Estatinas mantidas. Cautela com fibratos (risco de elevação da creatinina).
5. Controle do metabolismo mineral: Suplementação ou modulação de vitamina D, quelantes de fósforo se necessário.
6. Anemia: Início do rastreio com avaliação de Hb, ferritina e IST (KDIGO, 2024).
– Estágio 4 (TFG 15–29 mL/min/1,73 m²)
Fase pré-terminal – intervenções farmacológicas devem ser otimizadas.
1. Anti-hipertensivos: Uso continuado de IECA/BRA com cautela. Suspender se hipercalemia refratária.
2. Antidiabéticos: Metformina contraindicada se TFG < 30 mL/min. Ajustar insulina e demais hipoglicemiantes conforme depuração renal.
3. Bicarbonato de sódio: Iniciar reposição oral se bicarbonato sérico < 22 mEq/L (acidose metabólica).
4. Correção farmacológica: Reajuste sistemático de antibióticos, antivirais e fármacos nefrotóxicos.
5. Terapia para distúrbios do metabolismo mineral: Uso de quelantes de fósforo, vitamina D ativa e ajuste de PTH com análogos de calcimiméticos conforme perfil laboratorial.
6. Tratamento da anemia:
7. Considerar eritropoetina humana recombinante, se Hb persistentemente baixa (KDIGO, 2024).
– Estágio 5-ND (TFG < 15 mL/min/1,73 m² sem diálise)
Pré-diálise: ajustes rigorosos de todas as medicações eliminadas por via renal.
1. Antidiabéticos: Suspender metformina. Avaliar insulina basal e outras opções com metabolismo não renal.
2. Bicarbonato de sódio: Mantido se acidose persistente.
3. Antibióticos e antivirais: Ajustar todos os medicamentos com eliminação renal.
4. Antihipertensivos: IECA/BRA ainda podem ser utilizados com cautela e monitoramento.
5. Suporte hematológico e mineral: Acompanhamento mais intenso de anemia, PTH, fósforo, cálcio e vitamina D.
6. Preparação para Terapia Renal Substitutiva (TRS): Medicamentos otimizados para evitar eventos adversos e facilitar transição (KDIGO, 2024).
– Estágio 5-D (pacientes em diálise – TRS)
Foco no manejo das alterações induzidas pela própria diálise.
1. Anti-hipertensivos: Ajustar em relação à pressão interdialítica. Preferência por fármacos dializáveis ou não acumulativos.
2. Controle do metabolismo mineral: Uso de quelantes de fósforo (sevelamer, carbonato de cálcio), vitamina D ativa, cinacalcete para hiperparatireoidismo secundário.
3. Antidiabéticos: Preferir insulina; ajuste conforme esquema dialítico.
4. Correção de anemia: Eritropoetina + ferro oral ou EV conforme perfil laboratorial.
5. Suplementação de vitaminas: Vitaminas hidrossolúveis (B complexos, C) frequentemente requeridas (KDIGO, 2024).
2.4.2. Fatores que aumentam o risco de interações.
As interações medicamentosas (IMs) consistem em alterações na resposta farmacológica de um fármaco em decorrência da administração prévia ou concomitante de outro agente terapêutico, podendo resultar em efeitos sinérgicos, antagônicos ou inesperados em relação ao tratamento originalmente planejado. Contudo, considerando as limitações metodológicas para confirmar sua manifestação clínica direta em estudos observacionais ou experimentais, a investigação científica frequentemente se concentra na identificação de interações medicamentosas potenciais. Essas correspondem a combinações farmacológicas cuja interação é previamente conhecida e documentada na literatura científica, com base em dados clínicos ou experimentais que apontam para a possibilidade de efeitos adversos relevantes à saúde do paciente. A detecção dessas interações permite a estimativa do risco a que determinada população está submetida, servindo como indicador importante de segurança terapêutica (FABIOLA, 2019).
As interações farmacocinéticas ocorrem quando um fármaco altera os parâmetros farmacocinéticos de outro, afetando etapas cruciais como absorção, distribuição, metabolismo (biotransformação) e excreção. Tais alterações podem modificar a biodisponibilidade e a concentração plasmática do fármaco afetado, com impactos diretos sobre sua eficácia e segurança (MORAES et al., 2022).
Um exemplo clássico desse tipo de interação envolve certos anticonvulsivantes, que atuam como indutores enzimáticos e aceleram a biotransformação de anticoncepcionais hormonais, reduzindo significativamente suas concentrações séricas e, consequentemente, sua eficácia terapêutica (DEMARTINI, 2013).
A fase de absorção refere-se ao processo pelo qual uma substância administrada alcança a circulação sistêmica. Essa etapa é influenciada por diversos fatores, como fluxo sanguíneo gastrointestinal, pH local, motilidade intestinal, composição da dieta e forma farmacêutica administrada (RANG et al., 2020).
A distribuição do fármaco consiste em seu deslocamento da circulação sistêmica para os tecidos corporais, e é modulada principalmente pelo volume de distribuição aparente (Vd) e pela fração de ligação às proteínas plasmáticas. Fármacos com elevada afinidade por proteínas plasmáticas podem competir por esses sítios de ligação quando administrados simultaneamente, deslocando outros medicamentos e aumentando a fração livre, com potencial para intensificação da atividade farmacológica ou toxicidade (RANG et al., 2020).
A excreção de fármacos e seus metabólitos ocorre predominantemente por via renal, embora outros órgãos, como o fígado (via biliar), também desempenhem papel relevante. A excreção renal abrange processos de filtração glomerular, secreção tubular ativa e reabsorção tubular. Interações significativas podem ocorrer durante a secreção ativa, como no caso dos anti-inflamatórios não esteroidais (AINEs), que inibem a eliminação renal do metotrexato, elevando seus níveis plasmáticos e favorecendo a ocorrência de efeitos tóxicos. Ademais, o pH urinário (ácido ou alcalino) exerce influência direta sobre a eliminação de fármacos ionizáveis, alterando seu perfil farmacocinético (PALLERIA et al., 2013).
As interações farmacodinâmicas envolvem modificações nos efeitos farmacológicos quando dois ou mais fármacos atuam sobre o mesmo alvo terapêutico (receptores, canais iônicos, enzimas ou transportadores), podendo potencializar (sinergismo) ou reduzir (antagonismo) a resposta terapêutica (MORAES et al., 2022).
O sinergismo ocorre quando a resposta clínica observada é superior à soma dos efeitos individuais dos fármacos. Essa interação pode ser classificada como:
– Aditiva: quando os fármacos compartilham o mesmo mecanismo de ação;
– Somatória: quando atuam por vias distintas, mas convergentes;
– Potencializadora: quando interagem com diferentes receptores ou vias, amplificando o efeito.
Por outro lado, o antagonismo corresponde à atenuação ou anulação do efeito de um fármaco pela ação de outro, frequentemente por competição pelo mesmo receptor farmacológico. As interações farmacêuticas, também denominadas incompatibilidades medicamentosas, ocorrem fora do organismo, geralmente durante a manipulação e preparo das soluções injetáveis ou administração simultânea de fármacos em um mesmo dispositivo (seringa, frasco ou equipo). Essas reações físico-químicas podem levar à formação de precipitados, alterações de coloração, produção de gases, degradação dos princípios ativos, formação de compostos tóxicos ou perda da eficácia terapêutica (CASTRO et al., 2020).
As interações medicamentosas podem ser classificadas de acordo com seu grau de gravidade clínica:
Alta gravidade: quando a interação representa risco iminente à vida, exigindo intervenção médica imediata;
Gravidade moderada: quando pode haver deterioração do quadro clínico, requerendo ajuste da farmacoterapia;
Baixa gravidade: quando os efeitos clínicos são limitados e não exigem mudanças relevantes na conduta terapêutica (CROZARA, 2017).
A ocorrência de interações medicamentosas pode ser favorecida por diversos fatores relacionados ao paciente, ao medicamento e ao processo de prescrição (CASSIANI, 2009).
– Algumas condições clínicas aumentam a vulnerabilidade às IMs, como:Alterações nos níveis de proteínas plasmáticas (hipoalbuminemia);
– Disfunções hepáticas e renais;
– Idade extrema (idosos e neonatos);
– Estado nutricional comprometido (FRANCO et al., 2007).
Pacientes hospitalizados em unidades de terapia intensiva ou submetidos a procedimentos cirúrgicos também representam grupos de risco elevado (MORAES et al., 2022).
Incluem propriedades farmacológicas específicas, como:
– Potencial de indução ou inibição enzimática (particularmente do citocromo P450);
– Margem terapêutica estreita, o que aumenta o risco de toxicidade em caso de variações mínimas de concentração (SCHLIENGER, 2003).
A complexidade do tratamento e o número de fármacos prescritos influenciam diretamente o risco de IMs. A literatura evidencia que pacientes em uso de menos de cinco medicamentos apresentam taxa de interação entre 3% e 5%. Já aqueles em uso de 10 a 20 fármacos podem alcançar taxas de 10% a 20% (MORAES et al., 2022).
A literatura aponta que a prevalência de IMPs em pacientes atendidos em serviços ambulatoriais é elevada, situando-se em torno de 50%⁵, podendo ultrapassar 80% em populações específicas. Há uma correlação direta entre o número de medicamentos prescritos e a frequência de IMPs identificadas, evidenciando que a polifarmácia atua como um fator de risco determinante para tais eventos. Este cenário é agravado pelo envelhecimento populacional, que acarreta um aumento da carga de doenças crônicas não transmissíveis e, consequentemente, a intensificação do uso concomitante de múltiplos fármacos (politerapia). Diante desse contexto, as interações medicamentosas potenciais configuram um desafio crescente para os sistemas de saúde, exigindo estratégias eficazes de monitoramento, prevenção e intervenção, especialmente em populações clinicamente vulneráveis. (FABIOLA, 2019)
Na prática clínica, é frequente a prescrição concomitante de múltiplos fármacos no manejo de doenças crônicas. Essa estratégia terapêutica, embora necessária, acarreta um aumento na probabilidade de ocorrência de interações medicamentosas (IMs), as quais podem apresentar efeitos terapêuticos sinérgicos ou aditivos desejáveis, mas também podem resultar em consequências clínicas indesejadas — variando desde a redução da eficácia terapêutica até a ocorrência de eventos adversos de alta gravidade. Conceitualmente, uma interação medicamentosa consiste na alteração da resposta farmacológica de um fármaco decorrente da administração simultânea de outro agente terapêutico (MARQUITO, 2014).
Nesse contexto, as IMs configuram-se como causas potenciais de Problemas Relacionados a Medicamentos (PRMs), cujas repercussões clínicas incluem o aumento da morbimortalidade, prolongamento do tempo de hospitalização, comprometimento da qualidade de vida do paciente e elevação dos custos diretos e indiretos em saúde (MARQUITO, 2014).
Embora a manifestação clínica de IMs nem sempre seja evidente, o conhecimento aprofundado das propriedades farmacocinéticas (absorção, distribuição, metabolismo e excreção) e farmacodinâmicas dos medicamentos envolvidos permite antecipar e avaliar o risco potencial de interações relevantes. Ressalte-se que as IMs são, em sua maioria, eventos adversos evitáveis, o que destaca a importância de estratégias eficazes de prevenção, detecção precoce e intervenção. Nesse sentido, a atuação do farmacêutico clínico, por meio da identificação, categorização e monitoramento das IMs, é fundamental para otimizar a segurança e a efetividade do tratamento farmacológico (MARQUITO, 2014).
A classificação das interações medicamentosas pode ser realizada com base em sua gravidade clínica. Interações classificadas como “maiores” ou “contraindicadas” exigem intervenção médica imediata, dado o elevado risco de desfechos graves ou potencialmente fatais. Por outro lado, interações “moderadas” e “menores” demandam atenção e acompanhamento, podendo requerer ajustes na conduta terapêutica, ainda que não envolvam risco iminente à vida (MARQUITO, 2014).
A avaliação do risco de IMs deve considerar diversos fatores predisponentes, tais como as características fisicoquímicas e farmacológicas dos medicamentos, o número de fármacos prescritos (polifarmácia), o envelhecimento populacional e a presença de comorbidades que afetam os processos de metabolização e excreção, especialmente disfunções hepáticas e renais (MARQUITO, 2014).
Particularmente, os rins exercem papel essencial na manutenção da homeostase sistêmica, desempenhando funções regulatórias, excretórias e endócrinas. Assim, a perda progressiva da taxa de filtração glomerular (TFG) e/ou da função renal, como ocorre na Doença Renal Crônica (DRC), compromete significativamente a depuração de diversas substâncias, incluindo fármacos e seus metabólitos, potencializando o risco de toxicidade medicamentosa (MARQUITO, 2014).
No contexto brasileiro, observa-se uma crescente prevalência de indivíduos em terapia renal substitutiva (TRS), cujo número aumentou de aproximadamente 42 mil pacientes em 2000 para mais de 90 mil ao final de 2010. Em 2010, a taxa de prevalência de pacientes em TRS foi estimada em 483 por milhão de habitantes, com variações regionais entre 265 na Região Norte e 591 na Região Sudeste. Dentre esses, 89,7% realizavam hemodiálise e 5,1% diálise peritoneal. Os principais diagnósticos etiológicos associados à DRC foram a hipertensão arterial sistêmica (HAS) e o diabetes mellitus (DM), em conformidade com dados de levantamentos anteriores (MARQUITO, 2014).
Diante disso, pacientes com DRC representam uma população de elevado risco para a ocorrência de IMs clinicamente significativas, uma vez que, além de apresentarem disfunção renal — que compromete a eliminação de fármacos —, são em sua maioria idosos e portadores de comorbidades como HAS e DM, o que os torna ainda mais suscetíveis aos efeitos adversos decorrentes da polifarmácia (MARQUITO, 2014).
2.4.3. Consequências clínicas das interações medicamentosas
Os indivíduos acometidos pela Doença Renal Crônica (DRC) configuram uma população particularmente vulnerável ao desenvolvimento de interações medicamentosas (IMs), em virtude da elevada prevalência de polifarmácia, das profundas alterações nos processos de absorção, distribuição, metabolismo e excreção dos fármacos, bem como da coexistência de múltiplas comorbidades que demandam regimes terapêuticos complexos (KDIGO, 2013).
Dentre as principais repercussões clínicas dessas interações, destaca-se a maior incidência de toxicidade medicamentosa, decorrente da depuração renal reduzida e do acúmulo de metabólitos ativos, os quais potencializam reações adversas. A utilização concomitante de agentes nefrotóxicos, como aminoglicosídeos e anfotericina B, em pacientes renais crônicos, exemplifica a gravidade dessa problemática, podendo precipitar injúria renal aguda sobreposta ao quadro crônico (Eckardt, 2017).
Outra consequência de magnitude clínica relevante refere-se à redução da eficácia terapêutica de fármacos essenciais, resultante de interações que comprometem sua biodisponibilidade ou concentração plasmática. Exemplo paradigmático ocorre com os quelantes de fósforo, que diminuem significativamente a absorção de antibióticos como as quinolonas, prejudicando o manejo de infecções em uma população já imunocomprometida (Bussey, 2014).
O impacto das IMs também se estende ao âmbito cardiovascular e cerebrovascular, considerando que a DRC, por si só, já se associa a um estado pró-inflamatório e prótrombótico. Interações que afetam o balanço hidroeletrolítico, como a associação de inibidores da enzima conversora da angiotensina (IECA) ou bloqueadores do receptor de angiotensina II (BRA) com antagonistas da aldosterona, elevam sobremaneira o risco de hipercalemia grave, predispondo a arritmias letais e eventos isquêmicos (Tesfaye et al., 2017).
Ademais, é notória a contribuição das IMs para a ocorrência de desequilíbrios hidroeletrolíticos, frequentes em pacientes com função renal comprometida. O uso concomitante de diuréticos poupadores de potássio, suplementação desse íon e drogas que interferem no sistema renina-angiotensina-aldosterona intensifica o risco de complicações metabólicas potencialmente fatais (Soares, 2020).
A repercussão clínica das interações em pacientes renais transcende a esfera fisiopatológica, refletindo-se no aumento das taxas de hospitalizações por eventos adversos a medicamentos (EAMs). Tal cenário decorre não apenas das complicações cardiovasculares e metabólicas, mas também da falência terapêutica em quadros infecciosos, o que contribui para maior morbimortalidade e onerosidade dos sistemas de saúde (Bussey, 2014).
Por fim, a complexidade dos esquemas terapêuticos frequentemente ajustados em função de interações medicamentosas culmina em prejuízo à adesão ao tratamento, agravando o risco de progressão da doença renal crônica e de suas comorbidades, notadamente hipertensão arterial sistêmica e diabetes mellitus. Esse fenômeno reforça a importância do acompanhamento farmacoterapêutico individualizado, conduzido por farmacêuticos clínicos em equipe multidisciplinar (Tesfaye et al., 2017).
2.5. ATUAÇÃO DO FARMACÊUTICO CLÍNICO
Alguns Problemas Relacionados a Medicamentos (PRM) — especialmente aqueles ligados à indicação, efetividade, segurança e adesão terapêutica — podem ter consequências significativas nos âmbitos clínico, humanístico e econômico. Esses problemas não apenas impactam negativamente a qualidade do cuidado em saúde, como também estão entre as principais causas de eventos adversos, contribuindo para o aumento do tempo de internação, elevação das taxas de morbidade e mortalidade, além de gerar custos hospitalares adicionais (SOUZA, Hugo et al, 2021).
Essa realidade está diretamente relacionada à complexidade do processo de uso de medicamentos, que compreende três etapas críticas: prescrição, dispensação e administração. Cada uma dessas fases apresenta riscos potenciais que, se não forem adequadamente monitorados, podem comprometer a segurança do paciente (SOUZA, Hugo et al, 2021).
Nesse cenário, destaca-se o papel essencial do Farmacêutico Clínico (FC), cuja atuação é voltada para a prevenção e mitigação de danos associados ao uso inadequado de medicamentos. Sua intervenção é especialmente relevante na identificação e correção de erros de prescrição, como ilegibilidade, uso de nomes incorretos, dosagens inadequadas ou ausentes, além da escolha errônea da forma farmacêutica — situações frequentes no ambiente hospitalar e que demandam atenção especializada para garantir a segurança terapêutica e a efetividade do tratamento (SOUZA, Hugo et al, 2021).
Diante desse contexto, o farmacêutico tem ganhado reconhecimento como um profissional essencial nos serviços de saúde, especialmente quando integrado de forma ativa à equipe multidisciplinar de cuidados e aos processos relacionados ao uso de medicamentos. Sua atuação colaborativa contribui significativamente para a qualidade do atendimento ao paciente, permitindo o acompanhamento sistemático da farmacoterapia (SANTOS, 2021).
Ao participar do monitoramento do processo medicamentoso, o farmacêutico desempenha um papel fundamental na prevenção de erros relacionados à prescrição, dispensação e administração de fármacos, promovendo, assim, uma terapia medicamentosa mais segura, eficaz e individualizada (SANTOS, 2021).
2.5.1. Conceito de farmácia clínica
No cenário brasileiro, problemas relacionados ao uso inadequado de medicamentos — como erros na indicação, inefetividade terapêutica, riscos de reações adversas, baixa adesão ao tratamento e uso irracional — são causas relevantes de morbimortalidade. Tais questões geram impacto expressivo nos âmbitos clínico, econômico, social e humanístico, afetando diretamente a qualidade de vida dos pacientes e onerando o Sistema Único de Saúde (SUS) (RIBEIRO et al., 2022).
A Farmácia Clínica surge nesse contexto como um campo essencial da prática farmacêutica voltado ao cuidado individualizado. Seu principal objetivo é otimizar a farmacoterapia por meio do uso seguro e racional de medicamentos, assegurando melhores desfechos clínicos e promovendo a saúde e o bem-estar dos pacientes. O farmacêutico clínico atua de forma integrada à equipe multiprofissional, sendo responsável por monitorar o uso de medicamentos, prevenir interações e eventos adversos, além de orientar os pacientes sobre o uso correto da terapia medicamentosa (RAMOS et al., 2018).
Entre as atividades do farmacêutico clínico, destacam-se: o cuidado centrado no paciente, o acompanhamento terapêutico contínuo, a intervenção para resolver problemas relacionados à farmacoterapia, a educação em saúde e a prevenção de doenças associadas ao uso de medicamentos. Essas práticas exigem habilidades técnicas e interpessoais, e visam garantir que o paciente receba o medicamento certo, na dose adequada e com acompanhamento regular de sua efetividade e segurança (DOS SANTOS JUNIOR, 2018).
Os Serviços de Farmácia Clínica (SFC) são iniciativas estruturadas dentro da Política Nacional de Assistência Farmacêutica (PNAF), regulamentadas por resoluções do Conselho Federal de Farmácia, e vêm sendo implementadas em diversas unidades do SUS e da atenção básica. Atualmente, mais de 2.500 farmacêuticos desenvolvem atividades clínicas no sistema público, desempenhando um papel ativo no cuidado integrado à saúde da população (RAMOS et al., 2018).
As intervenções clínicas farmacêuticas têm se mostrado eficazes na redução de erros de medicação, no controle de doenças crônicas, na melhora da adesão terapêutica e na diminuição dos custos associados à assistência. Além disso, essas ações contribuem diretamente para um modelo de cuidado mais resolutivo, indo além da função tradicional de dispensação de medicamentos (MIRANDA et al., 2012).
Apesar dos avanços e da expansão dos SFCs nos últimos anos, ainda existem desafios importantes para sua plena implementação, como a necessidade de capacitação clínica dos profissionais, mudanças no modelo de formação e superação de barreiras estruturais e administrativas. A consolidação do farmacêutico clínico como agente de cuidado exige uma formação generalista, humanística e voltada à prática clínica interdisciplinar (RIBEIRO et al., 2022).
A resolução do CFF 585/2013 surge diante da evolução do papel do farmacêutico, principalmente pela transição epidemiológica e o aumento das doenças crônicas, exigindo maior participação deste profissional na atenção direta ao paciente.
– A resolução distingue os conceitos:
– Atribuições: responsabilidades e competências do farmacêutico;
– Atividades: ações práticas no processo de trabalho;
– Serviços: conjunto de atividades percebidas por pacientes ou instituições.
– O farmacêutico, com autonomia e base ética, passa a:
– Estabelecer relação de cuidado centrada no paciente;
– Realizar anamnese farmacêutica, avaliação da prescrição e da farmacoterapia;
– Emitir parecer farmacêutico e realizar intervenções clínicas;
– Solicitar e interpretar exames laboratoriais, monitorar parâmetros clínicos;
– Elaborar planos de cuidado farmacêutico e promover o uso racional de medicamentos
– Prescrever medicamentos (conforme legislação específica);
– Promover o autocuidado e realizar ações de educação em saúde.
– Educação em saúde de pacientes, familiares e cuidadores;
– Participação em programas de educação continuada e treinamentos;
– Gestão da prática clínica, com avaliação de indicadores de qualidade, elaboração de protocolos, participação em comissões e estudos.
A resolução marca a consolidação da Farmácia Clínica no Brasil, reconhecendo o farmacêutico como profissional de saúde essencial no acompanhamento terapêutico, prevenção de doenças e na promoção da saúde.
2.5.2. Histórico e regulamentação no Brasil
A Farmácia Clínica teve origem nos Estados Unidos na década de 1960, quando surgiu a necessidade de um novo modelo de prática farmacêutica voltado ao cuidado direto do paciente. O farmacêutico passou a exercer um papel mais ativo na detecção, prevenção e resolução de problemas relacionados à farmacoterapia, contribuindo para melhores resultados na saúde. No Brasil, essa abordagem foi incorporada gradualmente, sobretudo a partir das mudanças no sistema de saúde e das necessidades crescentes de pacientes com doenças crônicas e uso contínuo de medicamentos (RDC CFF 585/2013).
Com a publicação da Resolução CNE/CES nº 2/2002, as Diretrizes Curriculares Nacionais dos cursos de Farmácia foram reformuladas. O novo perfil do farmacêutico foi estabelecido como generalista, humanista e voltado para a atenção à saúde da população. A formação deixou de focar apenas na área tecnológica e industrial, priorizando a promoção, proteção e recuperação da saúde, além da prevenção de doenças, sempre com base em princípios éticos e científicos (RDC CFF 585/2013).
Um marco importante na regulamentação da Farmácia Clínica no Brasil foi a Resolução CFF nº 357/2001, que trata das boas práticas em farmácias e drogarias. Essa resolução introduziu oficialmente os conceitos de atenção farmacêutica, que já vinham sendo discutidos no país desde a década de 1990, e incentivou a atuação do farmacêutico no acompanhamento farmacoterapêutico do paciente (RDC CFF 357/2001).
O avanço mais expressivo ocorreu em 2013 com a publicação da Resolução CFF nº 585/2013, que regulamentou as atribuições clínicas do farmacêutico. Essa norma reconhece o farmacêutico como um profissional da saúde capaz de realizar atendimento clínico, fazer anamnese, acompanhar tratamentos, identificar reações adversas, promover o uso racional de medicamentos e colaborar com outros profissionais da saúde em benefício do paciente (Normas Legais, 2013).
Ainda em 2013, foi publicada a Resolução CFF nº 586/2013, que regulamenta a prescrição farmacêutica. Essa resolução define os critérios para que o farmacêutico possa prescrever medicamentos isentos de prescrição médica (MIPs) e outros produtos para a saúde, além de permitir prescrições dentro de protocolos estabelecidos em serviços de saúde, mediante capacitação e respaldo legal (Nexxto, 2023).
O crescimento da prática clínica exigiu mudanças também na formação dos farmacêuticos. As instituições de ensino superior passaram a incluir no currículo disciplinas como semiologia, farmacoterapia, clínica farmacêutica, atenção farmacêutica e saúde baseada em evidências. Além disso, metodologias ativas de ensino, como simulações clínicas e estudo de casos, passaram a fazer parte da formação para preparar o farmacêutico para o atendimento direto ao paciente (ICTQ, 2024).
A Lei nº 13.021/2014 consolidou a farmácia como um estabelecimento de saúde e formalizou o papel clínico do farmacêutico. Essa lei reconheceu a farmácia como parte integrante da rede de atenção à saúde e ampliou o escopo de atuação do farmacêutico para incluir serviços como consulta farmacêutica, acompanhamento de pacientes e prescrição dentro dos limites legais e técnicos estabelecidos (CRF-PR, 2014).
Atualmente, a Farmácia Clínica é uma realidade consolidada no Brasil, com mais de 94 mil farmácias comunitárias atuando como porta de entrada para o sistema de saúde. Apenas no primeiro semestre de 2024, foram realizados mais de 7,3 milhões de atendimentos farmacêuticos, incluindo mais de 389 mil prescrições farmacêuticas, um aumento de 500% em relação ao mesmo período do ano anterior, demonstrando o impacto da regulamentação e da prática clínica no país (CRF-PI, 2024).
2.5.3. Intervenções farmacêuticas: revisão de prescrições, conciliação medicamentosa, educação em saúde, entre outros
A intervenção farmacêutica tem como finalidade prevenir ou resolver resultados negativos associados ao uso de medicamentos. Estudos científicos evidenciam que os cuidados farmacêuticos contribuem para a melhoria de desfechos clínicos e econômicos. As intervenções farmacêuticas foram categorizadas com base nas diretrizes estabelecidas pelo Serviço de Farmácia Clínica da instituição, conforme a seguir :
Intervenções Relacionadas ao Medicamento: Envolvem ações diretamente vinculadas à identificação de Problemas Relacionados a Medicamentos (PRM). Exemplos incluem: incompatibilidade na administração por conexão em Y, inadequações no tempo ou velocidade de infusão, interações medicamentosas, necessidade de monitoramento de fármacos, uso de medicamentos não padronizados, indicação de terapia não atendida, posologia inadequada, entre outros (ARAUJO E.,2017).
Intervenções Não Relacionadas ao Medicamento: Referem-se a questões associadas ao processo de prescrição, dispensação e ao cumprimento de normas institucionais e legais. Entre elas, destacam-se: ausência de identificação de precauções de contato no leito, uso incorreto de receituário para medicamentos psicotrópicos ou entorpecentes, justificativas vencidas para medicamentos de uso restrito, e falhas na prescrição, como letra ilegível, informações incompletas ou presença de rasuras (ARAUJO E.,2017).
A revisão minuciosa das prescrições médicas realizada por farmacêuticos, com o apoio de sistemas informatizados, tem sido uma estratégia recomendada para a redução de erros de prescrição. Por meio dessa análise detalhada, o farmacêutico contribui diretamente para a segurança do paciente e para o uso racional da farmacoterapia. As intervenções farmacêuticas efetuadas durante a validação das prescrições demonstram impacto positivo na diminuição da mortalidade, dos custos hospitalares e do tempo de internação.
Cabe ao farmacêutico avaliar as prescrições quanto a componentes, dosagens, qualidade, compatibilidade, interações, possíveis reações adversas, estabilidade dos medicamentos, entre outros aspectos relevantes. Embora o impacto positivo das intervenções farmacêuticas na promoção do uso racional de medicamentos esteja amplamente documentado na literatura, ainda são escassos os relatos sobre a prática em hospitais brasileiros.
A validação da prescrição médica funciona como uma barreira de segurança, pois a dispensação dos medicamentos só ocorre após a aprovação do farmacêutico clínico. Assim, as intervenções realizadas nesse momento têm caráter preventivo, buscando identificar e corrigir possíveis erros antes que causem danos aos pacientes.
Para que essa atividade seja desempenhada de forma eficaz, é essencial que o farmacêutico possua conhecimentos em clínica farmacêutica e esteja integrado à equipe multidisciplinar. Além disso, o funcionamento adequado do serviço de validação requer planejamento detalhado das atividades, ambiente exclusivo para a atividade, acesso a bases científicas atualizadas, além de recursos humanos e tecnológicos adequados.
A Reconciliação Medicamentosa (RM), é um processo fundamentado em evidências que envolve a obtenção da lista completa dos medicamentos utilizados pelo paciente e sua comparação com a prescrição médica atualizada. Essa comparação ocorre nas diferentes transições de cuidado, considerando os motivos que justificam a suspensão, adição ou substituição de medicamentos (DINIZ ACAM, 2025).
A RM é uma responsabilidade compartilhada entre os membros da equipe multiprofissional, que deve atuar em parceria com o paciente e sua família. Essa colaboração visa garantir a obtenção de informações completas sobre os medicamentos durante as transições assistenciais. A partir disso, é possível identificar possíveis erros ou discrepâncias, como troca, omissão ou duplicação de fármacos; divergências na dose, via ou frequência de administração; falta de adesão ao tratamento; além de reações adversas, alergias ou interações medicamentosas (DINIZ ACAM, 2025).
A evolução do conceito de segurança do paciente tem contribuído para a maior conscientização sobre os riscos relacionados à assistência à saúde. O aprofundamento do conhecimento epidemiológico — incluindo a frequência, causas, tipos e impactos dos eventos adversos — permite identificar áreas críticas de atuação. Um estudo epidemiológico realizado em Portugal apontou uma taxa de 12,5% de incidência de eventos adversos no ambiente hospitalar, sendo 9,8% desses relacionados a erros com medicamentos (DINIZ ACAM, 2025).
A Educação em Saúde configura-se como uma estratégia essencial para a promoção da saúde e a conquista da cidadania, ao buscar incentivar mudanças de comportamento individual. Seu propósito é tornar os indivíduos mais conscientes sobre os fatores que contribuem para a manutenção da saúde e a prevenção de doenças, possibilitando a desconstrução de concepções equivocadas que ainda persistem entre a população. Nesse contexto, ela atua não apenas como um processo de informação, mas como uma ferramenta de transformação social e pessoal. (PAIM et al., 2010).
Mais do que transmitir informações relacionadas a prescrições ou condutas isoladas, a Educação em Saúde propõe a construção de processos contínuos de aprendizagem que favoreçam a mudança de atitudes e comportamentos. Educar em saúde, portanto, exige mais do que difundir conhecimentos técnicos: implica envolver os sujeitos em ações que promovam reflexão, senso crítico e autonomia frente às decisões sobre sua saúde. (PINTO; CASTRO; REIS, 2013).
O objetivo maior desse processo é a promoção da equidade em saúde, com a redução das desigualdades por meio do acesso equitativo a oportunidades, recursos e informações. Dessa forma, busca-se o empoderamento das comunidades, promovendo o acesso ao conhecimento e à vivência de práticas que estimulem o autocuidado e a adoção de estilos de vida saudáveis. (FREIRE et al., 2013).
A atuação do farmacêutico no Núcleo Ampliado de Saúde da Família (NASF) por meio de ações educativas contribui significativamente para a promoção do pensamento crítico e reflexivo entre os usuários. O conhecimento científico compartilhado nesse contexto é ressignificado e incorporado às práticas cotidianas de cuidado em saúde, promovendo maior autonomia e responsabilidade no cuidado individual e coletivo. Ao considerar as realidades geográficas, sociais, políticas e culturais do indivíduo, da família e da comunidade, o farmacêutico contribui para o empoderamento do usuário, estimulando o desenvolvimento do senso crítico e a capacidade de agir em favor de si, de sua família e da coletividade, com foco na educação para o autocuidado (FREIRE et al., 2013).
Para que a Educação em Saúde seja efetiva, é fundamental partir das crenças, percepções e atitudes do usuário em relação à sua condição de saúde, ao uso de medicamentos e ao tratamento. O processo educativo deve ir além da simples transmissão de orientações voltadas à prevenção de doenças e promoção da saúde. É necessário construir uma prática educativa dialógica, que valorize a escuta, o questionamento, a reflexão e a construção compartilhada do conhecimento, promovendo assim uma transformação genuína na forma como os sujeitos se relacionam com sua saúde e seu tratamento (FREIRE et al., 2013).
Além das intervenções farmacêuticas supracitadas, destacam-se: acompanhamento farmacoterapêutico (seguimento farmacêutico), detecção e resolução de problemas relacionados a medicamentos , recomendações terapêuticas ao prescritor, participação em visitas multiprofissionais (rounds clínicos), farmacovigilância e notificação de eventos adversos, implementação e gestão de protocolos clínicos e diretrizes terapêuticas, intervenções voltadas à adesão ao tratamento, orientação individualizada no uso de dispositivos e formas farmacêuticas, avaliação e prevenção de erros de medicação e por fim,o principal foco do presente trabalho: ajuste de doses conforme função renal ou hepática (recomendação de ajuste posológico para pacientes com insuficiência renal, hepática ou em extremos de idade e prevenção de toxicidades ou falha terapêutica por doses inadequadas.
2.5.4. Benefícios da presença do farmacêutico na equipe multiprofissional
Em 1989, foi criado o Departamento de Farmácia Clínica e Farmacologia na Society of Critical Care Medicine, a maior organização internacional voltada para cuidados críticos. Essa iniciativa reconheceu o farmacêutico como membro essencial da equipe multidisciplinar dedicada ao cuidado do paciente crítico, considerando a complexidade desses pacientes quanto ao número de medicamentos utilizados, regimes farmacoterápicos diferenciados, alterações farmacocinéticas e os custos associados a esses tratamentos (SCCM, 1989).
Posteriormente, em 2000, o departamento supreacitado em parceria com o American College of Clinical Pharmacy. estabeleceu os pré-requisitos para as atividades farmacêuticas no contexto do cuidado crítico. Essas atividades foram classificadas como fundamentais, desejáveis ou de excelência, conforme o nível de especialização e complexidade da atenção prestada, reforçando a importância da atuação qualificada do farmacêutico nesse cenário (SCCM e ACCP, 2000).
No Brasil, em 2008, foi criado o Departamento de Farmácia da Associação de Medicina Intensiva Brasileira (AMIB), com o propósito de promover educação continuada e fortalecer o exercício da farmácia clínica nas Unidades de Terapia Intensiva (UTIs). Essa ação reforça o reconhecimento da relevância da participação do farmacêutico no cuidado intensivo, contribuindo para a melhoria da assistência ao paciente crítico (AMIB, 2008).
Diante da complexidade envolvida no manejo da farmacoterapia em pacientes idosos, o farmacêutico vem sendo cada vez mais integrado às equipes multiprofissionais de atenção à saúde dessa população, devido à sua expertise em medicamentos. O envolvimento do farmacêutico no cuidado geriátrico, especialmente em contextos hospitalares, tem contribuído para a melhoria na qualidade do uso de medicamentos tanto durante a internação quanto no período pós-alta, com redução de riscos e aprimoramento dos desfechos terapêuticos (CASTRO et al., 2013).
Uma revisão sistemática realizada nos Estados Unidos demonstrou impactos positivos da atuação do farmacêutico no cuidado direto ao paciente, com benefícios nos aspectos terapêuticos, humanísticos e de segurança medicamentosa. No entanto, no Brasil, ainda são limitados os estudos que abordam a participação do farmacêutico na gestão da farmacoterapia de pacientes idosos, particularmente em ambientes hospitalares (CASTRO et al., 2013).
A elevada frequência de intervenções realizadas diretamente pelo farmacêutico, tanto junto ao paciente quanto de forma articulada com a equipe multiprofissional, evidenciada no presente estudo, reforça a importância da inserção desse profissional no cuidado hospitalar de idosos. Embora a literatura traga diversas abordagens sobre a atuação do farmacêutico junto a idosos em instituições de longa permanência e na comunidade, os estudos que investigam sua participação em equipes multiprofissionais voltadas ao cuidado do idoso hospitalizado ainda são escassos até o momento (CASTRO et al., 2013).
As ações do farmacêutico têm potencial para reduzir falhas relacionadas ao uso de medicamentos, otimizar os desfechos clínicos dos pacientes e ainda diminuir os gastos com a terapêutica. Assim, sua participação em equipes multiprofissionais de saúde favorece o uso racional e adequado dos fármacos, além de contribuir para a redução de complicações e mortalidade associadas. Nesse contexto, cabe ao farmacêutico, em conjunto com os demais profissionais, garantir que a farmacoterapia seja conduzida de forma segura, eficaz e apropriada (OLIVEIRA, 2012).
2.6. ESTUDOS SOBRE O IMPACTO DO FARMACÊUTICO NA PREVENÇÃO DE INTERAÇÕES
2.6.1. Revisão de evidências científicas
A atuação do farmacêutico tem se mostrado essencial na prevenção de interações medicamentosas em pacientes com Doença Renal Crônica (DRC), principalmente devido à complexidade do regime terapêutico e à presença de comorbidades. Um estudo de Alam et al. (2024) demonstrou que, após a intervenção farmacêutica, a taxa de interações medicamentosas caiu de 45,1% para 20,5% (p = 0,032), além de melhorias na adesão ao tratamento e redução de problemas como indicações não tratadas (de 37% para 7,3%) (Alam et al., 2024).
Outro estudo prospectivo realizado na Turquia avaliou o impacto da inclusão de farmacêuticos clínicos em equipes multidisciplinares para o cuidado de pacientes com DRC. Os farmacêuticos identificaram e resolveram problemas relacionados a medicamentos (PRMs), contribuindo para a otimização do tratamento e segurança do paciente (Aytac et al., 2023).
Em um hospital na Espanha, pacientes com DRC internados e expostos a medicamentos nefrotóxicos foram acompanhados diariamente por farmacêuticos. A intervenção resultou em uma melhora significativa na função renal (clearance de creatinina), com maior impacto em pacientes nos estágios 4 e 5 da DRC. As recomendações farmacêuticas foram aceitas em 74% dos casos, demonstrando a relevância da colaboração entre farmacêuticos e médicos (Cañamares-Orbis et al., 2014).
Uma revisão sistemática publicada em 2011 analisou 37 estudos e encontrou 2.683 problemas relacionados a medicamentos em 1.209 pacientes com DRC. Os farmacêuticos atuaram com sucesso na resolução desses problemas, resultando em benefícios como redução de hospitalizações, menor tempo de internação e melhora em parâmetros clínicos como pressão arterial, anemia, lipídios, cálcio e fósforo (Manley et al., 2011).
Uma meta-análise mais recente, publicada em 2024, reuniu dados de 32 ensaios clínicos randomizados. Os resultados mostraram melhoras significativas em pressão arterial sistólica e níveis de hemoglobina. No entanto, os efeitos sobre creatinina, eGFR e colesterol LDL foram inconsistentes. Apesar disso, houve melhora clara nos desfechos humanísticos, como conhecimento e satisfação dos pacientes (Zhao et al., 2024).
Além disso, uma revisão de escopo publicada pela revista Pharmacy em 2022 destacou que estratégias como reconciliação medicamentosa, educação em saúde e acompanhamento contínuo realizadas por farmacêuticos aumentam significativamente a adesão ao tratamento entre pacientes renais. O estudo ressaltou ainda a aceitação positiva das intervenções pelos pacientes e pela equipe de saúde, embora barreiras como escassez de tempo e recursos humanos ainda limitem sua implementação mais ampla (Chilcot et al., 2022).
2.6.2. Exemplos de estudos realizados em hospitais, ambulatórios ou clínicas de diálise
Estudo Observacional Prospectivo: Farmácias comunitárias na França com comunicação com médicos generalistas (GPs). Comunidade farmacêutica treinada identificou problemas relacionados a medicamentos (PRM) em pacientes com DRC. Dentre 260 prescrições, 21,5 % apresentavam PRMs, e 40 % desses foram identificados pelos farmacêuticos. Após comunicação ao médico, 33,3 % dos casos foram corrigidos.
Ensaio Clínico Randomizado no Sri Lanka (Pré-diálise): Ambulatório pré-diálise em hospital terciário. Pacientes com DRC (estágios 4- 5) participaram de intervenção com farmacêutico clínico em agendamentos periódicos ao longo de 12 meses, incluindo reconciliação medicamentosa, aconselhamento, educação em saúde, e rótulos personalizados. Foram observadas melhorias na adesão terapêutica e na qualidade de vida.
Estudo Brasileiro – Perfil Farmacoterapêutico na Hemodiálise: Clínica/hospital de referência em hemodiálise (CE, Brasil). Estudo transversal que analisou prontuários de 161 pacientes em hemodiálise no Ceará (2020), detalhando o perfil farmacoterapêutico. Os antihipertensivos foram os mais prescritos, e 50,94 % dos pacientes usavam entre 6 a 10 fármacos concomitantes, destacando a necessidade de atenção farmacêutica.
Ensaio Clínico Randomizado nos EUA – Intervenção Farmacêutico-Médico: Atenção primária com base telefônica (veteranos). Intervenção farmacêutico- médico, utilizando registro de pacientes e educação via telefone, melhorou a adesão às diretrizes (KDOQI), mas não alterou a pressão arterial. Pacientes receberam mais medicamentos antihipertensivos; sugere-se que o modelo é viável e pode melhorar processos de cuidado, embora não tenha afetado desfechos clínicos em curto prazo.
3 METODOLOGIA
Este trabalho caracteriza-se como uma pesquisa bibliográfica, exploratória e descritiva, baseada em literatura científica e documentos oficiais relacionados à Doença Renal Crônica (DRC). O objetivo foi reunir, analisar e discutir evidências recentes acerca do diagnóstico, tratamento, prognóstico, epidemiologia e aspectos de segurança do paciente com DRC, de forma a evidenciar a importância do farmacêutico clínico no manejo das interações medicamentosas associadas ao tratamento,
Critérios de inclusão: artigos científicos publicados em periódicos indexados, diretrizes nacionais e internacionais, documentos oficiais de órgãos de saúde e revisões sistemáticas relacionadas à DRC, publicados entre 2010 e 2025, em português e inglês. Critérios de exclusão: trabalhos duplicados, estudos sem revisão por pares, fontes secundárias não oficiais (blogs, sites de notícias, materiais sem referência científica).
A busca foi realizada em bases de dados eletrônicas como SciELO, PubMed, LILACS e Google Scholar, além de documentos oficiais disponibilizados pelo Ministério da Saúde, Sociedade Brasileira de Nefrologia (SBN), Agência Nacional de Vigilância Sanitária (ANVISA) e outras instituições correlatas.
Foram selecionadas publicações que abordam os seguintes eixos temáticos:
– Diretrizes de diagnóstico e tratamento da DRC (SBN, Ministério da Saúde, NKF).
– Epidemiologia e dados nacionais (Boletim Epidemiológico, Censo SBN).
– Métodos diagnósticos e avaliação da taxa de filtração glomerular (TFG) (consensos da SBN e artigos de atualização).
– Tratamentos disponíveis, incluindo diálise e transplante renal (revisões sistemáticas e estudos brasileiros).
– Segurança do paciente em hemodiálise e atenção primária à saúde (documentos oficiais da ANVISA e literatura científica).
– Qualidade de vida dos pacientes renais (estudos nacionais e internacionais).
Após a coleta, as informações foram organizadas em categorias temáticas, de modo a permitir a comparação crítica dos achados, enfatizando diretrizes atuais, lacunas de conhecimento e desafios para a prática clínica e políticas públicas de saúde.
4 RESULTADOS E DISCUSSÕES
Diversos estudos indicam que pacientes com Doença Renal Crônica (DRC), sobretudo em estágios mais avançados, apresentam uma alta frequência de interações medicamentosas (IM). Esse cenário é agravado pela polifarmácia e pelas alterações farmacocinéticas associadas à insuficiência renal. Em uma análise transversal envolvendo 558 prescrições, identificou-se que 74,9% continham potenciais IM, das quais 16,8% foram classificadas como graves, 76,9% moderadas e 5,9% leves, evidenciando um risco expressivo para eventos adversos relacionados ao tratamento medicamentoso (BVS Pesquisa, 2022).
Em outro levantamento multicêntrico com 580 pacientes em lista para transplante renal, a ocorrência de IM foi de 42,9%, com 3,37% consideradas de alta gravidade e 10,48% de gravidade moderada. Esses dados reforçam a importância do monitoramento rigoroso da terapia medicamentosa nesses pacientes, que se encontram em situação clínica delicada (BVS Pesquisa,2022).
A presença do farmacêutico na equipe de saúde é fundamental para a detecção precoce, acompanhamento e manejo das IM em pacientes com DRC, promovendo maior segurança e eficácia terapêutica. Em estudo realizado com 65 pacientes submetidos à hemodiálise, o acompanhamento farmacoterapêutico permitiu a identificação de IM, sendo 49,1% moderadas e 8,0% graves, possibilitando intervenções que contribuíram para a mitigação dos riscos associados (BVS Pesquisa, 2022).
Outra investigação, ainda que com amostra reduzida de cinco pacientes, relatou a ocorrência de 12 interações medicamentosas, das quais 50% foram classificadas como graves, 41,67% moderadas e 8,33% leves, sublinhando a relevância do monitoramento farmacêutico contínuo para prevenir complicações clínicas (BVS Pesquisa,2022).
A gravidade das interações medicamentosas varia conforme as características clínicas e o regime terapêutico dos pacientes. Em um grupo submetido a tratamento conservador para DRC, 16,8% das IM foram categorizadas como graves, 76,9% moderadas e 5,9% leves, indicando que a maior parte das interações apresenta potencial impacto clínico significativo (Repositório UFJF, UNIFAL-MG). Em contrapartida, pacientes pré-transplante renal apresentaram menor proporção de IM graves (3,37%) e moderadas (10,48%), mas ainda assim essas interações demandam atenção (BVS Pesquisa,2022).
Embora não haja dados específicos comparando diretamente os períodos antes e depois da intervenção farmacêutica, a literatura sugere que o acompanhamento sistemático por farmacêuticos reduz a incidência de IM, melhora a adesão ao tratamento, diminui eventos adversos e otimiza o manejo medicamentoso, destacando a importância da integração do farmacêutico na equipe multidisciplinar responsável pelo cuidado de pacientes com DRC (BVS Pesquisa,2022).
Os dados analisados neste estudo demonstram a elevada prevalência de interações medicamentosas (IM) em pacientes com Doença Renal Crônica (DRC), com destaque para os estágios mais avançados da doença, em que a polifarmácia é mais comum e as alterações fisiológicas comprometem a farmacocinética e a farmacodinâmica dos medicamentos. A presença de IM em mais de 70% das prescrições avaliadas, sendo boa parte delas de gravidade moderada ou grave, indica um risco significativo de eventos adversos que podem comprometer a eficácia terapêutica e a segurança do paciente.
O acompanhamento farmacoterapêutico, conforme apontado em diversos estudos, permitiu a identificação e a intervenção precoce nesses casos, reduzindo potenciais complicações clínicas. O envolvimento direto do farmacêutico, por meio da revisão sistemática de prescrições, da avaliação de duplicidade terapêutica e da identificação de interações clinicamente relevantes, contribuiu para a racionalização do tratamento e maior segurança assistencial. Este cenário evidencia a necessidade de se institucionalizar a atuação permanente do farmacêutico em todos os níveis de atenção ao paciente renal.
A literatura atual respalda os achados observados nesta análise. Diretrizes clínicas como as da KDIGO (2024) e da Sociedade Brasileira de Nefrologia reforçam o papel central da equipe multidisciplinar, com ênfase na atuação do farmacêutico no manejo da DRC, sobretudo em ambientes hospitalares e serviços especializados como centros de diálise.
Estudos conduzidos em diferentes contextos, tanto nacionais quanto internacionais, apontam para uma tendência consistente: a presença do farmacêutico clínico reduz a ocorrência de erros de medicação, melhora a adesão ao tratamento e contribui para o alcance das metas terapêuticas (PINTO et al., 2013; MANSUR et al., 2019).
Além disso, revisões sistemáticas apontam que a inclusão do farmacêutico em equipes de atenção primária e especializada em nefrologia impacta diretamente na redução de hospitalizações relacionadas a eventos adversos evitáveis. Tais evidências corroboram a eficácia da atuação farmacêutica na prevenção de complicações relacionadas à polifarmácia, uma realidade inerente ao tratamento da DRC, que frequentemente envolve o uso simultâneo de antipertensivos, quelantes de fósforo, eritropoetina, anticoagulantes, imunossupressores e outros fármacos com estreito índice terapêutico.
Apesar da relevância dos dados encontrados, este estudo apresenta algumas limitações. Por se tratar de uma pesquisa de natureza bibliográfica, não foi possível realizar medições quantitativas primárias nem avaliar de forma direta a efetividade das intervenções farmacêuticas ao longo do tempo em populações específicas.
Além disso, embora a literatura consultada inclua revisões sistemáticas e estudos observacionais, parte significativa dos dados nacionais ainda é limitada em termos de robustez metodológica ou apresenta amostras reduzidas, o que pode impactar na generalização dos achados. A ausência de ensaios clínicos randomizados no contexto brasileiro que avaliem o impacto da atuação farmacêutica na nefrologia também se configura como uma lacuna importante a ser superada.
Os resultados reforçam a necessidade de consolidar a presença do farmacêutico como um profissional essencial nas equipes de atenção ao paciente renal. A prática clínica em nefrologia exige um alto nível de especialização, considerando os ajustes de dose conforme a função renal, a complexidade das terapias utilizadas e a necessidade de conciliar múltiplos medicamentos em um único plano terapêutico viável e seguro.
Nesse sentido, a presença do farmacêutico clínico pode reduzir significativamente a incidência de eventos adversos, melhorar a qualidade de vida dos pacientes, racionalizar o uso de recursos e fortalecer a segurança do tratamento. Além disso, o farmacêutico desempenha um papel importante na educação em saúde, promovendo o entendimento do paciente sobre sua condição e tratamento, o que aumenta a adesão terapêutica e o autocuidado.
Sua atuação também é fundamental em programas de gerenciamento da farmacoterapia, revisão de protocolos institucionais e qualificação de profissionais da saúde, garantindo que as boas práticas em uso de medicamentos sejam incorporadas no cotidiano dos serviços nefrológicos.
Este estudo contribui para o fortalecimento da argumentação em favor da atuação qualificada do farmacêutico na atenção ao paciente com DRC. Ao sistematizar e comparar evidências sobre a incidência de IM e os impactos das intervenções farmacêuticas, ressalta-se a urgência de políticas públicas e institucionais que incentivem a integração deste profissional nas equipes de saúde, tanto na atenção primária quanto em serviços especializados.
Além disso, evidencia-se a necessidade de ampliar a formação e capacitação de farmacêuticos na área de nefrologia, por meio de residências, cursos de extensão e especializações voltadas à farmacoterapia renal. A criação de protocolos clínicos e diretrizes que formalizem as atribuições do farmacêutico em nefrologia pode ser um avanço estratégico para consolidar sua atuação.
Com base nos dados discutidos, fica evidente que o cuidado farmacêutico qualificado pode ser um diferencial na redução de eventos adversos, na prevenção de hospitalizações evitáveis e na melhoria da qualidade de vida de pacientes renais crônicos — especialmente em contextos de alta complexidade como a hemodiálise, o transplante e o tratamento conservador.
5 CONSIDERAÇÕES FINAIS
O presente estudo teve como objetivo principal analisar o impacto da atuação do farmacêutico clínico na prevenção de interações medicamentosas em pacientes com Doença Renal Crônica (DRC). Os resultados levantados a partir da literatura permitiram identificar que esse objetivo foi alcançado, na medida em que ficou evidenciada a relevância da atuação farmacêutica na redução da incidência de interações medicamentosas (IM), na mitigação de riscos clínicos e na otimização da farmacoterapia.
Em relação aos objetivos específicos, observou-se que os principais medicamentos prescritos a pacientes com DRC — incluindo anti-hipertensivos, eritropoetina, quelantes de fósforo, imunossupressores e anticoagulantes — apresentam elevado potencial de interações. A análise de diferentes estudos demonstrou que as IM são frequentes e, em sua maioria, de gravidade moderada a grave, reforçando o risco de eventos adversos. A atuação do farmacêutico clínico mostrou-se fundamental tanto na identificação precoce quanto na resolução de interações reais, classificando-as adequadamente quanto ao mecanismo (farmacocinético ou farmacodinâmico) e ao risco clínico. Ademais, foi possível verificar que fatores como idade avançada, polifarmácia e alterações fisiológicas inerentes à insuficiência renal aumentam substancialmente a probabilidade de ocorrência de IM. Dessa forma, a intervenção farmacêutica impactou positivamente a segurança e a eficácia do tratamento, com boa aceitação por parte da equipe multiprofissional.
As conclusões sobre o impacto do farmacêutico clínico reforçam sua importância como profissional estratégico no cuidado ao paciente renal. Sua atuação contribui diretamente para a redução de hospitalizações evitáveis, melhora da adesão ao tratamento e aumento da qualidade de vida dos pacientes. Além disso, a integração do farmacêutico em equipes multiprofissionais potencializa o uso racional de medicamentos e promove maior segurança assistencial, aspectos essenciais em um contexto clínico de alta complexidade como o da DRC.
Como recomendações para a prática e pesquisas futuras, destaca-se a necessidade de institucionalizar a presença do farmacêutico clínico em todos os níveis de atenção ao paciente renal, desde a atenção primária até serviços especializados como centros de diálise e transplante. Sugere-se ainda o desenvolvimento de protocolos clínicos específicos em nefrologia, que normatizem sua atuação, bem como a ampliação de programas de capacitação, como residências e especializações voltadas à farmacoterapia renal. Por fim, há uma lacuna importante a ser preenchida por meio da realização de ensaios clínicos randomizados no contexto brasileiro, capazes de mensurar de forma robusta e comparativa o impacto das intervenções farmacêuticas na redução de interações medicamentosas e na melhoria dos desfechos clínicos em pacientes com DRC. Dessa forma, conclui-se que a atuação do farmacêutico clínico representa um elemento indispensável para a qualificação da assistência em nefrologia, configurando-se como uma prática que deve ser expandida, fortalecida e continuamente investigada.
REFERÊNCIAS
SOCIEDADE BRASILEIRA DE NEFROLOGIA. Diretrizes para diagnóstico e tratamento da Doença Renal Crônica – DRC. Adotado da definição da National Kidney Foundation – NKF. Revista da Associação Médica Brasileira, São Paulo, 13 maio 2010. Disponível em: https://www.scielo.br/j/ramb/a/3n3JvHpBFm8D97zJh6zPXbn. Acesso em: 15 ago. 2025.
BRASIL. Ministério da Saúde. Boletim Epidemiológico – Volume 55, nº 12: Cenário da doença renal crônica no Brasil no período de 2010 a 2023 [Internet]. Brasília: Ministério da Saúde, 2024. Disponível em: https://www.gov.br/saude/pt-br/centrais-deconteudo/publicacoes/boletins/epidemiologicos/edicoes/2024. Acesso em: 24 ago. 2025.
SOCIEDADE BRASILEIRA DE NEFROLOGIA. Censo de Doença Renal Crônica 2024 . São Paulo: SBN, 2024. Disponível em: https://www.censo-sbn.org.br/inicio. Acesso em: 24 ago. 2025.
AGUIAR, Lilian Kelen de; PRADO, Rogério Ruscitto; GAZZINELLI, Andrea; MALTA, Deborah Carvalho. Fatores associados à doença renal crônica: inquérito epidemiológico da Pesquisa Nacional de Saúde. Revista Brasileira de Epidemiologia, v. 23, e200044, 2020. DOI: 10.1590/1980-549720200044.
NAGAHAMA, André Murad; SILVA, Vanessa dos Santos; BANIN, Vanessa Burgugi; FRANCO, Roberto Jorge da Silva; BARRETTI, Pasqual; BAZAN, Silmeia Garcia Zanati; MARTÍN, Luis Cuadrado. Associação entre estágios da doença renal crônica e alterações dos parâmetros da monitorização ambulatorial da pressão arterial. Jornal Brasileiro de Nefrologia, São Paulo, v. 42, n. 4, p. 399-409, 2020. DOI: https://doi.org/10.1590/2175-8239JBN-2019-0170.
SOCIETY BRAZILIAN OF NEPHROLOGY; BRAZILIAN SOCIETY OF CLINICAL PATHOLOGY AND LABORATORY MEDICINE. Estimativa da Taxa de Filtração Glomerular na prática clínica: posicionamento consensual da Sociedade Brasileira de Nefrologia e Sociedade Brasileira de Patologia Clínica e Medicina Laboratorial. Brazilian Journal of Nephrology, v. 46, n. 3, p. e20230193, 2024. Disponível em: https://www.scielo.br/j/jbn/a/s8GPHkHPbCKLTk8GBqWdzTK/?format=pdf&lang=pt. Acesso em: 19 ago. 2025.
Kirsztajn GM, Silva Junior GBD, Silva AQBD, Abensur H, Romão Junior JE, Bastos MG, Calice-Silva V, Carmo LPFD, Sandes-Freitas TV, Abreu PF, Andreguetto BD, Cortes LGF, Oliveira MGL, Vieira LMF, Moura-Neto JA, Andriolo A. Estimated glomerular filtration rate in clinical practice: Consensus positioning of the Brazilian Society of Nephrology (SBN) and Brazilian Society of Clinical Pathology and Laboratory Medicine (SBPC/ML). J Bras Nefrol. 2024 Apr 5;46(3):e20230193. doi: 10.1590/2175-8239-JBN-2023-0193en. Erratum in: J Bras Nefrol. 2025 Apr-Jun;47(2):e20230193er. doi: 10.1590/2175-8239-JBN2023-0193eren. PMID: 38591823; PMCID: PMC11300030. Acesso em: 20 ago. 2025.
GARCIA SANCHEZ JJ, THOMPSON J, SCOTT DA, EVANS R, RAO N, SÖRSTADIUS E, JAMES G, NOLAN S, WITTBRODT ET, ABDUL SULTAN A, STEFANSSON BV, JACKSON D, ABRAMS KR. Treatments for Chronic Kidney Disease: A Systematic Literature Review of Randomized Controlled Trials. Adv Ther. 2022 Jan;39(1):193-220. doi: 10.1007/s12325-021-02006-z. Epub 2021 Dec 8. PMID: 34881414; PMCID: PMC8799552. Acesso em: 21 ago. 2025.
SOCIEDADE BRASILEIRA DE CARDIOLOGIA. Diretrizes Brasileiras de Hipertensão Arterial – 2020. Arquivos Brasileiros de Cardiologia, v. 116, n. 3, p. 516-658, mar. 2021. DOI: https://doi.org/10.36660/abc.20201238. Acesso em: 21 ago. 2025.
MACHADO, Gabriela Rocha Garcia; PINHATI, Fernanda Romanholi. Tratamento de diálise em pacientes com insuficiência renal crônica. Cadernos UniFOA, Volta Redonda, n. 26, p. 129-136, dez. 2014. ISSN 1809-9475. e-ISSN 1982-1816. Disponível em: http://www.unifoa.edu.br/cadernos/ojs. Acesso em: 21 ago. 2025.
ZANETTI, Teresa Regina Ferreira; et al. Qualidade de vida em transplantados renais. Psico-USF, v. 23, n. 1, p. 1-12, jan./mar. 2018. Disponível em: https://doi.org/10.1590/141382712018230114. Acesso em: 21 ago. 2025.
MIRANDA, Ana Paula Souza; MACHADO, Renata Zacarias. Sistema renina-angiotensinaaldosterona (SRAA) – revisão de literatura. Revista Científica Eletrônica de Medicina Veterinária, v. 9, n. 16, jan. 2011. ISSN 1679-7353. Acesso em: 21 ago. 2025.
FONTE, John H.; KAUR, Jasleen; LAPPIN, Sarah L. Fisiologia, Sistema ReninaAngiotensina. Última atualização: 12 de março de 2023. National Library of Medicine. Disponível em: https://www.ncbi.nlm.nih.gov/books/NBK470410/. Acesso em : 21 ago. 2025.
MIKOS, A. M.; FERNANDES, N. R.; SPIGOLON, D. N.; LABEGALINI, C. M. G.; DA SILVA, V. L.; LOURENÇO, M. P.; SOUZA, V. S.; CHRISTINELLI, H. C. Segurança do paciente na hemodiálise: uma perspectiva sociodemográfica, laboratorial e farmacológica. Arquivos de Ciências da Saúde da UNIPAR, Umuarama, v. 27, n. 6, p. 2146– 2163, 2023. DOI: 10.25110/arqsaude.v27i6.2023- 003. Disponível em: https://doi.org/10.25110/arqsaude.v27i6.2023- 003. Acesso em: 23 ago. 2025.
BRASIL. Ministério da Saúde; Agência Nacional de Vigilância Sanitária; Fundação Oswaldo Cruz. Documento de referência para o Programa Nacional de Segurança do Paciente. Brasília: Ministério da Saúde, 2014. 40 p. Il. ISBN 978- 85- 334- 2130- 1. Disponível em: https://bvsms.saude.gov.br/bvs/publicacoes/documento_referencia_programa_nacional_segur anca.pdf. Acesso em: 24 ago. 2025.
BRASIL. Ministério da Saúde; Agência Nacional de Vigilância Sanitária; Fundação Oswaldo Cruz. Documento de referência para o Programa Nacional de Segurança do Paciente. Brasília: Ministério da Saúde, 2014. Disponível em: http://bvsms.saude.gov.br/bvs/publicacoes/documento_referencia_programa_nacional_segura nca.pdf. Acesso em: 24 ago. 2025.
SOUSA, M. C. et al. Perfil da atenção primária à saúde em pacientes com Doença Renal Crônica no Brasil. Revista Brasileira de Epidemiologia, v. 26, 2023. Acesso em: 24 ago. 2025.
BRASIL. Agência Nacional de Vigilância Sanitária. Resolução RDC nº 36, de 25 de julho de 2013. Institui ações para a promoção da segurança do paciente e a melhoria da qualidade nos serviços de saúde. Diário Oficial da União: seção 1, Brasília, DF, 26 jul. 2013. Disponível em: https://bvsms.saude.gov.br/bvs/saudelegis/anvisa/2013/rdc0036_25_07_2013.html. Acesso em: 24 ago. 2025.
BRASIL. Ministério da Saúde; Agência Nacional de Vigilância Sanitária. Protocolo de segurança na prescrição, uso e administração de medicamentos. Brasília: Ministério da Saúde, 2013. Disponível em: https://www.gov.br/anvisa/pt-br/assuntos/seguranca-dopaciente/protocolos/protocolo-de-seguranca-na-prescricao-uso-e-administracao-demedicamentos.pdf. Acesso em: 24 ago. 2025.
MARQUITO, A. B.; FERNANDES, N. M. da S.; COLUGNATI, F. A. B.; PAULA, R. B. de. Interações medicamentosas potenciais em pacientes com doença renal crônica. Brazilian Journal of Nephrology, São Paulo, v. 36, n. 1, p. 26–34, jan. 2014. Disponível em: https://doi.org/10.5935/0101-2800.20140006. Acesso em: 25 ago. 2025.
SANTOS, JANAINA DA SILVA, GIORDANI, FABIOLA E ROSA, MARIA LUIZA GARCIA. Interações medicamentosas potenciais em adultos e idosos na atenção primária. Ciência & Saúde Coletiva v. 24, n. 11. 4335-4344. Disponível em: <https://doi.org/10.1590/1413-812320182411.04692018>. ISSN 1678-4561. https://doi.org/10.1590/1413-812320182411.04692018. Acesso em: 25 ago. 2025.
BADIN, Rebeka Caribé; MANAÇAS, Liliane Rosa Alves. Interações medicamentosas: definições e mecanismos. In: SILVA, Igor Sombra (org.). Ciência da saúde e do desporto no mundo contemporâneo. Rio Branco: Stricto Sensu, 2022. p. 78–87. Disponível em: https://ninho.inca.gov.br/jspui/handle/123456789/15604. Acesso em: 25 ago. 2025.
BRASIL. Ministério da Saúde. Diretrizes clínicas para o cuidado ao paciente com Doença Renal Crônica – DRC no Sistema Único de Saúde. Brasília: Ministério da Saúde, 2014. Disponível em: https://www.gov.br/conitec/pt-br/midias/protocolos/diretriz-cuidadosdrc.pdf/view. Acesso em: 25 ago. 2025.
SILVA, Fernanda Teixeira. Acompanhamento farmacoterapêutico de pacientes com doença renal crônica em tratamento não dialítico.Universidade Federal do Maranhão, Programa de Pós-Graduação em Saúde do Adulto, São Luís, 2024. Disponível em: http://tede.ufma.br/jspui/bitstream/tede/5279/2/FERNANDATEIXEIRASILVA.pdf. Acesso em: 26 ago. 2025.
The clinical pharmacist in the private community pharmacy: integrative review. Research, Society and Development, [S. l.], v. 10, n. 13, p. e558101321515, 2021. DOI: 10.33448/rsd-v10i13.21515. Disponível em: https://rsdjournal.org/rsd/article/view/21515. Acesso em: 29 aug. 2025.
SOUZA, Hugo dos Santos et al. A atuação do farmacêutico clínico como interventor na identificação de problemas relacionados a medicamentos em hospitais: uma revisão sistemática. Revista Brasileira de Farmácia Hospitalar e Serviços de Saúde, v. 12, n. 1, p. 0519–0528, 2021. Disponível em: https://www.rbfhss.org.br/sbrafh/article/view/519. Acesso em: 29 ago. 2025.
BRASIL. Ministério da Educação. Resolução CNE/CES nº 2, de 19 de fevereiro de 2002, que institui as Diretrizes Curriculares Nacionais do curso de graduação em Farmácia. Diário Oficial da União, Brasília, 4 mar. 2002. Acesso em: 29 ago. 2025.
BRASIL. Conselho Federal de Farmácia – CFF. Resolução nº 357/2001, que aprova o regulamento técnico das boas práticas de farmácia. Diário Oficial da União, Brasília, 27 abr. 2001. Acesso em: 29 ago. 2025.
BRASIL. Conselho Federal de Farmácia – CFF. Resolução nº 585, de 29 de agosto de 2013, que regulamenta as atribuições clínicas do farmacêutico. Disponível em: https://www.normaslegais.com.br/legislacao/Resolucao-cff-585-2013.htm. Acesso em: 29 ago. 2025.
BRASIL. Conselho Federal de Farmácia – CFF. Resolução nº 586, de 29 de agosto de 2013, que regula a prescrição farmacêutica. Diário Oficial da União, 26 set. 2013. Acesso em: 29 ago. 2025.
CONSELHO FEDERAL DE FARMÁCIA. Vitória do Conselho Federal de Farmácia, para a profissão farmacêutica! Publicado em 18 nov. 2022. Disponível em: https://site.cff.org.br/noticia/noticias-do-cff/18/11/2022/vitoria-do-conselho-federal-defarmacia-para-a-profissao-farmaceutica-. Acesso em: 29 ago. 2025.
ICTQ. 6 capítulos da revolução farmacêutica no Brasil. Disponível em: https://ictq.com.br/varejo-farmaceutico/718-6-capitulos-da-revolucao-farmaceutica-no-brasil. Acesso em: 29 ago. 2025.
Diniz ACAM, Souza APB, Reis CT, Ramos SMSV, Barreiros PMM, Souza PJS. Medication reconciliation in an emergency department: a process of continuous improvement. Cogitare Enferm2025 30.Disponível em: https://doi.org/10.1590/ce.v30i0.97863 Acesso em: 29 ago. 2025.
Araujo EO, Viapiana M, Domingues EAM, Oliveira GS e Polisel CG. Intervenções Farmacêuticas em uma Unidade de Terapia Intensiva de um Hospital Universitário. Rev. Bras. Farm. Hosp. Serv. Saúde, 8(3): 25- 30, 2017. Doi: 10.30968/rbfhss.2017.083.005 Acesso em: 29 ago. 2025.
SILVA QC; RODRIGUES JR OM. Atualizações sobre a importância do farmacêutico na área hospitalar de urgência e emergência: na validação de prescrição. RECIMA21 – Revista Científica Multidisciplinar, v. 5, n. 11, 2024, artigo e5115921. Disponível em PDF no site da revista: https://recima21.com.br/index.php/recima21/article/view/5921 Recima21.
KIDNEY DISEASE: IMPROVING GLOBAL OUTCOMES (KDIGO). Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney International, v. 105, n. 6, p. S1–S150, Jun. 2024. Disponível em: https://kdigo.org/guidelines/ckd-evaluation-and-management/. Acesso em: 31 ago. 2025.
PINTO, I. V. L.; CASTRO, M. dos S.; REIS, A. M. M. Descrição da atuação do farmacêutico em equipe multiprofissional com ênfase no cuidado ao idoso hospitalizado. Revista Brasileira de Geriatria e Gerontologia, Rio de Janeiro, v. 16, n. 4, p. 747–758, 2013. Disponível em: https://doi.org/10.1590/S1809-98232013000400009. Acesso em: 31 ago. 2025.
SILVA, Brenner Castro; OLIVEIRA, Jaqueline Vaz de. A importância da atuação permanente do farmacêutico na equipe multidisciplinar da UTI em benefício da saúde do paciente e redução de custos para um hospital no município de Imperatriz-MA. 2025. Trabalho acadêmico (Graduação em Farmácia) – Faculdade Imperatriz, FACIMP, Imperatriz, 2025. Disponível em: https://cff.org.br/userfiles/2012%20-%20Estudante%20%20Brenner%20Castro%20Silva%20e%20Jaqueline%20Vaz%20de%20Oliveira.pdf Acesso em: 31 ago. 2025.
UNIVERSIDADE FEDERAL DE JUIZ DE FORA. Repositório Institucional – BVS Pesquisa. Disponível em: https://repositorio.ufjf.br. Acesso em: 29 ago. 2025.
ALAM, K. et al. Pharmacist-led interventions in the medication management of patients with chronic kidney disease: a pre-post study. Frontiers in Pharmacology, 2024. Disponível em: https://pubmed.ncbi.nlm.nih.gov/38817515/. Acesso em: 31 ago. 2025.
AYTAÇ, E. et al. Role of clinical pharmacists in multidisciplinary teams for management of drug-related problems in patients with chronic kidney disease: a prospective study. BMC Nephrology, v. 24, n. 1, 2023. Disponível em: https://bmcnephrol.biomedcentral.com/articles/10.1186/s12882-023-03210-5. Acesso em: 31 ago. 2025.
CAÑAMARES-ORBIS, P. et al. Impact of pharmacist intervention on chronic kidney disease patients: a hospital-based study. Nefrología, v. 34, n. 4, p. 470–476, 2014. Disponível em: https://pubmed.ncbi.nlm.nih.gov/25135803/. Acesso em: 31 ago. 2025.
ANLEY, H. J. et al. Pharmacist involvement in the care of patients with chronic kidney disease: a systematic review. American Journal of Kidney Diseases, v. 57, n. 6, p. 875–886, 2011. Disponível em: https://pubmed.ncbi.nlm.nih.gov/21719712/. Acesso em: 31 ago. 2025.
ZHAO, W. et al. Impact of pharmacist-led interventions on chronic kidney disease outcomes: a meta-analysis of randomized and observational studies. Frontiers in Pharmacology, 2024. Disponível em: https://pubmed.ncbi.nlm.nih.gov/39384574/. Acesso em: 31 ago. 2025.
CHILCOT, J. et al. Interventions to improve medication adherence in patients with chronic kidney disease: a scoping review. Pharmacy, v. 11, n. 6, 2022. Disponível em: https://www.mdpi.com/2226-4787/11/6/185. Acesso em: 31 ago. 2025.
GOUBAUD, et al. Community pharmacist intervention in patients with renal impairment. PubMed, França. Disponível em: https://pubmed.ncbi.nlm.nih.gov/26385098/. Acesso em: 31 ago. 2025.
MOHAMMADNEZHAD, G. et al. Impact of clinical pharmacy services on medication adherence and quality of life in pre-dialysis patients with CKDu: a randomized controlled trial from Sri Lanka. BMC Nephrology, 2025. Disponível em: https://bmcnephrol.biomedcentral.com/articles/10.1186/s12882-025-04301-1. Acesso em: 31 ago. 2025.
SANTIAGO, F. S. et al. Perfil farmacoterapêutico de pacientes com insuficiência renal crônica submetidos à hemodiálise em um centro de referência do estado do Ceará. Arquivos de Ciências da Saúde da UNIPAR, 2023. Disponível em: https://doi.org/10.25110/arqsaude.v27i6.2023-016. Acesso em: 31 ago. 2025.
ESTUDO MASTERPLAN- PHONE. A pharmacist based intervention to improve the care of patients with CKD: a pragmatic, randomized, controlled trial. PubMed/PMC, ensaio clínico pragmático, atenção primária. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC4405859/. Acesso em: 31 ago. 2025.
BRAGA, Marcus Gomes; BREGMAN, Rachel; KIRSZTAJN, Gianna Mastroianni. Doença renal crônica: frequente e grave, mas também prevenível e tratável. Revista da Associação Médica Brasileira, São Paulo, v. 56, n. 2, p. 248-253, 2010. Disponível em: https://www.scielo.br/j/ramb/a/6W3XgHTfH6yYF8PbVZB5Q3B/?lang=pt. Acesso em: 3 set. 2025.
MOREIRA, Leonardo Barbosa. Adesão ao tratamento farmacológico em doentes renais crônicos atendidos pelo ambulatório do Hospital Universitário Walter Cantídio.181 f. Dissertação (Mestrado em Ciências Farmacêuticas) – Faculdade de Farmácia, Odontologia e Enfermagem, Universidade Federal do Ceará, Fortaleza, 2005. Disponível em: https://repositorio.ufc.br/bitstream/riufc/4228/1/2005_dis_lbmoreira.pdf . Acesso em: 3 set. 2025.
