EVALUATION OF THE USE OF PROPOLIS AS AN ADJUVANT TREATMENT FOR LABIAL HERPES IN IMMUNOCOMPETENT PATIENTS: A LITERATURE REVIEW
REGISTRO DOI: 10.69849/revistaft/cl10202510141536
Mykael Sales Sagama de Sousa¹
Rute de Aguiar Pingarilho²
Prof. Dr. Daniel Berretta Moreira Alves³
Resumo
O herpes vírus é um patógeno que infecta mais de 70% da população mundial, caracterizando-se por sua alta contagiosidade e que seu tratamento é voltado principalmente para controle de sintomas. Logo, o trabalho avaliativo aborda este tema e estabelece como objetivo principal enumerar os benefícios do uso de própolis, sinergicamente ao Aciclovir adjunto da identificação de suas respectivas concentrações e tipos. Onde o fato da mesma ser comercializada como um suplemento natural a torna acessível e de baixo custo que possibilita notáveis efeitos terapêuticos quando utilizada como alternativa aos fármacos já usados para controle dos sintomas inflamatórios provenientes do HSV-1. Sendo aplicada a metodologia de busca eletrônica via plataformas como VLH Regional Portal, Google Scholar, SciELO e PubMed, sob critérios de inclusão artigos de ensaios clínicos, estudos in vitro e in vivo que comprovassem a efetividade terapêutica da própolis. Com resultados que demonstram eficácia quanto a implicações contra ação bacteriana e inflamação promovendo também recuperação tecidual nas regiões orais lesionadas, conseguindo ainda aumentar o período de tempo entre as recidivas da doença. Sem contar que, os produtos à base de própolis, principalmente a verde e vermelha, são disponibilizados como creme, cápsula, comprimido e solução, usualmente nas concentrações de 5%, 10%, 15% e 30%. Conclui-se, então, que a associação da própolis ao aciclovir, como terapia complementar, é um protocolo terapêutico firmado como seguro e eficaz, promovendo saúde e revitalização funcional das áreas lesionadas proporcionando bem-estar físico e social à vida dos pacientes.
Palavras-chave: Vírus do Herpes Simplex 1; aciclovir; própolis.
ABSTRACT
The herpes virus is a pathogen that infects more than 70% of the world’s population, characterized by its high contagiousness, and its treatment is mainly aimed at symptom control. Therefore, this evaluative work addresses this topic and sets as its main objective to enumerate the benefits of using propolis synergistically with acyclovir, along with identifying their respective concentrations and types. Since it is marketed as a natural supplement, propolis is accessible and low-cost, enabling notable therapeutic effects when used as an alternative to drugs currently employed for the management of inflammatory symptoms caused by HSV-1. The methodology applied involved electronic searches via platforms such as the VLH Regional Portal, Google Scholar, SciELO, and PubMed, under inclusion criteria of clinical trial articles, in vitro and in vivo studies that demonstrated the therapeutic effectiveness of propolis. The results show efficacy regarding its implications against bacterial action and inflammation, also promoting tissue recovery in injured oral regions, and even extending the interval between disease recurrences. Furthermore, propolis-based products, especially green and red types, are available in forms such as cream, capsule, tablet, and solution, usually at concentrations of 5%, 10%, 15%, and 30%. It is thus concluded that the combination of propolis with acyclovir, as a complementary therapy, is an established therapeutic protocol that is safe and effective, promoting health and the functional revitalization of injured areas, thereby providing physical and social well-being to patients’ lives.
Keywords: Herpes Simplex Virus 1; acyclovir; propolis.
1. INTRODUÇÃO
De acordo com a Organização Mundial da Saúde (OMS), estima-se que o vírus herpes já tenha entrado em contato com aproximadamente 70% da população mundial (Silva, 2018). Trata-se de um vírus que, na maioria dos casos, permanece em estado latente nos gânglios nervosos, podendo manifestar-se futuramente em decorrência de fatores como estresse físico ou emocional, exposição solar, febre, imunossupressão e alterações hormonais (Neville et al., 2009).
A herpes labial configura-se como a manifestação mais comum da infecção pelo Herpes Simplex Vírus tipo 1 (HSV-1), sendo uma condição frequentemente observada nos consultórios odontológicos. Esta patologia afeta de maneira recorrente milhares de indivíduos, uma vez que o vírus pode ser transmitido também pela saliva, o que resulta em elevada transmissibilidade e potencial de reativação.
A infecção pelo HSV-1 apresenta três períodos clínicos distintos: prodrômico, clínico ativo e reparatório. O período prodrômico caracteriza-se por sinais iniciais como sensibilidade, prurido e ardência no local onde a lesão irá se desenvolver. Em seguida, ocorre a fase ativa, considerada a mais contagiosa, marcada pela formação de lesões vesiculares agrupadas contendo líquido, que podem evoluir para pústulas, causando dor e desconforto. Por fim, o período reparatório é caracterizado pela formação de crostas, indicando a regeneração da pele. O ciclo clínico da infecção tem duração aproximada de 7 a 14 dias (Silva, 2018), período que gera considerável incômodo devido à sintomatologia dolorosa e prolongada.
Nesse contexto, a atuação dos cirurgiões-dentistas no tratamento do herpes labial (HSV-1) torna-se cada vez mais relevante, sendo fundamental a orientação e a prescrição de fármacos antivirais, como o Aciclovir, amplamente utilizado. Adicionalmente, terapias naturais têm ganhado destaque como alternativas tópicas coadjuvantes no manejo das lesões herpéticas.
Entre essas terapias, destaca-se a própolis, uma substância resinosa natural produzida pelas abelhas, reconhecida por suas propriedades anti-inflamatórias, anestésicas e antivirais (Ordem dos Farmacêuticos, 1999; Adelmann, 2005; Santiago et al., 2016; Sforcin, 2016; Conte et al., 2021a). Estudos científicos demonstram que a própolis apresenta efeitos benéficos na cicatrização das lesões herpéticas, especialmente quando utilizada em associação com o Aciclovir (Jautová et al., 2019).
Em 1999, Manara et al. realizaram uma revisão sobre o uso da própolis na Odontologia. A análise de diversos estudos revelou que a própolis possui atividade antimicrobiana, atribuída à presença de flavonoides, ácidos aromáticos e ésteres; ação bactericida, relacionada aos ácidos ferúlico e cafeico; além de demonstrar atividade antiviral in vitro contra o vírus Herpes Simplex e Influenza, em função dos flavonoides e derivados de ácidos aromáticos. Também foram observadas ações imunoestimuladoras, hipotensivas, citostáticas e antiulcerativas (com auxílio na cicatrização).
O uso terapêutico da própolis remonta a mais de 5.000 anos, sendo empregada por civilizações egípcia, grega e romana como antisséptico e cicatrizante (Manara et al., 1999; Silva-Carvalho et al., 2015). Atualmente a própolis é amplamente estudada devido ao baixo custo e eficácia no tecido-alvo. Em 2009, Pensin et al. demonstraram que uma pomada orabase de própolis a 5% acelerou a cicatrização de úlceras aftosas, reduziu a dor e aumentou o intervalo entre recorrências da doença promovendo saúde e bem-estar à vida dos pacientes.
Diante das múltiplas vantagens e possibilidades terapêuticas oferecidas pelo uso da própolis na odontologia, o presente trabalho propõe-se a investigar o impacto do uso do extrato de própolis como terapia coadjuvante no tratamento do herpes labial (HSV-1) em lesões orais e periorais em pacientes imunocompetentes.
Os objetivos deste estudo incluem demonstrar as vantagens do protocolo terapêutico que associa o extrato de própolis ao Aciclovir, bem como expor os tipos e concentrações ideais, assim como as respectivas disponibilidades biológicas visando à promoção de uma cicatrização mais rápida das lesões de herpes labial e a redução do número de recorrências da doença.
2. REFERENCIAL TEÓRICO
2.1 HERPES
O herpes vírus infecta o ser humano na infância, por meio do contato direto com o vírus, ocorrendo a infecção primária que pode ser sintomática ou não, alojando-se no organismo em estado inativo. O vírus penetra no organismo e permanece dormente nos gânglios nervosos, especificamente no gânglio trigêmeo na maioria dos casos (Arduino; Porter, 2008; Bressan et al., 2021). Mais de um terço da população já teve contato com herpes vírus tipo 1 sintomático, sendo muitos assintomáticos. Estimativas mostram que 45% a 98% da população mundial já foram infectadas por HSV-1(Fatahzadeh; Schawartz, 2007; Chabaane et al., 2019)
Pertencente à família do vírus herpes seus demais membros integram um total de mais de 200 conhecidos e catalogados, sendo o: vírus herpes simples 1 (HSV-1) e herpes simples 2 (HSV-2), varicela zoster vírus (VZV), vírus Epstein-Barr (EBV), citomegalovírus (CMV ou HHV-5), e descobertos mais 3 vírus que embora não tenham muitas especificações científicas reveladas até o presente momento, já fazem parte da tabela de patógenos humanos (HHV-6, HHV-7 e HHV-8). Sendo possível a transmissão de todos esses vírus por meio de infecções primárias.
2.1.1 SINAIS E SINTOMAS
O Herpes Simplex Tipo 1 (HSV-1) ocorre o primeiro contato geralmente em faixa etária jovem, quando o indivíduo não tem os anticorpos e denomina-se infecção primária. Muitas vezes tem o padrão assintomático, não causando comorbidades visíveis. Contrai-se quando uma pessoa infectada está liberando ativamente o vírus ou com lesões periorais ativas, porém condições como aglomeração, má higiene, e baixa condição socioeconômica podem expor precocemente ao vírus. Mas não se torna um parâmetro para invulnerabilidade, já que em países desenvolvidos também tem exposição, se não logo na infância, irá ocorrer posteriormente na idade universitária (Neville et al., 2009).
Após a infecção primária o vírus percorre os nervos sensitivos até os gânglios, podendo ficar em estado de latência no organismo. Onde pode ser reativado por contaminação via secreções salivares ou condições de vulnerabilidade como estresse, idade avançada, doenças sistêmicas, gravidez, mudanças de temperaturas e alterações hormonais (Neville et al., 2009). A manifestação sintomática mais comum na infecção primária é a gengivoestomatite herpética primária aguda, representando 90% dos casos. Ocorre entre 6 meses e 5 anos, com prevalência entre 2-3 anos. Casos abaixo de 6 meses são raros devido aos anticorpos maternos. O desenvolvimento inicial são lesões vesiculares que formam feridas múltiplas pequenas e avermelhadas, como na Figura 1. Localiza-se na mucosa e afeta a gengiva, que fica sensível e inchada, como na Figura 2. Os casos se resolvem em 5-7 dias (Neville et al., 2009).
Figura 1 – Gengivoestomatite herpética aguda.
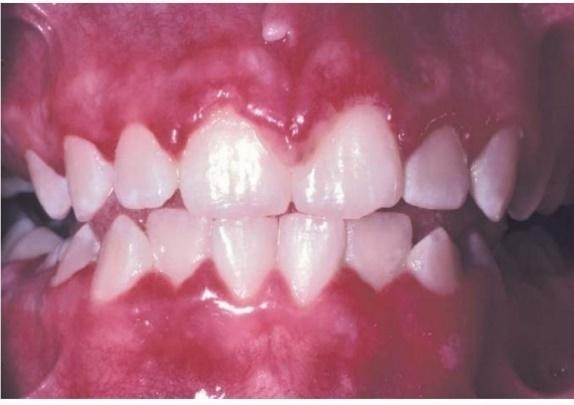
Fonte: Neville et al. (2009, p.244).
Figura 2 – Gengivoestomatite herpética aguda.
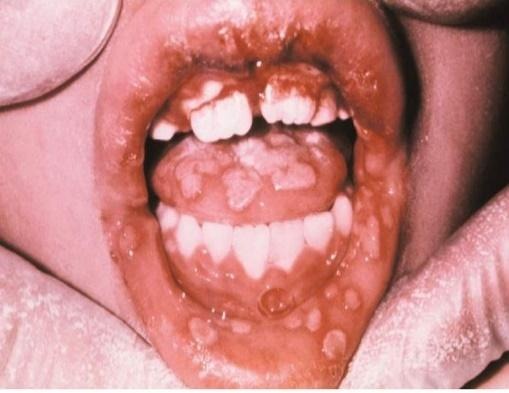
Fonte: Neville et al. (2009, p.243).
Já a faringotonsilite é manifestação tardia de infecção primária sintomática, com desenvolvimento nas amígdalas e parte posterior da faringe. Apresenta lesões herpéticas, vesículas que formam ulcerações, febre, dor de garganta e mal estar (Neville et al., 2009). Na infecção secundária, o vírus é reativado. Alguns pacientes possuem o vírus nas partículas salivares sem sintomas aparentes, enquanto outros apresentam manifestações clínicas recorrentes. A transmissão é perigosa, pois ocorre tanto por lesões ativas quanto pela liberação assintomática do vírus (Neville et al., 2009).
As lesões ocorrem na região orolabial e possuem características vesiculares e pústulas com líquido exsudato virulento contagioso. O paciente pode sentir associadamente febre, dor, náuseas, dificuldades para se alimentar e mal estar (Kolokotronis; Doumas, 2006).
As infecções secundárias têm, geralmente, um padrão de localização. Manifestando-se sintomaticamente no local onde a infecção primária foi atingida, ou muitas vezes na borda do vermelhão do lábio e adjunto a área perioral. Esta é a condição mais conhecida da infecção secundária, o herpes labial, representado na Figura 3.
Figura 3 – Herpes Labial.
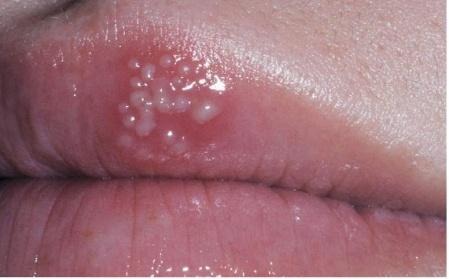
Fonte: Neville et al. (2009, p.244).
O vírus HSV-1 apresenta três estágios de manifestação clínica: prodrômico, clínico ativo e reparatório. O prodrômico consiste nas primeiras 24 horas antes da aparição das vesículas, representada na Figura 4. Importante salientar que este é período para intervenção terapêutica para não progressão de estágio (Silva, 2018).
Figura 4 – Período prodrômico.
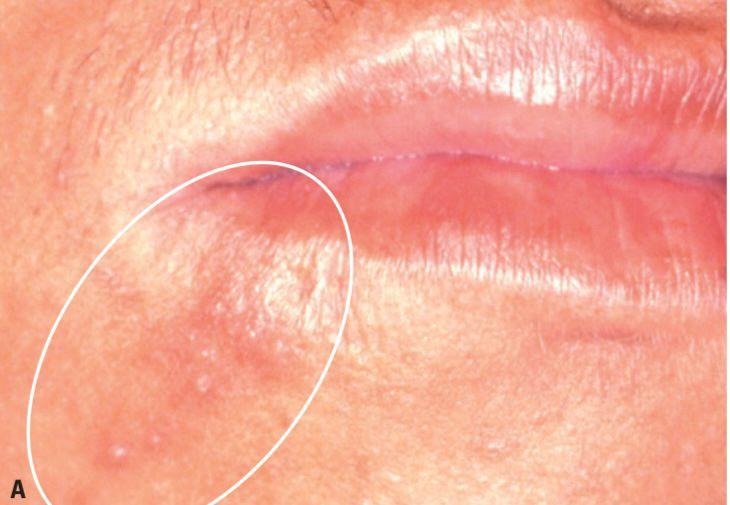
Fonte: Consolaro; Consolaro (2009).
O segundo estágio é o período ativo, a aparição visível de pápulas que em breve formarão vesículas com bolhas na região orofacial, melhor evidenciadas na Figura 5. Estas lesões herpéticas têm duração aproximada de 2 a 4 dias e tem alta taxa de contaminação devido ao rompimento das bolhas com o líquido virulento. Consistindo na fase mais desagradável da doença (Silva, 2018).
Figura 5 – Período ativo.
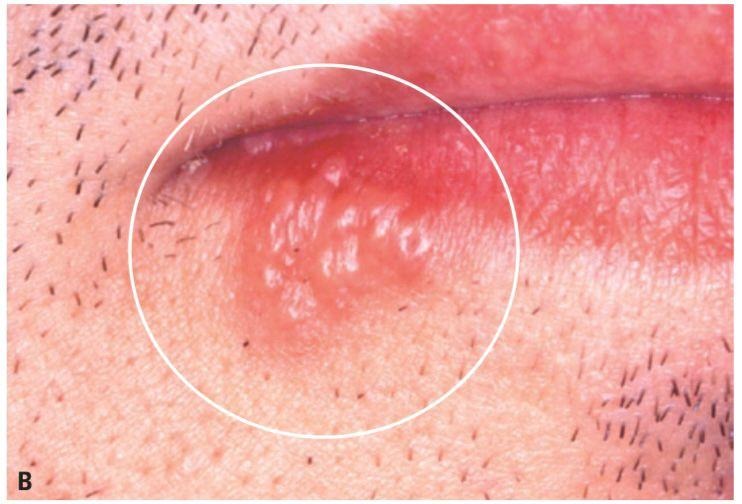
Fonte: Consolaro; Consolaro (2009).
Posteriormente, após o rompimento das bolhas a sintomatologia começa a decair e melhorar, como ilustrado na Figura 6. As lesões finalmente entram em processo de cicatrização, formando crostas indicando o fim da manifestação clínica herpética. Este é o último estágio chamado de período reparatório (Silva, 2018).
Figura SEQ. – período reparatório.
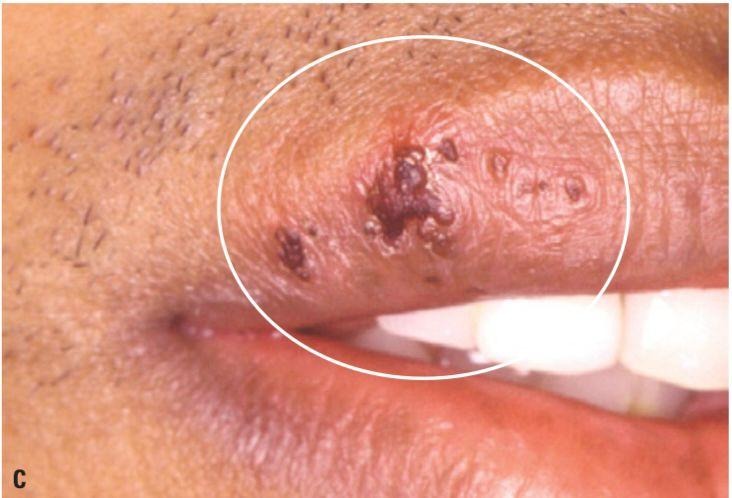
Fonte: Consolaro; Consolaro (2009)
2.1.2 DIAGNÓSTICO
Em critérios de avaliação o HSV-1 recorrente possui um determinado padrão de manifestações dos quais são presentemente acompanhados de vesículas, que evoluem e se rompem tornando-se úlceras que comprometem tarefas simples como a fala e deglutição de alimentos por promoverem dor e desconforto ao paciente (Vazzoller et al., 2016; Bressan et al., 2021). Essas características precedem sintomas como coceira, formigamento, ardência na região, dor em um período entre 6 e 24 horas antes dos sinais clínicos (Balasubramaniam; Kuperstein; Stoopler, 2014).
É importante citar que o número de recidivas pode variar por fatores como imunidade, estresse, problemas hormonais, exposição UV, envelhecimento, gravidez, traumas e doenças sistémicas, com recorrência geralmente limitada à duas vezes por ano, embora existam casos mensais e semanais (Neville et al., 2016; Bressan et al., 2021; Balasubramaniam, Kuperstein, Stoopler, 2014). O ciclo do HSV-1 possui duas formas distintas: entre 5 a 7 dias em casos leves e até 14 dias em casos graves, com encerramento em até 21 dias (Bressan et al., 2021). Por isso é altamente recomendada a avaliação por um cirurgião dentista, com testes laboratoriais para diferenciar lesões do HSV de outras infecções semelhantes como estomatite recorrente, herpangina e síndrome mão-pé-boca (Stoopler et al. 2003).
O intuito desses testes é uma avaliação criteriosa dos pacientes com lesões atípicas para um correto diagnóstico e dentre as opções é digno de ressalve que o método mais sensível e com resultados precisos para a detecção do HSV é a reação em cadeia da polimerase (RCP), realizada em tempo real. Este teste é amplamente reconhecido como a escolha ideal para esse diagnóstico, pois não necessita da presença de vírus viáveis ou células infectadas. Além disso, a RCP oferece a capacidade crucial de discriminar entre os tipos de HSV, uma distinção vital para a elaboração de um plano de tratamento preciso e eficaz (Strick; Wald, 2006).
Portanto, a adoção da RCP não é apenas uma opção, mas uma necessidade indispensável para garantir diagnósticos precisos e tratamentos adequados visando menor tempo de uso de medicação aliada a mais resultados benéficos ao paciente.
2.1.3 TRATAMENTO
Até o presente período da realização desse estudo não há fármacos ou vacinas que consigam eliminar o vírus do HSV-1 completamente do organismo do paciente. Sendo assim os meios de tratamentos se resumem em prevenção, combate dos sintomas e redução da replicação viral diminuindo os danos teciduais, as chances de transmissão e as taxas de recorrências.
Há múltiplos registros de pacientes que testaram positivo para o HSV-1 que não tiveram nenhuma manifestação clínica sendo desnecessário então alguma forma de tratamento, apenas orientações e acompanhamento. Entretanto, todos os portadores devem seguir à risca os cuidados na higiene pessoal para evitar a transmissão para outros locais e indivíduos (Simón, 2012). Para os que precisam de tratamento há um rol de fármacos antivirais que são fundamentais para dificultar a replicação do herpes vírus como o Aciclovir (AVC), Valaciclovir e Famciclovir. O AVC atua inibindo a síntese de DNA total, já o Valaciclovir é uma variação que logo após ser ingerido se torna o Aciclovir (McClain et al., 2015).
Segundo Miranda (2002) fármacos como Foscarnet® e o Cidofovir® também são opções para o tratamento de herpes labial causada por cepas virais que possuem resistência ao Aciclovir e demais medicamentos com a mesma fórmula.
Em contrapartida, para combater os sintomas gerados pelas lesões do HSV-1 é lançado mão dos mais variáveis fármacos presentes no mercado como analgésicos (dipirona, paracetamol, tramadol) e anti-inflamatórios (ibuprofeno, nimesulida, dexametasona, betametasona, piroxicam) que ao serem comprados sem prescrição e devidas orientações podem ser usados de forma excessiva por quem os-procuram, um fato indiscutivelmente preocupante devido existir o risco de superdosagem (Dal Pizzol et al., 2006).
Tão alarmante essa realidade onde fármacos (drogas farmacêuticas) são usados de forma leviana pela população que desconhecem os perigos que essa prática pode causar como resistência bacteriana, sangramento digestivo, hipersensibilidade e ainda a contribuição para ocultar sintomas sobre doenças que passam despercebidas a partir do momento que se adquire o desejado alívio momentâneo, permitindo então sua progressão de forma silenciosa.
É inegável que o ser humano busca soluções práticas e rápidas em momentos de dor e desconforto. Essa inclinação reflete a sabedoria ancestral no uso de produtos naturais como alternativas medicinais para tratar enfermidades, demonstrando a relevância de integrar essas soluções em tratamentos contemporâneos. De acordo com Manara (1999) a própolis, derivada das abelhas, é comercializada em forma de comprimido, creme e solução que, com baixo investimento, podem ser usados terapeuticamente por sua ação anestésica, antiinflamatória e antibacteriana, demonstrando aplicabilidade no ramo odontológico com resultados notáveis em cariologia, cirurgia bucal, endodontia, odontopediatria, periodontia e patologia oral.
Análises foram conduzidos para investigar o potencial do gel à base de própolis em lesões causadas por próteses e o resultado foi remissão clínica completa do edema e eritema palatino em casos de estomatite protética sendo relatado alívio quase imediato pelos pacientes. Quanto a estomatite aftosa em pacientes fazendo uso de comprimidos, 500mg/dia, com própolis em sua composição foi registrado a redução das ocorrências, promoção de ausência de dor e melhora no quadro clínico para fala e deglutição (Samet et al., 2007; Santos et al., 2008).
Um estudo comparativo com tratamentos farmacológicos convencionais para controle de sintomas revelou que a pomada de própolis a 5% acelera significativamente a cicatrização de lesões por HSV-1. Investigações adicionais com pacientes portadores do vírus, utilizando creme de própolis a 0,5%, ratificam essa descoberta. Todos os participantes deste estudo estavam na fase vesicular da doença e seguiram um protocolo rigoroso: aplicação da pomada quatro vezes ao dia, com uma média de 0,2g do creme por lábio. Notavelmente, não houve reações alérgicas ou efeitos adversos, e os resultados foram impressionantes: alívio imediato de dores, inchaço e queimação, acompanhado de cicatrização epitelial completa em apenas três dias (Variani et al., 2017; Jautová et al., 2019).
Esses achados confirmam de maneira conclusiva a eficácia do creme de própolis no tratamento do herpes labial, estabelecendo-a como uma opção terapêutica valiosa para pacientes cujas vidas, aparência e atividades diárias são prejudicadas por essa doença incômoda.
2.2 PRÓPOLIS
Composta por materiais resinosos e estruturas naturais que incluem brotos, botões florais, pólen e cascas de árvores que após enzimas salivares se tornam partes do produto encontrado nas colmeias e usado em funções protetivas, térmicas, de armazenamento e antissépticas a própolis é um composto de aroma característico e coloração variada, podendo ser esverdeada, vermelha ou marrom escuro devido às peculiaridades da flora e fauna locais que determinam sua composição e funções. O seu nome deriva do grego e significa “em frente da comunidade ou cidade”. Sendo um produto não tóxico coletado por abelhas Apis Mellifera, esse composto natural tem sido usado como medicação no controle de enfermidades devido seus efeitos biológicos como antiinflamatório, antimicrobiano, anestésico, cicatrizante, antioxidante, antiviral e antifúngico, aumentando sua procura e instigando pesquisas sobre seus benefícios e aplicabilidade. (Castaldo; Capasso, 2002; Adelmann, 2005; Salatino et al., 2005; Búfalo et al., 2009).
Segundo Manara (1999) a própolis foi amplamente pesquisada para os mais diversos usos, na odontologia em específico, mostrou resultados nas áreas como cirurgia oral (como mediador no controle de dor e edema), endodontia (medicação intracanal e solução irrigadora), periodontia (diminuição de biofilme bacteriano), odontopediatria (verniz brasileiro a 1%,2,5% e 10%) e patologia oral (pomadas de fácil uso sob lesões orais e periorais). Fabricada e comercializada em forma de pastilhas, pastas, comprimidos, goma de mascar, loções, cremes corporais, pomadas, soluções para bochecho (combinado com melissa, salva, malva ou alecrim) e cápsulas exemplificam sua ampla versatilidade útil nos mais diversos campos que fazem parte do cotidiano em meio ao convívio social.
Devida a ampla variedade de tipos de própolis, justificado devido a mais diversificada flora brasileira que aliada ao seu clima tropical favorecem para que as inúmeras e assinaladas espécies de abelhas a produzam em grande escala e mais variadas formas de própolis, foi feito uma classificação dessas em 12 grupos distintos de acordo com suas propriedades físico-químicas e posições geográficas, mais simplificada no Quadro 3, que se sucedeu várias séries de estudos avaliativos onde constatou-se que cada uma delas, dependendo de sua composição, apresentavam variações nas suas respectivas atividades biológicas. Vale salientar que houve uma nova classificação catalogada, o 13° tipo de própolis, de coloração avermelhada, originada do mangue do estado de Alagoas. Já em relação às propriedades biológicas, na ação antimicrobiana, verificaram que as do grupo 6 (região nordeste) mostrou alta atividade contra bactérias Staphylococcus aureus e Streptococcus mutans, quanto a atividade antioxidante, praticamente todos os grupos mostraram alta eficiência, com exceção do grupo 9, que não demonstrou nenhuma atividade desse quesito. Em relação a inibição de enzimas capazes de degradar mucopolissacarídeos, responsável por alguns processos inflamatórios, destacou-se as dos grupos 6, 7 e 8, em contraste as do grupo 11 apresentaram a menor atividade, quanto a atividades antitumorais, destacou-se as dos grupos 6 e 7 que apresentarem alta efetividade contra células tumorais (Park et al., 2000; Trusheva et al., 2006; Daugsch et al., 2008).
Essa classificação teve por finalidade correlacionar as mais diversas própolis brasileiras às suas atividades biológicas de maiores impactos, resultados esses obtidos graças à técnica de cromatografia líquida de alta eficiência (CLAE). Isso possibilitou avanços desde o campo até à indústria farmacêutica onde todos passaram a ter controle de qualidade e faixas de concentração estabelecidos, permitindo a síntese de produtos mais eficazes e precisos que estariam voltados agora para a necessidade principal de quem os-procura (Marcucci; Ferreres; Custódio, 2000; Wagh, 2013).
Desse modo, os produtos originados a partir do conhecimento dessa tabela promoveriam uso direcionado à necessidade específica do paciente bem como o uso do tipo e concentração ideal da própolis.
Quadro 3 – Classificação da Própolis Brasileira de acordo com características físico-químicas e origem geográfica.
| Tipo | Cor | Origem da Própolis |
| G1 (RS5) | Amarelo | Sul |
| G2 (RS1) | Marrom | Sul |
| G3 (PR7) | Marrom Escuro | Sul |
| G4 (PR8) | Marrom | Sul |
| G5 (PR9) | Marrom Esverdeado | Sul |
| G6 (BA11) | Marrom Avermelhado | Nordeste |
| G7 (BA51) | Marrom Esverdeado | Nordeste |
| G8 (PE5) | Marrom Escuro | Nordeste |
| G9 (PE3) | Amarelo | Nordeste |
| G10 (CE3) | Amarelo Escuro | Nordeste |
| G11 (PI11) | Amarelo | Nordeste |
| G12 (SP12) | Verde ou Marrom Esverdeado | Sudeste |
| G13 (AL) | Vermelha | Nordeste |
Fonte: Adaptado de Park et al. (2000).
2.2.1 COMPOSIÇÃO QUÍMICA
É estimada uma das substâncias mais heterogêneas de origem natural e seus constituintes somam mais de 300 já catalogados em diferentes amostras de própolis. Foi observado que seus compostos são originados de três fontes: exsudatos de plantas, substâncias secretadas pelas abelhas e as que são introduzidas durante o seu processo de sintetização. Ao analisar suas estruturas e suas respectivas atividades biológicas foi averiguado que essas, em sua maioria, são provenientes dos compostos fenólicos, que são abundantemente encontrados pela natureza. Estando eles então proporcionalmente ligadas a esses componentes integrativos que conferem a ela os atributos na qual lhe conferiu notoriedade. Todavia essas características integrativas estão sujeitas a alterações por fatores como o tipo de espécie da abelha, flora e o período do ano em que se faz a coleta. Quanto aos flavonoides, junto do ácido fenil cafeico (CAPE), são fenólicos conhecidos por sua competência quando se refere a crescimento e divisão celular, interferência na mobilidade celular de microrganismos e aumento da permeabilidade da membrana. Entretanto, mesmo que estes sejam alvo da pluralidade dos estudos quando se trata de própolis não se pode resumir que suas propriedades terapêuticas sejam somente por contê-los em sua estrutura pois os demais componentes exercem sua influência sobre essas propriedades farmacológicas (Banskota, 1998; Burdock, 1998; Awale et al., 2005; Boyanova et al., 2006; Ahn et al., 2007; Simões et al., 2008).
2.2.2 O USO DE PRÓPOLIS EM CASOS DE HERPES LABIAL
O extrato de própolis tem componentes que proporcionam ação anti-inflamatória, anestésica, cicatrizante, antioxidante e antimicrobiana. Após a descoberta e comprovação dessas propriedades diversos estudos foram realizados para testar sua eficácia no vírus do herpes labial (HSV-1). Além de ser um vírus, ele acompanha manifestações clínicas muito desagradáveis, como lesões vesiculares que além de dor, causa sensibilidade, ardência e desconforto. Dado essa realidade a própolis apresentou um resultado excelente devido suas propriedades.
A mesma tem ação anti-inflamatória e anestésica que são capazes de reduzir significativamente o edema, vermelhidão e dor associada nas lesões vesiculares (Silva et al., 2019).
É importante salientar também a ação cicatrizante da própolis que estimula a proliferação celular, deposição de colágeno e a regeneração da área afetada, acelerando o processo de cicatrização e recuperação (Faria et al., 2023).
Prova desse fato, foram as revisões e avaliações utilizando a pomada de própolis a 5% para tratamento de lesões causadas pelo vírus herpes labial (HSV-1). Foi constatado que a pomada reduziu as dores periorais, ardência, e além disso foi capaz de prolongar o tempo de intervalo de incidências das lesões herpéticas (Variani et al., 2017). Concluindo que a pomada de própolis acelera o processo de cicatrização e se mostra uma promissora ferramenta na esfera odontológica.
Ademais, estudos foram feitos comparando a eficácia com um creme com aciclovir na composição e creme contendo própolis GH 2002 a 0,5%. As pesquisas foram feitas em aproximadamente quatrocentas pessoas divididas em dois grupos. Metade do grupo que utilizou o creme com própolis, demonstrou incrustação da ferida em aproximadamente três dias, enquanto o grupo com o aciclovir teve média de quatro dias. Além de acelerar a cicatrização, o creme com própolis reduziu a dor, coceira e ardência em dois dias (Jautová et al., 2019).
Ensaios clínicos reforçaram essa tese, estudos com pacientes portadores de herpes labial recorrente indicaram que usando uso tópico de pomada com própolis resultou em uma cicatrização mais acelerada e melhora de sintomas. Além disso, foi evidenciado redução na frequência de recorrências (Variani et al., 2017).
Diante dos fatos é evidente que o uso de própolis em tratamento de herpes labial é promissor devido suas particularidades anestésicas, cicatrizantes, anti-inflamatórias e anestésicas.
3. METODOLOGIA
O estudo em questão refere-se à uma revisão integrada da literatura científica, constituída por meio de busca eletrônica nas bases VLH Regional Portal, Medical Literature Analysis and Retrieval System Online (MEDLINE/PubMed), Scientific Eletronic Library Online (SciELO) e Google Scholar. A estratégia de busca foi construída com base nos descritores e sinônimos contidos no Health Sciences Descriptors and Medical Subject Headings (DeCS/MeSH) fazendo uso dos operadores booleanos “AND” e “OR”. A busca por artigos teve seu início e término no período entre os meses de março à setembro de 2025. Utilizou-se critérios de inclusão: artigos de ensaios clínicos, pesquisas de extensão e estudos de caráter comparativo realizados em humanos, estudos in vitro disponibilizados na íntegra, de forma online e gratuita; em linguagem: português, inglês e espanhol; publicados no período de tempo dos últimos 28 anos (1998-2025); que demonstrassem comprovação de eficácia dos produtos derivados de extrato de própolis no controle de respostas anti-inflamatórias, analgésicas, antivirais e antibacterianas em lesões orais e periorais provenientes do vírus causador do HVC-I (herpes Simples). Utilizou-se como critério de exclusão: artigos duplicados, revisões literárias, estudos com animais; estudos cujas infecções analisadas fossem em demais outras regiões fora a bucal.
4. RESULTADOS E ANÁLISE DOS DADOS
Com base em uma vasta gama de artigos e ensaios de natureza investigativa, é inegável a eficácia e segurança do uso da própolis como um complemento sinérgico ao aciclovir, o fármaco principal, no tratamento de lesões orais e periorais herpéticas. Estudos comprovam que medicamentos à base de própolis oferecem uma ação anestésica imediata, aliviando a dor logo após as primeiras aplicações. Além disso, a própolis atua como uma poderosa barreira antimicrobiana, protegendo a superfície lesionada contra bactérias, protozoários e outros patógenos. Sua ação anti-inflamatória é notável, regulando eficazmente as células imunológicas e se destacando como um anti-inflamatório natural de grande potência. Sem contar que, a capacidade cicatrizante da própolis acelera a epitelização e a divisão celular nas áreas afetadas, resultando em uma revitalização tecidual significativamente mais rápida quando comparado com os protocolos farmacológicos convencionais. Logo a própolis não é apenas uma alternativa a ser explorada, mas uma necessidade no tratamento eficaz de lesões herpéticas.
5. CONSIDERAÇÕES FINAIS
De acordo com os 75 artigos usados nesse trabalho, a própolis se destaca como fonte de elevado potencial terapêutico para tratamento do HSV-1 em pacientes imunocompetentes. Oferece ação anestésica imediata, aliviando a dor após as primeiras aplicações, além de atuar como barreira antimicrobiana contra bactérias, protozoários e outros patógenos. Sua ação anti-inflamatória regula eficazmente as células imunológicas, e sua capacidade cicatrizante acelera a epitelização nas áreas afetadas. Os resultados demonstram superioridade aos fármacos sinérgicos ao aciclovir tradicionalmente usados no alívio das dores e revitalização tecidual. A ampla variedade de produtos à base de própolis, principalmente verde e vermelha, nas concentrações casuais de 5% a 30%, disponíveis em cremes, cápsulas e soluções, tornam-na acessível e fácil aplicação para cada estágio da doença. Contudo, mais estudos são necessários para consolidar sua aplicação terapêutica, principalmente quanto à propriedade antiviral em humanos. Logo, conclui-se que a própolis representa uma revolução potencial no tratamento do HVS-1, e a ciência deve continuar explorando suas possibilidades.
REFERÊNCIAS
ADELMANN, Juliana. Própolis: variabilidade composicional, correlação com a flora e bioatividade antimicrobiana/antioxidante. 2005, 186p. Tese de Doutorado. Dissertação (Mestrado em Ciências Farmacêuticas) -Universidade Federal do Paraná, Curitiba. Acessado em: março de 2025.
AHN, Mok-Ryeon et al. Suppression of tumor-induced angiogenesis by Brazilian propolis: major component artepillin C inhibits in vitro tube formation and endothelial cell proliferation. Cancer letters, v. 252, n. 2, p. 235-243, 2007. Disponível em:<https://doi.org/10.1016/j.canlet.2006.12.039>. Acessado em: setembro de 2025.
ARDUINO, P.G.; PORTER, S.R. Herpes simplex vírus type 1 infection: overview on relevant clinico-pathological features. J Oral Pathol Med, v. 37, n. 2, p. 107-21, 2008.
AWALE, S.; SHRESTHA, S.P.; TEZUKA, Y.; UEDA, J.Y; MATSUSHIGE, K.; KADOTA, S. Neoflavonoides and related constituintes from Neapalese própolis and their nitric oxide production inhibitory activity. Journal of Natural Products, v.68, n.6, p. 858-864. 2005. Disponível em:<https://www.academia.edu/download/50002749/Neoflavonoids_and_Related_Constituents_f20161031-16530-1d84r0a.pdf>. Acessado em: setembro de 2025.
BALASUBRAMANIAM, R., Kuperstein, A. S., e Stoopler, E. T. (2014). Atualização sobre Infecções por Vírus do Herpes Oral. Clínicas Odontológicas Da América Do Norte, 58(2), p. 265-280.
BANSKOTA, Arjun H. et al. Chemical constituents of Brazilian propolis and their cytotoxic activities. Journal of Natural Products, v. 61, n. 7, p. 896-900, 1998. Disponível em:< https://www.academia.edu/download/77044015/np980028c20211222-19607-wt50b2.pdf>. Acessado em: setembro de 2025.
BOYANOVA, L.; KOLAROV, R.; GERGOVA, G.; MITOV, I. In vitro activity of Bulgarian própolis against 94 clinical isolates of anaerobic bactéria. Anaerobe, v. 12, p. 173-176. 2006. Disponível em:<https://doi.org/10.1016/j.anaerobe.2006.06.001>. Acessado em: setembro de 2025.
BRESSAN, MARIA JULIA FERRO. Uso do laser de baixa potência no tratamento de herpes labial. 2021.
BUFALO, M. C.; CANDEIAS, J. M. G.; SFORCIN, J. M. In vitro cytotoxic effect of Brazilian green propolis on human laryngeal epidermoid carcinoma (HEp‐2) cells. Evidence‐Based Complementary and Alternative Medicine, v. 6, n. 4, p. 483-487, 2009. Disponível em:< https://doi.org/10.1093/ecam/nem147>. Acessado em: setembro de 2025.
BURDOCK, G. A. Review of the biological properties and toxicity of bee propolis (propolis). Food and Chemical toxicology, v. 36, n. 4, p. 347-363, 1998. Disponível em:<https://doi.org/10.1016/S0278-6915(97)00145-2>. Acessado em: setembro de 2025.
CASTALDO, Stefano; CAPASSO, Francesco. Propolis, an old remedy used in modern medicine. Fitoterapia, v. 73, p. S1-S6, 2002. Disponível em:<https://doi.org/10.1016/S0367-326X(02)00185-5>. Acessado em: setembro de 2025.
CHAABANE, Sonia et al. Herpes simplex virus type 1 epidemiology in the Middle East and North Africa: systematic review, meta-analyses, and meta-regressions. Scientific reports, v. 9, n. 1, p. 1136, 2019. Disponível em:<https://www.nature.com/articles/s41598-018-37833-8>. Acessado em: setembro de 2025.
CONSOLARO, Alberto; CONSOLARO, Maria Fernanda MO. Diagnóstico e tratamento do herpes simples recorrente peribucal e intrabucal na prática ortodôntica. Revista Dental Press de Ortodontia e Ortopedia Facial, v. 14, p. 16-24, 2009. Disponível em:<https://doi.org/10.1590/S1415-54192009000300003>. Acessado em: setembro de 2025.
CONTE, Fernanda Lopes et al. Propolis from southeastern Brazil produced by Apis mellifera affects innate immunity by modulating cell marker expression, cytokine production and intracellular pathways in human monocytes. Journal of Pharmacy and Pharmacology, v. 73, n. 2, p. 135-144, 2021. Disponível em:<https://doi.org/10.1093/jpp/rgaa023>. Acessado em: maio de 2025.
DAL PIZZOL, Tatiane da Silva et al. Uso não-médico de medicamentos psicoativos entre escolares do ensino fundamental e médio no Sul do Brasil. Cadernos de Saúde Pública, v. 22, p. 109-115, 2006. Disponível em:<https://doi.org/10.1590/S0102-311X2006000100012>. Acessado em: setembro de 2025.
DAUGSCH, Andreas et al. Brazilian red propolis—chemical composition and botanical origin. Evidence‐Based Complementary and Alternative Medicine, v. 5, n. 4, p. 435-441, 2008. Disponível em:<https://doi.org/10.1093/ecam/nem057>. Acessado em: setembro de 2025.
DE FARMÁCIA HOSPITALAR, Conselho da Especialidade. da Ordem dos Farmacêuticos, (1999)–Manual de Boas Práticas em Farmácia Hospitalar. Ordem dos Farmacêuticos. 1ª Edição. p. 1-111. Acessado em: março de 2025.
FARIA, Talita Faraj et al. Cicatrização de feridas agudas tratadas com produto em pó à base de própolis verde. Revista de Enfermagem do Centro-Oeste Mineiro, v. 13, 2023. Disponível em:<https://doi.org/10.19175/recom.v13i0.4796>. Acessado em: setembro de 2025.
FATAHZADEH, M.; SCHWARTZ, R. A. Human Herpes simplex vírus infections: epidemiology, pathogenesis, symptomatology, diagnosis, and management. J Am Acad Dermatol, v. 57, n. 5, p. 737-763; quis 764-766, Nov 2007. Disponível em:<https://www.ncbi.nlm.nih.gov/pubmed/17939933>. Acessado em: agosto de 2025.
JAUTOVÁ, Jagienka et al. Lip creams with propolis special extract GH 2002 0.5% versus aciclovir 5.0% for herpes labialis (vesicular stage): Randomized, controlled double-blind study. Wiener Medizinische Wochenschrift (1946), v. 169, n. 7, p. 193-201, 2019. Disponível em:<https://pmc.ncbi.nlm.nih.gov/articles/PMC6497618/>. Acessado em: março de 2025.
KOLOKOTRONIS, A.; DOUMAS, S. Herpes simplex virus infection, with particular reference to the progression and complications of primary herpetic gingivostomatitis. Clinical microbiology and infection, v. 12, n. 3, p. 202-211, 2006.
MANARA, Lúcia Regina Barros et al. Utilização da própolis em odontologia. Rev. Fac. Odontol. Bauru, p. 15-20, 1999. Disponível em:<http://www.hu.usp.br/wp-content/uploads/sites/350/2010/07/1999203.pdf>. Acessado em: abril de 2025.
MARCUCCI, Maria Cristina et al. Evalution of phenolic compounds in Brazilian propolis from different geographic regions. Zeitschrift für Naturforschung C, v. 55, n. 1-2, p. 76-81, 2000. Disponível em:<https://doi.org/10.1515/znc-2000-1-215>. Acessado em: setembro de 2025.
MCCLAIN, L. et al. Broad-spectrum non-nucleoside inhibitors of human herpesviruses. Antiviral Res, v. 121, p. 16-23, Sep 2015. Disponível em:<https:www.ncbi.nlm.nih.gov/pubmed/26079681>. Acessado em agosto de 2025.
MIRANDA, M. M. F. S. Viroses dermatrópicas. Rio de Janeiro: 2002.
NEVILLE, B. W. et al. Patologia oral e maxilofacial. 4. ed. Rio de Janeiro: Elsevier, 2016.
NEVILLE, B. W.; DAMM, D. D.; ALLEN, C. M.; BOUQUOT, J. E. Infecções virais. In: NEVILLE, B. W. et al. Patologia oral e maxilofacial. 3. ed. Rio de Janeiro: Elsevier, 2009. cap. 7, p. 241–248.
PARK, Y. K.; IKEGAKI, M.; ALENCAR, S. M.; MOURA, F.F. Evaluation of Brazilian propolis by both physicochemical methods and biological activity. Honey Bee Science.; v. 21, p. 85-90. 2000.
PENSIN, N. R. et al. Efeito de pomada de própolis em orabase para tratamento de ulcerações aftosas recorrentes – um estudo piloto. Arq. Ciênc. Saúde Unipar. v. 13, n. 3, p. 199-204, set./dez. 2009. Disponível em:<https://unipar.openjournalsolutions.com.br/index.php/saude/article/download/3199/2237>. Acessado em: agosto de 2025.
SALATINO, Antonio et al. Origin and chemical variation of Brazilian propolis. Evidence‐Based Complementary and Alternative Medicine, v. 2, n. 1, p. 33-38, 2005. Disponível em:<https://doi.org/10.1093/ecam/neh060>. Acessado em: setembro de 2025.
SAMET, N. et al. The effect of bee própolis on recurrent aphthous stomatitis: a pilot study. Clinical Oral Investigations, v.11, n.2, p.143-147, 2007. Disponível em:<https://cdn.awsli.com.br/1883/1883637/arquivos/The%20effect%20of%20bee%20propolis%20on%20recurrent%20aphthous%20stomatitis%20A%20PILOT%20STUDY.pdf>. Acessado em agosto de 2025.
SANTIAGO, Karina Basso et al. Immunomodulatory/anti-inflammatory effects of a propolis-containing mouthwash on human monocytes. FEMS Pathogens and Disease, v. 74, n. 8, p.1-8, 2016. Disponível em:<https://doi.org/10.1093/femspd/ftw081>. Acessado em: maio de 2025.
SANTOS, V. R. et al. Efficacy of Brazilian própolis gel for the management of denture stomatitis: a pilot study. Phytotherapy Research, v.22, n.11, p.1544-1547, 2008. Disponível em:<https://www.academia.edu/download/49787216/Efficacy_of_Brazilian_propolis_gel_for_t20161022-14279-1vvsum1.pdf>. Acessado em: setembro de 2025.
SFORCIN, José M. Biological properties and therapeutic applications of propolis. Phytotherapy research, v. 30, n. 6, p. 894-905, 2016. Disponível em:<https://doi.org/10.1002/ptr.5605>. Acessado em: abril de 2025.
SILVA, A.C.F. Desenvolvimento e avaliação de composições precursoras de filmes formados in situ contendo anestésico para tratamento de infecções por Herpes simplex. Universidade de São Paulo, Ribeirão Preto, 2018. Disponível em:<https://doi.org/10.11606/D.60.2018.tde-23052018-092147>. Acesso em: abril de 2025.
SILVA, F. R. G. et al. Phytochemical screening and in vitro antibacterial, antifungal, antioxidant and antitumor activities of the red propolis Alagoas. Brazilian Journal of Biology, v. 79, n. 3, p. 452-459, 2019. Disponível em:<https://doi.org/10.1590/1519-6984.182959>. Acessado em: setembro de 2025.
SILVA-CARVALHO, R.; BALTAZAR, F.; ALMEIDA-AGUIAR, C. Propolis: a complex natural product with a plethira of biological activities that can be explored for drug development. Evidence-based Complementary and Alternative Medicine, n.2015 p.1-29, 2015. Disponível em:<https://onlinelibrary.wiley.com/doi/epdf/10.1155/2015/206439>. Acessado em: maio de 2025.
SIMÕES, Cinthia Coelho; ARAÚJO, Danilo Barral de; ARAÚJO, Roberto Paulo Correia de. Estudo in vitro e ex vivo da ação de diferentes concentrações de extratos de própolis frente aos microrganismos presentes na saliva de humanos. Revista Brasileira de Farmacognosia, v. 18, p. 84-89, 2008. Disponível em:<https://doi.org/10.1590/S0102-695X2008000100016>. Acessado em: setembro de 2025.
SIMÓN, A. Herpes Labial: Centro de informação do medicamento. 2012.
STOOPLER, E. T. et al. Herpes simplex and varicela-zoster infections: clinical and laboratory diagnosis. Gen Dent, v. 51, n.3, p. 281-286, 2003.
STRICK, L. B.; WALD, A. Diagnostics for herpes simplex virus: is PCR the new gold standard? Mol Diagn Ther, v. 10, n. 1, p. 17-28, 2006.
TRUSHEVA, Boryana et al. Bioactive constituents of Brazilian red propolis. Evidence‐Based Complementary and Alternative Medicine, v. 3, n. 2, p. 249-254, 2006. Disponível em:<https://onlinelibrary.wiley.com/doi/pdf/10.1093/ecam/nel006>. Acessado em: setembro de 2025.
VARIANI, G. C. C. R.; PALLUDO, A. G.; PENSIN, N. R.; HAHN, C. F. P.; BOLETA-CERANTO, D. de C. F. Avaliação do efeito de pomada de própolis para tratamento de herpes labial recorrente – um estudo piloto. Arquivos de Ciências da Saúde da UNIPAR, Umuarama, v. 21, n. 1, p. 13–18, jan./abr. 2017. Disponível em:<https://unipar.openjournalsolutions.com.br/index.php/saude/article/download/6071/3390>. Acessado em: junho de 2025.
VAZZOLLER, Rafael Marinho Souza et al. Tratamento do herpes simples por meio da laserterapia: relato de casos. Rev Cient ITPAC, v. 9, n. 1, p. 1-11, 2016.
WAGH, Vijay D. Propolis: a wonder bees product and its pharmacological potentials. Advances in Pharmacological and Pharmaceutical Sciences, v. 2013, n. 1, p. 308249, 2013. Disponível em:<https://doi.org/10.1155/2013/308249>. Acessado em: setembro de 2025.
WATANABE, A. Herpes vírus. 2018. Disponível em:<http://bit.ly/2EJnjLf>. Acessado em: agosto de 2025.
1Discente no Instituto Esperança de Ensino Superior-IESPES. http://lattes.cnpq.br/3983663001641860 – mykael.sousa@iespes.edu.br
2Discente no Instituto Esperança de Ensino Superior IESPES – pingarilhoaguiar@gmail.com
3Docente no Instituto Esperança de Ensino Superior-IESPES – danielberreta@hotmail.com
