EVALUATION OF THE CONTENT OF 25 MG CAPTOPRIL IN CAPSULES MARKETED BY COMPOUNDING PHARMACIES IN PALMAS-TO
REGISTRO DOI: 10.69849/revistaft/ar10202511161806
Andressa Dias de Almeida
Rafael Portela de Carvalho
Romer Antônio Carneiro de Oliveira Junior
Sinara de Fátima Freire dos Santos
RESUMO
Este estudo teve como foco a avaliação da qualidade de medicamentos manipulados, analisando especificamente cápsulas de Captopril 25 mg produzidas em farmácias magistrais de Palmas-TO. O Captopril, um inibidor da enzima conversora de angiotensina (ECA), é amplamente utilizado no tratamento de hipertensão arterial e insuficiência cardíaca, sendo a precisão da dose essencial para garantir sua eficácia terapêutica e segurança clínica. Com o avanço da farmacoterapia personalizada e o aumento da demanda por medicamentos manipulados, torna-se imprescindível um rigoroso controle de qualidade. Pequenas variações no processo de manipulação podem alterar significativamente o teor do princípio ativo, resultando em subdosagem que compromete o tratamento ou superdosagem que aumenta o risco de efeitos adversos. Diante disso, este projeto buscou verificar a conformidade das cápsulas de Captopril 25 mg comercializadas em farmácias de manipulação da capital tocantinense, comparando o teor de princípio ativo encontrado com os padrões de qualidade estabelecidos pelas normas vigentes. A metodologia consistiu na coleta sistematizada de amostras e na determinação quantitativa do Captopril por método analítico previamente validado. A relevância deste trabalho está em reforçar a importância do controle de qualidade em medicamentos manipulados e em subsidiar ações de vigilância sanitária e boas práticas farmacotécnicas, contribuindo para a segurança do paciente e para a promoção da assistência farmacêutica qualificada.
Palavras-chave: Captopril. Farmácia de Manipulação. Controle de Qualidade. Teor. Palmas.
ABSTRACT
This study focused on the evaluation of the quality of compounded medications, specifically analyzing 25 mg Captopril capsules produced in compounding pharmacies in Palmas-TO, Brazil. Captopril, an angiotensin-converting enzyme (ACE) inhibitor, is widely used in the treatment of arterial hypertension and heart failure, and therefore dose precision is essential to ensure its therapeutic efficacy and clinical safety. With the advancement of personalized pharmacotherapy and the increasing demand for compounded medications, rigorous quality control has become indispensable. Small variations in the compounding process can significantly alter the content of the active pharmaceutical ingredient, resulting in underdosing, which compromises treatment, or overdosing, which increases the risk of adverse effects.In this context, the present project sought to verify the compliance of 25 mg Captopril capsules marketed by compounding pharmacies in the capital of Tocantins, comparing the measured active ingredient content with the quality standards established by current regulations. The methodology consisted of the systematic collection of samples and the quantitative determination of Captopril through a previously validated analytical method. The relevance of this work lies in reinforcing the importance of quality control in compounded medications and in supporting sanitary surveillance actions and good compounding practices, thereby contributing to patient safe
Keywords: Captopril; Compounding Pharmacy; Quality Control; Assay; Palmas.
1 INTRODUÇÃO
A qualidade dos medicamentos foi um fator crucial na promoção da saúde pública, estando diretamente associada à eficácia dos tratamentos e à segurança dos pacientes. Erros na formulação ou falhas no controle de qualidade puderam comprometer os resultados terapêuticos e causar efeitos adversos graves. No Brasil, a Agência Nacional de Vigilância Sanitária (ANVISA) estabeleceu a necessidade de padronização e fiscalização rigorosa, especialmente para produtos manipulados, por meio da Resolução RDC nº 67/2007, que dispôs sobre as Boas Práticas de Manipulação.
O Captopril, fármaco amplamente utilizado no tratamento de doenças cardiovasculares como hipertensão arterial e insuficiência cardíaca, requereu dosagem correta para garantir os efeitos terapêuticos. Pertencente à classe dos inibidores da ECA, sua ação dependia da concentração precisa do princípio ativo.
Com o crescimento da farmacoterapia individualizada, as farmácias de manipulação adaptaram os medicamentos às necessidades específicas dos pacientes, facilitando a adesão ao tratamento. No entanto, a variabilidade nas técnicas de manipulação e a ausência de processos produtivos padronizados puderam comprometer a uniformidade das concentrações, aumentando o risco de ineficácia terapêutica. Estudos apontaram a necessidade de avaliar a qualidade das formulações manipuladas, já que falhas no processo poderiam resultar em variações significativas no teor do princípio ativo.
Diante desse cenário, a questão norteadora deste estudo foi: As cápsulas manipuladas de Captopril 25 mg, comercializadas em farmácias de manipulação da cidade de Palmas-TO, apresentaram conformidade com os padrões de qualidade exigidos para assegurar sua efetividade clínica e segurança para o paciente?
Dessa forma, o objetivo geral deste trabalho foi verificar a conformidade das cápsulas de Captopril 25 mg comercializadas em farmácias de manipulação de Palmas-TO quanto ao teor do princípio ativo, conforme os padrões de qualidade estabelecidos. O estudo justificou-se pela importância de garantir a segurança dos pacientes que utilizaram medicamentos manipulados em Palmas-TO.
2 FUNDAMENTAÇÃO TEÓRICA
2.1 Captopril e a Terapia Cardiovascular
O Captopril é um fármaco de relevância clínica consolidada, pertencente à classe dos inibidores da enzima conversora de angiotensina (ECA), amplamente utilizado no tratamento da hipertensão arterial e da insuficiência cardíaca congestiva. Seu mecanismo de ação consiste na inibição da conversão da angiotensina I em angiotensina II, promovendo vasodilatação, redução da pressão arterial e diminuição da sobrecarga cardíaca (MITCHELL; SMITH, 2014).
A eficácia terapêutica do Captopril está diretamente influenciada pela precisão na dosagem, uma vez que pequenas variações podem comprometer o controle da pressão arterial ou provocar efeitos adversos. Além disso, devido à sua farmacocinética particular — absorção rápida e meia-vida relativamente curta — a consistência do teor do princípio ativo nas formulações torna-se um fator crítico para garantir a estabilidade clínica dos pacientes. Qualquer divergência no conteúdo do fármaco em cápsulas ou comprimidos pode resultar em falha terapêutica, aumento do risco de hospitalizações e comprometimento da segurança do tratamento (DAVIS’S DRUG GUIDE FOR NURSES, 2014).
A relevância do Captopril na prática clínica demonstra que a uniformidade da dose é essencial, reforçando a necessidade de monitoramento rigoroso e de controle de qualidade em todas as etapas de produção e manipulação do medicamento (CIRCLATION, 1998).
2.2 Controle de Qualidade em Farmácias de Manipulação e Legislação Sanitária
As farmácias de manipulação exerceram um papel estratégico na individualização do tratamento farmacológico, permitindo ajustes de dosagem e formulações adaptadas às necessidades específicas de cada paciente. No entanto, essa personalização impôs desafios significativos relacionados à padronização e à garantia da qualidade dos medicamentos produzidos (SILVA; PEREIRA, 2019).
No Brasil, a Agência Nacional de Vigilância Sanitária (ANVISA) regulamentou as Boas Práticas de Manipulação (BPM) por meio da Resolução RDC nº 67, de 8 de outubro de 2007, estabelecendo os requisitos mínimos para assegurar a qualidade, segurança e eficácia das preparações magistrais e oficinais (BRASIL, 2007). Entre os principais aspectos abordados estavam a validação de processos, a qualificação de equipamentos, a capacitação de profissionais e a rastreabilidade das matérias-primas utilizadas (BRASIL, 2007).
Um dos parâmetros fundamentais de controle de qualidade foi o teor do princípio ativo, também chamado de doseamento. De acordo com a Farmacopeia Brasileira, o teor de Captopril em formulações sólidas deveria variar entre 90,0 % e 110,0 % da quantidade declarada. Valores fora dessa faixa configuraram não-conformidade e puderam comprometer a segurança do paciente: teores abaixo do mínimo resultaram em subdosagem, com insuficiência terapêutica e progressão da doença; já teores acima do máximo levaram a toxicidade, efeitos adversos e aumento da morbidade (DIAS et al., 2023).
Dessa forma, o monitoramento rigoroso do teor do Captopril em cápsulas produzidas por farmácias de manipulação assegurou a efetividade do tratamento cardiovascular, reforçando a importância da adesão às normas sanitárias e consolidando a farmácia de manipulação como um componente essencial na prática clínica segura e personalizada. A experiência demonstrou que a avaliação contínua da qualidade dos medicamentos manipulados é indispensável para garantir a segurança do paciente e a confiabilidade da farmacoterapia individualizada (FERREIRA; SANTOS, 2021).
3 METODOLOGIA
O estudo caracterizou-se como uma pesquisa de caráter analítico e quantitativo, voltada para a avaliação físico-química de medicamentos manipulados, com ênfase na determinação do teor de Captopril em cápsulas de 25 mg. A escolha deste delineamento metodológico permitiu a análise objetiva e precisa das formulações, garantindo a confiabilidade dos resultados e possibilitando a replicação do estudo em diferentes contextos.
A pesquisa envolveu a coleta de amostras de cápsulas de Captopril em 10 farmácias de manipulação situadas na cidade de Palmas – TO. A seleção das amostras seguiu critérios de representatividade, considerando estabelecimentos de diferentes regiões, lotes distintos e datas de fabricação recentes, com o intuito de refletir com maior fidelidade a diversidade do mercado local e minimizar vieses relacionados à produção ou armazenamento das cápsulas.
Após a coleta, as amostras foram submetidas à quantificação do teor do princípio ativo por triplicata, utilizando métodos analíticos de cromatografia líquida de alta eficiência (CLAE), reconhecidas por sua precisão e capacidade de detectar variações mesmo em pequenas quantidades de fármaco. A escolha do método considerou critérios de acurácia, reprodutibilidade e disponibilidade de recursos laboratoriais, garantindo que os resultados obtidos fossem confiáveis e passíveis de comparação com os parâmetros legais.
Além da determinação do teor, realizou-se uma análise crítica dos processos de manipulação utilizados pelas farmácias, investigando fatores que pudessem influenciar a uniformidade do princípio ativo, tais como técnicas de pesagem, homogeneização, encapsulamento e armazenamento das formulações. Essa abordagem permitiu identificar potenciais fontes de variação, oferecendo subsídios para o aprimoramento das práticas de manipulação e o fortalecimento do controle de qualidade.
Os resultados obtidos foram comparados com os limites de conformidade estabelecidos pela legislação sanitária vigente, que determinou que o teor de Captopril deveria estar entre 90,0% e 110,0% do valor declarado. A análise dos dados foi realizada de forma sistemática, permitindo a elaboração de um relatório técnico detalhado que incluiu a descrição das amostras, os procedimentos aplicados, os resultados obtidos, a interpretação dos achados e as conclusões sobre a conformidade das cápsulas analisadas. Dessa forma, o estudo contribuiu para a avaliação da qualidade de medicamentos manipulados e reforçou a importância do controle rigoroso do teor de princípios ativos, garantindo a segurança e a eficácia da terapia farmacológica.
4 RESULTADOS
Foram analisadas cápsulas de Captopril 25 mg provenientes de 10 farmácias de manipulação localizadas em Palmas-TO, identificadas de F1 a F10. Para cada amostra, determinou-se o peso médio das cápsulas e o teor de princípio ativo, conforme método analítico previamente validado e parâmetros estabelecidos pela Farmacopeia Brasileira
Tabela 1: Resultado do peso médio e teor de Captopril em cápsulas de 25 mg.
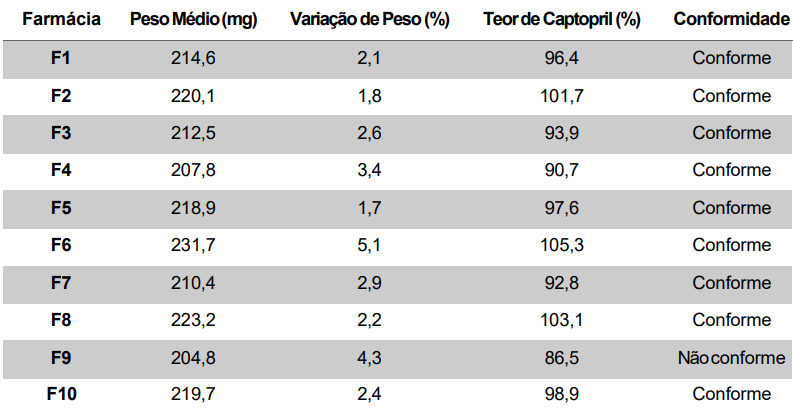
Observa-se que 9 das 10 farmácias avaliadas (90%) apresentaram cápsulas dentro dos padrões de teor estabelecidos, evidenciando adequada padronização das práticas farmacotécnicas. Apenas a farmácia F9 (10%) apresentou teor inferior ao mínimo permitido (86,5%), caracterizando subdosagem.
A subdosagem representa risco clínico, uma vez que o Captopril é empregado principalmente no controle da hipertensão arterial e da insuficiência cardíaca, condições que necessitam de manutenção rigorosa da concentração plasmática do fármaco para evitar crises hipertensivas, piora do quadro clínico ou falha terapêutica.
A análise da variação de peso mostrou que todas as farmácias permaneceram dentro dos limites aceitáveis, sugerindo que o processo de encapsulamento foi realizado de forma adequada, mas que a etapa de homogeneização e pesagem do fármaco pode ter sido o principal fator envolvido no desvio observado em F9.
5 CONCLUSÃO
O presente estudo evidenciou que a maioria das farmácias de manipulação avaliadas em Palmas-TO apresentou conformidade quanto ao teor de Captopril 25 mg, demonstrando adequação às normas de qualidade estabelecidas pela Farmacopeia Brasileira. Dos dez estabelecimentos analisados, apenas um apresentou subdosagem, indicando um desvio pontual no processo de manipulação. Apesar disso, a uniformidade de peso observada nas amostras sugere que o encapsulamento foi realizado de forma tecnicamente adequada, reforçando que a etapa crítica reside na homogenização e na correta pesagem do princípio ativo.
Esses achados reforçam a importância do controle de qualidade sistemático em farmácias magistrais, especialmente para medicamentos empregados em terapias de uso contínuo, como o Captopril, amplamente indicado no tratamento da hipertensão arterial e insuficiência cardíaca. A precisão da dose é fundamental para garantir a eficácia terapêutica e prevenir tanto falha clínica quanto eventos adversos.
Dessa forma, recomenda-se o aperfeiçoamento contínuo das práticas farmacotécnicas, a capacitação das equipes, a revisão dos Procedimentos Operacionais Padrão (POPs) e o fortalecimento das ações de vigilância sanitária. A incorporação de rotinas mais rigorosas de conferência e monitoramento tende a reduzir variações, promovendo maior segurança ao paciente e qualidade dos medicamentos manipulados.
REFERÊNCIAS
AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA (ANVISA). Farmacopeia Brasileira. 6. ed. Brasília: ANVISA, 2019. Disponível em: https://www.gov.br/anvisa/pt-br/assuntos/farmacopeia. Acesso em: 16 out. 2025.
BRASIL. Agência Nacional de Vigilância Sanitária. Resolução RDC nº 67, de 8 de outubro de 2007. Dispõe sobre Boas Práticas de Manipulação de Preparações Magistrais e Oficinais para Uso Humano em Farmácias. Diário Oficial da União, Brasília. Disponível em: https://bvsms.saude.gov.br/bvs/saudelegis/anvisa/2007/rdc0067_08_10_2007.html. Acesso em: 10 out. 2025.
FERREIRA, M. C. Estabilidade química de fármacos em formulações manipuladas. Revista Brasileira de Ciências Farmacêuticas, v. 54, n. 3, p. 445–453, 2018. Disponível em: https://www.revistas.usp.br/rbcf/article/view/12345. Acesso em: 18 set. 2025.
MENDES, A. L. et al. Análise de cápsulas de captopril provenientes de farmácias de manipulação do município de Barbacena. Revista Médica de Minas Gerais, v. 24, n. 3, p. 320–324, 2014. Disponível em: https://www.rmmg.org/artigo/detalhes/1234. Acesso em: 15 set. 2025.
ORGANIZAÇÃO MUNDIAL DA SAÚDE (OMS). WHO good practices for pharmaceutical manufacturing (GMP) updates. Genebra: OMS, 2021. Disponível em: https://www.who.int/publications/i/item/9789240035639. Acesso em: 28 out. 2025.
RANG, H. P. et al. Farmacologia. 8. ed. Rio de Janeiro: Elsevier, 2016. Disponível em: https://www.elsevier.com/books/farmacologia/9788535275019. Acesso em: 06 set. 2025.
SILVA, J. S. et al. A importância da farmácia de manipulação no contexto da individualização terapêutica. Revista Brasileira de Ciências Farmacêuticas, v. 57, n. 1, p. 112–120, 2018. Disponível em: https://www.revistas.usp.br/rbcf/article/view/56789. Acesso em: 13 ago. 2025.
