ASSOCIATION BETWEEN SINGLE-DOSE TAFENOQUINE USE AND REDUCTION IN PLASMODIUM VIVAX MALARIA RECURRENCES: A BIBLIOGRAPHIC REVIEW
REGISTRO DOI: 10.69849/revistaft/fa10202509222233
Joyce Karolina Dantas Melo¹
Ellyda Etheline Torres Noronha²
Dra. Alcione de Oliveira dos Santos³
RESUMO
Introdução: A malária vivax permanece como desafio para o controle da doença no Brasil, devido às recaídas relacionadas à ativação de hipnozoítos hepáticos e à baixa adesão ao esquema convencional com primaquina. A tafenoquina, uma 8aminoquinolina de meia-vida prolongada, surge como alternativa terapêutica promissora em dose única. Metodologia: Trata-se de revisão integrativa da literatura, contemplando ensaios clínicos, estudos observacionais e evidências programáticas publicadas entre 1999 e 2024. Resultados e discussão: Os estudos clínicos demonstraram que a tafenoquina apresenta eficácia semelhante à primaquina na prevenção de recaídas, com taxas de pacientes livres de parasitemia variando entre 62% e 89% em seis meses, superando amplamente a cloroquina isolada. Ensaios no Brasil confirmaram efetividade em condições operacionais, com impacto positivo em adesão, viabilidade logística e custo-efetividade. A implementação piloto evidenciou boa aceitação entre profissionais e cobertura crescente nos estados amazônicos. Entretanto, foram relatados eventos adversos, sobretudo hemólise em portadores de deficiência de G6PD e alterações hematológicas e oculares, reforçando a necessidade de triagem quantitativa e protocolos de farmacovigilância. Conclusão: A tafenoquina representa avanço terapêutico relevante por simplificar o tratamento da malária vivax, com potencial de reduzir significativamente os casos de recaída, mas sua utilização segura requer rastreamento prévio de G6PD e monitoramento clínico adequado.
Palavras-Chave: Recaída de Malária, Tafenoquina, Tratamento de malária.
ABSTRACT
Introduction: Plasmodium vivax malaria remains a major challenge for control in Brazil due to relapses driven by activation of hepatic hypnozoites and poor adherence to the conventional multi-day primaquine regimen. Tafenoquine, a long-half-life 8aminoquinoline, has emerged as a promising single-dose alternative. Methods: We conducted an integrative review of the literature, including randomized trials, observational studies, and programmatic evidence published between 1999 and 2024. Results: Clinical studies show tafenoquine achieves relapse prevention comparable to primaquine, with six-month recurrence-free proportions ranging from 62% to 89%, and consistently outperforming chloroquine monotherapy. Trials and operational evaluations in Brazil indicate effectiveness under real-world conditions, with favorable impacts on adherence, logistical feasibility, and cost-effectiveness. Pilot implementation demonstrated good provider acceptance and expanding coverage across Amazonian states. Adverse events were reported, notably hemolysis among individuals with glucose-6-phosphate dehydrogenase (G6PD) deficiency, as well as hematologic and ocular changes, underscoring the need for quantitative G6PD testing and robust pharmacovigilance protocols. Conclusions: Tafenoquine represents a meaningful therapeutic advance by simplifying P. vivax radical cure and has the potential to substantially reduce relapse burden. Safe use, however, requires prior G6PD screening and appropriate clinical monitoring.
Keywords: Malaria Relapse, Tafenoquine, Malaria Treatment.
INTRODUÇÃO
A malária é uma doença infecciosa febril aguda causada por protozoários do gênero Plasmodium e transmitida pela picada da fêmea do mosquito Anopheles. Em 2023, consoante a Organização Mundial da Saúde (WHO, 2023), foram registrados aproximadamente 263 milhões de casos e 597 mil óbitos atribuídos à doença em nível global. No Brasil, no mesmo período, a transmissão concentrou-se na Região Amazônica — que abrange os estados do Acre, Amazonas, Amapá, Maranhão, Mato Grosso, Pará, Rondônia, Roraima e Tocantins —, responsável por cerca de 99% dos casos autóctones, com predomínio da infecção por Plasmodium vivax (82%) (BRASIL, 2025).
Entre os desafios relacionados à espécie P. vivax, destaca-se a ocorrência de recaídas, fenômeno que representa importante obstáculo para o controle da malária. A recaída é caracterizada pelo ressurgimento da parasitemia e das manifestações clínicas devido à reativação de hipnozoítos dormentes no fígado (SIMÕES, 2012). Esse fenômeno é responsável por manter a transmissão ativa, aumentar a morbidade e dificultar estratégias de controle da doença.
Nesse contexto, o tratamento assume papel central na tentativa de reduzir a transmissão e prevenir novas recaídas. O tratamento padrão no Brasil para P. vivax consiste na administração de cloroquina por 3 dias associada à primaquina por 7 dias na primoinfecção, ou da combinação artemeter + lumefantrina por 3 dias com primaquina por 14 dias nos casos de recaída em até 60 dias (BRASIL, 2010). Embora eficaz, esse regime enfrenta limitações importantes quanto à adesão. Fatores como baixa escolaridade, condições socioeconômicas precárias, efeitos adversos e dificuldades de acesso ao sistema de saúde contribuem para a interrupção precoce do tratamento (PEREIRA et al., 2013; GAMA et al., 2014; GONÇALVES; SILVA; GUERRA, 2013).
Nesse cenário, a tafenoquina, uma 8-aminoquinolina de meia-vida prolongada (aproximadamente, 15 dias), surge como alternativa promissora. Administrada em dose única de 300 mg, em associação à cloroquina, a tafenoquina visa promover a cura radical por eliminação dos hipnozoítos, representando potencial solução para superar falhas de adesão observadas nos esquemas prolongados com primaquina (LACERDA et al., 2019).
Contudo, a utilização da tafenoquina exige rastreamento prévio da deficiência de glicose-6-fosfato desidrogenase (G6PD), devido ao risco de hemólise grave, característica comum às 8-aminoquinolinas. A necessidade desse teste pré-tratamento representa desafio logístico, especialmente em áreas remotas da Amazônia, onde a infraestrutura laboratorial é limitada (BRITO et al., 2024). Apesar dessa limitação, a aprovação da tafenoquina pela Food and Drug Administration (FDA, 2018) e, mais recentemente, por agências regulatórias de países endêmicos, reforça sua relevância como inovação terapêutica no controle da malária vivax.
Considerando a elevada carga da malária vivax no Brasil, as elevadas taxas de recaída que perpetuam a transmissão e a dificuldade de adesão ao regime convencional, torna-se essencial analisar a evidência disponível sobre a tafenoquina. A simplificação posológica em dose única pode não apenas reduzir a recorrência clínica e a transmissão comunitária, mas também gerar impacto positivo em políticas públicas de controle e eliminação da malária (WHO, 2023; BRASIL, 2021; LACERDA et al., 2019; BRITO et al., 2024).
METODOLOGIA
Trata-se de uma revisão integrativa estruturada da literatura, conduzida com o objetivo de reunir e analisar evidências científicas acerca da eficácia da tafenoquina em dose única na prevenção de recidivas de Plasmodium vivax. A busca bibliográfica contemplou artigos publicados entre 1999 e 2024, utilizando as bases
PubMed/MEDLINE, SciELO, LILACS, além de documentos oficiais do Ministério da Saúde e da Organização Mundial da Saúde (OMS). Foram empregados descritores controlados (DeCS/MeSH) e não controlados, combinados por operadores booleanos, como “tafenoquine”, “Plasmodium vivax”, “relapse”, “clinical trial”, “randomized controlled trial”, “recurrence” e “Brazil”.
Foram incluídos ensaios clínicos randomizados de fase II e III que avaliaram a eficácia da tafenoquina na prevenção de recidivas de P. vivax, estudos observacionais ou de efetividade operacional em contexto real de saúde pública, particularmente no Brasil, além de revisões sistemáticas e narrativas que sintetizaram dados clínicos relevantes sobre a droga. Também foram considerados artigos disponíveis em português, inglês ou espanhol, desde que com acesso integral ao texto.
RESULTADOS E DISCUSSÃO
Propriedades farmacológicas
A tafenoquina é uma 8-aminoquinolina estruturalmente relacionada à primaquina, mas com características farmacológicas que a tornam distinta. Seu principal mecanismo de ação consiste na eliminação dos hipnozoítos hepáticos do Plasmodium vivax, sendo, portanto, um fármaco de cura radical (LACERDA et al., 2019). Diferentemente da primaquina, cuja meia-vida é de aproximadamente 6 horas, a tafenoquina apresenta meia-vida prolongada de cerca de 14 a 17 dias, o que permite sua administração em dose única de 300 mg (WATSON et al., 2024). Além disso, sua ampla distribuição tecidual e o metabolismo hepático via citocromo P450 garantem níveis plasmáticos sustentados, conferindo eficácia comparável à primaquina em regimes prolongados (CHU et al., 2021).
Evidências de eficácia
O ensaio DETECTIVE fase 2b, produzido por Llanos-Cuentas et al. (2014), foi multicêntrico, duplo-cego, de seleção de dose (n=329). Após seis meses, a proporção de pacientes livres de recidiva foi de 89,2% no grupo tafenoquina 300 mg e 91,9% no grupo tafenoquina 600 mg, comparados a 77,3% no grupo primaquina 14 dias e apenas 37,5% no grupo cloroquina isolada.
O ensaio DETECTIVE fase 3, dirigido por Lacerda et al. (2019), incluiu 502 pacientes. Após seis meses, 62,4% dos pacientes que receberam tafenoquina estavam livres de recidiva, contra 27,7% no grupo placebo e 69,6% no grupo primaquina (15 mg/dia por 14 dias).
Em outro estudo de fase 3, Llanos-Cuentas et al. (2019) compararam diretamente a tafenoquina (300 mg dose única) e a primaquina (15 mg/dia por 14 dias), ambos em associação à cloroquina. Após seis meses, 67% dos pacientes no grupo tafenoquina e 72,8% no grupo primaquina permaneceram livres de recidiva.
Mais recentemente, Sutanto et al. (2023) avaliaram a tafenoquina em associação à dihidroartemisinina–piperaquina (DHA-PPQ) em região com resistência à cloroquina. O grupo que recebeu tafenoquina apresentou risco significativamente menor de recidiva em seis meses em comparação ao DHA-PPQ isolado.
Ensaios anteriores já haviam indicado seu potencial anti-hipnozoítico. Walsh et al. (2004) demonstraram que regimes de três doses de tafenoquina preveniam recidivas de P. vivax, enquanto Walsh et al. (1999) já mostravam eficácia em estudos dose-ranging com prevenção significativa de recaídas.
Evidências sobre a administração de tafenoquina no Brasil
Em estudos conduzidos no Brasil, a tafenoquina em dose única demonstrou eficácia promissora na redução de recidivas de Plasmodium vivax em cenários reais. Um projeto retrospectivo com 5.554 casos registrados entre 2021 e 2022 mostrou recorrência livre em 180 dias de 75,8% com tafenoquina, contra 73,4% com primaquina de 7 dias, com destaque para pacientes ≥16 anos com G6PD normal — que apresentaram eficácia de 88,6% até o dia 90 (BRITO et al., 2024). Além disso, o programa piloto TRuST demonstrou viabilidade operacional e potencial para escalar a estratégia de cura radical com tafenoquina e testagem quantitativa de G6PD no SUS (TRuST, 2024). Estudos de modelagem econômica também indicaram que essa abordagem é custo-efetiva em comparação ao regime atual com primaquina (PEIXOTO et al., 2025).
Atualmente, múltiplas iniciativas nacionais sustentam sua adoção programática. A Nota Informativa nº 2/2024 do Ministério da Saúde regulamentou a implementação do esquema com tafenoquina (300 mg) associada à cloroquina, vinculada ao uso do teste semiquantitativo de G6PD como requisito de segurança (BRASIL, 2024a). Desde a incorporação da tafenoquina pelo SUS em junho de 2023, o país vem adotando uma abordagem escalonada e territorialmente ampla: já são 49 municípios e 9 DSEIs atendidos, com quase 3 mil profissionais capacitados até abril de 2025; estados como Roraima e Amazonas assumiram liderança operacional, e Porto Velho já alcançou 87,5% de cobertura nas unidades de tratamento. Esses dados demonstram que o Brasil está efetivamente avançando na estratégia “teste G6PD + tafenoquina dose única”, com ampla aceitação por profissionais e viabilidade operacional nos contextos estaduais e indígenas (AGÊNCIA BRASIL, 2025; VIGILÂNCIA EM SAÚDE DE RORAIMA, 2025; FVS-AM, 2025; REVISTAFT, 2025; AGÊNCIA PARÁ, 2024).
Em síntese, a Tabela 1 apresenta os principais achados dos estudos supracitados, os quais corroboram a efetividade da tafenoquina no tratamento da malária vivax.
Tabela 1. Quadro comparativo dos ensaios clínicos com a tafenoquina
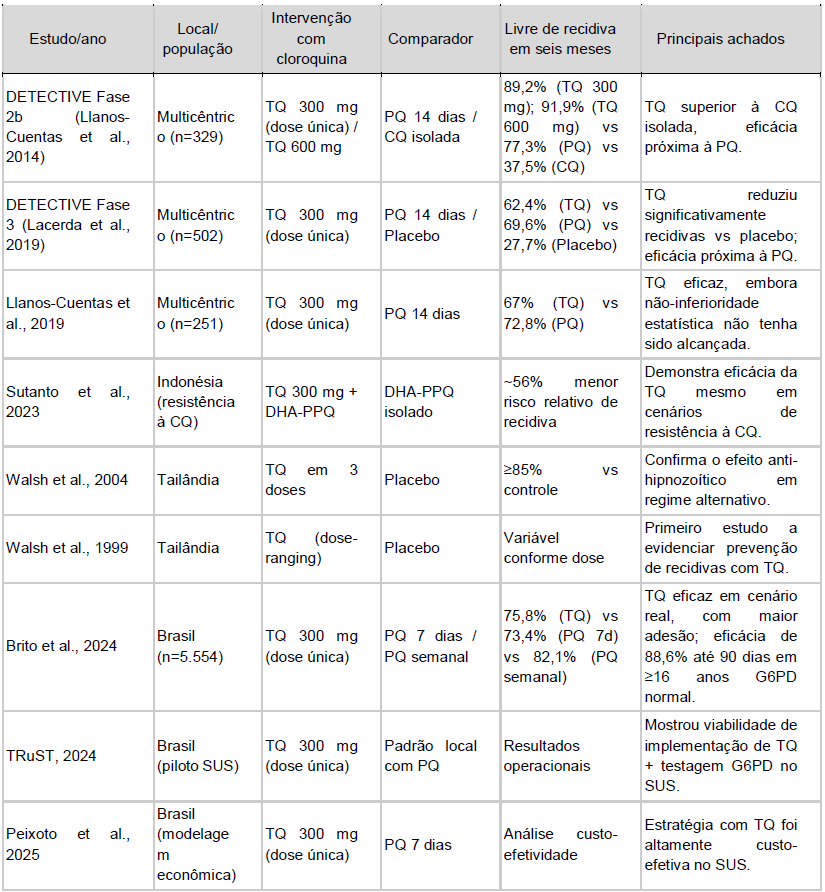
Limitações e efeitos adversos
Apesar da eficácia, os estudos relatam eventos adversos relevantes. No ensaio DETECTIVE fase 3, 5,4% dos pacientes no grupo tafenoquina apresentaram queda de hemoglobina >3 g/dL, contra 1,5% no grupo placebo e 1,6% no grupo primaquina (LACERDA et al., 2019). Esse achado reforça a necessidade de triagem quantitativa de G6PD antes da prescrição, já que a hemólise é o principal risco associado ao uso da tafenoquina e de outras 8-aminoquinolinas.
No estudo de Llanos-Cuentas et al. (2019), eventos hematológicos também foram mais frequentes no braço tafenoquina, incluindo reduções discretas de hemoglobina. Ainda que esses episódios tenham sido autolimitados na maioria dos casos, representam um alerta importante em populações endêmicas com alta prevalência de deficiência de G6PD.
Ensaios de fase II também trouxeram pontos controversos. Fukuda et al. (2017) avaliaram esquemas de tafenoquina em altas doses (1.200 mg divididos em três dias), comparando-os a cloroquina + primaquina. Embora a eficácia inicial tenha sido semelhante, o grupo tafenoquina apresentou clareamento sanguíneo mais lento (82,5h vs 40h), além de maior frequência de trombocitopenia (13%), metemoglobinemia (47,8%) e queratopatia (31,8%), sugerindo riscos importantes quando utilizada em monoterapia.
Estudos de profilaxia também levantaram preocupações. Nasveld et al. (2010) avaliaram a tafenoquina (200 mg semanal) em militares australianos comparada à mefloquina. Embora a eficácia profilática tenha sido equivalente, o grupo tafenoquina apresentou 69 casos de queratopatia, ainda que reversíveis em até um ano. De forma semelhante, Novitt-Moreno et al. (2022) relataram incidência elevada de ceratopatia verticilata (54,5%) e náusea (13%) em regimes prolongados. Esses achados indicam que a vigilância oftalmológica é necessária quando a tafenoquina é utilizada por longos períodos.
Outros estudos apontam que alguns efeitos adversos são dependentes da dose. Chu et al. (2021) destacaram a dor abdominal como efeito adverso dose-dependente em análises de segurança acumuladas. Já Watson et al. (2024), em uma metanálise com dados individuais de pacientes, sugeriram que a dose padrão de 300 mg pode ser insuficiente em determinados perfis de adultos, indicando a necessidade de mais pesquisas sobre dose-resposta.
No cenário brasileiro, o estudo retrospectivo de Brito et al. (2024) reforça a importância da testagem quantitativa de G6PD antes da prescrição, já que, embora a tafenoquina tenha demonstrado eficácia semelhante ou superior à primaquina, a ocorrência de hemólise permanece como fator limitante. Assim, protocolos de farmacovigilância são essenciais para a implementação segura da terapia no Sistema Único de Saúde (SUS).
Em síntese, embora a tafenoquina represente um avanço importante por simplificar o tratamento e reduzir falhas de adesão, a segurança clínica depende diretamente de estratégias robustas de triagem, monitoramento hematológico e oftalmológico, além da definição mais precisa de regimes posológicos ideais em diferentes populações.
CONCLUSÃO
A tafenoquina, administrada em dose única de 300 mg em associação à cloroquina ou a outros esquizonticidas em cenários de resistência, apresenta eficácia consistente na redução de recaídas por Plasmodium vivax. No Brasil, evidências recentes reforçam sua efetividade em condições operacionais, além de demonstrar viabilidade programática e custo-efetividade. Sua principal vantagem reside na simplificação do regime terapêutico, superando barreiras de adesão frequentemente observadas nos esquemas prolongados com primaquina.
Entretanto, a implementação em larga escala requer cautela, uma vez que a segurança do uso da tafenoquina depende da testagem quantitativa da atividade da G6PD e da existência de protocolos robustos de farmacovigilância. Dessa forma, a tafenoquina deve ser entendida como uma alternativa terapêutica inovadora e promissora, com potencial de gerar impacto significativo tanto no nível individual — ao reduzir morbidade e recorrência — quanto no nível coletivo, ao contribuir para o fortalecimento das estratégias de controle e para a meta de eliminação da malária vivax no Brasil.
REFERÊNCIAS
WHO – World Health Organization. World malaria report 2023. Geneva: WHO, 2023. Disponível em: https://globalhealth.org/wp-content/uploads/2023/02/GHBB23MalariaBrief.pdf
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde e Ambiente. Boletim Epidemiológico, volume 56, n. 12, 2025. Disponível em: https://www.gov.br/saude/ptbr/centrais-de-conteudo/publicacoes/boletins/epidemiologicos/edicoes/2025/boletimepidemiologico-volume-56-no-12-26-de-ago.pdf. Acesso em: 13 set. 2025.
SIMÕES, L. R. Recaídas de malária vivax na região amazônica brasileira. 2012. Dissertação (Mestrado em Ciências da Saúde) – Universidade Federal do Acre, Rio Branco, 2012.
BRASIL. Ministério da Saúde. Guia prático de tratamento da malária no Brasil. Brasília: MS, 2010. Disponível em: http://bvsms.saude.gov.br/bvs/publicacoes/guia_tratamento_malaria.pdf. Acesso em: 9 set. 2025.
PEREIRA, E. A. et al. Fatores associados à adesão ao tratamento da malária em áreas endêmicas da Amazônia brasileira. Texto & Contexto – Enfermagem, v. 22, n. 4, p. 1086-1094, 2013. DOI: 10.1590/S0104-07072013000400019.
GAMA, G. E. et al. Fatores que interferem na adesão ao tratamento da malária: percepções de pacientes atendidos na Amazônia. Revista Eletrônica de Enfermagem, v. 16, n. 3, p. 587-594, 2014.
GONÇALVES, M. J. F.; SILVA, R. A.; GUERRA, M. R. Factores condicionantes da adesão ao tratamento da malária: revisão sistemática. Enfermería Global, v. 12, n. 32, p. 302-314, 2013.
LACERDA, M. V. G. et al. Tafenoquina em dose única para prevenir recaída da malária por Plasmodium vivax. The New England Journal of Medicine, v. 380, n. 3, p. 215-228, 2019. DOI: 10.1056/NEJMoa1710775.
BRITO, M. A. et al. Operational effectiveness of tafenoquine and primaquine for the prevention of Plasmodium vivax recurrence in Brazil: a retrospective observational study. The Lancet Infectious Diseases, 2024. Disponível em: https://pubmed.ncbi.nlm.nih.gov/38452779/. Acesso em: 9 set. 2025.
Mayence A, Vanden Eynde JJ. Tafenoquine: A 2018 Novel FDA-Approved Prodrug for the Radical Cure of Plasmodium vivax Malaria and Prophylaxis of Malaria. Pharmaceuticals (Basel). 2019 Jul 30;12(3):115. doi: 10.3390/ph12030115. PMID: 31366060; PMCID: PMC6789594.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde e Ambiente. Boletim Epidemiológico, Número Especial | Nov. 2021. Disponível em: https://www.gov.br/saude/pt-br/assuntos/saude-de-a-a-z/m/malaria/situacaoepidemiologica-da-malaria/boletins-epidemiologicos-de-malaria/boletimepidemiologico-numero-especial-nov-2021-malaria/view
WATSON, J. et al. Radical cure of Plasmodium vivax with tafenoquine: análise de dados individuais. eLife, v. 13, e91283, 2024. DOI: 10.7554/eLife.91283.
CHU, C. S. et al. Tafenoquine and its potential for malaria elimination: evidence and challenges. Expert Opinion on Drug Metabolism & Toxicology, v. 17, n. 2, p. 123-135, 2021. DOI: 10.1080/14740338.2021.1859476.
LLANOS-CUENTAS, A. et al. Tafenoquina mais cloroquina no tratamento e prevenção de recaída da malária vivax (DETECTIVE): estudo multicêntrico, duplocego, randomizado, fase 2b, de seleção de dose. The Lancet, v. 383, n. 9922, p. 10491058, 2014. DOI: 10.1016/S0140-6736(13)62568-4.
LLANOS-CUENTAS, A. et al. Tafenoquina versus primaquina para prevenção de recaída da malária por Plasmodium vivax. The New England Journal of Medicine, v. 380, n. 3, p. 229-241, 2019. DOI: 10.1056/NEJMoa1802537.
SUTANTO, I. et al. Tafenoquine co-administered with dihydroartemisinina– piperaquina for radical cure of Plasmodium vivax malaria: a randomized, placebocontrolled study. The Lancet Infectious Diseases, v. 23, n. 8, p. 1011-1022, 2023. DOI: 10.1016/S1473-3099(23)00213-X.
WALSH, D. S. et al. Randomized trial of 3-dose regimens of tafenoquine for prevention of Plasmodium vivax malaria relapse. Clinical Infectious Diseases, v. 39, n. 8, p. 1095-1103, 2004. DOI: 10.1086/424507.
WALSH, D. S. et al. Randomized dose-ranging study of WR-238605 (tafenoquine) in prevention of relapse of Plasmodium vivax malaria in Thailand. The Journal of Infectious Diseases, v. 180, n. 4, p. 1282-1287, 1999. DOI: 10.1086/315011.
TRuST – Tafenoquine Roll-out Study. Implementação piloto de tafenoquina e testagem quantitativa de G6PD no SUS brasileiro. The Lancet Global Health, 2024. Disponível em: https://www.vivaxmalaria.org/news-events/news/lancet-global-healthpublishes-groundbreaking-results-tafenoquine-roll-out-study. Acesso em: 9 set. 2025.
PEIXOTO, H. M. et al. The cost-effectiveness of tafenoquine following screening with STANDARD™ G6PD screening for the treatment of vivax malaria in the Brazilian Public Health System. The Lancet Regional Health – Americas, v. 51, p. 101216, 2025. DOI: 10.1016/j.lana.2025.101216.
BRASIL. Ministério da Saúde. Nota Informativa nº 2/2024-CEMA/CGHDE/DEDT/SVSA/MS: implementação do teste semiquantitativo de G6PD e da tafenoquina em dose única para cura radical de Plasmodium vivax. Brasília: MS, 2024a. Disponível em: https://www.gov.br/saude/pt-br/centrais-deconteudo/publicacoes/notas-tecnicas/2024/nota-informativa-no-2-2024. Acesso em: 9 set. 2025.
AGÊNCIA BRASIL. Brasil reduz 26% dos casos de malária no primeiro trimestre de 2025. Agência Brasil, 11 abr. 2025. Disponível em: https://agenciagov.ebc.com.br/noticias/202504/brasil-reduz-26-dos-casos-demalaria-no-primeiro-trimestre-de-2025. Acesso em: 9 set. 2025.
VIGILÂNCIA EM SAÚDE DE RORAIMA. CGVS/Sesau realiza treinamento para o uso da tafenoquina no tratamento da malária em Roraima. Boa Vista, 27 mar. 2025. Disponível em: https://vigilancia.saude.rr.gov.br/2025/03/27/cgvs-sesau-realizatreinamento-para-o-uso-da-tafenoquina-no-tratamento-da-doenca-em-roraima/. Acesso em: 9 set. 2025.
FUNDAÇÃO DE VIGILÂNCIA EM SAÚDE DO AMAZONAS (FVS-AM). Municípios do Amazonas iniciam uso da tafenoquina para malária. Manaus, 2025. Disponível em: https://www.fvs.am.gov.br/noticias_view/8890. Acesso em: 9 set. 2025.
REVISTAFT. Retomada na implantação da testagem de G6PD e uso de tafenoquina no tratamento da malária por P. vivax: experiência do município de Porto Velho. Revista F&T, mar. 2025. Disponível em: https://revistaft.com.br/retomada-naimplantacao-da-testagem-de-g6pd-e-uso-de-tafenoquina-no-tratamento-da-malariapor-p-vivax-experiencia-do-municipio-de-porto-velho/. Acesso em: 9 set. 2025.
AGÊNCIA PARÁ. Capacitação profissional aborda novo tratamento em dose única para malária. Belém, ago. 2024. Disponível em: https://www.agenciapara.com.br/noticia/59215/capacitacao-profissional-abordanovo-tratamento-em-dose-unica-para-malaria. Acesso em: 9 set. 2025.
FUKUDA, M. M. et al. Tafenoquine monotherapy in Plasmodium vivax malaria: randomized controlled trial. PLoS ONE, v. 12, n. 11, e0187376, 2017. DOI: 10.1371/journal.pone.0187376.
NASVELD, P. E. et al. Randomized trial of tafenoquine versus mefloquina para profilaxia de malária em militares australianos. Antimicrobial Agents and Chemotherapy, v. 54, n. 9, p. 4085-4091, 2010. DOI: 10.1128/AAC.00331-10.
NOVITT-MORENO, A. et al. Tafenoquine for malaria prophylaxis: safety outcomes. Travel Medicine and Infectious Disease, v. 47, 102293, 2022. DOI: 10.1016/j.tmaid.2022.102293.
1Discente de Medicina do Centro Universitário Aparício Carvalho joycedanttasm@gmail.com http://lattes.cnpq.br/6233031067025574
2Discente de Medicina do Centro Universitário Aparício Carvalho ethelinetorres@gmail.com, http://lattes.cnpq.br/0319450730557544
3Docente do Curso de Medicina Centro Universitário Aparício Carvalho, mestrado e doutorado em Biologia Experimental pela Universidade Federal de Rondônia – UNIR, prof.santos.alcione@fimca.com.br,ORCID: 0000-0001-9476-0761. , http://lattes.cnpq.br/8120484084533828
