REGISTRO DOI: 10.5281/zenodo.7509706
Cinthya Iamille Frithz Brandão de Oliveira
Renato de Andrade Fernandes
Bárbara Letícia da Costa Corrêa
Gabriela Alarcón Alcântara
Resumo
O combate à pandemia causada pelo SARS-CoV-2 está relacionado à elaboração de estratégias farmacológicas para o enfrentamento dessa pandemia. Nesse cenário, diversos fármacos estão sendo utilizados para o tratamento dos pacientes com COVID-19, sendo que muitas classes de medicamentos estão sendo testadas, como antivirais, corticoides, anti-inflamatórios, antiparasitários e antibióticos. Apesar disso, esses fármacos estão sendo questionados em diversos estudos por não causarem uma melhora clínica significativa nos pacientes, e nesse contexto, foi realizada uma revisão sistemática e retrospectiva, utilizando-se busca manual de artigos científicos no Google acadêmico, PubMed, Scielo, periódico CAPES, Cochrane Methodology Register, na Medline, na LILACS, no Google Scholar e na Cochrane Library, no período de julho de 2020 a julho de 2021, com o objetivo de analisar os principais fármacos disponíveis para o tratamento de pacientes com COVID-19, e a eficácia desses medicamentos para esse tratamento, e nesse cenário, os medicamentos analisados foram Remdesevir, Favipiravir, Tocilizumabe, Molnupiravir, Cloroquina, Hidroxicloroquina, Ivermectina, Azitromicina e Dexametasona. Nesse contexto, apesar de alguns desses medicamentos serem relativamente seguros e certos fármacos promoverem melhora clínica de pacientes com COVID-19 em determinados cenários, ainda são necessários mais ensaios clínicos randomizados com esses medicamentos, a fim de analisar os efeitos adversos, interações medicamentosas e eficácia desses fármacos para o tratamento dos pacientes com COVID-19.
Palavras-chave: Farmacologia, COVID-19, pandemia, estratégias farmacológicas, medicamentos, ensaios clínicos, medicina.
Abstract
The fight against the pandemic caused by SARS-CoV-2 is related to the elaboration of pharmacological strategies to face this pandemic. In this scenario, several drugs are being used for the treatment of patients with COVID-19, and many classes of drugs are being tested, such as antivirals, corticosteroids, anti-inflammatory, antiparasitic, and antibiotics. Despite this, these drugs are being questioned in several studies for not causing a significant clinical improvement in patients, and in this context, a systematic and retrospective review was conducted using a manual search of scientific articles in Google academic, PubMed, Scielo, CAPES journal, Cochrane Methodology Register, in Medline, in LILACS, in Google Scholar and in the Cochrane Library, in the period July 2020 to July 2021, with the aim of analyzing the main drugs available for the treatment of patients with COVID-19, and the effectiveness of these drugs for this treatment, and in this scenario, the drugs analyzed were Remdesevir, Favipiravir, Tocilizumab, Molnupiravir, Chloroquine, Hydroxychloroquine, Ivermectin, Azithromycin, and Dexamethasone. In this context, although some of these drugs are relatively safe and certain drugs promote clinical improvement of patients with COVID-19 in certain settings, further randomized clinical trials with these drugs are still needed in order to analyze the adverse effects, drug interactions, and efficacy of these drugs for the treatment of patients with COVID-19.
Keywords: Pharmacology, COVID-19, pandemic, pharmacological strategies, drugs, clinical trials, medicine.
Introdução
O enfrentamento da pandemia causada pelo coronavírus, SARS-CoV-2, está associado ao desenvolvimento de estratégias farmacológicas para o combate a essa pandemia, e como meios para esse combate há medicamentos voltados ao tratamento da infecção causada por esse agente infeccioso, como drogas voltadas à inibição da replicação desse vírus. Nesse cenário, alguns desses fármacos possuem eficácia científica comprovada para outras doenças, e outros seguem sendo questionados quanto a essa eficácia, com intuito de diminuir sinais e sintomas causados pela COVID-19, além da propagação e o número de mortes causadas por esta doença. Nesse contexto, esses medicamentos, ensaios clínicos desses fármacos e análises dessa eficácia podem contribuir para limitar a disseminação de SARS-CoV-2 e diminuir a mortalidade dessa infecção, contribuindo, dessa forma, para esse enfrentamento.
Metodologia
Foi realizada uma revisão sistemática e retrospectiva, utilizando-se busca manual de artigos científicos no Google acadêmico, PubMed, Scielo, periódico CAPES, Cochrane Methodology Register, na Medline, na LILACS, no Google Scholar e na Cochrane Library, no período de julho a outubro de 2020. A estratégia de seleção dos artigos foi baseada nas palavras chaves dos medicamentos selecionados, com a atualização das informações referentes ao mecanismo de ação e respostas terapêuticas relacionadas aos distúrbios respiratórios.
Resultados e Discussão
Com base nos dados publicados durante a pandemia do SARS-CoV-2, várias terapias medicamentosas foram utilizadas com objetivo de desacelerar o avanço do processo infeccioso, evitar complicações decorrentes da infecção e recuperar o paciente acometido pelo vírus. Alguns dos medicamentos mais utilizados no Brasil foram os seguintes:
Remdesivir
Possui atividade antiviral contra o RNA de fita simples viral, de filovírus, pneumovírus, paramixovírus e os coronavírus MERS-CoV e SARS-CoV. Como pró-droga, é metabolizado em sua forma ativa, GS-441524, uma adenina análoga de nucleotídeo que interfere com a atividade da enzima RNA polimerase de RNA dependente, RdRp, o que promove a inibição da síntese do RNA viral, atuando precocemente na infecção e na diminuição dos níveis de RNA viral de maneira dependente da dose, paralela ao comprometimento da carga viral in vitro.¹.
Figura 01: Fórmula química estrutural do Remdesivir
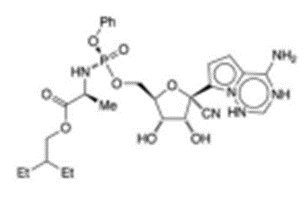
Fonte:https://www.acs.org/content/acs/en/molecule-of-theweek/archive/r/remdesivir.ht ml
Em um experimento de cultura com células Vero E6 símias infectadas com SARS-CoV2, remdesivir foi capaz de inibir a infecção por este vírus. Neste mesmo estudo, os ensaios clínicos de fase 3 mostraram que na concentração de 1,76 µmol, a droga inibe a infecção por esse vírus de células Huh-7 de câncer de fígado humano, e o tratamento profilático em macacos Rhesus 12 horas, após a inoculação do MERS-CoV, proporcionou benefícios clínicos, como a redução da replicação viral no epitélio respiratório e diminuição da ocorrência e gravidade de lesões pulmonares, assim como a prevenção de hemorragia pulmonar e redução dos títulos virais do pulmão em murinos com MERS-CoV.¹ Em testes clínicos iniciais indicou-se que esse medicamento pode reduzir o período de recuperação em adultos hospitalizados, dessa infecção em cerca de 4 dias, sendo superior ao placebo². Trata-se de um medicamento em fase experimental, não estando amplamente disponível.
Em relação à dados farmacocinéticos, considerando que ainda há escassez destas informações, essa droga possui uso intravenoso, normalmente em ambiente intra-hospitalar,³ não atravessa a barreira placentária, possui baixa absorção pelo trato gastrointestinal, e é considerada de baixo risco para uso durante a lactação. No estudo de fase 1, o remdesivir foi considerado seguro para uma dose de 250 mg/kg/dia, com meia-vida intracelular superior a 35 horas, e essa pesquisa demonstrou que o uso desse medicamento em dose única de 200mg seguida de doses de infusão diárias de 100 mg, por 9 a 13 dias, resultou em melhora clínica em 36 dos 53 pacientes, equivalente a 68% destes indivíduos.¹.
Entretanto, o uso de remdesivir não é recomendado em pacientes com taxa de filtração glomerular inferior a 30 ml/min, e possui alguns efeitos adversos, como anemia, hipoalbuminemia, hipocalemia, hiperlipidemia, constipação e síndrome do desconforto respiratório agudo.⁴ Apesar disso, ensaios clínicos mostraram que em um subgrupo de 175 pacientes tratados com esse medicamento, 9 pacientes experimentaram efeitos adversos graves, indicando que esse fármaco é relativamente seguro,¹ e que são necessários futuros estudos para entender melhor a eficácia dessa droga.
Favipiravir
É uma substância derivada da azinecarboxamida e análoga da guanina, que sendo um pró-farmaco é ribosilado e fosforilado intracelularmente para formar o metabólito ativo ribofuranosil-5′-trifosfato, capaz de inibir seletiva e potentemente a enzima RNA polimerase de RNA dependente, RdRp, de vírus de RNA, o que induz mutações neste agente infeccioso e produz assim um vírus com fenótipo não viável. Além da inibição do vírus influenza, este medicamento mostra efeitos inibitórios em flavovírus, filovírus e o SARS-CoV2, e esta droga também é capaz de reduzir significativamente a liberação da citocina inflamatória TNF-alfa,⁵ o que pode controlar efeitos patogênicos causados pelo vírus no pulmão.
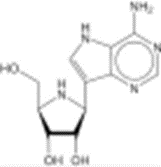
Figura 02: Fórmula química estrutural do Favipiravir
Fonte:https://www.acs.org/content/acs/en/molecule-of-theweek/archive/f/favipiravir.html
Dados dessa droga sobre segurança, eficácia e interações medicamentosas ainda são escassos, uma vez que esse medicamento ainda está em experimentação, em ensaios clínicos de fase 3.⁶ Ensaios clínicos realizados no Japão entre março e maio de 2020, com 89 pacientes, mostraram resultados positivos com o uso dessa medicação nos estágios inicial e médio da infecção por SARS-CoV2, sendo que 55% dos pacientes apresentaram melhora dessa infecção no sétimo dia de tratamento. ⁷ Por outro lado, testes clínicos realizados no Centro Nacional de Biotecnologia da China com 80 pacientes portadores desse vírus mostraram que este fármaco reduz o tempo de melhora para 4 de 11 dias, em casos não graves.⁸.
Quanto à informações relacionadas à farmacocinética dessa droga, estudos com voluntários japoneses saudáveis mostraram que a concentração plasmática inicial máxima desta medicação ocorreu 2 horas após administração oral, e que esse medicamento possui vida útil de 2 a 5,5 horas.⁸ Além disso, esse fármaco tem uma porcentagem de ligação com albumina sérica humana de 65,0%, e sofre metabolismo no fígado principalmente pela Aldeído Oxidase, AO, e parcialmente pela xantina oxidase, produzindo um metabólito oxidativo T-705m1, excretado pelos rins. Em um distinto estudo, a injeção venosa em ratos de 250 mg/kg dessa droga em 1 dia resultou em rápida captação e depuração através do fígado, rins e intestino.⁸.
Todavia, o uso desse fármaco pode causar alguns efeitos adversos, como diarreia leve à moderada, hiperuricemia, aumento das transaminases no sangue, aborto e má-formação fetal, por isso, não é recomendado esse uso em gestantes.⁷ Já em relação à precaução quanto à interações medicamentosas e a esse uso, a dose diária máxima recomendada de acetaminofeno quando combinado com favipiravir é de 3 g,⁸ e estudos in vitro demonstram que moduladores seletivos do receptor de estrogênio, como raloxifeno e tamoxifeno, bloqueadores dos canais de cálcio, como felodipina e verapamil, propafenona, citalopram, amitriptilina e cimetidina são potentes inibidores da AO, portanto esses medicamentos, se em uso com favipiravir, devem ser cuidadosamente monitorizados.⁸ Na tabela a seguir é possível observar medicamentos inibidores de replicação de SARS-CoV2 e as respectivas verificações da eficácia destes fármacos contra esse vírus:
Medicamentos Eficácia contra SARS-CoV2 em testes Remdesivir Verificada Lopinavir Não verificada Ritonavir Não verificada Umifenovir Verificada no uso com outras drogas associadas Favipiravir Verificada
Tocilizumabe
É um anticorpo monoclonal humanizado recombinante dirigido contra o receptor de IL-6 solúvel e ligado à membrana. É indicado para o tratamento de artrite reumatoide, artrite idiopática juvenil, artrite de células gigantes e síndrome de liberação de citocinas por células T receptoras de antígenos quiméricos,5-8 e é uma substância relacionada à terapias direcionadas a citocinas, proteínas envolvidas na resposta inflamatória excessiva associada à infecção por SARS-CoV-2, sendo que essas terapias podem ter um papel importante no embotamento da hiperinflamação e na contenção do dano pulmonar.1,4
Dada a associação de níveis elevados de IL-6 com COVID-19 grave e mortalidade, os bloqueadores de IL-6 parecem ser uma alternativa de tratamento para a infecção por SARS-CoV-2.2-4 Nesse contexto, estudos retrospectivos recentes sugeriram que tocilizumabe pode estar associado a um menor risco de morte ou intubação em pacientes com pneumonia grave por SARS-CoV-2.9-13 Em um desses estudos, um ensaio clínico prospectivo e aberto randomizou pacientes hospitalizados com 18 anos ou mais entre 31 de março e 11 de junho de 2020, com pneumonia por SARS-CoV-2, para receber tocilizumabe ou tratamento padrão em 24 hospitais na Itália.10 Ademais, dezessete desses pacientes de 60 (28,3%) em uso de tocilizumabe e 17 de 63 (27,0%) no grupo de controle apresentaram piora clínica em 14 dias desde a randomização, sendo que dois pacientes no grupo experimental e 1 no grupo controle morreram antes de 30 dias da randomização.
Entretanto, apesar do efeito anti-IL-6 intrínseco do tocilizumabe, que é a redução da febre e o nível de PCR sérico em pacientes com COVID-19,10,14 eventos adversos graves ocorreram nessa pesquisa em 3 pacientes, sendo 2 infecções graves no grupo controle e 1 sangramento do trato gastrointestinal superior com a utilização desse fármaco. Já em relação a efeitos adversos de menor gravidade, ocorreram 21 (17,1%), 14 (23,3%) no grupo tocilizumabe e 7 (11,1%) no grupo controle, sendo que os mais comuns foram aumento do nível de alanina aminotransferase e diminuição da contagem de neutrófilos.9 Também houve limitações nesse estudo, como o tamanho limitado da amostra, e a natureza observacional deste tipo de estudo dificulta a avaliação do efeito de tocilizumabe.
Dessa forma, neste ensaio clínico randomizado, a administração de tocilizumabe em pacientes com pneumonia por COVID-19 e uma razão Pao2/Fio2 entre 200 e 300 mm Hg não reduziu o risco de piora clínica e não foi observado com este utilização nenhum benefício na progressão da doença em comparação com o tratamento padrão.10 Sendo assim, são necessários mais ensaios clínicos randomizados controlados por placebo, cegos, para confirmar os resultados e avaliar as possíveis aplicações de tocilizumabe em diferentes estágios da doença, assim como é necessária a exploração de possíveis aplicações de tocilizumabe em diferentes estágios desta doença, como em pacientes com uma relação Pao2 / Fio2 inferior a 200 mm Hg.14
Molnupiravir
É um pró-fármaco do antiviral ativo ribonucleosídeo análogo de ß-d-N4 hidroxicitidina, e demonstrou o potencial para tratar infecções causadas por vírus de RNA, incluindo SARS-CoV-2, e vírus influenza.1,6 Após distribuição em vários tecidos, este medicamento é convertido, por quinases, em seu correspondente 5-trifosfato, que é um substrato competitivo para vírus de RNA dependente de RNA polimerase, e cuja incorporação na cadeia nascente de RNA viral induz um efeito de erro-catástrofe, que se baseia no aumento da taxa de mutação viral além de um limiar tolerável biologicamente, resultando em comprometimento da aptidão viral e da replicação viral.1
Esse medicamento está em testes clínicos de fase III contra a infecção por SARS-CoV-2, e, de acordo com o Instituto de Ciências Biomédicas da Georgia State University, em 24 horas, o molnupiravir suprime completamente a transmissão do vírus, inibe o progresso do paciente portador dessa infecção para doença grave e, dessa forma, encurta a fase infecciosa desse vírus.5 Além disso, em furões, foi altamente eficaz no bloqueio da transmissão de SARS-CoV-2, em uma dose terapêutica de 5 mg/kg, e demonstrou atividade in vitro contra a SARS-CoV-2 em humanos, a partir de culturas de células epiteliais das vias aéreas.3,7
Outrossim, a exposição plasmática adequada do molnupiravir para ser eficaz no bloqueio da transmissão de SARS-CoV-2 é alcançada, em humanos, em doses entre 200 e 800 mg, e foi bem tolerado nessas doses quando administrado 2 vezes ao dia, por 5 dias, e em doses únicas até 1600 mg.4 Além disso, esse fármaco pode ser administrado de forma oral ou intravenosa, e, em ensaios clínicos, possuiu rápida absorção, assim como meia-vida intracelular de 3 horas em células Huh-7, uma linha de células de fígado humano.2
Entretanto, o uso desse medicamento pode causar alguns efeitos adversos, como cefaleia, dor orofaríngea, dor nas extremidades, diarreia, e também podem ocorrer com esse uso, em menor frequência, erupção cutânea, troncular, maculopapular e pruriginosa.4 Apesar disso, em estudos com esse fármaco, não houve eventos adversos graves ou tendências de aumento da gravidade dos eventos adversos, com doses mais altas de molnupiravir.4,5
Cloroquina e hidroxicloroquina
A cloroquina é uma forma acidotrópica de amina da quinina que foi sintetizada na Alemanha pela Bayer em 1934 , e este medicamento em conjunto com seu análogo hidroxicloroquina (HCQ), ambos 4-aminoquinolinas, têm sido amplamente utilizados no tratamento da malária e para doenças autoimunes como artrite reumatóide (AR), lúpus eritematoso sistêmico (LES), devido às propriedades imunomoduladoras e antitrombóticas destas drogas, e o tratamento com esses medicamentos foi proposto para vários vírus em humanos, incluindo o Sars-Cov-2. A hidroxicloroquina difere da cloroquina pela presença de um grupo hidroxil no final da cadeia lateral: o substituinte N-etil é βhidroxilado, e, embora o mecanismo de ação dessas medicações contra a SARS-CoV-2 não tenha sido totalmente elucidado, acredita-se que esses agentes podem impedir a glicosilação terminal de seu receptor de entrada funcional, receptor da enzima conversora de angiotensina 2, inibindo assim a entrada viral.
A hidroxicloroquina está atualmente disponível apenas na forma de comprimido administrado por via oral, disponível em 200 mg, a maioria dos estudos concluiu que as concentrações máximas dessa droga são observadas dentro de 3–5 h, e a hidroxicloroquina apresenta padrões semelhantes à cloroquina quanto à distribuição nos tecidos, sendo que esses medicamentos demonstraram se concentrar bastante nos pulmões, rins, fígado e baço em modelos animais. Além disso, a excreção dessa droga é feita por via renal e com uma meia-vida de eliminação terminal média (± SD) de 32 (± 9) dias (Tett et al.,1989).
Embora os efeitos adversos mais comuns da hidroxicloroquina sejam de natureza gastrointestinal, as toxicidades ocular e cardíaca são indiscutivelmente as mais preocupantes, e efeitos adversos oculares associados incluem retinopatia, alterações da córnea e diminuição da acuidade visual; no entanto, eles são mais comumente associados ao uso de longo prazo.
Até agora, os dados clínicos publicados sobre essas medicações são limitados e referem-se apenas a estudos clínicos pequenos, mal controlados ou não controlados. Gautret et al (2020) realizaram um protocolo de braço único com 26 pacientes recebendo 600 mg de HCQ diariamente (200 mg por três vezes ao dia) e 16 pacientes controle, e vinte casos tratados neste estudo, mostraram uma redução significativa da carga viral após 6 dias de internação em comparação com os controles, e uma duração média de carga viral muito menor daquela relatada na literatura para pacientes não tratados. Outrossim, um estudo randomizado realizado por Chen et al (2020) comparou o uso de hidroxicloroquina na dose de 400mg/dia por 5 dias mais tratamento convencional e observou uma redução do tempo da recuperação e melhora da pneumonia na Tomografia Computadorizada (TC) de tórax no grupo de HCQ.
Dessa forma, não apenas a eficácia clínica, mas também o regime de dosagem ideal, o nível terapêutico, a duração do tratamento e a farmacocinética em pacientes com diferentes graus de gravidade da doença são incertos e, atualmente, não existem dosagens padrão ou duração do tratamento para o tratamento de pacientes com COVID-19. É necessário considerar que a cloroquina pode causar torsades de pointes e cardiotoxicidade e, portanto, o uso desse medicamento não é recomendado em associação com outras drogas.
Ivermectina e Azitromicina na COVID-19
A ivermectina é um agente semissintético derivado de um grupo de substâncias naturais, as avermectinas, obtidas a partir de um microrganismo actinomicético (Streptomyces avermitilis), utilizada no tratamento de infecções como a filariose, ascaridíase, escabiose, e é aprovada pela FDA (Gonzalez Canga et al., 2008), sendo que essa medicação atua nas aberturas dos canais iônicos de cloro, nos invertebrados, e pelo aumento da condutância ao íon cloro, levando à hiperpolarização da célula, paralisação muscular e morte do parasita, e os efeitos adversos dessa droga incluem erupções cutâneas e prurido, mas, em geral, o fármaco é muito bem tolerado.
Após a administração oral da ivermectina, as concentrações plasmáticas são aproximadamente proporcionais à dose, e a concentração plasmática máxima é atingida em aproximadamente quatro horas depois da ingestão, além de que sua meia-vida plasmática é de 22-28 horas nos adultos, com volume aparente de distribuição de aproximadamente 47 litros. Também, a metabolização é hepática e a maior concentração tissular é encontrada no fígado e no tecido adiposo, e a excreção dos produtos dessa metabolização é, principalmente, por meio de fezes em um período estimado de 12 dias.
Quanto à sua utilização contra a COVID-19, uma pesquisa realizada por Caly et al (2020) evidenciou sua atividade antiviral, em teste in vitro, contra o SARS-CoV-2, e relata-se que a ivermectina auxilia na redução da replicação viral desestabilizando a importina heterodímera (IMP) α/β1 30 que se liga à proteína de carga do vírus e o move para dentro do núcleo da célula hospedeira. Assim, ao reduzir o processo de entrada do vírus na célula, a resposta inata celular melhora, sendo que esses resultados, em 48 horas, mostraram um efeito na inibição da replicação viral em até 5.000 vezes, mas, apesar desses resultados promissores, existem poucas evidências em relação à sua atividade in vivo.
Em um estudo internacional, multicêntrico, observacional de caso-controle procurou-se avaliar a eficácia clínica do uso de ivermectina em pacientes com COVID-19. Ao total, foram coletados dados de 704 pacientes que fizeram uso de ivermectina e 704 pacientes no grupo controle, e a dose média de ivermectina utilizada foi de 150 mcg/kg, e no estudo, a taxa de mortalidade foi menor no grupo que recebeu ivermectina. Destacou-se que esses resultados colocam a ivermectina como um agente potencial para o tratamento de Covid-19, inclusive em pacientes em uso de ventilação mecânica, entretanto, vale ressaltar que se trata de um estudo observacional e que, assim, não se adequaria estabelecer uma relação de causa e efeito. Além disso, Ootro estudo de aumento escalonado de dose, duplo-cego, controlado por placebo avaliou a segurança e farmacocinética da Ivermectina administrada em doses mais altas e / ou mais frequentes do que as atualmente aprovadas para uso humano e evidenciou que a ivermectina é geralmente bem tolerada com doses mais altas e regimes mais frequentes (Guzzo, et al.; 2002)
Outro fármaco em evidência para o tratamento da COVID-19 é a azitromicina, e os estudos acerca desse terápico geralmente o avaliam em associação com outros medicamentos, como a hidroxicloroquina ou a ivermectina, sendo que esse medicamento é um antibiótico bacteriostático de amplo espectro (bactérias gram-negativas e gram-positivas) do grupo dos macrolídeos – ou ainda um azalídeo segundo alguns autores -, cuja estrutura difere da eritromicina porque seu anel de lactona contém um átomo de nitrogênio.
O mecanismo de ação desse medicamento ocorre através da inibição da síntese proteica dependente de RNA, através da ligação em receptores localizados na porção 50S do ribossomo, particularmente na molécula 23S do RNA, impedindo, assim, as reações de transpeptidação e translocação, e estudos alegam ainda a capacidade da azitromicina de reduzir a energia celular nas mitocôndrias e o seu efeito anti-inflamatório.
Após a administração oral, esse medicamento é amplamente distribuído pelo corpo; a sua biodisponibilidade é de aproximadamente 37% e o tempo necessário para alcançar os picos de concentração plasmática é de duas a três horas. Outrossim, essa droga possui meia-vida plasmática de dois a quatro dias, e pode ser administrada no paciente a qualquer hora do dia, além de possuir eliminação primariamente por via hepática, sendo que pequena quantidade é encontrada na urina
Alguns autores comentam sobre o uso da azitromicina (AZT) no tratamento da COVID-19 à medida que sua ação reduz a produção de interleucina-6 (IL-6) e atua como imunomodulador ao promover a produção de anticorpos (imunoglobulinas) in vitro, e assim poderia ser modificadora de infecções virais graves; novos estudos demonstraram que essa droga é capaz de aumentar o pH das células hospedeiras e reduzir os níveis de furina e assim dificultar os processos de entrada, replicação e dispersão do SARS-CoV-2. Entretanto, embora existam esses estudos, o mecanismo da AZT contra o SARS-CoV-2 não está claro. Além disso, sua depuração é reduzida em pacientes com insuficiência renal grave, e tem o risco de prolongar o intervalo QT, com probabilidade de aumento da arritmia ventricular (torsade de pointes), e por essa razão deve-se ter cautela ao combinar-se com outras drogas que também alteram o intervalo QT, como cloroquina e hidroxicloroquina (HCQ).
Contudo, os estudos reiteram que não deve ser usada HCQ em associação com AZT, e não recomendam o uso de AZT até que resultados de ensaios clínicos controlados randomizados, duplo cego, evidenciem seus benefícios (Choudhary et al., 2020). Já em junho de 2020, publicou-se na Revista Brasileira de Terapia Intensiva, diretrizes para o tratamento farmacológico da COVID-19, e seus resultados evidenciaram que não havia indicação para uso de rotina de hidroxicloroquina, cloroquina, azitromicina, lopinavir/ritonavir, corticosteroides ou tocilizumabe no tratamento da COVID-19.
Aqueles que receberam hidroxicloroquina, azitromicina, ou ambos, apresentaram maior probabilidade do que aqueles que não receberam nenhum medicamento de possuir: diabetes, obesidade, frequência respiratória < 22 IR/min, achados anormais nos exames de imagem torácica, saturação de O2 < 90% e aspartato aminotransferase > 40 U/L. Nesse contexto, os pacientes que receberam hidroxicloroquina isoladamente apresentaram maior prevalência de doença pulmonar crônica (25,1%) e doenças cardiovasculares (36,5%), e aqueles que receberam hidroxicloroquina + azitromicina, apresentaram doença clinicamente mais grave.
Em uma primeira análise, não foram encontradas diferenças significativas na mortalidade entre os pacientes que receberam hidroxicloroquina + azitromicina, hidroxicloroquina sozinha ou azitromicina sozinha, em comparação com os que não receberam nenhum dos medicamentos. Isso também foi observado nos modelos de regressão logística para análise dos achados anormais de ECG, entretanto, em relação ao evento de parada cardíaca, sua probabilidade foi maior em pacientes que receberam hidroxicloroquina + azitromicina comparado aos demais grupos; e em pacientes que tomaram hidroxicloroquina isoladamente se comparado aos que tomaram apenas azitromicina.
Há uma maior frequência, nesses estudos, de parada cardíaca em pacientes que receberam hidroxicloroquina + azitromicina, e as pesquisas também confirmaram maior mortalidade de infecção por SARS-CoV-2, associada ao sexo masculino; a condições preexistentes como hipertensão, obesidade e diabetes, à disfunção hepática e renal. No entanto, a interpretação desses achados pode ser limitada pelo desenho observacional do estudo.
Nesse cenário, essas pesquisas demonstram resultados promissores da ivermectina e azitromicina nos estudos in vitro, todavia, é muito importante avaliarmos a eficácia dos medicamentos in vivo e de forma controlada no contexto da pandemia. Além disso, relevantemente, devemos considerar os efeitos colaterais dos seus usos, especialmente a azitromicina – distúrbios gastrintestinais, renais e aumento do intervalo QT. Dessa forma, é necessária a realização de mais estudos que acumulem evidências e que sejam validados pelos pesquisadores por sua acurácia dos métodos utilizados – uso de placebo, teste duplo cego, estudos multicêntricos, quantidade de amostras/pacientes, análise de resultados.
Dexametasona
É um corticosteróide de efeitos anti-inflamatórios e imunossupressores que são aproximadamente 30 vezes mais potente que o cortisol, e quanto ao mecanismo de ação desse fármaco, no mecanismo genômico, há a ligação do glicocorticoide (GC) ao seu receptor citoplasmático, o receptor de glicocorticoide (RG), que é um ligante regulado pelo fator de transcrição da superfamília dos receptores nucleares, sendo que esses receptores ativam ou reprimem a expressão de milhares de genes. Essa regulação pelo processo conjunto de metilação do DNA e a deacetilação da histona, através da ação das histonas deacetilases (HDACs) ativadas por esses receptores, levam ao silenciamento do gene através de sinais que compactam o DNA em torno da histona, ocultando as áreas de ligação, e estima-se que os GC regulem diretamente de dez a cem genes por célula, e indiretamente, através da interação com fatores de transcrição e coativadores.
Já os dois mecanismos principais de ações não-genômicas dos GC estariam associados à membrana plasmática, aos canais iônicos e à entrada do cálcio no interior da célula, sendo que os sinais não-genômicos podem modular a transcrição nuclear por diferentes mecanismos, incluindo alterações na fosforilação de moléculas importantes de sinalização nuclear, e por meio da sua atuação ,essa medicação é considerada potencial tratamento para pacientes com COVID-19 submetidos a suporte respiratório, principalmente em casos de pneumonia com hiper inflamação e de síndrome do desconforto respiratório agudo (SDRA).
Os benefícios da dexametasona nesse contexto são devidos provavelmente às propriedades imunossupressoras desse medicamento, e essa droga regula não só negativamente os genes associados ao receptor de células B e a sinalização do receptor Toll-like 7, como também positivamente a citocina anti-inflamatória IL-10 ; atuam nas células T para amortecer a sinalização entre seus receptores e a expressão de citocinas; entre outros, além de inibirem a produção de citocinas pró-inflamatórias (IL-1, TNF e IL-6), quimiocinas e outros mediadores solúveis, como a prostaglandina E 2, leucotrienos e histamina, que atuam na vasculatura para promover vasodilatação e recrutamento de leucócitos. A atividade da droga no tratamento de SARS – Cov2 também pode ser atribuída às interações inibitórias entre receptores intracelulares de glicocorticóides (GRs) e os fatores de transcrição NF-κB e AP-, pois servem como ‘centros’ em os terminais de várias vias de sinalização, incluindo receptores Toll-like, de citocinas, Fc e de células B e T.
O estudo RECOVERY (Horby, P. et al,2020) analisou o uso de dexametasona oral de 6 mg, aplicada uma vez ao dia, e essa quantidade tem provável intuito de complementar a atividade do cortisol endógeno para suprimir a imunopatologia associada a COVID-19, enquanto evita os efeitos adversos da terapia com altas doses; e apesar dessa droga diminuir mortalidade em 28 dias entre aqueles que estavam recebendo ventilação mecânica invasiva ou oxigênio isolado, não houve um efeito claro da dexametasona entre os pacientes que não estavam recebendo suporte respiratório ,ou seja, os resultados são por hora, apenas significativos em enfermos gravíssimos.
A dexametasona via oral é rápida e completamente absorvida pelo trato gastrointestinal e liga-se à albumina em 65 a 90%, e atinge o efeito máximo após administração oral em 1 a 2 horas e sua ação dura 1,25 a 1,5 dias. Além disso, a meia-vida dessa medicação é de 150 a 270 minutos, e a meia-vida biológica (tecidual) é de 24 a 72 horas, e esse medicamento após a metabolização hepática é excretado pela urina, sendo que quase todos os metabólitos são excretados em 72 horas. Outrossim, essa droga é considerada um corticóide de ação lenta, e a medicação também pode ser utilizada de forma injetável (intramuscular) aplicada desde casos de síndrome inflamatória em infecções graves.
Por fim, quanto aos efeitos adversos, tratamentos curtos, por apenas uma semana, não costumam provocar esses efeitos adversos relevantes, dessa forma, os efeitos colaterais são mais extensos quando a dexametasona é administrada na forma oral ou intravenosa, por longos períodos, sendo que os principais efeitos adversos são obesidade, síndrome de Cushing, diabetes mellitus, hipertensão arterial, imunossupressão, edema, alterações menstruais, doenças do trato gastrintestinal e infertilidade.
Considerações finais
Diversas classes de medicamentos foram utilizadas para o tratamento de pacientes com COVID-19, apesar disso, até o momento, os fármacos testados e analisados no estudo, Remdesevir, Favipiravir, Tocilizumabe, Molnupiravir, Cloroquina, Hidroxicloroquina, Ivermectina, Azitromicina e Dexametasona não se mostraram estatísticamente eficazes na profilaxia da doença, além disso, não foi encotrado um medicamento com ação antiviral efetiva para o enfrentamento do SARS-CoV-2. Nesse contexto, apesar de alguns desses medicamentos serem relativamente de uso seguro, e certos fármacos promoverem melhora clínica de pacientes com COVID-19 em determinados cenários, são necessários futuros ensaios clínicos randomizados com esses medicamentos, a fim de analisar os efeitos adversos, interações medicamentosas e eficácia desses fármacos para o tratamento dos pacientes com COVID-19.
Referências
1. Borba MGS, Val F de A, Sampaio VS, et al (2020) Chloroquine diphosphate in two different dosages as adjunctive therapy of hospitalized patients with severe respiratory syndrome in the context of coronavirus (SARS-CoV-2) infection: preliminary safety results of a randomized, double-blinded, phase IIb clinical trial. 2020.
2. CAI, Qingxian et al. Experimental Treatment with Favipiravir for COVID-19: An Open-Label Control Study. Elsevier, [S. l.], p. 2-5, 16 de abril de 2020.
3. Chen J, Liu D, Liu L, et al. A pilot study of hydroxychloroquine in treatment of patients with common coronavirus disease-19 (COVID-19). Journal of Zhejiang University 2020; In Press.
4. CHEN, Xiao-Ping et al. Favipiravir: Pharmacokinetics and Concerns About Clinical Trials for 2019-nCoV Infection. Clinical Pharmacology & Therapeutics, [S. l.], p. 1-6, 1 de agosto de 2020.
5. Guaraldi G, Meschiari M, Cozzi-Lepri A, et al. Tocilizumabe em pacientes com COVID-19 grave: um estudo de coorte retrospectivo. The Lancet Rheumatology. 2020.
6. Gautret P., Lagier J.C., Parola P., et al. Clinical and microbiological effect of a combination of hydroxychloroquine and azithromycin in 80 COVID-19 patients with at least a six-day follow up: a pilot observational study. Travel Med. Infect. Dis. 2020;(April (11))
7. Gautret et al. (2020) Hydroxychloroquine and azithromycin as a treatment of COVID‐19: results of an open‐label non‐randomized clinical trial. International Journal of Antimicrobial Agents – In Press 17 March 2020.
8. Heidary F, Gharebaghi R. Ivermectin: a systematic review from antiviral effectsto COVID-19 complementaryregimen. Received: 21 April 2020 / Revised: 5 May 2020 / Accepted: 17 May 2020. The JournalofAntibiotics.
9. Leon Caly Kylie L C M, Druce J D. A droga ivermectina aprovada pela FDA inibe a replicação da SARS-CoV-2 in vitro – Volume 178, Junho 2020, 104787Junho 2020.
10. MÉDICOS SEM FRONTEIRAS. DEXAMETHASONE injectable. Clinical guidelines -Diagnosis and treatment manual, [s. l.], 2020.
11. Morrisette, T., Lodise, T.P., Scheetz, M.H. et al. The Pharmacokinetic and Pharmacodynamic Properties of Hydroxychloroquine and Dose Selection for COVID-19: Putting the Cart Before the Horse. Infect Dis Ther (2020).
12. PAINTER, Wendy et al. Human safety, tolerability, and pharmacokinetics of molnupiravir, a novel broad spectrum oral antiviral agent with ativity against SARS-CoV-2. Antimicrobial Agents and Chemotherapy, [S.I.], p. 1-19, 1 de março de 2021.
13. Pani, A et al. “Macrolides and viral infections: focus on azithromycin in COVID-19 pathology.” International journal of antimicrobial agents, 106053. 10 Jun. 2020.
14. Price CC, Altice FL, Shyr Y, et al. Tratamento com tocilizumabe para a síndrome de liberação de citocinas em pacientes com COVID-19 hospitalizados: sobrevida e resultados clínicos. Chest. Publicado em 15 de junho de 2020.
15. STERNBERG, Ariane et al. Candidate drugs against SARS-CoV-2 and COVID-19. Elsevier, [S. l.], p. 2-7, 22 de abril de 2020.
16. WANG, Yeming et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. The Lancet, [S. l.], p. 2-9, 16 de maio de 2020.
