REGISTRO DOI: 10.69849/revistaft/ra10202511042356
Carla Regina Ribeiro; Cadma da Silva Pereira; Cristhiane Taimara Haito; Eliane Gabriel de Lima Negraes; Denise Cristina Vargas Albuquerque; Daniela Falcão Nobre; Rafaela Rodrigues Gomes Alencar; Fernanda Kincheski de Almeida; Marcela Cristina Borges dos Santos; Jessica Ribeiro Martins Lanis
RESUMO
A analgesia neonatal é o manejo da dor, enquanto a sedação é a diminuição da atividade e ansiedade, que pode levar à amnésia, mas não elimina a dor. Ambos são usados na UTI neonatal para aliviar o desconforto durante procedimentos, ventilação mecânica ou após cirurgias. O manejo é complexo e deve considerar fatores como uso de escalas de avaliação da dor, terapia farmacológica e não farmacológica, e os potenciais efeitos a longo prazo. O tratamento da dor no recém-nascido consiste em medidas não-farmacológicas (sucção não-nutritiva, glicose) e farmacológicas (analgésicos não-opióides, opióides e anestésicos locais). A sedação em recémnascidos é produzida por fármacos que agem diminuindo a atividade, a ansiedade e a agitação do paciente, podendo levar à amnésia de eventos dolorosos ou nãodolorosos. A sedação pode ser feita pela administração de hidrato de cloral, barbitúricos, propofol e benzodiazepínicos. Palavras-chave: Analgesia e sedação neonatal, dor neonatal, sedação neonatal, analgesia neonatal.
ABSTRACT
Neonatal analgesia is pain management, while sedation is the reduction of activity and anxiety, which can lead to amnesia but does not eliminate pain. Both are used in the NICU to relieve discomfort during procedures, mechanical ventilation, or after surgery. Management is complex and must consider factors such as the use of pain assessment scales, pharmacological and non-pharmacological therapy, and potential long-term effects. The treatment of pain in newborns consists of non-pharmacological measures (non-nutritive suction, glucose) and pharmacological measures (non-opioid analgesics, opioids and local anesthetics). Sedation in newborns is produced by medications that affect the patient’s activity, anxiety and improvement, which can lead to amnesia for painful or non-painful events. Sedation can be achieved by administering chloral hydrate, barbiturates, propofol and benzodiazepines. Keywords: Neonatal analgesia and sedation, neonatal pain, neonatal sedation, neonatal analgesia.
INTRODUÇÃO
Dor é uma qualidade inerente da vida, que aparece precocemente na ontogenia, para servir como um sistema de sinalização para o dano tecidual. As sinalizações incluem respostas comportamentais e fisiológicas que são consideradas como bons indicadores da dor. Para as crianças prematuras, esses indicadores precisam ser avaliados por outros”
Anand and Craig
Cada RN internado em UTI recebe de 50 a 150 procedimentos potencialmente dolorosos ao dia e RN com peso menor que 1.000 g sofrem cerca de 500 ou mais intervenções dolorosas ao longo de sua internação. Conforme “Tanuri et al…2016”
DEFINIÇÕES:
DOR: Experiência desagradável de caráter emocional ou sensorial associada a lesão tecidual.
SEDACAO: Diminuição do grau de consciência varia em intensidade: ansiólise, sedação moderada, sedação profunda e anestesia geral.
ANALGESIA: Diminui ou elimina a percepção de dor. Conforme “Tanuri et al…2016”
MANIFESTAÇÕES ORGÂNICAS:
Importante frisar, que no período neonatal, os estímulos dolorosos se manifestam em múltiplos órgãos e sistemas fisiológicos. Tais alterações podem ocasionar aumento da morbidade e mortalidade neonatal, e evolução clínica desfavorável. Conforme “Tanuri et al…2016”
As manifestações sistêmicas da dor no período neonatal são as seguintes:
- Sistema cardiovascular: aumento da frequência cardíaca e pressão arterial sistólica e diastólica e variação de pressão intracraniana;
- Sistema respiratório: elevação do consumo de oxigênio, queda na saturação de oxigênio e alteração na relação ventilação/perfusão; • Sistema digestivo: diminuição da motilidade gástrica;
- Alterações hormonais: perante dor intensa ocorre grande liberação de adrenalina, corticosteroides, glucagon, hormônio de crescimento, supressão da produção de insulina, retenção de hormônio antidiurético e hipercoagulabilidade, tanto durante como após o episodio doloroso. Conforme “Tanuri et al…2016”
As respostas comportamentais a dor também vem sendo presenciadas no período neonatal, destacando-se o choro, gemido, a movimentação da face, a atividade corporal e o estado do sono e vigília, e logicamente a irritabilidade. Conforme “Tanuri et al…2016”
O Choro ou gemidosugestivo de dor pode ser reconhecido facilmente pelos profissionais da equipe, bastando apenas, poucos segundos para tal percepção, não necessariamente precisem ser treinados. Conforme “Tanuri et al…2016”
ATIVIDADE MOTORA CORPORAL:
Os neonatos a termo e pré-termo na grande maioria das vezes respondem a procedimentos dolorosos com flexão e/ou adução de membros superiores e inferiores e arqueamento do tronco e do pescoço, associados a caretas, choro ou gemidos. Conforme “Tanuri et al…2016”
Salienta-se, que o estado do sono e vigília, ou seja, a redução do sono REM e a indisponibilidade visual e auditiva para com a mãe apresentadas pelo neonato após sofrer um estimulo doloroso tem sido interpretadas como um mecanismo de fuga do meio ambiente provocador do estimulo doloroso. Conforme “Tanuri et al…2016”
Os efeitos acumulativos dos estímulos dolorosos, frente as respostas fisiológicas e comportamentais causadas por punções venosas, aspiração traqueal, punções capilares, procedimentos de enfermagem e ventilação mecânica podem determinar ainda o aparecimento ou o agravamento de lesões neurológicas, tais como hemorragias intraventriculares e leucomalácia periventricular. Conforme “Tanuri et al…2016”
AVALIAÇÃO DA DOR:
Conforme, bem explicitado acima, apesar de parecer difícil diagnosticar um RN com dor, esse mesmo RN da todas as dicas apontando para o profissional por meio de suas reações de resposta fisiológica hormonal e sensitiva desencadeado pelo sistema nervoso o caminho para que seja tomada as medidas para o alivio da dor diante dos procedimentos potencialmente dolorosos. Conforme “Tanuri et al…2016”
A avaliação da dor na população neonatal não é tarefa fácil; a natureza subjetiva da experiência dolorosa e a existência de poucos instrumentos confiáveis, validos e com aplicabilidade clinica para mensurar a presença e a intensidade da dor são barreiras difíceis de transpor, porém, não impossível de diagnosticar. Conforme “Tanuri et al…2016”
Os recém-nascidos, mesmo os prematuros, encontram-se aptos do ponto de vista neurológico para sentir dor. Para avaliar e reduzir a dor do neonato, deve-se utilizar instrumentos validados, de maneira consistente, durante todo o período de analgesia. Conforme “Tanuri et al…2016”
É consenso que a avaliação objetiva da dor no RN deve ser feita por meio de escalas que englobem vários parâmetros e procurem uniformizar os critérios de mensuração das variáveis. Assim, tais critérios devem ser repetidos regularmente, de forma sistemática e protocolar. Entre as inúmeras escalas de avaliação da dor do RN descritas na literatura, varias podem ser aplicadas na pratica clinica de forma simples e didática. Conforme “Tanuri et al…2016”
NIPS (NEONATAL INFANTPAINSCALE)
A NIPS (Escala de Avaliação de Dor no RN e no Lactente) e composta por cinco parâmetros comportamentais e um indicador fisiológico, avaliados antes, durante e após procedimentos invasivos agudos em RN a termo e pré-termo. A maior dificuldade reside na avaliação do parâmetro choro em RN intubados nesse caso; dobra-se a pontuação da mimica facial, sem avaliar o item choro. A escala deve ser aplicada sempre que se registrem os sinais vitais. Conforme “Tanuri et al…2016”
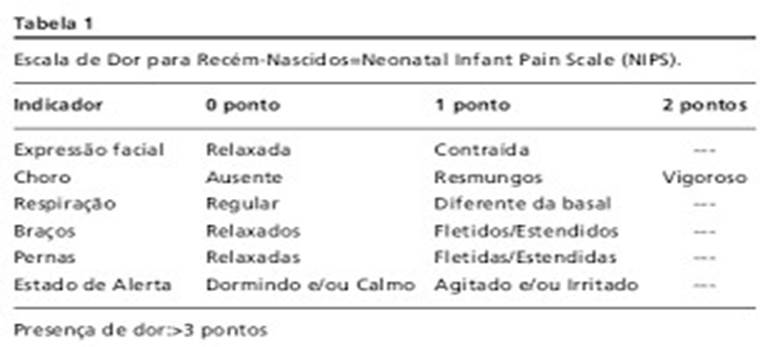
No mais, e na mesma toada, podemos lançar mão de outros parâmetros e escalas.
NFCS (NEONATAL FACIAL CODING SYSTEM)
Devemos aplicar a escala NFCS de acordo com as situações abaixo:
- Pontuação da NIPS > 3;
- Recém-nascidos submetidos a cirurgia de qualquer porte;
- Pacientes submetidos a drenagem torácica;
- Neonatos submetidos a intubação traqueal e ventilação mecânica;
- Pacientes submetidos na flebotomia e/ou inserção de cateter percutâneo; • Recém-nascidos com fraturas ósseas;
- Neonatos com enterocolite.

TRATAMENTO DA DOR NO RECÉM-NASCIDO
Tratamento Não-Farmacológico
Uso de Sucção Não-Nutritiva
Pode ser utilizada em pequenos procedimentos. Embora haja controvérsias a respeito do uso da chupeta em unidades neonatais devido a sua associação a um possível desestímulo ao aleitamento materno, a sucção não-nutritiva, em pacientes prematuros e muito manipulados, parece ser de grande utilidade na organização neurológica e emocional do recém-nascido após o estímulo agressor, diminuindo as repercussões fisiológicas e comportamentais. Assim, acredita-se que o seu uso deva ser estimulado de maneira seletiva em populações específicas de recém-nascidos. Constitui-se em medida coadjuvante para o tratamento da dor do recém-nascido, parecendo não apresentar propriedades analgésicas intrínsecas. Tudo isso, segundo“Gaspardo et al…2005”
Solução Glicosada
Nos últimos anos, vem-se discutindo a utilização da água com açúcar como analgésico. Demonstrou-se, em modelos animais, que o efeito analgésico da glicose pode ser revertido com antagonistas de opióides, o que sugere um mecanismo de ação envolvendo a liberação de endorfinas. A revisão do Cochrane Group mostra redução significativa dos indicadores de dor quando a glicose foi usada como analgésico em recém-nascidos prematuros e de termo submetidos à coleta de sangue. O efeito mais consistente é a redução do tempo total de choro. Poucos trabalhos consideram efeitos adversos e ressaltam que esses são mínimos, como a diminuição temporária de saturação da hemoglobina pelo oxigênio. Não existe um consenso sobre a dose adequada de glicose a ser usada (0,012 a 0,12 g) e doses repetidas parecem ser mais eficazes que uma dose única. Além disso, parece haver sinergismo entre o uso de chupetas (sucção não-nutritiva) com a glicose. Assim, é possível recomendar o emprego clínico de soluções glicosadas por via oral, cerca de um a dois minutos antes de pequenos procedimentos, como punções capilares, venosas ou arteriais. Tudo isso, segundo“Gaspardo et al…2005”
Tratamento Farmacológico
Analgésicos Não-Opióides
Antiinflamatórios não-hormonais são os principais medicamentos do grupo. Esses fármacos agem inibindo a cicloxigenase, diminuindo a síntese de prostaglandinas e, conseqüentemente, o processo inflamatório. São indicados para dor leve ou como adjuvante no tratamento da dor moderada e intensa ou quando a dor está associada a algum processo inflamatório. Tudo isso, segundo“Gaspardo et al…2005”
Paracetamol
O paracetamol é um medicamento seguro para uso no período neonatal. O início da ação analgésica é lento, cerca de uma hora, sendo pouco efetivo em processos dolorosos intensos. A dose preconizada em neonatologia é de 10 a 15 mg.kg em recém-nascidos de termo e 10 mg.kg em prematuros; com intervalo de seis horas não devendo exceder cinco doses do fármaco ao dia. Deve ser administrado por via oral uma vez que o paracetamol venoso não está disponível no Brasil. Ele está indicado no tratamento de dor com intensidade leve e moderada, é útil como coadjuvante na analgesia pós-operatória de recém-nascidos, pois não interfere na agregação plaquetária nem induz irritação gástrica. Apresenta baixa hepatotoxicidade em recém-nascidos, uma vez que as vias enzimáticas hepáticas responsáveis pela produção do metabólito tóxico estão imaturas. O fármaco está contra-indicado em recém-nascidos portadores de deficiência de glicose-6-fosfatodesidrogenase. Tudo isso, segundo“Gaspardo et al…2005”
Dipirona
Em decorrência da falta de estudos clínicos e farmacológicos que respaldem seu uso, o fármaco não é recomendado nessa faixa etária. Porém, a grande experiência com seu uso no Brasil demonstra a segurança e eficácia analgésica e antitérmica, inclusive no período neonatal, sem incidência aumentada de efeitos colaterais comprovados. A dose é de 10 a 15 mg.kg a cada seis horas, podendo ser administrada por via oral ou venosa. Tudo isso, segundo“Gaspardo et al…2005”
Indometacina
Seu uso está indicado em recém-nascidos para tratamento da persistência do canal arterial, não havendo estudos que justifiquem seu emprego como analgésico no período neonatal. Tudo isso, segundo“Gaspardo et al…2005”
Analgésicos Opióides
Constituem a mais importante arma para o tratamento da dor em recém-nascidos gravemente enfermos. Os analgésicos opióides ligam-se aos três maiores grupos de receptores de membrana na medula espinal e no córtex: µ, k e d. O estímulo aos receptores inibe a transmissão do estímulo nociceptivo aos centros superiores de processamento. Os opióides inibem a aferência da dor na medula espinal e ativam as vias descendentes inibitórias. Devido à ação em outros receptores opióides, podem causar depressão respiratória, sedação, íleo, retenção urinária, náusea, vômitos e dependência física . A via oral é de mais fácil administração e proporciona níveis séricos constantes, mas não é apropriada para pacientes gravemente enfermos ou após grandes procedimentos cirúrgicos. Nesse caso, a via venosa deve ser usada ponderando-se o uso em infusão contínua a fim de se evitar flutuações nos níveis séricos do fármaco. Deve-se evitar a aplicação intramuscular porque ela causa dor, mas esses agentes podem ainda ser usados pelas vias transdérmica, transmucosa, retal, subcutânea, intratecal e peridural. De acordo com “Stevens et al…2004”.
Morfina
É o padrão dentre os agonistas do receptor µ, sendo potente analgésico e sedativo, além de apresentar baixo custo. O início de ação varia de três a cinco minutos com T1/2Ke0 (meia vida de equilíbrio entre o plasma e o local de ação – cérebro) de 30 minutos. Estudos de farmacocinética após doses em bolus mostraram que em recém-nascidos prematuros, menores e maiores de 30 semanas de gestação, observa-se meia-vida de eliminação maior e depuração diminuída nos pacientes mais prematuros, apesar de variações individuais importantes terem sido notadas nos dois grupos. Avaliando-se a meia-vida de eliminação, a depuração e o metabolismo da morfina em recém-nascidos de 24 a 40 semanas, de idade gestacional do primeiro ao sexagésimo dia de vida, notou-se um espectro amplo de variação nos parâmetros farmacocinéticos, e a meia-vida tende a diminuir e a depuração a aumentar com o aumento da idade gestacional. Todos os recémnascidos excretaram mais de 20% da morfina de forma não-metabolizada e um terço deles não metabolizou a morfina em seus metabólitos primários. Considerando-se o uso da morfina em infusão contínua em recém-nascidos, os estudos de farmacocinética mostraram também aumento do clearance e da meia-vida de eliminação se comparados com os pacientes adultos. O aumento do clearance da morfina nos primeiros seis meses de vida se deve mais à elevação do poder de glicuronidação do que às mudanças na ligação a proteínas ou à percentagem de sulfatação. Assim, a concentração plasmática da morfina mostrou-se duas a três vezes maior em recém-nascidos de termo e quatro vezes maior no prematuro do que em crianças maiores. Além disso, o nível plasmático do fármaco tende a aumentar mesmo depois que ele tenha sido descontinuado devido à recirculação enterohepática.De acordo com “Stevens et al…2004”.
Poucos investigadores têm tentado caracterizar a concentração mínima de morfina necessária para analgesia em recém-nascidos. Chay e col. mostraram que uma concentração de morfina de 125 ng.mL era necessária para produzir sedação adequada em 50% dos recém-nascidos estudados (de termo e prematuros). Como concentrações de 4 a 65 ng.mL são consideradas como analgésicas em crianças maiores, uma explicação para a discrepância entre as necessidades aumentadas de morfina no período neonatal são as baixas concentrações do metabólito morfina-6glicuronídeo (M6G) que são produzidas e a imaturidade do sistema receptor opióide (diminuição da concentração de receptores e/ou da afinidade pelos receptores) no encéfalo do recém-nascido. Além dos efeitos colaterais comuns a todos os opióides (depressão respiratória, náuseas, vômitos e retenção urinária), a morfina desencadeia liberação de histamina, podendo provocar broncoespasmo em recémnascidos portadores de doença pulmonar crônica. A liberação de histamina e a inibição do tônus adrenérgico podem levar à hipotensão arterial, sobretudo em recém-nascidos hipovolêmicos. A tolerância e a síndrome de abstinência podem ser observadas dependendo do tempo de utilização e da estratégia empregada para a suspensão do fármaco.De acordo com “Stevens et al…2004”.
As doses recomendadas para o período neonatal são:
– administração intermitente de 0,05 a 0,20 mg.kg por dose até a cada quatro horas por via venosa; administração contínua para recém-nascidos de termo de 5 a 20 µg.kg.h e para recém-nascidos prematuros de 2 a 10 µg.kg.h. Fentanil
É muito usado em neonatologia devido à sua capacidade de prover rápida analgesia com estabilidade hemodinâmica . Apresenta início de ação mais rápido e duração mais curta (menos de duas horas) comparando-se com a morfina, sendo seu T1/2Ke0 de 6,4 minutos e meia-vida contexto-sensitiva após quatro horas de infusão de 260 minutos. Redistribui-se dos receptores opióides para outros tecidos, como músculos, estômago e gordura. Assim, aumentos transitórios da concentração plasmática em virtude da redistribuição do fármaco a partir desses tecidos podem ocorrer. Apresenta alto metabolismo hepático e o clearance é primariamente dependente do fluxo hepático. A farmacocinética pode estar alterada na presença de aumento da pressão intra-abdominal, pois nessas situações observa-se diminuição do fluxo hepático e do débito cardíaco, permitindo o acúmulo do fentanil em locais de má perfusão e recirculação posteriormente. Doses altas (acima de 5 µg.kg), quando injetadas rapidamente, podem levar à rigidez muscular, em especial da caixa torácica, dificultando a ventilação e induzindo laringoespasmo em recém-nascidos. De acordo com “Stevens et al…2004”.
As doses recomendadas para o período neonatal são:
Administração intermitente de 1 a 4 µg.kg por dose, a cada 2 a 4 horas, por via venosa; –administração contínua em recém-nascidos de termo de 0,5 a 3 µg.kg.h por via venosa e para recém-nascidos prematuros de 0,5 a 2 mg.kg.h por via venosa. A desvantagem da infusão contínua é o aparecimento rápido do efeito de tolerância, sendo necessárias doses crescentes do fármaco para se obter o efeito analgésico desejado.De acordo com “Stevens et al…2004”.
Sufentanil
Opióide sintético, agonista potente do receptor µ apresentando meia-vida curta. Sua meia-vida contexto sensitiva após quatro horas de infusão é de 30 min, apresentando meia-vida de eliminação de 2,2 a 4,6 horas e equilíbrio entre o plasma e o encéfalo de 6,2 minutos. Como o sufentanil é altamente ligado à glicoproteína ácida alfa-1, a ligação protéica do fármaco é dependente dos níveis séricos dessa proteína. Como a concentração plasmática dessa proteína é diminuída em recémnascidos, o fármaco na forma livre é muito maior nesses pacientes do que em crianças maiores. Os estudos de farmacocinética do sufentanil mostram resultados semelhantes aos do fentanil, como clearance diminuído e meia-vida de eliminação aumentada nos recém-nascidos prematuros, comparados com os recém-nascidos de termo e crianças maiores. A dose é de 0,5 a 1,5 µg.kg por dose. A injeção rápida pode levar a rigidez torácica, vômitos e convulsões.De acordo com “Stevens et al…2004”.
Alfentanil
Opióide sintético derivado do fentanil apresentando um quarto de sua potência. O início de ação após infusão venosa é imediato e o pico do efeito acontece em um minuto com um t1/2Ke0 de 0,9 a 1,4 minuto. A meia-vida contexto sensitiva após quatro horas de infusão é de 60 minutos e a duração de ação é de cerca de um terço da do fentanil. De maneira geral, o clearance do alfentanil está diminuído nos recém-nascidos e sua meia-vida é prolongada . O volume de distribuição pode estar aumentado por causa da maior percentagem de água corporal e/ou pela diminuição da ligação às proteínas.De acordo com “Stevens et al…2004”.
Remifentanil
Opióide sintético, agonista dos receptores µ, possuindo a mesma potência do fentanil. Apresenta todas as características farmacodinâmicas de sua classe (analgesia, estabilidade hemodinâmica, depressão respiratória e rigidez muscular), porém apresenta perfil farmacocinético único devido à estrutura éster que o torna suscetível ao rápido metabolismo por esterases plasmáticas e teciduais nãoespecíficas e que redunda em sua ação ultracurta. A meia-vida contexto-sensitiva após quatro horas de infusão é de apenas quatro minutos, fazendo com que o término da ação independa do tempo de infusão. Assim, a recuperação dos efeitos do remifentanil ocorre rapidamente (dentro de cinco a dez minutos) e um nível fixo de concentração é atingido após cinco a dez minutos de uma mudança na velocidade de infusão. Durante a meia-vida de distribuição (0,9 minuto) e eliminação (6,3 minutos) é estimado que 99,8% do remifentanil seja eliminado. Portanto, ao contrário de outros análogos do fentanil a duração de ação do remifentanil não aumenta com a administração prolongada. Além disso, a farmacocinética não se altera na presença de insuficiência hepática ou renal desde que o metabolismo pelas esterases não-específicas esteja preservado. Os efeitos farmacodinâmicos seguem de perto as concentrações sangüíneas, permitindo correlação direta entre dose, níveis sangüíneos e a resposta. Podem ocorrer alterações hemodinâmicas (hipotensão arterial e bradicardia); respiratórias (depressão respiratória); rigidez muscular relacionada com a dose e a velocidade de infusão de um bolus. Por outro lado, não se observa liberação de histamina em doses convencionais.De acordo com “Stevens et al…2004”.
Samartino e col. avaliaram a eficácia e segurança do uso contínuo por via venosa de remifentanil em recém-nascido prematuro que seriam submetidos à laserterapia para tratamento da retinopatia da prematuridade. A recuperação rápida e o retorno ao status pré-operatório, associado à ausência de efeitos colaterais e aos excelentes níveis de analgesia e anestesia obtidos confirmaram a eficácia e a segurança da administração contínua de remifentanil em recém-nascidos prematuros e dão substrato à escolha desse opióide. De acordo com “Stevens et al…2004”.
As doses variam de acordo com o objetivo desejado e, em recém-nascidos a dose inicial em bolus para intubação varia de 1 a 3 µg.kg e para infusão contínua de 0,1 a 5 µg.kg.min.
Outros Opióides
O tramadol e a codeína também são utilizados para o tratamento da dor moderada. O tramadol tem 1/10 da potência da morfina e seu mecanismo de ação inclui características de opióides e não-opióides. Estimula a liberação de serotonina nas terminações nervosas e inibe a recaptação tanto de serotonina quanto de noradrenalina. Causa pouca depressão respiratória e constipação intestinal, além de ter um menor potencial para desenvolver tolerância e dependência. Apesar das vantagens potenciais do emprego, os estudos com a aplicação desse fármaco em crianças são escassos e por isso seu uso em neonatologia ainda é limitado. A meperidina, por outro lado, está praticamente proscrita para o tratamento da dor, sobretudo em decorrência da formação de metabólitos tóxicos (normeperidina) que podem diminuir o limiar convulsivo.De acordo com “Stevens et al…2004”.
Anestésicos Locais
O EMLA® (mistura eutética de lidocaína e prilocaína) produz anestesia em pele intacta, é seguro no recém-nascido quando aplicado isoladamente em um único procedimento e é eficaz para reduzir a dor causada por circuncisão, punções arteriais, venosas e punção lombar. Como desvantagens, pode-se citar a latência de cerca de 60 minutos; vasoconstrição que dificulta a punção venosa e o risco de metaemoglobinemia. O ELA-Max creme é um anestésico local também para uso tópico sendo seu início de ação em cerca de 30 minutos. Causa menos vasoconstrição do que o EMLA.De acordo com “Anand et al…2006”.
A infiltração local de anestésico local (lidocaína) é indicada na punção lombar, inserção de cateter central, drenagem torácica e, eventualmente, na punção arterial. O início da ação é quase imediato e a duração do efeito, de 30 a 60 minutos após a infiltração. Deve-se sempre respeitar a dose máxima de 5 mg.kg.De acordo com “Anand et al…2006”.
SEDAÇÃO NO RECÉM-NASCIDO
A sedação em recém-nascidos é produzida por fármacos que agem diminuindo a atividade, ansiedade e a agitação do paciente, podendo levar à amnésia de eventos dolorosos ou não-dolorosos. No entanto, tais medicamentos em geral não reduzem a dor e, pelo contrário, poderiam potencializá-la, apesar de alguns analgésicos opióides como a morfina também terem a capacidade de sedação. Antes da prescrição de qualquer sedativo, todas as possíveis causas de agitação devem ser pesquisadas e tratadas de forma adequada, como dor, fome, hipoxemia, hipotermia, hipertermia, lesões inflamatórias, inadequação dos parâmetros de ventilação mecânica, entre outras. As principais indicações de sedação no recém-nascido são a realização de procedimentos diagnósticos que exigem algum grau de imobilidade (tomografia computadorizada e ressonância magnética); suporte ventilatório agressivo em recém-nascidos agitados com hipoxemia persistente e pós-operatório de intervenções cirúrgicas como as de fechamento de parede abdominal. Algumas escalas são mais apropriadas para avaliar o grau de sedação do paciente nessa faixa etária, como a escala de COMFORT.De acordo com “Anand et al…2006”.
Hidrato de Cloral
O hidrato de cloral é sedativo e hipnótico, sendo utilizado para procedimentos diagnósticos ou terapêuticos de curta duração. Seu mecanismo de ação ainda não está bem elucidado e sua eliminação é dependente da idade, sendo lenta no recémnascido. Pode-se observar ainda, em prematuros, efeito residual do fármaco até 64 horas após a sua administração. Seu metabólito ativo, o tricloroetanol, é mutagênico e pode causar lesão cromossômica. Também pode levar a hiperbilirrubinemia direta e indireta e acidose metabólica em recém-nascidos. Pode causar irritação gástrica, com aparecimento de náuseas, vômitos e diarréia, alucinações, cefaléia, depressão residual do sistema nervoso com sonolência, depressão miocárdica com disritmia cardíaca, obstrução de vias aéreas e depressão respiratória. Por causa desses efeitos ele não é recomendado para uso no período neonatal. De acordo com “Anand et al…2006”.
Barbitúricos
Os barbitúricos são potentes depressores do sistema nervoso central e têm efeito anticonvulsivante. Não apresentam atividade analgésica intrínseca e podem até intensificar a sensação de dor. O nível de depressão da atividade neurológica depende da farmacocinética do agente, da dose, da via de administração, da condição clínica e do uso simultâneo de outros fármacos.De acordo com “Anand et al…2006”.
Propofol
O propofol é um potente depressor do sistema nervoso central, cuja ação é rapidamente reversível, sem deixar sedação residual. O início da ação ocorre, em geral, em cerca de um a três minutos após a infusão do fármaco, durando cerca de 15 a 20 minutos. O medicamento possui atividade antiemética, sendo indicado para sedação durante procedimentos diagnósticos, terapêuticos ou para indução de anestesia geral em crianças maiores e adultos. Causa depressão respiratória e hipotensão arterial, potencializadas pelo uso concomitante de opióides, cetamina ou óxido nitroso. A segurança para o uso na população neonatal ainda é motivo de estudo. A síndrome de infusão do propofol é uma preocupação quando o fármaco é usado em infusão contínua por longos períodos de tempo (mais de 24 horas) e em altas doses (mais de 75 µg.kg.min). De acordo com “Anand et al…2006”.
Benzodiazepínicos
Os benzodiazepínicos são os fármacos mais empregados para sedação, ansiólise e indução de amnésia. Não apresentam qualquer atividade analgésica e podem, inclusive, exercer efeito antianalgésico. Podem levar ao aparecimento de depressão respiratória, obstrução de vias aéreas, hipotensão arterial e excitação paradoxal e os seus efeitos são potencializados pelos opióides. De acordo com “Anand et al…2006”.
Diazepam
É um potente sedativo ansiolítico com ação anticonvulsivante. No entanto, a tolerância ao efeito sedativo é rápida. Interfere na ligação albumina-bilirrubina aumentando a quantidade de bilirrubina livre circulante. Raramente é utilizado em Unidades de Terapia Intensiva Neonatal, a não ser como dose isolada para promover sedação de duração prolongada, na dose de 0,05 a 0,2 mg.kg por via venosa, apresentando início de ação em dois a três minutos e duração de duas a seis horas.De acordo com “Anand et al…2006”.
Midazolam
É um benzodiazepínico com boa atividade sedativa hipnótica, que apresenta potência duas a quatro vezes maior do que o diazepam, tem rápido início de ação e pode causar amnésia. Apresenta tempo de equilíbrio plasma-encéfalo (t1/2Ke0) entre 0,9 e 5,6 minutos, sendo de 2,7 minutos o período de tempo necessário para que 87,5% desse equilíbrio ocorra. Em recém-nascidos gravemente enfermos a meiavida de eliminação pode estar muito prolongada (6,5 a 12 horas) assim como seu clearance diminuído (0,07 a 0,12 L.h.kg). Pode ainda causar depressão respiratória e hipotensão arterial, potencializadas pelo uso concomitante de opióides, além de poder levar à dependência física se usado de forma contínua por mais de 48 horas. Apesar de ser um sedativo eficaz comparado com o placebo, ainda não se podem tirar conclusões definitivas sobre sua efetividade e segurança no recémnascido. Quando usado por via venosa intermitente, as doses em bolus são de 0,05 a 0,20 mg.kg, administrado a cada duas a quatro horas, com início de ação de um a três minutos, pico de ação de três a cinco minutos e duração de uma a duas horas. Se usado por via venosa contínua, em geral as doses variam de 1 a 6 µg.kg.min. A via intranasal tem sido desaconselhada, devido ao risco de toxicidade ao sistema nervoso central ao ser absorvido, entrando em contato direto com o nervo olfatório via placa crivosa . Um possível efeito colateral é o aparecimento de convulsões quando é feita a administração rápida e em doses elevadas. Pode ainda causar diminuição do fluxo sangüíneo para artéria cerebral média em recém-nascidos prematuros, além de efeitos neurológicos transitórios (hipertonia, hipotonia, movimentos coréicos, movimentos discinéticos, mioclonia e atividade epileptiforme).De acordo com “Anand et al…2006”.
Não há dados suficientes para promover o uso de infusão contínua de midazolam como sedativo para recém-nascidos em Unidades de Terapia Intensiva Neonatal. Apesar de o midazolam ser usado muitas vezes de forma indiscriminada, de modo isolado ou em associação ao fentanil nas Unidades de Terapia Intensiva Neonatais, foi demonstrado que o seu uso em infusão contínua em recém-nascidos prematuros está associado a efeitos adversos graves, como morte, leucomalácia e hemorragia periintraventricular. De acordo com “Anand et al…2006”.
Antagonistas de Benzodiazepínicos e de Opióides
A disponibilidade de antagonistas específicos para os benzodiazepínicos e para os opióides aumentou a segurança da sedação para procedimentos, já que a depressão respiratória pode ser revertida com rapidez. De acordo com “Anand et al…2006”.
A naloxona é um antagonista não-seletivo de opióides, extremamente potente e que deve ser usada na dose de 1 a 4 µg.kg para reverter depressão respiratória causada pelo uso dos opióides. Como tem meia-vida curta (meia-vida de eliminação de 60 minutos) a maioria dos pacientes pode necessitar de doses repetidas, infusão contínua ou depósito intramuscular, além de monitoração, para evitar efeito rebote do quadro de sedação e depressão respiratória. É um antagonista não apenas dos efeitos adversos, como depressão respiratória, rigidez muscular e efeitos gastrintestinais, mas também da sedação e da analgesia. De acordo com “Anand et al…2006”.
O flumazenil é um antagonista puro dos benzodiazepínicos que inibe de forma competitiva o complexo receptor GABA-diazepínico no sistema nervoso central. É utilizado para reverter os efeitos sedativos dos benzodiazepínicos após sedação ou intoxicação. Tem duração de ação mais curta do que a maioria dos benzodiazepínicos. O antagonismo inicia-se um a dois minutos após a dose por via venosa, com pico em seis a dez minutos. A dose utilizada varia de 4 a 20 µg.kg e, como efeitos colaterais podem ocorrer náuseas, vômitos, zumbidos, cefaléia, convulsões, ansiedade e labilidade emocional.De acordo com “Anand et al…2006”.
Síndrome de Abstinência no Recém-Nascido
Se durante a retirada ou após a suspensão dos fármacos utilizados para sedação e analgesia surgirem sinais e sintomas de abstinência, como taquicardia, agitação, sudorese, náusea, vômitos, diarréia, distúrbios do sono e mesmo rebote da dor, deve-se considerar a possibilidade de iniciar o tratamento de abstinência que envolve várias opções terapêuticas, como a metadona, o fenobarbital, a clonidina, o lorazepam ou associações entre eles . A monitoração dos sintomas de abstinência pode ser feita por meio de escala própria, como a escala de Finnegan.De acordo com “Anand et al…2006”.
CONCLUSÃO
Diante de tudo que foi escrito, importante frisar, que a morfina vem sendo preconizada como fármaco de escolha segundo os consensos mundiais de sedação e analgesia em recém-nascidos. Entretanto, devemos lembrar, que a morfina não é sempre a melhor escolha para analgesia e sedação de recém-nascidos prematuros, isso porque, (prematuros de 27 a 29 semanas de idade gestacional) foi observada uma diferença estatística significativa de hemorragia peri-intraventricular grave nos pacientes submetidos a infusão contínua de morfina. Desta forma, a morfina apresenta o incomodo de ter seu metabolismo dependente da função renal e hepática do recém-nascido, podendo manter grau de sedação residual por mais tempo, o que implica no retardo da extubação. Os estudos de farmacocinética da morfina mostraram variabilidade considerável em recém-nascidos de termo e também em prematuros, e o clearance plasmático da morfina está diminuído em recém-nascidos prematuros. Por outro lado, estudos têm mostrado a segurança e eficácia do remifentanil na analgesia e anestesia de crianças e recém-nascidos, assim como em recém-nascidos prematuros. Isso porque, o remifentanil não apresenta efeito de sedação residual após sua suspensão, pode-se tornar uma opção na sedação e analgesia de recém-nascidos prematuros pelos profissionais.
MÉTODOS
Trata-se de uma revisão narrativa sobre os aspectos epidemiológicos, fisiopatológicos e clínicos sobre o manejo da dor, sedação e analgesia no recémnascido. Para tal fim, realizou-se um levantamento bibliográfico a partir da base de dados “Lillacs”, sendo incluídos os seguintes termos para direcionar a pesquisa: “sedação do recém-nascido, dor, sedação e analgesia no recém-nascido”.
Os critérios de inclusão para a seleção dos estudos, adotaram-se: (a) artigos nos idiomas português, espanhol e ingles; (b) estudos de revisão de literatura ou de revisão sistemática; (c) ano de publicação de janeiro de 1992 a novembro de 2025; (d) relevância do estudo; (e) presença dos termos ” sedação do recém-nascido, dor, sedação e analgesia no recém-nascido” no título e/ou resumo cientifico. Com relação aos critérios de exclusão, foram levados em consideração: (a) estudos não relacionados ao tema; (b) artigos publicados anteriormente ao ano de 1992; (c) artigos que não contemplem os demais critérios de inclusão. Assim, foram levantados trinta e cinco artigos, restando vinte e dois selecionados para esta revisão de literatura após a utilização dos critérios de elegibilidade descritos.
DISCUSSÃO
O profissional que atua na UTI neonatal, deve certifica-se que o RN pode apresentar quadro de dor, devendo levar em consideração entre outros sintomas e sinais, o básico que envolve a fisionomia do RN, bem como, ter em mente de que qualquer procedimento e manipulação neonatal pode desenvolver resposta dolorosa.
REFERÊNCIAS
- Neonatologia prática / Richard A. Polin, Mervin C. Yoder; tradução Camila Nogueira. – 5. ed. – Rio de Janeiro: Elsevier, 2016.
- American Academy of Pediatrics. Committee on Fetus and Newborn. Committee on Drugs. Section on Anesthesiology. Section on Surgery. Canadian Paediatric Society. Fetus and Newborn Committee. Prevention and management of pain and stress in the neonate. Pediatrics 2000. 105:454-61.
- Gaspardo CM, Linhares MB, Martinez FE. The eficacy of sucrose for the relief of pain in neonates: a systematic review of the literature. J. Pediatr. 2005. 81: 435- 442.
- Leite AM. Effects of breastfeeding on painrelief in full-termnewborn.. Clin. J. Pain 2009. 25:827-832.
- Anand KJ, Hall RW. Vtherapy for analgesia and sedation in the newborn. Arch. Dis. Child Fetal Neonatal 2006. 91: 448-453.
- Chana SK, Anand KJ. Can we use methadone for analgesia in neonates? Arch. Dis. Child Fetal Neonatal 2001. 85: 79-81.
- Yamada J. A review of systematic reviews on paininterventions in hospitalizedinfants. Pain. Res. Manag 2008. 13: 413-420.
- Guinsburg R. Avaliacao e tratamento da dor no recem-nascido. J Pediatr(RJ)1999. 75::149-160.
- Guinsburg R Avaliação e tratamento da dor no recém-nascido. J Pediatr (RJ), 1999;75:149-160.
- Franck LS, Lawhon G Environmental and behavioral strategies to prevent and manage neonatal pain. Semin Perinat, 1998; 22:434-443.
- Anand KJ Clinical importance of pain and stress in preterm neonates. Biol Neonate, 1998;73:1-9.
- Chermont AG, Guinsburg R, Balda RCX et al. O que os pediatras conhecem sobre avaliação e tratamento da dor no recém-nascido? J Pediatr (RJ), 2003;79:265-272.
- Walco GA, Cassidy RC, Schechter NL Pain, hurt and harm. The ethics of pain control in infants and children. N Engl J Med, 1994;293:918-919.
- Bauchner H, May A, Coates E Use of analgesic agents for invasive medical procedures in pediatric and neonatal intensive care units. J Pediatr, 1992;121:647-649.
- Barker DP, Rutter N Exposure to invasive procedures in neonatal intensive care admissions. Arch Dis Child, 1995;72:47-48.
- Anand KJ International Evidence-Based Group for Neonatal Pain Consensus statement for the prevention and management of pain in the newborn. Arch Pediatr Adolesc Med, 2001; 155:173-180.
- Menon G, Anand KJ, McIntosh N Practical approach to analgesia and sedation in the neonatal intensive care unit. Semin Perinatol, 1998;22:417424.
- Machado MGP, Barbosa RFB, Silva YP A dor em neonatologia, em: Silva YP, Silva JF Dor em Pediatria. Rio de Janeiro, Guanabara Koogan, 2006;105-115.
- Gray L, Miller LW, Philipp BL et al. Breastfeeding is analgesic in healthy newborns. Pediatrics, 2002;109:590-593.
- Blass EM, Hoffemeyer LB Sucrose as an analgesic for newborn infants. Pediatrics, 1991;87:215-218.
- Rebouças EC, Segato EN, Kishi R et al. Effect of the blockade of mu1-opioid and 5HT2A-serotonergic/alpha1-noradrenergic receptors on sweet-substanceinduced analgesia. Psychopharmacology, 2005;179:349-355.
- Stevens B, Yamada J, Ohlsson A Sucrose for analgesia in newborn infants undergoing painful procedures. Cochrane Database Syst Rev, 2004;3:CD001069.
