AGRANULOCYTOSIS RELATED TO THE USE OF DIPYRONE: A LITERATURE REVIEW
REGISTRO DOI: 10.5281/zenodo.7726033
Rebeca Ferreira Nery1
Fernando José de Morais Silva2
Lívia Menezes Escorel3
Antonio Rafael da Silva Figueredo4
Giovana Caroline Martins Santos5
Julia Cristina Martins Dantas6
Cellina Nava de Simas Lima7
Pedro Henrique Barroso e Silva8
Nayara Sangreman Aldeman Melo9
Camila Melo de Freitas10
Ricardo da Costa Freire Carvalho11
Aléxya Eduarda Andrade12
Murilo Rodrigues da Silva13
Jármison Luciano Pinheiro14
Lara Beatriz Amorim Barbosa15
Anderson Ferreira da Silva16
Jaciara Pereira de Moura17
Rafael Campos Guedes18
Ciro José Cavalcante Nascimento19
Dyenifer Sara Lopes Neves20
Beatriz Dias Oliveira21
Raphaella Machado Resende Cabral22
RESUMO
INTRODUÇÃO: Os medicamentos são utilizados para fins terapêuticos de forma preventiva e curativa. Efeitos colaterais são esperados após o uso de um medicamento, já que eles ocasionam mudanças fisiológicas e biológicas através do seu mecanismo. OBJETIVO: Verificar o uso indiscriminado da Dipirona como causa da Agranulocitose. MÉTODOS: O presente estudo trata-se de uma revisão integrativa da literatura, foi realizado um levantamento bibliográfico de caráter descritivo e exploratório, através das bases de dados: Medline e Lilacs, utilizando os descritores: Agranulocitose OR Agranulocytosis OR Agranulocitose e Dipirona OR Dipyrone OR Dipirona. RESULTADOS: A dipirona (ácido 1-fenil-2,3-dimetil-5-pirazolona-4-metilamino metanossulfônico; Novalgina®; Metamizol), é um dos analgésicos/antipiréticos mais utilizados no Brasil, com base nos estudos realizados pode se considerar que o uso da dipirona está frequentemente relacionado aos casos de agranulocitose, sendo que na maioria dos estudos o risco de desenvolver agranulocitose e neutropenia após uma prescrição de dipirona foi de 1:1.602 (IC95% 1:1.926–1:1.371). CONCLUSÃO: O desenvolvimento de agranulocitose após o uso de dipirona causa hospitalização de longo prazo e pode exigir o uso de medicamentos no manejo do tratamento, estando relacionado a casos de agranulocitose, porém com uma baixa incidência na população. Dessa forma, se faz necessário estudos mais aprofundados para entender a relação de uso / efeito colateral dessa medicação. Além disso, cabe aos profissionais de saúde orientar os pacientes sobre os riscos aos quais estão expostos e, como fazer o uso correto do medicamento.
Palavras-chave: Agranulocitose, dipirona, reação adversa.
Abstract
INTRODUCTION: Drugs are used for therapeutic purposes in both preventive and curative ways. Side effects are expected after the use of a drug, since they cause physiological and biological changes through their mechanism. OBJECTIVE: To verify the indiscriminate use of Dipyrone as a cause of Agranulocytosis. METHODS: This study is an integrative literature review, a descriptive and exploratory literature survey was conducted using the following databases: Medline and Lilacs, using the descriptors: Agranulocytosis OR Agranulocytosis OR Agranulocytosis and Dipyrone OR Dipyrone OR Dipyrone. RESULTS: Dipyrone (1-phenyl-2,3-dimethyl-5-pyrazolone-4-methylamino ethanesulfonic acid; Novalgina®; Metamizol) is one of the most widely used analgesics/antipyretics in Brazil. Based on the studies performed, it can be considered that the use of dipyrone is frequently related to cases of agranulocytosis, and in most studies the risk of developing agranulocytosis and neutropenia after a dipyrone prescription was 1:1. 602 (95% CI 1:1,926-1:1,371). CONCLUSION: The development of agranulocytosis after dipyrone use causes long-term hospitalization and may require the use of drugs in the management of treatment, and is related to cases of agranulocytosis, but with a low incidence in the population. Thus, further studies are needed to understand the side effect/use relationship of this medication. In addition, it is up to health professionals to guide patients on the risks to which they are exposed and how to make the correct use of the medication.
Keywords: Agranulocytosis, dipyrone, adverse reaction.
1 INTRODUÇÃO
Metamizol sódico ou Dipirona sódica é um fármaco da classe dos anti-inflamatórios não esteroidais (AINEs) que é empregado, principalmente, como analgésico e antipirético pertence à família das pirazolonas, as substâncias mais antigas obtidas por síntese farmacêutica. A antipirina foi a primeira a ser obtida em 1883, por Fischer, Knorr e Filehne (PANAROTTO et al., 2013).
No Brasil é o analgésico e antipirético mais vendido, empregando dezenas de nomes comerciais, principalmente como constituinte de associações medicamentosas. É um medicamento isento de prescrição (MIP), de menor preço e com variadas formulações farmacêuticas: solução oral, injetável, comprimidos e supositórios, o que provavelmente, contribui para o abuso deste fármaco (NIKOLOVA et al. 2013). Sua absorção é eficaz pelas diferentes vias de administração, por via oral sua ação é observada em aproximadamente 30 minutos, é rapidamente hidrolisado pelo suco gástrico no metabólito ativo 4-N-metilaminoantipirina (MAA), o qual é imediatamente absorvido pelo organismo, tendo como duração de seu efeito farmacológico de quatro a seis horas (KARIN; OLAV, 2002).
O ponto controverso em sua utilização seria o possível efeito depressor sobre a medula óssea, o que poderia levar a uma anemia aplásica ou, principalmente, agranulocitose. em países como Espanha, Polônia, Rússia, Índia e, praticamente, em toda a América Latina sua venda é liberada, sendo inclusive comercializada no Brasil nas diversas apresentações farmacêuticas como medicamento isento de prescrição (GUIMARÃES, et al., 2021). Seu uso é contraindicado na gravidez, amamentação e em pacientes com alergia à dipirona sódica ou a qualquer um dos componentes da fórmula, discrasias sanguíneas ou depressão da medula, e histórico de doenças do sistema hematopoiético (UHLEN et al., 2019).
Nesse sentido, considerando a possibilidade da ocorrência de discrasias sanguíneas como agranulocitose, devido ao uso da dipirona, um fármaco de fácil acesso de venda livre de prescrição médica, o presente artigo teve como objetivo avaliar a ocorrência de agranulocitose decorrente do uso dessa medicação, reforçando a importância do acompanhamento farmacoterapêutico do paciente, através de prática de atenção farmacêutica clínica com avaliação sobre a utilização do fármaco.
2 METODOLOGIA
O presente estudo trata-se de uma revisão integrativa da literatura realizada no mês de fevereiro de 2023, que se utiliza de uma metodologia exploratória e descritiva. (PEREIRA, et al., 2018).
Inicialmente, foram pesquisados estudos nas bases de dados eletrônicas: Literatura Latino – Americana e do Caribe em Ciências da Saúde (Lilacs e Medical Literature Analysis and Retrieval System Online (Medline). Inicialmente foram selecionados os seguintes descritores: Agranulocitose OR Agranulocytosis, OR Agranulocitosis e Dipirona OR Dipyrone OR Dipirona. Utilizando o operador booleano “AND”. Os dados foram organizados durante a revisão de literatura de forma a elencar os estudos relacionados à temática em questão, a filtragem dos artigos encontrados teve como critério de inclusão, artigos nos últimos 5 anos (2018 a 2023), nos idiomas: inglês e alemão, sendo os tipos de documentos: estudo observacional; estudo de etiologia, estudo diagnóstico, estudo prognóstico, estudo de fatores de risco; estudo de rastreamento e ensaio clínico controlado; e como critério de exclusão, foram descartados os artigos que não contemplassem a pergunta de pesquisa, publicações de teses e dissertações, artigos em outros idiomas, textos antes de 2019, e artigos de revisão. Após essa filtragem ficou disponível 86 artigos, sendo que após leitura dos títulos e resumos, foram selecionados 17 artigos que mais se encaixavam na proposta desse estudo para compor a presente revisão, ademais foi realizado e excluído textos em duplicação.
O estudo dispensou submissão ao Comitê de Ética em Pesquisa, por tratar-se de uma pesquisa com dados secundários e de domínio público, assim, não envolvendo nenhuma pesquisa clínica com seres humanos e animais.
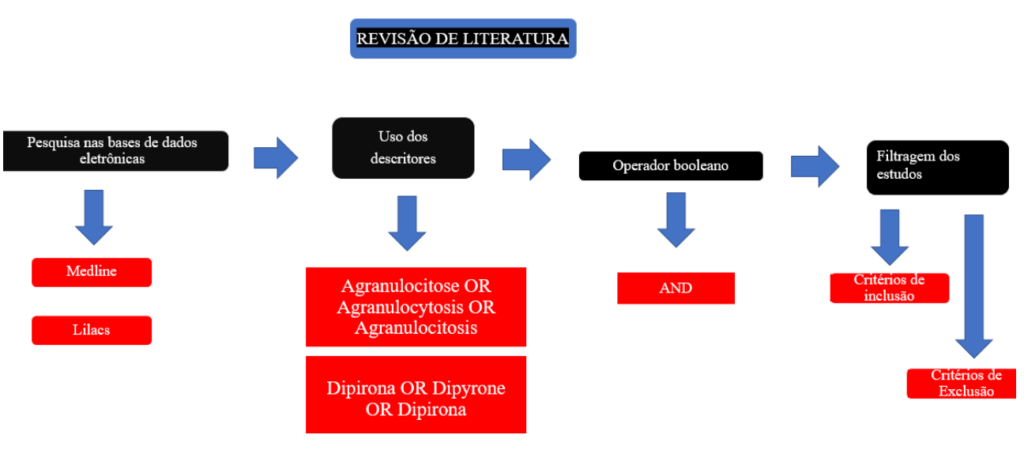
Figura 1: Fluxograma esquematizando a metodologia do estudo
Fonte: Autores, 2023.
Quadro 1-Distribuição dos dados da pesquisa em relação à base de dados e ano da publicação.
Artigo Base de dados Ano de publicação A possible increased risk of metamizole-associated neutropenia among COVID-19 patients. MEDLINE 2021 Paediatric Agranulocytosis Associated with Metamizole Treatment. MEDLINE 2021 Genome-Wide Association Study of Metamizole-Induced Agranulocytosis in European Populations. MEDLINE 2020 Metamizole-induced reactions as a paradigm of drug hypersensitivity: Non-allergic reactions, anaphylaxis, and delayed-type allergy. MEDLINE 2020 [Agranulocytosis after use of metamizole – an underestimated risk?] / Agranulozytose nach Metamizol-Einnahme ein unterschätztes Risiko? MEDLINE 2020 Agranulocytosis attributed to metamizole: An analysis of spontaneous reports in EudraVigilance 1985-2017. MEDLINE 2020 Metamizole and the risk of drug-induced agranulocytosis and neutropenia in statutory health insurance data. MEDLINE 2020 GUIMARÃES, Flávia de Paula Gonçalves et al. POLÍTICA DE PROIBIÇÃO DA DIPIRONA. Revista Augustus, v. 27, n. 54, p. 96-108, 2021. GOOGLE ACADÊMICO 2021 Metamizole-associated neutropenia: Comparison of patients with neutropenia and metamizole-tolerant patients. MEDLINE 2019 Drug safety surveillance within a strategy for the management of non-chemotherapy drug-induced neutropenia. MEDLINE 2019 Is it time to restrict the clinical use of dipyrone? / ¿Es tiempo de restringir el uso clínico de la dipirona? LILACS 2029 [Leukemia caused by collision with a wild pig?] / Leukämie durch Kollision mit Wildschwein? MEDLINE 2019 Fatal Agranulocytosis and Fournier’s Gangrene due to the Use of Metamizole: Correspondence. MEDLINE 2029 Metamizole (dipyrone)-induced agranulocytosis: Does the risk vary according to ethnicity? MEDLINE 2019 Evaluation of hematological alterations after therapeutic use of dipyrone in healthy adults: a prospective study. MEDLINE 2019 Reply to Ziesenitz, Victoria; Erb Thomas; Trachsel, Daniel; van den Anker Johannes, regarding their comment “Safety of dipryone (metamizole) in children-what’s the risk of agranulocytosis?” MEDLINE 2018 Safety of dipyrone (metamizole) in children-What’s the risk of agranulocytosis? MEDLINE 2018
Fonte: Autores, 2023.
3 RESULTADOS
3.1 O Fármaco Dipirona
A dor faz parte da história da humanidade como integrante fundamental do ciclo de vida de cada indivíduo, apesar do desconforto causado a dor tem como função desencadear ações protetoras e de alerta ao nosso organismo, como um aviso de que algo vai mal. A procura crescente da população por alívio e tratamento dos sintomas da dor, estimulam as indústrias farmacêuticas a desenvolverem novas fórmulas de analgesia, assim como melhorar as existentes no mercado.
O fármaco dipirona é considerado como um potente analgésico/antipirético, sendo indicado para o tratamento de patologias como cefaleia, nevralgias, dores reumáticas e de fibras musculares lisas, pós-operatórias e outras origens. Do mesmo modo é indicado para febre causada por quadros em que a utilização do ácido acetilsalicílico (AAS) é desaconselhada. Sua absorção é eficaz pelas diferentes vias de administração, através da via oral sua implicação antipirética é observada em aproximadamente trinta minutos, É rapidamente hidrolisado pelo suco gástrico no metabólito ativo 4-N-metilaminoantipirina (MAA), o qual é imediatamente absorvido pelo organismo, tendo como duração de seu efeito farmacológico entre quatro e seis horas. (KNAPPMANN et al., 2010).
3.2 Agranulocitose Medicamentosa
Agranulocitose é o termo utilizado para definir uma redução total do número de granulócitos circulantes no sangue periférico, tecnicamente, essa redução inclui neutrófilos, eosinófilos, basófilos e monócitos, elementos que são de extrema importância contra agentes infecciosos, é uma discrasia aguda do sangue a qual submete ao indivíduo, o elevado risco de adquirir infecções, contra as quais o organismo fragilizado, não se encontra preparado para defender-se (SOUZA et al., 2013).
A doença tem como principal sintomatologia no período prodrômico manifestações clínicas como febre, calafrios, amigdalite e faringite, já na fase aguda da doença as manifestações são astenia, prostração, sepse, estomatite e pneumonia (BERNARD et al., 2000)
O diagnóstico de agranulocitose se dá após a avaliação de vários fatores e exames, primeiramente o profissional realizará a anamnese do paciente o exame físico e clínico, após a suspeita de agranulocitose deve solicitar exames laboratoriais específicos como hemograma, contagem de leucócitos em lâmina microscópica e mielograma para que seja confirmado com urgência o diagnóstico de agranulocitose (PANAROTTO et al., 2013).
3.3 Dipirona Como Causa de Agranulocitose
Em geral, todos os medicamentos podem causar algum tipo de efeito colateral, dentre esses efeitos aparecem às desordens hematológicas, observadas em bula como possível reação em vários fármacos. O efeito supressor medular da dipirona na formação de glóbulos brancos foi descrito pela primeira vez em 1934, o qual motivou alguns países como (Estados Unidos, Reino Unido, Austrália, Suécia entre outro) a suspender o medicamento da lista OTC (over- the- counter), limitando o seu uso somente a nível hospitalar (HAMERSCLAK et al., 2005).
Através deste trabalho foi possível observar que, a agranulocitose após o uso de metamizol é uma reação adversa grave ao medicamento que pode afetar pacientes de todas as idades. Frequentemente, apenas sintomas clínicos distintos, como temperatura de origem desconhecida, disfagia e amigdalite em combinação com abscessos na área da cabeça e pescoço, resultam na detecção de agranulocitose induzida por metamizol. Uma agranulocitose provoca cirurgia parcialmente radical e/ou medidas de terapia intensiva e pode levar à sepse com falência de órgãos ou mesmo à morte (KATHARINA et al., 2020).
Como parte do sistema tioredoxina, TXN é uma enzima antioxidante encontrada em uma variedade de células, incluindo granulócitos (UHLEN et al., 2019).
O metamizol é proibido em alguns países principalmente por causa de uma rara associação com neutropenia, definida como contagem absoluta de neutrófilos <1,5 × 10 9 /L, e agranulocitose fatal, definida como contagem absoluta de neutrófilos <0,2 × 10 9 /L. Existe uma ampla variação em relação à incidência relatada de neutropenia e agranulocitose associadas ao metamizol (NIKOLOVA et al. 2013).
Como pudemos observar, na Suécia, a incidência relatada de agranulocitose foi estimada em pelo menos 1:1.439 prescrições (KARIN; OLAV, 2002).
Um pequeno número de pacientes foi diagnosticado com manifestação do espectro da síndrome de Stevens-Johnson/necrólisis epidérmica tóxica (SSJ/NET) (n = 5), reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS) (n = 4), exantema flexural (n = 3) ou agranulocitose (n = 5).
4 CONCLUSÃO
O desenvolvimento de agranulocitose após o uso de metamizol causa hospitalização de longo prazo e pode exigir o uso de medicamentos no manejo do tratamento. Considerando a disponibilidade de opções alternativas para tratar febre e dor, e dado o perfil de efeitos colaterais do metamizol, não deve ser o tratamento antipirético de primeira linha preferencial em crianças. A agranulocitose é uma reação adversa perigosa ou mesmo mortal após o uso de metamizol. Embora o risco de agranulocitose pareça aumentar com a duração do uso, recomendamos a educação do paciente, bem como a documentação de até mesmo uma única administração de metamizol. Isso pode facilitar o diagnóstico precoce de agranulocitose induzida por metamizol e, assim, prevenir o aparecimento de complicações graves com possível resultado letal. Até o presente momento a retirada da dipirona do mercado não se faz necessária, devido a sua eficácia farmacológica, porém deve se agir com bom senso na avaliação sobre a utilização do fármaco, avaliando o risco para cada caso com relação a outros medicamentos que apresentem uma toxicidade menor ao paciente.
Referências
LERMAN, Tsahi T. et al. A possible increased risk of metamizole‐associated neutropenia among COVID‐19 patients. British Journal of Clinical Pharmacology, v. 87, n. 7, p. 2902-2906, 2021.
KILIÇ, Ömer et al. Paediatric agranulocytosis associated with metamizole treatment. Pediatric Drugs, v. 23, p. 105-110, 2021.
CISMARU, Anca Liliana et al. Genome-wide association study of metamizole-induced agranulocytosis in European populations. Genes, v. 11, n. 11, p. 1275, 2020.
TRAUTMANN, Axel; BROCKOW, Knut; STOEVESANDT, Johanna. Metamizole‐induced reactions as a paradigm of drug hypersensitivity: Non‐allergic reactions, anaphylaxis, and delayed‐type allergy. Clinical & Experimental Allergy, 2020.
SCHINZ, Katharina et al. Agranulocytosis after use of metamizole-an underestimated risk?. Laryngo-Rhino-Otologie, v. 99, n. 10, p. 707-712, 2020.
HOFFMANN, Falk; BANTEL, Carsten; JOBSKI, Kathrin. Agranulocytosis attributed to metamizole: An analysis of spontaneous reports in EudraVigilance 1985‐2017. Basic & clinical pharmacology & toxicology, v. 126, n. 2, p. 116-125, 2020.
KLOSE, Sebastian et al. Metamizole and the risk of drug-induced agranulocytosis and neutropenia in statutory health insurance data. Naunyn-Schmiedeberg’s Archives of Pharmacology, v. 393, p. 681-690, 2020.
GUIMARÃES, Flávia de Paula Gonçalves et al. POLÍTICA DE PROIBIÇÃO DA DIPIRONA. Revista Augustus, v. 27, n. 54, p. 96-108, 2021.
RUDIN, Deborah et al. Metamizole-associated neutropenia: Comparison of patients with neutropenia and metamizole-tolerant patients. European journal of internal medicine, v. 68, p. 36-43, 2019.
REVUELTA-HERRERO, José Luis et al. Drug safety surveillance within a strategy for the management of non-chemotherapy drug-induced neutropenia. International Journal of Clinical Pharmacy, v. 41, p. 1143-1147, 2019.
GÓMEZ-DUARTE, Oscar Gilberto. Is it time to restrict the clinical use of dipyrone?. Colombian Journal of Anestesiology, v. 47, n. 2, p. 81-83, 2019.
ZIMMERMANN, Maximilian; BENDAS, Gerd; FELDMANN, Georg. Leukämie durch Kollision mit Wildschwein?. DMW-Deutsche Medizinische Wochenschrift, v. 144, n. 05, p. 335-339, 2019.
ERGÜN, Hakan; GÜNER, Müberra Devrim. Fatal Agranulocytosis and Fournier’s Gangrene due to the Use of Metamizole: Correspondence. The Indian Journal of Pediatrics, v. 86, n. 6, p. 565-567, 2019.
SHAH, Rashmi R. Metamizole (dipyrone)‐induced agranulocytosis: Does the risk vary according to ethnicity?. Journal of clinical pharmacy and therapeutics, v. 44, n. 1, p. 129-133, 2019.
DE SOUZA, Ernane C. et al. Evaluation of hematological alterations after therapeutic use of dipyrone in healthy adults: a prospective study. Journal of Basic and Clinical Physiology and Pharmacology, v. 29, n. 4, p. 385-390, 2018.
ZIESENITZ, Victoria C. et al. Safety of dipyrone (metamizole) in children-What’s the risk of agranulocytosis?. Paediatric anaesthesia, v. 28, n. 2, p. 186-187, 2018.
ZIESENITZ, Victoria C. et al. Safety of dipyrone (metamizole) in children-What’s the risk of agranulocytosis?. Paediatric anaesthesia, v. 28, n. 2, p. 186-187, 2018.
PEREIRA, Adriana Soares et al. Metodologia da pesquisa científica. 2018.
1Graduanda em Enfermagem pela Faculdade São Francisco da Paraíba, Cajazeiras, Paraíba, Brasil.
2, 7, 8, 9Graduando em Medicina pela Faculdade de Ciências Humanas, Exatas e da Saúde do Piauí-FAHESP-Instituto de Educação Superior do Vale do Parnaíba-IESVAP, Parnaíba-PI, Brasil.
3Graduanda em Medicina pelo Centro Universitário de João Pessoa – UNIPÊ, João Pessoa-PB, Brasil.
4Graduando em Odontologia pelo Centro Universitário da Grande Fortaleza, UNIFAMETRO- Fortaleza, CE, Brasil.
5,6Graduanda em Medicina pelo Centro Universitário Tocantinense Presidente Antônio Carlos (UNITPAC), Araguaína -TO, Brasil.
10Graduanda em Medicina pela Faculdade Pitágoras de Medicina de Eunápolis, Eunápolis, BA, Brasil.
11Graduando em Medicina pela Universidade de Rio Verde, FESURV, Formosa-GO Brasil.
12Graduanda em Medicina pela Universidade de Rio Verde -Unirv- (Campus Goianésia), Goianésia-GO, Brasil.
13Médico Residente de Clínica Médica no Hospital Regional do Cariri, Juazeiro do Norte – CE, Brasil.
14,15Graduando em Medicina pela Universidad Del Valle – UNIVALLE, Tiquipaya, Cochabamba, Bolivia.
16Graduando em Medicina pela Universidade de Rio Verde-UniRV, Formosa – GO, Brasil.
17Enfermeira pelo Centro Universitário Santo Agostinho, Teresina, PI, Brasil.
18Graduado em Medicina pelo Centro Universitário de Brasília (UNICEUB), Brasília, DF, Brasil.
19Médico pelo Centro Universitário UniFacid – Campus Horto, Teresina, Piauí, Brasil.
20,21,22Graduanda em Medicina pela Universidade de Rio Verde Campus Aparecida de Goiânia, Extensão Goiânia, Goiânia-GO
