THE USE OF CELL CULTURE IN PRECISION MEDICINE: THE CREATION OF MINI-ORGANS FROM STEM CELLS
REGISTRO DOI: 10.69849/revistaft/cl10202506101236
Karen Marry da Silva Frontelmo1
Keyla Farias Martins1
Stephanie Bruno da Silva1
Orientador: Raphael Rangel2
RESUMO: A medicina de precisão está emergindo como uma abordagem revolucionária na prática clínica, visando personalizar o tratamento de doenças com base nas características genéticas, moleculares e ambientais de cada paciente. No entanto, apesar de seu potencial promissor, ainda existem desafios significativos a serem superados na integração efetiva do cultivo celular na prática clínica de medicina de precisão. Todavia, a combinação da tecnologia de células-tronco IPS com a criação de mini órgãos oferecerá uma plataforma inovadora e altamente eficaz para o estudo de doenças complexas, teste de drogas e desenvolvimento de terapias personalizadas. Portanto, o objetivo deste estudo é descrever a criação de mini órgãos a partir da utilização de células troncos IPS e sua importância na medicina de precisão. A metodologia utilizada para a elaboração deste artigo foi uma revisão sistemática da literatura, através de descritores em inglês. Os critérios de inclusão adotados foram: artigos publicados nos últimos cinco anos (2020 a 2025), disponíveis integralmente, gratuitos, em inglês ou português, e que abordassem diretamente os tópicos relacionados aos objetivos deste estudo. A análise dos artigos selecionados revelou avanços significativos na aplicação de células-tronco pluripotentes induzidas (iPSCs) na criação de miniórgãos e no desenvolvimento da medicina de precisão. Os estudos abordaram desde aspectos técnicos, como a otimização do microambiente extracelular para geração de organoides renais, até aplicações práticas, como a modelagem de doenças cardiovasculares e neurológicas com potencial terapêutico. Em conclusão, apesar dos avanços científicos relevantes, ainda persistem desafios técnicos, regulatórios e éticos que precisam ser superados para a plena integração dessa tecnologia à prática clínica. A padronização dos protocolos, a estabilidade genética das células, os riscos associados à pluripotência e a garantia da segurança em ensaios clínicos são fatores que exigem contínuo investimento em pesquisa e regulamentação.
Palavras-Chave: Cultivo Celular. Medicina de Precisão. Mini Órgãos.
ABSTRACT: Precision medicine is emerging as a revolutionary approach in clinical practice, aiming to personalize disease treatment based on each patient’s genetic, molecular and environmental characteristics. However, despite its promising potential, there are still significant challenges to be overcome in the effective integration of cell culture into the clinical practice of precision medicine. However, the combination of IPS stem cell technology with the creation of mini organs will offer an innovative and highly effective platform for studying complex diseases, testing drugs and developing personalized therapies. Therefore, the objective of this study is to describe the creation of mini organs using IPS stem cells and their importance in precision medicine, through a systematic review of the literature. The methodology used to prepare this article was a systematic review of the literature, using descriptors in English. The inclusion criteria adopted were: articles published in the last five years (2020 to 2025), available in full, free of charge, in English or Portuguese, and that directly addressed topics related to the objectives of this study. The analysis of the selected articles revealed significant advances in the application of induced pluripotent stem cells (iPSCs) in the creation of mini-organs and in the development of precision medicine. The studies addressed everything from technical aspects, such as the optimization of the extracellular microenvironment for the generation of renal organoids, to practical applications, such as the modeling of cardiovascular and neurological diseases with therapeutic potential. In conclusion, despite the relevant scientific advances, there are still technical, regulatory, and ethical challenges that need to be overcome for the full integration of this technology into clinical practice. The standardization of protocols, the genetic stability of cells, the risks associated with pluripotency and ensuring safety in clinical trials are factors that require continuous investment in research and regulation.
Keywords: Cell Cultivation. Precision Medicine. Mini Organs.
RESUMEN: La medicina de precisión está surgiendo como un enfoque revolucionario en la práctica clínica, cuyo objetivo es personalizar el tratamiento de la enfermedad en función de las características genéticas, moleculares y ambientales de cada paciente. Sin embargo, a pesar de su potencial prometedor, aún quedan desafíos importantes por superar en la integración efectiva del cultivo celular en la práctica clínica de la medicina de precisión. Sin embargo, la combinación de la tecnología de células madre IPS con la creación de miniórganos ofrecerá una plataforma innovadora y altamente efectiva para estudiar enfermedades complejas, probar medicamentos y desarrollar terapias personalizadas. Por tanto, el objetivo de este estudio es describir la creación de mini órganos utilizando células madre IPS y su importancia en la medicina de precisión. La metodología utilizada para elaborar este artículo fue una revisión sistemática de la literatura, utilizando descriptores en inglés. Los criterios de inclusión adoptados fueron: artículos publicados en los últimos cinco años (2020 a 2025), disponibles en su totalidad, de forma gratuita, en inglés o portugués, y que abordaran directamente temas relacionados con los objetivos de este estudio. El análisis de los artículos seleccionados reveló avances significativos en la aplicación de células madre pluripotentes inducidas (iPSC) en la creación de miniórganos y en el desarrollo de la medicina de precisión. Los estudios abarcaron desde aspectos técnicos, como la optimización del microambiente extracelular para la generación de organoides renales, hasta aplicaciones prácticas, como el modelado de enfermedades cardiovasculares y neurológicas con potencial terapéutico. En conclusión, a pesar de los avances científicos relevantes, aún existen desafíos técnicos, regulatorios y éticos que deben superarse para la plena integración de esta tecnología en la práctica clínica. La estandarización de los protocolos, la estabilidad genética de las células, los riesgos asociados a la pluripotencia y la garantía de la seguridad en los ensayos clínicos son factores que requieren una inversión continua en investigación y regulación.
Palabras-clave: Cultivo celular. Medicina de precisión. Miniórganos.
INTRODUÇÃO
Na última década, a medicina progrediu no estudo da tecnologia de organóides, que são versões em miniatura de órgãos humanos. Estes avanços têm suas origens baseados em pesquisas realizadas desde o século passado, onde cientistas investigaram a capacidade de auto-organização celular. Métodos como cultivo de fragmentos de tecido e cultivo em gotas suspensas foram inovadores, possibilitando a observação direta do desenvolvimento dos tecidos (Yamanaka, 2020).
Com o tempo, essas técnicas evoluíram, resultando na criação de organóides mamários e intestinais. Todavia, o campo também dedicou esforços para aprimorar a vascularização dos organóides, visando aumentar sua viabilidade (Mansour et al, 2018). Apesar disso, ainda existem desafios a serem superados, como a variação entre os organóides e a necessidade de padronização de ensaios funcionais. Portanto, o futuro reserva a exploração de transplantes de organóides para regeneração de tecidos, bem como o desenvolvimento de fontes celulares autólogas para a produção de organóides, o que abre novas perspectivas terapêuticas (Zhao et al, 2015).
Desde que as células-tronco foram descobertas em 2006, os cientistas têm trabalhado para usar um tipo especial delas, chamadas de iPSCs, em tratamentos médicos. Para fazer isso, eles precisam transformar células do corpo que já têm uma função específica de volta ao um estado inicial, onde podem se tornar qualquer tipo de célula novamente. Nesse sentido, usando esse conhecimento, os cientistas conseguiram com sucesso transformar células maduras em iPSCs em laboratório (Aguirre et al, 2023).
Dessa forma, a medicina de precisão está emergindo como uma abordagem revolucionária na prática clínica, visando personalizar o tratamento de doenças com base nas características genéticas, moleculares e ambientais de cada paciente. Nesse contexto, o cultivo celular tem se destacado como uma ferramenta fundamental para avançar os objetivos da medicina de precisão. O cultivo celular permite a manipulação e observação de células humanas em condições controladas, proporcionando compreensões acerca do funcionamento molecular e as respostas a diferentes terapias (Lodrini et al, 2020).
No entanto, apesar de seu potencial promissor, ainda existem desafios significativos a serem superados na integração efetiva do cultivo celular na prática clínica de medicina de precisão. Uma das principais problemáticas enfrentadas reside na complexidade da transição dos resultados obtidos em culturas celulares para a aplicação direta no tratamento de pacientes. Apesar dos avanços tecnológicos, replicar fielmente o ambiente in vivo em um ambiente de cultura celular ainda é um desafio, o que pode comprometer a relevância clínica dos dados gerados (Sisodiya, 2021).
Além disso, questões relacionadas à variabilidade inter e intra-individual das células, bem como a dificuldade em manter a estabilidade genética ao longo das passagens celulares, representam obstáculos adicionais. Essas questões destacam a necessidade premente de desenvolver abordagens mais robustas e padronizadas para a utilização eficaz do cultivo celular na medicina de precisão (Hovland et al, 2022). Neste sentido, considera-se importante abordar as questões levantadas, e avançar significativamente no uso do cultivo celular na medicina de precisão, potencializando sua capacidade de personalizar o tratamento de doenças com base nas características individuais de cada paciente.
O uso de miniórgãos originados de células-tronco iPS, representa um marco no avanço da saúde personalizada, oferecendo novas perspectivas para o tratamento e prevenção de doenças complexas. Os organoides também representam uma grande promessa para testar novos medicamentos e para eliminar a necessidade de testes em modelos animais. Assim, a combinação da tecnologia de células-tronco IPS com a criação de miniórgãos oferecerá uma plataforma inovadora e altamente eficaz para o estudo de doenças complexas, teste de drogas e desenvolvimento de terapias personalizadas.
Portanto o objetivo geral é descrever a criação de mini órgãos a partir da utilização de células troncos IPS e sua importância na medicina de precisão, através de uma revisão sistemática da literatura. Enquanto os objetivos específicos são: investigar os métodos de obtenção e reprogramação de células-tronco IPS para a aplicação na medicina de precisão; analisar os avanços recentes no uso de células-tronco IPS na modelagem de doenças e no desenvolvimento de terapias personalizadas; compreender a criação de miniórgãos a partir da reprogramação de células adultas para um estado pluripotente; e avaliar os desafios e as perspectivas futuras da utilização de células-tronco IPS, considerando aspectos éticos, regulatórios e técnicos.
Devido ao aumento de doenças de causas idiopáticas se faz necessário que a medicina de precisão esteja cada vez mais no âmbito social e, por isso, descrever como esse processo acontece é de importância nos dias atuais. A bióloga Nuria Montserrat, pesquisadora do Instituto de Bioengenharia da Catalunha, enfatiza a importância da utilização de células tronco induzidas pluripotentes para criação de miniórgãos, no qual ela coordena a plataforma de Biomodelos e Biobancos, que gerou mais de um milhão de amostras de miniórgãos a partir de células de feto em útero em 2022.
Além disso, em pesquisas junto a bases de dados científicos brasileiros, constatou-se que há em média 100 trabalhos publicados sobre a utilização do cultivo celular na medicina de precisão, porém menos da metade deles abordam alternativas sobre sua relevância de fato para o futuro. Dessa forma, este estudo se justifica pela necessidade acadêmica e social do desenvolvimento de mais pesquisas sobre essa temática, com o propósito de garantir o avanço benéfico do cultivo celular.
METODOLOGIA
A metodologia utilizada para a elaboração deste artigo foi uma revisão sistemática da literatura, realizada com o objetivo de reunir e analisar estudos relevantes sobre a utilização de células-tronco pluripotentes induzidas (iPSCs) na criação de miniórgãos e sua aplicação na medicina de precisão. As bases de dados consultadas foram a National Library of Medicine (PubMed), Literatura Latino-Americana e do Caribe em Ciências da Saúde (LILACS), a Biblioteca Virtual em Saúde (BVS) e a Scientific Electronic Library Online (SciELO).
Foram utilizados os seguintes descritores em inglês, combinados com o operador booleano “AND”: “Induced Pluripotent Stem Cells”, “Organoids”, “Precision Medicine”, “Disease Modeling”, “Personalized Therapy” e “Cell Reprogramming”. As buscas seguiram as seguintes combinações principais: [“Induced Pluripotent Stem Cells” AND “Organoids” AND “Precision Medicine”], [“Induced Pluripotent Stem Cells” AND “Disease Modeling”], e [“Cell Reprogramming” AND “Personalized Therapy”].
Os critérios de inclusão adotados foram: artigos publicados nos últimos cinco anos (2020 a 2025), disponíveis integralmente, gratuitos, em inglês ou português, e que abordassem diretamente os tópicos relacionados aos objetivos deste estudo. Foram excluídos artigos duplicados, resumos, revisões narrativas, estudos que não apresentavam relação direta com a temática abordada e publicações que não atendiam aos critérios de qualidade metodológica estabelecidos.
RESULTADOS
A partir da metodologia descrita foram encontrados inicialmente 242 artigos, sendo 68 artigos do Scientific Eletronic Library Online (SciELO), 31 artigos da Literatura Latino-Americana e do Caribe em Ciências da Saúde (LILACS), 79 artigos da Biblioteca Virtual em Saúde (BVS) e 64 da National Library of Medicine (PubMed). Inicialmente foi realizada uma triagem, aplicando os critérios de inclusão por indisponibilidade em formato online, integralidade e gratuidade, restando 116 artigos. Posteriormente foram excluídos 82 artigos em relação aos critérios de língua e tempo de publicação, dos últimos 5 anos. Adiante foram analisados integralmente 34 artigos, excluindo-se 22 artigos por não atenderem à proposta temática, e ao final, foram selecionados 8 artigos que estavam de acordo com os objetivos do presente artigo.
Figura 1: Fluxograma da metodologia da etapa de seleção e inclusão dos estudos
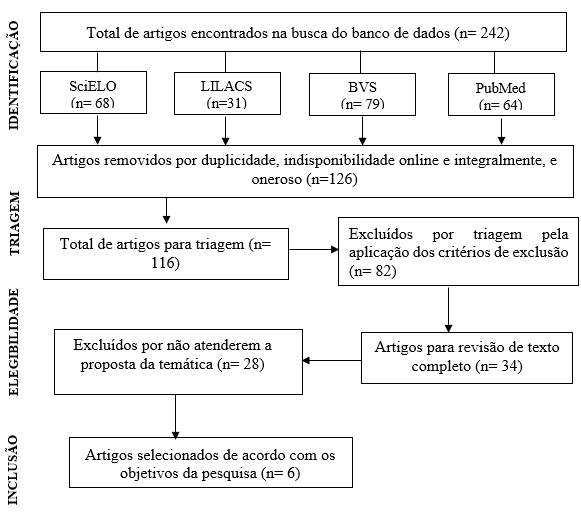
Fonte: Dados da Pesquisa, 2024.
Diante da elegibilidade dos artigos, os artigos foram sintetizados a partir das suas principais considerações na tabela 1.
Tabela 1: Caracterização dos artigos
| Título | Autor / Ano | Objetivos | Principais Resultados |
| Mini-organs forum: how to advance organoid technology to organ transplant community | Berishvili; et al (2021) | Apresentar um resumo das conquistas iniciais que facilitam a derivação e a cultura de organoides. | Foi apresentado discussões iniciais entre biólogos de células-tronco, bioengenheiros e a comunidade de transplantes, a fim de melhor direcionar a pesquisa básica em organoides para o avanço do campo do transplante de órgãos. |
| Fine tuning the extracellular environment accelerates the derivation of kidney organoids from human pluripotent stem cells | Garreta et al (2021) | Gerar organoides renais que correspondem transcriptomicamente aos rins fetais humanos do segundo trimestre através da exposição das células-tronco pluripotentes humanas (hPSCs). | Essa abordagem criou um microambiente in vivo flexível que promoveu o crescimento e a diferenciação dos organoides renais implantados, além de fornecer um componente vascular. |
| Applications of human organoids in the personalized treatment for digestive diseases | Wang; et al (2022) | Destacar os avanços no campo da tecnologia de organoides sob a perspectiva da modelagem de doenças e da terapia personalizada. | Os organoides representam um modelo de pesquisa promissor, ajudando-nos a obter uma compreensão mais profunda dos órgãos digestivos; este modelo também pode ser usado para fornecer aos pacientes um tratamento preciso e individualizado e para construir modelos de teste in vitro rápidos para triagem de medicamentos ou terapia gênica/celular, conectando a pesquisa básica ao tratamento clínico. |
| Induced Pluripotent Stem Cells for Cardiovascular Disease Modeling and Precision Medicine: A Scientific Statement From the American Heart Association | Musunru et al (2023) | Resumir o estado da ciência com relação ao uso de iPSCs para modelagem de características e distúrbios cardiovasculares e para triagem terapêutica; identificar as oportunidades e desafios no uso de iPSCs para modelagem de doenças e medicina de precisão; e delinear estratégias que facilitarão o uso de iPSCs para aplicações biomédicas. | Foi abordado sobre abordar o uso de células-tronco como terapia regenerativa, como transplante no corpo para tratar doença cardíaca isquêmica ou insuficiência cardíaca. |
| In Vivo Reprogramming Using Yamanaka Factors in the CNS: A Scoping Review | Cho; et al (2024) | Resumir o estado atual da pesquisa em reprogramação in vivo no sistema nervoso central, com foco no uso de fatores de Yamanaka. | A reprogramação in vivo utilizando fatores de Yamanaka demonstrou resultados promissores em diversos modelos animais de doenças do sistema nervoso central. Estudos demonstraram que essa abordagem pode promover a geração de novos neurônios, melhorar os resultados funcionais e reduzir a formação de cicatrizes. |
| An in vivo model of functional and vascularized human brain organoids | Mansour et al (2024) | Estabelecer um método para transplantar organoides cerebrais humanos para o cérebro de camundongos adultos | Os enxertos de organoides demonstraram diferenciação e maturação neuronal progressiva, gliogênese, integração da microglia e crescimento de axônios em múltiplas regiões do cérebro do hospedeiro. O registro extracelular in vivo combinado com optogenética revelou atividade neuronal intraenxerto e sugeriu conectividade sináptica funcional enxerto-hospedeiro. |
Fonte: Dados da Pesquisa, 2025.
A análise dos artigos selecionados revelou avanços significativos na aplicação de células-tronco pluripotentes induzidas (iPSCs) na criação de miniórgãos e no desenvolvimento da medicina de precisão. Os estudos abordaram desde aspectos técnicos, como a otimização do microambiente extracelular para geração de organoides renais, até aplicações práticas, como a modelagem de doenças cardiovasculares e neurológicas com potencial terapêutico. Também foram destacadas as possibilidades de uso dos organoides em triagens de medicamentos personalizados e a integração funcional de organoides cerebrais transplantados em modelos animais. Além dos avanços técnicos, os artigos discutiram os desafios éticos e regulatórios envolvidos, ressaltando o papel das iPSCs como uma ferramenta promissora para o futuro da medicina personalizada.
DISCUSSÃO
De acordo com Berishvili et al (2021), a geração de mini-órgãos humanos, os chamados organoides, é um dos maiores avanços científicos na medicina regenerativa. Essa tecnologia explora técnicas tradicionais de cultura tridimensional que apoiam as respostas de auto-organização celular autônoma de células-tronco para derivar versões de órgãos humanos em tamanhos de micrômetros a milímetros. A convergência da tecnologia de organoides com o transplante de órgãos ainda está em fase inicial, mas espera-se que essa aliança abra novos caminhos para mudar a forma como conduzimos a pesquisa em transplantes e organoides.
Originalmente, para produzir células iPS humanas, era necessário usar vetores que se incorporaram ao genoma, o que poderia causar mutações e prejudicar a eficácia dessas células em pesquisas e tratamentos médicos. Todavia, a ciência descobriu um método para obter células iPS humanas sem a necessidade de integração ao genoma, utilizando vetores epissômicos. Após a eliminação desses vetores, as células iPS resultantes não contém qualquer material genético estranho e se assemelham às células-tronco embrionárias humanas em termos de capacidade de crescimento e diferenciação (Hovland et al, 2022).
Encontrar células-tronco capazes de se diferenciar em todos os tipos de tecido é um desafio. Porém, as células-tronco embrionárias atendem a essas condições, mas seu processo de obtenção é encontrado com oposição de natureza ética (Fus-Kujawa et al, 2021). Entretanto, após Yamanaka (2020) e Cho et al (2024) publicarem os resultados sobre a reprogramação de fibroblastos embrionários de camundongos em um novo tipo de célula, chamadas células-tronco pluripotentes induzidas (iPSCs), esses desafios passam a ser superados.
O número de ensaios clínicos utilizando células-tronco pluripotentes humanas (hPSC) — tanto células-tronco embrionárias quanto células-tronco pluripotentes induzidas (hESC/iPSC) — expandiu-se nos últimos anos além das expectativas. Até o final de 2021, um total de 90 ensaios clínicos haviam sido registrados em 13 países, com mais de 3.000 participantes. No entanto, apenas EUA, Japão, China e Reino Unido estão conduzindo ensaios clínicos baseados em hESC e hiPSC. Juntos, EUA, Japão e China registraram 78% (70 de 90) de todos os ensaios clínicos em todo o mundo (Ilic; Ogilve, 2022).
Nos últimos anos, a reprogramação in vivo utilizando fatores de Yamanaka surgiu como uma abordagem promissora para a regeneração do sistema nervoso central. Com as novas descobertas, estudos revelaram que os principais fatores transcricionais necessários para a reprogramação celular, são, nomeadamente, Oct4, Sox2, Klf4 e c-Myc (OSKM). Estes fatores, ao serem introduzidos nas células somáticas, são capazes de reprogramar-las em iPSCs, abrindo assim novas perspectivas na compreensão da patogênese de diversas doenças e no desenvolvimento de terapias inovadoras.
Nas ideias de Hovland et al (2022), os fatores de Yamanaka são essenciais para o estabelecimento da pluripotência em células-tronco embrionárias, mas sua função em populações de células-tronco multipotentes é pouco compreendida. De forma que OCT4 e SOX2 cooperam com fatores de transcrição específicos de tecido para promover a formação da crista neural. Ao avaliar células da crista neural aviária e humana em diferentes estágios de desenvolvimento, os autores caracterizaram as alterações epigenômicas que ocorrem durante sua especificação, migração e diferenciação inicial.
Esta análise determinou que o dímero OCT4-SOX2 é necessário para estabelecer uma assinatura epigenômica da crista neural que se perde com o comprometimento do destino celular. Os alvos genômicos de OCT4-SOX2 na crista neural diferem daqueles das células-tronco embrionárias, indicando que o dímero apresenta funções específicas ao contexto. A ligação de OCT4-SOX2 a intensificadores da crista neural requer o fator pioneiro TFAP2A, que interage fisicamente com o dímero para modificar seus alvos genômicos. Os resultados de Hovland et al (2022) demonstram como os fatores Yamanaka são reaproveitados em células multipotentes para controlar a organização da cromatina e definir seu potencial de desenvolvimento.
De acordo com Yamanaka (2020), o uso de células-tronco embrionárias e células tronco pluripotentes induzidas tem sido empregado como forma de terapia em casos de lesões e doenças. No entanto, em alguns ensaios clínicos com células-tronco embrionárias humanas, foram observados desafios como tumorigenicidade, imunogenicidade e heterogeneidade. Desse modo, essas adversidades destacam a importância de pesquisas adicionais para entender melhor as propriedades das células-tronco, desenvolver métodos de produção mais eficazes e aprimorar as técnicas de administração, visando minimizar esses riscos e maximizar os benefícios terapêuticos.
O estudo de Austin et al. (2022) revelou que os fatores identificados por Yamanaka têm o poder de afetar a organização do material genético e ajudar no desenvolvimento das células da crista neural, as quais desempenham um papel crucial na formação do sistema nervoso. Esse processo ocorre porque o par de proteínas OCT4-SOX2 regula a ativação ou desativação de genes dentro dessas células. Os locais específicos de DNA impactados pelo OCT4-SOX2 nas células da crista neural diferem daqueles presentes nas células-tronco embrionárias, o que sugere uma resposta singular dessas células aos estímulos de regulação.
Ainda sobre isso, Londrini et al (2020) aponta que a reprogramação de células somáticas adultas em células-tronco pluripotentes induzidas (iPSCs) revolucionou o complexo campo científico da modelagem de doenças e terapia personalizada. A diferenciação cardíaca de iPSCs humanas em cardiomiócitos (hiPSC-CMs) tem sido utilizada em uma ampla gama de modelos saudáveis e de doenças, derivando MCs de diferentes células somáticas. Embora, as hiPSC-CMs precisam ser aprimoradas, pois os protocolos existentes não são completamente capazes de obter MCs maduras que recapitulem as propriedades fisiológicas das células cardíacas adultas humanas. Portanto, melhorias e avanços capazes de padronizar as condições de diferenciação são necessários.
Ainda, em estudo semelhante, Munsunuru et al (2023) as células-tronco pluripotentes induzidas (iPSCs) oferecem uma oportunidade sem precedentes para estudar a fisiologia e as doenças humanas em nível celular. Elas também têm o potencial de serem utilizadas na prática da medicina de precisão, por exemplo, em testes personalizados de medicamentos. Esta declaração descreve de forma abrangente a procedência das linhagens de iPSCs, seu uso na modelagem de doenças cardiovasculares, seu uso na medicina de precisão e estratégias para promover seu uso mais amplo em aplicações biomédicas.
As iPSCs humanas apresentam propriedades que as tornam singularmente qualificadas como sistemas modelo para o estudo de doenças humanas: são de origem humana, o que significa que carregam genomas humanos; são pluripotentes, o que significa que, em princípio, podem ser diferenciadas em qualquer um dos tipos de células somáticas do corpo humano; e são células-tronco, o que significa que podem ser expandidas de uma única célula para milhões ou até bilhões de células descendentes (Munsumuru et al, 2023).
As iPSCs oferecem a oportunidade de estudar células geneticamente compatíveis com pacientes individuais, e ferramentas de edição genômica permitem a introdução ou correção de variantes genéticas. Houve progresso inicial no uso de iPSCs para melhor compreender cardiomiopatias, distúrbios do ritmo, distúrbios valvares e vasculares, e fatores de risco metabólicos para doença cardíaca isquêmica, começando a ser usadas para identificar os medicamentos ideais a serem usados em pacientes dos quais as células foram derivadas (Munsumuru et al, 2023).
De acordo com Garreta et al (2021), a geração de organoides é um dos maiores avanços científicos na medicina regenerativa. Em seu estudo, os autores, ao prolongar o tempo de exposição das células-tronco pluripotentes humanas (hPSCs) a um microambiente tridimensional e ao aplicar sinais indutivos renais definidos, geraram organoides renais que correspondem transcriptomicamente aos rins fetais humanos do segundo trimestre. Esses resultados foram validados usando ensaios ex vivo e in vitro que modelam o desenvolvimento renal. Além disso, foi desenvolvido um método de transplante que utiliza a membrana corioalantoica de galinha.
Essa abordagem de Garreta et al (2021) criou um microambiente in vivo flexível que promoveu o crescimento e a diferenciação dos organoides renais implantados, além de fornecer um componente vascular. A rigidez do microambiente da membrana corioalantoica in ovo foi recapitulada in vitro pela fabricação de hidrogéis complacentes. Esses biomateriais promoveram a geração eficiente de vesículas renais e estruturas de néfrons, demonstrando que um ambiente suave acelera a diferenciação de organoides renais derivados de hPSC.
Ainda, Wang et al (2022) destaca que Nas últimas décadas, o uso de organoides levou a uma compreensão avançada da composição de cada órgão digestivo e facilitou a modelagem de doenças, a previsão da dose de quimioterapia, a intervenção genética CRISPR-Cas9, a triagem de medicamentos de alto rendimento e a identificação de alvos para SARS-CoV-2 e infecção patogênica. No entanto, os organoides existentes do sistema digestivo incluem principalmente o sistema epitelial, sendo necessário estabelecer um modelo organoide mais completo e fisiológico.
De forma semelhante, Mansour et al (2024), para fornecer um modelo in vivo vascularizado e funcional de organoides cerebrais, estabeleceram um método para transplantar organoides cerebrais humanos para o cérebro de camundongos adultos. Os enxertos de organoides demonstraram diferenciação e maturação neuronal progressiva, gliogênese, integração da microglia e crescimento de axônios em múltiplas regiões do cérebro do hospedeiro. Imagens de dois fótons in vivo demonstraram redes neuronais e vasos sanguíneos funcionais nos enxertos. Por fim, o registro extracelular in vivo combinado com optogenética revelou atividade neuronal intraenxerto e sugeriu conectividade sináptica funcional enxerto-hospedeiro. Essa combinação de organoides neurais humanos e um ambiente fisiológico in vivo no cérebro animal pode facilitar a modelagem de doenças em condições fisiológicas.
Ilic e Ogilve (2022) ressaltam que mais da metade de todos os ensaios clínicos (51%) concentram-se no tratamento de doenças oculares degenerativas e neoplasias, envolvendo quase 2/3 de todos os participantes em ensaios clínicos baseados em hPSC. Embora não tenham sido relatados eventos adversos graves resultando em morte ou morbidade devido à terapia celular baseada em hPSC recebida, as informações sobre segurança e eficácia clínica ainda são muito limitadas.
Com a disponibilidade de novas tecnologias para edição precisa do genoma, uma nova tendência no desenvolvimento de terapias celulares baseadas em células-tronco gênicas humanas (hPSC) parece estar emergindo. A engenharia de linhagens universais de células-tronco gênicas (hPSC) de doadores tornou-se um santo graal nessa área. De fato, devido à sua eficácia e simplicidade, a nanomedicina e a administração in vivo de terapia gênica podem se tornar mais vantajosas do que as terapias celulares para o tratamento de múltiplas doenças (Ilic; Ogilve, 2022).
No entanto, para Cho et al (2024) ainda existem vários desafios que precisam ser enfrentados antes que essa abordagem possa ser aplicada à prática clínica. Esses desafios incluem otimizar a eficiência da reprogramação, compreender a célula de origem de cada fator de transcrição e desenvolver métodos para reprogramação em áreas da zona não subventricular. Mais pesquisas são necessárias para superar os desafios restantes, mas essa abordagem tem o potencial de revolucionar a forma como tratamos distúrbios do sistema nervoso central.
Por conseguinte, a obtenção de células-tronco para cultivo pode envolver questões éticas, principalmente quando se trata de células-tronco embrionárias, que são obtidas a partir de embriões humanos. Há preocupações éticas sobre a destruição de embriões, o consentimento informado e a proteção dos direitos dos doadores. Outrossim, antes que as terapias baseadas em células-tronco ou miniórgãos possam ser aplicadas clinicamente, é necessário garantir a segurança e a eficácia dessas abordagens por meio de rigorosos testes pré-clínicos e ensaios clínicos (Ilic; Ogilvie, 2022).
Sendo assim, isso requer tempo, recursos e considerações éticas para proteger os participantes de pesquisa e os potenciais pacientes. No entanto, ao longo dos anos, as enfermidades do sistema nervoso central, especialmente as neurodegenerativas, têm sido um desafio no campo da medicina, levando a uma busca incessante por terapias eficazes. Como resultado, o uso das iPSC no tratamento dessas complexas doenças foi novamente considerado (Cho et al, 2024).
Ademais, com o avanço da medicina, estudos também comprovaram a eficiência do uso de iPSC na prática da medicina de precisão, a fim de identificar os medicamentos ideais a serem usados em pacientes dos quais as células foram derivadas, em doenças cardiovasculares. Logo, o fato de serem geneticamente combinados com a pessoa de quem foram derivados os torna ideais para o estudo de doenças com forte causa genética subjacente, o que permite entender melhor como os genótipos da doença no nível genético se manifestam como fenótipos no nível celular (Musunucu et al., 2018).
Em suma, a criação de miniórgãos humanos, conhecidos como organóides, representa um dos mais significativos avanços da ciência na área da medicina de precisão. Essa técnica inovadora se utiliza de métodos tradicionais de cultivo tridimensional, que possibilita a auto-organização das células-tronco para originar réplicas em micro e milímetros de órgãos humanos. A intersecção entre a tecnologia dos organóides e o transplante de órgãos ainda está em estágios iniciais, porém espera-se que essa parceria abra novas possibilidades para revolucionar não só os transplantes, mas também a pesquisa envolvendo os organoides.
CONSIDERAÇÕES FINAIS
A presente revisão sistemática demonstrou que a utilização de células-tronco pluripotentes induzidas (iPSCs) no cultivo de miniórgãos representa um avanço substancial na medicina de precisão, oferecendo novas possibilidades para a modelagem de doenças, desenvolvimento de terapias personalizadas e estudos pré-clínicos de medicamentos. A criação de organoides, por meio de técnicas sofisticadas de cultivo celular tridimensional, permite a reprodução de estruturas humanas complexas em laboratório, o que favorece uma abordagem mais específica e eficaz no diagnóstico e tratamento de diversas enfermidades, especialmente aquelas de origem genética ou idiopática.
No entanto, apesar dos avanços científicos relevantes, ainda persistem desafios técnicos, regulatórios e éticos que precisam ser superados para a plena integração dessa tecnologia à prática clínica. A padronização dos protocolos, a estabilidade genética das células, os riscos associados à pluripotência e a garantia da segurança em ensaios clínicos são fatores que exigem contínuo investimento em pesquisa e regulamentação. Portanto, é essencial que novas investigações sejam estimuladas, tanto para aprimorar os métodos já existentes quanto para consolidar a aplicação clínica das iPSCs e organoides. Com isso, a medicina de precisão poderá alcançar um novo patamar, promovendo cuidados cada vez mais individualizados, eficazes e eticamente sustentáveis.
REFERÊNCIAS
AGUIRRE, Marisol; et al. Application of the Yamanaka Transcription Factors Oct4, Sox2, Klf4, and c-Myc from the Laboratory to the Clinic. Genes vol. 14,9 1697. 26 Aug. 2023. Disponível em: https://doi.org/10.3390/genes14091697. Acesso: 19 de abr.2024.
BERISHVILI, Ekaterine; et al. Mini-organs forum: how to advance organoid technology to organ transplant community.” Transplant international : official journal of the European Society for Organ Transplantation vol. 34,9. 2021. Disponível em: https://doi.org/10.1111/tri.13988. Acesso em 23 de abr.2024.
CHO, Han Eol; et al. In Vivo Reprogramming Using Yamanaka Factors in the CNS: A Scoping Review. Cells vol. 13,4 343. 15 Feb. 2024. Disponível em: https://doi.org/10.3390/ cells13040343. Acesso: 20 de abr.2024.
FUS-KUJAWA, Agnieszka; et al. Potential of Induced Pluripotent Stem Cells for Use in Gene Therapy: History, Molecular Bases, and Medical Perspectives. Biomolecules vol. 11,5 699. 7 May. 2021. Disponível em: https://doi.org/10.3390/biom11050699. Acesso em: 21 de abr.2024.
GARRETA, E.; et al. Fine tuning the extra-cellular environment accelerates the derivation of kidney organoids from human pluripotent stem cells. Nat Mar 2021. Disponível em: https://doi.org/10.1038/s41563-019-0287-6. Acesso: 23 de abr.2024.
HOVLAND, Austin S.; et al. Pluripotency factors are repurposed to shape the epigenomic landscape of neural crest cells. Developmental cell vol. 57,19. 2022. Disponível em: https://doi.org/10.1016/j.devcel.2022.09.006. Acesso: 20 de abr.2024.
ILIC, Dusko; OGILVIE, Caroline. Pluripotent Stem Cells in Clinical Setting-New Developments and Overview of Current Status.” Stem cells (Dayton, Ohio) vol. 40,9. 2022. Disponível em: https://doi.org/10.1093/stmcls/sxac040. Acesso: 20 de abr.2024.
LODRINI, Alessandra Maria; et al. Human Induced Pluripotent Stem Cells Derived from a Cardiac Somatic Source: Insights for an In-Vitro Cardiomyocyte Platform. International journal of molecular sciences vol. 21,2 507. 13 Jan. 2020. Disponível em: https://doi.org/10.3390/ ijms21020507. Acesso em: 23 de abr.2024.
MANSOUR, Abed AlFatah; et al. An in vivo model of functional and vascularized human brain organoids. Nature biotechnology vol. 36,5. 2024. Disponível em: https://doi.org/10.1038/nbt.4127. Acesso: 20 de abr.2024.
MUSUNURU, Kiran; et al. Induced Pluripotent Stem Cells for Cardiovascular Disease Modeling and Precision Medicine: A Scientific Statement From the American Heart Association. Circulation. Genomic and precision medicine vol. 11,1. 2023. Disponível em: 10.1161/HCG.0000000000000043. Acesso em: 21de abr.2024.
SISODIYA, Sanjay M. Precision medicine and therapies of the future. Epilepsia vol. 62 Suppl 2, Suppl 2. 2021. Disponível em: https://doi.org/10.1111/epi.16539. Acesso em: 23 de abr.2024.
WANG, Qinying; et al. Applications of human organoids in the personalized treatment for digestive diseases. Signal Transduct Target Ther, 2022 Sep 27;7:336. Disponível em: 10.1038/s41392-022-01194-6. Acesso em 16 mai. 2025.
YAMANAKA, Shinya. Pluripotent Stem Cell-Based Cell Therapy-Promise and Challenges. Cell stem cell vol. 27,4, 2020. Disponível em: https://doi.org/10.1016/j.stem.2020.09.014. Acesso: 19 de abr.2024.
ZHAO, Zeguo; et al. Structural Design of engineered Costimulation Determines Tumor Rejection Kinetcs and Persistence of CAR T Cells. Cancer cell vol. 28,4. 2015. Disponível em: https://doi.org/10.1016. Acesso em: 21de abr.2024.
1Acadêmica. Universidade Grande Rio Afya – Duque de Caxias-RJ, Brasil.
2Orientador. Universidade Grande Rio Afya – Duque de Caxias-RJ, Brasil. Instituição: Universidade do Grande Rio Afya – Duque de Caxias-RJ, Brasil.
