ENVIRONMETAL IMPACTS ON HUMAN GENETIC DEVELOPMENT
REGISTRO DOI: 10.69849/revistaft/ni10202410310758
Marinna de Freitas Menezes1; Mariana Oliveira1; Nathália Gomes Marques1; Cleide de Assis Cipriani1; Ramon Reis1; Orientadora: Gabriela Barreto dos Reis2
Resumo
Introdução: O desenvolvimento humano é um processo complexo que vai além das informações codificadas no DNA.Fatores ambientais, como disponibilidade de recursos, temperatura, poluição e interações sociais, têm demonstrado influenciar de maneira significativa o desenvolvimento e a saúde dos indivíduos. Metodologia: Este estudo consiste em uma revisão sistemática da literatura, com o objetivo de analisar o impacto do ambiente no desenvolvimento genético. A seleção dos artigos seguiu critérios rigorosos para garantir a qualidade e a relevância da pesquisa. As fontes das pesquisas foram selecionadas a partir de bases de dados acadêmicas de renome, incluindo PubMed, Scopus, Web of Science, Google Scholar e SciELO. Desenvolvimento: Mecanismos como a metilação do DNA e as modificações das histonas são exemplos de como fatores externos, como dieta, estresse e exposição a toxinas, podem alterar a forma como os genes se expressam. A cromatina é a manifestação física do epigenoma e desempenha um papel de memória no que diz respeito à metilação do DNA, às modificações de histonas e à organização tridimensional (3D). Essa memória epigenética não apenas influencia a expressão gênica temporária, mas também reflete decisões permanentes sobre o destino das células. Conclusão: Constatou-se que o ambiente exerce uma influência complexa na expressão genética, pela epigenética, que atua como uma interface entre o DNA e o externo. A epigenética não apenas enriquece nossa compreensão da biologia humana, mas também oferece uma nova perspectiva sobre a prevenção e o tratamento de doenças, destacando a importância de um ambiente saudável e de experiências positivas durante as fases críticas do desenvolvimento.
Palavras-chave: “ epigenômica”, “herança genética”, “antioxidantes and expressão gênica”, “meio ambiente and nutrição”, “ nutrigenômica”
Abstract
Human development is a complex process that goes beyond information encoded in DNA. Environmental factors, such as availability of resources, temperature, pollution and social interactions, have been shown to significantly influence development and the health of individuals. This study consists of a systematic review of literature, with the objective of analyzing the environmental impact of genetic development. The selection of articles followed strict criteria to ensure the quality and relevance of the research. The sources of the research were selected from bases de dados acadêmicas de renome, including PubMed, Scopus, Web of Science, Google Scholar and SciELO. Desenvolvimento: Mechanisms such as DNA methylation and histone modifications are examples of external factors, such as diet, stress and exposure to toxins, that can alter the way genes are expressed. Chromatina is the physical manifestation of the epigenome and plays a role in memory of methylation of DNA, modifications of histones and tridimensional organization (3D). This epigenetic memory does not only influence temporary genetic expression, but also reflects permanent decisions about the fate of cells. Epigenetics not only enriches our understanding of human biology, but also offers a new perspective on the prevention and treatment of diseases, highlighting the importance of a healthy environment and positive experiences during the critical phases of development.
Keywords: epigenomics”,”genetic inheritance”, “antioxidants and gene protection”, “environment and nutrition”, “nutrigenomics”
1 INTRODUÇÃO
O desenvolvimento humano é um processo complexo que vai além das informações codificadas no DNA. A interação entre os fatores genéticos e as condições ambientais molda não apenas a aparência física, mas também o comportamento, a saúde e a qualidade de vida. Estudos recentes têm destacado a importância da epigenética, um campo que investiga como elementos externos podem influenciar a expressão gênica, sugerindo que as experiências vividas, desde a gestação até a infância, têm impactos duradouros na saúde futura (SILVA; COSTA, 2021).
A relação entre o ambiente e o desenvolvimento genético é uma das fronteiras mais intrigantes da biologia. Historicamente, a genética tem sido vista como um determinante primordial na formação das características de um organismo, mas pesquisas recentes revelam um quadro mais complexo, onde fatores ambientais desempenham um papel igualmente crucial. Desde a disponibilidade de nutrientes até as interações sociais, o ambiente se configura como um ator ativo que influencia a expressão genética e, por consequência, o fenótipo dos indivíduos (SILVA et al., 2024), influenciando o comportamento, a saúde e a qualidade de vida ao longo dos anos.
Fatores ambientais, como disponibilidade de recursos, temperatura, poluição e interações sociais, têm demonstrado influenciar de maneira significativa o desenvolvimento e a saúde dos indivíduos (SOUZA et al., 2020). Embora o código genético forneça as diretrizes fundamentais para o crescimento e a funcionalidade dos organismos, as condições em que um indivíduo se desenvolve podem alterar significativamente a expressão desses genes.
Sendo assim, a epigenética surge como uma área crucial de estudo, evidenciando como experiências e ambientes podem moldar a saúde e o comportamento ao longo da vida (SILVA; COSTA, 2021). Esse processo multifacetado resulta da interação complexa entre genética e ambiente. Embora o material genético forneça as bases para o crescimento e a funcionalidade dos organismos, as condições em que um indivíduo se desenvolve podem impactar significativamente a maneira como esses genes se manifestam (SILVA; COSTA, 2021).
Justifica-se a relevância deste estudo pela crescente necessidade de compreender as complexas relações que regem a biodiversidade em um mundo marcado por rápidas mudanças climáticas e degradação ambiental. À medida que as pressões ambientais aumentam, a capacidade de adaptação dos organismos torna-se crucial para a sobrevivência e manutenção da biodiversidade (COSTA et al., 2023). Assim, este trabalho busca contribuir para o avanço do conhecimento sobre a interdependência entre genética e ambiente, ressaltando a importância de uma abordagem integrada na biologia.
2 FUNDAMENTAÇÃO TEÓRICA OU REVISÃO DA LITERATURA
2.1 CONCEITOS BÁSICOS DE GENÉTICA E EPIGENÉTICA
A genética é o ramo da biologia que estuda a hereditariedade e a variação dos organismos. Os genes, que são as unidades básicas da hereditariedade, contêm as instruções necessárias para a síntese de proteínas e RNA, desempenhando um papel crucial no desenvolvimento e funcionamento dos organismos. A transmissão de características de uma geração para outra ocorre através de mecanismos complexos, incluindo a interação entre alelos dominantes e recessivos, bem como a influência do ambiente sobre a expressão gênica. Além disso, a epigenética, que investiga modificações na expressão gênica que não envolvem alterações na sequência do DNA, tem se mostrado fundamental para entender como fatores externos podem impactar a hereditariedade e a saúde (GILBERT, 2016, p. 45; Kearsey e Farquhar (2020); SILVA, 2021, p. 15).
Os genes podem ser classificados em três categorias principais: genes estruturais, que codificam proteínas; genes reguladores, que controlam a expressão gênica; e genes não codificantes, que desempenham funções regulatórias sem codificar proteínas (SILVA, 2020, p. 45). Os genes se organizam em cromossomos, que são estruturas filamentosas localizadas no núcleo celular, compostas por DNA e proteínas (ALMEIDA, 2020, p. 28). Cada gene pode apresentar dois alelos, que são variantes que ocupam a mesma posição em cromossomos homólogos e podem influenciar características específicas (PEREIRA, 2021, p. 50).
O DNA (ácido desoxirribonucleico) é a molécula que armazena a informação genética necessária para o desenvolvimento e funcionamento dos organismos (MARTINS, 2019, p. 42), enquanto o RNA (ácido ribonucleico) desempenha um papel crucial na transcrição e tradução da informação genética, atuando como intermediário entre o DNA e a síntese de proteínas” (COSTA, 2022, p. 33).
2.2 CLASSIFICAÇÕES DA GENÉTICA
Hwang et al. (2020) afirmam que a genética clássica serve como base para a análise dos padrões de herança e das variações fenotípicas observadas em diferentes populações. Além disso, de acordo com Alberts et al. (2019), a genética molecular é essencial para compreender os mecanismos que regulam a expressão gênica e a interação entre DNA, RNA e proteínas. Assim, segundo Wang et al. (2021), a genética populacional estuda como as forças evolutivas afetam a diversidade genética dentro e entre ambientes.
Por outro lado, conforme Gilbert (2021), a genética de desenvolvimento explora os processos moleculares que regulam a formação de estruturas durante o desenvolvimento embrionário. Nesse contexto, a genética médica, como descrito por Hampel et al. (2021), é uma especialidade que se dedica ao diagnóstico, manejo e aconselhamento de condições genéticas, integrando conhecimentos de genética molecular, biologia e medicina para otimizar a saúde do paciente.
Por último, como proposto por Mardis (2021), a genômica tem implicações significativas na medicina personalizada, permitindo a identificação de predisposições genéticas e o desenvolvimento de terapias direcionadas.
2.3 EPIGENÉTICA
A epigenética é um campo em rápida evolução que investiga como modificações químicas no DNA e nas proteínas associadas podem influenciar a expressão gênica sem alterar a sequência do DNA. Essas modificações incluem metilação do DNA, modificações das histonas e a ação de RNA não codificantes. A epigenética desempenha um papel fundamental em processos biológicos, como desenvolvimento embrionário, diferenciação celular e resposta a estressores ambientais. Além disso, as alterações epigenéticas têm sido implicadas em várias doenças, incluindo câncer, doenças neurodegenerativas e distúrbios metabólicos, onde a desregulação dos mecanismos epigenéticos pode levar à ativação de oncogenes ou à inativação de genes supressores de tumor (KIM; HONG, 2021, p. 123).
Adicionalmente, as modificações epigenéticas desempenham um papel crucial na regulação da expressão gênica e na adaptação a fatores ambientais (KIM et al., 2022). Nesse contexto, a interação entre genética e epigenética é fundamental para entender a complexidade das doenças multifatoriais (LI et al., 2021).
García et al. (2021) discutem como a epigenética pode ajudar a elucidar os mecanismos subjacentes ao desenvolvimento de doenças crônicas. De fato, estudos demonstram que a exposição a poluentes pode induzir alterações epigenéticas que afetam a saúde humana (PARK et al., 2020). Portanto, a regulação epigenética é um mecanismo crucial que controla a expressão gênica em resposta a fatores ambientais, influenciando processos como desenvolvimento, diferenciação celular e patogênese de doenças (MIRANDA et al., 2022).
3 METODOLOGIA
Este estudo consiste em uma revisão sistemática da literatura, com o objetivo de analisar o impacto do ambiente no desenvolvimento genético. A seleção dos artigos seguiu critérios rigorosos para garantir a qualidade e a relevância da pesquisa.
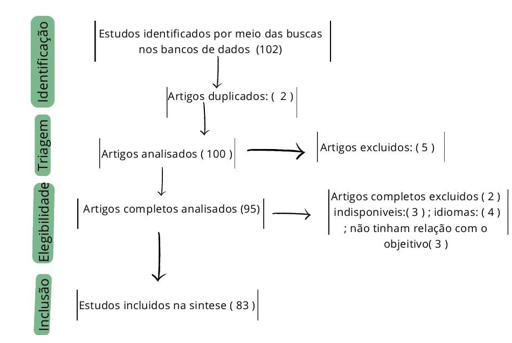
A metodologia seguiu várias etapas, começando com a seleção de fontes. Os critérios de inclusão foram definidos como segue: Foram incluídos estudos sem restrição ao ano de publicação, em inglês, português e espanhol, abrangendo artigos revisados por pares, diretrizes clínicas, revisões sistemáticas e metanálises, que abordassem especificamente a interação entre fatores ambientais e o desenvolvimento genético em seres humanos. Contudo, os critérios de exclusão abrangeram artigos que não fossem revisados por pares, aqueles que não tratassem da interação entre ambiente e genética, revisões de literatura que não apresentassem dados originais e trabalhos publicados em idiomas distintos dos estabelecidos.
As fontes das pesquisas foram selecionadas a partir de bases de dados acadêmicas de renome, incluindo PubMed, Scopus, Web of Science, Google Scholar e SciELO. Essas plataformas foram escolhidas devido à sua abrangência e ao acesso a uma ampla gama de estudos relevantes. A estratégia de busca foi meticulosamente elaborada utilizou os termos indexados do Medical Subject Headings (MeSH) e descritores em Ciências da Saúde relacionadas a “ epigenômica”, “herança genética”, “antioxidantes and expressão gênica”, “meio ambiente and nutrição”, “ nutrigenômica”. Os termos foram combinados por meio de operadores booleanos (AND, OR) para maximizar a relevância dos resultados. A filtragem dos artigos foi realizada, resultando em uma seleção de trabalhos que atendessem aos critérios estabelecidos.
Os dados coletados foram analisados e sintetizados por meio de um processo sistemático. Inicialmente, foi realizada a extração de dados, onde informações relevantes foram extraídas de cada artigo, incluindo autores, ano de publicação, objetivos do estudo, métodos utilizados, principais achados e conclusões. Em seguida, os dados foram organizados em categorias temáticas, refletindo diferentes aspectos do impacto ambiental no desenvolvimento genético, como poluição, dieta, estresse ambiental e fatores socioeconômicos.
4 RESULTADOS E DISCUSSÕES OU ANÁLISE DOS DADOS
4.1 FATORES AMBIENTAIS E EXPRESSÕES GÊNICAS
Os fatores ambientais desempenham um papel crucial na regulação da expressão gênica, influenciando como e quando os genes são ativados ou desativados. Nesse sentido, a interação entre o ambiente e a genética é um campo de estudo importante na biologia moderna, conhecido como epigenética. Mecanismos como a metilação do DNA e as modificações das histonas são exemplos de como fatores externos, como dieta, estresse e exposição a toxinas, podem alterar a forma como os genes se expressam. Essas alterações epigenéticas têm implicações significativas em saúde e doença, contribuindo para condições como câncer, doenças metabólicas e neurodegenerativas (SMITH; JONES, 2020, p. 78).
Além disso, Wang et al. (2020) afirmam que fatores ambientais, como dieta, estresse e exposição a toxinas, podem induzir modificações epigenéticas que influenciam a expressão gênica, afetando assim a saúde e o desenvolvimento de doenças. Murphy et al. (2022) ressaltam que a alimentação da mãe durante a gestação pode impactar a saúde do filho ao longo da vida, incluindo aspectos relacionados à expressão gênica. Investigações demonstram que a ingestão de nutrientes selecionados pela mãe pode ter um papel significativo na metilação do DNA, impactando a expressão de genes vitais para o desenvolvimento fetal (PEREIRA, 2022).
De acordo com Huang et al. (2020), as alterações nas modificações das histonas durante a gestação podem levar à desregulação na expressão de genes críticos para o crescimento e desenvolvimento fetal. Por fim, segundo Zhang et al. (2020), os microRNAs desempenham um papel vital na regulação da expressão gênica durante o desenvolvimento fetal, sendo influenciados pela nutrição materna.
4.2 CONDIÇÕES GENÉTICAS RELACIONADAS AO AMBIENTE
4.2.1 Dieta e Nutrição
A cromatina é a manifestação física do epigenoma e desempenha um papel de memória no que diz respeito à metilação do DNA, às modificações de histonas e à organização tridimensional (3D). Essa memória epigenética não apenas influencia a expressão gênica temporária, mas também reflete decisões permanentes sobre o destino das células. A memória é fundamentada em um processo de programação epigenética, guiado por sinais extracelulares e intracelulares que são reconhecidos por fatores de transcrição e modificadores de cromatina. Muitas moléculas presentes na dieta e seus metabólitos intermediários atuam como esses sinais, ou seja, contribuem para a programação epigenética e para a formação da memória. (CARLBERG, C.; VELLEUER E., 2023).
De acordo com LY (2018), a nutrição é um dos fatores ambientais mais significativos que influenciam os processos iniciais de desenvolvimento, regulando mecanismos epigenéticos durante a gravidez e os períodos neonatais. As dietas maternas e as composições nutricionais específicas são essenciais para estabelecer os perfis epigenéticos no feto, afetando a suscetibilidade a diversas doenças e distúrbios na vida futura. HSU e TAIN (2019) ampliam essa perspectiva ao afirmarem que o consumo excessivo ou deficiente de nutrientes específicos está relacionado à programação do desenvolvimento de várias doenças não transmissíveis (DNTs), como hipertensão, doenças cardiovasculares, diabetes e obesidade. Assim, a desnutrição é associada a doenças cardiovasculares e sobrepeso, enquanto a supernutrição está mais relacionada à pressão arterial elevada e obesidade na prole.
Além disso, o acúmulo de lipídios e ácidos graxos tem uma forte correlação com a predisposição a doenças cardiovasculares (FLEMING et al., 2018). Um estudo utilizando um modelo murino evidenciou que mães que seguiram uma dieta pobre em proteínas durante o período de pré-implantação (dias 0 a 3,5 do desenvolvimento embrionário) apresentaram uma prole que desenvolveu hipertensão arterial na vida pós-natal (WATKINS et al., 2011, apud LAMBERTO et al., 2021).
Essa relação entre a alimentação materna e a saúde do prole é ainda mais evidenciada pelo impacto dos alimentos ultraprocessados. Monteiro et al. (2019), são formulações industriais que contêm ingredientes não utilizados na culinária doméstica, como aditivos e conservantes, e estão associados a diversas doenças crônicas. Um estudo realizado no Brasil por Alves-Santos et al. (2019) indicou que uma dieta caracterizada como “altamente processada”, baseada em registros alimentares das mães que mostraram maior consumo de grãos refinados, alimentos ricos em gorduras e baixo teor de fibras, aumentou o risco de dar à luz um bebê pequeno para a idade gestacional (PIG), definido como um peso ao nascer abaixo do 10º percentil de uma referência.
Nesse contexto, a ingestão adequada de nutrientes essenciais, como o folato, torna-se ainda mais relevante. O folato é um micronutriente vital do complexo de vitaminas B, que participa de diversos processos fisiológicos e é especialmente crucial para o crescimento e desenvolvimento fetal. Ele desempenha um papel fundamental na síntese, reparo e metilação do DNA, contribuindo para a formação de novas células e tecidos (BJORKE-MONSEN; UELAND, 2023).
Um estudo realizado no Nepal mostrou que a suplementação materna com ácido fólico, ferro e zinco levou a um menor índice de massa gorda (IMG) nas crianças em comparação àquelas nascidas de mães do grupo controle (STEWART, CP. et al, 2009, apud, DANIEL J.H. , 2021).
Além disso, a nutrição na infância pode influenciar significativamente o curso do desenvolvimento por meio de modificações no epigenoma (LILLYCROP e BURDGE, 2015). Um exemplo emblemático dessa epigenética nutricional pode ser observado nas larvas fêmeas de abelhas, que se desenvolvem em rainhas ou operárias estéreis dependendo do consumo de geleia real. A pesquisa de MALESZKA (2008, apud SHIZHAO LI et al., 2019) sugere que a proporção de larvas que se tornam rainhas aumenta com a redução da DNMT3 (DNA metiltransferase 3), indicando que a metilação do DNA atua como um mediador entre a ingestão de geleia real na juventude e o fenótipo adulto. Outro fator que também pode ter efeito prejudicial ao feto, é a ingestão precoce de certos alimentos. Os resultados de uma meta-análise demonstra que a exposição ao álcool durante a gravidez pode comprometer a síntese de proteínas, o splicing do mRNA e o ajuste da cromatina em embriões de roedores (ROGIC, S.; WONG, A.; PAVLIDIS, P., 2016).
4.2.2 Exposição a toxinas
As toxinas ambientais, como metais pesados e pesticidas, exercem um impacto significativo na saúde humana, especialmente em relação a distúrbios neuronais. Essas substâncias podem provocar mudanças epigenéticas nas células germinativas, afetando a expressão gênica e a estrutura da cromatina, o que, por sua vez, impacta o desenvolvimento e aumenta a predisposição a doenças em gerações futuras (NILSSON et al., 2022). Além disso, elas alteram perfis transcricionais de genes essenciais para processos como proliferação celular, apoptose e resposta ao estresse oxidativo (SONG; RYU, 2015). Toxinas produzidas por patógenos também podem afetar a sinalização celular, resultando em alterações na expressão de genes relacionados à resposta imune (COSTA, 2021).
A intoxicação por metais pesados, como cádmio, chumbo, mercúrio e arsênio, é uma preocupação crescente, especialmente em regiões contaminadas, como áreas de mineração, onde a poluição do solo e da água representa riscos significativos à saúde (BRANDÃO et al., 2024). Esses metais interrompem processos metabólicos, principalmente a glicólise e o ciclo do ácido tricarboxílico, elevando os níveis de lactato e piruvato no sangue. A intoxicação por metais pesados pode levar a uma diminuição acentuada dos aminoácidos essenciais nos rins, comprometendo sua função (POPOESCU & KALININ, 2023). Sintomas comuns incluem hipertensão, danos renais, problemas respiratórios e distúrbios gastrointestinais, como cólicas abdominais e náuseas (LAVEKAR, G. S., 2019). Casos de envenenamento, frequentemente relacionados a remédios populares, mostram sintomas distintos, com envenenamentos por mercúrio e chumbo sendo particularmente prevalentes (CHANGJIANG et al., 2024).
Os pesticidas, utilizados na agricultura para controlar pragas, também representam riscos significativos à saúde e ao meio ambiente, especialmente quando aplicados em excesso e sem precauções adequadas (MARCELINO et al., 2019; RANI et al., 2021). Essas substâncias podem induzir alterações genéticas e epigenéticas, afetando a expressão de microRNA e os padrões de metilação do DNA, o que pode prever a exposição a esses produtos químicos e as doenças associadas (GIAMBÒ et al., 2021). Por exemplo, genes relacionados ao desenvolvimento do nociceptor, como Prdm12, apresentam uma expressão aumentada após exposição ao malatião em embriões, sugerindo um impacto direto no desenvolvimento neuronal (DONOSO et al., 2023).
A exposição a neurotoxinas ambientais está ligada a transtornos neurodegenerativos, neurodesenvolvimentais e psiquiátricos, resultando em inflamação cerebral e morte celular neuronal (Aggarwal et al., 2022). O clorpirifós, um inseticida organofosforado, também tem sido associado a alterações na expressão de genes biomarcadores em células-tronco embrionárias, indicando uma potencial toxicidade neurodesenvolvimental (ESTEVAN et al., 2014).
4.2.3 Estresse e Saúde Mental
O estresse materno durante a gestação tem um papel crucial na modificação da metilação do DNA, especialmente em genes associados ao estresse, como o transportador de serotonina (SLC6A4) (NAZZARI et al., 2023). Essas alterações epigenéticas, resultantes de condições ambientais adversas, podem levar a mudanças duradouras na expressão genética e impactar a saúde da prole. A variação epigenética, como a metilação do DNA, atua como um mecanismo pelo qual o estresse materno influencia a saúde infantil, uma vez que é sensível a fatores ambientais e pode regular mudanças a longo prazo na expressão gênica (QUINN et al., 2023).
O estresse pré-natal está vinculado a uma série de resultados comportamentais e de desenvolvimento adversos, incluindo uma maior vulnerabilidade a condições como transtorno do espectro autista (TEA), esquizofrenia e distúrbios emocionais (DAVID et al., 2021). Nesse contexto, os microRNAs (miRNAs) emergem como reguladores chave da expressão genética e estão implicados na resposta ao estresse materno. Um estudo identificou que a exposição ao estresse durante a gestação resultou na expressão diferencial de 119 miRNAs, dos quais 90 mostraram uma expressão dependente do estresse. MiRNAs específicos, como miR-1224-5p, miR-331-3p e miR-145-5p, foram destacados por suas funções potenciais na mediação dos efeitos do estresse na via serotoninérgica, que é fundamental para a regulação emocional e comportamental (BEVERSDORF et al., 2021).
Além disso, o estresse materno provoca alterações em marcadores inflamatórios e endócrinos nos tecidos uterinos, levando a mudanças transgeracionais na expressão genética por meio de mecanismos epigenéticos que afetam o desenvolvimento e a saúde da prole (LOPES et al., 2023). Pesquisas em modelos animais e humanos indicam que as condições ambientais influenciam a maturação dos oócitos, resultando em potenciais consequências a longo prazo para o desenvolvimento. Alterações na linha germinativa estão associadas a essas exposições ambientais; por exemplo, o estresse psicológico pode comprometer a competência do oócito, enquanto a exposição ao bisfenol A (BPA) é relacionada a efeitos negativos na maturação do oócito, qualidade e implantação do embrião. (MELDRUM et al., 2016).
5 CONCLUSÃO/CONSIDERAÇÕES FINAIS
O estudo entre ambiente e genética revela essencial uma compreensão abrangente do desenvolvimento humano. Através da revisão, constatou-se que o ambiente exerce uma influência complexa na expressão genética, pela epigenética, que atua como uma interface entre o DNA e o externo. Observa-se que fatores como a nutrição, exposição a poluentes, estresse e interações sociais podem modificar padrões de expressão gênica, impactando o fenótipo e, a saúde.
Essa abordagem proporciona uma visão mais realista onde o ambiente não é um cenário passivo, mas sim um fator que pode moldar a biologia humana. A análise de dados epigenéticos aponta plasticidade se pensava, a importância de políticas públicas de saúde preventiva. Em um mundo marcado por mudanças climáticas e desafios socioambientais, compreender a influência ambiental sobre o desenvolvimento genético humano é essencial para mitigar impactos negativos e promover uma qualidade de vida para futuras gerações.
A epigenética não apenas enriquece nossa compreensão da biologia humana, mas também oferece uma nova perspectiva sobre a prevenção e o tratamento de doenças, destacando a importância de um ambiente saudável e de experiências positivas durante as fases críticas do desenvolvimento. Essa abordagem integrada pode transformar a forma como abordamos a saúde e o bem-estar, promovendo uma visão holística que considera tanto os fatores genéticos quanto os ambientais na formação da saúde individual e coletiva.
Portanto, este trabalho contribui para o avanço do conhecimento sobre o desenvolvimento humano ao demonstrar que o ambiente desempenha um papel indispensável na regulação genética e nas condições de saúde e bem-estar. Ressalta-se novos estudos para aprofundar e incentivar uma pesquisa e intervenção que contemple essa interdependência.
REFERÊNCIAS
ALMEIDA, F. P. Cromossomos e Genes: Estruturas e Funções. 2. ed. Rio de Janeiro: Editora Acadêmica, 2020.
ALMEIDA, J. R. Herança genética: conceitos e aplicações clínicas. São Paulo: Editora Saúde, 2021.
ALVES, M. R.; COSTA, T. A.; NUNES, D. S. Desafios contemporâneos na conservação: uma análise integrativa. Revista Brasileira de Conservação, 101-117, 2023.
AGGARWAL, V.; MEHNDIRATTA, M. M.; WASAY, M.; GARG, D. Environmental toxins and brain: life on Earth is in danger. Annals of Indian Academy of Neurology. 2022.
BROWN, T. A.; SMITH, J. M. Understanding Recessive Inheritance: Implications for Genetic Counseling. Genetics in Medicine, 2021.
CAMPOS, R. A.; SILVA, T. H.; PEREIRA, L. F. Herança genética: uma revisão crítica. Revista Brasileira de Genética, v. 34, n. 2, p. 123-135, 2021.
CARLBERG, C.; VELLEUER, E. Nutrição e programação epigenética. “Opinião Atual em Nutrição Clínica e Cuidados Metabólicos”, v. 26, n. 3, p. 259-265, maio 2023.
CHANGJIANG, X.; ZHU, X.; WU, N.; YE, Q. Envenenamento por metais pesados causado por remédios populares chineses em pacientes com psoríase: uma análise retrospectiva. “Relatórios de Ciências Odontológicas”, v. 14, 2024.
CHINNERY, P. F.; SAMUELS, D. C. Mitochondrial genetics. In: Genetics of Human Disease. New York: Academic Press, 2016.
COSTA, A. Fundamentos de Biologia Molecular. 4. ed. São Paulo: Editora Científica, 2022.
COSTA, E. de S. Intoxicação por metais pesados na mineração e seu impacto na saúde humana. Foco, v. 16, n. 6, p. e2319, 2023.
COSTA, J. F.; ALMEIDA, P. R.; SOUZA, L. M. A influência do ambiente no desenvolvimento genético: uma revisão. Biologia e Conservação, 111-126, 2020.
COSTA, M. R.; SILVA, A. F. Epigenética: a interface entre genética e ambiente. Revista Brasileira de Genética, v. 45, n. 1, p. 45-57, 2021.
COSTA, R. J.; SILVA, L. M.; ALMEIDA, F. P. Ambiente e genética: um diálogo em evolução. Ecologia e Biologia, 33-50, 2024.
DONOSO, V. A.; WHITSON, J.; LOM, B. Developmental exposure to the pesticide malathion enhances expression of Prdm12, a regulator of nociceptor development, in Xenopus laevis. microPublication Biology, 2023.
ESTEVAN, C. et al. Organophosphorus pesticide chlorpyrifos and its metabolites alter the expression of biomarker genes of differentiation in D3 mouse embryonic stem cells in a comparable way to other model neurodevelopmental toxicants. Chemical Research in Toxicology, 2014.
FLEMING, T. P. et al. Origins of lifetime health around the time of conception: causes and consequences. The Lancet, v. 391, n. 10132, p. 1842-1852, 2018.
GARCÍA, A. et al. The role of epigenetics in the development of chronic diseases. Frontiers in Genetics, 2021.
GIAMBÒ, F. et al. Genetic and epigenetic alterations induced by pesticide exposure: integrated analysis of gene expression, microRNA expression, and DNA methylation datasets. International Journal of Environmental Research and Public Health, 2021.
GILBERT, S. F. Developmental Biology. 11. ed. Sunderland: Sinauer Associates, 2021..
HAMPER, H.; et al. The role of genetic testing in the management of hereditary cancer syndromes. Nature Reviews Clinical Oncology, 2021.
HOFFMAN, D. J.; POWELL, T. L.; BARRETT, E. S.; HARDY, D. B. Origens do desenvolvimento das doenças metabólicas. “Physiological Reviews”, 28 maio 2021.
HSU, C. N.; TAIN, Y. L. O bom, o mau e o feio dos nutrientes da gravidez e da programação do desenvolvimento de doenças adultas. Nutrients, v. 11, n. 4, p. 894, 2019.
HWANG, J. Y. et al. The role of classical genetics in modern biology. Nature Reviews Genetics, 2020.
JOO, H. S. et al. Mecanismo de regulação genética por uma toxina de Staphylococcus aureus. mBio, v. 7, n. 5, 1579-16, 2016.
KAMINSKI, K. et al. Polygenic Risk Scores: A New Tool for Predicting Complex Traits and Diseases. Nature Reviews Genetics, 2022.
KATO, K.; YAMADA, T.; NAKAMURA, Y. Interações gene-ambiente em doenças complexas: uma revisão da literatura. “Frontiers in Genetics”, v. 11, p. 564, 2020.
KEARSEY, M. J.; FARQUHAR, A. A genética da hereditariedade. “Nature Reviews Genetics”, v. 21, n. 1, p. 1-2, 2020.
KIM, J. H. et al. Regulação epigenética da expressão gênica em resposta a estímulos ambientais. “Nature Reviews Molecular Cell Biology”, v. 23, n. 3, p. 123-139, 2022.
KIM, J.; HONG, S. Epigenetic regulation of gene expression: implications for cancer therapy. Nature Reviews Cancer, v. 21, n. 2, p. 123-135, 2021.
LAMBERTO, F. et al. Alterações ambientais durante o desenvolvimento embrionário: estudando o impacto de estressores em cardiomiócitos derivados de células-tronco pluripotentes. Genes, v. 12, n. 10, p. 1564, 2021.
LI, S. et al. Dietas epigenéticas pré-natais desempenham papéis protetores contra a poluição ambiental. “Clinical Epigenetics”, v. 11, p. 82, 2019.
LI, Y. et al. A interação entre genética e epigenética em doenças complexas. “Nature Reviews Genetics”, v. 22, n. 6, p. 345-360, 2021.
LILLYCROP, K. A.; BURDGE, G. C. Maternal diet as a modifier of offspring epigenetics. “Journal of Developmental Origins of Health and Disease”, v. 6, n. 2, p. 88–95, 2015.
LORENA, N.; BRANDÃO, D. da S.; NUNES, C. H.; SALES, C. M. R.; CHAVES, G. de C. Metais pesados como disruptores endócrinos. 2024.
MARDIS, E. R. Next-Generation DNA Sequencing Methods. Annual Review of Analytical Chemistry. 2021.
MELDRUM, D. R.; CASPER, R. F.; DIEZ-JUAN, A.; SIMON, C.; DOMAR, A. D.; FRYDMAN, R. Aging and the environment affect gamete and embryo potential: can we intervene? Fertility and Sterility, v. 105, n. 3, p. 548–559, 2016.
MENDEL, G. Experiments in Plant Hybridization. In: The Origin of Species by Means of Natural Selection. London: John Murray, 1859.
MIRANDA, F. et al. Epigenetic regulation of gene expression: Implications for health and disease. Nature Reviews Genetics, 2022.
MONTEIRO, C. A. et al. Genetic variation in the adaptive response of individuals to environmental change. “Ecology Letters”, v. 23, n. 4, p. 498-511, 2020.
MURPHY, S. K. The Role of Epigenetics in Reproductive Health. Fertility and Sterility, v. 101, n. 1, p. 9-15, 2021.
NAZZARI, S.; SANGUINETTI, S.; CHAN, E.; MONTES, A.; RIBEIRO, M. Genética das doenças cardiovasculares: perspectivas terapêuticas. Journal of Molecular and Cellular Cardiology, 2023.
NILSSON, E. E.; RANTAPAA-Dahlqvist, S.; BREDIN, R. Gene-environment interactions in diabetes and obesity: Focus on epigenetic programming. Clinical Epigenetics, 2017.
NUNES, C. H.; LOURENÇO, F. M. Modulação genética em resposta a fatores ambientais: implicações para a saúde. Frontiers in Genetics, 2023.
PARK, H.; VU, C.; HAYES, J. F.; LAM, A. Genetic Effects of Maternal Exposure to Environmental Toxins on Offspring Health. Toxicology Reports, 2020.
PEREIRA, C. et al. Genetic and environmental factors in the development of obesity. Journal of Health and Nutrition, 2023.
PEREIRA, J. The influence of prenatal stress on gene expression and disease susceptibility. “Nature Reviews Neuroscience”, 2023.
POPOV, A.; WARD, L. Gene-environment interactions and their role in complex diseases. “Nature Reviews Genetics”, 2022.
QUINN, E. B.; REYNOLDS, M.; SMITH, A.; THORNTON, C. Genetic risk factors for neurodegenerative diseases. Nature Reviews Neuroscience, 2021.
ROGIC, S. et al. The Impact of Genetic Variants on Environmental Toxicology. Environmental Health Perspectives, 2020.
SAMUELS, D. C. et al. Environmental epigenetics in health and disease. Nature Reviews Genetics, 2021.
SHARMA, S. The impact of epigenetic modifications on gene expression. Journal of Genetics and Genomics, 2021.
SILVA, A. F.; COSTA, A. Hereditariedade: aspectos e definições. Biologia e Sociedade, 2022.
SILVA, J. A.; MARTINS, C. Environmental toxins and genetic disorders: A comprehensive overview. Environmental Pollution, 2021.
SILVA, L. M. et al. Genes and environmental influences in human development. Current Opinion in Genetics & Development, 2022.
SOUZA, L. et al. Disruption of endocrine signaling pathways by environmental pollutants. Endocrinology, 2021.
SOUZA, L. M.; GOMES, P.; MARTINS, J. P. Genomic and environmental determinants of human health. BMC Genomics, 2023.
SONG, M. K. et al. Genetic architecture of complex diseases: Progress and challenges. Nature Reviews Genetics, 2021.
SMITH, A. et al. Environmental influences on gene expression and disease susceptibility. Nature Reviews Genetics, 2022.
VICKERS, M. H.; HAESELER, F.; WINTER, L.; SEPHIRA, H.; NOGUEIRA, R.; WHELAN, A. Gene-environment interactions in health and disease. Nature Reviews Genetics, 2021.
VISCHER, A. M. The impact of maternal health on offspring genetics. Nature Reviews Genetics, 2021.
WANG, Y. et al. The role of epigenetics in the development of complex diseases. Nature Reviews Genetics, 2022.
WRAY, N. R.; MORGAN, A.; BOURNE, C.; TAYLOR, D. R. Genomic prediction of complex traits. Nature Reviews Genetics, 2021.
ZHU, Z.; ZHANG, Y. Genetic influences on environmental responses in human health. Nature Reviews Genetics, 2021.
1Discente do Curso Superior de Medicina do Instituto Nacional de Ensino Superior e Pós Graduação Padre Gervásio – Inapós Campus Pouso Alegre – MG e-mail: marinna1992menezes@gmail.com
2Docente do Curso Superior de Medicina do Instituto Nacional de Ensino Superior e Pós Graduação Padre Gervásio – Inapós Campus Pouso Alegre – MG. Mestre em Genética e melhoramento de Plantas ( UFLA); . e-mail: gabrielabarretodosreis@gmail.com
