CEPAS RESISTENTES INDISCRIMINATE USE OF ANTIBIOTICS RELATED TO THE CREATION OF NEW RESISTANT STRAINS
REGISTRO DOI:10.5281/zenodo.10204067
Ana Beatriz da Silva de Sousa
Luane Mayara Monteiro dos Santos
Ygor Lopes Campos
Gustavo José Vasco Pereira
RESUMO
Os antibióticos, sejam eles de origem natural ou sintética, possuem a capacidade de inibir ou eliminar bactérias, resultando em efeitos bacteriostáticos e bactericidas, respectivamente. No entanto, o uso indiscriminado e inadequado dessas substâncias deu origem a um sério problema de saúde pública: a resistência bacteriana aos antibióticos. A adaptação das bactérias à presença desses medicamentos, aliada ao consumo irracional, contribuiu significativamente para o surgimento de cepas bacterianas resistentes, tornando um desafio global e ocasionando impactos consideráveis na saúde pública e comunidade. Um dos principais impulsionadores desse uso inadequado dos antibióticos é a desinformação entre os pacientes, que muitas vezes consideram os antibióticos como solução universal para problemas de saúde, levando ao consumo excessivo. O fácil acesso e o uso inadequado dessas substâncias, tanto pela população em geral quanto nos serviços de saúde, provocaram o surgimento de cepas bacterianas resistentes. Na tentativa de diminuir esse problema e preservar a eficácia dos antibióticos, é crucial promover a conscientização sobre o uso racional e descarte adequado desses medicamentos. Destacar a indicação específica e a importância de seguir as orientações médicas é fundamental. Ademais, é necessário restringir o acesso a esses fármacos para promover a práticas de uso responsável tanto na comunidade quanto nos serviços de saúde, a fim de para reduzir o desenvolvimento de resistência bacteriana.
ABSTRACT
The antibiotics, whether natural or synthetic, have the ability to inhibit or eliminate bacteria, resulting in a bacteriostatic or bactericidal effect. However, the misuse of these substances has
given rise to a public health issue: bacterial resistance to antibiotics. The adaptation of bacteria to the presence of these medicines, together with their misuse, has contributed significantly to the appearance of resistant bacterial strains, becoming a global challenge and causing impacts on public health and communities. One of the principal contributors to the misuse issue is the misinformation among patients, who use antibiotics as a universal health solution, leading to uncontrolled use. The easy access and misuse of these substances, both by patients and medical staff, induce the growth of multiresistant bacterial strains. To address this problem and preserve the efficiency of antibiotics, it is crucial to promote awareness about the rational use and proper disposal of these medicines. Emphasizing the importance of the right prescription and following medical instructions is fundamental. Furthermore, it is essential to restrict access to antibiotics and promote careful, responsible use in the community and healthcare services to reduce the development of bacterial resistance.
1 INTRODUÇÃO
Assim como as doenças que assolam o homem civilizado desde seu princípio, sua cura também faz parte da civilização (FERNANDO PESSOA, 2013). Durante a História, a humanidade aprendeu a utilizar as ferramentas naturais para conseguir perpetuar sua espécie na Terra. Porém, os métodos de cura foram revolucionados por Alexander Fleming em meados de 1928 com a descoberta da Penicilina, sendo inicialmente utilizada exclusivamente pelo exército durante a Segunda Guerra Mundial (1939 – 1945). Sr. Fleming alertou que o uso impróprio pode levar à seleção de formas mutantes resistentes de Staphylococcus aureus. A penicilina descoberta por Fleming faz parte do grupo de antimicrobianos chamado de Beta-lactâmico, que atuam inibindo a etapa de síntese da parede celular das bactérias. Em aproximadamente um ano após a disponibilização para o público civil, um número significativo de mutações resistentes à penicilina havia sido descoberto. Após alguns anos, 50% dos casos não eram mais suscetíveis a esta droga (ALANIS, 2005).
É inegável que a descoberta do antibiótico faz parte das mais importantes tecnologias descobertas pela humanidade, porém assim como todos os medicamentos descobertos, se não bem administrado, pode gerar consequências para o paciente e também para a sociedade, tendo como exemplo redução da efetividade dos tratamentos, aumento dos índices de mortalidade e também
aumento nos custos para saúde pública (ORTIZ RODRÍGUEZ et al., 2011). A resistência bacteriana anteriormente ao século XXI era restrita a ambientes hospitalares, porém com a difusão dos antimicrobianos, podemos observar a disseminação da resistência mesmo em humanos saudáveis. Devido a intrínseca natureza das bactérias, a mutagênese ocorre de forma rápida.
Os microrganismos que estão envolvidos no processo de multirresistência são os chamados ESKAPE (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumanii, Pseudomonas aeruginosa e enterobacteriaceae), fazendo alusão a palavra escapar, enfatizando a capacidade desses microrganismos escaparem do tratamento comum (BOUCHER et al., 2009).
Mesmo com avanço nos campos tecnológicos a respeito da produção de novos fármacos, possuímos uma diminuição na introdução de novos antibióticos no mercado. “Lacuna de inovação” é a expressão utilizada para descrever esta circunstância observada desde 1962 (BASSETTI et al., 2013).
Figura 1: Descoberta dos antibióticos aos longos dos anos 1980-2011 (BASSETTI, M. et al., 2013).
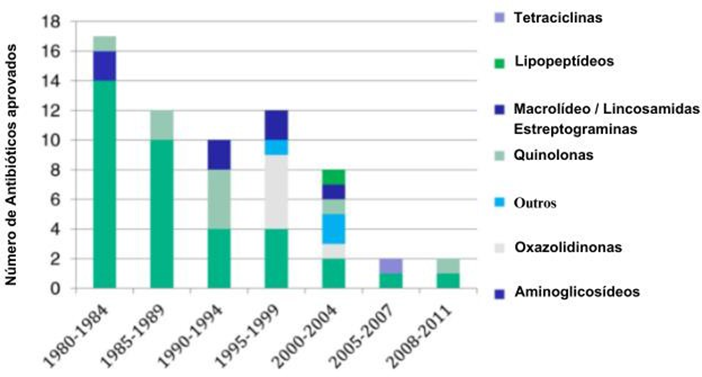
Alguns fatores favorecem para que haja a migração em relação ao interesse das indústrias farmacêuticas no tocante a pesquisa de novos antibióticos:
A indústria farmacêutica migrou a utilização de recursos para a criação de novas drogas que obtivessem um lucro maior, o antibiótico é usado durante um período de tempo curto, e há possibilidades de posteriormente a eficácia do medicamento perder sua efetividade devido a
resistência bacteriana. Dado novas políticas mais exigentes em relação ao lançamento de novas drogas pelos órgãos reguladores FDA (Food and Drug Administration) e Anvisa (Agência Nacional de Vigilância Sanitária), o desenvolvimento de novos antibióticos se tornaram mais caros (MAC GOWAN & MACNAUGHTON, 2017).
No Brasil, um dos maiores consumidores de medicamentos no mundo, um mercado de aproximadamente U$22,1 bilhões anuais, não é diferente. O uso indevido de antibióticos é um problema que assola principalmente países em desenvolvimento (MORGAN et al., 2011). Aproximadamente possuímos 1/3 dos hospitalizados no Brasil, são devido ao uso incorreto de medicamentos, mas a automedicação é dada por múltiplos fatores, incluindo a dificuldade da população em conseguir serviços de saúde, a crença nos benefícios providos pelos tratamentos e prevenções a doenças e a necessidade de alívio imediato dos sintomas (DOMINGUES et al., 2015). O objetivo deste estudo é explorar as percepções com relação a utilização indevida de antimicrobianos no âmbito mundial e correlacioná-los com os fatores socioeconômicos de países subdesenvolvidos.
2 MATERIAIS E MÉTODOS
Na elaboração do Trabalho de Conclusão de Curso, foi realizada uma revisão da literatura utilizando artigos. Os dados foram obtidos por meio de pesquisas nas bases de dados: Pubmed, Google Acadêmico e Scielo (Scientific Electronic Library), abrangendo o período de 2000 a 2023 e englobando artigos nos idiomas português, inglês e espanhol. A inclusão dos artigos escolhidos seguiu os seguintes critérios: Artigos renomados e de fontes confiáveis (tais como Pubmed, Google Acadêmico e Scielo), integralidade dos artigos em relação aos tópicos do trabalho e também foi considerada a disponibilidade de artigos redigidos nos idiomas português, inglês e espanhol.
No que diz respeito aos critérios de exclusão, foram considerados os seguintes fatores: A exclusão de artigos que se limitavam a dados estatísticos e a artigos que não apresentavam objetivos alinhados com o trabalho.
3 DESENVOLVIMENTO
3.1CONTEXTO HISTÓRICO DOS ANTIMICROBIANOS:
Inicialmente, as bactérias foram observadas pela primeira vez em 1670 por Van Leeuwenhoek após a invenção do microscópio. No entanto, somente no século XIX surgiu a hipótese de que esses microrganismos poderiam ser a causa de processos infecciosos, após experimentos conduzidos por Louis Pasteur. Posteriormente, na segunda metade do século XIX, o cientista Robert Koch identificou microrganismos responsáveis por doenças como tuberculose, cólera e febre tifoide, o que deu início a pesquisas em busca de substâncias químicas com propriedades antibióticas (GUIMARÃES et al., 2010).
Em 1934, a Proflavina foi desenvolvida e utilizada durante a Segunda Guerra Mundial no tratamento de infecções em feridas. No entanto, sua aplicação foi interrompida devido à alta toxicidade apresentada pela substância. Apesar desses avanços significativos, o marco histórico mais proeminente ocorreu em 1928 com a descoberta da penicilina (GUIMARÃES et al., 2010).
Em 1928, durante seus estudos com uma cultura de bactérias pertencentes ao gênero Staphylococcus, Alexander Fleming notou a presença de mofo contaminando uma dessas culturas. Ao observar mais detalhadamente, isolou o mofo e identificou que pertencia ao gênero Penicillium, capaz de inibir o crescimento de outras bactérias que causavam infecções em seres humanos. Cerca de uma década após essa descoberta, pesquisadores da Universidade de Oxford, incluindo Florey, Chain e Abraham, dedicaram-se ao estudo da penicilina. Eles constataram seus efeitos terapêuticos, e após isso, foi iniciado os desafios para a produção do antibiótico em larga escala (MARIA et al., 2012).
O uso generalizado após a Segunda Guerra Mundial resultou no surgimento das primeiras cepas de bactérias Gram-positivas que não eram suscetíveis aos antibióticos penicilínicos. Da mesma forma, os novos antibióticos lançados no mercado de medicamentos nos anos subsequentes começaram a apresentar limitações devido ao aumento da resistência das bactérias em relação aos antibióticos penicilínicos (SILVEIRA et al., 2006).
Ao longo dos anos, os avanços científicos na área de antibióticos tornaram-se progressivamente mais significativos. Entre 1940 e 1960, foram introduzidos no mercado de antibióticos semissintéticos eficazes no tratamento de patógenos Gram-positivos e Gram- negativos, semelhantes aos antibióticos naturais já existentes. Entre 1980 e 2000, a genômica e
triagens de coleções de compostos foram as principais ferramentas empregadas na descoberta de novos antibióticos. No entanto, houve uma limitação na identificação de novos protótipos de antibióticos, coincidindo com um aumento da resistência bacteriana (GUIMARÃES et al., 2010). A partir do ano 2000, houve uma introdução limitada de novos antibióticos para a terapia antimicrobiana. Em 2003, houve um ressurgimento dos esforços de pesquisa na indústria farmacêutica voltados para programas de descoberta de antibióticos de origem natural, o que resultou na aprovação da Daptomicina, um lipodepsipeptídeo natural, para uso terapêutico(GUIMARÃES et al., 2010).
3.2 MECANISMOS DE AÇÃO DOS ANTIBIÓTICOS MAIS COMUMENTE UTILIZADOS:
Vale ressaltar que a necessidade das descobertas de novos antibióticos vai além da multirresistência dos microbianos. É de suma importância pontuarmos que a necessidade de novas descobertas abrange a área de atuação desses novos fármacos em agentes etiológicos que ainda combatemos de forma ineficaz. Partindo do pressuposto que cada antibiótico tem seu mecanismo de ação específico para cada desempenho da bactéria, como por exemplo a Penicilina, que age combatendo a síntese da parede celular bacteriana. Sendo assim, não se faz eficaz combatendo o Mycoplasma genitalium, pois este organismo não possui parede celular. Para compreendermos melhor o mecanismo de ação da Penicilina, surge a necessidade de compreendermos o processo por trás da formação da parede celular bacteriana. As paredes bacterianas fazem parte do desenvolvimento normal das bactérias. Essas paredes são estruturas rígidas formadas por diversos ácidos, carboidratos e lipídios que formando uma macromolécula complexa chamada de Peptídeoglicano (PGN) (MONTEIRO DA SILVA et al, 2020).
Figura 2: Estrutura do Peptidoglicano (PGN) (FUNÇÕES, ESTRUTURA E SÍNTESE. MAESTROVIRTUALE, 2023).
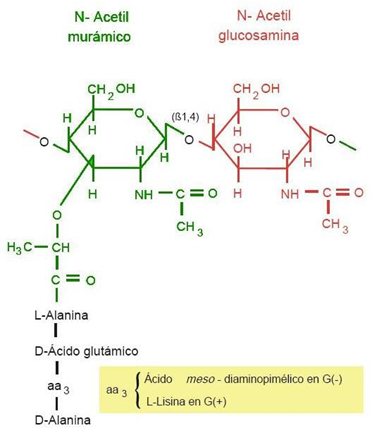
O PGN possui uma estrutura similar a uma treliça, configurando estabilidade e rigidez para a parede celular. É composta por pepitídeos e açúcares tais como: NAG (n-acetilglicosamina) e NAMA (ácido n-acetil muramico). Os peptídeos são tetrapepitídeos que interligam os resíduos de NAMA e um pentapeptídeo de glicina que realiza uma ligação covalente cruzada entre os resíduos de d-alanina e l-lisina, presentes entre os tetrapeptídeos adjacentes. Essa estrutura forma uma organização similar a uma trama, importante para a manutenção da forma e do controle da permeabilidade celular (PATRICK, G. L., & SPENCER, 2009).
A síntese do pepitídeo glicano envolve cerca de 30 enzimas, podendo ser dividido em 3 estágios principais:
Figura 3: Quadro de resumo das fases da biossíntese do peptidoglicano e as respectivas características (SOUSA, 2006).
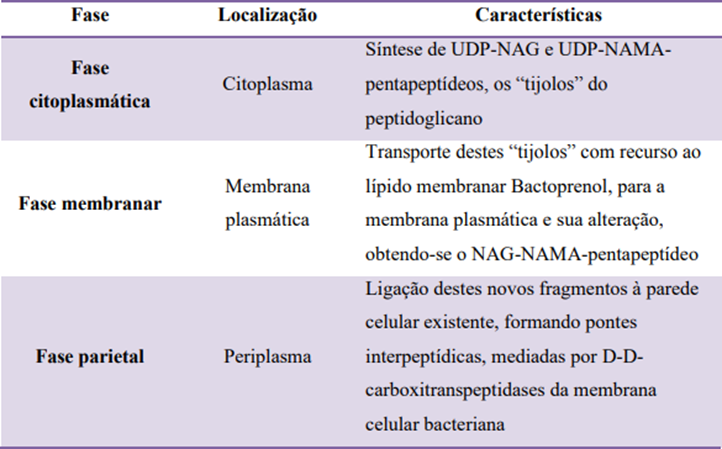
As penicilinas atuam como inibidores da enzima transpeptidase, responsável pela ligação final entre a D-alanina e a glicina terminal do pentapeptídeo, demonstrado na figura 2, tendo como resultado o aumento da flexibilidade da rede de PGN, exercendo assim uma ação bacteriolítica. Tendo em vista isso, o grupo dos antibióticos pertencentes a família dos β-lactâmicos atuam na síntese do PGN, ocasionando a autolisina bacteriana, quebrando as ligações covalentes do peptídeoglicano.
Figura 4: Esquema de formação da parede celular (SUAREZ e GUDIOL, 2009).
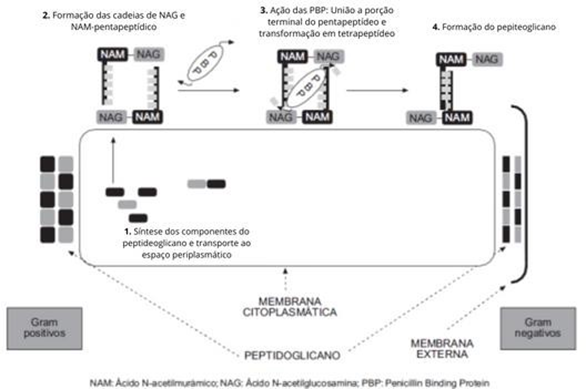
Além das Penicilinas, possuímos as Cefalosporinas, antibióticos também pertencentes ao grupo dos β-lactâmicos. A Cefalosporina teve seu descobrimento através do isolamento do fungo Cephalosporium acremonium de um esgoto na ilha de Sardenha, por volta de 1945 pelo farmacologista Giuseppe Brotzu. (Bo, 2000) Posteriormente isolando o fungo Cephalosporium acremonium, surgiu as cefalosporinas N, C e a P (REVISTA CIENTÍFICA ELETRÔNICA DE MEDICINA VETERINÁRIA-ISSN, 2023.) A Cefalosporina possui sua estrutura molecular muito semelhante Penicilina, tendo a presença do anel β-lactâmico em seu núcleo, que está fundido ao anel diidrotiazínico, que compõe o seu núcleo comum em todas as substâncias pertencentes as Cefalosporinas. Salientando sua diferença com as Penicilínas, onde também está presente o anél β- lactâmico, não obstante, o núcleo bicíclico é composto pela fusão do anel tiazolidínico. Conforme demonstra a imagem abaixo:
Figura 5: A imagem representa os mecanismos de ação das Penincilinas e Cefalosporinas (DOUTORA & SIMÕES, 2013).
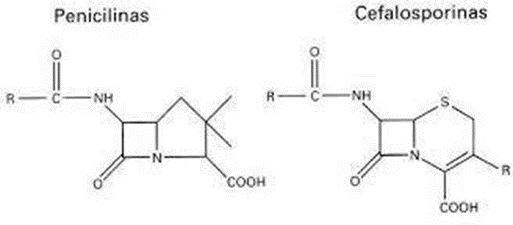
O mecanismo de funcionamento das Cefalosporinas é comparável ao da Penicilina, já que ambas atuam sobre a transpeptidase, a qual é responsável pela conexão entre a D-alanina e a glicina, essencial para a produção do PGN da estrutura celular. O processo tem início com um ataque nucleofílico ao par de elétrons da hidroxila da serina (D-alanina e glicina), em relação à carbonila do anel β-lactâmico das Cefalosporinas, resultando na formação de um intermediário tetraédrico protonado. Esse intermediário, por sua vez, passa por uma transferência de prótons, dando origem a um segundo intermediário tetraédrico, onde o próton está ligado à porção acetila. Posteriormente, esse intermediário sofre uma degradação, ocasionando a abertura do anel β-lactâmico e, por conseguinte, a eliminação do grupo ácido acético, o que leva à formação de um aduto covalente. Como resultado, ocorre uma inibição irreversível da enzima (HARRISON & BRATCHER, 2008).
Com o decorrer do tempo, as cefalosporinas se tornaram cada vez mais suscetíveis em relação ao aparecimento de bactérias multirresistentes a elas, fazendo com que houvesse a
necessidade de otimizar a molécula para que sua eficácia se mantivesse, e por isso, as Cefalosporinas foram sendo classificadas de acordo com suas gerações, tendo atualmente um total de 5 gerações.
3.3 FATORES QUE INFLUENCIAM A RESISTÊNCIA ANTIMICROBIANA NA SOCIEDADE:
A resistência bacteriana pode ser classificada como um fenômeno ecológico decorrente da adaptação das bactérias à exposição excessiva a antibióticos, o que possibilita sua proliferação no ambiente, onde se reproduzem rapidamente e podem compartilhar material genético com outras bactérias, independentemente de sua espécie. Antes do século XXI, a resistência bacteriana era predominantemente observada em ambientes hospitalares. No entanto, nos dias de hoje, ela pode estar relacionada a diversos fatores e afetar até mesmo indivíduos saudáveis (GUIMARÃES et al., 2010).
Os antibióticos, de forma natural, podem contribuir para o desenvolvimento da resistência bacteriana. O uso indiscriminado desses medicamentos gera um desafio significativo para a saúde pública em todo o mundo, afetando tanto países desenvolvidos quanto os em desenvolvimento (QUEIROZ SANTOS, 2004).
Em países em desenvolvimento, vários fatores socioeconômicos e comportamentais estão relacionados ao uso inadequado de antibióticos. Esses fatores incluem a prescrição inadequada por profissionais de saúde, a dispensação de medicamentos por pessoas não qualificadas, medicamentos de qualidade duvidosa, condições de higiene precárias e sistemas de vigilância inadequados. Em alguns desses países, é comum que os antibióticos sejam adquiridos e consumidos sem a necessária prescrição médica, muitas vezes sendo vendidos de maneira inadequada, o que promove a automedicação e o desenvolvimento da resistência a antibióticos. Isso se deve ao fato da não observância das recomendações de dosagem, uso adequado, indicações e contraindicações farmacêuticas, representando um risco significativo para a saúde pública e a eficácia dos tratamentos com antibióticos (“Perspectives Misuse of Antibiotics by Physicians in Clinical Practice”, [s.d.]
Ademais, a prática da automedicação na sociedade é também um dos fatores que pode agravar o potencial de resistência. Essa conduta engloba uma variedade de razões que podem levar
a população, sem avaliação do profissional da saúde, a se autoadministrar medicamentos, incluindo a utilização de sobras do medicamento e o descumprindo ás prescrições por meio da prolongação ou interrupção do tratamento antes do período estipulado pelo médico para alcançar os efeitos terapêuticos desejados. Alguns fatores, podem estar relacionados, entre eles de ordem econômica, política e cultural. Esses fatores estão relacionados à ampla disponibilidade de produtos, à simbolização da saúde que os medicamentos podem representar; publicidade irresponsável e a grande pressão para a conversão de medicamentos que necessitam de receita médica para medicamentos disponíveis sem prescrição, sendo vendidos nas prateleiras de farmácias (PEREIRA et al., 2007).
Segundo a Organização Mundial da Saúde, em todo mundo mais de 50% dos medicamentos são prescritos e dispensados de forma errônea, estimulando reações adversas e tendo como resultado uma maior resistência antimicrobiana – no Brasil, o uso de forma inadequada é fortemente motivado pela automedicação, propaganda e publicidades (USO RACIONAL DE ANTIBIÓTICOS – UMA EXPERIÊNCIA PARA EDUCAÇÃO EM SAÚDE COM ESCOLARES et al., 2012).
A utilização inadequada de medicamentos por parte dos usuários contribui significativamente para o desenvolvimento de resistência bacteriana, seja ao ser empregado por períodos superiores ou inferiores aos prescritos, ou mesmo quando utilizado para tratar sintomas que não se relacionam a infeções bacterianas (SOARES & DA COSTA GARCIA, n.d.).
Na esfera das instalações hospitalares, a Unidade de Terapia Intensiva (UTI) se destaca como o ambiente com a mais elevada incidência de infecções. Isso se deve ao fato de que a UTI é o setor que mais frequentemente acolhe pacientes com condições graves que requerem procedimentos invasivos e, ademais, é onde os pacientes permanecem por períodos prolongados, criando um ambiente propício para a colonização de patógenos resistentes, como a Klebsiella pneumoniae. As principais consequências da resistência a antibióticos em contextos hospitalares incluem o aumento da morbidade e mortalidade devido a doenças que anteriormente poderiam ser tratadas com eficácia através do uso terapêutico de antibióticos (GATO, 2021).
Outro fator crucial que contribui é a maneira como os antibióticos são descartados, pois quando eliminados no lixo comum, propiciam o surgimento de bactérias através da contaminação dos recursos hídricos. Além disso, certos micro-organismos desenvolvem resistência a esses fármacos, promovendo, assim, o crescimento de bactérias resistentes. Dessa maneira, é de extrema
importância disseminar entre a população a utilização adequada conforme prescrição médica, destacando os riscos de resistência associados ao uso inadequado, além de promover a prática correta de descarte (PINTEL et al., 2017).
3.4 AÇÃO DOS BACTERIANOS NO DESENVOLTIMENTO DA RESISTÊNCIA:
As bactérias habitam o planeta Terra desde o período mesoarqueano, neste momento, a Terra ainda era um ambiente hostil. Os seres existentes neste período ainda não tinham conquistado o ambiente terrestre, se contendo somente com o ambiente aquático, as temperaturas da superfície da terra ainda eram extremamente elevadas, e a camada de ozônio ainda não havia sido formada. Elas superaram todas as intemperes de um ambiente onde a vida ainda estava em desenvolvimento inicial, para chegar até a era moderna. Sua grande capacidade de adaptação está intrinsecamente ligada à sua perpetuação. Partindo do pressuposto da superação de todas as adversidades, a resistência bacteriana frente aos antibióticos pode ser atribuída a diversos fatores, mas principalmente a sua mutagênese, transdução ou seleção. O tempo reprodutivo bacteriano é relativamente baixo, se comparados com outros seres de outros reinos, possuindo uma maior variabilidade de genes a serem recombinados em um curto espaço de tempo (SA; FIOL; GROPPO, [s.d.]).
Atualmente, a resistência bacteriana está presente em quase todos os tipos de germes, podendo ser uma característica inerente, onde o mecanismo de ação do fármaco não age na bactéria por características morfológicas, ausência do sítio de ligação. Adquirida por mutações, ocorridas durante a reprodução do organismo ou por aquisição de um material exógeno, aquisição por transferência horizontal de genes, que possui um gene resistente ao antimicrobiano ou de forma induzida, sendo induzida por uma influência própria dos antibióticos ou agentes mutagênicos (DA SILVA OLIVEIRA et al., [s.d.]).
Vale ressaltar que a resistência bacteriana é inerente ao uso indevido de antimicrobianos de forma indevida, é um fator natural, assim como a resistência do micoplasma a antibióticos β- lactâmicos, E se faz inevitável, devido ao uso de antibióticos na sociedade, entretanto, a utilização correta dos fármacos da classe dos antimicrobianos, causará um menor índice de resistência bacteriana (“ TORTORA et al.,”, [s.d.]).
3.5 ATUAÇÃO FARMACÊUTICA PARA PROMOÇÃO DO USO RACIONAL DOS ANTIBIÓTICOS:
Por muitos anos e até o presente momento, os antibióticos têm sido administrados em quantidades que excedem as dosagens recomendadas. Em países em desenvolvimento, como a Índia, essa prática tem contribuído para o surgimento de altos níveis de resistência antimicrobiana. Esta situação é, em grande parte, atribuída à falta de assistência farmacêutica adequada, uma vez que as prescrições e orientações são realizadas por profissionais não qualificados (MEHTA et al., 2014).
Em virtude da resistência antimicrobiana, estima-se que até 2050 a disponibilidade de antibióticos eficazes no mercado possa estar comprometida. Diante da ausência de novos desenvolvimentos nessa área, é de extrema importância adotar um uso racional desses medicamentos, a fim de garantir sua disponibilidade a longo prazo. Isso se justifica pelo fato de que, caso os antibióticos se tornem ineficazes, doenças atualmente tratáveis com facilidade poderão acarretar um aumento significativo na taxa de mortalidade prematura (BELL et al., 2014).
Um estudo foi conduzido em um Hospital Cardiológico no Brasil em março de 2012, para a implementação do Programa de Antecedentes de Gestão Antimicrobiana (ASP), visando promover o uso racional de medicamentos e avaliar o impacto da presença do farmacêutico. Os resultados indicaram que, após a introdução do programa, a atuação do farmacêutico resultou na redução do consumo de antimicrobianos de forma inadequada e na adesão da equipe às recomendações do ASP, atingindo um índice de 64,1%. Houve uma redução significativa de 69% nos custos hospitalares com antibióticos. Dessa forma, nesse cenário a atuação da equipe multidisciplinar foi fundamental para potencializar o impacto positivo das intervenções e a promoção do uso apropriado dos medicamentos (MAGEDANZ et al., 2012).
Além disso, é de suma importância ressaltar o papel significativo do farmacêutico na Comissão de Controle de Infecção Hospitalar (CCIH). A Infecção Hospitalar é caracterizada pela sua ocorrência após a admissão do paciente no hospital, podendo se manifestar durante o período de internação ou após a alta médica. De acordo com a Resolução nº 300/97 do Conselho Federal de Farmácia (1997), a atuação dos farmacêuticos na CCIH é essencial, uma vez que esses profissionais possuem a capacidade técnica para contribuir em pesquisas relacionadas ao uso apropriado de antimicrobianos. Eles estão habilitados para oferecer esclarecimentos sobre
indicações, farmacocinética, farmacodinâmica, interações medicamentosas e informações sobre toxicidade e reações adversas. Tais contribuições farmacêuticas podem aumentar as chances de sucesso no tratamento e na cura de infecções bacterianas, resultando em melhores práticas e cuidados clínicos nos ambientes hospitalares (COSTA et al., 2020).
Portanto, podemos observar que o papel do farmacêutico é crucial para mitigar a resistência antimicrobiana, pois desempenha a função de orientar a população sobre as consequências do uso inadequado de antibióticos e sua atuação promove o uso responsável desses medicamentos, garantindo sua dispensação de maneira adequada e assegurando o cumprimento das prescrições médicas. Além disso, o farmacêutico não apenas tem um impacto direto na saúde individual dos pacientes, mas também repercute positivamente no sistema de saúde como um todo, tornando-se essencial para a sustentabilidade e eficácia dos tratamentos, ao mesmo tempo em que ajuda a enfrentar o desafio global da resistência antimicrobiana (LIMA et al., 2023).
4 CONSIDERAÇÕES FINAIS
Esse estudo abordou os principais tópicos sobre o uso indiscriminado de antibióticos na criação de novas cepas multirresistentes correlacionando principalmente os pretextos pelos quais os pacientes utilizam a classe de fármacos dos antimicrobianos de forma incorreta.
Os objetivos estabelecidos nesse estudo foram alcançados, visto que foi possível identificar o uso indevido de antimicrobianos afeta não somente ao paciente de forma individual, mas também o coletivo, uma vez que em países subdesenvolvidos, possuímos uma taxa maior de resistência antimicrobiana por falta de assistência farmacêutica correta, prescrição incorreta e principalmente automedicação. Adicionalmente também foi possível identificar que em um futuro não tão próximo, estaremos carentes de novas classes de antibióticos devido a multirresistência das bactérias por conta do uso indevido e em virtude da decadência do investimento das indústrias farmacêuticas no descobrimento de novas classes de antimicrobianos.
Com isso, foi possível responder ao questionamento levantado anteriormente onde verificou-se que a qualidade do sistema de saúde do país, juntamente com suas leis sanitárias, e aptidão da assistência farmacêutica impacta diretamente no acréscimo ou decréscimo dos casos de bactérias multirresistentes aos antibióticos disponíveis atualmente no mercado.
Através dos resultados deste trabalho foi possível observar que os fatores principais que afetam o aumento da multirresistência bacteriana estão relacionados com a automedicação, situação socioeconômica do país e que o decréscimo de lançamentos de novas classes de antibióticos está relacionado diretamente a migração do interesse das indústrias farmacêuticas para outros tipos de fármacos, por conta de sua baixa rentabilidade, devido a rápida aquisição de resistência ao medicamento frente ao seu tempo disponível no mercado.
Espera-se que esta pesquisa seja utilizada para profissionais da saúde como uma forma de contribuição no âmbito da conscientização da prescrição de fármacos da classe dos antibióticos, bem como conscientização no momento da dispensação deles.
5 REFERÊNCIAS BIBLIOGRÁFICAS:
FERNANDO PESSOA, U. As doenças infeciosas e a História dos Antibióticos. [s.l: s.n.]. ALANIS, A. J. Resistance to antibiotics: Are we in the post-antibiotic era? Archives of Medical Research, nov. 2005.
ORTIZ RODRÍGUEZ, S. P. et al. Characterising the purchase of antibiotics in drugstores in Bogotá: a users’ perspectiveinvestig.seg.soc. Volumen. [s.l: s.n.].
BOUCHER, H. W. et al. Bad bugs, no drugs: No ESKAPE! An update from the Infectious Diseases Society of America. Clinical Infectious Diseases, v. 48, n. 1, p. 1–12, 1 jan. 2009.
BASSETTI, M. et al. New antibiotics for bad bugs: where are we? [s.l: s.n.]. Disponível em:
<http://www.ann-clinmicrob.com/content/12/1/22>.
MACGOWAN, A.; MACNAUGHTON, E. Antibiotic resistance. Medicine (United Kingdom)
Elsevier Ltd, , 1 out. 2017.
MORGAN, D. J. et al. Non-prescription antimicrobial use worldwide: a systematic review. The Lancet Infectious Diseases, v. 11, p. 692–701, 2011.
DOMINGUES, P. H. F. et al. Prevalence of self-medication in the adult population of Brazil: A systematic review. Revista de Saude PublicaUniversidade de Sao Paulo, , 2015.
GUIMARÃES, D. O. et al. ANTIBIÓTICOS: IMPORTÂNCIA TERAPÊUTICA E PERSPECTIVAS PARA A DESCOBERTA E DESENVOLVIMENTO DE NOVOS
AGENTES Quim. Nova. [s.l: s.n.].
PEPTIDOGLICANO: Funções, Estrutura e Síntese. Maestrovirtuale, 2023. Disponível em: https://maestrovirtuale.com/peptidoglicano-funcoes-estrutura-e-sintese/. Acessado em: 15, setembro de 2023.
MARIA, C. et al. Penicilina: Efeito do Acaso e Momento Histórico QUÍMICA NOVA NA ESCOLA Química e Sociedade. [s.l: s.n.].
SILVEIRA, G. P. et al. ESTRATÉGIAS UTILIZADAS NO COMBATE A RESISTÊNCIA
BACTERIANAQuim. Nova. [s.l: s.n.].
MARISA, S.; AZEVEDO, M.; FERNANDO PESSOA, U. Farmacologia dos Antibióticos Beta- lactâmicos. [s.l: s.n.].
SUÁREZ, C.; GUDIOL, F. Beta-lactam antibiotics. Enfermedades Infecciosas y Microbiologia Clinica, v. 27, n. 2, p. 116–129, 2009.
LIMA, L.M., MONTEIRO DA SILVA, B.N., BARBOSA, G., & BARREIRO, E.J (2020) β-
lactam antibiotics: An overview from a medicinal chemistry perspective. European Journal of Medicinal Chemistry.
An Introduction to Medicinal Chemistry. . [s.l: 2012.].
BO, G. Giuseppe Brotzu and the discovery of cephalosporins. Clinical Microbiology and Infection, v. 6, n. S3, p. 6–8, 1 dez. 2000.
REVISTA CIENTÍFICA ELETRÔNICA DE MEDICINA VETERINÁRIA-ISSN: 1679-
7353. . [s.l: s.n.]. Disponível em: <www.faef.br.>.
DOUTORA, O. :; SIMÕES, M. J. Mecanismos de Resistência aos Antibióticos – Maria Galvão Baptista (20071294). [s.l: s.n.].
HARRISON, C. J.; BRATCHER, D. Cephalosporins: A Review. [s.l: s.n.]. Disponível em:
<http://pedsinreview.aappublications.org/>.
GUIMARÃES, D. O. et al. ANTIBIÓTICOS: IMPORTÂNCIA TERAPÊUTICA E PERSPECTIVAS PARA A DESCOBERTA E DESENVOLVIMENTO DE NOVOS
AGENTESQuim. Nova. [s.l: s.n.].
DE QUEIROZ SANTOS, N. A RESISTÊNCIA BACTERIANA NO CONTEXTO DA INFECÇÃO HOSPITALAR BACTERIAL RESISTENCE IN THE CONTEXT OF HOSPITAL INFECTION LA RESISTENCIA BACTERIANA EN EL CONTEXTO DE LA
INFECCIÓN HOSPITALARIATexto Contexto Enferm. [s.l: s.n.].
Perspectives Misuse of Antibiotics by Physicians in Clinical Practice. . [s.l: s.n.].
PEREIRA, F. S. V. T. et al. Automedicação em crianças e adolescentes. Jornal de Pediatria, v. 83, n. 5, p. 453–458, set. 2007.
Uso racional de antibióticos – uma experiência para educação em saúde com escolares . [s.d.].
SOARES, I. C.; DA COSTA GARCIA, P. RESISTÊNCIA BACTERIANA: a relação entre o
consumo indiscriminado de antibióticos e o surgimento de superbactérias. [s.l: s.n.].
GATO, P. C. PERFIL DE RESISTÊNCIA BACTERIANA DA KLEBSIELLA PNEUMONIAE NA UNIDADE DE TERAPIA INTENSIVA EM UM HOSPITAL DE ENSINO NO OESTE DO
PARÁ NO PERÍODO DE 2018 A 2019. Brazilian Journal of Development, v. 7, n. 12, p. 115549–115566, 1 dez. 2021.
DESCARTE DE MEDICAMENTOS: UMA REFLEXÃO SOBRE OS POSSÍVEIS RISCOS SANITÁRIOS E AMBIENTAIS HAYSSA MORAES PINTEL RAMOS 1 VANESSA RESENDE NOGUEIRA CRUVINEL 2 MICHELINE MARIE MILWARD DE AZEVEDO MEINERS 3 CAMILA ARAÚJO QUEIROZ 4 DAYANI GALATO 5. . [s.l: s.n.].
SA, F.; FIOL, D.; GROPPO, F. C. Resistência Bacteriana. [s.l: s.n.]. Disponível em
<https://www.researchgate.net/publication/257645108>.
DA SILVA OLIVEIRA, N. et al. REVISTA CIENTÍFICA ELETRÔNICA DE MEDICINA VETERINÁRIA-ISSN: 1679-7353 MECANISMOS DE RESISTÊNCIA BACTERIANA. [s.l:
s.n.].
TORTORA at al. [s.d.].
MEHTA, K. C. et al. Burdeen of antibiotic resistance in common infectious diseases: Role of antibiotic combination therapy. Journal of Clinical and Diagnostic ResearchJournal of Clinical and Diagnostic Research, , 20 jun. 2014.
BELL, B. G. et al. A systematic review and meta-analysis of the effects of antibiotic consumption on antibiotic resistance. [s.l: s.n.]. Disponível em:
<http://www.biomedcentral.com/1471-2334/14/13>.
MAGEDANZ, L.; SILLIPRANDI, E. M.; DOS SANTOS, R. P. Impact of the pharmacist on a multidisciplinary team in an antimicrobial stewardship program: A quasi-experimental study. International Journal of Clinical Pharmacy, v. 34, n. 2, p. 290–294, abr. 2012.
COSTA, I. R. DA et al. A importância do farmacêutico na CCIH / The importance of the pharmacist in CCIH. Brazilian Applied Science Review, v. 4, n. 6, p. 3720–3729, 2020.
LIMA, B. C. DE A. et al. The action of the pharmacist in front of bacterial resistance and rational use of antimicrobials in the hospital environment. Research, Society and Development, v. 12, n. 6, p. e7712642037, 9 jun. 2023.
