REGISTRO DOI: 10.5281/zenodo.7339732
Luiz Gustavo de Oliveira Carbos¹
Vicente Antonio de Senna Junior²
Leonardo Guimarães Andrade³
RESUMO
A doença de graves ou doença do bócio e uma doença autoimune que aparece frequentemente nos cidadãos. Essa doença é caracterizada pelo incentivo do receptor do TSH da célula folicular tireoidiana por autoanticorpos do receptor de tireotropina (TRAb), fazendo com que as sínteses de secreções de hormônios tireoidianos aumentem, como a triiodotironina (T3) e a tiroxina (T4) que no caso da doença causa tireotoxicose devido à hiperprodução deles. Ela possui diferentes tipos de tratamentos como a utilização do iodo radioativo, tratamento farmacológico e em casos mais graves a cirurgia. O Tratamento da doença citada é realizado seguindo os exames relacionados aos receptores do TSH, que dependendo do estado vai se utilizar um diferente modo de procedimento; o mais comum e o tratamento farmacológico sendo usado em casos com menos ricos, já o iodo radioativo e a cirurgia são usados em casos mais graves onde as pessoas estão correndo um maior perigo.
Palavra-chave: Doença de graves, tratamento, hormônio.
ABSTRACT
Grave’s disease or goiter’s disease is an autoimmune disease that appears frequently in citizens. This disease is characterized by the stimulation of the TSH receptor of the thyroid follicular cell by autoantibodies to the thyrotropin receptor (TRAb), causing the synthesis of thyroid hormone secretions to increase, such as triiodothyronine (T3) and thyroxine (T4), which in the case of the disease causes thyrotoxicosis due to their overproduction. It has different types of treatments such as the use of radioactive iodine, pharmacological treatment and, in more severe cases, surgery. The treatment is performed following the tests related to the TSH receptors, which depending on the state will use a different mode of procedure; the most common is the pharmacological treatment and is used in cases with less wealth, while radioactive iodine and surgery are used in more severe cases where people are in greater danger.
Keywords: Severe disease, treatment, hormone.
1 INTRODUÇÃO
A tireoide é a glândula motivadora pela secreção de tiroxina (T4) e triiodotironina (T3), que fazem as estimulações do metabolismo (HALL, 2017). Para que a tireoide tenha funcionamento necessita de um estímulo, o hormônio tireoestimulante (TSH) e da presença de iodo (GADELHA; MONTENEGRO, 2016). A produção de calcitonina também é de responsabilidade da glândula, pelas células C ou parafoliculares, que fazem o reparo da homeostase do cálcio (HALL, 2017).
A anomalia de maior relevância da tireoide é o hipotireoidismo (GOLDER et al., 2015), que é o crescimento dos níveis de TSH, em seu nível primário, e pela falta de produção T3 e T4, sendo pela alteração da tireoide, da hipófise ou do hipotálamo. Podendo ter uma classificação do hipotireoidismo, como: primário, secundário e terciário (FREITAS; LIMA, 2016; KIM; LADERSON, 2018). As causas maiores são a falta de dietética de iodo e a origem autoimune.
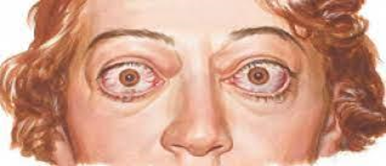
Fonte: http://rachelgomesoftalmologia.com.br/doencas/doenca-de-graves-risco-para-nossa-saude-ocular
A doença de Graves é a procedência mais comum do hipertireoidismo e é originado pelo incentivo do receptor do TSH da célula folicular tireoidiana por autoanticorpos do receptor de tireotropina (TRAb), fazendo com que a síntese e secreção de hormônios tireoidianos aumentem.
Em casos normais, a tireoide, logo após receber o estimulo do hormônio (TSH), sintetiza os hormônios triiodotironina (T3) e tiroxina (T4), eles por sua vez, possuem diversas funções no organismo, ajuda no funcionamento do metabolismo, no sistema cardiovascular, e no gastrointestinal, e ajudam no crescimento. No caso da Doença de Graves (DG), surgem autoanticorpos que se direcionam contra o receptor de TSH (TRAb), a glândula tireoide é bastante estimulada, levando a causa de uma hiperprodução de T3 e T4, o que causa os típicos sintomas de tireotoxicose (EHLERS, 2019; SMITHSON et al., 2019). A presença em excesso de T3 e T4 na corrente sanguínea é a tireotoxicose. Podendo ser associada à hiperprodução ou basicamente a uma liberação de dos hormônios pela glândula da tireoide.
2 Objetivos
2.1 Objetivo Geral
Apresentar os métodos de tratamento da doença de Graves para que as pessoas saibam se posicionar caso sofram ou encontrem pessoas afetadas pela mesma.
2.2 Objetivos Específicos
– Mostrar os diferentes tipos de tratamentos para a doença
– Explicar os efeitos causados pela doença no corpo humano
– Identificar os hormônios Afetados pela doença
– Demonstrar métodos de evitar o aumento dos sintomas
– Explicar a importância dos hormônios na glândula tireoide
3 METODOLOGIA
A realização deste trabalho teve como base a pesquisa bibliográfica, que foi realizada no período compreendido de agosto a novembro do ano de 2022, considerando a importância desta doença e em sua dificuldade foi utilizado de vários sites e meios para pesquisa como o Google Acadêmico, SciELO, Inesul, utilizando como descritores as palavras “Doença de graves”, “Tratamento”, “Sintomas ” e “Tireoide”.
4 JUSTIFICATIVA
A tireoide e uma glândula do corpo humano que produz os hormônios, porem quando afetado pode causa inúmeros problemas para a pessoa envolvida, como a Doença de Graves que em inúmeros casos pode ocasionar na morte se não for tratada do jeito correto.
5 DESENVOLVIMENTO
5.1 Diagnóstico
A doença de Graves se caracteriza por manifestações clínicas, bioquímicas e imagiológicas. Sabendo que os sintomas são palpitações, irritabilidade, intolerância ao calor. A junção desses dados com o alargamento difuso da glândula é muito sugestiva a doença. É necessária a junção dos sinais orbitopatia ou dermopatia, sendo assim, o doseamento plasmático das hormonas tireóideas. (WEETMAN 2000).
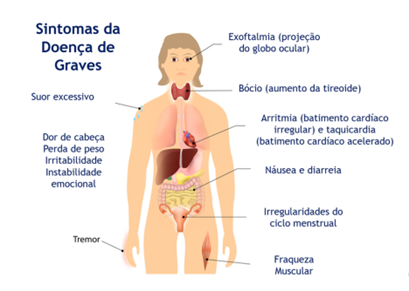
Fonte: www.carolinasantiago.com.br/post/2018/12/28/hipertireoidismo-graves
Em alguns casos raros são necessários exames de imagens para os diagnósticos da doença de Graves, hoje utilizado muito em caso de dúvidas. Geralmente são bem úteis para entender melhor as alterações da morfologia da tiroide em consequência da doença.
Cintilografia com iodo radioativo é utilizado para identificar um bócio tóxico multinodular (captação heterogénea por toda a tiroide) ou um nódulo tóxico (captação localizada) por oposição ao padrão difuso da doença de Graves. Também bem utilizado pelos médicos, para o auxilio de dose de radiação no tratamento.
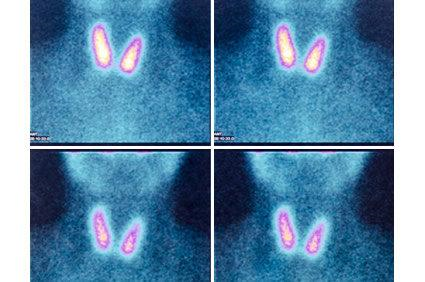
Fonte: https://www.abc.med.br/p/tireoide/1283858/cintilografia+da+tireoide.htm
Podem-se usar testes de laboratórios que se consegue identificarem os receptores da TSH. Existem dois tipos de testes, o primeiro detecta o soro do paciente ao receptor com ligação aos anticorpos, e o segundo a produção de AMPc se os TSH aumentam com a estimulação dos anticorpos.
Os testes de ligação são usados, sendo mais fáceis de utilização, apresentando uma sensibilidade bem maior. (AJJAN AND WEETMAN 2008).
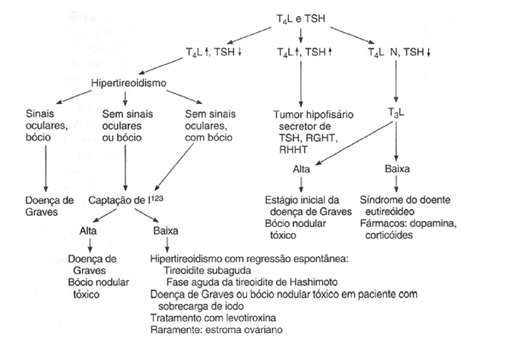
Fonte: Greenspan and Gardner (2004)
5.2 Tratamento
O tratamento da doença de graves pode ser feito por uso de medicamentos (carbimazol, tiamazol e propiltiouracila), terapias com iodo radioativo, ou a cirurgia da tireoide.
Dentre todos os tratamentos, não importa o escolhido, tem que ser feito a monitorização da dosagem do T4, e até o T3. Sendo a TSH podendo permanecer durante várias semanas após a estabilidade do T3 e T4.
5.2.1 Fármacos Antitiriodeus
Os fármacos que inibem a peroxidase tiroideia são os: Carbimazol, o metimazol e o propiltiouracilo, assim amenizando a síntese hormonal. O propilitiouracilo tem como ação o bloqueio a interligação de T4 em T3 nos tecidos. Já o metimazol, tem o efeito mais rápido ao hipertireoidismo, sendo aceito melhor ao pacientes. (COOPER 2005).
O carbimazol é um dos medicamentos utilizado na doença de Graves, sendo um tireostático, que significa uma droga que reduz as secreções do hormônio da tireoide. Sendo conhecido também como um pró-fármaco (pró-droga) é alterado no sangue tornando sua forma ativa.
Geralmente o Carbimazol tem uma dose inicial para adultos de 5 a 15 mg a cada 8 horas e para um tratamento de manutenção de 5 a 20 mg a cada 24 horas. As doses diminuem conforme o tempo vai passando, geralmente após 4 semanas, as dosagens ficam bem menores.
Metimazol é outro fármaco utilizado como agente antitireoidiano no tratamento da doença de graves, faz com que a produção de tiroglobulina seja inibida, e é o precursor dos hormônios da tireoide T3 e T4.
É um medicamento que inibe a peroxidase tireoidiana, que catalisa as moléculas de iodeto. Tem sua dosagem de 5 mg e podem ser ingeridos de 2 a 8 vezes ao dia. Sendo a dosagem geralmente recomendada de 5 mg a cada 8 horas.
O propiltiouracill tem um efeito maior que faz com que reduza a conversão de T4 para T3, por meio de uma inibição de deiodinase tipo 1, presente em todos os periféricos e na tireoide.
Sendo o Propiltiouracill a droga mais utilizada durante a gravidez e por lactantes, pois atinge a menor camada da placenta, e é encontrado em menor quantidade no leite materno. Sendo também a droga a ser escolhida no tratamento em caso grave ou em tempestade tiroidiana, em altas doses diminuem a conversão de T4 PARA T3. Doses elevadas correspondem a resultado maior.
Segundo o Hall e Guyton (2011), o Propiltiouracilo, o carbimazol e metilbazol, podemos concluir que todas as drogas citadas acima inibem a peroxidade tireóidea, fazendo a redução da síntese hormonais da tireoide. Já o Propiltiouracilo, bloqueia a desiodação extratiroidea de triiodotironina, o que leva a diminuição da concentração sérica e mais eficiente dos tratamentos.

Fonte: cenbrap.edu.br/Blog/Doença-de-Graves-tratamento
5.2.2 Iodo Radioativo
O iodo radioativo vem sendo utilizado desde 1941, é considerável fácil administrável, com o efeito rápido e de baixo custo. É um tratamento no qual induz o dano tecidual extenso (destruição da capacidade de síntese da glândula tireoide). Tem a capacidade de diminuir em 6 a 18 semanas a tireoide, levando a respostas no imuno aos antígenos tireoidianos. Faz com que as glândulas sejam acabadas, desenvolvendo o precoce de hipertireoidismo (NEVES et al., 2008).
De acordo com Guimarães et al. (2015), tratamento com iodo radioativo é contraindicado em lactantes e grávidas, pois ainda sim pode passar de mãe para o feto, e causar tireoide no bebê.
O tratamento com o iodo é o que gera uma tireoidite intensa secundária a radiação, e em seguida uma progressiva fibrose e atrofia glandular, dando um resultado no qual a distribuição da capacidade de síntese da glândula. Podendo induzir as respostas imune aos antígenos tireoidianos, sendo inicial e tardio.
Primeiramente, as células tireoidianas morrem e ai faz a liberação de antígenos na circulação, associada com um número alto de imunoglobulinas e na imunorreatividade celular. Logo depois, pode ocorrer a remoção de todo tecida tireoidiana e a logo assim a ausência de antígenos tireoidianos levando a redução autoimunidade.
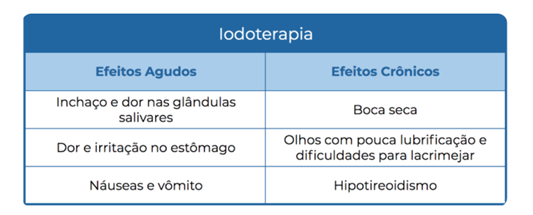
Fonte: : nicap.com.br/iodoterapia-indicacoes-e-cuidados
O iodo em comparação aos fármacos tem a menor chance de recorrência (5 a 20% dos pacientes, de acordo com a dose aplicada). Sendo assim, a melhoria inicial demora um pouco mais, tornando a porcentagem dos que sofrem de hipotireoidismo um pouco mais elevado (WEETMAN 2000).
5.2.3 Cirurgia
A cirurgia é o procedimento menos utilizado atualmente no tratamento da doença de graves, mas não deixando e ser importante em alguns casos clínicos, utilizada em doentes que não toleram a terapêutica com os fármacos, em gravidas que utilizam doses elevadas das drogas, os com bócio grande ou com nódulos em avaliação, utilizados em doentes que recusam o iodo, e para os que preferem tratamento de rápido efeito (HEGEDUS 2009).
Em doentes que se encontram em eutiroidismo usam os anti-titoideus, para se submeter à cirurgia. O pré-operatório pode ser utilizado iodo- orgânico saturando com iodeto de potássio ou lugol, sendo utilizado por uma semana, com o objetivo de abaixar a produção hormonal tiroidanas, e a vascularização (BRENT 2008).
Em alguns casos são necessárias intervenções urgentes, onde há evidência que pode ter um controle rápido usando tionaminas, solução saturada de iodeto de potássio, dexametasona e bloqueadores (WONDISFORD AND RADOVICK 2009).
Os cirurgiões recomendam a remoção total ou quase total na tiroidectomia. A cirurgia é de risco baixo, e com baixa taxa de efeitos secundários, sendo alguns frequentes, as lesões do nervo laríngeo- 0,7%- e o hipoparatiroidismo – 1% (WONDISFORD AND RADOVICK 2009). O uso da tiroxina é feito pelo resto da vida dos doentes de tiroidectomia total, sendo a recorrência quase nula.
6 CONCLUSÃO
A doença de graves vem se tornando mais comum com o tempo, sendo sua causa uma falha na glândula tireoide, podendo ter diferentes tipos de casos ou gravidades da doença que provoca diferentes tipos de tratamento.
Identificamos três tipos de contramedidas para a doença como os fármacos, exposição ao iodo e a cirurgia. Os três métodos podem ser eficazes para a pessoa dependendo da gravidade. Seu diagnóstico pode ser feito através de exames de sangue, para medir a quantidade de hormônio TSH e T4 no sangue e através de exames de imunologia para ver se há anticorpos que atacam a tireoide no corpo.
Mesmo com as diversas dificuldades da doença, vemos que se seguir um tratamento regular com acompanhamento de profissionais em muitos casos a pessoa pode viver uma vida normal e saudável, auxiliando assim no tratamento da mesma diminuindo diversos fatores que possam provocar o aumento dos sintomas.
BIBLIOGRAFIA
AZEVEDO, FVR. et al. Emerging comorbidities in Graves’ disease patients treated with radioiodine with more than 10 years of follow-up. Arquivos Brasileiros de Endocrinologia & Metabologia, v. 57, n. 1, p. 51-56, 2013. GUIMARÃES FILHO, SR. et al. Prevalência do tabagismo e sua influência sobre exoftalmia em pacientes que receberam diagnóstico de doença de graves em hospital- escola da Paraíba.
Revista Saúde & Ciência Online, v. 4, n. 1, p. 105-115, 2015.
Abraham P, Acharya A. Current and emerging treatment options for Graves’ hyperthyroidism. Ther Clin Risk Manag. 2010;6:29-40.
NEVES, C. et al. Doença de Graves. Arquivos de medicina, v. 22, n. 4- 5, p. 137-146, 2008.
HALL, John E.; GUYTON, Arthur C.. Tratado de fisiologia médica. 12 ed. Rio de Janeiro: Elsevier, 2011. HARVARD
MEDICAL SCHOOL. Doença de graves. Acesso em 10/09/2022
https://portal.wemeds.com.br/doenca-de-graves-manejo-clinico/ Acesso em : 16/10/2022
Thanh D. Hoang et al. 2022 Update on Clinical Management of Graves Disease and Thyroid Eye Disease. Endocrinol Metab Clin N Am 51 (2022) 1–18. https://www.tuasaude.com/tratamento-para-doenca-de-graves/#:~:text=O%20tratamento%20da%20doen%C3%A7a%20de,insufici%C3%AAncia%20card%C3%ADaca%20congestiva%20ou%20osteoporose.
Jameson JL, et al., eds. Hyperthroidism. In: Harrison’s Principles of Internal Medicine. 20th ed. New York, N.Y.: The McGraw-Hill Companies; 2018.
PINHEIRO, Pedro. Hipertireoidismo e doença de Graves: sintomas e tratamento, mdsaude, 2022. Disponível em: https://www.mdsaude.com/endocrinologia/hipertireoidismo/ . Acesso em : 16/10/2022
Bartalena L, Baldeschi L, Dickinson A, Eckstein A, Kendall-Taylor P, Marcocci C, et al. Consensus statement of the European Group on Graves’ orbitopathy (EUGOGO) on management of GO. Eur J Endocrinol. 2008;158(3):273-85. https://pebmed.com.br/endo-2022-consequencias-a-longo-prazo-do-tratamento-de-graves/. Acesso em : 10/09/2022
Rivkees SA, Stephenson K, Dinauer C. Adverse events associated with methimazole therapy of graves’ disease in children. Int J Pediatr Endocrinol. 2010;2010:176970
Yip J, Lang BH, Lo CY. Changing trend in surgical indication and management for Graves’ disease. Am J Surg. 2012;203(2):162-7.
Boelaert K, Syed AA, Manji N, Sheppard MC, Holder RL, Gough SC, et al. Prediction of cure and risk of hypothyroidism in patients receiving 131I for hyperthyroidism. Clin Endocrinol (Oxf). 2009;70(1):129-38
Lytton SD, Kahaly GJ. Bioassays for TSH-receptor autoantibodies: an update. Autoimmun Rev 2010; 10:116.
Suzuki N, Noh JY, Yoshimura R, et al. Does Age or Sex Relate to Severity or Treatment Prognosis in Graves’ Disease? Thyroid 2021; 31:1409.
¹Autor
²Orientador
³Co-orientador
