REGISTRO DOI: 10.5281/zenodo.7637606
Max Heitor Brito Lins
Vanessa de Carla Batista Santos
Katharina Jucá de Moraes Fernandes
Jaqueline Barbosa de Lima
Lorene Amorim Farias
Deborah Pereira de Oliveira
Catarina Rodrigues Rosa de Oliveira
Ângela Líbia Chagas Amaral Araujo
RESUMO
Objetivo: Destacar a importância da Odontologia na reabilitação de pacientes portadores de Miastenia Gravis, bem como discutir a qualidade de vida desses pacientes, buscando a correta conduta para uma reabilitação orofascial por meio de tratamentos complementares e funcionais satisfatórios como o LASER de baixa intensidade e reabilitação protética. Detalhamento do caso: Paciente de 46 anos, sexo Feminino, portadora de Miastenia Gravis, compareceu à Clínica Escola do Cesmac queixando-se de sua Prótese Parcial removível superior, que não estava fixa devido à grande perda de peso e uso de VNI, quando estava em situação de internamento durante tratamento da plasmaferése. Dessa forma, optou-se pelo pelo scanner intra-oral digital e, consequentemente, deu-se início a um protocolo individualizado de laser-terapia de baixa intensidade, intensidade de 2J com 20 pontos de aplicação no lábio superior e inferior, intra e extra-oral, somado a 6 pontos de aplicação em todo dorso da língua da paciente. Considerações finais: O paciente obteve uma melhora significativa da força muscular exercida tendo como protocolo odontológico a reabilitação protética e LASER de baixa intensidade. O tratamento foi bem-sucedido e indolor.
Palavras-chave: MIASTENIA GRAVIS; TERAPIA COM LUZ DE BAIXA INTENSIDADE; PRÓTESE MAXILAR.
ABSTRACT
Objective: To highlight the importance of dentistry in the rehabilitation of patients with Myasthenia Gravis, as well as discuss the quality of life of these patients, seeking the correct conduct for orofascial rehabilitation through satisfactory complementary and functional treatments such as low intensity laser and prosthetic rehabilitation. Case description: A 46-year-old female patient, with Myasthenia Gravis, came to the Clinical Escola do Cesmac complaining about her upper partial removable prosthesis, which was not fixed due to great weight loss and use of NIV, when she was in hospital during treatment for plasmapheresis. Thus, a digital intraoral scanner was chosen and, consequently, an individualized protocol of low intensity laser therapy was started, intensity of 2J with 20 points of application on the upper and lower lip, intra and extra-oral, added to 6 points of application on the entire dorsum of the patient’s tongue. Final considerations: The patient obtained a significant improvement in the muscle strength exerted having as dental protocol the prosthetic rehabilitation and low intensity laser. The treatment was successful and painless.
Keywords: MYASTHENIA GRAVIS; LOW-INTENSITY LIGHT THERAPY; PROSTHETIC DENTISTRY.
1 INTRODUÇÃO
A Miastenia é uma doença autoimune que causa uma desordem da junção neuromuscular, afeta os músculos do corpo de forma generalizada e seu diagnóstico pode ser feito a partir do exame laboratorial de anti-AChR (Anti-Acetilcoline Receptor) (MERIGGIOLI, et al., 2009).
Segundo Dracman (1994), os sintomas clínicos podem variar entre pacientes, mas em sua grande maioria apresentam fraqueza generalizada nos músculos oculares, bulbares e respiratórios. A fraqueza pode aumentar ao passar do dia e os sintomas se agravam quando algum tipo de atividade física é realizado, sendo necessário o uso de drogas anticolinesterásicos. (GROB, et al., 2008).
Paralelamente, a terapia com luz de baixa intensidade é opcional e complementar, demonstrando-se bastante eficaz diante de estudos randomizados recentes ao comparar a estética e funcional dos pacientes, por meio de análise quantitativa (MATOS, et al., 2021). Trata-se de uma radiação emitida pelo laser com a capacidade de induzir processos fotobiológicos atérmicos e não destrutivos para reabilitação muscular (SCHINDL, et al., 2020). Segundo Pessoa (2020), a aplicação de Laser, seguindo um protocolo correto, devolve a função muscular, ganho de força e amplitude muscular, principalmente ao tratar de músculos da mastigação.
No presente relato de caso, discorre-se sobre o impacto do odontólogo na reabilitação orofacial de um paciente que teve os músculos faciais atingidos por uma doença rara, associado à sua reabilitação protética que catalisará essa recuperação, principalmente na parte fonética e funcional dos músculos faciais e mastigatórios, trazendo resultados positivos que impactam diretamente as relações socioculturais e complementares para o tratamento da Miastenia Gravis.
O objetivo do trabalho é destacar a importância da Odontologia nos tratamentos de pacientes com desordens da junção neuromuscular e de doenças autoimunes que acometem o músculo facial.
2 DETALHAMENTO DO CASO
Este é um estudo de caso está sendo apreciado e aprovado pelo Comitê de Ética em Pesquisa (CEP) (ainda sem parecer), tendo a concordância do paciente com a assinatura do Termo de Consentimento Livre e Esclarecido (TCLE) e o paciente em questão assinou o Termo de Consentimento Livre e Esclarecido e Autorização do Uso de Imagem.
Paciente de 46 anos, sexo Feminino, portadora de Miastenia Gravis, compareceu à Clínica Escola do Cesmac queixando-se de sua Prótese Parcial removível superior, que não estava fixa devido à grande perda de peso e uso de VNI, quando estava em situação de internamento durante tratamento da plasmaferése. Dessa forma, optou-se pelo pelo scanner intra-oral digital e, consequentemente, deu-se início a um protocolo individualizado de laserterapia de baixa intensidade, intensidade de 2J com 20 pontos de aplicação no lábio superior e inferior, intra e extraoral, somado a 6 pontos de aplicação em todo dorso da língua da paciente.
A portadora de Miastenia Gravis, reagente para exame da enzima Acetil-colina, fazendo uso das seguintes drogas diariamente: 8x Mestinon (60mg), 2x Azatioprina (50mg), 1x Prednisona (5mg), apresentando uma fraqueza muscular generalizada, voz anasalada, com disfagia, compareceu à Clínica Escola do Cesmac relatando como queixa principal a sua antiga Prótese parcial removível tinha quebrado ao fazer uma tentativa de adaptação oral, pois a mesma estava folgada devido a sua rápida perda de peso e uso de VNI no momento em que ficou internada fazendo uso de plasmaferése, 17 sessões ao total, 8 sessões no primeiro internamento e 9 sessões na segunda crise miastênica com intervalo de 13 dias entre elas. Durante os exames clínicos intra e extra orais constatou-se que a paciente possuía um selamento labial falho, com abertura de 1mm entre os lábios superiores e inferiores, ausência dos elementos 12,11 e 21, assim como movimentos de protrusão e retrusão limitados, abertura da mandíbula dificultosa com apenas 22mm de abertura, fraqueza muscular que acometeu a língua, impedindo a paciente de fazer contato com palato ou contato com os dentes, dificultando sua fonação e mastigação, relatou que estava fazendo uso de comida pastosa e que durante a alimentação a língua fadigava fazendo-a pausar diversas vezes e que maioria das vezes resultava em disfagia.
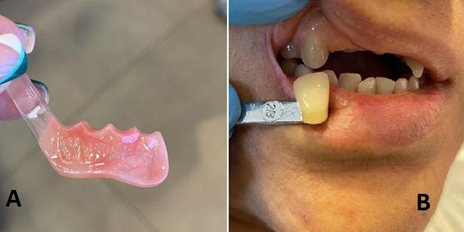
Diante desse quadro, foi indicado plano de tratamento iniciando com uma prótese provisória, respeitando as limitações físicas do paciente. Foram realizados os registros em DVO e DVR (Figura 1), O procedimento foi feito a partir de um scanner intraoral digital, obtendo-se o modelo digital da arcada dentária do paciente, sem a necessidade de moldeiras físicas, tendo uma maior precisão, rapidez, estética, previsibilidade e mais conforto para o paciente que possui limitações de abertura e risco de náuseas provocadas pelo protocolo padrão de moldagem e na mesma sessão já foi feita a seleção da cor dos elementos 12,11 e 21 e a escolha da cor da gengiva (Figura 2A), dentes TRILUX e cor final 3e da escala TRILUX (Figura 2B).
Figura 1: (A) Registro Dimensão Vertical Oclusal (B) Registro Intermaxilar
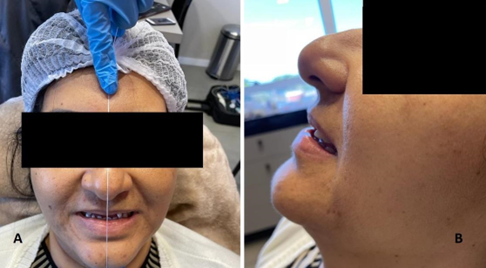
Figura 2: (A) Seleção da cor da gengiva (B) Seleção da Cor dos dentes
Após o procedimento, o paciente foi orientado para aguardar o resultado da impressão em 3D e confecção da prótese provisória no intervalo de 14 dias (Figura 3). Logo após, foi solicitado o retorno do paciente para consultório para a prova da prótese provisória, visto que esse procedimento por meio de um modelo digital tem como margem de erro quase nula, obtendo-se um resultado excelente que visa o conforto, economia de tempo, precisão, rapidez, previsibilidade e respeito as limitações físicas do paciente. Obtendo-se o resultado final (figura 4).
Figura 3 : (A) Vista occlusal da prótese (B) Vista vestibular do modelo 3D com prótese provisória
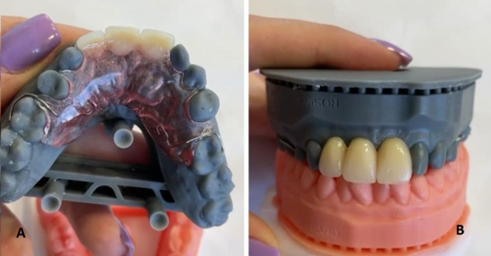
Figura 4 : Resultado Final
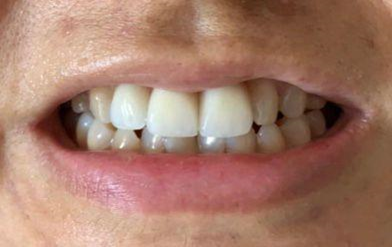
Com a reabilitação oral completa do paciente, deu-se segmento ao tratamento, através da realização do protocolo de LASER de baixa intensidade criado para a paciente em questão, foram realizadas 3 sessões, com aplicações intra e extra oral no lábio superior, inferior e na língua, visando obter uma maior resistência muscular. O LASER foi aplicado em 14 pontos no lábio superior e inferior (Figura 5) intra e extra oral, além de 6 pontos na língua. A dosagem foi de 2J por ponto, resultando em uma dose total de 28 J no lábio superior e 28J no lábio inferior. O equipamento foi ligado para emitir som, a irradiação foi feita encostando a ponteira do equipamento sobre a pele e mucosa oral do paciente. A ponta e parte do corpo do equipamento encapado com um filme plástico transparente, durante a aplicação tanto os aplicadores quanto o paciente utilizaram óculos de proteção fornecidos pela fabricante do equipamento.
Figura 5: Pontos de aplicação do laser de baixa intensidade
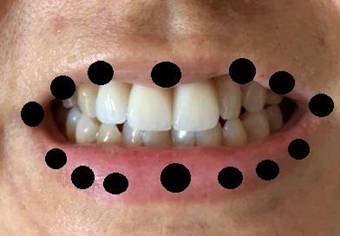
Seguindo-se as recomendações do fabricante e atendendo às normas de segurança estabelecidas pela ANVISA para utilização do LASER de baixa intensidade, tanto os alunos supervisionados tanto a paciente utilizaram óculos de proteção durante todo o procedimento. Após a aplicação do LASER, foram solicitados exercícios de máxima pressão labial, afim de proporcionar um maior restabelecimento da musculatura, foi solicitado o paciente “mandar beijo” e “sorrir ao máximo” como exercícios seguidos, repetidos por 10 vezes.
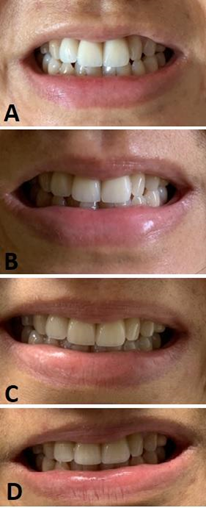
Após a primeira sessão o resultado foi perceptível (Figura 6A), conferindo uma maior resistência e força muscular, em seguida foi dado seguimento a segunda sessão (Figura 6B) previstas no protocolo criado para a paciente, as aplicações foram semanais.
Na terceira e última sessão da aplicação do LASER de baixa intensidade (figura 6C), para salientar a eficácia do LASER de baixa intensidade em pacientes que apresentam uma fraqueza muscular facial, em seguida foi registrado a força muscular do sorriso da paciente 15 dias após a terceira aplicação (Figura 6D).
Figura 6: (A) Pós da primeira sessão de Laserterapia de baixa intensidade (B) Pós-imediato da segunda sessão de Laserterapia (C) Pós-imediato da terceira sessão de laserterapia (D) Paciente 15 dias após a terceira sessão
3 DISCUSSÃO
A Miastenia Gravis (MG) pode ser considerada como uma doença autoimune de origem neuromuscular, que tem uma taxa considerável de mortalidade e morbidade. É uma doença tratável que deve ser diagnosticada e tratada o mais precocemente possível. O diagnóstico pode ser fechado através do exame de reagentes da enzima Acetilcolina, a maioria dos pacientes portadores dessa patologia tem em seu corpo auto anticorpos direcionados para a Acetilcolina, ou mais rara ainda, a quinase músculo-específica: MusK. Os principais sintomas clínicos da doença é uma fadiga muscular excessiva, que afeta os músculos oculares, músculos faciais, músculos da deglutição, músculos do tórax, causando complicações no fluxo respiratório em casos mais graves e não-tratados. Em alguns casos, a tomografia computadorizada deve ser feita em pacientes com MG para excluir a presença de um timoma. O uso de ressonâncias magnéticas em pacientes miastênicos não tem um bom desfecho, certos pacientes podem apresentar uma piora dos sintomas da Miastenia logo após a execução do exame. Geralmente, alguns pacientes tem uma segunda crise miastênica, como foi o caso do relato de experiência, a porcentagem gira em torno dos 15%, pacientes que podem desenvolver uma segunda crise autoimune durante a vida: ocorre em maior caso quando o mesmo foi diagnosticado de forma precoce, durante a primeira manifestação da doença e, não obstante, a tireoidite é a segunda causa mais comum, seguida pela hiperplasia tímica. (GILHUS NE, et al., 2015).
Ao examinar um paciente com Miastenia Gravis, o profissional da saúde deve gerar essa fadiga, na região onde o paciente mais reclama, principalmente. Com isso, um determinado grupo muscular deverá ser fadigado e por fim, será avaliado a força exercida por esses músculos. Caso a reclamação do paciente esteja relacionada aos músculos superiores, devem ser feitos testes de resistência repetida vezes, fazendo o paciente levantar o braço várias vezes e, por fim, manter o braço totalmente estendido, acima da cabeça, induzindo essa fraqueza fatigante. Caso a reclamação da paciente esteja relacionada aos membros inferiores, deve ser solicitado que a paciente sente e se levante de uma cadeira sem os apoios das mãos, entre 10-15 vezes. Esses testes clínicos são responsáveis por um diagnóstico inicial de fraqueza muscular e resistência muscular afetada, devendo encaminhar a paciente para exames específicos da patologia, como já foram citados anteriormente (RUCKER JC; TOMSACK TL, 2005).
A MG geralmente é tratada com fármacos que geram um bloqueio da acetilcolinesterase na junção neuromuscular. Esses medicamentos mantêm na fenda sináptica, um maior acesso e número de acetilcolina, evitando uma exaustão muscular e agravo da patologia. Os medicamentos usados durante o tratamento têm poucos efeitos colaterais, porém em alguns casos foram relatados efeitos adversos ao fármaco Azatioprina, um remédio autoimune, os efeitos colaterais relatados foram: mal-estar geral, tontura, febre, erupção cutânea, disfunção renal, disfunção hepática e hipotensão e independe de sua concentração. A diarreia, ainda é um dos efeitos colaterais mais comuns relacionado ao fármaco. Assim como foi o caso do relato de caso, pacientes que tem uma Miastenia Gravis ocular devem ser tratados com medicamentos autoimunes e, caso não corresponda efeitos clínicos suficientes, deve-se acrescentar corticoides. Em casos de Miastenia Gravis generalizada deve ser feito um tratamento em conjunto com o fármaco de origem autoimune associado com corticoides durante os primeiros anos. A dose deve ser ajustada de acordo com o paciente e a sintomatologia apresentada. Caso um paciente consiga dispensar aquele remédio em sua rotina de tratamento medicamentoso, é um sinal que o portador da patologia atingiu um sucesso em seu tratamento: atingiu a meta do imunossupressor, o que deve ser avaliado pelo Neurologista responsável se a dose deve ser diminuída ou o fármaco retirado de sua rotina de tratamento. Os casos positivos de Miastenia Gravis do tipo MusK, apresentam uma maior resistência ao tratamento via oral, tendo maior nível de reações medicamentosas e efeitos colaterais ao associar o medicamento Piridostigma, apresentação comercial: Mestinon, no tratamento (GILHUS NE; VERSCHUUREN JJ, 2015).
O fármaco Prednisona, sintético, glicocorticoide, tem potentes ações anti-inflamatórias, antialérgicas e antirreumáticas, utilizado amplamente no cenário odontológico, tem um efeito positivo ao associar com a MG. As concentrações mais comuns durante o tratamento do miastênico são entre 15-20mg e auxiliará pacientes com condições oculares afetadas em até 3 meses de tratamento contínuo, o portador da patologia deve ser paciente. Em casos mais graves, dosagens mais altas já foram registradas, porém, se após 2 ou 3 meses durante o tratamento com o Prednisona o paciente não obter resultados clínicos positivos, sua dosagem pode aumentar até 1mg/kg. A concentração pode ser diminuída após 3 meses de uma melhora e evolução da conduta clínica (BENATAR M, et al., 2016).
A Azatioprina pode ser utilizada em conjunto com o Prednisona por via oral, ou de forma isolada. É um medicamento autoimune que deve levar até 3 meses para seus primeiros efeitos positivos durante o tratamento da MG sejam notados. O efeito máximo do fármaco autoimune é descrito como potente e pode ser observado entre 6-18 meses de tratamento contínuo. Portanto, assim como foi descrito no caso, deve-se ter paciência para a diminuição da concentração do Prednisona, quando associado ao Azatioprina, para evitar alterações hepáticas e renais. Paralelamente, deve ser feito mensalmente, hemogramas completos e monitoramento das enzimas hepáticas, visto que, Azatioprina aumenta o risco de malignidades, principalmente de origem dermatológica. Embora o risco seja quase nulo, pacientes que já tiveram alterações de pele ou câncer na mucosa, devem ser monitorados de forma mais atenta possível com exames complementares mensais (PEDERSEN EG, et al., 2014).
A Rituximabe é um medicamento que é mais específico de quem tem a Miastenia Gravis do tipo MusK, que no qual não tem uma melhora da evolução clínica seguindo o protocolo de tratamento padrão, com Piridostigma, por exemplo (DE FEO LG, et al., 2002). Esse medicamento tem um efeito mais rápido do que todos citados anteriormente, estando limitado apenas à países onde foram realizados estudos de placebo duplos-cegos, o Brasil não se encontra entre eles. Este fármaco tem um efeito rápido e potente, podendo ser comparado a tratamentos como a imunoglobulina (HEHIR MK, et al., 2017).
A paciente em questão, passou por uma crise miastênica, que é quando grupos de músculos maiores, ou de forma generalizada, são atingidos de forma mais agressiva e grave. No caso, a sintomatologia da paciente era bastante parecida com características do tipo MusK: fraqueza generalizada nos músculos do tórax, ptose palpebral bilateral, fraqueza nos músculos da mastigação e fala, deglutição comprometida. Porém, resultados laboratoriais acusaram a paciente de ser portadora da Miastenia Gravis de origem na enzima acetilcolina. Nesses casos, o tratamento da Miastenia deve ser imediato, evitando a morte do paciente e complicações permanentes para o resto de sua vida. Uma crise miastênica requer uma internação urgente e observação durante todo o momento das vias respiratórias e bulbares. A Imunoglobulina humana e a Plasmaferese são utilizados em tratamentos de crises miastênicas. São tratamentos de curto prazo, geralmente tem entre 6-10 sessões, com o único objetivo de retirar o paciente da crise. Logo em seguida, após a confirmação do diagnóstico, já é iniciado o protocolo medicamentoso: corticosteroides juntamente com remédios autoimunes são iniciados em conjunto. As escolhas entre os dois tratamentos são complexas, Imunoglobulina e Plasmaferese, devem ser levadas em consideração as adversidades e condições únicas de cada paciente. Em casos de insuficiência renal, o tratamento com a imunoglobulina está contraindicado, não obstante, a Plasmaferese não pode ser iniciada em pacientes que tem sepse, algum distúrbio hepático ou desordens hematológicas. A plasmaferese pode ser mais útil e ter melhores resultados em pacientes com anti-MusK. Apesar de uma ausência de pesquisas comparativas na área entre os tratamentos, existe um grande consenso entre os médicos hematologistas que a Plasmaferese é mais útil e eficaz que o tratamento da imunoglobulina para uma retirada de uma crise de MG (GILHUS NE, VERSCHUUREN JJ, 2015).
Diante do exposto, a paciente em questão tinha acabado de sair de um quadro de crise miastênica, onde fez ao total 16 sessões de Plasmaferese. A paciente perdeu peso e foi colocada sob observação na Ventilação Não Invasiva (VNI), o que ocasionou a perca de sua Prótese Parcial Removível (PPR) superior, além disso, a paciente se queixava bastante da sua dificuldade de deglutição, sendo encaminhada para a Clínica de Odontologia do Cesmac, por intermédio de familiares para uma reabilitação protética e orofacial. Durante o atendimento, a paciente não conseguiu realizar a etapa de moldagem inicial/estudo para o início do protocolo de confecção de uma nova PPR. Dessa forma, optou-se pelo pelo scanner intraoral digital.
Desde 1990, a odontologia vem crescendo aliada à tecnologia. Procedimentos, principalmente da área ortodôntica, vem ganhando espaço cada vez mais no mercado odontológico pela praticidade, exposição do paciente e resultado final. Fotos digitais, registros com mapeamento intraoral digital, impressão de modelos em 3D estão se tornando padrão em todo mundo. (WHETTEN JL, et al., 2006; OKUNAMI TR, et al., 2007; WIRANTO MG, et al., 2013; AKYALCIN S, et al., 2013). Consequentemente, deu-se início a um protocolo individualizado de laserterapia de baixa intensidade, intensidade de 2J com 20 pontos de aplicação no lábio superior e inferior, intra e extraoral, somado a 6 pontos de aplicação em todo dorso da língua da paciente.
4. AGRADECIMENTOS
Agradecemos primeiramente a Deus por nos ter dado saúde e força para superar as dificuldades. À Professora Dra. Vanessa de Carla, juntamente a toda equipe de Propedêutica Clínica do Centro Universitário CESMAC, agradecemos por todo ensinamento, companheirismo e auxílio durante os atendimentos. À Professora Dra. Katharina Jucá por todo auxilio, incentivo e apoio. À Dra. Catarina Rosa por todo apoio e confiança. Em especial à Professora Dra. Ângela Líbia pela oportunidade e apoio psicológico durante momentos difíceis e na elaboração deste trabalho.
REFERÊNCIAS
MERIGGIOLI M, SANDERS D; Autoimmune myasthenia gravis: emerging clinical and biological heterogeneity. The Lancet Neurology, p. 475-490, v.8, n.5.
DRACHMAN D B. “Myasthenia gravis.” The New England journal of medicine, p. 1797–1810, vol. 330, n.25, (1994).
GROB DAVID, et al. ; Lifetime course of myasthenia gravis, Muscle & Nerve, p. 141-149 v.37 n.2, 2008
MATOS A.L., et al; “Efficacy of the laser at low intensity on primary burning oral syndrome: a systematic review.” Medicina oral, patologia oral y cirugia bucal vol. 26, n.2 p.216-225.
SCHINDL A., et al. “Low-intensity laser therapy: a review.” Journal of investigative medicine: the official publication of the American Federation for Clinical Research vol. 48, N.5, 312-326 (2020)
PESSOA DR, et al. “Association of facial massage, dry needling, and laser therapy in Temporomandibular Disorder: case report.” CoDAS vol. 30, n.6, 29 de Nov. 2018.
OLIVEIRA J. A. G., et al. (2014). Clareamento dentário x autoestima x autoimagem. Archives of Health Investigation, 3(2).
OLIVEIRA, A.F.S.S. Does photobiomodulation improve muscle performance and recovery – a systematic review. Revista Brasileira de Medicina do Esporte [online]. 2023, v. 29. e2021_0412.
GILHUS NE, NACU A, ANDERSEN JB, OWE JF. Myasthenia gravis and risks for comorbidity. Eur J Neurol. 2015 Jan;22(1):17-23.
Rucker JC, Tomsack TL. Binocular diplopia: a practical approach. Neurologist. 2005 Mar;11(2):98-110.
GILHUS NE, VERSCHUUREN JJ. Myasthenia gravis: subgroup classification and therapeutic strategies. Lancet Neurol. 2015 Oct 1;14(10):P1023-36.
BENATAR M, MCDERMOTT MP, SANDERS DB, WOLFE GI, BAROHN RJ, NOWAK RJ, et al. Efficacy of prednisone for the treatment of ocular myasthenia (EPITOME): a randomized, controlled trial. Muscle Nerve. 2016 Mar;53(3):363-9.
PEDERSEN EG, POTTEGÅRD A, HALLAS J, FRIIS S, HANSEN K, JENSEN PEH, et al. Risk of non-melanoma skin cancer in myasthenia patients treated with azathioprine. Eur J Neurol. 2014 Mar;21(3):454-8. https://doi. org/10.1111/ene.12329
DE FEO LG, SCHOTTLENDER J, MARTELLI NA, MOLFINO NA. Use of intravenous pulsed cyclophosphamide in severe, generalized myasthenia gravis. Muscle Nerve. 2002 Jul;26(1):31-6.
HEHIR MK, HOBSON-WEBB LD, BENATAR M, BARNETT C, SILVESTRI NJ, HOWARD JF JR, et al. Rituximab as treatment for anti-MuSK myasthenia gravis: multicenter blinded prospective review. Neurology. 2017 Sep 5;89(10):1069-77.
GILHUS NE, VERSCHUUREN JJ. Myasthenia gravis: subgroup classification and therapeutic strategies. Lancet Neurol. 2015 Oct 1;14(10):P1023-36.
WHETTEN JL, WILLIAMSON PC, HEO G, VARNHAGEN C, MAJOR PW. Variations in orthodontic treatment planning decisions of Class II patients between virtual 3-dimensional models and traditional plaster study models. Am J Orthod Dentofacial Orthop. 2006; 130: 485-91. 7.
OKUNAMI TR, et al., 2007. Assessing the American Board of Orthodontics objective grading system: Digital vs plaster dental casts. Am J Orthod Dentofacial Orthop. 2007; 131: 51-6. 8.
AKYALCIN S, DYER DJ, ENGLISH JD, SAR C. Comparison of 3-dimensional dental models from different sources: Diagnostic accuracy and surface registration analysis. Am J Orthod Dentofacial Orthop. 2013; 144: 831-7. 9.
WIRANTO MG, ENGELBRECHT WP, NOLTHENIUS HET, MEER WJ, REN Y. Validity, reliability, and reproducibility of linear measurements on digital models obtained from intraoral and cone-beam computed tomography scans of alginate impressions. Am J Orthod Dentofacial Orthop. 2013; 143: 140-7.
