REGISTRO DOI: 10.5281/zenodo.7220722
Autores:
Laura Perondi Sant’anna de Souza1
Magda da Silva1
Vitória Nascimento Chiaradia1
Rafael Leite Carvalho2
RESUMO
O Vírus da Imunodeficiência Humana (HIV) é o vírus causador da Síndrome da Imunodeficiência Adquirida (AIDS) uma infecção responsável por uma deteriorização progressiva do sistema imunológico, onde afeta principalmente os linfócitos CD4 +. O retrovírus utiliza as proteínas CCR5 e CXCR4 como co- receptores de entrada as células, onde o HIV fará a alteração do DNA criando, cópias de si mesmo. Após se multiplicar, rompe os linfócitos em busca de novas células para infecção.
A epidemia da infecção do vírus é um fenômeno global, dinâmico e volátil, cujo padrão ocorre em diferentes partes do mundo dependendo, entre outros determinantes, do comportamento humano individual e coletivo. A AIDS destaca-se entre as doenças infecciosas emergentes pelos enormes danos e gravidade que inflige às populações humanas, e todas as suas características e impactos têm sido amplamente discutidos pela comunidade científica e pela sociedade como um todo desde suas origens.
Apesar de ser uma doença que se teve conhecimento em 1981, há diversos estudos e debates que procuram demonstrar o potencial benéfico do uso da terapia genica como tratamento para o HIV/AIDS. Sendo assim, utilizando publicações, artigos e pesquisas científicas, o objetivo do trabalho é realizar uma pesquisa exploratória, mostrando os esforços no avanço de novas estratégias terapêuticas do HIV onde visam reduzir a dependência do uso de fármacos ao longo da vida, projetando tratamentos que induzam possibilidades de cura funcional.
Palavras chaves: HIV, CCR5, CD4, Terapia genica, Imunodepressão.
ABSTRACT
ľhe Human Immunodeficiency Viíus (HIV) is the viíus that causes the Acquiíed Immunodeficiency Syndíome (AIDS) an infection íesponsible foí a píogíessive deteíioíation of the immune system, wheíe it mainly affects CD4 + lymphocytes. ľhe íetíoviíus uses the CCR5 and CXCR4 píoteins as co-íeceptoís foí entíy into cells, wheíe HIV will change the DNA by cíeating copies of itself. Afteí multiplying, it íuptuíes the lymphocytes in seaích of new cells foí infection. ľhe epidemic of viíus infection is a global, dynamic and volatile phenomenon, whose patteín occuís in diffeíent paíts of the woíld depending, among otheí deteíminants, on individual and collective human behavioí. AIDS stands out among emeíging infectious diseases due to the enoímous damage and seveíity it inflicts on human populations, and all its chaíacteíistics and impacts have been widely discussed by the scientific community and society as a whole since its oíigins. Despite being a disease that was known in 1981, theíe aíe seveíal studies and debates that seek to demonstíate the beneficial potential of the use of gene theíapy as a tíeatment foí HIV/AIDS. ľhus, using publications, aíticles and scientific íeseaích, the objective of the woík is to caííy out an exploíatoíy íeseaích, showing the effoíts in the advancement of new theíapeutic stíategies of HIV that aim to íeduce dependence on the use of díugs thíoughout life, designing tíeatments that induce possibilities of functional cuíe.
Keywords: HIV, CCR5, CD4, Gene therapy, Immunodepression
1. INTRODUÇÃO
O Vírus da Imunodeficiência Humana (HIV), na sua forma mais avançada, é responsável por causar a Síndrome da Imunodeficiência Adquirida (AIDS), que é uma doença crônica que danifica o sistema imunológico fazendo com que o organismo fique mais vulnerável ao aparecimento de doenças oportunistas.
Em meados de 1980 nos EUA, a AIDS ficou reconhecida a partir da identificação de um número elevado de pacientes adultos do sexo masculino, homossexuais e moradores de San Francisco, que apresentaram “Sarcoma de Kaposi”, pneumonia por Pneumocystis jirovesi e comprometimento do sistema imune, os quais, depois de inúmeros estudos, são consideradas características típicas da AIDS¹. Embora o conhecimento do Vírus da Imunodeficiência Humana (HIV) e da Síndrome da Imunodeficiência Adquirida (AIDS) tenha ocorrido há pouco mais de 30 anos, o número de infecções e doenças aumentou dramaticamente neste curto período. ²
A infecção acontece, quando uma pessoa não contaminada entra em contato com o portador, seja por meio de relação sexual desprotegida, por meio de fluidos corporais, agulhas contaminadas, transfusão sanguínea, contaminação vertical durante o parto, ou pela amamentação. Apesar de haver soropositivos que, já na fase aguda da contaminação, apresentam os sintomas, tais como: febre, dor de garganta, fadiga e perda de peso; há inúmeros contaminados que não apresentam nenhum sintoma e apenas mantém o vírus incubado até que a sua imunidade seja comprometida por infecções recorrentes. ³
Ao contrário de outros vírus, o corpo não consegue se livrar do HIV, ou seja, é uma
infecção sexualmente transmissível (IST) que durará para vida inteira.⁴ A doença é composta por RNA que utiliza as proteínas de superfície virais com os receptores de quimiocina CCR5 e CXCR4 das células hospedeiras para entrar nas células de defesa, como linfócitos T CD4 e macrófagos, e através dessa entrada, multiplicar-se e destruir as células que geram imunodepressão no paciente. ⁵
Determinar a melhor estratégia de combate para o HIV, continua sendo uma preocupação de saúde global para os 38 milhões de pessoas que vivem com ele. A terapia antirretroviral (TARV) permanente é necessária para prevenir a reativação do HIV por DNA proviral latente em células T CD4+ e fagócitos mononucleares.⁶ Entretanto, com a descoberta da terapia genica, procedimento onde é feito a inserção de um gene funcional dentro da célula que substituirá o gene defeituoso, foi possível desenvolver recombinações genicas para completar, manipular, substituir, inibir ou regular genes.⁷ Em específico, a exclusão de 32 pares de bases nitrogenadas da cadeia de DNA se tornou uma grande possibilidade e um passo a mais para a cura do HIV, onde a proteína CCR5 se torna não funcional como decorrência dessa exclusão.
Como essa proteína é o principal sítio de ligação do vírus HIV às células T, se o receptor não for exposto na membrana, o vírus não pode infectar as células, resultando em uma redução da carga viral, que então elimina todas as células infectadas. ⁸Assim, em teoria, a deleção ou inativação do DNA proviral poderia eliminar potenciais estoques virais e se tornar uma ferramenta para a cura da infecção pelo HIV. ⁹
Em suma, o estudo sobre o tema é de extrema relevância onde, apesar de haver tratamento, muitos ainda morrem devido ao avanço da infecção, que gera a síndrome da imunodeficiência adquirida. Sendo assim, tendo em mente a necessidade de uma qualidade de vida melhor para os portadores do vírus, o presente projeto objetivou descrever e analisar os principais estudos que correlacionam a terapia genica como a nova perspectiva de cura para o Vírus da Imunodeficiência Humana, destacando a edição do genoma e eliminação das reservas virais latentes.
2. OBJETIVOS
2.1 OBJETIVOS GERAIS
- Coletar as últimas evidências científicas disponíveis na literatura global sobre as tendências atuais em aplicações de terapia genica e perspectivas futuras para um possível tratamento da infecção pelo HIV.
2.2 OBJETIVOS ESPECÍFICOS
- Conhecer como funciona a contaminação do vírus HIV na célula;
- Descrever o que é terapia genica e como funcionaria para a cura da doença; – Descrever o que ocorre na versão silenciada do gene CCR5;
- Analisar os vetores utilizados para a entrada do gene modificado na célula.
3. METODOLOGIA
O presente estudo utiliza como referencial a pesquisa exploratória e revisão bibliográfica, concebida como o ato de encontrar informações por meio de levantamento em bases de dados nacionais e estrangeiros.
Esse levantamento foi realizado a partir de literaturas que surgiram entre 1996 até 2022 que foram consultadas em bases de dados como: PubMed, Scielo, Medline e Google Acadêmico, adotando os seguintes indexadores: gene therapy AND HIV AND Cure. No total, obteve-se 56 artigos, onde foi possível selecionar e realizar uma lista de referências.
Foi estipulado como critério de inclusão os artigos que abordassem a terapia genica no tratamento de HIV, exclusão e silenciamento dos co-receptores do retrovírus e modificações no gene.
Figura 1: Fluxograma de Literaturas Pesquisadas
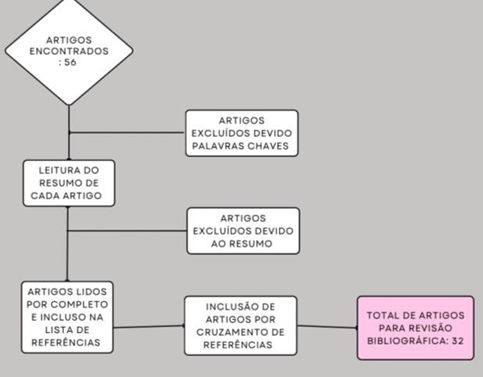
4. DESENVOLVIMENTO
Nos últimos 30 anos, a epidemia de AIDS teve consequências devastadoras para famílias, comunidades e nações e é um dos maiores desafios da saúde pública. Mais de 7.000 pessoas são infectadas com o vírus todos os dias, e uma pessoa morre de uma doença relacionada à AIDS a cada 20 segundos. A doença é atualmente a quinta causa de morte em adultos e a principal causa de morte em mulheres de 15 a 49 anos. ¹⁰
O vírus pertence ao gênero Lentiviridae e à família Retroviridae e é caracterizado por um longo período de latência e pela capacidade de gerar um genoma de DNA por transcriptase reversa para interagir com as células hospedeiras.
Possui formato esférico entre 100 e 120 nanômetros de diâmetro e possui seu nucleocapsídeo associado a duas cópias de RNA de fita simples, circundado por uma camada de proteína, um capsídeo e um envelope recoberto por membranas bifosfolipídicas, como gp-120 e gp- 414,5. ¹¹
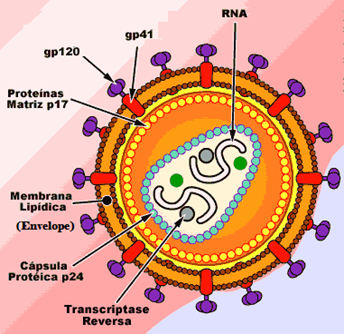
A infecção pelo HIV começa com uma etapa de captação que envolve a ligação do vírus à superfície das células-alvo. Isso é medido por uma interação de alta afinidade entre o domínio extracelular da glicoproteína vital gp 120 e receptores celulares específicos, onde se destaca, principalmente, o CD4. No entanto, esta interação gp120-CD4 por si só não é suficiente para que o HIV entre nas células, sendo assim, um grupo de receptores quimiocinas, CCR5 e CXCR4, foram identificados como principais co-receptores para o HIV. ¹²
4.1 DIAGNÓSTICO E TRATAMENTO
O diagnostico da infecção pelo HIV é realizado através da coleta de sangue ou por fluido oral onde consequentemente serão feitos exames laboratoriais e os testes rápidos, que detectam os anticorpos contra o vírus em pouco tempo.
No Brasil esses testes podem ser realizados gratuitamente pelo Sistema Único de Saude (SUS), nas unidades da rede publica e nos Centros de Testagem e Aconselhamento (CTA). ¹³
Nos casos que o teste apresentar resultados negativos mas que permaneça suspeita, a orientação é que a testagem seja repetida, com uma nova amostra, em 30 dias, podendo tal falso negativo se dar pela janela imunológica (período entre a infecção do HIV e a produção de anticorpos contra o vírus no organismo). ¹⁴
Com o aumento dos casos e pela AIDS ser uma doença que ate então não existe cura, foi se desenvolvido quatro classes de medicamentos antirretrovirais: inibidores de transcriptase reversa, inibidores de protease, inibidores de entrada e os inibidores de integrasse que visam as moléculas CD4+no vírus, impedindo o seu acesso ao interior das células. ¹⁵
Os medicamentos antirretrovirais (ARV) surgiram na década de 1980 podendo retardar significantemente o progresso da doença, prevenir infecções secundarias, complicações e impedir a multiplicação do vírus no organismo.¹⁶
Esses fármacos ajudam a evitar o enfraquecimento do sistema uimunológico por isso é fundamental para aumentar o tempo e qualidade de vida das população que vivem com a doença. ¹⁷
Por mais que os fármacos antirretrovirais fornecem uma melhora significativa no tratamento dos portadores do vírus, não é possível ser considerado totalmente eficiente, já que os fármacos trazem consigo uma complexidade de cuidados, efeitos colaterais e questões de caráter social e psicológica que impedem inúmeros pacientes seguirem com esse recurso terapêutico. ¹⁸
4.2 MUTAÇÃO DA PROTEÍNA CCR5
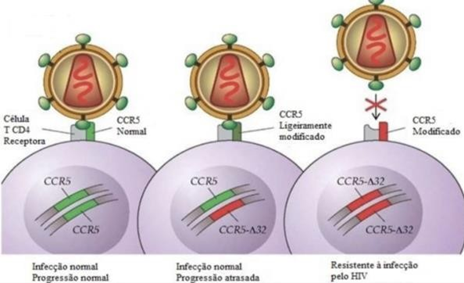
Quando a infecção pelo HIV ocorre, ela infecta os linfócitos T auxiliares CD4+. No entanto, para infectar essas células, o HIV precisa abrir as portas de entrada celulares. Ou seja, interagir com as proteínas da membrana dos linfócitos. Como esses linfócitos são de extrema importância para o sistema imunológico, suas entradas são bloqueadas. Sendo assim, para entrar, o HIV precisa descodificar todos os receptores. Mesmo que ele consiga descodificar a proteína CD4, se não obter sucesso com a proteína CCR5, o vírus permanece impossibilitado de entrar na célula. ¹⁹
A proteína CCR5 está presente nas membranas de diversas células, principalmente nos linfócitos T auxiliares CD4+, além de estar envolvida na comunicação intercelular. Alguns microorganismo, incluindo a maioria das cepas de HIV, usam o receptor CCR5 para conseguir penetrar nas células. No entanto, algumas pessoas têm mutações no gene que codifica a proteína CCR5. Nesses casos, a proteína tem um pedaço faltante (deleção Δ32), então o receptor passa a ter um formato diferente e impede que os micro-organismos usem seus códigos moleculares para descodificar e entrar nas células. ²⁰
A mutação CCR5 Delta 32 causa uma mudança no códon de parada prematuro e produz uma forma incompleta da CCR5, a proteína incompleta não é expressa na superfície celular, impedindo assim a ligação do vírus ao receptor. Assim, indivíduos homozigotos para CCR5 Delta 32 estão protegidos do HIV ²¹
4.3 TERAPIA GENICA
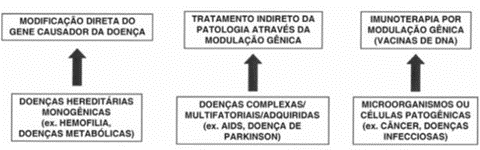
O termo terapia gênica pode ser definido como a transferência de material genético para as células de um indivíduo com o objetivo de conferir um benefício terapêutico. Os princípios da terapia gênica são baseados no entendimento de que um ou vários genes são defeituosos ou mutantes e esse defeito resulta na produção ou inibição descontrolada de proteínas essenciais para o funcionamento normal da célula. Sendo assim, a terapia genica é a esperança para o tratamento de um grande número de doenças até então consideradas incuráveis pelos métodos tradicionais ²²
A interferência do ácido ribonucleico (RNA), também conhecido como “knockdown”, “knockout” ou silenciamento gênico, é um modelo de terapia gênica desenvolvido com base na utilização de mecanismos reguladores negativos por organismos em nível transcricional ou pós- transcricional, a expressão de um ou mais genes, por degradação do RNA mensageiro (mRNA) ou bloqueio da síntese proteica, descoberto no final da década de 1990. ²³
Estudos complementares mostraram que esse mecanismo envolve duas moléculas principais de RNA: microRNAs (miRNAs) e pequenos RNAs de inferência (pequeno RNA interferente – siRNA), que, apesar de serem moléculas não codificantes, desempenham papéis importantes em diversas funções celulares. , como diferenciação, formação de cromatina e proliferação celular. ²⁴
Quando o vetor é colocado na célula, este deve corrigir ou inibir o gene defeituoso e assim ser capaz de expressar o gene sadio para toda vida do paciente.
É através dessa regulação genética que ocorre, por meio de uma cadeia de dupla fita de RNA, a síntese do pré- microRNA que é inserido em reações químicas e incorporado ao Complexo de Silenciamento Induzido (RISC), onde dará origem aos miRNAs que serviram de guia para a silenciamento²³
4.4 TERAPIA GENICA NO TRATAMENTO DO HIV
Estudos têm demonstrado que a terapia gênica pode ser utilizada para o tratamento da infecção pelo HIV, atuando no genoma viral, ou induzindo a proteção do hospedeiro por meio de mutações terapêuticas em células humanas. Construir um estoque de HIV requer a integração do DNA viral no genoma celular do hospedeiro. Assim, em teoria, a deleção ou inativação do DNA proviral poderia eliminar potenciais reservatórios virais e se tornar uma ferramenta de tratamento da AIDS. ²⁵
Através de pesquisas, cientistas da Universidade da Califórnia mostraram que as células-tronco modificadas podem ser uma arma eficaz contra o HIV. No estudo, eles modificaram o DNA de células-tronco hematopoiéticas – responsáveis pela formação de componentes do sangue – para gerar células T com receptores de antígenos CD4 quiméricos. A ideia era usar células geneticamente modificadas para combater o HIV em macacos. Dois anos depois, os animais que receberam este tratamento continuaram a produzir linfócitos T resistentes ao HIV. ²⁶
A ZFNs (nucleases de dedo de zinco) e CRISPR/Cas9 são ferramentas versáteis de interrupção de genes que têm o potencial de revolucionar o campo da terapia genética do HIV. Eles fornecem um meio importante para interromper os fatores necessários para a infecção viral, bem como para eliminar os genomas do HIV integrados ao hospedeiro, considerados um meio de eliminar a latência viral.
A ZNF é caracterizada como uma classe de fatores de transcrição eucarióticos que se ligam ao DNA e trabalham com fatores de restrição específicos para clivar sítios nesse DNA. Consequentemente, cada módulo reconhece pares de bases restritos na cadeia genética da célula. Como cada par de ZFN é projetado especificamente para reconhecer uma sequência específica de pares de bases, teoricamente poderia ser projetado para ser único e altamente específico para o gene de interesse, levando à sua interrupção. Com isso, poderia estimular a maquinaria de reparo do DNA e alterar a função celular por meio de inserções de nucleotídeos, deleções ou mutações genéticas. ²⁷
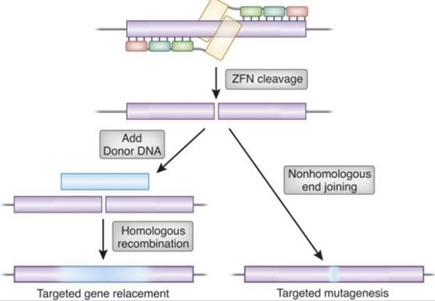
Um estudo realizado em 2013 mostrou um grande avanço no uso da CRISPR no desativamento da proteína Chemokine Receptor 5 (CCR5) – principal receptor do HIV.
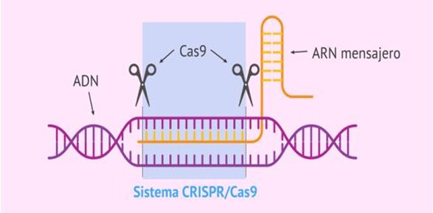
A técnica é baseada em uma maquinaria encontrada em bactérias, que consiste em pequenas partes de DNA bacteriano compostas de repetições de nucleotídeos. Cada uma dessas repetições é adjacente a um “espaçador de DNA” que corresponde a uma região não codificante inserida no DNA bacteriano após contato com o genomas invasores de bacteriófago ou plasmídeo. ²⁸
Os pequenos fragmentos de RNA produzidos pela transcrição do locus CRISPR são capazes de reconhecer DNA estranho específico e atuar como um guia para orientar a Cas nuclease, o que facilitará a clivagem e assim eliminará o DNA invasor caso ele entre novamente em contato com a bactéria. Como resultado, é capaz de editar o genoma, fazendo alterações precisas e direcionadas no genoma das células vivas. ²⁹
Com essa ferramenta, houve um avanço significativo no combate ao HIV devido a eliminação do vírus da sua fase aguda de infecção.
De acordo com Kaminski (2016), a edição de DNA CRISPR/Cas9 guiada por RNA consegue prevenir mais infecções pelo HIV-1 removendo com precisão todo o genoma do HIV-1 das células T CD4+ humanas infectadas. Também foi visto que o CRISPR/Cas9 entregue por lentivírus reduziu significativamente a replicação do HIV-1 em culturas de células T CD4+ primárias infectadas e reduziu radicalmente a carga de vírus em culturas ex vivo de pacientes infectados, demonstrando assim como o sistema CRISPR/Cas9 pode ser um meio vantajoso de alcançar curas funcionais. ⁵
5. RESULTADOS E DISCUSSÃO
O avanço da tecnologia possibilitou o enriquecimento de estudos sobre uma possível cura para o HIV. O desenvolvimento de pesquisas sobre o tema vem crescendo cada vez mais, possibilitando a realização de testes com resultados de diminuição e a erradicação do HIV no organismos de pacientes.
Conhecido como “Paciente de Berlim”, Timothy Ray Brown foi o primeiro dos quatros caso de cura do HIV comprovada. Após diversas tentativas falhas de quimioterapia para melhora do câncer presente no organismo, a equipe médica responsável pelo seu tratamento decidiu que o paciente precisava do transplante para substituir sua medula óssea doente por células normais. O objetivo do tratamento foi baseado na ideia de “destruir” seu sistema imunológico e criar um novo mecanismo de defesa que não só destruiria a leucemia, mas o HIV também. Sendo assim, o uso da medula óssea de um doador que possuísse a mutação da proteína CCR5 resultou na erradicação das reservas latentes do vírus. ³⁰
Por ser um procedimento complexo e com grandes efeitos colaterais, o uso do transplante de medula com mutação na CCR5 não se tornaria uma forma de tratamento viável para os 38 milhões de pessoas que possuem HIV no mundo. Entretanto, pesquisadores estão à procura de maneiras de como inserir a mutação genica nos pacientes soropositivos. ³¹
Após diversos estudos, as tecnologias ZFN (Nucleases de dedo de zinco) e CRISPR/Cas9 começaram a chamar a atenção dos pesquisadores por serem ferramentas versáteis para disrupção de genes. Elas fornecem meios poderosos para interromper fatores necessários para a infecção pelo vírus, bem como para eliminar o genoma do HIV integrado ao hospedeiro, sendo considerado um meio para erradicar a latência viral.
Tais tecnologias são capazes de imitar a mutação CCR5-delta-32 que, ao ser induzida, reduz a expressão das proteínas membranares da proteína. Sem elas, o HIV não encontra seu receptor e, portanto, o vírus não pode entrar e infectar a célula, tornando os pacientes resistentes ao vírus.
A parte pratica da pesquisa, realizada na Universidade da California, se deu inicio na realização de testes em animais, onde os camundongos tratados obtiveram uma diminuição considerável das reservas latentes do HIV, se tornando visível que o uso de células-tronco hematopoiéticas autólogas, modificadas pelas tais técnicas, pode ser uma abordagem clínica para o tratamento do vírus. ³²
6. CONSIDERAÇÕES FINAIS
As evidências apresentadas no artigo presente levam à ideia de que a terapia genica poderá se tornar uma ótima aliada na busca da cura do HIV.
O vírus age no organismo atacando o CD4 e o linfócito T, ocasionando a maior afinidade para o mesmo entrar na célula.
Na sequência o artigo apresenta a terapia genica, testada por meios de testes clínicos, que se baseia no silenciamento da proteína CCR5, através da seleção de 32 pares de bases nitrogenadas, para assim então, eliminar o invasor do organismo ainda na fase aguda e tornar as células hospedeiras do vírus imunes.
Atualmente temos 4 casos relatados da cura contra o HIV no mundo, onde os pacientes reportam aos seus médicos uma melhoria de vida.
Sendo assim, apesar terapia gênica ainda enfrentar dificuldades com a biotecnologia e efeitos ainda não descobertos, estudos vem dando passos promissores em relação ao tema, podendo-se especular um futuro controle e erradicação da epidemia mundial do vírus HIV.
REFERÊNCIAS BIBLIOGRÁFICAS
1. PINTO, A. C. S et al. COMPREENSÃO DA PANDEMIA DA AIDS NOS ÚLTIMOS 25 ANOS. Revisão, 28 abr. 2007. Disponível em: http://www.dst.uff.br/revista19-1-2007/7.pdf. Acesso em: 12 jul. 2022.
2. CANINI, S. R. M. S et al. QUALIDADE DE VIDA DE INDIVÍDUOS COM HIV/AIDS. UMA REVISÃO DE LITERATURA, v. 12, ed. 6, p. 940-945, 2004. Disponível em: https://www.scielo.br/j/rlae/a/gXLzvSVrnD8qPHvrG8dP9gR/?format=pdf&lang=pt. Acesso em: 26 maio 2022.
3. BACELAR JÚNIOR, A. J. et al. A ENGENHARIA GENÉTICA COMO NOVA METODOLOGIA DE COMBATE AO HIV: A TERAPIA GÊNICA, A INTERFERÊNCIA POR RNA E SUAS APLICAÇÕES. Brazilian Journal of Surgery and Clinical Research – BJSCR , ano (Dez 2015 – Fev 2016), v. 13, n. 3, p. 50-55, 5 dez. 2015. Disponível em: https://www.mastereditora.com.br/periodico/20160131_111757.pdf. Acesso em: 21 abr. 2022.
4. BRITO, A.M et al. AIDS e infecção pelo HIV no Brasil: uma epidemia multifacetada. Revista da Sociedade Brasileira de Medicina Tropical, v. 34, ed. 2, p. 207-217, 2000. Disponível em: https://www.scielo.br/j/rsbmt/a/zBSKHBDyfvfz7cLQp7fsSBg/?format=pdf&lang=pt. Acesso em: 28 jul. 2022.
5. MORAIS, P.B et al. Terapia Gênica: nova perspectiva no avanço à cura da infecção pelo HIV. Brazilian Journal of Development, Curitiba, v. 7, n. 6, p. 60983- 60999, 19 jun. 2021. Disponível em: https://brazilianjournals.com/ojs/index.php/BRJD/article/download/31589/pdf. Acesso em: 15 jun. 2022.
6. RODRIGUES, J. S.; FONSECA, L. C.; ALMEIDA, T. A. N. C. Avaliação da imunidade celular do CD4 no combate ao vírus do HIV, Revista Saúde em Foco, v. 10, P. 718-724,
7. BITANTE, J. O.; FILHO, O. R. Terapia genética: Nova perspectiva no avanço à cura da infecção pelo HIV. 2017. Disponível em: <http://cienciasecognicao.org/neuroemdebate/arquivos/3949> Acesso em 8 de Setembro de 2019.
8. DIDIGU, C. A. et al. Imultaneous Zinc-finger Nuclease Editing of the HIV Coreceptors CCR5 and CXCR4 Protects CD4+ T cells from HIV-1 infection. Blood., v.123, n. 1, p. 61-69, 2014. Estatísticas globais sobre HIV 2020. Disponível em< https://unaids.org.br/estatisticas/> Acesso em 20 de Fevereiro de 2021.
9. RODRIGUES , J.S. Avaliação da Imunidade Celular do CD4 no Combate ao Vírus do HIV. Revista Saúde em Foco, v. 10, 2018. Disponível em: https://portal.unisepe.com.br/unifia/wp- content/uploads/sites/10001/2018/08/083_AVALIA%C3%87%C3%83O-DA- IMUNIDADE-CELULAR-DO-CD4-NO-COMBATE.pdf. Acesso em: 11 maio 2022.
10. MARTINS, T. A. et al. Cenário Epidemiológico da Infecção pelo HIV e AIDS no Mundo. Rev Fisioter S Fun , n. 1, p. 4-7, 22 jun. 2014. Disponível em: http://www.periodicos.ufc.br/fisioterapiaesaudefuncional/article/download/20575/31009. Acesso em: 15 abr. 2022.
11. BACELAR JÚNIOR, A. J. et al. A Engenharia Genética Como Nova Metodologia de Combate ao HIV: A Terapia Gênica, A Interferência por RNA e suas Aplicações. Brazilian Journal of Surgery and Clinical Research – BJSCR , ano (Dez 2015 – Fev 2016), v. 13, n. 3, p. 50-55, 5 dez. 2015. Disponível em: https://www.mastereditora.com.br/periodico/20160131_111757.pdf. Acesso em: 21 abr. 2022.
12. FERREIRA, R. C. S. et al. HIV: Mecanismo de Replicação, Alvos Farmacológicos e Inibição por Produtos Derivados de Plantas. QUÍMICA NOVA, ano 2010, v. 33, n. 8, p. (8), 25 out. 2010. Disponível em: https://www.scielo.br/j/qn/a/YcnBsJYMxyvv9DnhCm8mdzB/?lang=pt. Acesso em: 5 maio 2022.
13. COUTINHO, M.F.C et al. Tratamento Antirretroviral: Adesão e a Influência da Depressão em Usuários com HIV/Aids Atendidos na Atenção Primária. ARIGO ORIGINAL , v. 42, ed. 116, p. 148-161, 2018. Disponível em: https://www.scielosp.org/pdf/sdeb/2018.v42n116/148-161/pt. Acesso em: 29 jul. 2022.
14. HIV/AIDS – Diagnóstico e Tratamento. SECRETARIA DE SAÚDE DO DISTRITO FEDERAL, 2022. Disponível em: https://www.saude.df.gov.br/hiv-aids-diagnostico-e- tratamento. Acesso em: 15 jun. 2022.
15. NETO, L.F.S.P et al. Protocolo Brasileiro para Infecções Sexualmente Transmissíveis 2020: infecção pelo HIV em adolescentes e adultos. Epidemiologia e Serviços de Saúde , 31 ago. 2020. Disponível em: http://scielo.iec.gov.br/scielo.php?script=sci_arttext&pid=S1679- 49742021000500013. Acesso em: 29 jul. 2022.
16. DIAGNÓSTICO. Departamento de Doenças de Condições Crônicas e Infecções Sexualmente Transmissíveis, 25 abr. 2022. Disponível em: https://www.gov.br/aids/pt-br/assuntos/hiv-aids/diagnostico. Acesso em: 23 abr. 2022.
17. BONOLO, P.F. Adesão à Terapia Anti-retroviral (HIV/aids): Fatores Associados e Medidas da Adesão. Epidemiologia e Serviços de Saúde, 13 maio 2007. Disponível em: http://scielo.iec.gov.br/scielo.php?script=sci_arttext&pid=S1679-49742007000400005. Acesso em: 20 maio 2022.
18. KALLÁS , E.G; DONINI, C.S. Perspectiva de Cura da Infeção pelo HIV. EDUCAÇÃO MÉDICA CONTINUADA, v. 2, ed. 5, 2016. Disponível em: https://www.bjid.org.br/index.php?p=revista&tipo=pdf- simple&pii=X2177511716600184. Acesso em: 15 jul. 2022.
19. Mutação no Gene CCR5 e Infecção por HIV. GENOPRIMER , 2022. Disponível em: https://www.genoprimer.com.br/mutacao-no-gene-ccr5-e-infeccao-por-hiv/. Acesso em: 5 jul. 2022.
20. OLIVEIRA, E.H.D et al. O Gene CCR5 e a Mutação que Confere Proteção Contra o Vírus HIV. SOCIEDADE BRASILEIRA DE GENÉTICA 2, 2021. Disponível em: https://www.geneticanaescola.com/revista/article/download/377/344. Acesso em: 10 jun. 2022.
21. RONSARD, L. Genetic Polymorphisms in the Open Reading Frame of the CCR5 gene From HIV-1 Seronegative and Seropositive Individuals From National Capital Regions of India. SCIENTIC REPORTS, 20 maio 2019. Disponível em: https://www.nature.com/articles/s41598-019-44136-z.pdf. Acesso em: 13 jul. 2022.
22. SILVA, C. D.; MATTE, U. S.; GIUGLIANI , R. Terapia gênica: uma nova estratégia para o tratamento de doenças, Revista HCPA, v. 3, p. 379-386, 2001
23. BARBOSA, A.S; LIN, C.J. Silenciamento de Genes Com RNA Interferência: Um Novo Instrumento Para Investigação da Fisiologia e Fisiopatologia do Córtex Adrenal. ATUALIZAÇÃO , v. 48, ed. 5, 2004. Disponível em: https://www.scielo.br/j/abem/a/MPnj785ZdXcCpFMVSVYKX9H/?format=pdf&lang=pt. Acesso em: 24 jun. 2022.
24. NYKANEN, A et al. ATP requirements and small interfering RNA structure in the RNA interference pathway. Cell 2001;107(3):309-21. – https://pubmed.ncbi.nlm.nih.gov/11701122/
25. Matalon S, et al. Istone Deacetylase Inhibitors for Purging HIV-1 from the Latent Reservoir. Mol Med 2011; 1: 466-72.
26. TERAPIA GENÉTICA PODE COMBATER O VÍRUS HIV. SOCIEDADE BRASILEIRA DE MICROBIOLOGIA , 1 fev. 2018. Disponível em: https://sbmicrobiologia.org.br/terapia-genetica-pode-combater-o-virus-hiv/. Acesso em: 19 maio 2022.
27. Carroll D. Genome Engineering with Zinc-finger Nucleases. Genetics. 2011 Aug;188(4):773-82. doi: 10.1534/genetics.111.131433. PMID: 21828278; PMCID: PMC3176093
28. SAAYMAN, S. et al. A aplicação terapêutica das tecnologias CRISPR/Cas9 para HIV. NCBI, 12 abr. 2015. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4581584/. Acesso em: 1 ago. 2022.
29. SISTEMA CRISPR-Cas: Como Funciona o Mecanismo de Imunidade dos Procariotos que se Tornou Tendência no Ramo da Edição Gênica. INSTITUTO DE MICROBIOLOGIA PAULO DE GÓES UFRJ, 2022. Disponível em: https://www.microbiologia.ufrj.br/portal/index.php/pt/graduacao/informes-da- graduacao/947-sistema-crispr-cas-como-funciona-o-mecanismo-de-imunidade-dos- procariotos-que-se-tornou-tendencia-no-ramo-da-edicao-genica. Acesso em: 10 jun. 2022.
30. SOUZA, T.L et al. PERSPECTIVA – SÉRIE ” DESMISTIFICANDO A CIÊNCIA”: TRATAMENTO PARA CURA DO HIV-1: ” O PACIENTE DE BERLIM”. REVISTA CIENTIFÍCA FMC, v. 7, ed. 1, 2012. Disponível em: https://www.fmc.br/ojs/index.php/RCFMC/article/download/95/75. Acesso em: 18 maio 2022.
31. O “PACIENTE de Berlim” a História do Primeiro Homem a Vencer a Aids. SERVIÇO DE ASSISTÊNCIA ESPECIALIZADA FAMILIAR MATERNO INFANTIL, 23 abr. 2019. Disponível em: https://www.ufpb.br/saehu/contents/noticias/a-historia-do- primeiro-homem-a-vencer-a-aids. Acesso em: 22 jul. 2022.
32. MUTAÇÃO FORÇADA PROTEGE CONTRA HIV. FABEMA, 6 mar. 2014. Disponível em: https://www.fapema.br/mutacao-forcada-protege-contra-hiv/. Acesso em: 22 jul. 2022.
1Discente da Universidade Anhembi Morumbi, São Paulo / SP, Brasil
2Docente da Universidade Anhembi Morumbi, São Paulo / SP, Brasil
