REGISTRO DOI: 10.69849/revistaft/ar10202412161746
Alessandro Ramos Júnior¹;
Paulo Estevão Chaves Silva².
Resumo – A Ressonância Magnética (RM) evoluiu ao longo de 30 anos, passando de uma técnica com grande potencial para se tornar a principal investigação diagnóstica em muitos problemas clínicos. Inicialmente, sua aplicação era restrita ao neuroeixo, mas agora abrange todas as regiões do corpo. Esse avanço foi possível graças ao aumento do conhecimento, que proporcionou uma melhor compreensão de como a RM pode ser melhor utilizada, seja de forma isolada ou em conjunto com outras técnicas, a fim de maximizar a certeza diagnóstica. Este artigo tem como objetivo descrever um breve histórico da ressonância magnética, abordando os princípios físicos da RM, os equipamentos utilizados, as sequências básicas, os artefatos, a segurança em RM, os agentes de contraste usados na técnica, as vantagens e desvantagens da ressonância magnética, sua aplicação na região maxilofacial e os avanços recentes na imagem por ressonância magnética.
Palavras-chave: Análogos quânticos, Ciclos termodinâmicos, Ensino de Física, máquinas térmicas.
I. INTRODUÇÃO
A ressonância magnética (RM) é um método não invasivo para mapear a estrutura interna e certos aspectos funcionais do corpo. Ela utiliza radiação eletromagnética não ionizante e não apresenta riscos associados à exposição. A técnica emprega radiação de radiofrequência (RF) na presença de campos magnéticos cuidadosamente controlados para produzir imagens seccionais de alta qualidade do corpo em qualquer plano. A imagem por RM é construída colocando o paciente dentro de um grande ímã, que induz um campo magnético externo relativamente forte. Isso faz com que os núcleos de muitos átomos no corpo, incluindo os de hidrogênio, alinhem-se com o campo magnético. Com a posterior aplicação de um sinal de RF, a energia é liberada do corpo, detectada e utilizada para construir a imagem por RM através de um computador. A Tabela 1 mostra um breve histórico do desenvolvimento da RM.
A. Princípios Básicos da Física da RM
Estrutura Atômica: O núcleo de um átomo consiste em duas partículas:
Prótons: Possuem carga positiva. Nêutrons: Têm carga neutra. Elétrons: Orbitando o núcleo, estão os elétrons, que carregam carga negativa. Os elementos são comumente classificados de acordo com duas propriedades:
Número atômico: Representa o número de prótons no núcleo e é o principal índice usado para diferenciar os átomos.
Massa atômica: É o número total de prótons e nêutrons. Átomos com o mesmo número atômico, mas diferentes pesos atômicos, são chamados de isótopos. Uma terceira propriedade dos núcleos atômicos é chamada de spin nuclear. Todas essas partículas estão em movimento; tanto os nêutrons quanto os prótons giram em torno de seus eixos.
Spin: O spin é uma propriedade fundamental da natureza, assim como a carga elétrica ou a massa. O spin vem em múltiplos de 1/2 e pode ser positivo ou negativo. Prótons, elétrons e nêutrons possuem spin. Elétrons, prótons e nêutrons individuais não emparelhados possuem cada um um spin de 1/2.
Propriedades do Spin: Quando uma partícula com spin é colocada em um campo magnético de força B, ela pode absorver um fóton de uma determinada frequência. Essa frequência depende da razão giromagnética da partícula. Os núcleos adequados para RM são aqueles que possuem um próton ou nêutron não emparelhado, que apresentam uma carga de spin líquida ou momento angular. Isso ocorre porque, como o spin está associado a uma carga elétrica, um campo magnético é gerado em núcleos com nucleons não emparelhados, fazendo com que esses núcleos atuem como ímãs com polos Norte e Sul (dipolos magnéticos).
Importância dos Núcleos de Hidrogênio na RM: O hidrogênio é o átomo mais abundante no corpo humano, na forma de água (H2O), e é o mais sensível à RM. Os núcleos de hidrogênio, que consistem em um único próton não emparelhado, agem como dipolos magnéticos. Esses dipolos magnéticos, na ausência de uma influência externa, estão orientados de forma aleatória e, portanto, têm magnetização líquida zero. Quando um campo magnético externo é aplicado, todos os eixos nucleares de hidrogênio se alinham na direção do campo magnético, produzindo uma quantidade de magnetização líquida. Esse alinhamento pode ocorrer de duas maneiras: na direção do campo externo, chamado de “spin para cima”, ou na direção oposta, chamado de “spin para baixo”. Essas orientações correspondem a estados de energia mais baixa ou mais alta do dipolo, respectivamente. Os núcleos podem ser feitos para transitar de um estado de energia para outro, absorvendo ou liberando uma certa quantidade de energia. Essa energia pode ser fornecida ou recuperada na forma de energia eletromagnética na faixa de RF do espectro eletromagnético, e essa transição de um nível de energia para outro é chamada de ressonância.
Quando um campo magnético externo é aplicado, os polos Norte e Sul dos núcleos de hidrogênio não se alinham exatamente na direção do campo magnético. Os eixos dos prótons em rotação oscilam ou vacilam com uma leve inclinação em relação à posição paralela ao fluxo do ímã externo. Essa inclinação ou oscilação é chamada de precessão. A taxa ou frequência de precessão é chamada de frequência de ressonância ou frequência de Larmor, que é proporcional à intensidade do campo magnético aplicado. A frequência de Larmor do hidrogênio é de 42,58 MHz em um campo magnético de 1 Tesla, onde um Tesla é 10.000 vezes o campo magnético da Terra. A intensidade do campo magnético usada para imagens por RM varia de 0,1 a 4,0 T.
II. FUNDAMENTAÇÃO TEÓRICA
A equação de Larmor é expressa como:
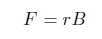
onde F é a frequência de ressonância, r é a razão giromagnética e B é o campo aplicado.
Resumo: Quando os núcleos são submetidos ao fluxo de um campo magnético externo, resultam dois estados de energia: Spin-up: alinhado com o campo magnético – Spin-down: na direção oposta ao campo magnético.
O efeito combinado desses dois estados de energia resulta em um momento magnético líquido fraco, ou vetor de magnetização (MV), paralelo ao campo magnético aplicado. Quando a energia na forma de uma onda eletromagnética de uma bobina de RF é direcionada para o tecido com prótons (núcleos de hidrogênio) que estão alinhados no eixo Z por um campo magnético externo estático (o ímã de imagem), os prótons no tecido que têm uma frequência de Larmor correspondente à da onda eletromagnética absorvem energia e se deslocam ou rotacionam afastando-se da direção induzida pelo ímã de imagem.
Quanto mais longo for o pulso de RF aplicado, maior será o ângulo de rotação. Se o pulso for de intensidade (duração) suficiente, ele rotacionará o vetor de magnetização líquida do tecido para um plano transversal (plano XY), que é perpendicular ao alinhamento longitudinal (eixo Z), fazendo com que todos os prótons precessem em fase. Isso é referido como um pulso de RF de 90° ou um ângulo de rotação de 90°. Nesse momento preciso, um sinal máximo de RF é induzido em uma bobina receptora. Este sinal depende da presença ou ausência de hidrogênio e também do grau em que o hidrogênio está ligado dentro de uma molécula. Por exemplo, no osso, devido à presença de átomos de hidrogênio fortemente ligados, eles não se alinham com o campo magnético externo e não produzem um sinal utilizável.
Nos tecidos moles e líquidos, devido à presença de átomos de hidrogênio fracamente ligados ou móveis, ocorre a inclinação e alinhamento para produzir um sinal detectável. A medida da concentração de núcleos de hidrogênio fracamente ligados disponíveis para criar o sinal é chamada de densidade de prótons ou densidade de spin do tecido em questão.
Quando as ondas de rádio (pulso de RF) são desligadas, dois eventos ocorrem simultaneamente: 1. A radiação de energia e o retorno dos núcleos ao seu estado de spin original em uma energia mais baixa. Esse processo é chamado de relaxamento, e a perda de energia é detectada como um sinal, que é chamado de decaimento da indução livre (FID). 2. Os núcleos em alinhamento transversal começam a se realinhar com o campo magnético principal, e a magnetização líquida retorna à orientação longitudinal original. Esse relaxamento é realizado por uma transferência de energia dos núcleos de hidrogênio individuais (spin) para as moléculas circundantes (lattice). A constante de tempo que descreve a taxa em que a magnetização líquida retorna ao equilíbrio por essa transferência de energia é chamada de tempo de relaxamento T1 ou tempo de relaxamento spin-lattice. (T1 – Curto – 500ms – recuperação do sinal em 20ms).
Uma imagem ponderada em T1 é produzida por um tempo de repetição curto entre os pulsos de RF e um tempo de recuperação de sinal curto. Como T1 é uma constante de tempo de crescimento exponencial, um tecido com T1 curto produz um sinal de RM intenso e é exibido como branco brilhante em uma imagem ponderada em T1. Um tecido com T1 longo produz um sinal de baixa intensidade e aparece escuro na imagem de RM. Além disso, os momentos magnéticos dos núcleos de hidrogênio adjacentes começam a interferir entre si, causando a defasagem dos núcleos e resultando na perda de magnetização transversal. A constante de tempo que descreve a taxa de perda de magnetização transversal é chamada de tempo de relaxamento T2 ou tempo de relaxamento transversal (spin). A magnetização transversal decai rapidamente (exponencialmente) para zero, assim como a amplitude e duração do sinal de rádio detectado.
Uma imagem ponderada em T2 é adquirida usando um tempo de repetição longo entre os pulsos de RF e um tempo de recuperação de sinal longo. Um tecido com T2 longo produz um sinal de alta intensidade e é brilhante na imagem, enquanto um com T2 curto produz um sinal de baixa intensidade e é escuro na imagem.
O contraste da imagem entre os vários tecidos do corpo é manipulado na RM variando a taxa na qual o pulso de RF é transmitido. Um tempo de repetição curto (TR) de 500ms entre os pulsos e um tempo de eco curto (TE) de 20ms produzem uma imagem ponderada em T1. Um TR longo (2000ms) e um TE longo (80ms) produzem imagens ponderadas em T2. Para cada tarefa diagnóstica, o operador deve decidir qual sequência de imagem trará o melhor contraste. As imagens ponderadas em T1 são chamadas de imagens de gordura porque a gordura tem o tempo de relaxamento T1 mais curto e o sinal mais forte em comparação com outros tecidos, aparecendo assim brilhante na imagem. Esse tipo de imagem permite um detalhe anatômico elevado devido ao bom contraste de imagem, sendo útil para a visualização de pequenas regiões anatômicas onde é necessária alta resolução espacial.
As imagens ponderadas em T2 são chamadas de imagens de água porque a água tem o tempo de relaxamento T2 mais longo, aparecendo brilhante na imagem. Em geral, o tempo de T2 dos tecidos anormais é mais longo do que o dos tecidos normais. As imagens ponderadas em T2 são mais comumente usadas quando o praticante está procurando por mudanças inflamatórias e tumores.
As imagens ponderadas em T1 são mais comumente usadas para demonstrar a anatomia. Na prática, as imagens geralmente precisam ser adquiridas com ponderações em T1 e T2 para separar os diferentes tecidos pela resolução de contraste.
A localização da RM para uma parte específica do corpo (selecionando um corte) e a capacidade de criar uma imagem tridimensional dependem do fato de que a frequência de Larmor de um núcleo é governada em parte pela intensidade do campo magnético externo.
O gradiente magnético é produzido por três bobinas eletromagnéticas dentro do túnel do ímã de imagem. As bobinas envolvem o paciente e produzem um campo magnético que se opõe e redireciona o fluxo magnético em três direções ortogonais ou em ângulo reto, para delinear volumes individuais de tecidos (voxels), que são submetidos a campos magnéticos de intensidade única. Particionando as linhas do campo magnético local, todos os prótons de hidrogênio em um voxel específico são alinhados na mesma frequência de ressonância. Isso é chamado de excitação seletiva. Quando um pulso de RF com uma faixa de frequências é aplicado, um voxel de tecido sintonizado para uma das frequências é excitado e, ao terminar a radiação de RF, o voxel excitado radia essa frequência distinta, identificando-o e localizando-o. A largura de banda ou espectro de frequências do pulso de RF e a magnitude do gradiente de seleção de corte determinam a espessura do corte. A espessura do corte pode ser reduzida aumentando a intensidade do gradiente ou diminuindo a largura de banda de RF (faixa de frequências).
A. Localização do Sinal
As técnicas para construir imagens: processo de codificação e dois conceitos que precisam ser separados. A relação física que possibilita a construção de uma imagem é a relação proporcional entre a frequência de ressonância e a intensidade do campo magnético (equação de Larmor).
Para entender a espacialidade da RM: 1. Frequência de Ressonância: Conforme a equação de Larmor, os spins precessam a uma frequência de ressonância alta quando em um campo magnético alto. 2. Frequência Espacial: Os componentes de alta frequência espacial de uma imagem correspondem aos detalhes finos dessa imagem.
A imagem é realizada utilizando as propriedades da relação de Larmor, mas, além disso, os dados são codificados no domínio da frequência espacial. Este último refere-se ao sinal amostrado estando no maravilhoso mundo do K-Space.
Os passos envolvidos na produção de um estudo de RM podem ser resumidos da seguinte forma: 1. Um campo magnético externo poderoso e uniforme é usado para alinhar as moléculas de água, que normalmente estão orientadas aleatoriamente, no tecido sendo examinado. 2. Esse alinhamento (ou magnetização) é perturbado ou interrompido pela introdução de energia de RF externa em uma frequência apropriada para induzir ressonância. A localização espacial é obtida através da aplicação de um campo magnético espacialmente dependente (referido como um gradiente) ao mesmo tempo que a energia de RF é introduzida no tecido. O campo de gradiente modula seletivamente a frequência de ressonância do paciente de acordo com a equação de Larmor. 3. Os núcleos retornam ao seu alinhamento de repouso através de vários processos de relaxamento e, ao fazê-lo, emitem energia de RF proporcional à magnitude de seu alinhamento ou magnetização inicial. 4. Após um período apropriado após a deposição inicial de RF, os sinais emitidos são medidos ou lidos. 5. Um processo matemático chamado transformação de Fourier é usado para converter as informações de frequência contidas no sinal de cada localização no plano da imagem para níveis de intensidade correspondentes, que são então exibidos como tons de cinza em uma matriz de, por exemplo, 256 x 256 pixels. 6. Os prótons nos vários tecidos no corte da imagem realinham-se com o campo magnético a diferentes velocidades, de modo que, a qualquer momento, há uma diferença na intensidade do sinal entre os vários tecidos. Essa diferença na intensidade do sinal de uma região para outra constitui a base do contraste tecidual e forma o substrato para a interpretação da imagem.
B. Gerador de campo
Será mais fácil observar um campo magnético se ele for representado por um conjunto de linhas paralelas. Em cada linha, a seta indica a direção do campo. Na superfície terrestre, a direção do campo magnético é diferente em diversos pontos, sendo definida com base nos seus polos, norte e sul. Apesar disso, a notação norte-sul não é utilizada em campos magnéticos empregados para a criação de imagens.
A maioria dos eletroímãs utilizados na produção de imagens gera um campo magnético que atravessa o orifício do ímã e está alinhado com o eixo central do paciente. Conforme previsto, o campo magnético emerge desse orifício, se difunde e envolve o ímã, formando uma área de franja externa. Essa área externa pode interferir no funcionamento de outros aparelhos e, por isso, geralmente é protegida por blindagem.
Cada ponto em um campo magnético possui uma intensidade específica, que é medida em unidades de tesla (T) ou gauss (G). A relação entre essas unidades é direta: 1,0 T corresponde a 10.000 G ou 10 kG. O campo magnético terrestre, por sua vez, é relativamente fraco, com uma intensidade inferior a 1 G. Para a produção de imagens por ressonância magnética, campos magnéticos com intensidades de 1,5 T ou mais são utilizados.
A ressonância magnética requer um campo magnético extremamente uniforme. A uniformidade é impactada pelo design do ímã, alterações ambientais e condições de uso. Para a formação de imagens, essa uniformidade deve ser mantida dentro de limites específicos, geralmente determinados em partes por milhão (ppm).
Há diferentes tipos de ímãs que podem ser empregados para gerar o campo magnético, cada qual com vantagens e desvantagens. A maioria dos sistemas de ressonância magnética utiliza ímãs supercondutores. Esses ímãs são capazes de gerar campos magnéticos mais intensos e estáveis em comparação aos ímãs resistivos ou permanentes.
Um ímã supercondutor é um eletroímã que opera em estado de superconductividade, ou seja, um estado em que o fio condutor não apresenta resistência ao fluxo de corrente elétrica. Isso permite a condução de correntes de alta intensidade sem superaquecimento. Esses fios são compostos, geralmente, de nióbio-titânio (Nb-Ti) e são revestidos por cobre, que atua como suporte mecânico e elétrico.
Para alcançar a superconductividade, o fio precisa ser resfriado a temperaturas extremamente baixas, frequentemente utilizando hélio líquido. No entanto, se a temperatura do fio exceder o limite crítico, ocorre a tempera, um fenômeno indesejado que resulta na perda do campo magnético devido ao aumento do calor e à diminuição da corrente elétrica.
Os ímãs supercondutores são frequentemente projetados na forma de solenoides cilíndricos. Um desafio comum desses sistemas é a sensação de claustrofobia relatada por alguns pacientes, devido ao espaço interno limitado. Para mitigar esse problema, avanços no design buscam criar ambientes mais confortáveis para os pacientes.
Ímãs resistivos, por outro lado, utilizam condutores comuns, como o cobre. Esses ímãs geram calor durante o funcionamento, o que limita sua capacidade de produzir campos magnéticos de alta intensidade. Já os ímãs permanentes não necessitam de eletricidade ou refrigeração para operar, mas também estão limitados a intensidades de campo mais baixas.
Apesar das limitações, os ímãs resistivos e permanentes apresentam vantagens, como menor interferência externa e espaços mais amplos para os pacientes, sendo alternativas viáveis para determinadas aplicações.
C. Gradiente
O sistema de ressonância magnética, quando em estado de inatividade, mantém um campo magnético uniforme ou homogêneo sobre a área do corpo do indivíduo, mas não gera imagens nessa condição. Durante o processo de formação de imagens, é essencial que o campo magnético seja mantido estável e livre de distorções.
Um gradiente no campo magnético representa a variação na intensidade do campo de um ponto para outro no organismo do paciente. Essas variações são geradas por um conjunto de bobinas de gradiente, que estão integradas ao sistema magnético. No processo de formação de imagens, os gradientes são ativados e desativados frequentemente, gerando o som característico ouvido durante a operação do equipamento.
Quando o ímã do sistema está em estado de repouso, ele gera um campo magnético uniforme. No entanto, ao ativar uma bobina de gradiente com uma corrente elétrica, ocorre uma variação na intensidade do campo magnético, criando um gradiente. Os sistemas de ressonância magnética possuem três conjuntos distintos de bobinas de gradiente, projetadas para gerar variações em três direções ortogonais, geralmente correspondentes aos eixos x, y e z. Além disso, as bobinas podem ser combinadas para criar gradientes em direções específicas conforme necessário.
Os gradientes desempenham várias funções essenciais durante a aquisição de imagens. Eles são responsáveis por criar propriedades espaciais ao definir as fatias ou voxels que compõem a imagem. Métodos de imagem por eco de gradiente utilizam essas variações para gerar os sinais necessários à formação da imagem. Além disso, os gradientes são aplicados em técnicas avançadas, como a angiografia de contraste de fase, utilizada em imagens vasculares, e na ressonância funcional.
Os gradientes também ajudam a minimizar artefatos nas imagens. A intensidade de um gradiente é medida em militesla por metro (mT/m), e sistemas modernos podem alcançar forças de gradiente superiores a 20 mT/m, consideradas adequadas para aplicações que demandam alta resolução.
Outro aspecto crítico dos gradientes é sua capacidade de alteração rápida. O tempo de subida refere-se ao intervalo necessário para que o gradiente atinja sua potência máxima, e a taxa de variação indica a rapidez com que a intensidade do gradiente muda no espaço. Por exemplo, um sistema pode apresentar um tempo de subida de 0,20 milissegundos (ms) e uma taxa de variação de 100 mT/m/ms, demonstrando alta eficiência e precisão.
D. Radiofrequência
A tecnologia de radiofrequência (RF) permite a transmissão de dados por meio de ondas eletromagnéticas, estabelecendo uma conexão com o corpo do indivíduo e possibilitando a criação de imagens. Todas as modalidades de imagem médica utilizam algum tipo de tecnologia baseada em radiação (como raios X e raios gama) ou energia (como o calor, no caso do ultrassom), para gerar e transferir a imagem de uma parte do sistema corporal do paciente.
No caso da ressonância magnética, ondas eletromagnéticas são utilizadas para captar e transmitir imagens do corpo. A radiofrequência (RF) é um tipo de radiação não ionizante. As ondas de radiofrequência transmitidas ao corpo são chamadas de pulsos de RF. Quando o tecido do paciente absorve esses pulsos, a energia é convertida em calor e em sinais que podem ser captados e utilizados para criar a imagem.
Uma quantidade mínima de água no corpo é essencial para o processo, pois a energia liberada pelo organismo é captada como sinais que permitem a reconstrução da imagem por meio de computadores. A imagem final não é uma reprodução direta, mas uma representação baseada nas diferenças de potência do sinal emitido por diversos tipos de tecidos.
As bobinas de radiofrequência, localizadas próximas ao corpo do paciente, atuam como antenas. Elas enviam sinais ao tecido e captam as informações emitidas em resposta. Existem diferentes modelos de bobinas projetados para áreas anatômicas específicas. As bobinas podem ser classificadas em três categorias principais: bobinas de corpo, de cabeça e de superfície. Em alguns casos, a mesma bobina é usada tanto para transmissão quanto para recepção de sinais. Em outros, são utilizadas bobinas separadas para cada função.
As bobinas de superfície, por exemplo, captam sinais de áreas anatômicas menores, permitindo uma qualidade de imagem superior em comparação com as bobinas de corpo e de cabeça. Elas podem consistir em uma única bobina ou uma combinação de várias, cada qual com seu próprio circuito receptor. Essa configuração, conhecida como matriz em fase, oferece imagens de alta qualidade e maior abrangência anatômica.
O transmissor de RF é responsável por gerar a energia aplicada nas bobinas e transmitida ao organismo. Ele é composto por moduladores de rádio, amplificadores de áudio e outros elementos. A potência necessária depende da intensidade do campo magnético do sistema. Por exemplo, um sistema de 1,5 T pode requerer cerca de nove vezes mais potência de RF que um sistema de 0,5 T.
Para garantir a segurança, um mecanismo de supervisão de potência é integrado ao transmissor, prevenindo a aplicação excessiva de energia ao paciente. Após a emissão de uma sequência de pulsos de rádio, o tecido do corpo responde ressoando e emitindo sinais de radiofrequência, que são captados pelas bobinas e enviados ao receptor. Esses sinais são então transformados em formato digital e armazenados temporariamente no computador, onde são processados para gerar a imagem final.
III. APLICAÇÕES DA RESSONÂNCIA MAGNÉTICA
IV. VANTAGENS DA RESSONÂNCIA MAGNÉTICA (RM)
Ausência de Radiação Ionizante: Os pulsos de radiofrequência (RF) utilizados na RM não causam ionização e, portanto, não possuem os efeitos nocivos associados à radiação ionizante. Isso torna a RM segura para uso em mulheres grávidas e crianças.
Não Invasiva: A RM é um método não invasivo, o que significa que não há necessidade de cirurgias ou inserção de instrumentos no corpo para obter as imagens.
Alta Resolução de Contraste: A principal vantagem da RM é sua capacidade de diferenciar tecidos adjacentes. A RM pode manipular o contraste entre diferentes tecidos ao alterar o padrão dos pulsos de RF, permitindo uma melhor distinção entre eles.
Imagens Multiplanares: Com a RM, é possível obter imagens diretas em planos sagital, coronal e oblíquo, algo que não é possível com a radiografia e a tomografia computadorizada (TC).
Diferenciação de Fases Patológicas: A RM consegue diferenciar entre fases agudas e crônicas de doenças, além de detectar mudanças histopatológicas nos tecidos.
Ausência de Artefatos Significativos: Em comparação com outros métodos de imagem, a RM não sofre de artefatos significativos causados por obturações dentárias.
Manipulação de Imagens: É possível manipular as imagens obtidas por RM para melhorar a visualização de estruturas específicas.
Espalhamento Intramedular: A RM é útil na determinação da extensão do espalhamento intramedular de patologias.
V. DESVANTAGENS DA RESSONÂNCIA MAGNÉTICA (RM)
Claustrofobia: Devido ao fato de o paciente precisar ficar dentro de um grande ímã por até uma hora, alguns pacientes podem desenvolver uma sensação mórbida de medo de espaços fechados (claustrofobia).
Custo Elevado: O equipamento de RM é caro tanto para aquisição quanto para manutenção e operação. Além disso, o desenvolvimento de hardware e software continua em progresso, o que pode aumentar os custos.
Risco para Pacientes com Implantes: O forte campo magnético utilizado na RM pode ser perigoso para pacientes com implantes elétricos, magnéticos ou mecânicos, como marcapassos cardíacos, desfibriladores implantáveis e algumas válvulas cardíacas artificiais.
Distúrbios na Imagem Causados por Metais: A presença de metal no corpo, como clipes cirúrgicos ou stents, pode distorcer as imagens de RM, dificultando a interpretação dos resultados.
Tempo de Escaneamento Longo: A RM exige um tempo de escaneamento relativamente longo e requer a cooperação do paciente para obter imagens de boa qualidade.
Problemas com Equipamentos: Os ímãs muito poderosos utilizados na RM podem causar problemas na instalação dos equipamentos, embora o uso de blindagem esteja se tornando mais sofisticado.
Ruído: Os scanners de RM são ruidosos, o que pode causar desconforto ao paciente.
Reações Alérgicas ao Contraste: Embora raro, existe a possibilidade de o paciente desenvolver uma reação alérgica ao agente de contraste utilizado na RM, ou uma infecção na pele no local da injeção.
Limitações na Identificação de Tumores: A RM nem sempre consegue distinguir entre tumores malignos e doenças benignas, o que pode resultar em falsos positivos.
Disponibilidade Limitada: A RM não está amplamente disponível, embora o desenvolvimento de sistemas menores e abertos adequados para hospitais distritais esteja em andamento.
Dificuldade na Diferenciação de Estruturas: Ossos, dentes, ar e objetos metálicos aparecem como áreas escuras nas imagens de RM, o que pode dificultar a diferenciação entre essas estruturas.
VI. CONCLUSÃO
A ressonância magnética é um sistema de imagem complexo, mas eficaz, com várias indicações clínicas diretamente relacionadas ao diagnóstico e tratamento de anomalias orais e maxilofaciais. Embora seu uso rotineiro na odontologia seja limitado, a aplicação adequada da RM pode melhorar significativamente a qualidade do atendimento ao paciente em casos selecionados. Avanços contínuos na imagem tridimensional (3D) e na varredura dinâmica prometem ampliar ainda mais o uso dessa técnica de imagem no futuro.
VII. REFERÊNCIAS
ASSHEUER, J.; SAGER, M. MRI and CT Atlas of the Dog. Oxford: Blackwell Science, 1997. 482p.
TUCKER, R. L.; GAVIN, P. R. Brain imaging. Veterinary Clinics of North America: Small Animal Practice, Philadelphia, v.26, n.4, p.735-758, 1996.
BLOCH, F. et al. The nuclear induction experiment. Physical Review, New York, v.70, n.7-8, p.474-485, 1946. Disponível em: http://prola.aps.org/abstract/PR/v70/i7-8/p4741. Doi: 10.1103/PhysRev.70.474.
BLOEMBERGEN, N. et al. Relaxation effects in nuclear magnetic resonance absorption. Physical Review, New York, v.73, n.7, p.679-712, 1948. Disponível em: http://prola.aps.org/abstract/PR/v73/i7/p6791. Doi: 10.1103/PhysRev.73.679.
CALLAGHAN, P. Principles of Nuclear Magnetic Resonance Microscopy. Oxford: Oxford University, 1994. 516p.
HEBEL, L. C.; SLICHTER, C. P. Nuclear spin relaxation in normal and superconducting aluminum. Physical Review, New York, v.113, n.6, p.1504-1519, 1959. Disponível em: http://prola.aps.org/abstract/PR/v113/i6/p15041. Doi: 10.1103/PhysRev.113.1504.
LAUTERBUR, P. C. Image formation by induced local interactions: examples employing nuclear magnetic resonance. Nature, v.242, n.16, p.190-191, 1973. Disponível em: http://www.nature.com/nature/journal/v242/n5394/abs/242190a0.html. Doi: 10.1038/242190a0.
LUFKIN, R. L. Manual de Ressonância Magnética. Rio de Janeiro: Guanabara Koogan, 1999. 338p.
MAGALHÃES, A. C. A. Ressonância Magnética do Sistema Nervoso Central. São Paulo: Atheneu, 1999. p.1-26.
MANSFIELD, P.; GRANNELL, P. K. NMR “diffraction” in solids? Journal of Physics Chemistry: Solid State Physics, Boston, v.6, n.22, p.L422-L426, 1973.
MENDONÇA, R. et al. Fundamentos da Ressonância Magnética. 1996. [p.29]. Apostila.
PURCELL, E. M. et al. Resonance absorption by nuclear magnetic moments in a solid. Physical Review, New York, v.69, n.1-2, p.37-38, 1946.
PYKETT, I. L. et al. Principles of nuclear magnetic resonance imaging. Radiology, Illinois, v.143, p.157-168, 1982.
SLICHTER, C. P. Principles of Magnetic Resonance: Springer Series in Solid States Sciences. Berlin: Springer-Verlag Berlin, 1989. v.1, 666p.
SMITH, H.; RANALLO, F. N. A Non-Mathematical Approach to Basic MRI. Wisconsin: Medical Physics, 1989. 203p.
THOMSON, C. E. et al. Magnetic resonance imaging – a general overview of principles and examples in veterinary neurodiagnosis. Veterinary Radiology & Ultrasound, Raleigh, v.34, n.1, p.2-17, 1993.
AVILA, L. F. Física em Ressonância Magnética. Parte A. São Paulo: Videoteca da Sociedade Brasileira de Radiologia, 2001. [Fita de Vídeo].
VILLAFANA, T. Fundamental physics of magnetic resonance imaging. Radiologic Clinics of North America, Philadelphia, v.26, n.4, p.701-715, 1988.
REVETT, K. An introduction to magnetic resonance imaging: from image acquisition to clinical diagnosis. Innovations in Intelligent Image Analysis, 2011, p.127-161.
FULLERTON, G. D. Basic concepts for nuclear magnetic resonance imaging. Magnetic Resonance Imaging, 1982, v.1, n.1, p.39-53.
GEVA, T. Magnetic resonance imaging: historical perspective. Journal of Cardiovascular Magnetic Resonance, 2006, v.8, n.4, p.573-580.
PARTAIN, C. L. The 2003 Nobel prize for MRI: significance and impact. Journal of Magnetic Resonance Imaging, 2004, v.19, n.5, p.515-526.
ANDREWS, C.; SIMMONS, A.; WILLIAMS, S. Magnetic resonance imaging and spectroscopy. Physics Education, 1996, v.31, p.80.
PEKAR, J. J. A brief introduction to functional MRI. Engineering in Medicine and Biology Magazine, IEEE, 2006, v.25, n.2, p.24-26.
STEHLING, M. K.; TURNER, R.; MANSFIELD, P. Echo-planar imaging: magnetic resonance imaging in a fraction of a second. Science, 1991, v.254, p.5028-5029.
EDZES, H. T.; VAN DUSSCHOTEN, D.; VAN AS, H. Quantitative T2 imaging of plant tissues by means of multi-echo MRI microscopy. Magnetic Resonance Imaging, 1998, v.16, n.2, p.185-196.
GORE, J. Out of the shadows MRI and the Nobel Prize. New England Journal of Medicine, 2003, v.349, n.24, p.2290-2292.
WHITE, S. C.; PHAROAH, M. J. Oral Radiology: Principles and Interpretation. Mosby, St. Louis, 2000. p.205-206.
PRUESSMANN, K. P. et al. SENSE: sensitivity encoding for fast MRI. Magnetic Resonance in Medicine, 1999, v.42, n.5, p.952-962.
BAKER, L. L. et al. Recent advances in MR imaging/spectroscopy of cerebral ischemia. American Journal of Roentgenology, 1991, v.156, n.6, p.1133.
GALLEZ, B. et al. Use of nitroxides for assessing perfusion, oxygenation, and viability of tissues: in vivo EPR and MRI studies. Magnetic Resonance in Medicine, 1996, v.35, n.1, p.97-106.
HAYES, C. E. et al. An efficient, highly homogeneous radio frequency coil for whole-body NMR imaging at 1.5T. Journal of Magnetic Resonance, 1985, v.63, p.622-628.
ROEMER, P. B. et al. The NMR phased array. Magnetic Resonance in Medicine, 1990, v.16, p.192-225.
HASHIMOTO, S.; KOSE, K.; HAISHI, T. Development of a pulse programmer for magnetic resonance imaging using a personal computer and a high-speed digital input-output board. Review of Scientific Instruments, 2012, v.83, p.053702.
LIKES, R. S. Moving gradient zeugmatography. US Patent 4307343, issued 22 Dec 1981.
BROWN, T. R.; KINCAID, B. M.; UGURBIL, K. NMR chemical shift imaging in three dimensions. Proceedings of the National Academy of Sciences USA, 1982, v.79, p.3523-3526.
LJUNGGREN, S. A simple graphical representation of Fourier-based imaging methods. Journal of Magnetic Resonance, 1983, v.54, p.338-343.
TWIEG, D. B. The k-trajectory formulation of the NMR imaging process with applications in analysis and synthesis of imaging methods. Medical Physics, 1983, v.10, p.610-621.
MANSFIELD, P. Multi-planar image formation using NMR spin echoes. Journal of Physics C: Solid State Physics, 1977, v.10, p.L55-58.
JOHNSON, G.; HUTCHISON, J. M. S. The limitation of NMR recalled echo imaging techniques. Journal of Magnetic Resonance, 1985, v.63, p.14-30.
AHN, C. B.; KIM, J. H.; CHO, Z. H. High-speed spiral-scan echo planar NMR imaging – i. IEEE Transactions on Medical Imaging, 1986, v.5, p.2-7.
RZEDZIAN, R. R.; PYKETT, I. L. Instant images of the human heart using a new, whole body MR imaging system. American Journal of Roentgenology, 1987, v.149, p.245-250.
SOUZA, S. P. et al. Echo-planar imaging with a non-resonant gradient power system. Proceedings of the 10th Annual Scientific Meeting of the SMRM, San Francisco, p.217, 1984.
¹Universidade Federal de Goiás, UFG
²Universidade Federal de Goiás, UFG
