REGISTRO DOI: 10.69849/revistaft/ar10202410040840
Djalma Gomes Neto¹; Ana Luiza Nascimento Gonçalves²; Gabriel Dias Coutinho Souza³; Giovanna Pimentel Passalini4; Izabela de Melo Alves5.
RESUMO
INTRODUÇÃO: A anemia falciforme é uma hemoglobinopatia hereditária e a doença hematológica mais comum no mundo, afetando cerca de 2% da população brasileira, com uma prevalência alta entre a população negra. Caracteriza-se por uma mutação no cromossomo 11 que altera a estrutura da hemoglobina, fazendo com que as hemácias assumam uma forma de foice em condições de baixa oxigenação. OBJETIVO: Descrever as principais complicações da anemia falciforme na gestação. MÉTODO: Uma revisão narrativa da literatura utilizando bases de dados Pubmed, Scielo com os descritores anemia falciforme na gestação, sendo selecionados seis artigos de forma subjetiva considerados relevantes para o tema. RESULTADO: A anemia falciforme está associada a várias complicações, incluindo episódios de vaso-oclusão, dor, infecções e síndrome torácica aguda. Durante a gestação, as mulheres com anemia falciforme enfrentam maiores riscos de complicações obstétricas e fetais, como placenta prévia, descolamento prematuro da placenta, aborto, parto prematuro e pré-eclâmpsia. O acompanhamento pré-natal rigoroso é essencial, incluindo monitoramento contínuo da saúde da mãe e do feto, testes laboratoriais regulares e medidas preventivas para minimizar os riscos associados. O tratamento da anemia falciforme inclui suporte transfusional, uso de hidroxiureia, vacinação adequada e acompanhamento contínuo. CONCLUSÃO: Durante a gravidez, é essencial ajustar as estratégias de tratamento e monitoramento para reduzir as complicações e melhorar a saúde materna e fetal. A combinação de diagnóstico precoce, manejo especializado e estratégias personalizadas é crucial para enfrentar os desafios da anemia falciforme durante a gestação e melhorar a qualidade de vida das pacientes.
PALAVRAS-CHAVE: Anemia falciforme; Doenças hematológicas; Gravidez de alto risco; Gravidez.
ABSTRACT
INTRODUCTION: Sickle cell anemia is a hereditary hemoglobinopathy and the most common hematological disease in the world, affecting around 2% of the Brazilian population, with a high prevalence among the black population. It is characterized by a mutation on chromosome 11 that alters the structure of hemoglobin, causing red blood cells to assume a sickle shape under conditions of low oxygenation. OBJECTIVE: To describe the main complications of sickle cell anemia during pregnancy. METHOD: A narrative review of the literature using Pubmed and Scielo databases with the descriptors sickle cell anemia during pregnancy, six articles being subjectively selected and considered relevant to the topic. RESULT: Sickle cell anemia is associated with several complications, including episodes of vaso-occlusion, pain, infections and acute chest syndrome. During pregnancy, women with sickle cell anemia face increased risks of obstetric and fetal complications, such as placenta previa, placental abruption, miscarriage, premature birth and pre-eclampsia. Close prenatal care is essential, including continuous monitoring of the health of the mother and fetus, regular laboratory tests, and preventive measures to minimize associated risks. Treatment of sickle cell anemia includes transfusion support, use of hydroxyurea, adequate vaccination and continuous monitoring. CONCLUSION: During pregnancy, it is essential to adjust treatment and monitoring strategies to reduce complications and improve maternal and fetal health. The combination of early diagnosis, specialized management and personalized strategies is crucial to face the challenges of sickle cell anemia during pregnancy and improve patients’ quality of life.
KEYWORDS: Sickle cell anemia; Hematological diseases; High-risk pregnancy; Pregnancy.
1. INTRODUÇÃO
A anemia falciforme representa uma das formas das hemoglobinopatias hereditárias sendo a doença hematológica mais comum no mundo. No Brasil, estima-se que cerca de 2% da população apresenta o traço falcêmico e que aproximadamente 0,1 a 0,3% da população negra seja portadora da anemia falciforme. (REZENDE, et al, 2019)
Trata-se de uma doença genética autossômica recessiva resultante de uma mutação do cromossoma 11 que leva à substituição de um aminoácido na cadeia que codifica a beta globina, resultando na formação de uma hemoglobina com estrutura alterada e instável, que, na presença de baixa concentração de oxigênio, precipita-se, formando uma molécula levemente curva, em forma de foice. Caracteriza-se por anemia crônica, sendo que o diagnóstico é feito pela eletroforese de hemoglobina e ao hemograma é possível visualizar anemia normocítica normocrômica. (ZUGAIB, et al, 2019)
Durante a gestação, esse grupo de mulheres apresenta maior taxa de complicações obstétricas, hematológicas e fetais em relação à população em geral, porém este fato não contraindica a gestação. A mortalidade materna entre as gestantes portadoras de doença falciforme tem sido relatada em diversos estudos e varia de 0,05%, a 11,4%, que pode ser minimizado com acesso precoce e acompanhamento em serviços de pré-natal especializado (FEBRASGO, 2019). Sendo assim, este estudo possui como finalidade descrever as principais complicações hematológicas, infecciosas e obstétricas em gestantes portadoras de anemia falciforme, identificando as estratégias de manejo e tratamento disponíveis, e propondo recomendações baseadas em evidências para melhorar os desfechos obstétricos em gestantes com essa condição.
2. METODOLOGIA
A metodologia de pesquisa adotada consistiu na realização de uma revisão de literatura no formato narrativo. Esta abordagem envolveu a coleta de informações nas bases de dados PubMed, SciELO Brasil (Scientific Electronic Library Online) e Biblioteca Virtual da Saúde (BVS), FEBRASGO, Ministério da saúde. Foram utilizados os seguintes descritores registrados no DeCS (Descritores em Ciências da Saúde): “Anemia falciforme”, “Doenças hematológicas”, “Gravidez de alto risco” e “Gravidez”.
O período de pesquisa abrangeu de 2017 a 2024. A seleção das publicações foi baseada nos critérios estabelecidos pelos descritores mencionados. Inicialmente, os artigos foram selecionados com base no primeiro descritor recomendado. Em seguida, foram avaliados trabalhos nos idiomas português, inglês e espanhol, considerando-se o tema central, os títulos, os resumos e, quando disponível, o texto completo.
Durante o processo de seleção, foram excluídos títulos duplicados presentes nas bases de dados, bem como aqueles que não estavam alinhados com os objetivos deste estudo ou que foram classificados em categorias internas. Após essa triagem, um total de seis artigos foi selecionado para compor esta revisão.
3. RESULTADOS E DISCUSSÃO
3.1 DEFINIÇÃO
Na anemia falciforme é uma doença genética caracterizada pela presença da hemoglobina S (HbS) em vez da hemoglobina A (HbA). Ocorre por uma mutação no gene HBB, que codifica a cadeia beta da hemoglobina. Resultando na substituição do ácido glutâmico pela valina como sexto aminoácido na beta globina, levando a formação da hemoglobina S. Sob condições de baixas oxigenação a hemoglobina S tende a polimerizar, modificando a forma bicôncava da hemoglobina para a forma de “foice” ou “meia-lua”. Por serem menos flexíveis que as hemácias normais, os eritrócitos falcizados obstruem a microcirculação de tecidos e órgãos, acarretando episódios de vaso-oclusão. A vida útil desses eritrócitos é consideravelmente menor em relação à hemoglobina normal, resultando em hemólise crônica, que agrava a vaso-oclusão e gera uma resposta inflamatória contínua, na qual as citocinas liberadas aumentam ainda mais a adesão dos eritrócitos ao endotélio perpetuando o ciclo oclusão/inflamação. (CHAVES, et al, 2020)
3.2 QUADRO CLÍNICO
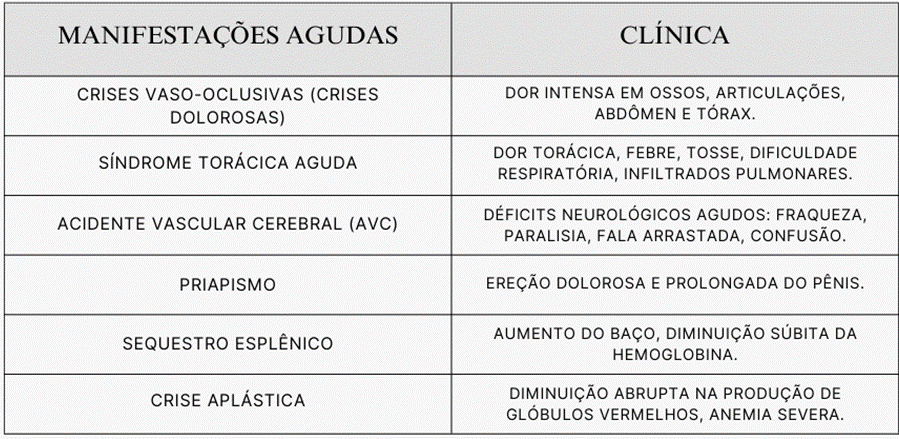
A Hemoglobinopatia S apresenta um quadro clínico diverso, com manifestações agudas e crônicas que podem afetar variados sistemas do corpo. Os sintomas podem começar a aparecer desde o início da vida, com isso, é extremamente importante o diagnóstico precoce como medida de impacto positiva na assistência de qualidade às pessoas com a doença.
A dor na doença falciforme é a característica padrão da doença, e pode se manifestar de forma aguda, subaguda, crônica ou episódica, acometendo diversas regiões do corpo, conforme exposto na figura 1. Os pacientes podem sentir dor somática, visceral, neuropática ou até mesmo iatrogênica, embora a maioria das dores seja espontânea, e muitos episódios requerem internação hospitalar e cuidados adequados. (DA SILVA, et al, 2018).
A síndrome torácica aguda é uma forma severa de doença pulmonar que pode evoluir para a síndrome do desconforto respiratório agudo (SARA). Alterações radiológicas podem aparecer tardiamente, tornando o diagnóstico mais difícil. A lesão pulmonar ocorre devido a três mecanismos principais relacionados com a vasoclusão: infecção, embolia gordurosa e sequestro de células falciformes nos vasos pulmonares, resultando em infarto pulmonar. Esta lesão compromete a ventilação e a perfusão, causando hipoxemia, aumento da desoxigenação da hemoglobina S (HbS) e agravamento da vasoclusão. Novos eventos vaso oclusivos reiniciam o processo, levando a infarto da medula óssea e embolia gordurosa. (SANTOS NETO, et al, 2020)
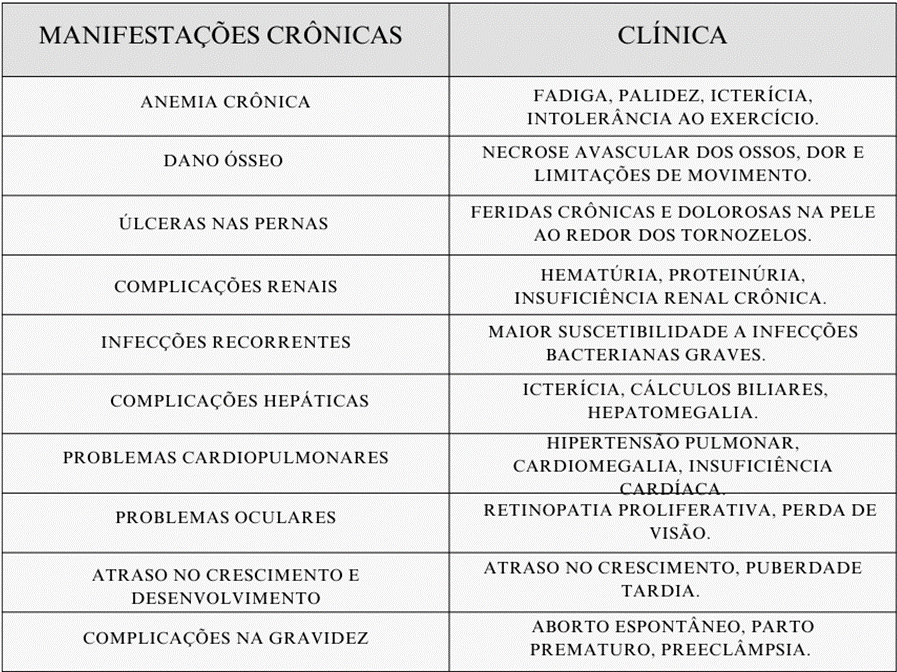
Dentre as manifestações crônicas, a mais comum é a anemia do tipo hemolítica na qual ocorre destruição prematura das hemácias marcada por vários episódios de vaso oclusão que é frequentemente acompanhada de outros sintomas, como fadiga, fraqueza, e palidez, descrito na figura 2 causando complicações secundárias como infecções, sequestro esplênico e crise aplásica. (MACHADO, et al, 2019).
Pacientes com doença falciforme têm uma maior predisposição a infecções. Muitos apresentam disfunção esplênica devido a infartos repetidos, hemólises e estases no sistema retículo endotelial, resultando em deficiência na fagocitose, inibição da migração neutrofílica, redução dos níveis de IgM e diminuição da atividade de opsonização. Infecções comuns incluem pneumonia, osteomielite e infecções do trato urinário. Infecções podem precipitar crises vaso-oclusivas, e viroses podem afetar a adesão e as propriedades das células endoteliais através de citocinas e fatores de necrose tumoral. A prevenção de infecções é crucial para pacientes com doença falciforme (DE OLIVEIRA SANTANA, et al, 2017).
A crise do sequestro esplênico é a segunda principal causa de morte em crianças menores de seis anos. Esta grave complicação é caracterizada pelo aprisionamento de hemácias na circulação esplênica, o que agrava a anemia e provoca uma esplenomegalia que se instala rapidamente. Por outro lado, a crise aplásica é causada pela infecção pelo parvovírus B19 ou eritrovírus B19, que destrói temporariamente os precursores eritropoiéticos, interrompendo a produção de hemácias. Como os pacientes com doença falciforme já estão em constante hemólise, essa mielossupressão temporária pode piorar a anemia basal. Diferentemente da crise do sequestro esplênico, a crise aplásica não apresenta esplenomegalia e é acompanhada por uma contagem reduzida de reticulócitos, ao invés de aumentada (DE OLIVEIRA SANTANA, et al, 2017).
3.3 DIAGNÓSTICO
As alterações laboratoriais associadas à anemia falciforme são principalmente decorrentes da hemólise. Essa condição resulta em anemia normocítica e normocrômica, aumento dos níveis de desidrogenase láctica (DHL) e bilirrubina indireta, além da redução dos níveis de haptoglobina. A avaliação do esfregaço de sangue periférico revela alterações mais específicas da doença falcêmica, como a presença dos drepanócitos, ou hemácias em forma de foice. No entanto, para confirmar o diagnóstico, é necessário detectar grandes quantidades de hemoglobina S (HbS) através de testes especializados. A eletroforese de hemoglobinas, que separa as hemoglobinas com base em sua carga elétrica, e a cromatografia líquida de alta performance, que utiliza solventes para essa separação, são métodos eficazes para essa identificação (DA SILVA, et al, 2018).
Como mencionado, a anemia falciforme pode levar a complicações graves, tornando essencial a detecção precoce da doença para evitar tais problemas. O teste do pezinho é o exame realizado para identificar as hemoglobinas no sangue dos recém-nascidos. Esse teste classifica as hemoglobinas detectadas em ordem decrescente de concentração, permitindo a identificação precoce de hemoglobinopatias, incluindo a anemia falciforme. (DA SILVA, et al, 2018).
3.4 TRATAMENTO
A anemia falciforme é uma condição complexa que causa tanto complicações agudas quanto crônicas, resultando em alta morbimortalidade e uma expectativa de vida cerca de 20 anos menor em comparação com a média da população. O tratamento para essa doença envolve não apenas o manejo específico das diversas complicações, mas também estratégias gerais, como suporte transfusional e quelação de ferro para evitar a sobrecarga de ferro associada às transfusões. A hidroxiureia também desempenha um papel importante no tratamento. Seu efeito terapêutico decorre da inibição da enzima ribonucleotídeo redutase, que é crucial para a produção de nucleotídeos e, por conseguinte, para a síntese de DNA. Ao bloquear essa enzima, a hidroxiureia promove vários benefícios para os pacientes com anemia falciforme. O principal benefício é o aumento da produção de hemoglobina fetal (HbF), o que diminui a concentração de hemoglobina S (HbS) e reduz a formação de células em forma de foice, aliviando assim os sintomas da doença (CHAVES, et al, 2020).
É recomendado administrar a vacina contra o pneumococo polivalente. Além disso, deve-se considerar a vacinação contra H. influenzae tipo B e contra o meningococo tipo C. É importante verificar a situação das vacinas para hepatite B e outras vacinas do calendário de imunizações. Para gestantes, vacinas com vírus vivos são desaconselhadas. Em vez disso, devem receber as vacinas contra a gripe sazonal e a gripe H1N1 (“gripe suína”), bem como garantir o reforço da vacina contra o pneumococo (ZUGAIB, et al, 2019).
3.5 GESTAÇÃO
Para gestantes com doença falciforme, a gravidez é uma situação potencialmente grave. A saúde da mãe pode já estar comprometida antes da gravidez e pode agravar-se, pois a microcirculação placentária é um ambiente com alto grau de desoxigenação da hemoglobina. Esse ambiente facilita a falcização, estase e infartos placentários, com consequências para a mãe e para o feto. (ANDRADE, et al, 2024)
O volume da placenta na gestante falciforme pode ser reduzido devido à vaso-oclusão, que diminui o fluxo sanguíneo. Isso resulta em menor aporte de nutrientes ao feto e em anormalidades na integridade da membrana placentária, prejudicando tanto a mãe quanto o feto. Alterações no tamanho, localização, aderência à parede uterina e histologia da placenta são observadas em pacientes com anemia falciforme. A redução do tamanho da placenta geralmente se deve à diminuição do fluxo sanguíneo provocada pela vaso-oclusão. Embora as causas da maior incidência de placenta prévia e descolamento prematuro de placenta em todos os genótipos de doença falciforme não estejam totalmente claras, as alterações histopatológicas comuns incluem fibrose das vilosidades, infartos e calcificações. A maior taxa de aborto, retardo de crescimento intrauterino, parto prematuro e mortalidade perinatal pode ser explicada pela fisiopatologia da doença falciforme. (ANDRADE, et al, 2024)
Durante a gravidez, a anemia tende a se agravar devido à combinação da hemodiluição fisiológica com a hemólise das hemácias anômalas. A maior incidência de placenta prévia e descolamento prematuro de placenta na doença falciforme é observada, embora as causas exatas não sejam bem compreendidas. O estudo histopatológico das placentas de pacientes com doença falciforme revela uma maior incidência de fibrose das vilosidades, infartos e calcificações. A microvasculatura placentária, danificada pelas hemácias falcizadas, pode ser uma das causas para a maior incidência de aborto e retardo de crescimento intrauterino. (DE OLIVEIRA SANTANA, et al, 2017).
Os fetos de mães com doença falciforme geralmente nascem prematuramente. As razões exatas para isso não estão totalmente esclarecidas, mas fatores como anemia, restrição do crescimento intrauterino, placenta prévia e descolamento prematuro de placenta contribuem para a maior incidência de parto pré-termo. A pré-eclâmpsia é cerca de cinco vezes mais frequente em gestantes com doença falciforme e pode também contribuir para o parto prematuro. (ANDRADE, et al, 2024) Além disso, outros fatores independentes, como gestação múltipla, consumo de álcool e drogas, tabagismo, estado nutricional inadequado, ganho de peso materno, infecção urinária e corioamnionite, também contribuem para as complicações observadas em gestantes com doença falciforme. (DE OLIVEIRA SANTANA, et al, 2017).
A anemia falciforme transforma a gravidez em uma situação de alto risco devido às suas implicações fisiopatológicas, que afetam tanto a saúde da mãe quanto o desenvolvimento do feto. Um ponto importante é a elevada incidência de partos prematuros, com uma idade gestacional média de 34 semanas. Os recém-nascidos de mães com anemia falciforme frequentemente enfrentam problemas como baixo peso, dificuldades respiratórias graves e infecções neonatais, o que pode levar a desfechos fatais. O parto nessas gestantes também é frequentemente complicado. Entre as principais complicações estão a ruptura prematura das membranas e a pré-eclâmpsia, que são comuns nessas pacientes. A maioria dos partos é realizada por cesariana, e a taxa pode ser o dobro em comparação com gestantes sem anemia falciforme. A necessidade de cesárea apresenta vários desafios, pois a instabilidade hemodinâmica da mãe pode contraindicar a utilização de anestesia bloqueadora. (ZUGAIB, et al, 2019)
3.6 ACOMPANHAMENTO NA GESTAÇÃO
Durante o acompanhamento pré-natal, é essencial monitorar diversos aspectos da saúde da gestante e do feto. Deve-se observar o crescimento fetal, a pressão arterial, o risco de parto prematuro, a orientação nutricional apropriada e a detecção precoce de infecções e fatores que possam precipitar crises de dor. O exame físico deve incluir a avaliação do tamanho do baço. Os exames iniciais de pré-natal devem contemplar um hemograma completo com reticulócitos, eletroforese de hemoglobina, perfil de ferro (incluindo ferro sérico, ferritina e capacidade total de ligação do ferro), além de testes de função renal, hepática e de eletrólitos, glicemia, ácido úrico, sorologia para hepatite A, B e C, HIV l e ll, HTLV l e ll, rubéola e sífilis, toxoplasmose, citomegalovírus, listeriose, exame de urina com urocultura, MIF e teste para detecção de anticorpos contra eritrócitos (DA SILVA, et al, 2018). Em casos de hemoglobina SS homozigótica, a hemoglobina basal geralmente varia entre 6 e 8 g/dL. Mulheres com hemoglobinopatias S, C e talassemias SB tipicamente têm níveis de hemoglobina entre 9 e 12 g/dL. O grau de hemólise pode ser avaliado através das dosagens de bilirrubina, DHL e reticulócitos. Para pacientes que receberam múltiplas transfusões, é necessário realizar um painel completo de anticorpos antieritrocitários devido ao risco de aloimunização. Também é importante identificar e tratar adequadamente a bacteriúria assintomática. Avaliações adicionais, como o Ecodopplercardiograma para a função cardíaca e o ultrassom abdominal total para a investigação de cálculos biliares e a visualização do baço, são recomendadas para prevenir complicações futuras. A frequência das consultas de pré-natal deve ser ajustada conforme a gravidade da condição da gestante, durante o primeiro e o segundo trimestres, as consultas devem ser realizadas a cada três semanas. O objetivo é educar a paciente, orientando-a sobre como identificar episódios de crise vaso-oclusiva e iniciar o tratamento da crise álgica, incluindo hidratação oral e uso de analgésicos em casa. Em cada visita, deve ser solicitado um hemograma completo, com contagem de reticulócitos. A monitorização do crescimento fetal deve ser realizada por ultrassonografias seriadas, e o bem-estar fetal deve ser avaliado por meio de Dopplervelocimetria, cardiotocografia e perfil biofísico fetal (FEBRASGO, 2019).
A decisão sobre o modo de parto será tomada entre 38 e 39 semanas, com base na evolução da saúde materna e fetal, e a analgesia durante o trabalho de parto é aconselhada. As pacientes devem receber suplementação de ácido fólico na dose de 5 mg diariamente. Se houver uma acentuada piora da anemia (com uma redução de 30% nos níveis iniciais de hemoglobina) ou se os níveis de hemoglobina estiverem abaixo de 6 g/dL, é necessário realizar transfusões de sangue. A eficácia das transfusões de troca para prevenir complicações durante a gestação não é bem estabelecida, e não há recomendação para a adoção generalizada dessa prática. Devido à ausência de estudos consistentes sobre a segurança da continuidade do tratamento com hidroxiureia, esta medicação deve ser interrompida. (MONTENEGRO, et al, 2019)
A orientação pré-concepcional é fundamental e deve incluir explicações sobre possíveis complicações da gestação, o uso de anticoncepcionais que contêm derivados de progesterona pode aumentar os níveis de hemoglobina F e diminuir a frequência de crises em pacientes que não desejam engravidar, e o aconselhamento dos pais sobre a probabilidade de ter uma criança afetada pela doença, com base no exame de eletroforese de hemoglobina do parceiro (DA SILVA, et al, 2018).
4. CONSIDERAÇÕES FINAIS
A anemia falciforme, uma das hemoglobinopatias hereditárias mais prevalentes globalmente, representa um desafio significativo para a saúde pública, especialmente no contexto da gestação. A revisão realizada revela a complexidade da gestão desta condição, evidenciando tanto as suas complicações agudas e crônicas quanto os desafios específicos enfrentados durante a gravidez.
Os resultados mostram que a anemia falciforme não apenas provoca uma série de sintomas debilitantes e complicações, como dor crônica, infecções e crises vaso-oclusivas, mas também que essas manifestações podem ser exacerbantes durante a gestação. A presença da doença falciforme durante a gravidez aumenta o risco de complicações graves tanto para a mãe quanto para o feto, incluindo maior incidência de parto prematuro, baixo peso ao nascer e complicações placentárias.
O diagnóstico precoce e o manejo adequado são cruciais para minimizar os riscos associados a essa condição. Estratégias como a realização de testes laboratoriais especializados, a administração de vacinas adequadas e o monitoramento rigoroso durante o pré-natal são fundamentais para o sucesso do tratamento e a melhoria dos desfechos obstétricos. Além disso, o acompanhamento contínuo da saúde materna e fetal, bem como a adequação das intervenções terapêuticas, desempenham um papel vital na redução das complicações e na promoção de uma gestação mais segura.
Este estudo reforça a necessidade de um cuidado multidisciplinar e especializado para gestantes com anemia falciforme. Recomenda-se a implementação de práticas baseadas em evidências e a continuação de pesquisas para aprimorar as estratégias de manejo e tratamento, visando a melhoria da qualidade de vida e dos resultados obstétricos para essas pacientes. Em síntese, a combinação de diagnóstico precoce, monitoramento contínuo e estratégias de tratamento personalizadas é essencial para enfrentar os desafios impostos pela anemia falciforme e proporcionar um suporte adequado às mulheres afetadas durante a gestação.
5. REFERÊNCIAS
MONTENEGRO, Carlos Antonio Barbosa; REZENDE FILHO, Jorge de. Obstetrícia fundamental, Rezende. 14.ed. Rio de Janeiro: Guanabara Koogan, 2019, 1002. p.
Zugaib, Marcelo; Francisco, Rossana Pulcineli Vieira (eds). Zugaib obstetrícia [4.ed.]. BARUERI: Manole, 2019. 1424p.
Fernandes CE, Silva de Sá MF, eds. Tratado de Obstetrícia Febrasgo. 1ªed. Rio de Janeiro: Elsevier; 2019.
DOS SANTOS NETO, João Lourenço et al. Gestação na anemia falciforme e suas principais complicações. Caderno de Graduação-Ciências Biológicas e da Saúde-UNIT-ALAGOAS, v. 6, n. 2, p. 114-114, 2020.
DA SILVA, Cairo Soares; COELHO, Verônica Andressa Ortega. Gestação em pacientes portadoras de anemia falciforme. Revista de Patologia do Tocantins, v. 5, n. 4, p. 64-69, 2018.
DE OLIVEIRA SANTANA, Izabella; BASTOS, Rodrigo Almeida. Gestação em mulheres com anemia falciforme: uma revisão sobre as complicações maternas e fetais. Enfermagem Brasil, v. 16, n. 1, p. 54-61, 2017.
CHAVES, Marcela Pessoa et al. Assistência Integral: Condutas Profiláticas e Terapêuticas em Gestantes com Anemia Falciforme. Brazilian Journal of Health Review, v. 3, n. 5, p. 11989-12002, 2020.
MACHADO, Fernanda Aiume Carvalho. Mulheres adoecidas por Anemia Falciforme: perspectivas de gestação. Anais dos Seminários de Iniciação Científica, n. 23, 2019.
DE ANDRADE, Luana Alves et al. GESTANTES PORTADORAS DE ANEMIA FALCIFORME E SUAS COMPLICAÇÕES. Revista Ibero-Americana de Humanidades, Ciências e Educação, v. 10, n. 3, p. 2203-2209, 2024.
¹Instituição: FAMESC – Faculdade Metropolitana São Carlos
Av. Gov. Roberto Silveira, 910, Bom Jesus do Itabapoana – RJ, 28360-000
Email: dgneto@yahoo.com.br
https://orcid.org/0000-0003-3044-1109
²Instituição: FAMESC – Faculdade Metropolitana São Carlos
Av. Gov. Roberto Silveira, 910, Bom Jesus do Itabapoana – RJ, 28360-000
Email: anagnluiza@gmail.com
https://orcid.org/0009-0000-6364-4928
³Instituição: FAMESC – Faculdade Metropolitana São Carlos
Av. Gov. Roberto Silveira, 910, Bom Jesus do Itabapoana – RJ, 28360-000
Email: gabriel2dias15@gmail.com
https://orcid.org/0009-0001-2711-6105
4Instituição: FAMESC – Faculdade Metropolitana São Carlos
Av. Gov. Roberto Silveira, 910, Bom Jesus do Itabapoana – RJ, 28360-000
Email: gigipassalini10@gmail.com
https://orcid.org/0009-0005-9764-5917
5Instituição: FAMESC – Faculdade Metropolitana São Carlos
Av. Gov. Roberto Silveira, 910, Bom Jesus do Itabapoana – RJ, 28360-000
Email: izabelameloa@gmail.com
https://orcid.org/0009-0006-8886-8155
