REGISTRO DOI:10.5281/zenodo.12661208
Aline Toledo Salgado
Orientadora: Professora Adriana Maria Vieira Silveira
RESUMO
A patência apical ainda é uma das principais controvérsias na endodontia contemporânea. Este artigo revê alguns problemas, vantagens e resumos das técnicas de patência atuais para ajudar os leitores a desenvolverem suas estratégias próprias baseadas em conhecimento científico.
Palavras-chaves: patência apical, o forame apical, sobre instrumentação, sob instrumentação
ABSTRACT
Apical patency remains one of the main controversies in contemporary endodontics. This paper reviews some problems, advantages and shortcomings of current patency techniques to assist the readers in developing their own strategies on the basis of scientific knowledge.
INTRODUCTION
The question of the location of the apical endpoint for root canal preparation and filling is still a vehemently debated controversy in endodontics1. For several decades one of the principles of H. Schilder from 1974 (confine instrumentation to the root canals themselves)2 has repeatedly been challenged and even rejected as outdated3. Instead, a widevariety of ideas have led to so-called patency techniques (see below for definitions and procedures)being recommended. Mainly mechanical objectives (access to the apical foramen) as well as biological objectives (microbial depletion by mechanical cleaning of the foramen) have been quoted to support this recommendation4. The claimed advantages of patency techniques include:
- irrigants and medicated dressings are given access to the apical foramen and periradicular tissue
- less loss of working length during preparation
- lower incidence of preparation errors
- less preparation-induced root canal transportation
- largely avoidance of canal blockages 3,4.
Meanwhile these ideas conflict, for example, with the conclusions drawn from classic histology studies,5,6 which advise against mechanically irritating the foramen with patency instruments. The debate about the pros and cons of patency techniques is currently shifting between these two ‘poles’. However, discussions about the location of the apical endpoint are not merely of sophistry, but also clinical importance, as proved impressively by two meta analyses.According to these analyses, significantly different success rates are apparently to be expected, depending on the endpoint of the root canal filling 7,8. On the other hand, it is virtually impossible to tell from the extremely sparse data currently available in the relevant literature if the widely accepted significance in terms of the prognosis of root canal treatment
should actually be attached to the above-mentioned preparation errors 9-11. Rather than presenting an assessment of the pros and cons of patency techniques, the aim of this contribution to the discussion is to help rationalize what is occasionally an emotional debate by analysing the available literature on this subject. As is widely known, not only do many roads lead to Rome, but at least as many routes lead to the apical endpoint of the root canal—wherever that may lie.
Keywords: apical patency, apical foramen, over-instrumentation, under instrumentation
PATÊNCIA APICAL: FATO OU FICÇÃO – Um mito ou uma realidade?
Uma Contribuição para a Discussão
A patência apical ainda é uma das principais controvérsias na endodontia contemporânea. Este artigo revê alguns problemas, vantagens e resumos das técnicas de patência atuais para ajudar os leitores a desenvolverem suas estratégias próprias baseadas em conhecimento científico.
1 INTRODUÇÃO
A questão da localização do ponto final apical para a preparação da raiz no canal e a obturação ainda é veementemente debatida pelos endodontistas (1) .Por várias décadas um dos princípios de SCHILDER H em 1974( limita a instrumentação para os canais; eles próprios),( 2) tem repetidas vezes sido desafiadas e até mesmo rejeitada como fora de moda (3) .Ao invés disso, uma ampla variedade de ideias tem conduzido a então chamada técnica de patência( veja abaixo para as definições e procedimentos), sendo recomendada, principalmente pelos objetivos mecânicos(acesso ao forame apical) quanto objetivos biológicos(esgotamento da microbiota por limpeza mecânica do forame) foram citadas para apoiar esta recomendação (4). As vantagens das técnicas de patência incluem:
– Irrigação e curativos medicamentosos têm acesso ao forame apical e tecidos periradicular.
– Menos perda do comprimento de trabalho durante a preparação.
– Menor incidência de erros durante a preparação
– Menos indução do transporte do canal durante a preparação
– Evitar o bloqueio do canal
De vez em quando estas idéias entram em conflito, por exemplo, com as conclusões tiradas de estudos, (5,6) de histologia clássica, a qual adverte que mecanicamente se irrita o forame com instrumentos de patência.
O debate sobre os pós e os contras das técnicas de patência é atualmente deslocado entre estes dois pólos. Entretanto, discussões sobre a localização do ponto final não é meramente um sofisma, mas também uma importância clínica, como provada impressivamente por duas meta- análises. De acordo com estas análises, significativamente as taxas de sucesso são aparentemente diferentes, em função do ponto de extremidade da raiz do canal (7,8) .Por outro lado, é praticamente impossível dizer a partir dos dados extremamente escassos atualmente disponíveis na literatura relevante se a ampla significância em termos de prognóstico do tratamento do canal, deve realmente ser ligada aos erros de preparação mencionados acima (9,11).
Ao invés de apresentar uma avaliação dos pós e contras das técnicas de patência, o objetivo desta contribuição é ajudar a radionalizar o que é ocasionalmente um debate emocional para analisar a literatura disponível nesta matéria. Como é amplamente conhecido, não somente muitas estradas levam a Roma, mas pelo menos muitas rotas levam ao ponto final apical do canal radicular- seja onde for que ela estiver.
1.1 DEFINIÇÕES DO TERMO “ PATÊNCIA”
No glossário de Termos da Associação Americana de Endodontistas (AAE) (12), a patência é definida como uma técnica de preparação em que a região apical do canal radicular é mantida livre de detritos recapitulando através do forame fisiológico(constrição apical) com uma lima fina.
No Offizielles Endodonto Logisches Lexikon de sociedade Alemã de Odontologia Restauradora (DGZ) (13), de 1999, a referências de que as limas de patência é: Limas de tamanho pequeno ISO (ISO 10 ou menor) deve ser colocada a uma curta distância além da constrição apical sem pressão quando realiza- se alguma técnica de preparação da raiz do canal com a finalidade de checar se a raiz apical; ou melhor, se a área apical da raiz do canal está bloqueada com pedaços da dentina. No entanto, na realidade, há toda uma gama de definições muito diferentes e perversidade de conceitos e técnicas.
1.2 PUB MED + PATÊNCIA = PROBLEMA
Uma pesquisa na internet; exemplo: via Pub/ Med (http///www.ncbi.mim.nih.gov/sites/entrez), para artigos nesta matéria de “ patência” é inicialmente algo surpreendente, há nada menos que 25.172 itens( como em 8 de agosto).Reduzir a pesquisa ou tornando os termos da pesquisa mais precisos, nos propicia em relato mais claro.
1.3 PATÊNCIA DO CANAL RADICULAR
Estes nos dá 44 artigos. Bem como alguns dos artigos referidos mais tarde nesta revisão, estes sucessos incluem:
– Herrera M. Abalos C., Planos AJ,Llamas R. Influência do diâmetro da constrição apical do canal ZX precisão do locador de ápice.Endod 2007; 33(8)995-998.
– Molteni G, Spinelli R, Panigatti S, Colombo L, Ronchi P. Mucocele Frontoetimoidal volumosa com envolvimento epidural. Tratamento cirúrgico por abordagem coronal. Acta Otorhnolaryngol etal 2033.23(3)185-190.
-Yesilsoy C, Gordon W. Porras O. Hoch B, A observação da profundidade e da incidência do sulco mesial entre os orifícios mesiovestibular e mesiolingual nos molares inferiores.J Endod 2002-28(7)507-509.
– Padachey N. Patel V, Santerre, Cvitkovtch D, Lawrence HP, Friedman . Resistência de um selador endodôntico a penetração de bacterias in vitro. J Endod 2000.26(11) 656-659.
– Lliev ME, van der Zypen E. Frankbauser F. Inglaterra C Transconjuntival aplicação de mitomicina C, em combinação com o laser esclerostomia interno: um estudo de longo prazo morfológico no processo de cicatrização pós- operatório. Eye Res Exp 1997, 64(6)10131026.
1.4 PATÊNCIA APICAL
Este teve 76 artigos. A parte endodôntica destes estudos coincidem com aquelas encontradas no artigo sobre patência do canal radicular, mas contém mais artigos não- endodônticos.
1.5 EXTRUSÃO APICAL
Fornece 339 informações, mas estas podem ser reduzidas para 76 administrável, acrescentando Endodontia é uma extensa literatura sobre os materiais de obturação e irrigantes, os seguintes artigos são listados:
– Ng YL, Mann V. Rahbaran S, Lewsey J. Gulabilava K. Resultados do tratamento primário do canal radicular; revisão sistemática da literatura- Parte 2. Influência de fatores clínicos. Int. Endod I 2008- 41(1)6-31
– Siqueira JF JR. Causas microbianas de endodôntico flare- ups. (Revisão) Int Endod J 2003-36(2)453-463.
2 SOBRE INSTRUMENTAÇÃO
Este teve 20 trabalhos de sucesso e estas incluem:
– Debelian GJ, Olsen , .Tronstad Profiling de L.O perfil de acnes próprionibacterium recuperado do canal durante e após o tratamento endodôntico. Endo Dent Traumatol 1992;E(6).248-254.
-Holland R. Soares I,Soares IM.Influência da irrigação e curativo intra-canal no processo de cura de dentes de cães com periodontite apical.Endod Dent Traumatol 1992,8(6) 223-229.
Ambos os artigos acima definitivamente estabelecem uma consideração em relação a qualquer debate sobre patência,mas eles não estavam listados ou catalogados sob termos de pesquisa previamente mencionados.
Já ficou claro de seu resumo breve que a literatura necessária para a metade de uma discussão completa não pode ser melhorada de uma busca na internet apenas. Isto é devido a vários fatores, a parte do fato de que a patência é um termo de busca muito geral, o assunto é relativamente novo e muito complexo, de forma que ele não pode ser exposto com apenas algumas palavras chaves.
Mesmo que as revistas especializadas incluem palavras chaves, (Journal of Endodontics, por exemplo, não dá palavras –chave), elas não são padronizadas e portanto não são de grande ajuda para uma busca ou pesquisa neste contexto.
3 ALGUMA FORMA DE PATÊNCIA
Agora esta é uma fonte antiga de 1997 entre 53 escolas de Odontologia dos Estado Unidos (91% resposta), 24 (50%) afirmaram que eles incluíram um conceito de patência( alguma forma de patência) no seu ensino.Dezesseis dos 24 escolas de odontologia ensinaram o conceito em níveis de faculdade e todos ensinaram nos cursos de pós- graduação. Pelo que as limas para a patência estão concernidos, 42% usaram uma lima de tamanho 10K File;33% usaram uma lima de tamanho 15 K e 25% usaram uma lima de tamanho 25.
Isto de novo reflete a variabilidade do “conceito patência”já resulta das definições.
Fig 1 Patência é geralmente definida como regular instrumentação de um canal radicular com um fino instrumento para 1mm da constrição apical( forame fisiológico).
4 ESPREITANDO ATRAVÉS
Na literatura mais recente mencionando e discutindo a então chamada “técnica de patência”, a referência da literatura regularmente citado é a publicação feita por LS Buchanam do Jornal da Associação Dentária da Califórnia em 1989 sob o título de Administração da raiz de canal curva (15).
Neste estudo (o qual não é um estudo experimental, mas uma exposição dos pensamentos do autor e uma descrição de seus métodos) após esboçar o problema de diferentes canais com curvaturas e consequente necessidade de ser sondado e preparado com instrumentos pré-curvos, Buchnan enfoca em evitarmos o bloqueio apical.
Patência apical, é o oposto de bloqueio apical, que significa a ausência de bloqueio no terço apical da raiz do canal como um resultado do tecido mole e duro. É importante mantermos a patência apical, quando estamos preparando canais com raiz curva. Se um canal curvo permanece patente, conseguimos persuadir as limas e deslizar em até mesmo ganchos apicais severos. Se no entanto o bloqueio ocorrer, a força exercida na lima resultaria em um vetor de força diferente e mais linear e haveria assim uma divergência da trilha original do canal. Buchanan define a “ lima de patência” como uma lima-K pequena e flexível (nunca uma lima hesdtroem) que se move passivamente através da constrição apical sem alargá-lo (Fig. 1). Se uma lima de tamanho 15 não se adequar, instrumentos de tamanhos 08 e 10 seriam as apropriadas limas de patência. Durante o curso de preparação, estes instrumentos devem ser usados antes da irrigação( espiando através da constrição apical) de forma a afrouxar os tecidos remanescentes, e depois removê-los do forame e da área apical do canal por agitação da solução de irrigação.
De acordo com Buchan, o uso das limas de patência após a irrigação é menos eficaz, porque os tecidos remanescentes ainda estão presentes no terço apical do canal, devido ao efeito irrigante limitado. Os tecidos remanescente são na realidade arrastados pela lima de patência e inicialmente entram na solução. Elas se estabelecem, mas são rapidamente depositados de volta na constrição onde são então compactadas e pode bloquear irreversivelmente a raiz do canal.
Mullaney et al (16) basicamente concorda com Buchanan e diferencia entre dois tipos de preparação apical nos seguintes métodos:
- preparação de uma “matriz apical de dentina” o que equivale a uma paragem coronal apical para a constrição;
- preparação de um bisel contínuo do ápice anatômico para a entrada da raiz do canal.
No primeiro caso, é a parte apical da raiz do canal até a parada que deve ser patente e no segundo caso, é a parte apical mais distante ou longe da raiz do canal. A preparação sem patência deixaria as escórias da dentina e produtos de degradação da polpa, tanto quanto as bactérias na parte apical do canal ou apical para a parada. Aqui as bactérias não conseguem ser alcançadas pela resistência imunológica do corpo. Especula-se que o material expelido apicalmente é degradado e neutralizado pelo corpo de defesa.. De acordo com sua próprias experiências subjetivas usando a técnica de patência não resultaria em uma alta incidência de dor pós-operatória, mas reduziria a frequência dos bloqueios apicais. No entanto, os autores recomendam o uso de técnica de patência em combinação com a técnica de preparação da coroa para baixo para evitar dos detritos serem transportadas na direção apical durante a instrumentação. Se a dor pós- operatória ocorrer, a presença de um forame não bloqueado ajudaria na drenagem.
5 AMANTES DA POLPA E BÁRBAROS APICAIS
Esse título em que o provocador Nounce (17) comenta sobre a controvérsia técnicas de patência. Ele divide o mundo endodôntico em duas escolas de pensamento.
– Os amantes da polpa atentos a instrumentação e obturação da raiz do canal até a constrição apical de acordo com Mounce.
– O grupo de bárbaros apicais, por outro lado, atribui grande importância a ser capaz de empurrar uma pequena lima- K. (tamanho 06 a 15) a uma certa distância( 0.5 a 1 mm) através do forame dentro do tecido periapical.
Ele corretamente observa que nenhuma dessas duas escolas de pensamento pode reivindicar uma taxa elevada de sucesso. Entretanto, apesar de todas as suas contradições, eles concordam que a localização do forame fisiológico e seu diâmetro deve ser alterado tão pouco quanto a posição do canal radicular, e esse abiselamento uniforme da raiz do canal, ou melhor, de sua preparação deve ser tentada. Sua comparação dos argumentos destes dois campos ilustra a elevada natureza especulativa do debate e reconhece que sua recomendação da técnica de patência é empírica, e que a evidência baseada na superioridade das duas escolas ainda está pendente.
6 AGITAR AS MÃOS COM O LIGAMENTO PERIODONTAL
Em um artigo explicando a técnica de patência Bellamy (18) expressamente insiste que a endodontia não deveria se limitar ao canal radicular. Isto não passa de uma invaginação do tecido mesenquimal, o qual tem a mesma origem que o ligamento periodontal. É, portanto, um processo contínuo, o qual deve ser tratado como tal.
Ele afirma que o ponto final apical exato de uma raiz de canal não pode ser identificado, isto aplica-se, por exemplo, de canais radiculares com bifurcações apicais, múltiplos portais apical de saída ou um delta apical do canal principal. O único ponto radiográfico fixo é aparentemente o ápice radiográfico.
De acordo com Bellany, tratamento bem sucedido requer que a raiz do canal esteja obturação através do forame ou ápice radiográfico, o que pressupõe prioridade na remoção de detritos até este ponto. Por outro lado, isto não é possível usando a técnica de patência. Ele não considera passar um instrumento fino (tamanho ISO 06 10) não mais profundo que uma fração de um milímetro no periodonto apical como uma irritação maior do tecido periapical. Por outro lado, a passagem repetida de numerosos instrumentos dentro das lesões periapicais ou do osso periapical leva a inflamação e exudação e pode substancialmente impedir o tratamento .De acordo com H Schilder, ele acredita que não há razão para temer um pouquinho de excesso de material (“puff”) quando se está obturando através de um forame patente.
A patência reduz a frequência de bloqueios apicais, formação e trança de borda e transporte do canal, perfurações e problemas no pós operatório. Sem a patência, os conteúdos do canal radicular não podem ser completamente eliminados. No entanto, esta é a rota para uma endodontia de sucesso.
7 DANO OU PREJUÍZO GENTIL E NÃO GENTIL
Após sondagem da região apical com limas pré-curvadas tamanho 10, Ruddle (19) recomenda instrumentação cautelosa e passiva (gentil) de 1mm além do forame. Ele afirma que é necessário para manter a patência do forame, toda subsequente preparação, de modo que as soluções irrigantes pode atingir o ponto final apical do canal radicular e circular na anatomia lateral, e assim o objetivo biológico do tratamento, denomina-se a remoção de todos os tecidos remanescentes, bactérias e endotoxinas, podem ser atingidas. O risco dos erros de preparação, tais como; bloqueios, saliências ou perfurações, pode ser reduzida desta maneira em concordância com estudos de Schilder, contudo a posição do forame não deve ser deslocada e o próprio forame deve ser mantido, tão pequeno quanto prático para desinfecção subsequente e obturação. Em virtude do fluxo sangue e imunocompetência do tecido perirradicular, estabelecer e manter esta patência através de preparação subsequente é visto como não-prejudicial.
A recomendação é usar um instrumento fino para penetrar o forame fisiológico por 1 mm passivamente, em outras palavras sem contar, novamente depois de cada passo da preparação. Neste sentido, a patência primariamente significa o controlar a transitabilidade do forame.
8 UMA FRAÇÃO DE MILÍMETRO
No início de 1974, Herbert Schilder comentou a administração do forame apical em seu lendário artigo limpeza e modelagem do canal radicular. Na sua quarta regra no esboço da preparação do formato (objetivos do desenhos ). Ele aconselha que forame apical deve manter sua posição original em relação ao osso e à superfície da raíz, em outras palavras não deve haver transporte. A regra número 5 diz que a abertura parcial deve ser mantida tão pequena quanto seja prático em todos os casos. Ele reafirma que passar um instrumento repetidas vezes, desloca a abertura parcial do canal radicular para o exterior da curvatura. Para as obturações com gutta-percha, a preparação apical é requerida de tal maneira que confine a gutta-percha no canal radicular, qual é mais fácil atingir um forame pequeno.
Nas suas cinco regras biológicas ele enfatiza o seguinte:
– confinar a instrumentação no canal radicular.
– cuidado com material necrótico forçado além do forame durante o preparo do canal.
– remover todos os detritos do canal radicular.
Quando o ápice anatómico ou radiográfico é medido e o ponto final desejado e destinados de todos endodônticas de acordo com Schilder, a instrumentação além do forame
Fisiológico é inevitável. Seus comentários a respeito disto são: A passagem inadvertida de um instrumento fino passando pelo ápice durante a medida inicial do canal radicular ou ocasionalmente suave sondagem não mais profunda do que um fração de milímetro para dentro do espaço do ligamento periodontal durante a limpeza e modelagem não é o maior irritante para os tecidos periapicais. A passagem repetida de numerosos instrumentos dentro das lesões periapicais ou osso, entretanto produzirá inflamação apical e considerável exudato, causando desconforto e interrupção do tratamento. No entanto, ele enfoca que o canal deve permanecer patente e não deve ser bloqueado por detritos.
9 OS ALVOS DA PATÊNCIA
Uma forma de patência já foi usada antes da era de Schilder: uma ampla variedade de drogas foram forçadas através do canal acessível e forame patente dentro do tecido apical onde eles promoveriam a desinfecção e a cicatrização. Os agentes usados para aspiração e irrigação dos canais radiculares incluíram iodo ou produtos de cálcio, mas também hidróxido de cloro e Gás (20) H2O2 solução rivano (21) ou cloramina (22). Este tipo de patência é certamente interessante de uma perspectiva histórica, mas não será explorada mais longe nesta discussão.
10 PATÊNCIA SUÍÇA
Uma outra variedade da técnica de patência foi apresentada por Velvart e Sigurdsson (23). O objetivo de sua técnica de preparação com instrumentos NiTi, é minimizar a frequência de incidentes intra-operatórios, tais como a perda de comprimento ou de transporte do canal, e nesse aspecto ,concordar com Buchanan. Após um instrumento com conicidade 2% ser inserido para trabalhar o comprimento, um instrumento do mesmo tamanho, com conicidade (0,023) é utilizado um instrumento com conicidade mais profunda 0,026. Quando as pontas destes instrumentos são iguais, o segundo e o terceiro instrumento somente cortam coronalmente. Isto é pretendido para manter a “patência” do canal radicular e reduzir o risco da formação de um obturador de dentina apical. A preparação é completada com instrumentos de tamanhos ascendentes com inclinação de 2%, a qual funciona apicalmente após a inclinação coronal já ocorrer. Como, somente parte da parede dentina é cortada durante esta instrumentação, poucos chips de dentina são produzidos e transportados em uma direção apical.
Em um estudo em canais plásticos com curvatura de 45 graus (os quais foram preparados até o tamanho 40) esta forma de patência se realiza significativamente melhor em termos de perda de comprimento do que a técnica de força equilibrada/ balanceada envolvendo instrumentos de corte e não cortantes no ápice e preparação manual com limas Flex Files (Dentply DeTrey, Konstanz, Alemanha). Neste contexto o termo patência não esta confinado ao forame, mas diz respeito a toda a raiz do canal. Embora esta técnica tenha o mesmo objetivo que a patência proposta por Buchanam, ela não envolve instrumentação ativa das constrições fisiológicas.
11 QUEBRA, ROMPIMENTO, ATRAVESSAR
O termo é dado uma interpretação bastante diferente, quando os autores descrevem a patência sendo atingida por vários métodos. Estas descrições muito frequentemente se refere ao tempo que se gasta no trabalho manual para atingir este objetivo. A maioria dos artigos ou estudos não mencionam como a presença da patência foi checada(medida de comprimento elétrico, sangramento, sensação de dor apical, instrumento radioficamente super estendido). Nesta interpretação a patência é entendida como o meio de aplicar a passabilidade apical do forame de maneira que um instrumento de secção transversal de tamanho definido( normalmente ISO 10 ) pode passar. Estudos de caso provam que a patência do forame não foi necessariamente atingida em cada um destes casos, mas as perfurações são descritas como patência, no sentido literal; não necessariamente incorretamente( Figs. 2ª a c).
Fig. 2ª a e c. A intencional criação da patência apical pode ser conseguida à custa de uma perfuração apical em um canal curvo.
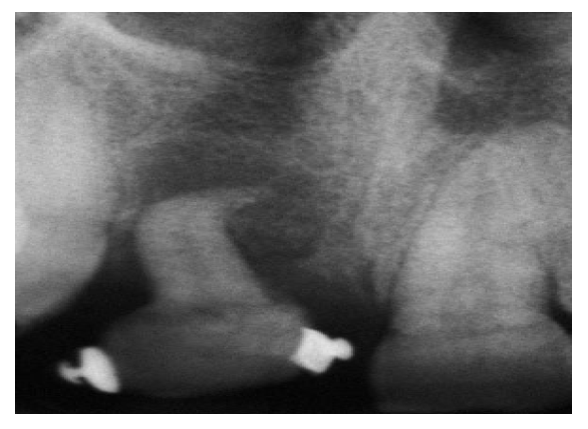
Fig. 2a A radiografia pré-operatória mostra uma acentuada curvatura do canal radicular na região apical.
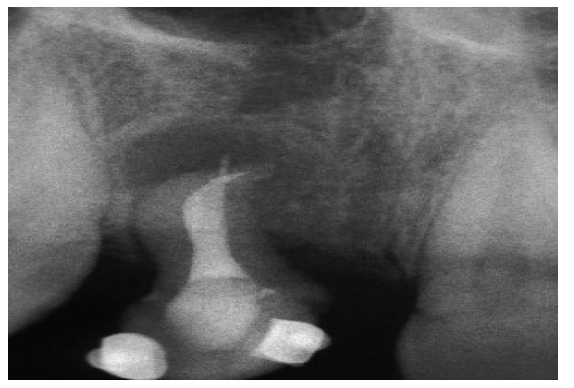
Fig. 2b A radiografia de verificação inicial, após obturação do canal radicular definitivo mostra uma perfuração apical após uma tentativa de alcançar permeabilidade.
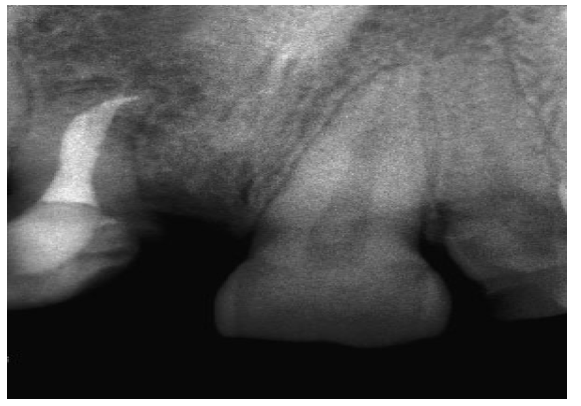
Fig. 2c Um ano verificando a radiografia. Apesar da perfuração, a lesão apical foi resolvida no caso presente.
12 TERRITÓRIO CRÍTICO
Por várias razões a parte apical da raiz do canal radicular pode ser considerada como território crítico, tanto pelos microorganismos e defesas do hospedeiro, mas também por endodontistas do ponto de vista clínico. Do ponto de vista biológico, a preparação deve ser considerada como ideal se:
-Todo ou quanto mais tecido infectado for removido do canal radicular e também do forame fisiológico.
– Se o canal radicular não estiver bloqueado apicalmente
– Nenhum material infectado foi transportado para o periápice.
Se é possível atingir todos esses objetivos é o que tem de ser questionado. Por outro lado, a pergunta deve ser levantada quanto à possibilidade ou não se esta preparação é ideal e necessária para o sucesso endodôntico ou até que ponto ela influencia a taxa de sucesso ou fracasso.
13 LINGUAGEM CORPORAL
A patência já existe se:
– A polpa ainda for vital, porque ela só pode penetrar no canal radicular via um “forame patente”.
– A periodontite aplical esteja presente, porque a patência é o único caminho que as toxinas bacterianas, mucopolissacarídeos e em alguns casos a própria bactéria podem penetrar dentro no tecido periapical, colocar-se em movimento e sustentar a inflamação.
Em um estudo em 36 dentes foi demonstrado que a patência do canal estava presente em todos os casos, embora estes (em 7 casos) não pudesse ser detectado em radiografias. Em 25% das amostras, a raiz do canal era histologicamente mais do que 0,2 mm (equivalente a dois tamanhos , ISO) mais largo do que radiograficamente era suspeito (25).
Um alto risco de fraturas do instrumento e a divergência da preparação do eixo da raiz foram reveladas em um estudo experimental em 46 raízes de canal não penetráveis. As descobertas de palpação provaram ser um bom indicador da penetrabilidade, se a ponta do instrumento não se envolver; isto indicava obliterações, embora da ponta do instrumento apontava para a possibilidade de penetração mais profunda (26).
Na maioria dos dentes com periodontite apical (11 de 12 dentes) nos quais as raízes do canal não puderam ser detectadas clinicamente ou por radiografia, imagem foi bem sucedida com contraste radiopaco médio (10%-solução de iodo de potássio iodeto). Em dentes sem periodontite apical, no entanto, nenhuma ligação com a região periapical foi descoberta em 13 dos 14 casos (27). Se o canal radicular não pudesse ser detectado na radiografia, a taxa de sucesso clínico para os 52 dentes foi 89% após dois 12 anos. A taxa de sucesso foi 97,9% se não houvesse periodontite aplical, mas apenas 62,5% se houvesse uma lesão periapical (28). Mantendo em mente o pequeno número de casos, pode ser concluído que a penetração do forame fisiológico provavelmente não é necessária para o sucesso do tratamento em dentes sem qualquer inflamação perirradicular.
15 PORTAIS DE SAÍDA: QUAL FORAM?
Nas discussões sobre o benefício e a necessidade de uma técnica de patência, é útil e necessário recapitular a anatomia da região apical (Fig.3 e 4). A representação clássica da região por Kuttler (29) foi expandida por Dummer entre outros (30). Além da simples constrição, podem haver vias cônicas para canais apicais sem uma constrição, multi-constrições ao estreitamento paralelo. Existem muitos estudos sobre o diâmetro pré-operatório da constrição apical e a anatomia da região apical, de acordo com a qual a secção transversal varia muito, dependendo da idade do paciente e do tipo de dente. Entretanto, é quase universalmente o-0,25mm ou mais (31). De acordo com Vertucci (32) e Morfis et al (33) o tamanho médio do forame principal (forame apical), dependendo do tipo de dente, é 210 μm (pré-molares superior) a 390 μm ( raiz distal dos molares inferiores).Kuttler 29 dá uma gama de 502-681 μm . O diâmetro na junção cemento-dentina varia de 292 a 233 μm de acordo com Ponce et al (34). Eles estudaram a região aplical de 18 incisos maxilares por meio de secções cortes histológicas. Eles descobriram o forame no lado mesial da raiz em três casos (Fig. 5a e b), no lado distal oito vezes, duas vezes sobre o lado do palato e apenas cinco vezes no ápice anatômico (vértice) da raiz. Isto é corroborado por Pineda e Kuttler (35), que também descrevem a localização lateral do forame apical em 70 a 90%. Os desvios da forame apical a partir do eixo longitudinal da raiz varia de 0,06 a 1,1 mm (36). Burch e Hulen (37) encontraram 78 a 98% forame apical lateral para ao ápice anatômico.
Baseado no exame de microscopia eletrônica de fora de 140 ápices radiculares de dentes extraídos, Gutierrez e Aguayo (38) demonstram com impressionante diversidade de imagem o formato da região apical, e especifica que somente 52 dentes tinha um único forame, os outros tinham de duas a cinco aberturas, as quais estavam localizadas a uma distância de 0.9 a 3.8 mm do ápice da raiz (Fig 6).O corte transversal da foramina medida do lado de fora da raiz é dado como 100 a 520 μm ( principalmente de 200 a 250 μm). A foramina acessória são menores, seu corte transversal varia entre 60 a 80 μm com um espectro de 26 a 200 μm (39).
Ainamo e Loe (40) usaram estereomicroscópica para estudar os ápices de 910 dentes e descreveram 9 foramina. Morfis et al (33) sempre achou mais de um forame apical em 213 dentes, com exceção das raízes palatinas dos molares maxilares e as raízes distais dos molares mandibulares. Uma outra descoberta interessante deste estudo é que nenhum forame principal pode ser encontrados em 24% dos pré-molares maxilares e 26% dos incisivos maxilares. Foramina acessórias foram encontradas em todos os dentes, a sua secção transversal média foi de 53,4 μm no caso dos pré-molares.
Canais laterais, secundária ou acessório foram encontra em 27,4% dos 1140 dentes, predominantemente na região apical, mas também no meio da raiz e bifurcação (41) (Veja Figs 4, 7ª e b).Duas foramina foram encontradas nas raíz mesial e mesiovestibular dos primeiros molares maxilar e mandibular (n= 1,097) em 87,06% e 71,15% respectivamente, haviam foramina acessória presente em 33% e 26% das raízes respectivamente e o formato do foramen era oval em 70% dos casos. Os diâmetros mais estreitos e mais largos foram em média de 0.2 a 0.26 mm em molares mandibulares, 0.18 a 0.25 mm em raízes mesiobucal e distobucal e 0.22 a 0.29 mm em raíz palatina dos molares maxilares (42).
Estes dados provam que na maioria dos casos clínicos, mesmo com instrumentação, patência e/ou preparação e limpeza do forame fisiológico, existem foramina apical adicional o lateral e furca com diferentes cortes transversais, nas quais a técnica de patência não é aplicada, observe nestas figuras, de acordo com Weine (43); a importância clínica de tais canais laterais e vias de ligação a região apical e periodonto lateral, precisa ser colocada em perspectiva; inflamação extra-radicular pode ser provocada e sustentada através destas conexões, mais claramente isto não acontece na maioria dos casos.
A posição lateral do forame apical em muitos casos evita problema de instrumentação além do forame fisiológico( Veja Figura 4). Se a constrição localizada lateralmente, uma instrumento fino é preferido, que trabalha e se endireita o lado do forame em direção a curvatura externa. Foi demonstrado que até mesmo usando uma lima de patência tamanho 10 para mensurável transporte do forame em um terço dos casos estudados (44).
O formato e tamanho da constrição apical também deve ser levado em consideração, se o diâmetro da constrição é 0.25mm, o tamanho da lima de patência ISSO 10, avançada 1mm além do forame somente teria um diâmetro de 0,12 mm na constrição dado conicidade de 2%. Assim haveria somente contato com a parede do canal em um ponto e os detritos e tecidos remanescentes não poderiam ser removidos de todas as outras áreas da parede. No entanto somente o forame principal seria instrumentado, este necessariamente não seria o mais largo, portanto presumivelmente o mais contaminado forame, mas o mais facilmente acessível de vários portais, não meramente portais de saída apical( Fig.8).
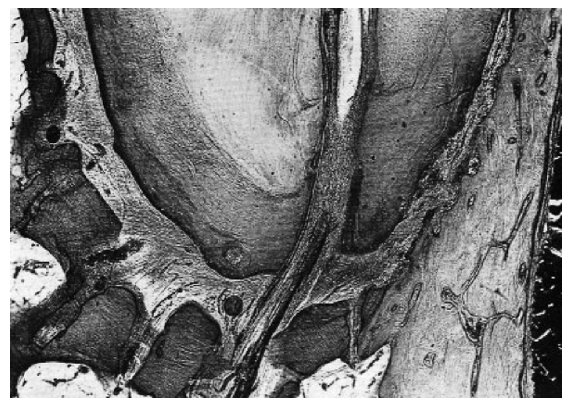
Fig. 3 Imagem histológica de uma “região apical clássica ‘’
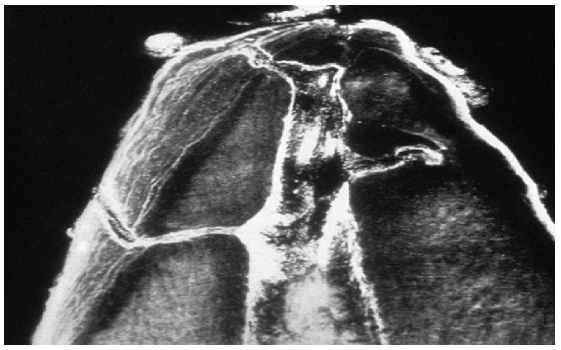
Fig. 4 As principais curvas do canal bruscamente pouco antes do ápice radiográfico, uma curva que seria muito difícil de ser instrumentada em muitos casos. Apesar da constrição apical tendo sido aprovada, a radiografia iria transmitir a impressão de que a patência ainda não foi alcançado. Quer ou não a patência foi conseguida só poderia ser verificado neste caso eletro metrically ou por um ensaio de ponto de papel (e quaisquer sintomas clínico paciente pode ter).
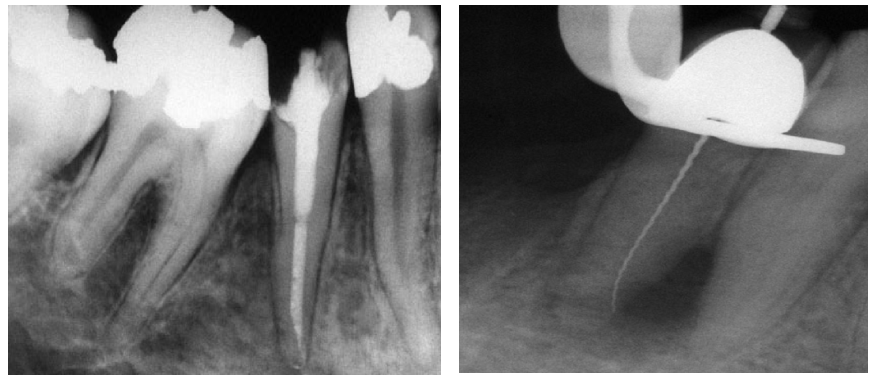
Fig. 5 a E e b. Em muitos casos, o forame apical tende a ser deslocado lateralmente em vez de ser na ponta da raiz.
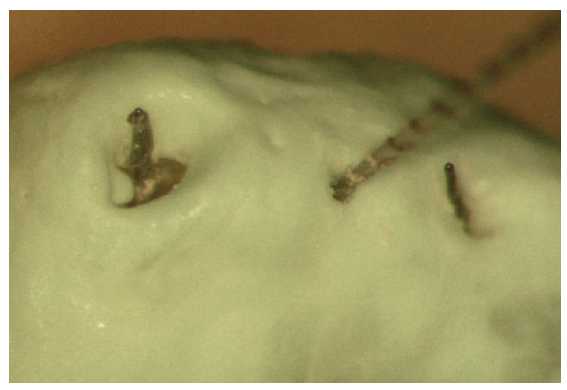
Fig. 6 A parte externa do ápice da raiz, muitas vezes mostra vários forames, cujo diâmetro é sujeito a grandes variações.
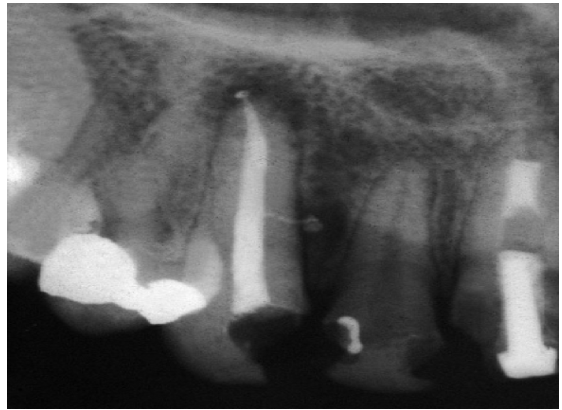
Fig. 7 a Canal lateral grande. Em casos isolados, um canal lateral grande pode levar ao desenvolvimento de periodontite localizada lateralmente de origem endodôntia. Visualização do canal lateral através, pressionado em cimento não permite tirar qualquer conclusão sobre a sua limpeza ou o aperto da obturação.
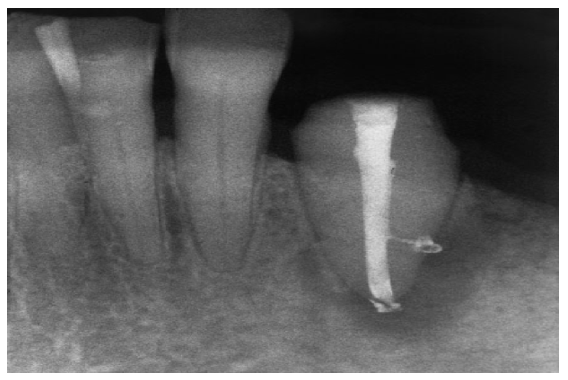
Fig. 7b Parcialmente cheio os canais laterais com ponto lateral associada a osteólise
Limpo, mas não puro?
Souza 4 discute a diferença entre a patência apical e a limpeza do forame. Ele afirma que a colonização microbiana dos então chamados “canais de cemento”, assim a porção da raíz do canal margeada pelo cemento e apical para a constrição foi demonstrada na literatura. De acordo com Cohen e Buns (45) existe bastante espaço para aproximadamente 80.000 estreptococcus no caso da necrose pulpar quando a preparação é feita até 1mm coronal para o ápice. Como eles estabelecem, isto é biologicamente inaceitável. O objetivo da técnica de patência deve ser manter o forame limpo de detritos, tecidos remanescentes e chips de dentina. Por outro lado, não pode-se presumir que o irrigante será eficaz no “canal cementário”. Para esta finalidade, alguns autores recomendam que um instrumento seja usado não apenas passivamente penetre no forame, mas também tenha contato com a área na constrição( isto é, ISO tamanho 20 e maior) para aumentar o efeito da limpeza. Entretanto, isto acarretaria o risco de super pressionar detritos porque o instrumento agora atua como um selo. Souza (4 ) recomenda usar uma lima de patência que seja tamanho 2 ISO menores do que o diâmetro do forame ou do que uma lima que gruda no forame. Além disso, isto somente garantirá a patência e ajuda a evitar uma acumulação de detritos, mas não limparia o forame e o canal cementário. (Fig. 9 ). Ele afirma que o bloqueio do forame não pode ser evitado pela irrigação apenas.
Para alcançar ambos os objetivos, Souza (4) recomenda assegurar a patência do forame com uma lima Kfile fina (objetivo mecânico) e usando um instrumento mais grosso com fricção no forame para limpar o forame e o canal cementário ( objetivo biológico) em alguns casos, por exemplo se uma lesão perirradicular persiste o qual não tem respondido ao tratamento incluindo a abordagem da patência, o forame precisa ser enlarguecido intencionalmente para destruir o biofilme na porção apical mais distante do canal radicular que agora é divergente de novo.A instrumentação excessiva apical deve se estender de 1 a 2 mm. Entretanto, a técnica de patência não é indicada como uma questão de princípio no caso da polpa vital. Isto é porque qualquer remoção do tecido saudável é basicamente inútil. No entanto partindo do princípio que os chips da dentina e do tecido seria transportado em uma direção apical e comprimido ali durante a instrumentação, Souza por fim recomenda o uso da técnica de patênco com instrumentos finos mesmo em casos vitais.
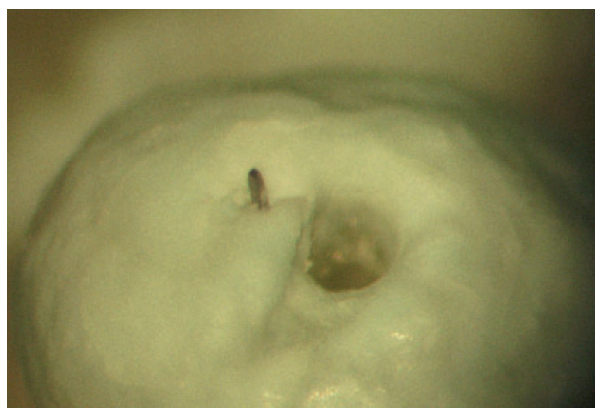
Fig. 8 O instrumento penetra no forame apical menor que é mais fácil de alcançar através de uma rota direta, o forame apical maior a abertura permanece a adição de instruções.
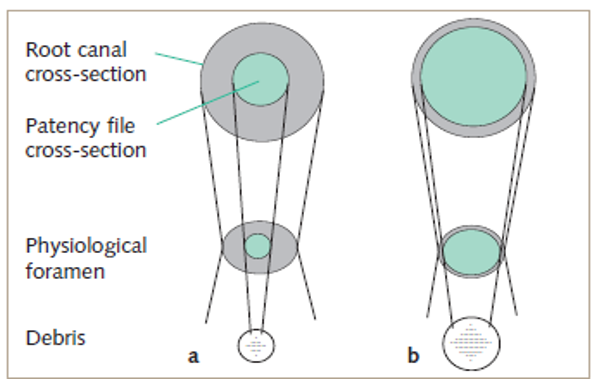
Fig. 9 Forame com instrumento que não tem parede contacto, detritos pouco se overpressed, a circunferência do canal da raiz no forame não está completamente trabalhado detritos é deixado para trás na parede do canal. Forame b com confortavelmente ajustado o instrumento, a parede do canal radicular está completamente trabalhada, o detritos é removido; mais detritos é extruído para região apical periapical porque do efeito do selo do instrumento.
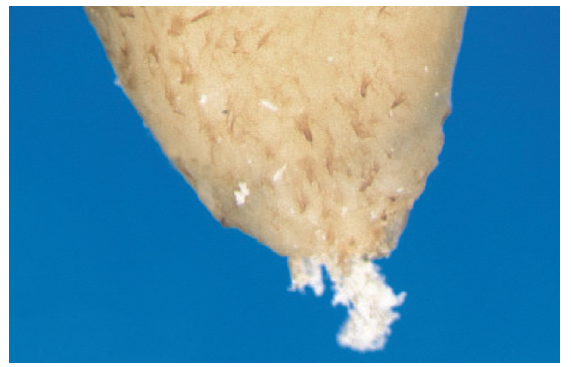
Fig. 10 Whether é ou não é de todo possível para evitar sobredosagem de detritos completamente sem obstrução apical parece questionável.
15 PAREDE. ONDE AS BACTÉRIAS FICAM ALOJADAS
Fukushima et al (46) estudaram a colonização microbiana de 21 dentes extraídos com periodontite apical assintomática clinicamente. Em 15 das 21 amostras examinadas por microscopia eletrônica de varredura, eles descobriram massas bacterianas na porção apical do canal radicular, mas eles não encontraram nenhuma massa na área do forame apical abaixo da constituição ou do lado de fora da raiz.
Em um estudo de luz e microscopia eletrônica, Nair (47) descreve a flora bacteriana de 31 dentes com lesões apicais( 30 granulomas, um cisto). As bactérias foram detectadas na lesão em cinco espécimes( lesões sintomáticas em cada caso), mas em outros dentes, os microorganismos intracanal ficaram separados da lesão por uma parede densa de neutrófilos polimorfonuclear(PMN) ou um ‘plug epitelial’ epitelial. Esta parede é interpretada como uma resposta quimiotática do PMNS para a invasão dos microorganismos ou seus produtos de degradação para o espaço periradicular. Entretanto, a formação de uma vedação apical por um obturador epitelial, provavelmente não pode de forma eficaz e permanentemente prevenir a fronte bacteriana de avançar para dentro do tecido periapical. Ricucci e Langeland 6 também fazem referência à parede do PMNs.
Em outro estudo de microscopia de luz eletrônica em 12 amostras de biópsia das lesões resistentes à terapia. Nair et al (48) descobriu microrganismos intra-radiculares em nove espécies, um canal lateral colonizado por bactérias em um caso, e microorganismos no forame apical em um caso.
16 EXTRUSÃO APICAL
A extrasão parcial das detritos e soluções de irrigação ocorrem em muitos casos durante a preparação (49). A ligação definitiva entre a profundidade de penetração da preparação dos instrumentos e da quantidade de material extruído tem sido demonstrada em vários estudos.
Lambrianidis et al (50) estudaram a quantidade de extrusão periapical, quando aplica-se a técnica de patência.(Fig 10).Trinta incisivos superiores foram instrumentados sem usar uma lima de patência e a quantidade de material expelido (detritos e irrigantes) foi medido. A constrição apical foi então intencionalmente alargada com uma lima tamanho 30 se reextendendo por 3mm, e uma nova construção foi criada coronalmente por uma técnica step-back. A irrigação do canal radicular foi repetida e a quantidade de material expelido foi medido de novo.Durante a preparação, uma lima de patência clássica que manteria o forame aberto não foi usada em nenhum dos dois grupos. Os autores encontraram diferenças significantes na quantidade de material expelido, mais detritos e fluído irrigante sendo super-pressionado em casos onde a constrição ficou intacta e não foi alargada. Eles atribuem o resultado aparentemente paradoxal a formação de um plug apical dos chips de dentina durante a stepback, que bloqueou a extrusão para o periápice. Torna-se claro que este estudo contrasta com a técnica de patência original, que afirmava que objetivo é prevenir tal plug a se desenvolver. Assim sendo, os resultados não podem ser transferidos para a técnica de patência clássica.
17 CONDIÇÕES MÉDICAS DE PATÊNCIA E CONDIÇÕES GERAIS
Apesar das supostas vantagens e desvantagens das técnicas de patência detalhadas acima, alguns problemas médicos gerais dos pacientes não devem ser ignorados quando se escolhe a técnica de preparação adequada. Baseado no conhecimento atual, o uso da técnica de patência deve ser evitado nas seguintes situações.
• Pacientes que estejam tomando bisfosfonatos ou que os tomam em anos recentes, nestes paciente irritação externa pode claramente promover a formação de osteonecrose, e desta forma irritações marginal e apical durante o tratamento do canal devem absolutamente serem evitadas. O maior cuidado deve ser tomado quando se coloca o grampo e o dique de borracha para não irritar a gengiva. A instrumentação excessiva apical do canal deve definitivamente ser evitada (51,52).
- Pacientes com distúrbios de coagulação ou pacientes recebendo tratamento anticoagulante, mais uma vez qualquer instrumentação excessiva do canal deve ser cuidadosamente evitada durante a preparação do canal (53).
- Pacientes que necessitam de proteção apical contra bacteremia transitória durante ou após o tratamento do canal. Bacteremia como uma consequência do tratamento do canal pode acontecer especialmente como um resultado da instrumentação excessiva, mas também após a instrumentação puramente intracanal (54,)56.Esta é a razão pela qual a técnica de patência não deve ser usada em pacientes que requerem proteção antibiótica prévia ao tratamento de canal, de acordo com as recomendações da Associação Americana do Coração (57). A categoria dos paciente são:
- Paciente com válvula cardíaca( prótese biológica e mecânica).
- Pacientes que já tiveram endocardite infecciosa
- Pacientes com doenças congênitas
- Defeitos cardíacos cianóticos que não foram operados ou paliativamente com problema pulmonar sistêmico.
- Defeito cardíacos que foram operados, mas ficaram sequelas.
- Nos primeiros 06 meses após a cirurgia para defeitos cardíacos, usando material protético.
- Pacientes com transplante cardíaco que desenvolveram valvulopatia cardíaca. A técnica de patência é ainda mais contra indicado no caso de (58):
- Pacientes imunossuprimidos seguida de transplante de órgão, citostática ou radioterapia na área da mandibular.
- Pacientes com quadril artificial.
18 PLUG DENTINAL OU PATÊNCIA COM POLPA VITAL
Quando um dente vital com pulpite irreversível está sendo tratado, pode se presumir que precauções assépticas são mantidas( particularmente é rigoroso a utilização de um dique de borracha), ausência de microrganismo será encontrado na porção apical da raiz do canal radicular ou no tecido perirradicular. Portanto, o tratamento objetica exercer um efeito terapêutico específico na saúde, ou no máximo, o tecido inflamado parece não ser nem necessário nem desejável. Além disso, deve se dar preferência à mínima instrumentação excessiva em termos da técnica de patência ou para o risco de bloqueio mínimo da região apical com chips de dentina não infectada deve ser discutido nestes casos. O bloqueio apical com chips de dentina autólogos em tais casos já foi discutido no início de 1930 (59).
Foi demonstrado em estudos posteriores que em muitos casos, os chips de dentina são deixados para trás no canal radicular e que alguns destes são transportados apicalmente durante o decurso da preparação. Este plug apical pode também conter tecidos remanescentes( Fig11). O coto pulpar remanescente no canal , incluindo o depósito de chips de dentina gerado intra- operatório, pode auxiliar na cicatrização em termos de formação de tecido apical rígido/ duro (60,62), um conceito que já foi exposto por Ketterll (63) ( Técnica de ombro de Mayer). O vazamento apical( cálcio radioativamente rotulado) diminuiu com o aumento e preparação da formação de um ‘plug apical’ dos chips da dentina (64).
Por outro lado; ElDeeb et al (65 ) não pode detectar fechamento apical melhorado na presença de um plug dentinal, mas a irrigação e a obturação puderam ser confinadas para o lúmen do canal significativamente melhor. Super pressão do irrigante foi reduzido de 66,7%( sem constrição, nenhum plug) para 17,5 % ( constrição intacta, e não plug) ou 5,8% dos casos ( constrição intacta e plug dentinal) extravasamento excessivo foi evitado em todos os casos. Pitts et al (66) confirmaram isto em estudos com animais, um plug dentinal provou ser mais estável do que um plug feito de hidróxido de cálcio. Ambos levaram à cura parcial e a posição de cemento em todos os casos .Entretanto, Ca( OH)2 tinha sido lavado depois de 9 meses em muitos casos.
Por outro lado, em dentes extraídos submetidos a teste de penetração com corante, Jacobsen et al (67) descobriu pobre selagem apical após artificial preparação dos plugs dentinais apicais e sua obturação lateral com gutta- percha condensada e com selador que nos canais que podiam ser instrumentados para completar o comprimento trabalhado exatamente através da completude da preparação em todos os canais, a patência apical somente foi checada antes da preparação usando uma lima de patência ISO 10. Exame de microscopia eletrômica de varredura, revelou que os plugs dentinais não eram homogênios, com numerosas cavidades ocas no interior e entre os plugs e a parede do canal.
Em um estudo animal em 134 canais radiculares, após extirpação vital com mais de um instrumento por 2 mm, Benatti et al (68), alargou o forame intencionalmente usando tamanhos 40, 60, 80, obturados 1 a 3 mm aquém do forame, e examinado histologicamente a região apical depois de 3 a 120 dias. Uma lesão periapical se desenvolveu em 2 casos. Após 3 dias o nervo danificado respondeu com reações inflamatórias graves. Entretanto, após apenas 30 dias, foi descoberto em muitas espécies que o tecido conjuntivo tinha crescido dentro da porção apical não obturada do canal e formou um coto pulpar artificial. Após 120 dias uma fina camada de cemento pode ser vista adicionalmente sobre a parede do canal, em ausência de inflamação induzida bactérias e infecção, apesar do alargamento e destruição da constrição apical e danos no tecido periapical, boa cura foi alcançada, o que também envolveu o osso periapical traumatizado.
Em outro estudo in vivo em animais, ficou demonstrado que a instrumentação excessiva em raízes de canais não infectados alcançaram melhores resultados com instrumentos tamanho 80 do que com os tamanho 40. O fato de que melhor regeneração se seguiu(formação de cemento, crescido dentro do tronco da polpa composta de tecido conjuntivo, reorganização do osso), apesar de grande trauma de instrumentação, é interpretado pelos autores como o significado de que maior alargamento com melhor limpeza do sistema de canal, capacita o Hidróxido de Cálcio curativo a adaptar melhor ao tecido e propicia mais espaço para crescimento interno do tecido enquanto ao mesmo tempo elevando o risco de extrusão do curativo (69).
Em estudos com animais Tronstad (60) investigou a resposta do tecido apical do canal radicular com intencional entupimento com chips de dentina não infectado. Vinte e dois de 24 dentes tratados foram tidos como bem sucedidos. Em muitos casos a histologia revelou completa liberdade de inflamação e aposição de tecido duro similar a cemento nas paredes na região apical dos canais e a interface entre os chips da dentina e o tecido apical vital.
Em alguns casos, esta deposição de cemento também foi observada em canais laterais. Dos 21 dentes nos quais a pulpectomia e a obturação do canal foram realizadas sem um tampão apical de dentina, somente 10 dentes puderam ser avaliado com sucesso no tratamento, em seis desses sucessos, um plug dentinal não intencional foi desenvolvido, apesar do máximo de cautela.
Horsted e Nygaard – Ostby (70) realizou extirpação vital na distância ou tamanho do forame apical em 20 dentes, então preparou e obturou os canais a aproximadamente 2 a 4 mm coronal até o ápice radiográfico. Este exame histológico realizado, após de 2 a 10 meses mais tarde, mostrou crescimento interno de tecido conjuntivo na cavidade abaixo do material obturante.
Osswald e Fried Rubber daman (58) , preparou sob isolamento absoluto canais radiculares de dentes vitais de gatos, intencionalmente instrumentado sobre- instrumentação em 1 mm com uma lima Kfile tamanho 50 com frequente irrigação com solução salina estéril. Eles assim alargaram o forame, para depois obturar está perfuração com uma camada de chips autólogo da dentina com 1mm de espessura. A outra parte da raíz do canal foi obturada com gutta – percha e o dente foi selado coronalmente. A avaliação histológica após 3, 5 ou 8 meses demonstrou cura mais rápida com osso e cemento ,e apenas mínimos sinais de inflamação ou ligamento periodontal intacto, quando o forame foi obturado com chips da dentina. Os dentes de controle também foram instrumentados excessivamente mas obturados sem um plug e houveram infiltrações crônicas e agudas, fragmentos de seladores, sinais de fagocitose, mas também células similares às osteoblastos. Havia poucas reações inflamatórias nos checados 8 meses do que após 3 ou 5 meses, mas havia ainda mais sinais de inflamação pronunciada do que em dentes com plug apical. De acordo com as conclusões dos autores, o traumatismo causado por instrumentação excessiva ( dado a parte vital e a raíz do canal não infectada ) é seguida por cicatrização periapical se as dentina são compactos na região apical. Além disso, estes podem impedir a superextensão do material obturador.
Se a formação de um barreira apical feita de uma substância autólogo foi realmente um sucesso, iniciado em um canal radicular não infectado, isto teria que ser considerado como a melhor vedação apical com material separado de obturação e tecido vital autólogo. Estudos experimentais in vivo demonstraram que isto é possível. Se os resultados podem ser reproduzidos em condições clínicas tem que ser questionado em qualquer evento, a evidência para isto não está disponível. Isto é o porque muitos autores estabelecem que, quando lidamos com polpa vital, deixar um tronco de polpa vital para trás em uma porção apical da raiz do canal não prejudica a cura ou reduz o sucesso, mas tende a promover a cura e a formação de um novo cemento. Este tronco pulpar seria removido ou traumatizado se a técnica de patência fosse aplicada. Entretanto, sob obturação após completa extirpação pulpar ,bem quanto a produção de um plug dentinal apical ou deixá-lo no lugar não reduz a taxa de sucesso e a boa cura pode ser confirmada histologicamente.
Como o sucesso do tratamento do canal em casos não infectados, assumindo os métodos assépticos não seja dependente da extensão parcial de preparação e obturação, o uso da técnica de patência provavelmente não será refletida negativamente no resultado do tratamento. Entretanto, esta é uma especulação e não prova suficiente. Nenhuma vantagem clara desta técnica não-infectada pode ser endodonticamente identificada.

Fig. 11 Tampão apical de chips de dentina e tecidos remanescentes. Se um canal está infectado, este chips também contém microorganismos. É claro para ver que os chips não fornecem uma parede consistente para vedação do canal radicular.
19 AGITAR AS MÃOS
No tratamento da polpa necrótica infectada, determinando o comprimento trabalhado, é extremamente importante para o sucesso do tratamento. O debate sobre este tema entre as alternativas de deixar o tecido necrótico, na parte mais apical da raiz do canal ou transportar o tecido infectado para dentro do tecido periapical quando estiver atravessando ou estiver instrumentando. Tem sabido há muito conhecido que a extrusão do tecido remanescente detritos e dentinais durante a preparação leva à inflamação apical, e pode causar dor e impede a cura (71- 74).
Num estudo em dentes de cães , Holland et al (75) investigou o processo de cura apical em dentes com e sem patência. Quarenta incisos vitais e pré-molares foram trepanado sob uma instrumentação excessiva com instrumentos de tamanho 25 para atingir o crescimento interno do tecido conjuntivo para a raiz do canal. Após sete dias o tecido crescido internamente foi deixado em 20 dentes ( não faziam parte do grupo de patência ), no grupo de patência o tecido foi removido. As raízes dos canais foram obturados com gutha- percha condensado lateralmente e com cimento Grossman ou um selados baseado em Ca (OH)2 (Sealer Plus). O exame histológico 60 dias após o tratamento mostrou resultados mais significativos para o grupo de não patência do que para o grupo de patência, o selador Ca(OH)2 foi bem melhor do que o cimento Grossman. No grupo Ca(OH)2 sem patência do forame principal e os canais laterais foram frequentemente selados apicalmente por neocemento, no grupo Grossman nova formação de cemento foi mais rara e o tecido necrótico foi detectado mais frequentemente em canais laterais, o ligamento periodontal apareceu bem organizado. A combinação de Ca(OH)2 e selador patência também levou para a formação de novo cemento e biológico entupimento de muitos canais laterais. Entretanto, nenhum plug de cemento foi visível na foramina principal. Reações inflamatórias no tecido periapical foram vistas no caso de super obturação. Quando o cimento Grossman foi usado como um selador no grupo de patência, tecido necrótico e reações inflamatórias foram detectadas com mais frequência. O fechamento biológico do canal principal não ocorreu em nenhum dos casos.
Usando 35 dentes extraídos com canais infectados( abscesso apical crônico ou aguda) e dez dentes de controle com polpa vital, Gutierrez et al (76) estudou o efeito da instrumentação excessiva de menos que 0,5mm ( 20 canais) até lima ISO 40 e a instrumentação excessiva com super extravasamento ( 15 canais). Após a instrumentação excessiva intencional com alargamento do forame, houveram microorganismos periapicais do lado de fora da raiz em 66,6% dos dentes ou nas lâminas cortantes dos instrumentos mais prolongada ausência de microorganismos foram descoberta no exterior das raízes neste estudo, concluindo que as bactérias devem ter sido empurrados para fora do forame sempre que uma lima penetrava o ápice de um canal de raiz infectada (Fig 12).
Izu et al (77) chegou a um resultado contraditório em um estudo com o uso da lima de patência contaminada com Streptococcus sanguis em um tratamento de canal preenchido com Naocl 5,25% não provocou nenhuma contaminação microbiana do periápice. Foi suspeitado que a quantidade e a concentração de solução irrigante encontrada no canal eram o suficiente para eliminar os microorganismos, achados nos instrumentos. Deve ser notado, entretanto, que isto envolveu uma única instrumentação excessiva por 2 a 3mm após a conclusão da preparação. Assim, as condições clínicas foram apenas incompletamente, porque repetiu o mínimo sobre instrumentação e recomendado.
Em um estudo histológico, Ricucci e Langeland (6) examinaram biópsia de amostras de ápices radiculares com tecido adjacente dos dentes tratados endodonticamente nos quais apitectomias ou extrações tinham sido realizadas. As medidas endodônticas foram confinadas para dentro do canal no caso de 43 raízes, e obturação excessiva ocorreu em seis casos. Nestes casos uma reação periradicular inflamatória severa puderam sempre ser detectadas. Onde as medidas foram confinadas para dentro do canal, dependendo das descobertas básicas, havia tecido de polpa inflamado, em alguns casos ainda vital, e o ligamento periodontal livre de inflamação (casos vitais )mais também variando de grau de reações inflamatórias no tecido perirradicular( casos necróticos). No presente estudo, no entanto, o tecido pulpar que ainda era vital pode também ser visto na raiz do canal em vários casos( 6 dos 16), mesmo quando uma lesão radiográfica ocorreu. Nos outros 10 casos, o tecido necrótico foi achado na porção apical da raiz do canal na junção com o ligamento periodontal, o qual foi rodeado por uma camada densa de polimorfonuclear (PMNs) , neutrófilo, granulócitos. Os autores recomendaram sempre estabelecer o comprimento de trabalho até o forame fisiológico, porque isto é onde a menor superfície da lesão deve ser encontrada. Na opinião dos autores, a técnica de patência viola os princípios de cura da lesão porque o tecido não lesado é incisivamente penetrado e a área da lesão é alargada.
Em dentes com uma constrição apical alargada ou destruída( instrumentação excessiva por 2 mm com instrumentos tamanho 15 a 30) Tinaz et al (78) descrevem mais extrusões apicais com o aumento do diâmetro apical. Se o curativo intra- canal ( Ca(OH02) CHX como um gel ou pasta) foi removida usando uma lima de patência, uma menor quantidade de medicação foi deixada na parte apical da raiz do canal do que no grupo comparative de não- patência (79). Entretanto, raízes de canais plenamente limpos não podiam ser alcançadas desta maneira. O hidróxido de cálcio ou o curativo são afrouxados pela lima de patência e eles podem ser transportados para fora mais facilmente pela solução de irrigação. Os autores recomendam o uso de um instrumento de patência para remover o curativo.
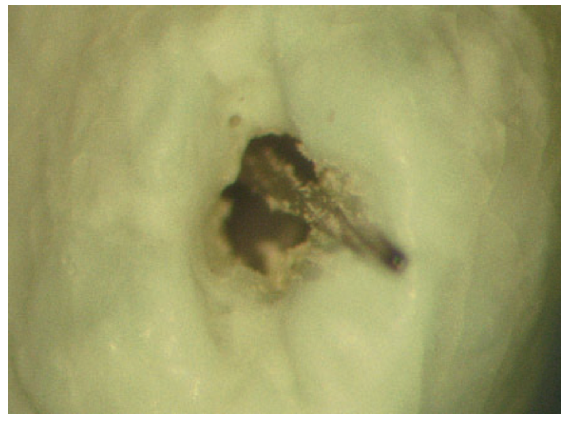
Fig. 12 A imagem mostra claramente que o instrumento (ISO 10 ) está contaminado com detritos, e transporta está para o periápice mesmo que a raiz do canal seja preenchida com hipoclorito de sódio. Na área de a constrição, detritos permanecem, apesar da técnica de patência a constrição apical não é limpa.
20 SOB INSTRUMENTAÇÃO
Se o comprimento de trabalho e assim a profundidade de penetração do instrumento são limitados para o forame fisiológico no caso do endodontico infectado, lá permanece, dependendo da sua localização 1 a 3 mm de distância da porção contaminada potencialmente da raiz do canal que não for instrumentada e nem mecanicamente limpa. Isto é descrito também como um “ canal cementário” por alguns autores. Sob certas circunstâncias isto pode significar que uma quantidade considerável de microorganismo são deixados para trás, os quais tem mais ou menos acesso ao tecido periapical( e assim também bastante substrato para sobreviver). Nair (47) demonstrou em um estudo de microscopia eletrônica que as bactérias podem sobreviver por muito tempo na constrição parcial em dentes obturados com lesões periapicais. Fukushima et al (45) descobriu bactérias entre o final apical da raiz de canal obturado e o forame apical em 60% dos casos.
Langeland (80,81) , Lin et al (82) bem como Ricucci e Langeland (6) por outro lado, mostrou que a parte apical da raiz do canal frequentemente contém tecido que ainda é vital, mesmo no caso de necrose pulpar e periodontite apical, a qual é a causa de parecer sensível confirma o tratamento ao nível da constrição. Isto também se aplica para os canais acessório e lateral, na área onde eles saem do canal principal, a aparência histológico é de fato a mesma, mas existe tecido vital elevado à medida que a distância do canal principal aumenta.
21 COMPRIMENTO TRABALHADO E DOR PÓS-OPERATÓRIA INCLINAÇÃO COM INSTRUMENTAÇÃO EXCESSIVA
Os microrganismos desempenham função importante na etiologia da dor pós- operatória (72,83,84), mas também aquela irritação mecânica do tecido periapical no evento da instrumentação excessiva pode levar à dor de curta duração como expressão de inflamação aguda. A quantidade de detritos pressionada para dentro do espaço periapical varia consideravelmente e depende parcialmente da técnica de preparação, e menos escória é pressionada em excesso se as técnicas de crown-down são usadas assim imediatamente, avançando o comprimento trabalhado (85).
Torabinejad et al (86) avaliou 2.000 registros de tratamento de dentes com polpa vital para identificar fatores que correlaciona-se com o incidente da dor pós operatória. As dores pós-operatória foram documentadas em mais da metade dos casos e não houveram tais incidentes para a outra metade dos casos. Instrumentação em excesso leve com instrumentos finos durante a preparação e tendo medidas radiográficas não teve influência no incidente da dor pós-operatória, a proporção com dor pós-operatória foi aproximadamente 50% em ambos os grupos.
Em um estudo clínico envolvendo 627 dentes com polpa necrótica ou exigindo re-tratamento, onde dores pós-operatória ocorreu em 15,2% dos casos. As dores variaram de leve (10%) à moderada (3,3%) e severa flare ups (1,9%) . A instrumentação foi acompanhada de irrigação com NAOCl (2,5%) e um curativo de Ca(OH)2 e paramonoclorofenol canforado. A patência foi alcançada e mantida após cada etapa da preparação com um “pequeno” instrumento posicionado na medida do ápice radiográfico. As dores foram frequentes com dentes sintomáticos sem lesões periapicais. Entretanto, nenhuma outra correlação foi encontrada (87).
Em um ensaio clínico envolvendo 245 pacientes, 21% relatou dor leve, 15% moderada e 7 % severa após preparação. A incidência da dor foi mais elevada após ( não- intencional) instrumentação excessiva ( não há informação sobre o comprimento da instrumentação excessiva) do que quando a preparação foi confinada ao canal nenhuma outra correlação foi encontrada (88).
Uma incidência mais elevada de dor pós- operatória foi encontrada em casos de extrusão de material obturante do que quando obturado acima de 1 mm coronal até o ápice radiográfico (89).
Em experimentos com ratos, tamanhos ISO 08 até 20 foram usados para instrumentar excessivamente e intencionalmente por 1 a 2mm além do forame apical. Metade dos animais receberam uma injeção subperiosteal de dexametasona, a outra metade uma injeção de solução salina. No grupo de solução salina reações inflamatórias severas no periápice foram encontradas no caso do tecido necrótico e também acompanhando a extirpação vital (90).
22 BLOQUEIO APICAL
Qualquer discussão sobre os pós e contras das técnicas de patência deve fazer considerações sobre os riscos e problemas tanto da instrumentação excessiva quanto da sub- instrumentação. Se a profundidade de penetração dos instrumentos fica limitada precisamente no forame fisiológico, há um risco que esta será bloqueado por pedaços da dentina apicalmente pressionados e remanescentes do tecido. Este risco depende da técnica de preparação entre outros fatores. Em uma comparação entre 08 técnicas de preparação diferentes realizadas em dentes extraídos, a técnica Stepback foi a pior (85) , um total de 52 dos 208 canais foram bloqueados e o material expelido apicalmente foi encontrada em 169 canais. Se possível mantenha o forame livre de maneira previsível e reprodutível sem bloqueio e extrusão tem de ser questionados..
Em um estudo animal, Holland et al (91) examinou histologicamente a região periapical após bloqueio apical intencional dos canais infectados com pedaços de dentina. Quarenta canais de cães foram trepanados e deixados abertos por cinco dias, desinfectados e obturados. O bloqueio apical com pedaços de dentina infectados antes da obturação ocorreu em metade dos dentes. Neste grupo, a histologia após 90 dias revelou um espaço de ligamento periodontal alargado na saída do canal principal. Este espaço era preenchido com tecido de granulação. Além disso, micro- abscessos assim com reabsorção óssea e do cemento foram detectadas. Estas reações não foram descobertas na foramina lateral destes dentes. Os autores concluíram que o processo de cura nos dentes com periodontite apical pode ser impedido por um plug(obturador/ tampão) apical da dentina infectada. Torneck et al73 também achou resultados similares. Por contraste, quando se trata um dente vital com tecido não infectado, deixando um coto pulpar apical no lugar ou com pedaços de dentina autólogos, provou não ser problemática e a cura não foi afetada 60. Yusuf 92 realizou um exame histológica de amostras de biópsias de 284 tecido periapical e descobriu materiais estranhos, ou corpos estranhos em 33 % dos granulomas. Uma reação inflamatória aguda foi frequentemente encontrada bem como tecido de cicatrização em poucos casos ao redor do cemento e pedaços de dentina; os quais foram descobertos em 45 amostra de biópsias. No seguinte de 556 re-tratamento, houveram 195 dentes(35%) com evidência de instrumentação excessiva e obturação excessiva.
A proporção com cura completa foi muito mais baixa no grupo de dentes instrumentados em excesso e obturados em excesso(36%) do que em grupo com instrumentação limitada para o lúmen do canal e com obturação(62%).Em 228 dentes, foi (documentado) instrumentação excessiva( ápice limpo); estes dentes tiveram uma maior frequência de lesões periapicais (93).
O fato que super pressionado apicalmente tecido infectado do canal radicular( tecido necrótico,cemento e pedaços de dentina) podem iniciar uma inflamação perirradicular agora é aceito.
23 PATÊNCIA E OBTURAÇÃO EXCESSIVA
Monset et a (94) relatou que após canais de dentes extraídos tivessem sido preparados com tamanho 35 e obturados com gutta-percha e cimento, menor penetração foi observada em teste de corante quando a patência tinha adicionalmente sido criada com um instrumento ISO tamanho 15. Nenhum detalhe da técnica de obturação foi dada. Em um estudo de modelo matemático Gimlin et al (95) mediu a tensão de condensação na condensação vertical da gutta- percha nos modelos de canais sem patência apical. Se o canal fosse apicalmente patente, a concentração de stress do forame, o que era atribuído ao gutta-percha sendo pressionado dentro do forame. Isto leva a melhor adaptação da gutta-percha às paredes do canal, mas eleva o risco de fraturas da dentina. Onde o ápice foi bloqueada a distribuição uniforme através do canal inteiro se seguiu.
Estudos retrospectivos de taxas de sucesso do tratamento endodôntico mostraram na maioria dos casos uma taxa radiográfica mais baixa quando materiais de obturação foram expelidos via ápice. Se esta maneira de fazer foi somente causada por obturação excessiva ou (também) por prévia instrumentação excessiva, isto não pode ser dito nestes estudos(Fig. 13 a a c). Sem dúvida a extrusão do material de obturação pode ser feita até sem o uso da lima de patência(Figs. 14 a e b).
De acordo com Wu e Wesselink (96) as melhores taxas de sucesso são reportadas para casos nos quais a obturação do canal termina de 0 a 2mm coronal ao ápice radiográfico. Entretanto, isto inclui obturações além do forame fisiológico porque este usualmente fica de 0.5 a 3 mm coronais ao ápice radiográfico. Isto significa que uma proporção não determinável de obturação do canal, os quais terminam radiograficamente 1 mm do ápice, já projeta- se além do forame fisiológico.
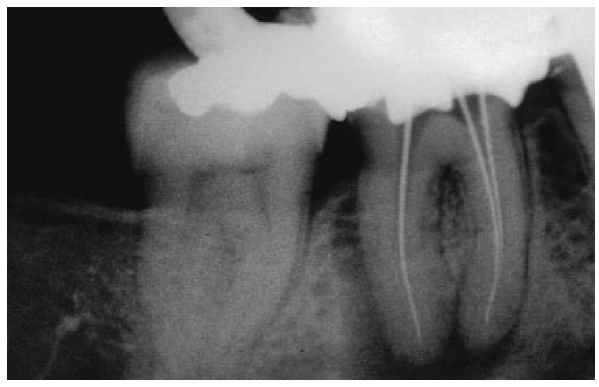
Fig. 13 a A radiografia com a lima mostra uma lesão perirradicular extensa.
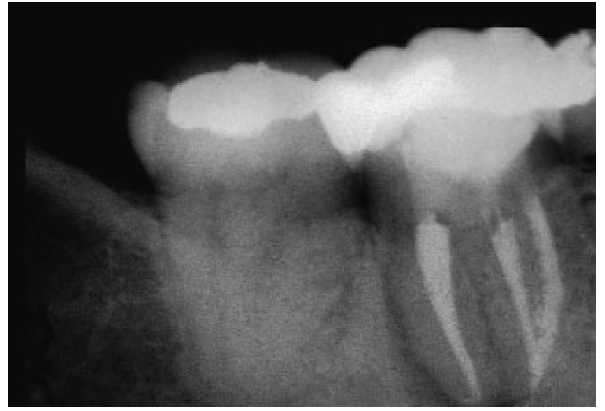
Fig. 13b A radiografia de verificação após a obturação mostra extrusão leve do após a utilização da técnica de desobstrução.
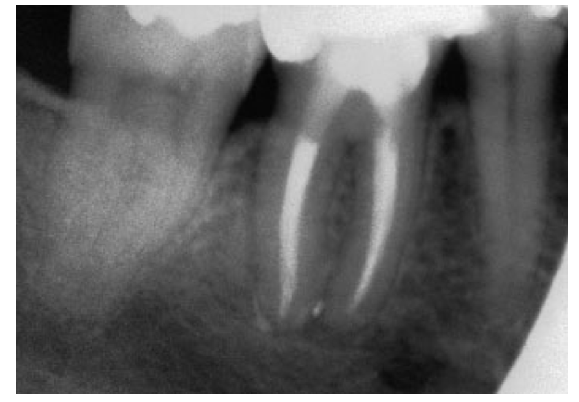
Fig. 13 c A radiografia de verificação mostra 2 anos de reparo bom.
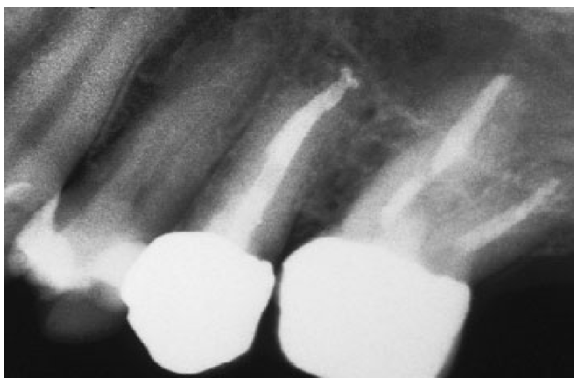
Fig. 14 a Apesar de não trabalhar com patência arquivos ocorreu, houve ligeira extrusão cimento. A verificação de 2 anos mostra um cura da região periapical.
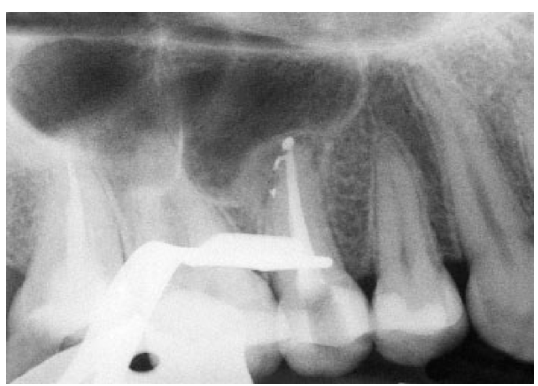
Fig. 14 b Patência do sistema de canal radicular, ligeira extrusão do cimento pode ser visto em ambas canal principal e os dois canais laterais.
24 ALISAMENTO DO CANAL E TRANSPOSTE APICAL COM A TÉCNICA DE PATÊNCIA
Goldberg e Massone (43) preparou 30 incisivos laterais superiores com instrumentos de aço tamanho 10,15,20 e 25 pré-curvados 1 mm além da constrição apical. No segundo grupo instrumentos NiTi de tamanho 15 a 25 foram usados ao invés de limas de aço após o tamanho ISO 10. Todos os instrumentos foram movidos três vezes através do forame. Após o uso de cada instrumento o formato foi fotografado e as imagens foram medidas. Dezoitos das 30 espécies(60%) mostraram transporte apical do forame, não houve diferença entre os dois grupos. Em ambos os grupos, o transporte do forame foi identificado em 55 % dos nove casos após trabalhar com instrumento tamanha 10. Após a instrumentação com ISO tamanho 15, os valores aumentaram para 33 % e 11 % respectivamente, após preparação por tamanho 20 por outro 11 % em ambos os grupos. Os autores atribuíram este alisamento demonstrável apesar do trabalho ao fato que, até mesmo em canais retos, ou aparentemente somente um pouquinho de curvatura, os canais com um forame localizado lateralmente, o instrumento sempre toca e trabalha a curvatura apicalmente externa mais do que a interna de forma que esta pode levar ao transporte até mesmo quando usa-se instrumentos pequenos e flexíveis.
Em um estudo sobre cânulas plásticas, Weine et al (97) indicaram que, quando o forame é penetrado ele é alargado na direção da curvatura externa, resultando em uma então chamada “lágrima apical”.
Tsesis et al (98) preparou os canais de 40 molares mandibulares extraídos e molares maxilares usando quatro técnicas diferentes, força balanceada e velocidade da luz/ leve.( Tecnologia San Antonio, TX USA) ambas com e sem patência. As preparações foram feitas até o tamanho 40, uma sequência stepback tamanho 70 foi feita. Nos dois grupos de patência, a patência do forame foi assegurada com tamanho 10k após cada tamanho de instrumento. O grau de preparação induziu ao endireitamento da raiz do canal e foi acertada por radiografias digitais pré-operatórias e pós- operatórias. Nenhuma diferença significativa entre os grupos foi encontrada, nem em relação à perda de comprimento de trabalho ou em relação ao alisamento do canal.
25 REPERCUSSÕES SISTÊMICAS
Baumgrtner et al (99) analisaram amostras de sangue após preparação dos dentes com polpa vital após instrumentação excessiva por 1 a 3 mm. A irrigação foi feita com Naocl 5,25%; após a instrumentação excessiva , a bacteremia de origem endodôntica foi detectada em um dos 6 casos; as outras amostras foram negativas. Bender et al (100,101), mostrou que a probabilidade de bacteremia é mais elevada após a instrumentação excessiva (15%) do que quando a preparação é confinada ao canal (0%). Entretanto, Debelian et al (102), não achou diferença em relação a incidência de bacteremia seguido de instrumentação por 1 mm antes ou 2mm apical para o forame. Os autores atribuíram isto ao fato que os pedaços de dentina infectados podem ainda serem pressionados sobre o forame, até mesmo se a preparação é limitada e a instrumentação é confinada ao canal.
26 PATÊNCIA E SUCESSO CLÍNICO
Não existem ensaios clínicos explícitos sobre a influência das técnicas de patência na taxa de sucesso. Em um estudo retrospectivo, Hoskinson et al (103) examinou 200 dentes com 489 raízes de 4 a 5 anos pós- operatório. Os dentes tinham sido tratados de acordo com dois protocolos diferentes, em ambos os casos com a técnica de patência(instrumento tamanho 10, “sempre que possível”). As taxas de sucesso para os dois grupos foram 78% e 76% respectivamente. Entretanto, a influência da técnica de patência no sucesso não pode ser confirmada devido à falta de grupo de controle.
Um outro estudo lidou com taxa de sucesso dos tratamentos nos quais o canal não podia ser completamente aberto. Setenta dentes com canais obliterados( isto é, menos que um terço da raiz do canal foi penetrável e nenhum lúmen do canal pode ser detectado nas radiografias) foram submetidos a tratamento endodôntico puramente ortograduado foi feito e 51 casos foram acompanhados após de 2 a 12 anos. A taxa de sucesso foi 89%, se não ocorresse periodontite apical no pré-operatório, a taxa foi na realidade 97,9 % embora fosse apenas 62,5 % onde qualquer mudança periradicular estivesse presente (27) (Figs 15 a e b).
Schaeffer et al (7) realizaram uma meta- análise sobre o comprimento ideal de obturação do canal, analisando quatro estudos com pelo menos 2 anos. O número total de dentes considerados foi aproximadamente 1800. Os melhores resultados alcançados com obturação de canal que terminaram de 0 a 1mm do ápice radiográfico. Quando a obturação do canal terminar de 1 a 3 mm coronal do ápice, a taxa de sucesso era 5,9 % e com obturação excessiva, até mesmo inferior a 28,9%. Quando a localização exata da constrição não pode ser feita, não pode ser deduzida a partir destes dados se a técnica de patência é superior ou inferior à preparação confinada ao forame fisiológico. Entretanto, se os resultados de patência em obturações excessivas, isto obviamente tem consequências adversas. Tem sido mostrado várias vezes por meio de análise na literatura que os dentes com obturação de canal extensa além do ápice radiográfico tem um prognóstico bem pior do que aquele, onde a obturação do canal está confinada ao lúmen do canal( 0 a 2mm coronal para o ápice radiográfico) (5,7,,8). A obturação de canais que terminam na área de 0 a 1mm e 0 a 2mm do ápice anatômico tiveram 28,8% ou 15.7 % taxa de sucesso mais elevada, respectivamente do que aqueles nos quais havia extrusão do material de obturação (7,8).
De acordo com duas meta-análises, atualmente o nível mais alto de evidência, pode ser resumido assim que estender a obturação do canal além do ápice radiográfico está associado com perspectiva de sucesso mais baixo (7,8).
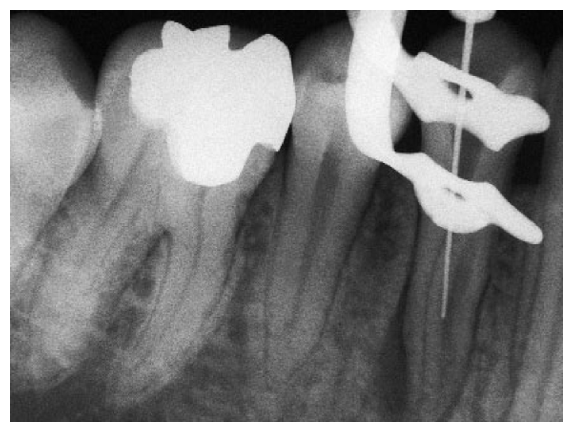
Fig. 15 a A instrumentação para o comprimento de trabalho desejado não foi alcançado.
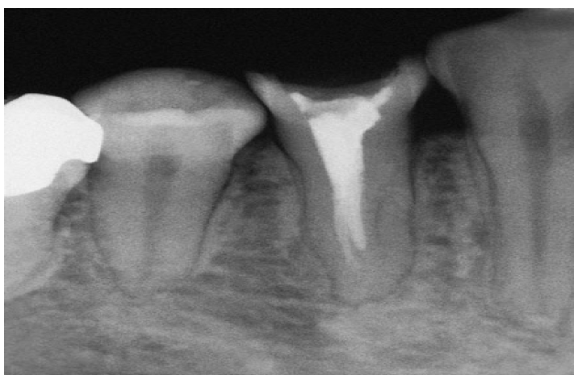
Fig. 15 b Apesar de instrumentação incompleta, o tratamento do canal foi bem sucedido.
27 CONCLUSÃO
Apesar de todos os dados descritos na ideia repostada na literatura, a qual às vezes é muito contraditória, os seguintes aspectos podem ser registrados como conclusões.
- Pressão excessiva periapicalmente leva tecido infectado pode contribuir para a formação e/ou persistência de periodontite apical e provavelmente tem uma função importante na etiologia das dores pós-operatórias(Inflamação aguda).
- Microorganismos remanescentes na porção apical do canal, os quais ganham acesso aos tecidos perirradiculares, são um fator etiológico no desenvolvimento ou persistência da inflamação perirradicular (principalmente inflamação crônica).
- Se existe toda uma possibilidade de limpeza com limas de patência cujo diâmetro seja menor que aquele do forame fisiológico deve ser questionado.
- Somente a saída maior e mais reta apical para o canal, mas não saídas laterais numerosas, podem ser instrumentados por meio da técnica de patência. Muitas destas saídas não podem ser instrumentadas por causa do desvio e posição lateral do forame apical.
- A técnica de patência não é comprovada ter uma influência positiva ou negativa no resultado do tratamento. Ainda não há ensaios clínicos controlados disponíveis sobre este tema.
- Como questão de princípio, as técnicas de patência não devem ser usadas em pacientes com certas desordens médicas gerais.
- O uso da técnica de potência deve ser rejeitada quando o dente é vital, não há indicação aqui (ou até mesmo mera justificativa) para instrumentação intencional além do forame fisiológico.
- Na presença de necrose pulpar infectada, a extrusão das detritos e bloqueio apical devem igualmente ser evitadas através de irrigação e recapitulação com um instrumento fino para trabalhar o comprimento. O objetivo da recapitulação é afrouxar ou liberar os detritos de forma que elas possam ser removidas com a solução de irrigação antes de fazer o bloqueio. Ao mesmo tempo, o irrigante também é colocado nesta parte do canal e regularmente revigorado.
- Os dados atualmente disponíveis sobre o prognóstico de longo prazo do tratamento do canal 104, todos se relacionam com estudos onde nenhuma técnica de patência foi usada.
28 CONSIDERAÇÕES FINAIS
Esta monografia foi uma adaptação da tradução do artigo científico intitulado: Apical patency: fact and fiction—a myth or a must? A contribution to the discussion. dos autores
Michael Hülsmann and Edgar Schäfer. ENDO (Lond Engl) 2009;3(3):171–184.
29 REFERÊNCIAS BIBLIOGRÁFICAS
1. Bergenholtz G, Spangberg L. Controversies in endodontics.Crit Rev Oral Biol Med 2004;15:99-114.
2. Schilder H. Cleaning and shaping the root canal. Dent Clin North Am 1974;18:269-296.
3. Bellamy R. Confine yourself to the canal. Irish Dentist2003;13:10-11.
4. Souza R. The importance of apical patency and cleaning of the apical foramen on root canal preparation. Braz Dent J2006;17:6-9.
5. Ricucci D, Langeland K. Apical limit of root canal instrumentation and obturation. Part 1. Literature review. Int Endod J 1998;31:384-393.
6. Ricucci D, Langeland K. Apical limit of root canal instrumentation and obturation. Part 2. A histological study. Int Endod J 1998;31:494-509.
7. Schaeffer MA, White RR, Walton RE. Determining the optimal obturation length: a meta-analysis of literature. J Endod 2005;31:271-274.
8. Kojima K, Inamoto I, Nagamatsu K, Hara A, Nakata K, Morita I, Nakagaki H, Nakamura H. Success rate of endodontic treatment of teeth with vital and nonvital pulps. A metaanalysis. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2004;97:95-99.
9. Jafarzadeh H, Abbott PV. Ledge formation: Review of a great challenge in endodontics. J Endod 2007;33:1155-1162.
10. Lin LM, Rosenberg PA, Lin J. Do procedural errors cause endodontic treatment failure? J Am Dent Assoc 2005; 136:187-193.
11. Schäfer E, Dammaschke T. Development and sequelae of canal transportation. Endodontic Topics (im Druck).
12. American Association of Endodontists: Glossary of Endodontic Terms. 7th ed., Chicago, IL, USA, 2003.
13. DGZ: Offizielles Endodontologisches Lexikon. In Heidemann D (Hrsg.). Endodontie. 4th edn. Munich: Urban & Fischer,2001:277-308.
14. Cailleteau JG, Mullaney TP. Prevalence of teaching apical patency and various instrumentation and obturation techniques in United States dental schools. J Endod 1997;23: 394-396.
15. Buchanan LS. Management of the curved root canal. J Calif Dent Assoc 1989;17:19-27.
16. Mullaney TP, Cailleteau J, Duell R. The case for patency in apical root canal enlargement. Endod Practice 1998;1:6-14.
17. Mounce R. What is apical patency and does it matter? Compend Cont Educ Dent 2005;28:62-66.
18. Bellamy R. The art of patency. Endodontic Practice 2006;9:9-12.
19. Ruddle CJ. Cleaning and shaping the root canal system. In: Cohen S, Burns R (Ed.). Pathways of the Pulp. 8th edn., St. Louis: Mosby, 2002:244-277.
20. Greve HC. Die sogenannte ‘Wurzelfüllung’ von geschichtlichem und neuzeitlichem Standpunke aus betrachtet. Z Stomatol 1942;20:757-796.
21. Kerschgens H. Eine neue Methode konservativer Gangränbehandlung. Zahnärztl Rundschau 1938;43:1857-1860.
22. Plathner CH. Ist die Behandlung des gangränösen Wurzelkanales erfolgreich durchzuführen? Dtsch Zahnärztl Z 1955;10:1638-1642.
23. Velvart P, Sigurdsson A. Root canal instrumentation with a patency technique. Pract Period Aesthet Dent 1999;11:947-952.
24. Siqueira JF jr. Reaction of periradicular tissues to root canal treatment: benefits and drawbacks. Endodontic Topics 2005;10:123-147.
25. Kuyk JK, Walton RE. Comparison of the radiographic appearance of root canal size to its actual diameter. J Endod1990;16:528-533.
26. Molven O. Nonpenetrable root canals as assessed by a standardized instrumentation procedure. Oral Surg Oral Med Oral Pathol 1973;35:232-237.
27. Hasselgren G, Strömberg T. The use of iodine as a contrast medium in endodontic therapy. Oral Surg Oral Med Oral Pathol 1976;41:785-788.
28. Akerblom A, Hasselgren G. The prognosis for endodontic treatment of obliterated root canals. J Endod 1988;14:565-567.
29. Kuttler Y. Microscopic investigation of root apexes. J Am Dent Assoc 1955;50:544-552.
30. Dummer PMH, McGinn JH, Rees DG. The position and topography of the apical constriction and apical foramen. Int Endod J 1984;17:192-198.
31. Baugh D, Wallace J. The role of apical instrumentation in root canal treatment: A review of the literature. J Endod 2005;31:333-341.
32. Vertucci FJ. Root canal morphology and its relationship to endodontic procedures. Endodontic Topics 2005;10:3-29.
33. Morfis A, Sylaras SN, Georgopoulou M, Kernani M, Prountzos F. Study of the apices of human permanent teeth with the use of a scanning electron microscope. Oral Surg Oral Med Oral Pathol 1994;77:172-176.
34. Ponce EH, Fernandez JA. The cemento-dentinal-canal junction, the apical foramen, and the apical constriction. J Endod 2003;29:214-219. ENDO (Lond Engl) 2009;3(3):171–184 Hülsmann/Schäfer Apical patency—a myth or a must?
35. Pineda F, Kuttler Y. Mesiodistal and buccolingual roentgenographic investigation of 7.275 root canals. Oral Surg Oral Med Oral Pathol 1972;32:101-110.
36. Mizutani T, Ohno N, Nakamura H. Anatomical study of the root apex in the maxillary anterior teeth. J Endod 1992;18:344-347.
37. Burch IG, Hulen S. The relationship of the apical foramen to the anatomic apex of the tooth. Oral Surg Oral Med Oral Pathol 1972;34:262-268.
38. Gutierrez JH, Aguayo P. Apical foraminal openings in human teeth. Oral Surg Oral Med Oral Pathol Oral adiol Endod1995;79:769-777.
39. Hess JC, Culieras MJ, Lamiable N. A scanning electron microscopic investigation of principal and accessory foramina on the root surfaces of human teeth: thoughts about endodontic pathology and therapeutics. J Endod 1983;9:215-221.
40. Ainamo J, Löe H. A stereomicroscopic investigation of the anatomy of the root apices of 910 maxillary and mandibular teeth. Odontol Tidskr 1968;76:417-426.
41. De Deus QD. Frequency, location, and direction of the lateral secondary, and accessory canals. J Endod 1975;1.361-366.
42. Briseno-Marroquin B, El-Sayed MA, Willershausen-Zönnchen B. Morphology of the physiological foramen: I. Maxillary and mandibular molars. J Endod 2004;30:321-328.
43. Weine FS. The enigma of the lateral canal. Dent Clin North Am 1984;28:833-852.
44. Goldberg F, Massone EJ. Patency file and apical transportation: an in vitro study. J Endod 2002;28:510-511.
45. Cohen S, Burns R. Pathways of the Pulp. 6th edn., St. Louis: Mosby, 1994.
46. Fukushima H, Yamamoto K, Hirohata K, Sagawa H, Leing KP, Wallker CB. Localization and identification of root canal bacteria in clinically asymptomatic periapical pathosis. J Endod1990;16:534-538.
47. Nair PNR. Light and electron microscopic studies of root canal flora and periapical lesions. J Endod 1987;13:29-39.
48. Nair PNR, Sjögren U, Krey G, Kahnberg KE, Sundqvist G. Intraradicular bacteria and funghi or root-filled, asymptomatic human teeth with therapy-resistant periapical lesions: a long-term light and electron microscopic follow-up study.J Endod 1990;16:580-588.
49. Hülsmann M, Rödig T, Nordmeyer T. Complications during root canal irrigation. Endodontic Topis (im Druck).
50. Lambrianidis T, Tosounidou E, Tzoanopoulou M. The effect of maintaining apical patency on periapical extrusion. JEndod 2001;27:696-698.
51. Katz H. Endodontic implications of biphosphonate-associated osteonecrosis of the jaw: A report of three cases. J Endod 2005;31:831-834.
52. Sarathy AP, Bourgeois SL, Goodell GG. Biphosphonate-associated osteonecrosis of the jaws and endodontic treatment:Two case reports. J Endod 2005;31:759-763.
53. Schulte A, Ott KHR. Zur Indikation der Wurzelkanalbehandlung bei Patienten mit Gerinnungsstörungen. Dtsch Zahnärztl Z 1990;45:226-228.
54. Murray CA, Saunders WP. Root canal treatment and general health: a review of the literature. Int Endod J 2000;33:1-18.
55. Debelian GJ, Olsen I, Tronstad L. Systemic diseases caused by oral microorganisms. Endod Dent Traumatol 1994;10:57-65.
56. Debelian GJ, Olsen I, Tronstad L. Anaerobic bacteremia and fungemia in patients undergoing endodontic therapy: an overview. Ann Periodontol 1998;3:281-287.
57. American Heart Association. Guidelines from the American Heart Association: Prevention of infective endocarditis. Circulation 2007;116:1736-1754.
58. Schäfer E. Allgemeinmedizinische Probleme. In: Hülsmann M, Schäfer E, Bargholz C, Barthel C. Probleme in der Endodontie. Berlin: Quintessenz, 2007:73-108.
59. Osswald RJ, Friedman CE. Periapical response to dentin fillings. Oral Surg Oral Med Oral Pathol 1980;49:344-355.
60. Erausquin J. Periapical tissue response to the apical plug in root canal treatment. J Dent Res 1972;51:483-487.
61. Tronstad L. Tissue reactions following apical plugging of the root canal with dentin chips in monkey teeth subjected to pulpectomy. Oral Surg Oral Med Oral Pathol 1978;45:297-304.
62. Engstroem B, Spangberg L Wound healing after partial pulpectomy. A histologic study performed on contralateral tooth pairs. Odontol Tidskr 1967;75:5-18.
63. Ketterl W. Zementverschluss nach Vitalexstirpation. Zahnärztl Welt 1968;11:368-369.
64. Yee RD, Newton CW, Patterson SS, Swartz ML. The effect of canal preparation on the formation and leakage characteristics of the apical dentin plug. J Endod 1984;10:308-317.
65. ElDeeb ME, Thuc-Quyen NT, Jensen JR. The dentinal plug: its effect on confining substances to the canal and on apical seal. J Endod 1983;9:355-359.
66. Pitts DL, Jones JE, Oswald RJ. A histological comparison of calcium hydroxide plugs and dentin plugs used for the control of gutta-percha root canal filling material. J Endod1984;10:283-293.
67. Jacobsen EL, Bery PF, BeGole EA. The effectiveness of apical dentin plugs in sealing endodontically treated teeth. J Endod 1985;11:289-293.
68. Benatti O, Valdrighi L, Biral RR, Pupo J. A histological study of the effect of diameter enlargement of the apical portionof the root canal. J Endod 1985;11:428-434.
69. Holland R, Nery MJ, de Mello W, de Souza V, Bernabé PF, Otoboni Filho JA. Root canal treatment with calcium hydroxide. II. Effect of instrumentation beyond the apices. Oral Surg Oral Med Oral Pathol 1979;47:93-96.
70. Hørsted P, Nygaard-Østby N. Tissue formation in the root canal after total pulpectomy and partial root filling. Oral Surg Oral Med Oral Pathol 1978;46:275-282.
71. Seltzer S, Soltanoff W, Sinai I, Goldenberg A, Bender IB. Biologic aspects of endodontics. 3. Periapical tissue reactions to root canal instrumentation. Oral Surg Oral Med Oral Pathol 1968;26:694-705.
72. Seltzer S, Naidorf IJ. Flare-ups in endodontics: I. Etiological factors. J Endod 1985;11:472-478.
73. Torneck CD, Smith JS, Grindall P. Biologic effects of endodontic procedures on developing incisor teeth. II. Effect of pulp injury and oral contamination. Oral Surg Oral Med Oral Pathol 1973;35:378-388.
74. Torneck CD, Smith JS, Grindall P. Biologic effects of endodontic procedures on developing incisor teeth. III. Effect of debridement and disinfection procedures in the treatment of experimentally induced pulp and periapical disease. Oral Surg Oral Med Oral Pathol 1973;35:532-540.
75. Holland R, Sant Anna A jr, de Souza V, Dezan E jr, Otoboni Filho JA, Bernabé PFE, Nery MJ, Murata SS. Influence of apical patency and filling material on healing of dogs’ teeth with vital pulp after root canal therapy. Braz Dent J 2005;16:9-16.
76. Gutierrez JH, Brizuela C, Villota E. Human teeth with periapical pathosis after over-instrumentation and overfilling of the root canals. Int Endod J 1999;32:40-48.
77. Izu KH, Thomas SJ, Zhang P, Izu AE, Michalek S. Effectiveness of sodium hypochlorite in preventing inoculation of periapical tissues with contaminated patency files. J Endod 2004;30:92-94.
78. Tinaz AC, Alacam T, Uzun O, Maden M, Kayaoglu G. The effect of disruption of apical constriction on periapical extrusion. J Endod 2005;31:533-535.
79. Lambrianidis T, Kosti E, Boutsioukis C, Mazinis M. Removal efficacy of various calcium hydroxide/chlorhexidine medicaments from the root canal. Int Endod J 2006;39:55-61.
80. Langeland K. The histopathologic basis in endodontic treatment. Dent Clin North Am 1967;11:491-520. ENDO (Lond Engl) 2009;3(3):171–18422 Hülsmann/Schäfer Apical patency—a myth or a must?
81. Langeland K. Tissue response to dental caries. Endod Dent Traumatol 1987;3:149-171.
82. Lin L, Shovlin F, Skribner J, Langeland K. Pulp biopsies from the teeth associated with periapical radiolucencies. J Endod 1984;10:436-448.
83. Siqueira JF, Barnett F. Interappointment pain: mechanisms, diagnosis, and treatment. Endodontic Topics 2004;7:93-109.
84. Siqueira JF. Reaction of periradicular tissues to root canal treatment: benefits and drawbacks. Endodontic Topics 2005;10:123-147.
85. Al-Omari MAO, Dummer PMH. Canal blockage and debris extrusion with eight preparation techniques. J Endod 1995;21:154-158.
86. Torabinejad M, Kettering JD, McGraw JC, Cummings RR, Dwyer TG, Tobias TS. Factors associated with interappointment emergencies of teeth with necrotic pulps. J Endod 1988;14:261-266.
87. Siqueira JF jr, Rocas IN, Favieri A, Machado AG, Gahyva SM, Oliveira JC, Abad EC. Incidence of postoperative pain after intracanal procedures based on an antimicrobial strategy. J Endod 2002;28:457-460.
88. Georgopoulou M, Anastassiadis P, Sykaras S. Pain after chemomechanical preparation. Int Endod J 1986;19:309-314.
89. Harrison JW, Baumgartner JC, Svec TA. Incidence of pain associated with clinical factors during and after root canal therapy.Part 2. Postobturation pain. J Endod 1983;9:434-438.
90. Nobuhara WK, Carnes DL, Gilles JA. Anti-inflammatory effects of dexamethasone on periapical tissues following endodontic over-instrumentation. J Endod 1993;19:501-507.
91. Holland R, de Souza V, Nery MJ, de Mello W, Bernabé PF, Otoboni Filho JA. Tissue reactions following apical plugging of the root canal with infected dentin chips. A histologic study in dogs’ teeth. Oral Surg Oral Med Oral Pathol 1980;49:366-369.
92. Yusuf H. The significance of the presence of foreign material periapically as a cause of failure of root treatment. Oral Surg Oral Med Oral Pathol 1982;54:566-574.
93. Bergenholtz G, Lekholm U, Milthon R, Engstroem B. Influence of apical over-instrumentation and overfilling on retreated root canals. J Endod 1979;5:310-314.
94. Monsef M, Hamedzadeh K, Soluti A. Effects of apical patency on the apical seal of obturated canals. (AAE-abstract OR 15). J Endod 1997;23:253.
95. Gimlin DR, Parr CH, Aguirre-Ramirez G. The effect of apical foramen patency on condensation stress. Endod Dent Traumatol 1986;2:252-255.
96. Wu MK, Wesselink PR. Überlegungen zum apikalen Endpunkt der Wurzelkanalbehandlung. Endodontie 2001;10:9-18.
97. Weine FS, Kelly RF, Lio PJ. The effect of preparation procedures on original canal shape and on apical foramen shape.J Endod 1975;1:255-262.
98. Tsesis I, Amdor B, Tamse A, Kfir A. The effect of maintaining apical patency on canal transportation. Int Endod J 2008;41:431-435.
99. Baumgartner JC, Heggers JP, Harrison JW. The incidence of bacteremias related to endodontic procedures. I. Nonsurgical endodontics. J Endod 1976;2:135-140.
100. Bender IB, Seltzer S, Yermish M. The incidence of bacteremia in endodontic manipulation. Oral Surg Oral Med Oral Pathol 1960;13:363-360.
101. Bender IB, Naidorf IJ, Garvey GJ. Bacterial endocarditis: a consideration for physicians and dentists. J Am Dent Assoc 1984;109:415-420.
102. Debelian GJ, Olsen I, Tronstad L. Bacteremia in conjunction with endodontic therapy. Endod Dent Traumatol 1995;11:142-149.
103. Hoskinson SE, Ng YL, Hoskinson AE, Moles DR, Gulabivala K. A retrospective comparison of outcome of root canal treatment using two different protocols. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2002;93:705-715.
104. Stellungnahme der DGZMK und der DGZ. Zur Prognose von Wurzelkanalbehandlungen. Dtsch Zahnärztl Z 2001;56:206-207.
