MEDICATION-RELATED OSTEONECROSIS OF THE JAWS
REGISTRO DOI: 10.69849/revistaft/ra10202409302118
Luis Fernando Alves Correa 1
João Kleber Silva Dias 2
Ludymilla De Lima Lopes 3
Resumo
A alta afinidade pelo tecido ósseo e consequente alteração do turnover ósseo causada pelos bisfosfonatos (BFs, fármacos antirreabsortivos) colocam em cheque a segurança da execução de procedimentos odontológicos invasivos nos maxilares em pacientes que fazem uso dessas medicações, apontando tais condutas como o principal gatilho para o surgimento de uma osteonecrose nos maxilares. Por conseguinte, vários autores e associações têm classificado a terapia com BFs como um fator limitante ou até mesmo excludente para a instalação de implantes dentários. A presente revisão de literatura teve como proposição identificar a existência ou não de um perfil de risco individual do paciente que fez ou faz uso de BFs, determinado por vários fatores, como: a via de administração, potência do fármaco, duração da terapia e doença base. Além disso, essa pesquisa buscou informações sobre contraindicação de instalação de implantes em pacientes sob terapia com BFs. Com base na literatura consultada foi possível concluir que os principais fatores que aumentam o risco de desenvolvimento de OMRM incluem: BFs administrado por via endovenosa; Pacientes com neoplasia maligna e mieloma múltiplo como doença base; Droga mais potente: ácido zoledrônico; Valor de CTX: < 150 pg/ml; Tempo de uso de BFs VO maior que três anos ou associado a corticoide; Sítio do implante: região posterior de mandíbula. Dentro das limitações deste trabalho, é possível afirmar que o uso de BFs não é uma contraindicação absoluta para a instalação de implantes.
Palavras-chave: Osteonecrose; Bisfosfonato; Implantodontia.
ABSTRACT
The high affinity for bone tissue and consequent change in bone turnover caused by bisphosphonates (BFs, anti-resorptive drugs) call into question the safety of performing invasive dental procedures in the jaws in patients who use these medications, pointing to such conduct as the main trigger for the appearance of osteonecrosis in the jaws. Therefore, several authors and associations have classified therapy with BFs as a limiting or even excluding factor for the installation of dental implants. This literature review aimed to identify the existence or not of an individual risk profile of the patient who used or uses BPs, determined by several factors, such as: route of administration, drug potency, duration of therapy and disease base. In addition, this research sought information on contraindications for installing implants in patients undergoing therapy with BFs. Based on the consulted literature, it was possible to conclude that the main factors that increase the risk of developing OMRM include: BFs administered intravenously; Patients with malignant neoplasm and multiple myeloma as the underlying disease; Most potent drug: zoledronic acid; CTX value: < 150 pg/ml; Time of use of oral BPs greater than three years or associated with corticosteroids; Implant site: posterior region of the mandible. Within the limitations of this study, it is possible to state that the use of BFs is not an absolute contraindication for the installation of implants.
Keywords: Osteonecrosis; bisphosphonate; implant dentistry.
1 INTRODUÇÃO
A osteonecrose dos maxilares relacionada ao uso de medicamentos (OMRM) provem de efeitos secundários de tratamentos conduzidos com algumas classes de fármacos, como por exemplo, os antiangiogênicos e os antirreabsortivos, sendo os inibidores do receptor ativador do fator nuclear-κB ligante (RANK-L) e os bisfosfonatos (BFs) representantes dessa última classe (RUGGIERO et al., 2014). Pacientes submetidos ao tratamento para osteoporose, doença de Paget ou neoplasias malignas, são os mais propícios a fazerem uso dessas medicações (HOFF et al., 2018).
Embora os benefícios dos antirreabsortivos no tratamento de desordens esqueléticas sejam amplamente reconhecidos, em 2003 foram descritos os primeiros casos de osteonecrose dos maxilares associado ao uso de BFs (MARX, 2003), que clinicamente caracteriza-se por uma área de osso necrótico exposto na região gramática ou passível de sondagem através de fístula intra ou extrabucal, sem cicatrização após o período de oito semanas, cuja ocorrência acomete pacientes que fizeram ou fazem uso terapêutico de antirreabsortivo e/ou antiangiogênico e sem histórico prévio de radioterapia ou doença metastática na região de cabeça e pescoço (RUGGIERO et al., 2009)
Apesar de haver várias hipóteses para o desenvolvimento da OMRM, sua fisiopatogênese ainda não se encontra totalmente elucidada, todavia, a literatura sustenta como principal processo fisiopatológico, o fato de que os diferentes mecanismos antirreabsortivos destes fármacos alterem a viabilidade dos osteoblastos e osteoclastos, o que acarreta um desequilíbrio da remodelação óssea, diminuindo sua taxa de renovação e favorecendo a necrose (RUGGIERO, 2011; HE et al., 2020; AGUIRRE; CASTILLO; KIMMEL, 2021). Além disso, a cavidade oral e os ossos gnáticos possuem características intrínsecas que favorecem a ocorrência da OMRM (RUGGIERO, 2011; HE et al., 2020).
A alta afinidade pelo tecido ósseo e consequente alteração do turnover ósseo causada pelos BFs colocam em cheque a segurança da execução de procedimentos odontológicos invasivos nos maxilares em pacientes que fazem uso dessas medicações, apontando tais condutas como o principal gatilho para o surgimento de uma OMRM. Por conseguinte, vários autores e associações têm classificado a terapia com BFs como um fator limitante ou até mesmo excludente para a instalação de implantes dentários (RUGANI et al., 2015).
Atualmente existe controvérsia na literatura sobre a segurança da cirurgia para instalação de implantes em pacientes em uso de BFs para enfermidades ósseas (OLIVEIRA et al., 2017), e muita das vezes a decisão de realizar ou não uma cirurgia para instalação de implantes em pacientes que fazem uso de antirreabsortivos é complexa e baseia-se no perfil de risco individual do paciente e da compreensão do assunto por parte do profissional.
A presente revisão de literatura tem como proposição identificar a existência ou não de um perfil de risco individual do paciente que fez ou faz uso de BFs, determinado por vários fatores, como: a via de administração, potência do fármaco, duração da terapia e doença base. Além disso, essa pesquisa buscou informações a respeito das contra indicações de cirurgia para instalação de implantes em pacientes sob terapia antirreabsortiva.
2 REVISÃO DA LITERATURA
2.1 BISFOSFONATOS
O osso é um tecido dinâmico continuamente reabsorvido por osteoclastos e depositado pelos osteoblastos, e esse equilíbrio é regulado por fatores sistêmicos e locais. Os BFs são compostos análogos sintéticos do pirofosfato inorgânico, e apresentam em sua estrutura molecular dois grupamentos fosfato ligados covalentemente a um carbono central, sucedidos por duas cadeias, uma cadeia curta responsável pela alta afinidade do BF ao tecido ósseo e uma cadeia longa responsável por seu potencial anti-reabsortivo (FIG. 1). O BFs são quelados ao tecido ósseo, e acabam sendo metabolizados e interiorizados pelos osteoclastos, logo, as moléculas de BFs provocam a morte programada dessas células graças à cadeia longa. Os BFs não-nitrogenados metabolizados provocam a apoptose da célula clástica por citotoxicidade. Já os BFs nitrogenados, após absorvidos pelos osteoclastos parecem atuar interrompendo a via do mevalonato, e a interrupção desse mecanismo compromete o metabolismo celular, causa apoptose e afeta diretamente a reabsorção óssea (RUGGIERO; WOO, 2008). Os BFs ainda acarretam redução do estímulo de células endoteliais, ocasionando aumento da apoptose e queda na proliferação de celular, promovendo o arrefecimento na quantidade de vasos sanguíneos (GEGLER et al., 2006).
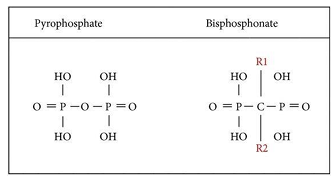
Figura 1 – Estrutura molecular básica do BF.
Fonte: Google Imagens, 2022.
DOENÇA BASE
Os BFs atuam inibindo a atividade dos osteoclastos, e isso reflete na redução da reabsorção óssea. Dessa forma, esses compostos são amplamente utilizados para tratamento de condições patológicas onde a reabsorção óssea é significativa, como por exemplo, a osteoporose, doença de Paget, hipercalcemia maligna e doenças metastáticas provenientes de tumores malignos (HOFF et al., 2008). A OMRM é observada com maior frequência em pacientes com doença metastática óssea proveniente de neoplasias malignas sólidas (principalmente câncer de mama, próstata e pulmão) e em pacientes com mieloma múltiplo, pois normalmente essas patologias são tratadas com BFs mais potentes e administrados via endovenosa (EV) (FICARRA; BENINATI, 2007).
A maioria dos casos de OMRM acomete pacientes com carcinomas metastáticos e mieloma múltiplo, enquanto sua incidência em pacientes com osteoporose, artrite reumatoide e doença de Paget é rara (MARTINS et al., 2009).
OMRM
A etiopatogenia da OMRM ainda não está totalmente elucidada, porém, a redução da capacidade regenerativa do tecido ósseo e prejuízos na angiogênese causados pelo mecanismo de ação dos BFs é entendido como ponto de partida para o desenvolvimento da necrose óssea. Além disso, é preciso lembrar que a mandíbula e a maxila são recobertas por um fino tecido mucoso que as separa do meio externo, a cavidade oral, um ambiente habitado por inúmeros microrganismos patogênicos. Ademais, processos infecciosos em alguma estrutura do sistema estomatognático e a necessidade de intervenções terapêuticas invasivas na cavidade oral, não são eventos raros, o que pode ser mais um fator predisponente ao desenvolvimento da OMRM (FIG. 2) (FICARRA; BENINATI, 2007; RUGGIERO; WOO, 2008; HE et al., 2020). Ainda, o tecido ósseo gnático apresenta rico suprimento sanguíneo, e por causa de sua acelerada capacidade de renovação e à alta demanda por remodelação óssea em função das cargas aplicadas ao periodonto, os BFs concentram-se abundantemente nesses ossos (JESUS et al., 2019).
O conceito que define a condição de OMRM, é o aparecimento e persistência de osso necrótico na cavidade oral por período mínimo de oito semanas, em indivíduo com relato de tratamento prévio ou atual com BFs, sem histórico de radioterapia na região da cabeça-pescoço (AAOMS, 2007). Os sinais e sintomas incluem: quadro álgico, dentes com mobilidade, ulceração, drenagem de secreção, aumento de volume na mucosa, osteomielite, exposição óssea e fratura patológica (MARTINS et al., 2009).
A OMRM pode ser classificada em três estágios de acordo com os sinais e sintomas apresentados: Estágio 1 – exposição e necrose assintomática; Estágio 2 – exposição e necrose associada a sintoma doloroso e foco infeccioso; Estágio 3 – osso necrótico e exposto, sintoma doloroso, foco infeccioso, fístula extraoral, osteólise e fratura patológica (RUGGIERO et al., 2006).
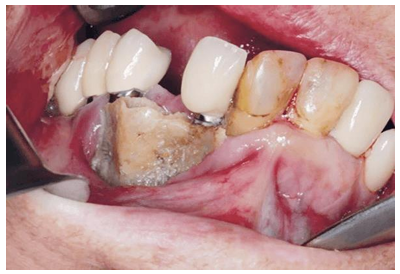
Figura 2 – OMRM.
Fonte: Google Imagens, 2022.
POTÊNCIA DO FÁRMACO
A potência dos diferentes tipos de BFs está inicialmente relacionada à sua estrutura molecular, pois os BFs nitrogenados apresentam maior potência quando comparados aos não nitrogenados. Os nitrogenados inibem a atividade da enzima farnesil difosfato sintase, o que resulta no bloqueio da osteoclastogênese, impossibilitando a ativação de osteoclastos maduros e causando morte programada de osteoclastos inativos, sendo que este processo de diferenciação das células clásticas desempenha importante papel na cicatrização e remodelação óssea (MENEZES et al., 2021).
É possível observar a relação da potência do fármaco com o tempo de surgimento da OMRM. Essa proposição pode ser observada em pacientes com câncer de mama que utilizam o zoledronato e desenvolveram a OMRM em um intervalo de tempo menor quando comparado com outros pacientes tratados com outros BFs (HOFF et al., 2008).
As propriedades antirreabsortivas dos BFs aumentam de acordo com as suas gerações (TABELA 1).
TABELA 1 – Potência relativa dos BFs
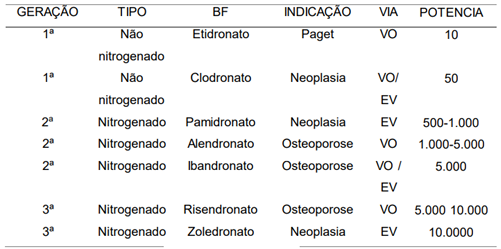
Fonte: Tabela adaptada de Ruggiero e Woo (2008).
Figura 3 – Apresentação comercial do zoledronato.
Fonte: Google Imagens.
VIA DE ADMINISTRAÇÃO
A administração EV parece atribuir um risco mais alto para o desenvolvimento da OMRM do que a administração por VO (MARTINS et al., 2009; COLÉTE et al., 2019), e isso ocorre porque os BFs EV possuem elevada biodisponibilidade em comparação aos de VO, pois no mínimo 50% da dose administrada EV é absorvida pelo organismo e quelado à hidroxiapatita, contrapondo-se à absorção de apenas 1% da droga administrada VO (STRAMANDINOLI-ZANICOTTI et al., 2018). Os BFs de administração EV normalmente são utilizados para tratar condições associadas ao câncer (AAOMS, 2007), enquanto os BFs de administração por VO estão mais relacionados ao tratamento de doenças ósseas como, osteoporose, osteopenia, doença de Paget e osteogênese imperfeita (STRAMANDINOLI-ZANICOTTI et al., 2018).
DURAÇÃO DA TERAPIA COM BF
Os BFs são incorporados ao tecido ósseo e não são metabolizados, por essa razão pressupõe-se que tratamentos a longo prazo com essa medicação afete a taxa de renovação óssea por muitos anos (LAZAROVICI et al., 2010). O desenvolvimento de OMRM também está relacionada com a duração mediana de doença maligna ou das metástases ósseas, o que coloca em pauta a relação de tempo da administração da droga e maior acúmulo de dose (HOFF et al., 2008). A média de tempo para início do aparecimento da OMRM, depende do tipo de BFs usado na terapia. Para o zoledronato a média de tempo é de 16 meses, para o pamidronato é de 34 meses e para BFs orais é de 4,5 anos (MARTINS et al., 2009).
Um marcador de reabsorção óssea pode ser usado como parâmetro para avaliação de risco de desenvolvimento de OMRM, denominado teste CTX sérico (telopeptídeo carboxiterminal do colágeno tipo I) capaz de avaliar a eliminação de fragmentos gerados pela hidrólise do colágeno tipo I. Há uma relação exponencial direta entre o período de uso dos BFs e a dimensão da exposição óssea. É recomendado que os pacientes com valores de CTX inferiores a 150 pg/ml sejam encaminhados ao médico responsável por seu tratamento, para que a possibilidade de suspensão do fármaco seja levada em consideração durante um intervalo de tempo de quatro a seis meses, podendo estender esse período após novo teste com valores ainda abaixo de 150 pg/ml (MARX et al., 2007). Não há evidência na literatura o suficiente que sustente de forma veemente a teoria de descontinuação da terapia com BFs para promover a cicatrização de tecidos ósseos necróticos na cavidade oral, logo, a real necessidade de suspensão na terapia com o fármaco deve ser discutida com o médico que o prescreveu, levando em consideração o risco versus benefícios da descontinuação da droga. É importante lembrar que o tempo de meia-vida dos BFs EV é mensurado em anos, logo, a interrupção do fármaco por alguns meses pode ter efeito irrisório, uma vez que o BF está incorporado ao osso. Contudo, a atividade antiangiogênica pode ser minimizada significativamente com a interrupção da droga, favorecendo a cicatrização da mucosa sobrejacente (MIGLIORATI et al., 2005).
FATORES DE RISCO LOCAL
Os principais fatores de risco local são: exodontia, manipulação cirúrgica em geral, trauma causado por próteses removíveis e infecções orais (MIGLIORATI et al., 2005).
A maioria dos relatos de necrose nos maxilares em pacientes com histórico ou em uso de drogas antirreabsortivas estão diretamente relacionados ao traumatismo causado nas cirurgias orais, especialmente nas extrações dentárias, evidenciando esse procedimento como o principal fator de risco local (CAVAZANA, 2015.). A associação a outros fármacos (especialmente os corticoides) e outras doenças coadjuvantes, também podem estar ligadas ao início ou evolução da OMRM (MARX et al, 2005). Porém, vale salientar que a literatura traz relatos de casos de aparecimento espontâneo da OMRM, sem fator de risco local associado (CALDAS; DE MENEZES PONTES; ANTUNES, 2009).
A AAOMS (2007) propôs algumas diretrizes a respeito do tratamento odontológico de pacientes que fazem uso de BFs VO: tempo de uso de BFs VO inferior a três anos e sem outro fator de risco associado, deve-se manter o protocolo de atendimento cirúrgico convencional. Tempo de uso de BFs VO superior a três anos ou BFs VO associado a corticoide, necessitam cessar a administração dos BFs pelo menos três meses antes da cirurgia, e retomar o uso do BFs apenas após a cicatrização.
TRATAMENTO
O tratamento da OMRM é desafiador e controverso. Vários protocolos para tratamento estão relatados na literatura, e eles variam desde a prescrição de bochechos diários com clorexidina a 0,12% e acompanhamento regular, à terapia antimicrobiana e debridamento cirúrgico. Para casos mais severos, abordagens mais radicais podem ser necessárias, como as ressecções e reconstruções (JESUS et al., 2019). Outra proposta terapêutica para tratar OMRM é a terapia fotodinâmica antimicrobiana (Antimicrobial Photodynamic Therapy -aPDT), que emprega luz laser associada a um corante fotossensibilizador (MENEZES et al., 2021).
OMRM E IMPLANTE DENTÁRIO
O risco de ser um gatilho para desencadear a OMRM por causa da injúria provocada diretamente no tecido ósseo durante a instalação de um implante dentário em pacientes que estão ou estiveram em terapia com BFs coloca em cheque a segurança da reabilitação com implantes nesses indivíduos (DE CARVALHO et al. 2010).
A implantodontia vem ganhando cada vez mais espalho na reabilitação oral. Cirurgias para instalação de implantes dentários têm se tornado rotina dentro dos consultórios odontológicos e poucas são as contraindicações desse procedimento, todavia o grupo de pacientes que faz uso de antirreabsortivos pertencentes a classe de fármacos bisfosfonatos (análogos sintéticos dos pirofosfatos), podem ser acometidos por uma complicação de difícil manejo, a OMRM, logo, reabilitar um paciente que faz uso de BFs deve ser avaliado de forma individualizada, já que vários favores podem minimizar ou maximizar os riscos do aparecimento desta complicação (MATTIS; GOMES; MAYER, 2016).
De modo geral, a melhor forma do profissional prevenir a OMRM na implantodontia é analisar com atenção e esmero cada caso em suas particularidades, avaliando a real necessidade de reabilitar o paciente com prótese sobre implante, realizar a tomada de cuidados como, solicitar CTX sérico, se comunicar com o médico que acompanha esse indivíduo, conduzir a intervenção cirúrgica de forma menos traumática o possível, e prescrever medicamentos profiláticos e pós-operatório de maneira adequada MATTIS; GOMES; MAYER, 2016).
Se por um lado as pesquisas fazem ressalvas a respeito do maior risco de OMRM em pacientes que fazem terapia com antirreabsortivos e são submetidos à cirurgias orais, como é o caso da cirurgia para instalação de implante, por outro lado, estudos apontam que esses pacientes não apresentam maiores taxas de falha do implante em relação à osseointegração (GRANT et al., 2008).
3 METODOLOGIA
Esta revisão de literatura teve como objetivo compreender os aspectos da osteonecrose dos maxilares, com foco especial na osteonecrose induzida por medicamentos e nas abordagens de tratamento disponíveis. As fontes de dados utilizadas para a busca de literatura foram as bases de dados PubMed, BVS (Biblioteca Virtual em Saúde) e SciELO (Scientific Electronic Library Online). As palavras-chave selecionadas para a busca incluíram: “Osteonecrose dos maxilares”, “osteonecrose induzida por medicamentos”, “bifosfonatos” e “tratamento da osteonecrose dos maxilares”. A estratégia de busca consistiu em utilizar combinações das palavras-chave definidas, aplicando operadores booleanos (AND, OR) para otimizar os resultados. No PubMed, foram utilizados termos MeSH (Medical Subject Headings) para refinar as buscas.
Os critérios de inclusão para a seleção dos artigos foram: (1) artigos que abordassem especificamente a osteonecrose dos maxilares ou osteonecrose induzida por medicamentos, com ênfase em bifosfonatos; (2) estudos que apresentassem dados originais, revisões sistemáticas ou meta-análises relevantes; e (3) artigos disponíveis na íntegra, excluindo aqueles com apenas resumo disponível. Os critérios de exclusão consistiram em: (1) artigos que não se encaixassem no foco do trabalho; (2) estudos com apenas resumos disponíveis, sem acesso ao texto completo; e (3) publicações que não abordassem diretamente os tópicos de interesse, como osteonecrose não relacionada a medicamentos. O processo de seleção resultou em um total inicial de 60. Após a aplicação dos critérios de inclusão e exclusão, foram selecionados 33 artigos para análise detalhada. Cada artigo selecionado foi lido na íntegra e analisado quanto à relevância para o tema da revisão.
4 RESULTADOS E DISCUSSÕES
Mauri et al. (2009) realizaram um estudo randomizado, e observaram a ocorrência de OMRM foi em 13 (0,24%) dos 5.312 pacientes que faziam uso de BFs EV, e em 1 dos 5.382 pacientes no grupo controle. Todos os 13 eventos ocorreram em pacientes em tratamento com ácido zoledrônico (13/3.987, 0,33%). A partir dos resultados foi possível afirmar que o tratamento com ácido zoledrônico foi significativamente associado à ocorrência da OMRM. Segundo Ficarra e Beninati (2007) a OMRM é principalmente observada em pacientes que recebem terapia endovenosa (EV) com BFs, com maior incidência nas preparações EV de ácido zoledrônico e pamidronato, por outro lado, o risco para o desenvolvimento da condição parece ser mínimo em pacientes que fazem uso dos BFs por via oral (VO) (FICARRA; BENINATI, 2007). De acordo com Martins et al. (2009) quanto à potência, o zoledronato é mais potente que o pamidronato, que é mais potente que os BFs orais.
Marx et al. (2007) analisaram o risco e o tempo de evolução da OMRM. A pesquisa em questão possibilitou aos autores as seguintes conclusões: a região posterior de mandíbula foi a mais afetada (94,7%); aparecimento espontânea da OMRM foi de 50%, versus 50% em decorrência de cirurgia oral; 53% dos pacientes faziam uso de BF VO para osteopenia, 33,3% para osteoporose e 13,4% para osteoporose induzida por esteroide; a relação entre tempo de uso dos BF VO e tamanho da área necrótica apresentou relação exponencial direta; o CTX sérico demonstrou que os resultados se correlacionam com a duração do uso de BFs VO orais e podem sugerir recuperação da remodelação óssea com valores aumentados nos casos de suspensão de BFs. A classificação de risco relativo foi de: alto risco para CTX < 100 pg/mL, risco moderado para CTX entre 100 pg/mL e 150 pg/mL, e baixo risco para CTX acima de 150 pg/mL. Notou-se aumento nos valores de CTX mensurados entre 25,9 pg/mL e 26,4 pg/mL para cada mês de descontinuidade de uso do BF, indicando recuperação da remodelação óssea, o que sugere que cirurgias podem ser executadas com o menor risco de desenvolvimento de OMRM. Os autores concluíram que a OMRM induzida por BF VO é rara, menos é mais responsiva ao tratamento do que a osteonecrose induzida BF EV.
Marx et al. (2003) revisaram 119 casos de exposição óssea relacionada a bisfosfonatos, e detectaram que 97,5% foram associados a administração EV, contra 2,5% por VO, ainda nesta revisão, quatro casos (3,4%) de OMRM relacionados à instalação de implantes dentários foram identificados. GRANT et al. (2008) demonstraram em seu estudo retrospectivo, que não houve evidência de osteonecrose associada a bisfosfonatos dos maxilares em nenhum dos 468 implantes instalados em 115 pacientes que faziam uso de BF por VO, e as taxas de sucesso do implante para pacientes que receberam terapia com BF VO foram análogas àqueles que não utilizam o fármaco. LAZAROVICI et al. (2010) realizaram um estudo incluindo 27 pacientes que faziam uso de BFs e desenvolveram OMRM associado a implante dentário. Entre os pacientes que desenvolveram OMRM associada a Implante dentário, 59% estavam recebendo tratamento de BP por via EV, enquanto 41% estavam ingerindo BFs via oral. De Freitas et al. (2016), analisaram periódicos que analisaram pacientes que receberam implantes dentários antes, durante ou após o tratamento com BF, em comparação com pacientes saudáveis. Foram incluídos 15 estudos, o que totalizou em 1339 pacientes analisados, 3748 implantes colocados, 152 perdas de implantes e 78 casos de OMRM. Rosela et al. (2016) afirmaram em suas diretrizes clínicas e práticas, que a cirurgia dentoalveolar eletiva não é contraindicada em pacientes osteoporóticos que fazem uso de BFs por VO por um período inferior a quatro anos e sem outros fatores de risco associado, e que nenhuma modificação ou atraso da cirurgia é necessária, sendo possível a realização de todos os procedimentos odontológicos nestes casos. Quando o período de uso de BFs por VO nestes pacientes ultrapassa 4 anos, a instalação de implantes é possível, mas o paciente deve ser alertado sobre a possibilidade de perda de implantes dentários e risco de OMRM. Sher et al. (2021) realizaram uma revisão sistemática para avaliar a segurança da instalação de implantes em pacientes com histórico de terapia com antirreabsortivos, e os resultados demonstraram que terapia prévia com BFs para osteoporose não aumentam a falha do implante em relação à osseointegração, contudo, todos os pacientes com história de tratamento com BFs (EV ou VO) parecem estar em risco de osteonecrose da mandíbula relacionada à medicação desencadeada por cirurgia de implante.
CONCLUSÃO/CONSIDERAÇÕES FINAIS
Os BFs são importantes agentes terapêuticos para uma série de doenças relacionadas ao descompasso da reabsorção óssea, porém esse fármaco pode predispor os pacientes a uma complicação de difícil manejo, a osteonecrose dos maxilares. Essa condição pode iniciar de forma espontânea, mas na maioria das vezes está relacionada à uma injúria local. A instalação de implantes dentários em pacientes sob terapia com antirreabsortivos deve sempre ser ponderada, e algumas características do fármaco, e outras inerentes ao próprio indivíduo podem aumentar as chances de OMRM.
Fatores que aumentam o risco de desenvolvimento de OMRM:
• BFs administrado por via endovenosa;
• Pacientes com neoplasia maligna e mieloma múltiplo como doença base;
• Droga mais potente: ácido zoledrônico;
• Valor de CTX: < 150 pg/ml;
• Tempo de uso de BFs VO maior que três anos ou associado a corticoide; Sítio do implante: região posterior de mandíbula.
Com base na literatura, e dentro das limitações deste trabalho, é possível afirmar que o uso de BFs não é uma contraindicação absoluta para a instalação de implantes, porém, cabe ao implantodontista a avaliação do risco benefício após considerar todos os fatores predisponentes ao desenvolvimento da OMRM.
Outros estudos clínicos e de acompanhamento à longo prazo são necessários para testificar ou refutar as informações disponíveis até o momento.
REFERÊNCIAS
AAOMS. American Association of oral and Maxillofacial Surgeons Position Paper on Bisphosphonate – Related Osteonecrosis of the Jaws. J Oral Maxillo Fac Surg. v. 65, p. 369-376, 2007.
AGUIRRE, J. I.; CASTILLO, E. J.; KIMMEL, D. B. Biologic and pathologic aspects of osteocytes in the setting of medication-related osteonecrosis of the jaw (MRONJ). Bone, v. 153, p. 116168, 2021.
CALDAS, R. J.; DE MENEZES PONTES, J. R.; ANTUNES, F. S. Osteonecrose dos maxilares induzida por bisfosfonatos: relato de caso clínico. Revista Brasileira de Cancerologia, v. 55, n. 2, p. 151-155, 2009.
CAVAZANA, T. Efeito do ácido zoledrônico sobre o reparo dos tecidos moles sobrejacentes ao sítio de extração dental: estudo envolvendo os principais fatores de risco para o desenvolvimento de osteonecrose dos maxilares. 2015.
COLÉTE, J. Z. et al. Implantes em pacientes com osteonecrose dos maxilares associados ao uso de bifosfonatos: relato de caso e revisão da literatura. Arco. Investir na Saúde , pág. 20-27, 2019.
DE CARVALHO, P. S. P. et al. Principais aspectos da cirurgia bucomaxilofacial no paciente sob terapia com bifosfonatos. Revista da Faculdade de Odontologia UPF, v. 15, n. 2, 2010.
DE JESUS, A. P. et al. Tratamento cirúrgico para osteonecrose dos maxilares induzida por bisfosfonatos: relatos de casos. Revista da Faculdade de Odontologia-UPF, v. 24, n. 1, p. 22-30, 2019.
DE-FREITAS, N. R. et al. Bisphosphonate treatment and dental implants: A systematic review. Medicina oral, patologia oral y cirugia bucal, v. 21, n. 5, p. e644, 2016.
FICARRA, G.; BENINATI, F.. Bisphosphonate-related osteonecrosis of the jaws: an update on clinical, pathological and management aspects. Head and neck pathology, v. 1, n. 2, p. 132-140, 2007.
FLEISCH, H. Bisphosphonates–history and experimental basis. Bone, v. 8, p. S238, 1987.
GEGLER, A. et al. Bisfosfonatos e osteonecrose maxilar: revisão da literatura e relato de dois casos. Revista brasileira de cancerologia , v. 52, n. 1, pág. 2531, 2006.
GRANT, Bao-Thy et al. Outcomes of placing dental implants in patients taking oral bisphosphonates: a review of 115 cases. Journal of Oral and Maxillofacial Surgery, v. 66, n. 2, p. 223-230, 2008.
HE, L. et al. Pathogenesis and multidisciplinary management of medication related osteonecrosis of the jaw. International journal of oral science, v. 12, n. 1, p. 1-11, 2020.
HOFF, A O. et al. Frequency and risk factors associated with osteonecrosis of the jaw in cancer patients treated with intravenous bisphosphonates. Journal of Bone and Mineral Research, v. 23, n. 6, p. 826-836, 2008.
LAZAROVICI, Towy Sorel et al. Bisphosphonate-related osteonecrosis of the jaw associated with dental implants. Journal of Oral and Maxillofacial Surgery, v.68, n. 4, p. 790-796, 2010.
MARTINS, M. A. et al. Osteonecrose dos maxilares associada ao uso de bisfosfonatos: importante complicação do tratamento oncológico. Revista Brasileira de Hematologia e Hemoterapia, v. 31, p. 41-46, 2009.
MARX, R. E. et al. Bisphosphonate-induced exposed bone (osteonecrosis/osteopetrosis) of the jaws: risk factors, recognition, prevention, and treatment. Journal of oral and maxillofacial surgery, v. 63, n. 11, p. 1567-1575, 2005.
MARX, R. E. Pamidronate (Aredia) and zoledronate (Zometa) induced avascular necrosis of the jaws: a growing epidemic. Journal of oral and maxillofacial surgery, v. 61, n. 9, p. 1115-1117, 2003.
MARX, R. E.; CILLO JR, J. E..; ULLOA, J. J. Oral bisphosphonate-induced osteonecrosis: risk factors, prediction of risk using serum CTX testing, prevention, and treatment. Journal of Oral and Maxillofacial Surgery, v. 65, n. 12, p. 2397-2410, 2007.
MATTIS, F.; GOMES, F. V.; MAYER, L. Perda tardia de implante dentário devido a osteonecrose associada ao uso de bisfosfonatos: relato de caso clínico. Revista da AcBO-ISSN 2316-7262, v. 5, n. 1, 2016.
MAURI, Davide et al. Osteonecrosis of the jaw and use of bisphosphonates in adjuvant breast cancer treatment: a metanalysis. Breast cancer research and treatment, v. 116, n. 3, p. 433-439, 2009.
MENEZES, I. L. et al. Terapia fotodinâmica no tratamento de osteonecrose mandibular por bisfosfonatos: uma revisão. Brazilian Journal of Health Review, v. 4, n. 1, p. 2652-2665, 2021.
MIGLIORATI, C. A. et al. Managing the care of patients with bisphosphonate associated osteonecrosis: an American Academy of Oral Medicine position paper. The Journal of the American Dental Association, v. 136, n. 12, p. 1658-1668, 2005.
OLIVEIRA, G. M. B. et al. O impacto dos bisfofonatos e seus efeitos negativos no osso alveolar de pacientes reabilitados pela implantodontia–Revisão de literatura. Jornada Odontológica dos Acadêmicos da Católica, v. 3, n. 1, 2017.
ROSELLA, D. et al. Medication-related osteonecrosis of the jaw: Clinical and practical guidelines. Journal of International Society of Preventive & Community Dentistry, v. 6, n. 2, p. 97, 2016.
RUGANI, P. et al. Conceito de tratamento relacionado ao estágio da osteonecrose da mandíbula relacionada a medicamentos – uma série de casos. Investigações clínicas orais , v. 19, n. 6, pág. 1329-1338, 2015.
RUGGIERO, S. L. Bisphosphonaterelated osteonecrosis of the jaw: an overview. Annals of the New York Academy of Sciences, v. 1218, n. 1, p. 3846, 2011.
RUGGIERO, S. L. et al. American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw—2014 update. Journal of oral and maxillofacial surgery, v. 72, n. 10, p. 1938-1956, 2014.
RUGGIERO, S. L. et al. American Association of Oral and Maxillofacial Surgeons position paper on bisphosphonate-related osteonecrosis of the jaws—2009 update. Journal of Oral and Maxillofacial Surgery, v. 67, n. 5, p. 2-12, 2009.
RUGGIERO, S. L.; WOO, S.. Biophosphonate-related osteonecrosis of the jaws. Dental Clinics of North America, v. 52, n. 1, p. 111-128, 2008.
RUGGIERO, Salvatore L.; FANTASIA, John; CARLSON, Eric. Bisphosphonaterelated osteonecrosis of the jaw: background and guidelines for diagnosis, staging and management. Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology, and Endodontology, v. 102, n. 4, p. 433-441, 2006.
SHER, J. et al. Dental implant placement in patients with a history of medications related to osteonecrosis of the jaws: a systematic review. Journal of Oral Implantology, v. 47, n. 3, p. 249-268, 2021.
STRAMANDINOLI-ZANICOTTI, Roberta Targa et al. Implantes dentários em pacientes usuários de bifosfonatos: o risco de osteonecrose e perda dos implantes é real? Relato de três casos clínicos. RSBO: Revista Sul-Brasileira de Odontologia, v. 15, n. 1, 2018
1 Acadêmico do Curso Superior de Odontologia da Universidade Evangélica de Goiás, Anápolis-GO E-mail: luis.correa@aluno.unievangelica.edu.br
2 Acadêmico do Curso Superior de Odontologia da Faculdade Anhanguera de Anápolis, Anápolis-GO E-mail: joaokleber_si@hotmail.com
3 Professora especialista do curso superior de Odontologia da Faculdade Anhanguera de Anápolis, Anápolis-GO E-mail: ludymillalopes@yahoo.com.br
