REGISTRO DOI: 10.69849/revistaft/pa10202410231430
Darlene Glória Da Silva Lopes Antunes
Orientador(a): Profª. Caroline Gomes Carvalho
Coorientador(a): Prof.ª Drª. Karime Tavares Lima Da Silva
RESUMO
O estudo detalha a etiologia da doença, os medicamentos associados, os fatores de risco, as características clínicas e o diagnóstico, além das estratégias de prevenção e tratamento. A OMAM ocorre principalmente em pacientes que usam esses medicamentos para tratar condições como osteoporose e câncer, devido à inibição da remodelação óssea e da angiogênese. Explora a falta de consenso na literatura sobre o diagnóstico e tratamento da OMAM, enfatizando a importância do conhecimento dos cirurgiões-dentistas sobre os medicamentos envolvidos e o manejo adequado. O trabalho revisa a literatura científica sobre o tema e propõe que a prevenção, incluindo uma avaliação odontológica detalhada antes do início do tratamento com esses medicamentos, é crucial para reduzir os riscos da osteonecrose. O tratamento, por sua vez, varia desde abordagens conservadoras com uso de antibióticos e higiene bucal rigorosa até intervenções cirúrgicas mais agressivas, dependendo do estágio da doença. A terapia fotodinâmica é mencionada como uma técnica auxiliar promissora para o tratamento. Em suas considerações finais, o estudo destaca a necessidade de diagnósticos precoces e abordagens preventivas rigorosas para evitar complicações severas.Palavras-chaves: Difosfonatos. Osteonecrose. Maxilares. Medicamentos.
ABSTRACT
The study details the etiology of the disease, associated medications, risk factors, clinical characteristics and diagnosis, in addition to prevention and treatment strategies. MAOM occurs mainly in patients using these medications to treat conditions such as osteoporosis and cancer, due to the inhibition of bone remodeling and angiogenesis. It explores the lack of consensus in the literature on the diagnosis and treatment of AOM, emphasizing the importance of dental surgeons’ knowledge of the medications involved and appropriate management. The work reviews the scientific literature on the topic and proposes that prevention, including a detailed dental evaluation before starting treatment with these medications, is crucial to reducing the risks of osteonecrosis. Treatment, in turn, ranges from conservative approaches with the use of antibiotics and strict oral hygiene to more aggressive surgical interventions, depending on the stage of the disease. Photodynamic therapy is mentioned as a promising auxiliary technique for treatment. In its final considerations, the study highlights the need for early diagnosis and rigorous preventive approaches to avoid severe complications.
Keywords: Diphosphonates. Osteonecrosis. Jaws. Medicines.
1 INTRODUÇÃO
A Osteonecrose dos Maxilares Associada a Medicamentos (OMAM) caracteriza-se pela necrose vascular do osso maxilofacial, potencialmente dolorosa e incapacitante, em pacientes com histórico de uso ou em uso contínuo de bifosfonatos intravenosos, antirreabsortivos ou antiangiogênicos, e sem história de exposição à radioterapia de cabeça e pescoço. A OMAM apresenta incidência global de 1 a 8%, clinicamente pode se manifestar com dor, inflamação, mobilidade, eritema, supuração, exposição óssea e a formação de fístulas não cicatrizadas (Di et al., 2021; Filgueira et al., 2019; Eguia et al., 2020; Bullock et al., 2022).
Os antirreabsortivos, como bifosfonatos e denosumabe, são fármacos que regulam a calcificação e a reabsorção óssea, e seus mecanismos de ação incluem a inibição de osteoclastos, direta ou indiretamente, resultando na redução da capacidade de remodelação óssea e no desenvolvimento de necrose em áreas sujeitas a trauma. Enquanto os antiangiogênicos inibem fator de crescimento que atuam indiretamente na formação de osteoclastos e osteoblastos, diminuem o suprimento vascular, aumentando a probabilidade de isquemia tecidual (Chaves et al., 2018).
Observa-se na literatura científica a falta de consenso sobre métodos diagnóstico e formas de tratamento que precisam ser esclarecidas, para uma compreensão mais detalhada sobre o assunto. Atualmente, entende-se que o conhecimento do cirurgião-dentista sobre a terapia medicamentosa é de extrema importância, considerando a necessidade de compreender as limitações do paciente exposto à esse tipo de terapia.
Desta forma, o presente estudo tem por objetivo realizar uma revisão de literatura, a fim de descrever a etiologia, diagnóstico, classificação, características clínicas, assim como opções de tratamento e possíveis complicações associadas a OMAM.
2 METODOLOGIA
Para o estudo, foi realizado uma revisão bibliográfica, utilizando artigos publicados em inglês e português nas bases de dados como: Scientific Eletronic Library Online (SciELO), National Library of Medicine (PubMed), Google Acadêmico e Biblioteca Virtual em Saúde (BVS). Os Descritores em Ciência da Saúde (DeCS), utilizados foram: “Difosfonatos”, “Osteonecrose” e “Osteonecrose da Arcada Osseodentaria Associada a Difosfonato” sendo a cronologia dos artigos compreendendo de 2014 a 2024. Os critérios de inclusão foram textos completos, nos idiomas português e inglês, conforme a temática proposta, publicados em revistas científicas, compreendendo pesquisas longitudinais, observacionais, descritivas, transversais, qualitativas, quantitativas, relato de caso e revisão de literatura, com os textos concedidos gratuitamente nas bases de dados. Os critérios de exclusão foram artigos incompletos, não identificados nas bases de dados, duplicados, não abordando a temática proposta, e aqueles publicados em anos anteriores aos citados na cronologia.
3 DESENVOLVIMENTO
3.1 Definição e etiologia da OMAM
A OMAM acontece quando há uma diminuição no suprimento sanguíneo, fazendo com que o tecido ósseo perca sua capacidade de se remodelar devido à falta de angiogênese. Isso resulta em uma área necrótica na região onde foi realizada a intervenção (Figura 01). Essa condição pode ser provocada por intervenções traumáticas e infecções, estando também ligada ao uso contínuo de bisfosfonatos, antirreabsortivos e/ou antiangiogênicos (Dos Santos et al., 2020).
Figura 01: Imagem intrabucal apresentando extensa exposição do osso necrótico em região de rebordo alveolar maxilar anterior.
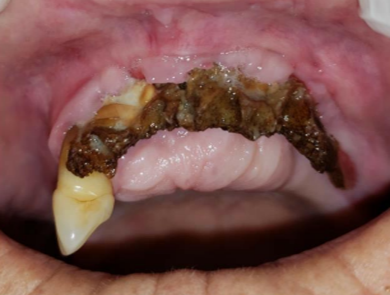
Fonte: Dos Santos et al., 2020.
A OMAM é uma condição que afeta tanto a maxila quanto a mandíbula, embora 65% dos casos ocorram predominantemente na mandíbula. Apenas 26% dos casos são registrados na maxila, e 9% envolvem ambas as estruturas. Clinicamente, observam-se áreas de osso exposto com necrose e secreção purulenta (Figura 02), que não cicatrizam rapidamente, em pacientes que fazem uso contínuo de bisfosfonatos, sem histórico de radioterapia. Os pacientes podem relatar dor, dificuldade na mastigação e parestesias, o que resulta em uma redução significativa na qualidade de vida (Sousa, et al., 2018).
Figura 02: Clinicamente, área óssea alveolar vestibular dos dentes pré-moalres e molares, e histologia de osso necrótico compatível com OMAM na mandíbula.
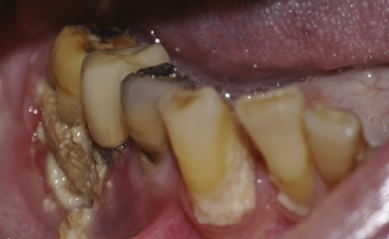
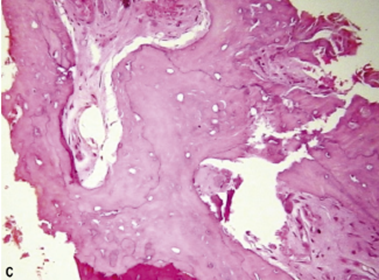
Fonte: Galitis et al.(2019, p. 118 e 123).
De acordo com a American Association of Oral and Maxillofacial Surgeons (AAOMS) em 2014 sobre a OMAM, foram estabelecidos os seguintes critérios para diagnóstico: presença de área de osso exposto ou osso que pode ser sondado através de uma fístula intra ou extraoral, surgida espontaneamente ou após cirurgia na região maxilofacial, que persista por 8 semanas ou mais; uso atual ou prévio de medicações antirreabsortivas ou antiangiogênicas; e ausência de histórico de radioterapia na região maxilofacial ou de evidência clara de doença metastática nos maxilares (Ruggiero et al., 2014).
Na oncologia, o principal objetivo da terapia com bisfosfonatos (BFF) é preservar ou melhorar a qualidade de vida dos pacientes. Pesquisadores acreditam que a OMAM pode ocorrer porque os BFF impedem o corpo de reparar danos microscópicos na mandíbula. O risco de desenvolver OMAM está relacionado à dose acumulada e à potência do agente. Consequentemente, pacientes com câncer são mais propensos a desenvolver OMAM do que aqueles com osteoporose, pois recebem agentes mais potentes e em doses mais frequentes (Gómez-Moreno G. et al., 2014).
3.2 Medicamentos Associados à Osteonecrose dos maxilares
Doenças como a osteoporose, a Doença de Paget e neoplasias, com ou sem metástases ósseas, afetam o metabolismo ósseo, gerando um desequilíbrio no processo de remodelação que provoca uma reabsorção excessiva, levando à redução da densidade e qualidade dos ossos. Para enfrentar esse problema, surgiram medicamentos antirreabsortivos e antiangiogênicos, cujo objetivo é reduzir essa reabsorção patológica (Bicudo, 2017).
3.2.1 Antirreabsortivos
Os fármacos antirreabsortivos são medicamentos amplamente utilizados no tratamento de doenças que envolvem a perda excessiva de massa óssea, como osteoporose, doença de Paget, metástases ósseas e hipercalcemia maligna. Sua principal função é reduzir a reabsorção óssea, preservando a densidade mineral dos ossos e prevenindo fraturas. Os antirreabsortivos mais comuns incluem os bisfosfonatos, o denosumabe e, em menor escala, moduladores seletivos do receptor de estrogênio (SERMs) (Menezes et al., 2021).
Os antirreabsortivos são indicados para diversas condições que afetam a saúde óssea. Na osteoporose, por exemplo, são prescritos para prevenir fraturas em indivíduos com baixa densidade óssea, especialmente em mulheres pós-menopáusicas e homens idosos. Eles também são usados no tratamento de doenças osteolíticas, como a doença de Paget e metástases ósseas, onde ajudam a controlar a destruição óssea causada por tumores. Além disso, são eficazes em controlar a hipercalcemia associada a malignidades (Ruggiero et al., 2014).
3.2.1.1 Bisfosfonatos
Os BFF são medicamentos antirreabsortivos, semelhantes ao pirofosfato, que reduzem amineralização óssea de maneira dependente da dose. Isso ocorre devido à inibição das vias que recrutam os osteoclastos, células responsáveis pela reabsorção óssea. Ao acelerar a apoptose dessas células, os BFF diminuem a taxa de remodelação óssea nas áreas afetadas pela reabsorção. Indicados para tratamento de doenças ósseas e metastáticas (Dias et al., 2016).
Eles atuam diminuindo a reabsorção óssea de maneira proporcional à dose, bloqueando a formação ou recrutamento dos osteoclastos, inibindo sua função e/ou promovendo sua apoptose, além de estimular a atividade dos osteoblastos. Esses medicamentos têm baixa lipossolubilidade, sendo apenas uma fração absorvida pelo trato gastrointestinal. Eles deixam o plasma rapidamente, com metade se depositando nos tecidos ósseos nas áreas de mineralização, onde podem permanecer por meses ou até anos até serem reabsorvidos, apresentando um efeito residual de 10 anos, no mínimo, após suspensão do uso. A outra parte, sem sofrer modificações, é excretada pelos rins (Sales & da Conceição, 2020).
Esses medicamentos agem primariamente inibindo a atividade dos osteoclastos, células responsáveis pela reabsorção óssea. No caso dos bisfosfonatos, eles são incorporados à matriz óssea e, ao serem reabsorvidos pelos osteoclastos durante o processo de degradação óssea, interrompem seu ciclo de vida, acelerando sua apoptose (morte celular programada). Isso resulta em uma redução na reabsorção óssea e, consequentemente, no aumento da densidade óssea (Dantas & da Silva, 2022).
3.2.1.2 Desonumabe
Medicamentos, como o Desonumabe, é um inibidor do RANKL, uma molécula que ativa os osteoclastos durante o processo de reabsorção óssea. Este medicamento não apresenta efeito residual, ou seja, uma vez que suspende o uso, a função dos osteoclastos é reestabelecida. Ainda, foi desenvolvido como uma alternativa ao alendronato e a medicamentos antiangiogênicos (Dos Santos et al., 2020).
Embora o Denosumabe tenha um amplo espectro de ação, seu uso pode levar ao desenvolvimento de reações adversas, que variam em frequência e sintomas. Exemplos incluem infecções do trato urinário, reações anafiláticas, hipocalcemia, desconforto abdominal, erupções cutâneas e dor musculoesquelética. Ademais, a osteonecrose dos maxilares é um dos principais eventos adversos de relevância para a odontologia (Dantas & da Silva, 2022).
3.2.2 Antiangiogênicos
O antiangiogênicos são medicamentos que impedem o crescimento e a formação de novos vasos sanguíneos, minimizando as chances de metástases tumorais em pacientes oncológicos. A osteonecrose dos maxilares associada a agentes antiangiogênicos (OMAA) ocorre pela interferência na angiogênese do processo de reparo ósseo, levando à diminuição do fluxo sanguíneo nos ossos maxilares e resultando em contaminação bacteriana do osso exposto (Caminha et al, 2019).
O processo de angiogênese é responsável pela formação e crescimento de novos vasos sanguíneos, características essenciais para a progressão de várias doenças, especialmente as oncológicas. Esse processo é regulado por sinais químicos do corpo, sendo o fator de crescimento endotelial vascular (VEGF) o mais importante. O VEGF se liga a receptores nas células endoteliais, que revestem a parte interna dos vasos, promovendo a angiogênese e alterando o equilíbrio da formação vascular. Os medicamentos antiangiogênicos agem bloqueando a ação direta ou indireta do VEGF. Alguns deles, como o bevacizumabe, um anticorpo monoclonal, inibem a ligação do VEGF às células endoteliais. Outros, como o sunitinibe, atuam internamente, impedindo que os receptores de VEGF enviem sinais para as células endoteliais, sendo considerados inibidores da tirosina-quinase (Jung et al., 2017).
3.3 Fatores de risco
O risco de desenvolver OMAM associada ao uso de BFF orais tende a aumentar após três anos de tratamento. Esse risco pode ser agravado pela presença de certas comorbidades, como o uso crônico de corticosteroides (Dorigan et al., 2021), indivíduos com diabetes mellitus, podendo causar alterações isquêmicas nos microvasos, reduzir a atividade das células endoteliais, levar à destruição de células ósseas e diminuir o metabolismo.
Além disso, indivíduos com alterações sistêmicas como doenças malignas, consumidores de álcool de forma crônica, pacientes imunossuprimidos, com doenças autoimunes, condições hematopoiéticas alteradas, doenças vasculares periféricas e problemas renais (Kim. et al., 2016).
Pacientes em quimioterapia com inibidores da divisão celular, corticosteroides e aqueles que recebem transfusões de células-tronco têm maior predisposição ao desenvolvimento de OMAM relacionada a BFF em comparação com outros, devido à imunidade comprometida e ao fluxo sanguíneo reduzido causado pela transformação da medula óssea (Kim. et al., 2016).
3.4 Características Clínicas e Diagnóstico
Clinicamente, a OMAM é caracterizada por mucosa ulcerada e osso exposto e desvitalizado. Além disso, os tecidos ao redor geralmente apresentam inflamação devido a infecções secundárias da mucosa. Sinais e sintomas como dor, desconforto oral, secreções purulentas, exsudatos e fístulas são comuns. A extração dentária é frequentemente realizada antes do surgimento da OMAM, embora doenças periodontais, implantes dentários e próteses mal ajustadas também sejam relatados como possíveis causas (Bullock et al., 2022).
Devido ao comprometimento ósseo causado pela osteonecrose, exames de imagem como radiografias panorâmicas, tomografias computadorizadas e tomografias computadorizadas de feixe cônico são amplamente empregados para auxiliar no diagnóstico preciso, orientação e determinação do estágio das lesões (Oliveira et al., 2020).
3.5 Prevenção e Tratamento da OMAM
O cuidado odontológico preventivo antes e durante a terapia com BFFs, antirreabsortivos e/ou antiangiogênicos reduz em cerca de 50% o risco de desenvolver osteonecrose dos maxilares, sendo comparável, por exemplo, ao preparo de um paciente que será submetido a uma cirurgia cardíaca. A avaliação do risco individual exige que o cirurgião-dentista compreenda fatores relacionados aos medicamentos, como as principais drogas associadas ao risco de OMAM, seus mecanismos de ação, indicações e a capacidade de incorporação óssea (Wan et al.,2020).
É consenso entre os especialistas que a prevenção é essencial para pacientes que estão prestes a iniciar, já estão em curso, ou já concluíram o tratamento com medicamentos antirreabsortivos, como os BFFs. Para isso, a avaliação do risco de desenvolvimento de osteonecrose dos maxilares é fundamental, permitindo um planejamento adequado e diminuindo as chances de complicações. Essa avaliação é feita por meio de uma anamnese detalhada, exame clínico e exames complementares minuciosos, com posterior classificação de risco e adequação do meio bucal, eliminando fontes de trauma e infecções dentoalveolares (Dorigan et al., 2021).
Além disso, uma anamnese detalhada é essencial para obter informações cruciais, como a via de administração (oral ou intravenosa), tempo de uso, dose, potência do medicamento, frequência de uso e datas da última e próxima administração. Fatores relacionados à saúde do paciente também devem ser considerados, como comorbidades sistêmicas, por exemplo, diabetes ou pacientes em tratamento quimioterápico, que podem ter a cicatrização prejudicada, aumentando o risco de osteonecrose. O uso de medicamentos como antitrombóticos e anticoagulantes também pode elevar o risco por interferir no processo de cicatrização (Wan et al.,2020).
O principal objetivo no manejo da OMAM deve ser controlar a infecção, a progressão da necrose óssea e a dor. Se a OMAM ocorrer enquanto o paciente estiver recebendo altas doses desses medicamentos, a continuidade do tratamento deve ser discutida com todos os envolvidos, considerando a gravidade e evolução da OMAM, a extensão da doença oncológica, a atividade da doença e os desejos do paciente (Galitis et al., 2019).
As abordagens conservadoras de tratamento incluem manter uma higiene oral rigorosa, eliminar doenças dentárias e periodontais ativas, além de utilizar enxaguantes bucais antibacterianos tópicos e antibióticos sistêmicos, conforme indicado pelas diretrizes locais. Essas estratégias são recomendadas para casos em que não há progressão evidente da doença, dor não controlada, ou quando a interrupção do tratamento com BFF ou denosumabe não é necessária devido à osteonecrose dos maxilares (Galitis et al., 2019)
Além das condutas recomendadas pela AAOMS, também existem terapias auxiliares que têm sido amplamente utilizadas e descritas na literatura para o manejo da osteonecrose dos maxilares, como a terapia fotodinâmica. O dessa terapia na odontologia é bastante diversificado, sendo aplicado em tratamentos de lesões em tecidos moles, por exemplo. No contexto da osteonecrose dos maxilares, o laser de baixa potência atua em duas fases: primeiro, ele ativa os osteoblastos, estimulando a produção de matriz óssea; em seguida, reduz a atividade dos osteoblastos por meio de mecanismos fisiológicos e estimula os osteoclastos, promovendo a reabsorção óssea e o consequente processo de remodelação, isto associado ao azul de metileno que possui capacidade antibacteriana (Menezeset al., 2021).
Quando ocorre a osteonecrose, o tratamento tem como principal objetivo o fechamento da ferida cirúrgica e o controle da dor e de infecções secundárias. O manejo deve ser baseado no estadiamento da lesão necrótica e nas condições sistêmicas do paciente, especialmente em casos como os de pacientes em tratamento oncológico, que podem exigir abordagens específicas para tratar a osteonecrose. Vale destacar que a terapia deve ser ajustada sempre que houver progressão da condição (Ruggiero et al., 2014).
Figura 03: A, Exposição óssea da região superir esquerda. B, Pré-operatório. Exploração mostrando demarcação do sequestro ósseo. C, Remoção da região óssea necrosada. D, Retalho reposicionado com fechamento da oclusal. E, Pós-operatório depois de 6 meses.
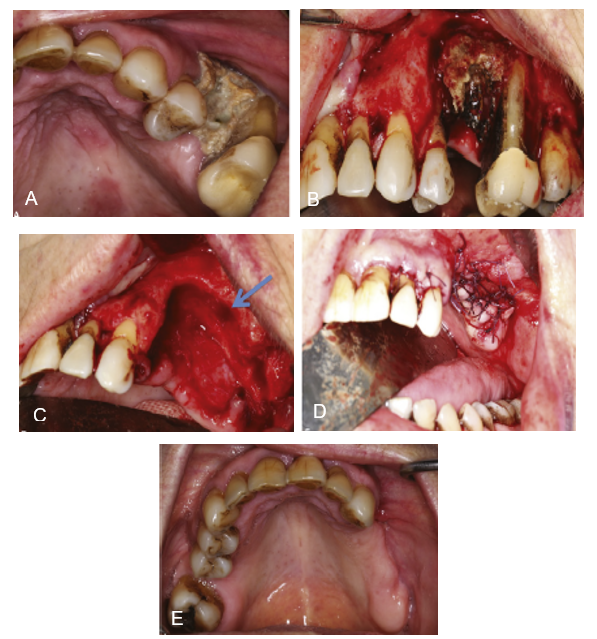
Fonte: Galitis et al. (2019, p. 128).
A AAOMS desenvolveu um protocolo com condutas recomendadas para o tratamento da complicação, que variam conforme o estágio da doença. No estágio 0, os pacientes são assintomáticos, mas apresentam fatores de risco; o recomendado é o acompanhamento clínico e orientações sobre higiene bucal. No estágio I, há a presença de osteonecrose assintomática, sem sinais de infecção; o tratamento envolve antibióticos e, se necessário, desbridamento local. No estágio II, os pacientes apresentam osteonecrose sintomática com infecção; o tratamento inclui antibióticos, desbridamento cirúrgico, cuidados com a higiene bucal e manejo da dor. Por fim, no estágio III, a osteonecrose é extensa, com infecção e perda óssea significativa. Nesse caso, intervenções cirúrgicas mais agressivas podem ser necessárias, incluindo a resecção da área afetada e, em algumas situações, a reconstrução óssea. O acompanhamento regular e a avaliação do risco são fundamentais em todos os estágios, sendo essencial discutir as opções de tratamento com um especialista, considerando as particularidades de cada paciente (Dorigan et al., 2021).
Esse protocolo pode ser combinado com terapias como fotodinâmica, laserterapia e ozonioterapia. O uso de fluorescência durante procedimentos cirúrgicos para diferenciar o osso saudável do necrótico tem mostrado grande eficácia, preservando o osso viável. Com isso, temos protocolos, terapias auxiliares e técnicas que apresentam alta taxa de sucesso no atingimento dos objetivos principais do tratamento (Oliveira et al., 2020).
Se as condições sistêmicas do paciente permitirem, o dentista deve considerar interromper a administração oral de BFFs por três meses antes e depois de uma intervenção cirúrgica dentária invasiva, a fim de minimizar a probabilidade de desenvolvimento de OMAM relacionada aos BFFs (Dorigan et al., 2021).
4 DISCUSSÃO
A primeira questão levantada é a dificuldade no diagnóstico precoce da OMAM, especialmente devido à ampla variedade de sintomas e à necessidade de exames complementares para identificar o comprometimento ósseo, como radiografias e tomografias. Estudos mostram que, em muitos casos, a OMAM é detectada apenas em estágios avançados, quando o paciente já apresenta dor intensa e exposição óssea. A American Association of Oral and Maxillofacial Surgeons (AAOMS) estabeleceu critérios diagnósticos baseados na presença de osso exposto por mais de oito semanas sem histórico de radioterapia na região maxilofacial (Ruggiero et al., 2014).
Com etiologia ainda pouco esclarecida, mas amplamente discutida na literatura, acredita-se que certos fatores específicos possam favorecer o desenvolvimento dessa condição. Entre eles, destacam-se características particulares da droga, como a inibição da renovação óssea e seu efeito antiangiogênico, além de aspectos como a dosagem, a via de administração, o tempo de uso, a patologia a ser tratada e a presença de fatores de risco locais e sistêmicos (Dantas & da Silva, 2022).
O tratamento da OMAM varia de acordo com o estágio da doença e as condições sistêmicas do paciente. Abordagens conservadoras são recomendadas, incluindo o uso de enxaguantes bucais antibacterianos e antibióticos para controlar infecções. Em casos mais graves, a cirurgia pode ser necessária para remover o osso necrótico. Um avanço significativo no tratamento inclui a utilização de laserterapia, que tem demonstrado ser eficaz na estimulação da regeneração óssea. Estudos indicam que a laserterapia pode ser utilizada como uma terapia auxiliar, promovendo a cicatrização e diminuindo a dor (Menezes et al., 2021).
Em relação à prevenção, o estudo destaca a importância de cuidados odontológicos rigorosos antes e durante o tratamento com bifosfonatos. A prevenção inclui a realização de uma anamnese detalhada, que deve considerar fatores como o tempo de uso dos medicamentos, sua via de administração e a presença de comorbidades, como diabetes e imunossupressão. Estudos ressaltam que o risco de desenvolvimento de OMAM aumenta significativamente após três anos de uso de bifosfonatos (Dorigan et al., 2021).
5 CONSIDERAÇÕES FINAIS
O conhecimento detalhado dos cirurgiões-dentistas sobre os medicamentos que podem causar osteonecrose dos maxilares é essencial para a prevenção e manejo da condição. Medicamentos como bisfosfonatos e denosumabe, aliados a fatores de risco locais e sistêmicos, são os principais causadores. O diagnóstico precoce e a prevenção, com acompanhamento rigoroso, são fundamentais para evitar complicações. Tratamentos conservadores e terapias, como a terapia fotodinâmica, têm se mostrado eficazes, mas é necessário adaptar as abordagens ao perfil do paciente. Mais estudos são recomendados para aprimorar o tratamento e a prevenção.
REFERÊNCIAS
ALMEIDA, Arthur Caetano de. et al. Tratamento da osteonecrose dos maxilares associada ao uso de medicamentos-revisão de literatura. 2021.Disponível em: Brazilian Journal of Otorhinolaryngology, v. 84, p. 102-108, 2018
Bicudo, L. L. (2017) Osteonecrose dos Maxilares: prevenção e manejo. Palestra. II Congresso Brasileiro de Odontologia Hospitalar e Intensiva. Curitiba, SP.
BULLOCK, George et al. A review into the effects of pamidronic acid and zoledronic acid on the oral mucosa in medication-related osteonecrosis of the jaw. Frontiers in Oral Health, v. 2, p. 822411, 2022.
CAMINHA, Raquel D’Aquino et al. Perfil de risco para osteonecrose dos maxilares associada a agentes antiogiogêncios. Einstein, 2019.
CHAVES RAC, Queiroz TP, Faloni APS. Bifosfonatos e denosumabes: mecanismos de ação e algumas implicações para a implantodontia. RebraM.2018;21(2):66-80.
DANTAS,Rebeca Carolina Moraes; DA SILVA, Aline Santos. DENOSUMABE E OSTEONECROSE DOS MAXILARES: O QUE O CIRUGIÃO-DENTISTA PRECISA SABER?. Revista Ciência Plural, 2022.
DIAS DHS, et al. Osteonecrose associada ao uso de alendronato de sódio: relato de caso. Rev Higei, 2016.
DI FEDE, O., Canepa, F., Panzarella, V., Mauceri, R., Del Gaizo, C., Bedogni, A., & Galvano, A. The Treatment of Medication-Related Osteonecrosis of the Jaw (MRONJ): A Systematic Review with a Pooled Analysis of Only Surgery versus Combined Protocols. International Journal of Environmental Research and Public Health, 2021, 18(16), 8432.
DORIGAN, Maria Caroline et al. A osteonecrose dos maxilares induzida por bifosfonatos:uma revisão de literatura. Research, Society and Development, v. 10, n.16, e92101623466, 2021.
DOS SANTOS, Wanderley Barros et al. Osteonecrose dos Maxilares associada ao uso crônico de bisfosfonatos: relato de caso. Revista Eletrônica Acervo Saúde / Electronic Journal Collection Health, 2020.
EGUIA, Asier; BAGAN, Leticia; CARDONA, Francisco. Review and update on drugs related to the development of osteonecrosis of the jaw. Medicina oral, patologia oral y cirugia bucal, v. 25, n. 1, p. e71, 2020
FERNEINI, E. M. Medication-related osteonecrosis of the jaw (MRONJ). Journal of Oral and Maxillofacial Surgery, 2021, 79(8), 1801-1802
FILGUEIRA, Sônia Luiza et al. Manifestações clínicas da osteonecrose induzida por medicamentos. Ciência Atual–Revista Científica Multidisciplinar do Centro Universitário São José, v. 13, n. 1, 2019.
FORTE ACCB, Frascino AVM. Interação dos bisfosfonatos na cirurgia odontológica. Atlas de Ciências da Saúde. 2016; 4(1):12-22.
GALITIS, Ourania Nicolatou et al. Medication-related osteonecrosis of the jaw: definition and best practice for prevention, diagnosis, and treatment. ORAL MEDICINE, Vol. 127 No. 2 February 2019.
Gómez-Moreno, G. et al. Bisphosphonate-associated osteonecrosis of the jaw 2 years after teeth extractions: a case report solved with non-invasive treatment. EuropeanReview for Medical and Pharmacological Sciences, (18), pp. 1391-1397, 2014.
Jung TY. Osteonecrosis of jaw after antiangiogenic agent administration in a renal cell carcinoma patient. Oral and Maxillofacial Surgery Cases. 2017;3(2):27-33.
Kim, T-H. et la. Evaluation of the predisposing factors and involved outcome of surgical treatment in bisphosphonate-related osteonecrosis of the jaw cases. J Korean Assoc Oral Maxillofac Surg, 2016.
Menezes, I. L., Sales, J. M., Targino, M. L. de M., Vasconcelos, R. G.&Marinho, S. A. Terapia fotodinâmica no tratamento de osteonecrose mandibular porBisfosfonatos:uma revisão. Brazilian Journal of Health Review, 4(1), 2652-2665, 2021.
Oliveira, M. E. de F. S., Líbera, J. D. L., Lucatto, N. F., Carvalho, M. M. de, Oliveira, L. F., Santana, M. R. de O., Villela-Rosa, A. C. M.&Simonato, L. E. Aspectos radiográficos da osteonecrose em maxilares por bisfosfonatos. Rev Odontol UNESP. 49, 1807-2577, 2020.
RIBEIRO, Guilherme H. et al. Osteonecrose da mandíbula: revisão e atualização em etiologia e tratamento. 2018.
RIGO RF, Gomes FV, Mayer L. Osteonecrose perimplantar relacionada ao uso de bisfosfonatos: revisão de literatura. RvAcBO.2017;26(1):31-37.
ROLDAN, C. J., Paniagua, L. (2014). Complications of New Medications. Western Journal of Emergency Medicine, (XVI/ NO.1/January 2015), pp. 154-156.
RUGGIERO, S. L., Dodson, T. B., Fantasia, J., Gooddav, R., Aghaloo, T., Mehrotra, B.&O’Ryan, F. American Association of Oral and Maxillofacial Surgeons Position Paper on Medication-Related Osteonecrosisofthe Jaw–2014Update. American Association of Oral and Maxillofacial Surgeons J Oral Maxillofac Surg.,72, 1938-1956, 2014.
RUGGIERO, Salvatore L. et al. American Association of Oral and Maxillofacial Surgeons’ Position Paper on Medication-Related Osteonecrosis of the Jaw–2022 Update. Journal of Oral and Maxillofacial Surgery, 2022.
SOUSA ,A.S et al. Protocolo de atendimento odontológico de pacientes em tratamento com bisfosfonatos. RevSaúde, 2018; 12(1-2): 54-61.
SALES, Kauanna Oliveira; da CONCEIÇÃO, Leandro Silva. A ATUAÇÃO DO CIRURGIÃO-DENTISTA FRENTE À OSTEONECROSE DOS MAXILARES ASSOCIADA AO USO DE BISFOSFONATOS: UMA REVISÃO DE LITERATURA. J Business Techn, 2020.
Wan, J. T., Sheeley, D. M., Somerman, M. J., & Lee,J. S. Mitigating osteonecrosis of the jaw (ONJ) through preventive dental care and understanding of risk factors. Bone Research, 2020.
