REGISTRO DOI: 10.5281/zenodo.8396327
Samara Abdelquader de goes Alves da Conceição
Amanda Bezerra Maciel
Saulo Albert Pereira Pinto
Jaqueline Lima Monteiro
Larissa Agata de Jesus Nascimento
Jaciara Cristina Tavares Silva
RESUMO
A obesidade e o excesso de peso pode estar associado ao desenvolvimento tumoral, que pode ser explicado pela produção de várias citocinas inflamatórias. Este artigo mostra as complicações causadas pela obesidade no tratamento e sobrevida de pacientes oncológicos. O objetivo desse estudo foi mostrar como a obesidade favorece o aparecimento de neoplasias e a dificuldade do tratamento em pacientes já diagnosticados, contendo artigos de 2007 a 2017, incluindo temas como: câncer e obesidade as doenças do século, e a interferência da obesidade no tratamento quimioterápico. Os estudos apontam que o aumento da adiposidade está associado com aumento da incidência ou morte de uma grande variedade de tipos de câncer. E, caso a obesidade fosse prevenida poderiam ser evitados aproximadamente até 20% dos casos de morte por câncer.
Palavras chave: Obesidade. Câncer. Processo Inflamatório. Alimentação. Prevalência.
Introdução
O câncer é uma das principais causas de morte no mundo, responsável por 13% de todas as mortes em 2008, cerca de 70% ocorreram em países de baixa e média renda. Estatísticas demonstram que as mortes por câncer irão continuar aumentando em todo o mundo (OMS, 2012).
A ligação entre obesidade e câncer é afirmada em vários estudos prospectivos. A junção mais forte é entre um IMC aumentado e o risco do surgimento de câncer. Uma ampla pesquisa americana, o American Cancer Prevention Study II, que incluiu um coorte de mais de 900 mil indivíduos sem neoplasias em 1982, seguidos durante uma média de 16 anos, encontrou uma conexão considerável entre obesidade e o câncer. Já entre os indivíduos com um IMC de 40 kg/m², o índice de mortalidade devido as causas de câncer foi 52% maior nos homens e 62% maior em mulheres do que em pessoas com um IMC normal (MELO, 2011).
Dentre os fatores de risco para o desenvolvimento do câncer que são passíveis de prevenção, depois do tabagismo, o sobrepeso/obesidade parece ser a causa mais importante do câncer que pode ser evitada na população com estilo de vida ocidentalizado. Fato este que vem sendo comprovado por vários estudos epidemiológicos (ABESO, 2010).
Mulheres com excesso de peso têm risco aumentado para o desenvolvimento de câncer do endométrio e câncer de mama após a menopausa. Além disso, evidências crescentes sugerem que o aumento da adiposidade está associado com o aumento da ocorrência ou morte de uma grande diversidade de tipos de câncer, incluindo cólon e reto, ovário, endométrio, vesícula, esôfago, pâncreas, rim, fígado, próstata e certas células hematopoiéticas. Sabe-se que o excesso de peso em homens e mulheres resulta no aumento de 1,52 e 1,62, respectivamente, no risco relativo de morte por câncer. E, caso a obesidade fosse prevenida, poderiam ser evitados aproximadamente 10% dos casos de morte por câncer em fumantes e 14 a 20% dos casos de morte por câncer em não fumantes. Dessa forma, é notável que as modificações metabólicas ocasionadas pela obesidade corroboram para a criação de um ambiente favorável que irá promover o desenvolvimento tumoral (ABESO, 2010).
Alguns autores alertam para o fato de que, nos pacientes obesos, a utilização do peso atual para a efetuação do cálculo da dose terapêutica possa culminar em larga toxicidade, principalmente quanto ao nível hematológico. Especialistas em oncologia, preocupados com a não-superestimava das doses quimioterapêuticas, têm aplicado redução empírica das mesmas. Essa adaptação das doses em pacientes obesas é assunto de grande interesse, particularmente para drogas com índice terapêutico “estreito”, podendo prejudicar substancialmente a eficácia da terapia (KIRJNER; PINHEIRO, 2007).
A busca pelo cálculo de dose ideal a ser ofertada ao paciente (através de suas adaptações) visa a maximizar a probabilidade da produção do efeito terapêutico desejável e, concomitantemente, minimizar os eventos tóxicos, mantendo-os em níveis toleráveis. Logo, teoricamente, a dose ótima é aquela que se encontra dentro da janela terapêutica, estando acima do nível que fornece o efeito antitumoral, porém abaixo do que fornece uma toxicidade inaceitável (KIRJNER; PINHEIRO, 2007).
Para expor o conteúdo, este trabalho teve como objetivo compreender e relatar as complicações causadas pela obesidade no tratamento e sobrevida de pacientes oncológicos. Identificando os fatores de risco para a obesidade, descrevendo o porquê a obesidade aumenta a incidência de câncer, indicando as implicações da obesidade no tratamento oncológico e revisando as medidas de prevenção e tratamento da obesidade.
Desenvolvimento
O presente estudo foi desenvolvido por meio de uma revisão bibliográfica de artigos e livros que tiveram como conteúdo: Obesidade como fator causal para câncer. A literatura escolhida abrangeu o período de 2007 a 2017, onde foi usado um modelo de investigação definido e passível de produção sobre o tema.
A revisão baseou-se na busca de artigos com os descritores: Obesidade, sobrepeso, rescindiva, complicações no tratamento, sobrevida de pacientes oncológicos obesos, nutrição. A escolha dos artigos foi produzida através da verificação das bases Scielo, PUBMED, INCA, Ministério da Saúde, Google acadêmico. A inclusão dos estudos conteve a história da obesidade como um fator de risco para o desenvolvimento de câncer, o papel da nutrição na prevenção da doença, análise da relação entre câncer e a nutrição, a importância dos alimentos na prevenção e tratamento do câncer, incluindo outros temas relevantes para o estudo.
OBESIDADE E CÂNCER: UNIDOS PELO PROCESSO INFLAMATÓRIO
A obesidade e o excesso de peso pode ser considerada como um estado de inflamação subclínica. Os possíveis mecanismos responsáveis pela associação da obesidade com o câncer, incluem a distribuição da gordura corporal, um estado de Hiperinsulinemia, resistência à insulina, acreditando que o excesso crônico desse hormônio reduziria os níveis de proteína ligante de IGF, ocorrendo um aumento de IGF-1ou somatomedina C, que é um fator de crescimento semelhante à insulina, a biodisponibilidade aumentada de hormônios esteroides e adipocinas (leptina e adiponectina), resultando em mudanças no ambiente celular, favorecendo o desenvolvimento tumoral (MEMDES, 2011).
A hipótese mais estudada envolve a ação da Hiperinsulinemia prolongada, constando que a obesidade, especificamente visceral, resulta em um aumento na liberação dos ácidos graxos livres, TNTα (Fator de Necrose Tumoral alfa), junto com uma diminuição na liberação de adiponectina na circulação e o desenvolvimento da resistência insulínica pelo acumulo de metabólicos de ácidos graxos dentro de tecidos que respondem à insulina. Assim, ocorre uma diminuição na eficiência de sinalização insulínica para regulação da glicose plasmática nos tecidos sensíveis a sua ação, como o musculo esquelético, fígado, tecido adiposo e endotélio, e um aumento na produção de insulina pelo pâncreas para manter os níveis de glicemia dentro da faixa de normalidade. A Hiperinsulinemia reduz a produção de IGFBP-1 e IGFBP-2, que se liga ao IFG-1 inibindo sua ação, resultando o aumento dos níveis de IFG-1 livre. O IFG-1 junto com a insulina, se liga aos seus receptores, resultando em fosforilação de proteínas IRS, que ativam a cascata de sinalização intracelular, representada pelas vias fosfoinositol-3-quinase (PI3K-Akt) e proteína quinase ativada pelo mitógeno (MAP quinase ou MAPK), ambas envolvidas no processo da carcinogênese. Essas vias ativam oncogênese Ras-MAPK, induzindo a proliferação celular e levando a mudanças no ambiente celular favorável à formação de tumores. A resistência à insulina e a Hiperinsulinemia são fatores que associados as neoplasias de mama, colón e próstata, pode promover uma diminuição da resposta ao tratamento contra o câncer. Sendo considerado também um fator de risco para o câncer de endométrio (FERRAZ & SIQUEIRA, 2015).
Outra ação que pode favorecer o desenvolvimento de neoplasias associada a obesidade é o estado crônico de inflamação subclínica ou de baixo grau, no qual envolve a produção de várias citocinas inflamatórias. Estas citocinas pró-inflamatórias podem então explicar a resistência tumoral que pode ser induzida por macrófagos ativados no tecido adiposo branco. O tecido adiposo contém altas concentrações de células pró-inflamatórias, em companhia com as células B e células dendríticas (DCs), mas além disso, tem altos níveis de células anti-inflamatórias. Os níveis de adipocitocinas aumentam na obesidade e tem sido relacionada e têm sido relacionadas à resistência à insulina (proteína estimuladora de acilação, fator de necrose tumoral-a, interleucina-6 e resistina). A leptina e adiponectina têm efeitos sobre a sensibilidade à insulina. Na obesidade, a resistência insulínica também está relacionada à resistência à leptina e aos teores plasmáticos reduzidos de adiponectina (GUIMARAES, 2007).
A ligação entre a tumorigênese e a obesidade. A obesidade central está relacionada livremente com a resistência insulínica e, esse hormônio não tem a capacidade de promover a homeostase da glicose e dos lipídeos, ocorrendo então a Hiperinsulinemia. Estas duas manifestações metabólicas estão relacionadas com o aumento da biodisponibilidade do fator de crescimento semelhante à insulina 1 (IGF-1), com efeitos carcinogênicos já denominados. A insulina interatua com o eixo IGF-1 diminuindo a síntese das proteínas ligadoras de IGF-1 (IGFBPs). Desta forma, ocorre um aumento da biodisponibilidade do IGF-1 e estímulo à tumorigênese. As adipocinas derivadas do tecido adiposo também estão envolvidas no processo de tumorigênese, já que a resistina contrapõe a ação da insulina, aumentando a RI. Além disso, tanto a leptina quanto a resistina são agentes que promovem o crescimento celular. (Figura 1.)
Figura 1. A ligação entre a tumorigênese e a obesidade.
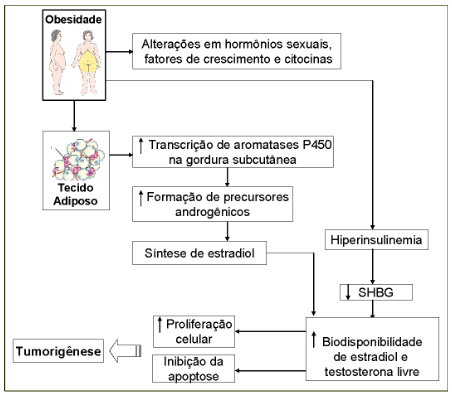
Adaptado de: JESUS & RIOS, 2016
ANÁLISE PROTEÔMICA
“A proteômica é uma tecnologia que permite o estudo do produto da expressão gênica através de amostras biológicas. O estudo proteômico permite analisar como as proteínas interagem com outras moléculas, induzem e controlam as vias metabólicas influenciando na proliferação celular, crescimento, apoptose e senescência, oferecendo-se, assim, uma única compreensão dos complexos sistemas biológicos. ” (CHUTHAPISITH. et al, 2007).
“Nos últimos anos a proteômica vem sendo aplicada a fim de elucidar uma variedade de vias de detecção e discriminação de enzimas lipolíticas em pacientes obesos. ” (KOCEVAR. et al, 2013).
FERRAZ e SIQUEIRA (2014) descrevem como imprescindível a identificação e compreensão sobre o comportamento dos marcadores biomoleculares na carcinogênese associada à obesidade por considerar que o tecido adiposo possivelmente esteja envolvido na formação de alguns processos neoplásicos tornando fundamental um entendimento aprofundado dos mecanismos envolvidos nessa associação.
Segundo CHUTHAPISITH. et al (2007) “a proteômica obtida do plasma de pacientes obesos para a identificação de potenciais biomarcadores de doenças específicas promete ser uma poderosa ferramenta de diagnóstico para a definição do início, progressão e prognóstico de neoplasias. ”
Em seu estudo FERRAZ e SIQUEIRA (2014) afirmam que pacientes portadores de obesidade possuem proteínas potencialmente carcinogênicas e que a compreensão da expressão dessas proteínas, permite a ampliação no arsenal diagnóstico e terapêutico para essas duas entidades, a obesidade e o câncer.
PREVALÊNCIA DO CÂNCER RELACIONADO COM A OBESIDADE
A obesidade tornou-se o principal fator de risco para todas patologias no mundo. Nos Estados Unidos, tendo como exemplo, na atualidade aproximadamente 70% dos adultos estão com sobrepeso, com IMC de 25Kg/m² e 36% estão obesos, IMC de 30Kg/m². Segundo a Organização Mundial da Saúde (OMS), além dos EUA houve um aumento continuo da prevalência da obesidade no Brasil visto ao longo das décadas. Esse excesso de peso e a obesidade tem sido correlacionado com o risco aumentado de neoplasias e outras doenças crônicas, como doenças cardiovasculares e diabetes tipo 2 (INSTITUTO ONCOGUIA, 2016).
Nos últimos 10 anos, o excesso de peso corporal em 2006 na população adulta aumentou de 42,6% para 53,8%, em 2016, isto é, mais da metade dos adultos brasileiros está acima do peso. Valores semelhantes são observados entre os jovens, um a cada 3 crianças de 5 a 9 anos e 1 a cada 5 adolescentes de 10 a 19 anos estão com excesso de peso. Esta ampla evidencia cientifica, comprovada pela Agência Internacional para Pesquisa em Câncer, da OMS, afirma que o excesso de gordura corporal representa risco para o desenvolvimento de pelo menos 13 tipos de câncer, como o câncer de estômago, esôfago (adenocarcinoma), pâncreas, vesícula biliar, cólon e reto, rins, mama (mulheres na pós-menopausa), ovário, endométrio, meningioma, tireoide e mieloma múltiplo (MELO, 2017).
CÂNCER DE MAMA
A obesidade pode ser vista como uma epidemia mundial, segundo dados do Instituto Brasileiro de Geografia e Estatística (IBGE), nas décadas de 70 e 80 o predomínio das mulheres acima de vinte anos com sobrepeso era 28,7% e de obesidade, 8%. Em 2008 e 2009, ocorreu um salto de mais de 50% nesses índices, mulheres com sobrepeso passou para 48% e de obesidade para 16,9%. Na literatura há dados suficientes que sustem a obesidade sendo um fator de risco para desenvolver o câncer de mama, principalmente nas mulheres pós-menopausas. Porém, nas mulheres já diagnosticadas com câncer de mama o papel da obesidade como fator de risco é menos esclarecido. Há vários estudos que debatem essa questão, e a maioria está em conciliação que a obesidade é um fator prognóstico, mas os estudos, com metodologias diversas e populações heterogêneas, chegam a diferentes resultados sobre o risco provocado pela obesidade. As possíveis causas do pior desfecho nas pacientes obesas são várias: como a associação com outras doenças, estágio avançado do diagnóstico, características tumorais desfavoráveis, crescimento acelerado do tecido tumoral devido defeitos na imunidade celular, estado pró-inflamatório e influencias hormonais, dentre elas níveis elevados de estrogênio e insulina (PAPA, 2013).
O índice de massa corporal (IMC), o peso, circunferência da cintura (CC) e do quadril (CQ) e a relação cintura/quadril (RCQ) são os indicadores mais utilizados para avaliar a quantidade e a distribuição do tecido adiposo corporal. Existem vários estudos que relaciona a ligação entre essas medidas antropométricas e o risco de câncer de mama de acordo com os níveis dos receptores hormonais. Os mecanismos hormonais têm sido apresentados como possíveis explicações para associações entre medidas antropométricas e risco de câncer de mama. Além disso, a possível relação entre obesidade central e risco de câncer de mama é consistente com o papel da resistência à insulina em mulheres na pré e pós-menopausa, já que a obesidade central é um prognostico de resistência insulínica independentemente da obesidade geral (PINHEIRO, 2009).
Alguns fatores podem estar relacionados com o aumento de risco para o câncer de mama como o uso de anticoncepcionais orais e a terapia hormonal, a obesidade pós menopausa e exposição à radiação ionizante também pode ser considerado um fator de risco para o câncer de mama e outros tipos de câncer. Fatores de risco ligados à vida reprodutiva e características genéticas podem estar associados ao aumento da incidência do câncer de mama, como o histórico familiar (1°grau); idade; menarca precoce (antes dos 12 anos); menopausa tardia (após os 50 anos) e nuliparidade (não ter filhos). Existe outros fatores como a ingestão de álcool, lactação, dieta rica em ácidos graxos e estresse podem estar associados ao câncer de mama (BORGHESAN, 2008).
CÂNCER DE ENDOMÉTRIO
A obesidade é um sério fator de risco para câncer endometrial, devido à alta prevalência de níveis de estrógeno em mulheres obesas. Logo, tal situação se associa aos altos níveis de insulina, hormônio com ação estimulante de mitose (JESUS E RIOS, 2009).
As lesões precursoras, também nomeadas hiperplasias, são resultantes de um estímulo estrogênico persistente, endógeno ou exógeno, não antagonizado pela progesterona. São categorizadas em simples ou complexas, de acordo com o grau de complexidade arquitetural e também pelas características do núcleo celular, podendo ser hiperplasia atípica ou não atípica (BITENCOURT, 2011).
CÂNCER DE PRÓSTATA
O câncer de próstata é o que ocorre com mais frequente entre os homens, depois do câncer de pele não melanoma. As estimativas apontam 61.200 casos em 2016, o que representa 28,6% do total, além, de ser a segunda causa de morte por câncer em homens no Brasil, segundo o Ministério da Saúde, de acordo com os dados do Sistema de Informação de Mortalidade (SIM), ocorreram mais de 14 mil óbitos. Idade, histórico familiar, sobrepeso e obesidade são fatores de riscos para o aparecimento e desenvolvimento do câncer de próstata (MS, 2017).
Uma maior existência do câncer de próstata em pacientes obesos desenvolve-se pela redução dos níveis da globulina ligadora de hormônios sexuais. O SHGB é uma glicoproteína que se liga aos hormônios sexuais, para ser mais claro, testosterona e estradiol, como também a progesterona e cortisol, deixando-os inativos, sendo assim, a biodisponibilidade dos hormônios sexuais é motivada pelo nível de SHGB. Fisiologicamente, apenas uma pequena quantidade da testosterona encontra-se “livre”, ou seja, biologicamente ativa e capaz de ativar os receptores das células prostáticas. Tendo o paciente obeso, níveis baixos de SHGB, é esperado que encontremos no mesmo, elevados níveis de testosterona ativa, o que resulta no desequilíbrio do crescimento do tecido prostático (ARAUJO. et al, 2012).
CÂNCER COLON-RETAL
De acordo com a grande maioria dos estudos, o principal mecanismo responsável pela associação entre obesidade e câncer de cólon e reto seria a Hiperinsulinemia, estimulada pelo excesso de peso. A insulina é um fator de crescimento tanto para as células cancerígenas quanto para as células normais da mucosa do cólon. O aumento dos níveis de insulina está vigorosamente associado à obesidade do tipo androide, isto é, aquela na qual concentra-se a gordura na região abdominal, que é mais comum nos indivíduos do sexo masculino. A obesidade, o aumento do consumo de calorias e a inatividade física estão associados a um elevado risco de desenvolvimento dessas neoplasias (SOARES, 2005).
Os nutrientes quando chegam ao intestinal distal provocam uma secreção, o Peptídio GLP-2, e produzem ácidos graxos de cadeia curta no cólon, substância esta que age como uma proteção contra o câncer de cólon-reto. Portanto, a pobreza de nutrientes no intestino distal liga o câncer de cólon a obesidade. Isso se deve a dietas com nutrientes altamente absorvíveis em grandes concentrações (incluindo elementos não-naturais, como o açúcar refinado), com poucas fibras e resíduos. Sendo possível absorvê-las de uma maneira eficiente já nas porções proximais do intestino, ocorrendo picos de absorção de nutrientes deixando o intestino distal vazio. Indivíduos obesos e sedentários, com uma dieta rica em carboidratos, pobre em legumes, verduras e frutas, aumentam as chances do surgimento de câncer de cólon-reto, isto se deve a dietas com baixo consumo de fibras, aumentando a tempo de trânsito intestinal, portanto ocorre o aumento na formação e no contato de substancias cancerígenas encontradas nas fezes com as paredes do intestino grosso, além da alteração da flora intestinal (MARTINS, 2017).
A ALIMENTAÇÃO COMO AGENTE DE RISCO PARA O CÂNCER
A nutrição e alimentação inadequadas são relacionadas como a segunda causa de câncer que pode ter prevenção. Sendo responsáveis por até 20% dos casos de câncer nos países em desenvolvimento, como o brasil e aproximadamente 35% das mortes pela doença (INSTITUTO NACIONAL DO CÂNCER, 2018).
A alimentação também pode desempenhar como um coeficiente na causa do câncer. Os embutidos são preparados com carnes vermelhas normalmente muito gordas e obtém na formula aditivos químicos chamados de nitratos, que após se modificarem em nitrosaminas, se alteram em agentes cancerígenos. Já o churrasco e os defumados, são introduzidos pelo alcatrão oriundo da fumaça do carvão o mesmo visto na fumaça do cigarro e que possui ação carcinogênica já conhecida. O sal e a bebida alcoólica em excesso também estão relacionados com alguns cânceres, como o de boca, esôfago, reto, fígado e mama. Uma dieta com baixo ingestão de fibras e com um alto nível calorico está ligada a um maior risco de câncer de cólon e de reto. Em associação aos cânceres de mama e de próstata, o consumo de gordura pode modificar os níveis de hormônio no sangue, expandindo o risco da doença (PERIN E ZANARDO, 2013).
A ALIMENTAÇÃO COMO FATOR PREVENTIVO CONTRA O CÂNCER
Segundo BARRÉRE et al. (2017) a nutrição é um fator preventivo primário do câncer de duas maneiras: através da ingestão de alimentos preventivos e evitando a ingestão de alimentos que contenham fatores cancerígenos.
Nenhum alimento sozinho é capaz de proteger contra o câncer, porem a combinação de certos alimentos pode estimular o sistema imunológico a defender o organismo contra a doença. Na luta contra o câncer, a alimentação tem valor, acima de tudo preventivo, mas quando já está diagnosticado com o câncer a dieta continua exercendo um papel importante (HYPPOLITO E RIBEIRO, 2014).
Os alimentos concedem uma serie de possibilidades de proteção para o nosso organismo contra os desenvolvimentos de neoplasias e outras doenças crônicas, dentre os fatores responsáveis por essa proteção estão os carotenoides, os compostos fenólicos, as vitaminas antioxidantes, os terpenóides, os esteroides, os indoles e as fibras. Existe alguns compostos, chamado agentes quimiopreventivos, que especialmente desempenha uma ação protetora característica contra o desenvolvimento do câncer, a maioria desses compostos químicos podem ser sintetizados em laboratórios ou podem ser encontrados disponíveis nos alimentos. Tendo como exemplo, o licopeno pode ser encontrado no tomate; as isoflavonas na soja; a quercetina na maçã; a luteína no espinafre; o resveratrol na uva; as antocianinas nas frutas vermelhas como a amora, cereja e a framboesa, entre outros (GOMES, 2007).
O passo de uma modificação epigenética ocorre no início do desenvolvimento de uma célula cancerígena, num momento em que isso é potencialmente reversível. Os cientistas não estão completamente cientes de como esse processo funciona. No entanto, é razoável recomendar uma dieta de promoção da saúde, rica em frutas, legumes, soja, ervas aromáticas terapêuticas, tais como açafrão, canela, chá verde e café (MAHAN. et al, 2012).
O consumo de frutas é um fator importante para a proteção contra câncer de boca, faringe, laringe, esôfago, colo do útero, pulmão e estômago. Os vegetais sem amido, como espinafre, tomate e pimentão, possivelmente apresentam proteção contra os cânceres de boca, faringe, laringe e esôfago; todos os legumes, em especial os das cores verde e amarelo, supostamente protegem contra o câncer de estômago (MAHAN. et al, 2012).
Agentes anticarcinogênicos achados nas frutas e vegetais envolvem antioxidantes como, vitaminas C e D, selênio e fitoquímicos. Os fitoquímicos que estão incluídos são os carotenoides, flavonoides, isoflavonas, lignanas, organossulfidos, compostos fenólicos e monoterpenos. Ainda não está claro quais substâncias das frutas e vegetais apresentam mais proteção contra o surgimento de neoplasias. Essas substâncias apresentam métodos complementares e sobrepostos, implicando na indução de enzimas de detoxificação, no bloqueio da produção de nitrosamina, distribuição de substrato para o surgimento de agentes quimioterápicos, diluição e ligação de carcinógenos no trato digestivo, transformação do hormônio e efeitos antioxidantes (MAHAN. et al, 2012).
As fibras também são fundamentais na prevenção de câncer, principalmente porque regulam o funcionamento do intestino, diminuindo o tempo de contato de substâncias que causam câncer com as paredes intestinais (INSTITUTO NACIONAL DO CANCER, 2018).
O consumo do cálcio é importante, por estar associado à prevenção de câncer. Evidências indicam que bile e ácidos graxos não absorvidos irritam a mucosa, propiciando a proliferação de células cancerígenas, já o cálcio atua formando complexos com esses compostos, tornando-os inofensivos (REVISTA BRASILEIRA DE REUMATOLOGIA, 2009). Contudo, há estudos que apontam um risco aumentando de formas agressivas de câncer de próstata com o consumo significativo de laticínios ou a suplementação de cálcio. As recomendações precisam ser mais pesquisadas antes de recomendações claras possam ser feitas (CHUNG. et al, 2009; HUNCHAREK. et al, 2009).
A deficiência de vitamina D está sendo encontrada em todas as faixas etárias, trazendo a análise do papel da vitamina D na prevenção do câncer. Devido a diminuição da exposição ao sol, ocorre uma redução na conversão da vitamina D na superfície da pele, o que pode levar há um aumento de deficiências. Pesquisas mostram que o aumento dos níveis séricos de hidroxivitamina 25-D (25 (OH) D) estão relacionados a menores taxas de ocorrência de cânceres de colón, mama, ovário, rins, pâncreas, próstata agressivo, e outros. Até que ocorra mais estudos sobre a interação entre a vitamina D e a prevenção do câncer, ingerir 2.000UI de vitamina D por dia para alcançar os níveis séricos de D25(OH) de 40-60ng/Ml sendo considerado assegurado (GARLAND, 2009; GARLAND. et al, 2011).
O consumo de chá é uma boa fonte de fenóis e antioxidantes, o chá verde por exemplo, é feito de folhas que foram cozidas, prensadas, secas e não torradas, e por isso o chá verde possui catequinas que apresentam atividade biológica com características antioxidantes, antiangiogênese e antiproliferativas que são fatores importantes para a prevenção do câncer (KUZUHARA, 2008).
Conclusão
A partir dos estudos que abordam o grande impacto da obesidade e sobrepeso na carcinogênese, pode-se afirmar a relevância que tem o controle de peso mantendo-o dentro dos parâmetros adequados, controlando a resistência à insulina, diminuindo os níveis de proteína ligante de IGF, consequentemente diminui a IGF-1, que é um fator de crescimento semelhante a insulina, evitando o aumento de hormônios esteroides e adipocinas (leptina e adiponectina) que estão relacionadas à tumorigênese, porem ainda precisa de um maior entendimento na área e estudos de abordagem mais especifica relacionando o câncer e a obesidade.
Vale ressaltar o incentivo a prática de atividade física regular, uma alimentação rica em carotenoides, vitaminas antioxidantes, frutas, vegetais, legumes, ervas aromáticas e rica em fibras e cálcio, mostram um grande efeito protetor contra o câncer.
REFERÊNCIAS
ARAUJO, Talles. et al. A obesidade e seus efeitos no diagnóstico do câncer de próstata e níveis séricos do antígeno prostático específico (PSA). Revista de Saúde, Vassouras, v.3, n.1, p.45-44, jan. /jun., 2012
ATTOLINI RC; GALLON CW. Qualidade de Vida e Perfil Nutricional de Pacientes com Câncer Colorretal Colostomizados. Rev bras Coloproct, 2010;30(3): 289-298.
BITENCOURT, Lívia Maria P. “Câncer de endométrio: mortalidade populacional e sobrevida de uma coorte hospitalar, no Rio de Janeiro, Brasil”. Fevereiro de 2011. Disponível em: < https://www.arca.fiocruz.br/bitstream/icict/23407/1/1017.pdf > Acesso em: 08 de Abril de 2018
BORDALLO, Maria Alice Neves. et al. Atualização terapêutica no tratamento dos craniofaringiomas. Arq Bras Endocrinol Metab, Nov 2011, vol.55, no.8, p.520-527. ISSN 0004-2730
BORGHESAN, Deise H. et al. Câncer de mama e fatores associados. Cienc Cuid Saude 2008;7(Suplem. 1):62-68. Disponível em: http://ojs.uem.br/ojs/index.php/CiencCuidSaude/article/view/6566/3886 Acesso em: 08 de Abril de 2018.
CATTAFESTA, Monica. et al. Consumo Alimentar de Pacientes com Câncer de Mama Acompanhados em Centro Especializado em Oncologia na Grande Vitória/ES-Brasil, Revista Brasileira de Oncologia Clínica. 2014
CHUNG, M. et al.; Vitamin D and Calcium:systematic review of health outcomes, Evid Rep Tech Assess 183, 2009
CHUTHAPISITH, S. et al. Perfil proteômico de células de câncer de mama MCF-7 com quimiorresistência a diferentes tipos de drogas anti-câncer. Oncol. 2007 jun; 30 (6): 1545-51
DUARTE, Nícia Correa. Obesidade e câncer: as doenças do século. Rev. Assoc. Med. Bras. Vol. 56 nº 1 São Paulo 2010
Disponível em: http://www.equilibrium.med.br/noticias/120/obesidade-e-cuncer-as-doenuas-do-suculo/. Acesso em: 29 de novembro de 2017
FERREIRA, Helena L.; NEVES, Ludmila L. M.; BINSFELD, Pedro C. A inserção dos fitoterápicos no complexo produtivo e inovação em saúde Inovação em Temas Estratégicos em Saúde Pública. 1ª Edição. Brasília: Editora MS, 2011. V.1, p. 104-119.
FERRAZ, Álvaro Antônio B.; SIQUEIRA, Teixeira de. Obesidade e Câncer. Anais do Gastrão 2015 p.001. Disponível em:http://www.infoteca.inf.br/gastrao/smarty/templates/arquivos_template/upload_arquivos/acervo/docs/PDFs/g0001.pdf Acesso em: 08 de Abril de 2018.
GARLAND, Cf. et al., Vitamin D for câncer Prevention: global perspective, Annual of Epidemiology 19:468,2009
GARLAND, Cf. et al., Vitamin d supplement doses and serum 25 hydroxy d in the range associated with cancer prevention, Anticancer Res 31:607,2011
GOMES, Fabio da Silva. Carotenóides: uma possível proteção contra o desenvolvimento de câncer. Rev. Nutr., Campinas , v. 20, n. 5, p. 537-548, Oct. 2007 . Available from <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1415-52732007000500009&lng=en&nrm=iso>. access on 09 June 2018. http://dx.doi.org/10.1590/S1415-52732007000500009.
GUIMARAES, Daniella Esteves Duque et al . Adipocitocinas: uma nova visão do tecido adiposo. Rev. Nutr., Campinas , v. 20, n. 5, p. 549-559, Oct. 2007 . Available from <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1415-52732007000500010&lng=en&nrm=iso>. access on 08 Apr. 2018. http://dx.doi.org/10.1590/S1415-52732007000500010.
HUNCHAREK , M. et al:Colorectal câncer risk and dietary intake of calcium, vitamin D and dairy products: a meta-analysis of 26,355 cases from 60 observatinal studies, Nutr Cancer 61:1,2009
INSTITUTO NACIONAL DO CÂNCER. Ministério da Saúde, 2018. Disponível em:< http://www2.inca.gov.br> Acesso em: 20 de maio de 2018.
Instituto Oncoguia, Obesidade pode ser fator de risco para desenvolvimento de câncer. 2016, disponível em: < http://www.oncoguia.org.br/conteudo/obesidade-pode-ser-fator-de-risco-para-desenvolvimento-de-cancer-diz-estudo/9854/7/>. Acesso em: 06 de Maio de 2018.
MARTINS, Énika Moreira. et al. Obesidade como um fator de risco para o câncer: uma nova visão para a enfermagem. Rev. Educ. Meio amb. Saú. 2017, vol 7, nº03, jul/set. Disponível em: < http://www.faculdadedofuturo.edu.br/revista1/index.php/remas/article/viewFile/146/233>. Acesso em: 03 de maio de 2018.
MELO, Maria Edna de. Doenças Desencadeadas ou Agravadas pela Obesidade. Disponível em: <http://www.abeso.org.br/uploads/downloads/28/5521afaf13cb9.pdf>. Acesso em: 29 de novembro de 2017
MENDES, Maria Carolina Santos. et al. Obesidade e Câncer: as Doenças do Século. Dezembro de 2011. Disponível em: < www.abeso.org.br/pdf/revista54/obesidade_cancer.pdf >. Acesso em: 27 de novembro de 2017
Ministério da Saúde; Instituto Nacional de Câncer; Coordenação Geral de Gestão Assistencial; Hospital do Câncer I; Serviço de Nutrição e Dietética. Consenso nacional de nutrição oncológica. Rio de Janeiro: INCA; 2011.
JESUS, Rosângela P.; RIOS Cecília S. Obesidade e câncer. Disponível em http://principo.org/obesidade-e-cncer-dra-rosngela-passos-de-jesus-e-ceclia-santos.html Acesso em: 04 de Abril de 2018
KIRJNER, LINE; PINHEIRO, Rosilene de Lima. Interferência da Obesidade no Tratamento Quimioterápico em Mulheres com Câncer de Mama. Revista Brasileira de Cancerologia 2007; 53(3): 345-354 Disponível em: <http://www.inca.gov.br/rbc/n_53/v03/pdf/revisao5.pdf >. Acesso em: 29 de novembro de 2017
MAHAN, L Kathleen; ESCOTT-STUMP, Sylvia; RAYMOND, Janice L. KRAUSE Alimentos, Nutrição e Dietoterapia. 15. ed. Rio de Janeiro: Elsevier, 2012
KUZUHARA, T. et al: Green tea catechin as a chemical chaperone in cancer prevention, Cancer Letter 261,2008
PAPA, Alexander M.et al. Impacto da obesidade no prognóstico do câncer de mama.
Revista Brasileira de Oncologia Clínica, Vol. 9, no 31 < janeiro / fevereiro / março < 2013 Disponível em: < https://www.sboc.org.br/sboc-site/revista-sboc/pdfs/31/artigo3.pdf> Acesso em: 08 de Abril de 2018
PERIN, Lisiane; ZANARDO, Polachini Skzypek. Alimentos funcionais: uma possível proteção para o desenvolvimento do câncer. PERSPECTIVA, Erechim. v.37, n.137, p.93-101, março/2013. Disponível em: < http://www.uricer.edu.br/site/pdfs/perspectiva/137_329.pdf>. Acesso em: 18 de maio de 2018.
PEREIRA, Gap. Et al. Cálcio dietético – estratégias para otimizar o consumo. Rev Bras Reumatol 2009; 49(2):164-80.
PINHEIRO, R.l. et al. Relationship between body mass index, waist circumference and waist to hip ratio and the steroid hormone receptor status in breast carcinoma of pre- and postmenopausal women. Breast; 18(1):8-12, 2009.
PRIETO-HONTORIA, Pl. et al. Role of obesity-associated dysfunctional adipose tissue in cancer: a molecular nutrition approach. Biochim Biophys Acta. 2011 Jun;1807(6):664-78.
SOARES, Luana Padua. Obesidade e mortalidade por neoplasias de colón/reto, mama e próstata: um estudo ecológico em capitais brasileiras selecionadas. Rio de janeiro, 2005. Disponível em: < https://thesis.icict.fiocruz.br/pdf/soareslpm.pdf>. Acesso em: 06 de maio de 2018.
TEIXEIRA, Julia Ferrari Carneiro. et al. A influência do tratamento antineoplásico sobre o peso de sobreviventes do câncer na infância. J. Pediatr. (Rio J.), Porto Alegre, v. 92, n. 6, p. 559-566, Dec. 2016. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0021-75572016000700559&lng=en&nrm=iso>. Acesso em: 27 de novembro de 2017. http://dx.doi.org/10.1016/j.jped.2016.04.003
WCRF, World Cancer Research Fund, American Institute for Cancer Research. Food, nutrition and the prevention of cancer: a global perspective. Washington: American Institute for Cancer Research, 2007.
