REGISTRO DOI: 10.5281/zenodo.10028985
Gustavo Matheus Macedo Godoy Mariani1
Priscila Damasceno2
Tauan de Carvalho Sales3
Orientador(a): Prof(a) Ms. Leticia Gomes Freire4
RESUMO
O presente estudo busca analisar os principais resultados obtidos através da utilização da Glutamina, em diversos tipos de tratamentos em adultos e crianças, prioritariamente nos tratamentos de pacientes em estado grave e/ou internados na Unidade de Terapia Intensiva, uma vez que esse aminoácido desempenha um papel importantíssimo no metabolismo e na função do sistema imunológico. Devido sua grande contribuição com as funções vitais no corpo humano e suas ações nos processos fisiológicos, como a Síntese Proteica, Função Imunológica, Regulação do Equilíbrio Ácido-Base, Saúde Intestinal, Resposta ao Estresse, Lesões, Suplementação e Performance Esportiva, entre outros benefícios. Fato que torna o tema pesquisado altamente relevante. A metodologia aplicada para o desenvolvimento foi a revisão bibliográfica em um total de quinze publicações, na qual procuramos destacar as principais contribuições dos autores e principalmente a analisar os resultados encontrados. Os estudos analisados são ensaios clínicos, na qual a grande maioria, buscou realizar um comparativo entre pacientes divididos em grupos, sendo o primeiro grupo tratado com a suplementação de Glutamina e o segundo grupo sem o uso da Glutamina. Assim é possível concluir que os indicadores que nortearam o objetivo central desse artigo, comprova a importância e eficiência do uso da Glutamina em pacientes adultos e infantis, com seus bons resultados, que são vitais para entender os mecanismos pelos quais esse aminoácido influencia a saúde e o funcionamento do corpo humano, na possível contribuição na melhora de pacientes em estado críticos e até mesmo na redução do tempo de permanência na Unidade de Terapia Intensiva (UTI) e internação hospitalar, bem como na redução dos custos hospitalares.
Palavras Chave: Glutamina, Análise de Resultados, Pacientes em Situações Graves; Tempo de permanência em Unidades de Terapia Intensiva (UTI).
ABSTRACT
The present study seeks to analyze the main results obtained through the use of Glutamine, in different types of treatments in adults and children, especially treating patients in serious condition and/or admitted to the Intensive Care Unit, since this amino acid plays an extremely important role in metabolism and immune system function. Due to its great contribution to vital functions in the human body and its actions in physiological processes, such as Protein Synthesis, Immune Function, Regulation of Acid-Base Balance, Intestinal Health, Response to Stress and Injuries, Supplementation and Sports Performance, among other benefits . A fact that makes the researched topic highly relevant, the methodology applied for its development was the bibliographic review of a total of fifteen publications, in which we sought to highlight the main contributions of the authors and mainly to analyze the results found. The studies analyzed are clinical trials, in which the vast majority sought a comparison between patients divided into groups, the first group being treated with Glutamine supplementation and the second group without the use of Glutamine. Therefore, it is possible to conclude that the indicators that guided the central objective of this article prove the importance and efficiency of using Glutamine in adult and pediatric patients and its results, which are vital to understanding the mechanisms through which this amino acid influences health and functioning. of the human body, in the possible contribution to improving patients in serious condition and even reducing the length of stay in the Intensive Care Unit (ICU) and hospital admission, as well as reducing hospital costs.
Keywords: Glutamine, Results Analysis, Patients in Serious Situations; Length of stay in Intensive Care Units (ICU).
1. INTRODUÇÃO
A Glutamina é o aminoácido mais abundante no corpo humano, conforme a classificação de (Xu; Yunshi, 2009) e desempenha funções importantes em diversas áreas, incluindo a síntese de proteínas, a regulação do equilíbrio ácido-base, a contribuição para o sistema imunológico e a promoção da saúde intestinal.
Para Curi (2001), os pioneiros em estudar a Glutamina foram Hlasiwetz e Habermann, no ano 1873, apreciando a glutamina como sendo uma molécula com propriedades biologicamente importantes.
A Glutamina é nutricionalmente classificada como um aminoácido não essencial, uma vez que pode ser sintetizada pelo organismo a partir de outros aminoácidos. (Cruzat, Petry e Tirapegui, 2007). Para Rothe (2007), a disponibilidade sistêmica de glutamina é determinada pelo equilíbrio entre a sua produção endógena (principalmente no tecido muscular), e seu uso por órgãos consumidores de glutamina (intestinos, rins, fígado e sistema imunológico).
Diversos estudos de pacientes catabólicos na Unidade de Terapia Intensiva (UTI), conforme afirmam (Petersson; Vinnars; Waller; Wernerman, 1992), “A produção endógena de glutamina muscular está aumentada, ao mesmo tempo em que os níveis plasmáticos dela se encontram diminuídos, indicando necessidades elevadas”.
De acordo com (Biolo; Antonione, 2005), também é visto que níveis plasmáticos baixos de glutamina (< 420μmol/L) no momento da admissão do paciente estão relacionados com maior risco de mortalidade. Assim é relevante uma entender a suplementação de glutamina para pacientes na UTI, como forma de repor o pool muscular, atenuar o efluxo deste aminoácido, (Oudemans-Van; Bosman; Treske; Van Der; Zandstra, 2001).
Ainda sobre a ótica dos autores “A glutamina exógena é necessária para atender às elevadas necessidades dos órgãos, para melhoria da síntese proteica, modulação do sistema imune, redução do estresse oxidativo e preservação da barreira intestinal”.
No entanto, essa hipótese tem sido desafiada por observações recentes, visto que os níveis plasmáticos de glutamina são extremamente variáveis entre pacientes na UTI. Alguns estudos afirmam que o aminoácido pode não estar associado ao aumento da mortalidade (Pimentel; Fernandes, 2020).
Ainda que a suplementação de glutamina não interrompa o refluxo muscular dessa substância, já que a produção muscular endógena, assim como seus níveis plasmáticos estão relacionados com a gravidade da doença. (Pimentel; Fernandes, 2020).
Diante desta contextualização, a problematização deste estudo, buscou encontrar uma possível resposta para a eficácia do uso da Glutamina em diferenciados tipos de tratamentos de pacientes em estado crítico, também foi analisado o uso da Glutamina contribuiu para redução do tempo de permanência na Unidade Terapia Intensiva e internação hospitalar.
Com esse cenário, torna-se altamente relevante para maior dimensão do estudo, efetuar uma análise na situação hospitalar no Brasil e quantificar os pacientes internados em estado grave e/ou na Unidade Terapia Intensiva – UTI, durante os últimos anos. Assim sendo, utilizamos como base o trabalho de (Albuquerque; Machado, 2022), que compilam os dados e indicadores, apresentados pelo observatório hospitalar do Instituto FioCruz.
Segundo (Albuquerque; Machado, 2022), os dados apresentados na tabela-1, revela a realidade hospitalar brasileira, mostrando o números de internações, números de pacientes que necessitam de tratamento na UTI, a média de permanência (em dia), a idade média dos pacientes, número de óbitos e o valor médio das internações, onde se pode mensurar se a contribuição da Glutamina para reduzir o tempo de internação e permanência na UTI , é eficaz, bem como se ela também pode contribuir para a redução de custos com os gastos hospitalares.
O período desse estudo, compreende os anos de 2016 até Jun/2022, conforme mostrado na primeira tabela.
Tabela 1: Internações e Indicadores do SUS no Brasil.
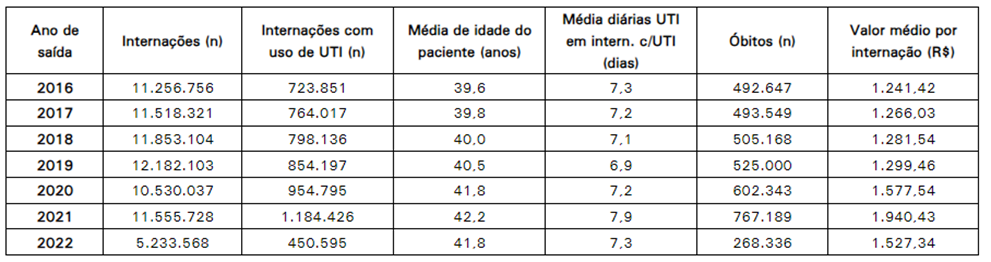
Fonte: Observatório Hospitalar – Fiocruz (Dados e Indicadores,2022).
Para Bergerson, (1996), a redução de complicações, com o uso da Glutamina pode ajudar de forma significativa no tempo de hospitalização, normalizando a resposta imunológica, mantendo ou melhorando o estado nutricional.
Para (Macburney; Young; Wilmore, 1994), seus estudos apontaram que os custos hospitalares foram de US$ 21,095 menores nos pacientes suplementados, em relação aos custos dos pacientes com a terapia padrão.
Gholamalizadeh M. et al (2021), descreve em suas análises, ter avaliado alguns ensaios clínicos que mostraram que o uso de glutamina é apropriado para reduzir a mortalidade e a necessidade de ventilação mecânica. Analise bem pertinente pois conforme os indicadores apresentados na tabela – 1, somente no ano de 2022 (junho), ocorreram mais de 268.336 mortes no Brasil.
2. MATERIAIS E MÉTODOS
O desenvolvimento desse estudo foi norteado pela revisão literária em um arcabouço de artigos científicos e publicações, reunindo e sintetizando resultados de pesquisas, sobre o presente tema investigado e assim permitindo a construção de uma análise ampla, ordenada e compilada em estudos anteriores. Para (McMahane; Mc Farland, 2020), revisões são traduções de subtemas científicos, citações dos artigos originais nas revisões, que coloca em destaque pela sua importância.
O acervo examinado neste trabalho de revisão, são estudos qualitativos descritivos que ofereceram uma valiosa contribuição teórica sobre os pacientes em estado grave e/ou internados na Unidade de terapia Intensiva, que tiveram a adição do suplemento de Glutamina em seu tratamento, assim a análise dos artigos, procurou compreender os efeitos da Glutamina nesses pacientes (melhoria do estado de saúde, tempo de permanência na Unidade de Terapia Intensiva, tempo de permanência hospitalar, números de óbitos, efeitos colaterais entre outros indicadores).
Cabe ressaltar que cada artigo pesquisado apresentou variações sobre a enfermidade dos pacientes e a gravidade de cada caso, bem como a diversidade de métodos, como por exemplo; estudo multicêntrico, duplo-cego, randomizado e controlado, ou divisão de pacientes em grupos e tratamentos diferenciados, sendo um grupo com o uso da Glutamina e outro sem, para análise comparativa dos resultados.
Para orientar a revisão integrativa, foi utilizado foi adotado o modelo PICO, que descreve os seguintes elementos: População: pacientes adultos com diagnóstico de condição crítica, admitidos na UTI; Intervenção: suplementação com glutamina; Comparação: suplementação e tratamento padrão. Desfechos: mortalidade, tempo de internação na UTI, tempo de internação hospitalar e efeitos adversos. Conforme (Stone, 2002), a estratégia PICO pode ser utilizada para construir questões de pesquisa de naturezas diversas, oriundas da clínica, do gerenciamento de recursos humanos e materiais, da busca de instrumentos para avaliação de sintomas, entre outras.
Contando com buscas nas bases de dados Medline (PubMed), Embase e Cochrane Library, sem restrições de idioma ou período de publicação. A estratégia de busca incluiu os seguintes termos: “glutamina”, “critical illness”, “intensive care units”, “mortality”, “ventilator-free days”, “length of stay”, “adverse effects”. Os termos foram combinados com operadores booleanos e adaptados a cada base de dados.
Na Pesquisa foram incluídos estudos que avaliaram a suplementação com glutamina em pacientes críticos na UTI, com desfechos relacionados à mortalidade, tempo de ventilação mecânica, tempo de internação na UTI, tempo de internação hospitalar e efeitos adversos. E os critérios de exclusão foram estudos e publicações datados há mais de 20 anos e que não avaliam pacientes que receberam a suplementação com glutamina durante seu tratamento, bem como os pacientes que não receberam.
A qualidade metodológica dos estudos incluídos será avaliada de acordo com a escala de qualidade de evidência GRADE (Grading of Recommendations Assessment, Development and Evaluation).
3. RESULTADOS/DISCUSSÃO
A partir da seleção, leitura dos artigos e coletados dos dados, foi possível a criação da segunda tabela, onde destaca-se a organização por agrupamento de informações-chave e de forma sintética, como o título de cada artigo, nome(s) do(s) autor(es), delineamento, parâmetros do desenvolvimento do experimento e os principais resultados apontando em cada um dos estudos.
Após a elaboração da tabela de referência, foi possível efetuar o cruzamento dos principais dados encontrados e chegarmos em algumas considerações que serão apresentadas nas conclusões finais deste artigo.
Tabela 2: Análise de Artigos sobre o uso da Glutamina e seus principais resultados.
Título Estudo Nº de pacientes e patologia apresentada Quantidade e forma de administração da Glutamina Resultados A Randomized Trial of Enteral Glutamine for Treatment of Burn Injuries. Heyland, et al., 2022. 1.209 pacientes com queimaduras graves. 596 pacientes receberam glutamina e 604 somente placebo. 0,5g/Kg de peso corporal / dia. Administrado via enteral. Menor tempo de internação e menor taxa de mortalidade em 6 meses no grupo da glutamina. Não houve diferença entre os grupos. Glutamine effects on heat shock protein 70 and interleukines 6 and 10: Randomized trial of glutamine supplementation versus standard parenteral nutrition in critically ill children. Jordan, et al., 2015. Estudo em observação de 49 crianças gravemente enfermas. 49 pacientes receberam nutrição parenteral no padrão (SPN, 49 indivíduos) ou nutrição parenteral padrão com suplementação de glutamina (SPN + Gln, 49 indivíduos). Ajudou a manter os níveis elevados de HSP-70 por um período maior. A suplementação de glutamina não teve interferência na IL-10 e não mostrou redução importante dos níveis de IL-6. Endogenous glutamine production in critically ill patients: the effect of exogenous glutamine supplementation. Mori et al., 2013. O estudo durante dois dias consecutivos, em pacientes sob ventilação mecânica (n = 11) na unidade de terapia intensiva (UTI), durante alimentação parenteral contínua. A Glutamina Ra foi aplicada via injeção em bolus de 13C-glutamina após um tempo de amostra, a glutamina exógena foi usada por infusão intravenosa de um dipeptídeo contendo glutamina, L-alanil-L-glutamina, 0,28 g/kg por 20 horas. Resultado é favorável para aferições repetitivas. A nutrição total hipotética enfraquecendo da produção endógena de glutamina durante a infusão de L-alanil-L-glutamina, como parte da nutrição completa, não foi percebida. Effects of different resuscitation fluid on severe acute pancreatitis. Gang et al., 2014.. 120 pacientes com PAS, no período de janeiro de 2007 e março de 2010. Divididos em grupos para análise dos resultados. A fração de solução salina normal para HES nos grupos HS e SHG foi de 3:1. A glutamina (dipeptídeo de glutamina a 20%, 100 mL/d) foi suplementada no líquido de reanimação no grupo SHG. A mistura de solução salina normal, HES e glutamina é mais eficaz na reativação da PAS, suavizando a inflamação e sustentando a barreira intestinal. Effects of two different glutamine-containing enteral supplements on stool frequency and density in elderly patients recovering from acute critical illness. Nobutoshi et al., 2017. 25 pacientes, maiores de 75 anos, em recuperação de doença crítica na unidade de terapia não intensiva e programados com alimentação por sonda. Separados em 2 grupos Grupo 1: fibra de glutamina-oligossacarídeo (n = 11). Grupo 2: glutamina F (n = 11). Com doses glutamina 3x ao dia na de 9 g/dia. A nutrição enteral foi a mesma dosagem para os grupos. Resulta no endurecimento e redução da frequência das fezes em idosos. A reação pode ter ocorrido por diferentes propriedades aditivos dos suplementos de glutamina. Efficacy and Safety of Glutamine-supplemented Parenteral Nutrition in Surgical ICU Patients: An American Multicenter Randomized Controlled Trial. Ziegler et al., 2016. 150 participantes (todos adultos), pós cirurgia gastrointestinal, vascular ou cardíaca que requer cuidados de NP e UTII. PN [1,5 g/kg/d aminoácidos (AAs) e energia a 1,3× gasto energético basal estimado]. Controles (n = 75) usou PN padrão sem GLN (STD-PN); o grupo GLN (n = 75) usou NP com dipeptídeo alanil-GLN (0,5 g/kg/d), trocado proporcionalmente AA em PN (GLN-PN). No grupo GLN-PN, ocorreram 11 mortes, segundo o grupo (STD-PN) registrou 13 mortes no grupo. Demais resultados clínicos e eventos contrários foram idênticos. β-Hydroxy-β-methylbutyrateArginine, and Glutamine Complex on Muscle Volume Loss in Critically Ill Patients: A Randomized Control Trial. Kensuke, et al., 2019. 88 pacientes em grupos de controle (43) e HMB (45) por ordem aleatória de pacientes da unidade de terapia intensiva (UTI). No segundo grupo HMB recebeu 3 g de HMB, 14 g de arginina e 14 g de glutamina diariamente, além da terapia nutricional padrão. O complexo HMB na fase aguda da terapia intensiva não impede a redução de volume muscular, os volumes caíram expressivamente. Effect of oral glutamine supplementation on gut permeability and endotoxemia in patients with severe acute pancreatitis: a randomized controlled trial. Singh, et al., 2014. Em um ensaio clínico por sete dias de forma randomizada, para receber placebo ou GL. Os pacientes foram distribuídos em dois grupos: GL (n = 41) e placebo (n = 39). Examinada pela excreção de lactulose/manitol na urina e endotoxemia e analisada por anticorpos primordiais de endotoxina tipo IgG e IgM (EndoCab IgG e IgM). A redução da inflamação e da endotoxemia não diminuiu complicações infecciosas na pancreatite aguda grave. Sem registro determinante para um efeito do GL na permeabilidade intestinal. Glutamine effects on brain growth in very preterm children in the first year of life. Kieviet, et al., 2013. 65 crianças prematuras, com tempo de gestação menor que trinta e duas semanas, O perímetro cefálico, o peso e o comprimento foram observados em relação aos bebês saudáveis. Houve um desenvolvimento do perímetro cefálico em crianças muito na maioria dos prematuros que utilizaram suplementação neonatal de Glutamina. Evaluation of the recovery after heart surgery following preoperative supplementation with a combination of beta-hydroxy-beta-methylbutyrateL-arginine, and L-glutamine: a double-blind randomized placebo-controlled clinical trial. Mona, et al., 2022. 70 pacientes submetidos à cirurgia cardíaca, divididos em dois grupos. um grupo consumiu Um grupo consumiu dois sachês de uma combinação de 7 g de L-arginina, 7 g de L-glutamina e 1,5 g de HMB por dia ou o outro grupo somente placebo, num período de 30 dias antes da operação. A suplementação perioperatória juntamente com Gln, Arg e HMB contribui com recuperação, diminuindo a lesão miocárdica e o tempo de internação hospitalar / UTI. A randomized trial of intravenous glutamine supplementation in trauma ICU patients. Pérez, et al., 2014. 142 pacientes no formato prospectivo, randomizado, duplo-cego e multicêntrico. Aplicação da glutamina não como item nutricional, mas sim como uma infusão completa. A suplementação de glutamina não conseguiu normalizar os índices plasmáticos de glutamina nos pacientes. No sexto dia, os níveis baixos de glutamina plasmática no dia 6 foram considerados o pior resultado. Improving rehabilitation after critical illness through outpatient physiotherapy classes and essential amino acid supplement: A randomized controlled trial. Jones, et al., 2015. 93 pacientes divididos em dois 2 grupos (45 anos ou mais), em terapia intensiva, com uma permanência mista na unidade de terapia intensiva/pré-unidade de terapia intensiva de cinco dias ou mais. Foram testados no planejamento fatorial 2 × 2: O primeiro ingeriu GEAA 2x ao dia por 3 meses. É o segundo PEPSE de seis semanas em 3 meses. O estudo mostra um resultado positivo com o uso da mistura do suplemento GEAA, que pode contribuir na recuperação física e minimizar a ansiedade e a depressão. Role of heat shock protein and cytokine expression as markers of clinical outcomes with glutamine-supplemented parenteral nutrition in surgical ICU patients. Wischmey et al., 2019. 150 pacientes adultos depois de uma cirurgia cardíaca, vascular ou gastrointestinal, com suporte de NP e cuidados em UTII, em 5 centros médicos acadêmicos. Aplicou-se NP isocalórica e isonitrogênica, com ou sem dipeptídeo GLN. As misturas séricas de eHSP70, eHSP27, interleucina-6 (IL-6) e 8 (IL-8) no soro no início da avaliação (antes do estudo NP) e 28 após. Observa-se a indicação que a concentração sérica de HSP70 tem probabilidade de ser um indicador para a gravidade da doença e possibilidade de recuperação na UTI. A PN suplementada com GLN não ampliou o eHSP70. Estudo piloto com suplementação de glutamina na nutrição enteral de pacientes pediátricos críticos. Moreira, et al., 1999. Nove bebês e buscou avaliar a tolerância e o impacto do suplemento de glutamina em bebês gravemente enfermos. Realizada uma divisão, o grupo de tratamento (n = 5) recebeu 0,3 g/kg de glutamina por via enteral, enquanto os controles receberam 0,3 g/kg de caseína durante 5 dias. As conclusões do estudo relatam que a suplementação enteral de glutamina com desnutrição, sepse e insuficiência respiratória, foi bem aceita e contribuiu para redução da morbidade e mortalidade séptica. O tempo na UTI e no hospital e sob ventilação artificial, foi numericamente com o uso da Glutamina.
Fonte: Elaborado pelos autores.
Heyland (2022), busca em seus estudos avaliar a eficiência positiva na resposta metabólica e ao estresse a lesões graves, direcionando os ensaios clínicos para pacientes com queimaduras graves. Porém a suplementação de glutamina não minimiza a quantidade da permanência hospitalar. Os estudos de Jordan. (2015), buscam investigar se a suplementação de glutamina (Gln) altera o estresse oxidativo, bem como resposta inflamatória em crianças gravemente enfermas. Não foi constatado nos níveis de glutamina diferenças estatísticas relevantes nos pacientes estudados.
Maiko Mori, (2014), pesquisa se a taxa de aparecimento de glutamina (Ra) pode ser utilizada como um cálculo da produção endógena de glutamina. Ocorreu um aumento de 14% na glutamina Ra endógena, foi encontrado no final do período de suplementação intravenosa em comparação com as medidas basais (P = 0,009).
Gang Zhao, (2013), tem como meta chegar os efeitos de desiguais de fluidos de reanimação na microcirculação, inflamação, barreira intestinal e ganhos clínicos na pancreatite aguda grave (PAS), com a Glutamina. Em comparação ao grupo NS, os pacientes dos grupos HS e HSG chegou mais rápido ao endpoint (3,9 ± 0,23 d e 4,1 ± 0,21 d vs 5,8 ± 0,25 d, P < 0,05) com menor volume de casos de infecção respiratória e abdominal minimizou valiosamente nos grupos HS e SHG, não foi observada diferença significativa na sepse. Em comparação, a relação L/M na urina e a endotoxina sérica foram menores no grupo SH e diminuíram ainda mais no grupo SHG líquidos (67,26 ± 28,53 mL/kg/ d, 61,79 ± 27,61 mL/kg por dia vs 85,23 ± 21,27 mL/kg por dia, P < 0,05). Em comparação com o grupo NS, a recorrência de disfunção renal, SDRA, MODS e SCA nos grupos HS e HSG foi claramente menor.
Sobre a ótica de Nobutoshi Fushimi, (2017), a glutamina apresentou vários papéis vantajosos no tratamento gastrointestinal. Porém todos os fechamentos em grupo de paciente sobre o uso de glutamina F, foram expressivamente menores do que no grupo tratado com glutamina-fibra-oligossacarídeo. A possibilidade da causa ser diferente, pode ser os componentes aditivos dos suplementos de glutamina.
Ziegle, (2016), tem objetivo de mensurar se a nutrição parenteral (NP) suplementada com glutamina (GLN) ajuda evoluir o quadro clínico de pacientes da unidade de terapia intensiva cirúrgica (UTI). Durante o estudo ocorreram 11 mortes (14,7%) no grupo GLN-PN e 13 mortes no grupo STD-PN (17,3%; outros indicadores como taxa incidente de infecção da corrente sanguínea foi de 9,6 e 8,4 por 1.000 dias de hospitalização nos grupos GLN-PN e STD-PN, (P = 0,73). Demais valores clínicos e eventos ao contrário foram idênticos.
Nakamura, (2020), Aferir a força do complexo HMB na diminuição de volume muscular no período de cuidados intensivos. Observou uma redução expressiva nos volumes durante os dias 1-10 (P <0,0001). As taxas de perda de volume corresponderam de 14,4 ± 7,1% para os participantes controle e 11,4 ± 8,1% para os participantes do HMB (P = 0,18). Constatou-se que em pacientes graves, a suplementação do complexo HMB na fase crítica da terapia intensiva não bloqueia a perda de volume muscular.
A investigação realizada por Kieviet, (2013), sobre a suplementação de glutamina no período neonatal, combinada ao aumento dos volumes da estrutura cerebral em idade escolar em crianças muito prematuras. O perímetro cefálico no 1 ano de vida foi válido, quando associado ao volume de substância branca e ao volume de substância cinzenta (variação r = 0,55-0,81, todos p < 0,002) na idade escolar. Resultados apontam o aumento específico no desenvolvimento do perímetro cefálico. Norouzi, (2022), procura demonstrar que o período pré-operatório é o momento apropriado para melhorar o estado nutricional, reparar falhas nutricionais e otimizar a função imunológica na cirurgia subjacente dos pacientes. A suplementação com uma mistura de L-glutamina (Gln), β-hidroxi-β-metilbutirato (HMB) e L-arginina (Arg), teve efeitos propícios na recuperação.
Para Pérez, (2014), suas análises buscam demonstrar o efeito da suplementação intravenosa (i.v.) de dipeptídeo L-alanil-L-glutamina na melhoria clínica de pacientes traumatizados internados em unidade de terapia intensiva (UTI). Observado o tempo de permanência na UTI, o tempo de internação hospitalar e a mortalidade na UTI, não foram encontradas diferenças significativas.
Jones, (2015), observa pacientes em recuperação de doenças críticas, que podem sofrer perda significativa de massa muscular. Pesquisa se um programa de fisioterapia aprimorada e exercícios estruturados (PEPSE) e uma bebida suplementar de aminoácidos essenciais (mistura de glutamina e aminoácidos essenciais [GEAA]). Nos resultados constam a redução expressiva nas taxas de ansiedade, o suplemento controle/PEPSE (P = 0,047) e suplemento GEAA/PEPSE (P = 0,036) e para suplemento GEAA/PEPSE na depressão (P = 0,0009). Wischmeyer, (2019), investiga nutrientes, como a glutamina (GLN), que danifica os níveis de uma família de proteínas denominadas proteínas de choque térmico (HSPs) em doenças críticas experimentais e clínicas. Os resultados observados pelo autor, mostra que o risco relativo para mortalidade hospitalar foi diminuído em 75% (RR = 0,25, p = 0,001) para pacientes da UTII com um queda mais rápida da eHSP70 e a suplementação com GLN não ampliou o eHSP70.
Moreira, (1999), observa bebês gravemente doentes com desnutrição protéico-calórica devido às demandas metabólicas da sepse e da insuficiência respiratória. A imunomodulação, o amparo intestinal e a cuidado da depleção de proteínas são citadas entre os seus efeitos positivos em tais circunstâncias, resultando em uma inclinação para redução da morbidade e mortalidade séptica.
4. CONCLUSÃO
Em conformidade aos artigos analisados observa-se que em todos os casos a aplicação de glutamina, gerou resultados positivos nos pacientes que receberam o tratamento. A diversidade de exemplos apresentados na segunda tabela de análise, retrata de forma benéfica o tratamento com glutamina, na maioria dos estudos.
Em especial destaque a menção da suplementação de glutamina em pacientes com doenças graves, como Câncer/HIV, queimaduras entre outras enfermidades, pois o conjunto literário escolhido compreendeu uma ampla diversidade, tanto em adultos como em tratamentos de crianças.
Mais um apontamento de extrema importância sobre o uso da Glutamina é a economia por ela proporcionada “Destaca-se nesse estudo que com o uso de Gln em UTI’s junto, gerou uma economia de 15% no geral dos custos hospitalares”, fato também apresentado na primeira tabela, que analisou os indicadores hospitalares no Brasil.
Nos casos de cânceres gastrointestinais e cabeça e pescoço, a suplementação de glutamina, mostrou-se como um aliado de recuperação mais ativa, minimizando o tempo de hospitalização e aumentando a massa muscular conforme indicam os resultados das pesquisas da Suplementação de Glutamina no tratamento de pacientes com Câncer.
Em uma visão global, podemos definir a realização deste estudo como de extrema importância devido o tema pesquisado e os resultados encontrados, assim esperando que num futuro muito breve novos estudos possam potenciar e comprovar o uso da Glutamina em crianças e adultos.
Referências:
ABILES, J. et al . Efectos de la suplementación con glutamina sobre el sistema antioxidante y la peroxidación lipídica en pacientes críticos con nutrición parenteral. Nutr. Hosp., Madrid , v. 23, n. 4, p. 332-339, agosto 2008 . Disponible en . accedido en 06 set. 2023.
ALBUQUERQUE Ceres; MACHADO Juliana. As internações do SUS na década de 2010 e nos anos de COVID-19, set 2022, https://observatoriohospitalar.fiocruz.br/debates-e-opinioes/internacoes-do-sus-na-decada-de-2010-e-nos-anos-de-covid-19, acessado em 12 out. 2023
BERGERSON SL. Nutritional Support in Bone Marrow Transplant Recipients. In: On call in… Bone Marrow Transplantation Burt RK, Deeg HS, Lothian ST, Santos GW. RG Lander Company and Chapman & Hall, Canada; 1996. P.343-55.
BIOLO G, Zorat F, ANTONIONE R, Ciocchi B. Muscle glutamine depletion in the intensive care unit. Int J Biochem Cell Biol. 2005;37(10):2169-79.
CURI R. Glutamina: metabolismo e aplicações clínicas e no esporte. Rio de Janeiro: Sprint, 2000. 261p.
CURI, R.; NEWSHOLME, P.; MARZUCA-NASSR, G.N.; TAKAHASHI, H.K.; HIRABARA, S.M.; CRUZAT, V.; KRAUSE, M.; BITTENCOURT, P.I.H., Jr. Regulatory principles in metabolism-then and now. Biochem. J. 2016, 473, 1845–1857.[CrossRef] [PubMed].
CRUZAT, Vinicius Fernandes; PETRY, Éder Ricardo; TIRAPEGUI, Julio. Glutamina: Aspectos Bioquímicos, Metabólicos, Moleculares e Suplementação. Rev Bras Med Esporte, São Paulo, v. 15, n. 5, p. 392-397, set. 2007
FERREIRA, Iára Kallyanna Cavalcante; FERNANDES, Sandra Lúcia. Terapia Nutricional em Unidade de Terapia Intensiva: a systematic review and meta-analysis. Revista Brasileira de Terapia Intensiva, Goiânia, v. 19, n. 1, p. 90-97, 19 jan. 2007.
FIOCRUZ, Observatório de Políticas e Gestão Hospitalar – OPGH, 2022. Acessado em 13-out.2023, https://observatoriohospitalar.fiocruz.br/dados-e-indicadores.
GHOLAMALIZADEH M. et al (2021). Effect of glutamine supplementation on inflammatory markers in critically ill patients supported with enteral or parenteral feeding. JPEN J Parenter Enteral Nutr. 2021 Jul 2. Epub ahead of print. PMID: 34213769. Disponível em: https://pubmed.ncbi.nlm.nih.gov/34213769/
MACBURNEY M, YOUNG LS, Ziegler TR, WILMORE DW. A cost-evaluation of glutamine-supplemental parenteral nutrition in adult bone marrow transplant patients J Am Diet Assoc 1994; 94: 1263- 1266.
McMAHAN P., McFARLAND D.A. 2021. Creative Destruction: The Structural Consequences of Scientific Curation. Am Sociol Review [online]. 86(2):341-376. [viewed 14 July 2021] http://doi.org/10.1177/0003122421996323 Available from: https://journals.sagepub.com/doi/10.1177/0003122421996323
MARTINS, Paulo. Glutamine in critically ill patients: is it a fundamental nutritional supplement?. Revista Brasileira de Terapia Intensiva, [S.L.], v. 28, n. 2, p. 112-118, 2016. GN1 Genesis Network. http://dx.doi.org/10.5935/0103-507x.20160022.
ORFILA, G. Mercadal; TALAVERÓNP, Jm Llop; GARCÍA, B. Gracia; PUIGSERVE, C. Martorell; MOLAS, M.ª Tubau; MASANES, R. Jodar. Uso de glutamina em nutrição parenteral no paciente crítico: efeitos na morbidade e mortalidade. Nutrición Hospitalaria, Barcelona, v. 22, n. 1, p. 61-67
OUDEMANS-VAN Straaten HM, BOSMAN RJ, TRESKES M, VAN DER SPOEL HJ, ZANDSTRA DF. Plasma glutamine depletion and patient outcome in acute ICU admissions. Intensive Care Med. 2001;27(1):84-90.
PETERSSON B, VINNARS E, WALLER SO, WERNERMAN J. Long-term changes in muscle free amino acid levels after elective abdominal surgery. Br J Surg. 1992;79(3):212-6.
PIMENTEL, Rodrigo Fernandes Weyll; FERNANDES, Sandra Lúcia. Effects of parenteral glutamine in critically ill surgical patients: a systematic review and meta-analysis. Nutrición Hospitalaria, [S.L.], v. 3, n. 37, p. 616-621, dez. 2020. ARAN Ediciones. http://dx.doi.org/10.20960/nh.02949.
ROTHE, E. T. (2007). Revisão sistemática x revisão narrativa. Acta paul. Enferm, 20(2), 5-6.
XU J, YUNSHI Z, Li R. Immunonutrition in surgical patients. Curr Drug Targets. 2009; 10(8):771-7.
