THE DIAPHRAGMATIC THICKNESS PROFILE IN CRITICAL PATIENTS POST-WEANING FROM MECHANICAL VENTILATION
REGISTRO DOI: 10.69849/revistaft/ra10202411181102
Noemia Dos Santos Dias 1
João Dereck Figueiredo Torres 2
Gabrielly Ferreira Alves 3
Thiago Augusto Sobral Mangueira 4
Axell Lins 5
Resumo
Introdução: O paciente crítico é aquele que desenvolve alteração das funções fisiológicas básicas para a manutenção da vida, sendo necessário a ventilação mecânica como forma de tentar estabilizar o quadro, porém quando prolongada, pode resultar em fatores maléficos como a fraqueza muscular diafragmática que em alguns casos resulta na falha do desmame da ventilação mecânica. A ultrassonografia diafragmática é uma alternativa a fim de evitar que tal fato ocorra. Objetivo: Mensurar espessura diafragmática de pacientes adultos intubados através da ultrassonografia e correlacionar com o sucesso de desmame ventilatório. Métodos: Trata-se de um estudo não randomizado, prospectivo, transversal com 41 pacientes que usaram ventilação mecânica por tubo orotraqueal e traqueostomia, avaliados até 24h pós desmame ventilatório. Foi realizada ultrassonografia diafragmática no nono espaço intercostal e entre as linhas axilar anterior e axilar média no hemicorpo direito e calculado a taxa de espessamento do mesmo com a média de 3 inspirações e expirações. Resultados: Os indivíduos com idade menor ou igual que 30 anos (p=0.0012*) apresentaram menos risco de óbito (p=0.0055*). Nesse contexto, os que usaram tubo orotraqueal apresentaram melhor resultado do que os que usaram traqueostomia (p= 0.0111*). A taxa de espessamento menor que 1,5mm que resultou em falha de desmame (p=<0.0001*). Dentre os pacientes que evoluíram com esse insucesso, 3 usaram Tubo orotraqueal e 4 com Traqueostomia. Conclusão: Pacientes com valores de espessura diafragmática menor que 2mm tiveram uma alta predisposição a intolerância ao desmame da ventilação mecânica, ficando claro também a sensibilidade elevada da ultrassonografia diafragmática na predição.
Palavras-chave: Ultrassonografia; Diafragma; Paciente Crítico; Desmame Ventilatório; Ventilação Mecânica Invasiva.
1 INTRODUÇÃO
O paciente crítico é aquele que desenvolve alteração das funções fisiológicas básicas para a manutenção da vida. Esta pode levá-lo à uma instabilidade hemodinâmica que, se não for sanada, pode resultar na morte. Sabendo disso, diversas abordagens, a fim de compensar esses distúrbios, podem ser utilizadas como por exemplo as drogas vasoativas, volumes, sedação, analgésicos, esteroides entre outros (Chaverri et al, 2022; Messina et al, 2022; Zampieri et al, 2023).
Nesse contexto, devido a criticidade do quadro que o paciente acaba desenvolvendo, medidas devem ser adotadas para evitar que haja uma piora e em sua maioria, o imobilismo induzido por esta acaba sendo um fator não positivo, porém necessário (Yonger 2023; Yang et al, 2023; Ely 2023). Já em outros casos, quando existe a viabilidade clínica para ser aplicado a mobilização precoce (<48h de internação) ou a fisioterapia motora (>48h de internação), o fisioterapeuta deve utilizar de lpO) provocado pelo agente causador da patologia de base (Megha 2021; Rosa et al, 2023 Teleanu et al, 2022; Wang et al, 2020).
A Ventilação Mecânica (VM), utilizada como forma de tentar estabilizar o quadro do paciente, quando prolongada, pode resultar em fatores maléficos como a fraqueza muscular diafragmática em virtude da inibição da contração muscular que leva a perda e/ou diminuição do sarcômero, comprometendo a atividade contrátil da fibra muscular e transformando as fibras de contração lenta em fibras de contração rápida. Não somente isso, em virtude da ausência de contratilidade, ocorre o encurtamento dessas estruturas diminuindo a amplitude de movimento e afetando indiretamente na força muscular. A nível neuromuscular, o desenvolvimento desse quadro desencadeia uma desmielinização e redução da atividade do fuso neuromuscular (Bureau et al, 2023; Spiesshoefer, et al, 2023; Takahashi et al, 2023; Zhang et al, 2023).
A VM prolongada associada a efeitos da síndrome do imobilismo pode resultar em desequilíbrio com a carga determinada ao sistema respiratório, desencadeando fadiga da musculatura ventilatória e dependendo do caso, pode levar à uma falha do desmame da ventilação mecânica (Bertoni et al, 2022). Sabendo que esse processo se trata de um passo muito importante para o paciente, pois, é a transição da ventilação artificial para a espontânea, é importante que a atividade muscular desse grupamento esteja dentro do ideal e para que isso seja possível, é importante observar fatores como espessura, tônus, amplitude e força.
Para que o processo seja bem-sucedido, é necessário que uma avaliação multidisciplinar seja realizada com a equipe responsável, visando diminuir os riscos ao paciente, haja vista que caso isso aconteça, as chances de morbimortalidade aumentam consideravelmente. Portanto, a fim de evitar tal ocorrência, medidas de avaliação beira leito são utilizadas para que se tenha mais certeza da conduta a ser executada, sendo uma delas a ultrassonografia diafragmática, que objetiva analisar a aeração pulmonar, a espessura da musculatura ventilatória, bem como o seu potencial de rebaixamento ao realizar uma contração e o seu relaxamento e retorno para a posição em repouso. Não somente isso, foi comprovado a fidedignidade desta avaliação para traçar metas diárias dentro das Unidades de Terapia Intensiva (UTI) (Boom et al, 2023; Monteagudo et al, 2022; Bertoni et al, 2021).
Dentro deste cenário, é de grande relevância abordar o uso da ultrassonografia para otimização das condutas e executar uma avaliação mais precisa do quadro ventilatório desses pacientes e assim diagnosticar alterações que coloquem em risco o prognóstico do paciente. Porém, ainda não existe um consenso sobre quais os valores da espessura diafragmática podem oferecer riscos ao indivíduo de não tolerar o desmame ventilatório. Portanto, o presente estudo possui como objetivo de avaliar a espessura diafragmática de pacientes adultos intubados através da ultrassonografia e correlacionar com o sucesso de desmame ventilatório.
2 METODOLOGIA
Trata-se de um estudo transversal, aprovado pelo comitê de ética em pesquisa com seres humanos do Centro Universitário Maurício de Nassau com parecer substanciado de número 6.075.344/2023, obedecendo os preceitos éticos do Conselho Nacional de Saúde 466/2012. A pesquisa foi realizada nas UTI’s adulto no Hospital Regional Dr. Abelardo Santos na cidade de Belém-PA, Brasil, no período de junho a novembro de 2023, com amostra selecionada por conveniência.
Foram incluídos no estudo, pacientes com idade igual ou maior que 18 anos, hemodinâmicamente estáveis, sem uso de sedação, sem droga vasoativa ou em uso com vazão menos que 0,2mcg/Kg/min, sem agitação no leito. Frequência cardíaca > 60 bpm e < 130bpm; Pressão arterial sistólica > 90mmHg < 180mmHg; Pressão arterial média > 60mmHg < 120mmHg, ausência de aumento de dose vasopressora nas últimas 2 horas. Do ponto de vista respiratório, frequência respiratória > 10irpm e < 25irpm e saturação periférica de oxigênio > 88%; com um tempo maior que 72h de uso de VMI, em uso de tubo orotraqueal e/ou traqueostomia e que tivesse o termo de consentimento livre e esclarecido assinado pelo responsável legal.
Foram excluídos do estudo pacientes com instabilidade hemodinâmica na hora da avaliação, que durante o processo de desmame ventilatório sofressem uma extubação acidental, que tiveram falha de desmame ventilatório por piora clínica em virtude da doença de base e os que evoluíssem a óbito.
Assim que fosse definido a viabilidade do desmame da ventilação mecânica e a retirada desse suporte fosse efetuada, os pesquisadores realizavam a ultrassonografia diafragmática beira leito até 24h pós-retirada da VM, para que dessa forma, os valores da espessura do músculo tanto na fase inspiratória quanto expiratória apresentasse uma confiabilidade elevada sem que houvesse suporte da Ventilação Mecânica Invasiva (VMI). Após realizar o exame, o paciente era acompanhado para analisar se haveria alguma falha de desmame ventilatório para assim determinar os valores que foram mais propícios à ineficácia do processo.
O exame foi realizado através do aparelho de ultrassonografia da marca Edan® no modelo Acclarix-AX8, com transdutor retilíneo no plano sagital com o Probe Mark® direcionado para cabeça do voluntário da pesquisa, sendo posicionado sobre a zona de aposição (za) (nono espaço intercostal) e entre as linhas axilar anterior e axilar média no hemicorpo direito. Foi mensurado a espessura do diafragma através da média dos valores obtidos na fase inspiratória e expiratória e depois, calculado a taxa de espessamento.
A Taxa de Espessamento (Te) foi calculada por meio da divisão da Média da Espessura Inspiratória (MEins) e da Média da Espessura Expiratória (MEexp) através da marcação realizada na janela de modo M.
Os dados foram analisados no programa estatístico GraphPad Prism (GraphPad Software Inc., San Diego, CA, USA). A distribuição de normalidade dos dados foi verificada por meio do teste de Qui-quadrado de aderência e Qui-quadrado de contingência. Para comparação dos dados, foi realizado por meio do teste T-Student não pareado, com nível de significância estatística de 5% para todos os testes.
3 RESULTADOS E DISCUSSÕES
Foram selecionados um total de 41 indivíduos para amostra final com base nos critérios de inclusão e excluídos 3 indivíduos devido evoluírem a óbito durante a internação na UTI, totalizando 44 indivíduos avaliados.
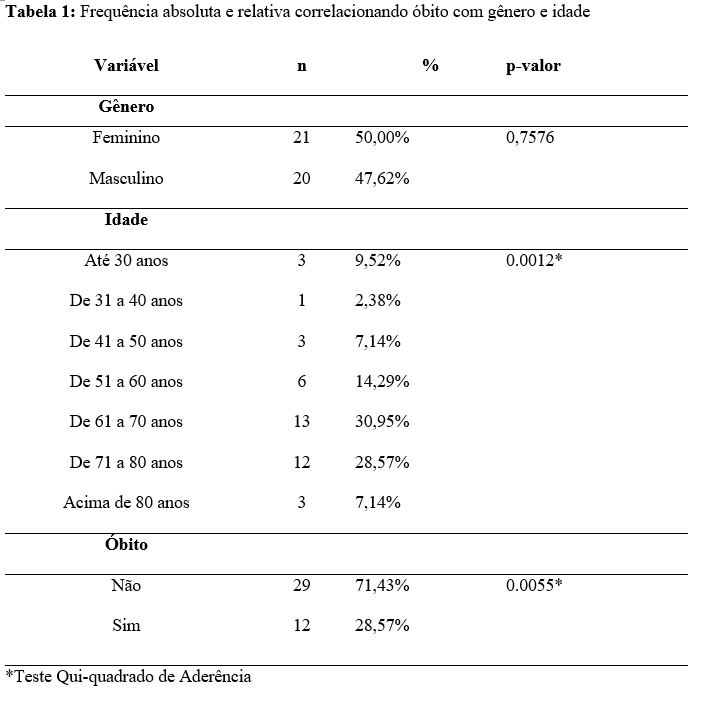
A tabela 1 evidencia o perfil clínico amostral, com base na frequência absoluta e relativa, onde a partir da correlação entre o gênero e a idade, pode-se perceber que os indivíduos que possuíam uma idade menor ou igual que 30 anos (p=0.0012*) apresentaram menos propensão de evoluir a óbito (p=0.0055*). Nesse contexto, a distribuição da amostra é mais homogênea do que o esperado, com 21 mulheres e 20 homens.
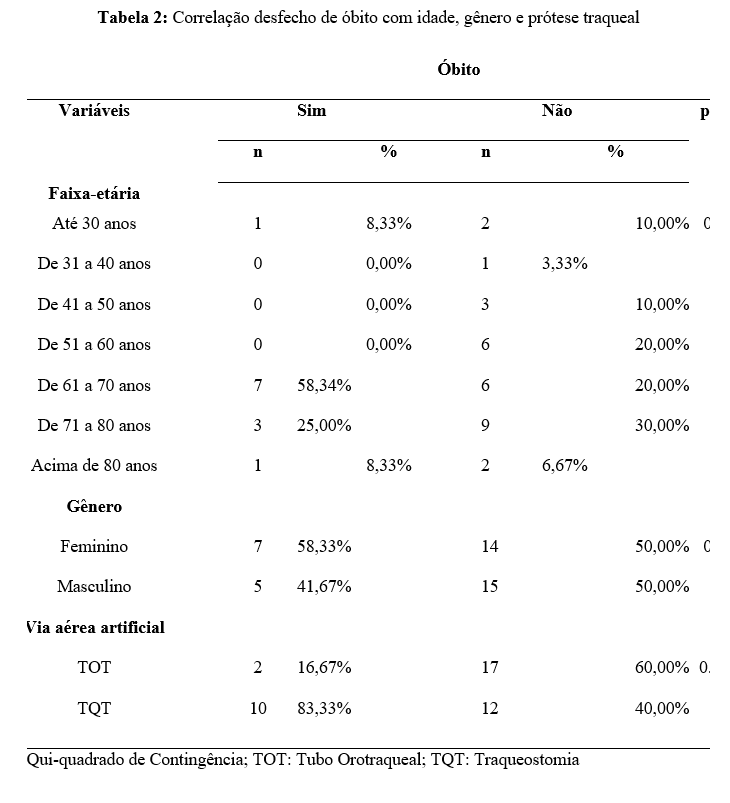
Já tabela 2, com a estratificação da amostra com base no desfecho de óbito, observa-se que o gênero e a idade não foram fatores que influenciaram diretamente tanto no desfecho positivo quanto negativo, porém, a prótese traqueal sim, uma vez que os pacientes que fizeram uso de Tubo Orotraqueal (TOT) apresentaram melhor resultado em comparação com os que tiveram que evoluir para a Traqueostomia (TQT) (p= 0.0111*), assim como a média de tempo de VMI foi de 11,3 dias para os pacientes intubados e de 23,4 dias para os pacientes que usaram TQT.
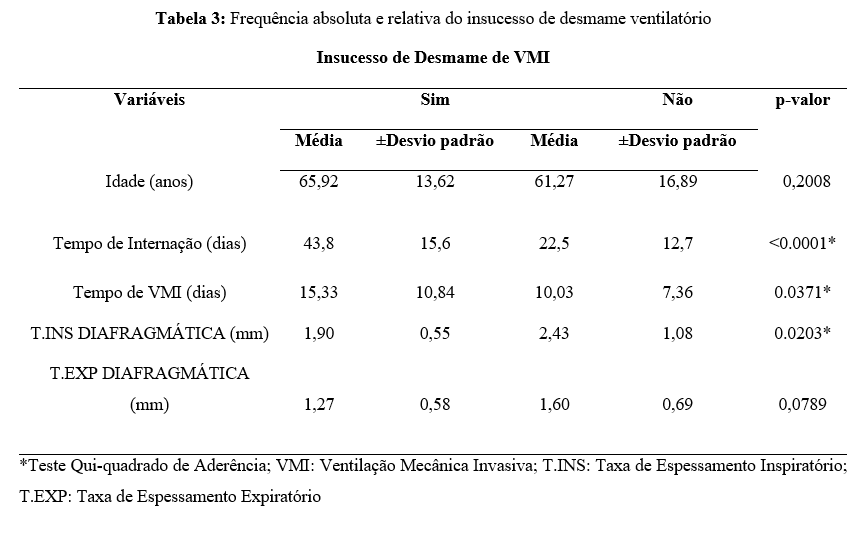
Partindo desse pressuposto, a respeito dos resultados do desmame ventilatório, conforme descrito na Tabela 3, foi possível observar que não houve uma correlação entre a idade e o sucesso da conduta, assim como a Taxa de Espessamento Expiratório (T.EXP). Porém, observa-se que com base nas variáveis analisadas, o tempo de internação foi o que teve maior impacto na falha do desmame da VMI e isso está diretamente ligado com o tempo de uso da ventilação mecânica que em conjunto com o suporte prolongado, diminuindo a carga de trabalho da musculatura diafragmática fez com que a Taxa de Espessamento Inspiratório (T. INSP) diminuísse consideravelmente. Haja vista que existem outros fatores que podem ser ligados à essa ideia, como a piora clínica, uso de sedação por tempo prolongado e comorbidades, conforme apresentado na Figura 1.
Figura 1: Principais causas da fraqueza diafragmática do paciente crítico
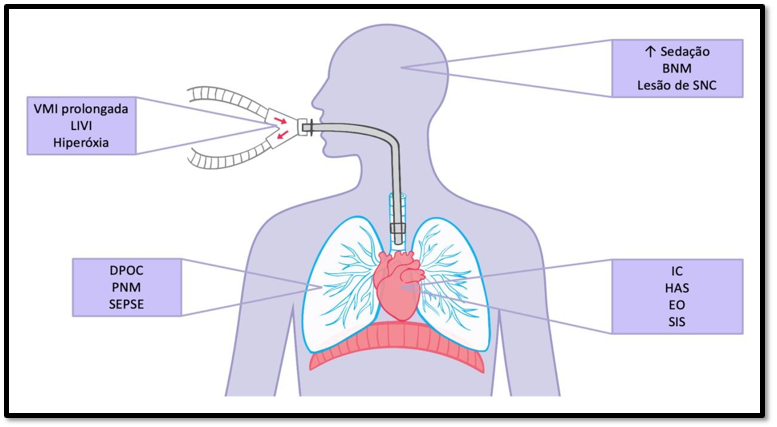
Fonte: Autores; VMI: Ventilação Mecânica Invasiva; LIVI: Lesão Induzida pela Ventilação Invasiva; DPOC: Doença Pulmonar Obstrutiva Crônica; PNM: Pneumonia; BNM: Bloqueador Neuromuscular; SNC: Sistema Nervoso Central; IC: Insuficiência Cardíaca; EO: Estresse Oxidativo; SIS: Síndrome Inflamatória Sistêmica.
A Figura 2 demonstra uma comparação da diferença de atividade contrátil do diafragma vista pela janela do modo M, onde observa-se que na Imagem A que o paciente consegue executar uma contração com um pouco mais de 5mm de espessura, porém, na imagem B o mesmo não consegue atingir mais do que 2mm. Vale ressaltar que estes achados não são do mesmo paciente, devido ao fato de que foi realizado apenas uma avaliação, tendo como foco dessa figura a análise comparativa da diferença entre os dois tipos de realidade do músculo.
Figura 2: Mensuração da contração diafragmática com maior valor (A) e menor valor (B)
Fonte: Autores; A (1, 2 e 3): Espessura Diafragmática Inspiratória; A (4, 5 e 6): Espessura Diafragmática Expiratória; B (1): Espessura Diafragmática Inspiratória; B (2, 3, 4): Espessura Diafragmática Expiratória, visualizadas pelo modo M.
Houve uma diversidade patológica na amostra estudada maior do que o esperado, onde, sendo a mais prevalente a Pneumonia Lobar, que apresentou um nível sarcopenia diafragmática elevado (Figura 3 – A) em comparação com a segunda doença mais prevalente que foi a Sepse, conforme apresentado na Figura 3 – B, valendo ressaltar que essas duas foram responsáveis por 30% de todas as falhas de desmame, seguida pelo Acidente Vascular Encefálico com 30% também, Pancreatite Aguda com 10%, Urgência Dialítica (10%), Broncopneumonia (10%) e Doença Pulmonar Obstrutiva Crônica (10%). Para tal, o Gráfico de incidência/prevalência (Figura 3 – C) descreve as outras doenças encontradas no público, tendo as duas primeiras que foram citadas anteriormente sido as que mais apresentaram disfunções da musculatura ventilatória (p=0.0001*).
Figura 3: Valores de espessura diafragmática de paciente com Pneumonia Lobar (A), Sepse (B) e Gráfico de Incidência por Prevalência de patologia (C)
Fonte: Autores; A e B (1,2 e 3): Espessura Diafragmática Inspiratória; A (4, 5 e 6): Espessura Diafragmática Expiratória visualizados pelo modo M; *p=<0.0001 em Teste T de Student não pareado. BPNM: Broncopneumonia, IRC: Insuficiência Renal Crônica, PNML: Pneumonia Lobar, ANG: Angiografia, ANGP: Angioplastia, SPS: Sepse, SF: Síndrome de Fournier.
Com base nos achados supracitados, a Figura 4 – A demonstra o nível de sarcopenia de um paciente que apresentou uma T.INS menor que 1,5mm que resultou em uma falha de desmame ventilatório e para reforçar esse achado, o gráfico da Figura 4 – B demonstra um p-valor estatisticamente significante (p=<0.0001*). Dentre os pacientes que evoluíram com esse insucesso, 3 usaram TOT e 4 com TQT.
Figura 4: Contração diafragmática reduzida (A) e Correlação positiva da diminuição da contração diafragmática com o aumento do tempo de VMI (B)
Fonte: Autores; A (1,2 e 3): Espessura Diafragmática Inspiratória; A (4, 5 e 6): Espessura Diafragmática Expiratória visualizado pelo modo M; *p=0.0203 para Teste de Qui-quadrado de Contingência; VMI: Ventilação Mecânica Invasiva.
Sabe-se que a atividade biológica de um indivíduo mais jovem apresenta uma resposta melhor quando atacada por algum agente patológico do que em pessoas mais velhas, uma vez que esse fator pode ser predisponente para o desfecho final do paciente, bem como traçar o seu prognóstico após a lesão. Pois, conforme já descrito na literatura, os mecanismos de reparo celular são mais atuantes nessas fases da vida, com pior progressão ao decorrer do avanço da idade (Bastard et al, 2022; Surmachevska 2023).
Entretanto, é importante salientar que o estilo de vida tanto profissional quanto pessoal, são fatores importantes para que o curso normal da função fisiológica aconteça, apesar de que na amostra estudada, variáveis como o gênero e a idade não foram fatores coligados ao desfecho do indivíduo. Sabendo que em virtude da criticidade do quadro do paciente, a necessidade de VMI acaba sendo alta e com isso, outros mecanismos como drogas vasoativas, sedoanalgésicos, bloqueadores neuromusculares, corticoterapias e antibioticoterapias são importantes a fim de manter a estabilidade hemodinâmica e a manutenção da vida, estudos enfatizam que essa terapêutica pode ser deletéria para a função diafragmática também, quando em uso prolongado (Bellaver et al, 2021; Sun et al, 2023; Tanaka et al, 2023).
No entanto, nessa fase do tratamento, muitos pacientes acabam apresentando uma boa resposta à conduta utilizada e mesmo assim alguns precisam ficar longos períodos na VMI (evoluindo com a necessidade de TQT) (Sklar et al, 2021), ficando propensos a desenvolvimento de infecções (Dridi et al, 2023), reagudização do quadro e óbito. Ainda nesse fato, o período elevado sob ventilação artificial desencadeia a sarcopenia diafragmática (Drummond et al, 2023), já que a pressão positiva somada ao tempo elevado de sedação (Li et al 2016), diminuem a espessura da musculatura ventilatória e assim enfraquecendo-a por desuso corroborando com os achados.
Partido do fato supracitado, estudos recentes (Li et al, 2021; Wang et al, 2021), demonstraram que não somente o contexto do suporte avançado de vida, mas também as alterações bioquímicas desencadeadas pelos patógenos agressores que desregulam o contexto biológico do paciente, propagam um aumento do processo inflamatório, levando a proliferação do estresse oxidativo que comumente pode levar à síndrome inflamatória sistêmica. Haja vista que a conduta profissional quando aplicada de forma incorreta pode facilitar o processo de desenvolvimento dessas desordens, como por exemplo a hiperóxia (TAYAR et al, 2022), desencadeada na maioria das vezes pela falta de monitoramento da resposta do paciente à oferta do oxigênio, aumentando a presença de radicais de superóxido proliferando das espécies reativas de oxigênio.
Sabe-se que as doenças respiratórias são as mais comuns dentro das UTI’s no mundo, em virtude disso, a sobrecarga da musculatura ventilatória que leva à fadiga se torna uma das principais causas de intubação no ambiente crítico e semicrítico. Nesse contexto, já ficou muito bem esclarecido que a fraqueza desse grupamento muscular é um grande causador do insucesso do desmame ventilatório (Er et al, 2023), porém o que ainda é incerto é até que valores de espessura muscular poderiam ser arriscado para realizar tal conduta. Um estudo categoriza valores abaixo de 2mm de espessura diafragmática como sendo risco de falha de desmame (Li et al, 2023), e partindo desse pressuposto, nós encontramos achados semelhantes a este, valendo ressaltar que o insucesso ligado à essa mensuração foi prevalente tanto em pacientes com TOT quanto os que usaram TQT. Uma vez que os indivíduos que tiveram um valor menor do que o já mencionado acabaram não tolerando a saída do suporte ventilatório, assim como foi difícil encontrar dados precisos até pela janela ultrassonográfica, pois em valores muito baixos não era possível analisar a mensuração da espessura pela Janela M, mas sim somente pela Janela B. Apesar desse fato, em um dos casos foi viável realizar essa mensuração pela Janela M, onde a média da avaliação foi de 1,14mm resultando na intolerância à respiração espontânea no caso desse paciente. Nesse contexto é demonstrado a correlação, onde quanto menor o valor, maior o risco de falha, assim como descreve as pesquisas.
Diversos mecanismos podem provocar esse tipo de comprometimento, podendo ser categorizados de acordo com sua ligação ao paciente, como por exemplo os descritos na Figura 1: mecanismos neurológicos (sedação, bloqueador neuromuscular, neuropatias congênitas e adquiridas), ventilatórios (VMI prolongada, super assistência ventilatória), cardiovascular e metabólico (estresse oxidativo, síndrome inflamatória sistêmica e hipoproteinemia). Nesse contexto, terapêuticas são utilizadas a fim de recrutar fibras musculares, melhora do trofismo e tônus através do treinamento muscular respiratório, com cargas lineares e não lineares objetivando o conforto e tolerância do desmame.
4 CONCLUSÃO
Em virtude disso, foi possível analisar os riscos de falha de desmame nos pacientes que apresentaram uma contratilidade diafragmática abaixo do valor já descrito na literatura, valendo ressaltar que o método ultrassonográfico apresenta uma alta confiabilidade, mas deve ser utilizado juntamente com outras formas de avaliação para que o protocolo de saída da ventilação mecânica seja bem-sucedido e dessa forma evitar o risco de morbimortalidade como encontrado em outro estudo.
Portanto, fica claro que pacientes com valores de espessura diafragmática menor que 2mm tiveram uma alta predisposição a intolerância ao desmame da ventilação mecânica tanto em usuários de traqueostomia quanto de tubo orotraqueal, estando diretamente ligado à dificuldade de superar a resistência imposta pelas vias aéreas superiores.
Espera-se que mais estudos com uma amostra maior possam ser realizados com essa temática para que seja possível evitar falhas de desmame e o aumento do risco de morbimortalidade.
REFERÊNCIAS
BASTARD, Paul, et al. Autoantibodies neutralizing type I IFNs are present in ~4% of uninfected individuals over 70 years old and account for ~20% of COVID-19 deaths. Sci Immunol. 2021 Aug 19;6(62): eabl4340. doi: 10.1126/sciimmunol. abl4340. PMID: 34413139; PMCID: PMC8521484.
BELLAVER, Priscila, et al. Association between neuromuscular blocking agents and the development of intensive care unit-acquired weakness (ICU-AW): A systematic review with meta-analysis and trial sequential analysis. Anaesth Crit Care Pain Med. 2023 Jun;42(3):101202. doi: 10.1016/j.accpm.2023.101202. Epub 2023 Feb 16. PMID: 36804373.
BERTONI, Michele, et al. Occurrence and Effects on Weaning from Mechanical Ventilation of Intensive Care Unit Acquired and Diaphragm Weakness: A Pilot Study. Front Med (Lausanne). 2022 Jul 22; 9:930262. doi: 10.3389/fmed.2022.930262. PMID: 35935791; PMCID: PMC9354572.
BOON, Andrea, et al. Electrodiagnostic and ultrasound evaluation of respiratory weakness. Muscle Nerve. 2023 Nov 17. doi: 10.1002/mus.27998. Epub ahead of print. PMID: 37975205.
BUREAU, Come, et al. Managing respiratory muscle weakness during weaning from invasive ventilation. Eur Respir Rev. 2023 Apr 5;32(168):220205. doi: 10.1183/16000617.0205-2022. PMID: 37019456; PMCID: PMC10074167.
CHAVERRI, José, et al. The Pharmacist’s Role in the Implementation of FASTHUG-MAIDENS, a Mnemonic to Facilitate the Pharmacotherapy Assessment of Critically Ill Patients: A Cross-Sectional Study. Pharmacy (Basel). 2022 Jun 30;10(4):74. doi: 10.3390/pharmacy10040074. PMID: 35893712; PMCID: PMC9326553.
DRIDI, Haikel, et al. Aberrant mitochondrial dynamics contributes to diaphragmatic weakness induced by mechanical ventilation. PNAS Nexus. 2023 Nov 7;2(11): pgad336. doi: 10.1093/pnasnexus/pgad336. PMID: 37954156; PMCID: PMC10635656.
DRUMMOND, Sarah, et al. Chronic Intermittent Hypoxia-Induced Diaphragm Muscle Weakness Is NADPH Oxidase-2 Dependent. Cells. 2023 Jul 12;12(14):1834. doi: 10.3390/cells12141834. PMID: 37508499; PMCID: PMC10377874.
ELY, Wesley. Early Active Mobilization during Mechanical Ventilation in the ICU. N Engl J Med. 2023 Feb 9;388(6):572. doi: 10.1056/NEJMc2216086. PMID: 36780684.
ER, Berrini, et al. Is diaphragm ultrasound better than rapid shallow breathing index for predicting weaning in critically ill elderly patients? Tuberk Toraks. 2023 Sep;71(3):197-202. English. doi: 10.5578/tt.20239701. PMID: 37740623.
J, Wang, et al. The application value of diaphragm ultrasound in the weaning of ventilator for patients undergoing heart valve replacement. Zhonghua Yi Xue Za Zhi. 2021 Dec 14;101(46):3814-3818. Chinese. doi: 10.3760/cma.j.cn112137-20210602-01261. PMID: 34895423.
JUNG, Boris, et al. Diaphragmatic dysfunction in patients with ICU-acquired weakness and its impact on extubation failure. Intensive Care Med. 2016 May;42(5):853-861. doi: 10.1007/s00134-015-4125-2. Epub 2015 Nov 16. PMID: 26572511.
LEWIS Kimberley, et al. Dexmedetomidine vs other sedatives in critically ill mechanically ventilated adults: a systematic review and meta- analysis of randomized trials. Intensive Care Med. 2022 Jul;48(7):811-840. doi: 10.1007/s00134- 022-06712-2. Epub 2022 Jun 1. PMID: 35648198.
LI, Shigang, et al. Application of bedside ultrasound in predicting the outcome of weaning from mechanical ventilation in elderly patients. BMC Pulm Med. 2021 Jul 9;21(1):217. doi: 10.1186/s12890-021-01605-4. PMID: 34243739; PMCID: PMC8267769.
LI, Wenrui, te al.. The risk factors of reintubation in intensive care unit patients on mechanical ventilation: A systematic review and meta-analysis. Intensive Crit Care Nurs. 2023 Feb; 74:103340. doi: 10.1016/j.iccn.2022.103340. Epub 2022 Nov 8. PMID: 36369190.
LIH, Chang. Inhibition of Src and forkhead box O1 signaling by induced pluripotent stem-cell therapy attenuates hyperoxia-augmented ventilator-induced diaphragm dysfunction. Transl Res. 2016 Jul; 173:131-147.e1. doi: 10.1016/j.trsl.2016.03.011. Epub 2016 Mar 22. PMID: 27055225.
MEGHA, Kb, então. Cascade of immune mechanism and consequences of inflammatory disorders. Phytomedicine. 2021 Oct; 91:153712. doi: 10.1016/j.phymed.2021.153712. Epub 2021 Aug 19. PMID: 34511264; PMCID: PMC8373857.
MESSINA, Antonio, et al. Fluid challenge in critically ill patients receiving haemodynamic monitoring: a systematic review and comparison of two decades. Intensive Crit Care. 2022 Jun 21;26(1):186. doi: 10.1186/s13054-022-04056-3. PMID: 35729632; PMCID: PMC9210670.
MNUSKINA, Sophia, et al. Single fibre cytoarchitecture in ventilator-induced diaphragm dysfunction (VIDD) assessed by quantitative morphometry second harmonic generation imaging: Positive effects of BGP-15 chaperone co-inducer and VBP-15 dissociative corticosteroid treatment. Front Physiol. 2023 Jun 27; 14:1207802. doi: 10.3389/fphys.2023.1207802. PMID: 37440999; PMCID: PMC10333583.
MONTEAGUDO, Ródenas, et al. Update on the use of ultrasound in the diagnosis and monitoring of the critical patient. Rev Esp Anestesiol Reanim (Engl Ed). 2022 Nov;69(9):567-577. doi: 10.1016/j.redare.2022.01.003. Epub 2022 Oct 14. PMID: 36253286.
ROSA, Débora, et al. The Effects of Early Mobilization on Acquired Weakness in Intensive Care Units: A Literature Review. Dimens Crit Care Nurs. 2023 May-Jun 01;42(3):146-152. doi: 10.1097/DCC.0000000000000575. PMID: 36996359.
SAAD, Marina et al. Ultrasonographic Assessment of Diaphragmatic Function and Its Clinical Application in the Management of Patients with Acute Respiratory Failure. Diagnostics (Basel). 2023 Jan 23;13(3):411. doi: 10.3390/diagnostics13030411. PMID: 36766515; PMCID: PMC9914801.
SKLAR, Michael, et al. Duration of diaphragmatic inactivity after endotracheal intubation of critically ill patients. Crit Care. 2021 Jan 11;25(1):26. doi: 10.1186/s13054-020- 03435-y. PMID: 33430930; PMCID: PMC7798017.
SPIESSHOEFER, Jens, et al. Kersten A, Enriquez Geppert J, Regmi B, Senol M, Kabitz HJ, Dreher M. State-of- the-Art Opinion Article on Ventilator-Induced Diaphragm Dysfunction: Update on Diagnosis, Clinical Course, and Future Treatment Options. Respiration. 2023;102(1):74-82. doi: 10.1159/000527466. Epub 2022 Dec 1. PMID: 36455543
SUN, Chuan, et al. Comparison of clinical outcomes in critically ill COVID-19 patients on mechanical ventilation with nosocomial pneumonia between Alpha and Omicron variants. Ther Adv Respir Dis. 2023 Jan- Dec; 17:17534666231213642. doi: 10.1177/17534666231213642. PMID: 38018405; PMCID: PMC10685785.
SURMACHEVSKA, Natália , et al. Corticosteroid Induced Myopathy. In: StatPearls, Treasure Island (FL): StatPearls Publishing. 2023 Jan–. PMID: 32491663. 2023 Apr 17
TANAKA, Aiko, et al. Association between tracheostomy and survival in patients with coronavirus disease 2019 who require prolonged mechanical ventilation for more than 14 days: A multicenter cohort study. Auris Nasus Larynx. 2023 Apr;50(2):276-284. doi: 10.1016/j.anl.2022.06.002. Epub 2022 Jun 13. PMID: 35764477; PMCID: PMC9189113.
TAKAHASHI, Yuta, et al. Diaphragm Dysfunction and ICU-Acquired Weakness in Septic Shock Patients with or without Mechanical Ventilation: A Pilot Prospective Observational Study. J Clin Med. 2023 Aug 9;12(16):5191. doi: 10.3390/jcm12165191. PMID: 37629233; PMCID: PMC10455261.
TAYAR, Ashraf, et al. Diaphragm Electromyography Versus Ultrasonography in the Prediction of Mechanical Ventilation Liberation Outcome. Respir Care. 2022 Jul 19: respcare.09779. doi: 10.4187/respcare.09779. Epub ahead of print. PMID: 35853707.
TELEANU, Daniel, et al. An Overview of Oxidative Stress, Neuroinflammation, and neurodegenerative diseases. Int J Mol Sci. 2022 May 25;23(11):5938. doi: 10.3390/ijms23115938. PMID: 35682615; PMCID: PMC9180653.
WANG, Huimei, et al. Nitric oxide inhibitory iridoids as potential anti-inflammatory agents from Valeriana jatamansi. Bioorg Chem. 2020 Aug; 101:103974. doi: 10.1016/j.bioorg.2020.103974. Epub 2020 May 25. PMID: 32512268.
YANG, Xiaolong, et al. Early Mobilization for Critically Ill Patients. Respir Care. 2023 Jun;68(6):781-795. doi: 10.4187/respcare.10481. Epub 2023 Apr 11. PMID: 37041029; PMCID: PMC10209006.
YOUNGER, David. Critical illness-associated weakness and related motor disorders. Handb Clin Neurol. 2023; 195:707-777. doi: 10.1016/B978-0-323-98818-6.00031-5. PMID: 37562893.
ZAMPIERI, Fernando, et al. Fluid Therapy for Critically Ill Adults with Sepsis: A Review. JAMA. 2023 Jun 13;329(22):1967-1980. doi: 10.1001/jama.2023.7560. PMID: 37314271.
ZHANG, Jumei, et al. Research progress on the pathogenesis and treatment of ventilator-induced diaphragm dysfunction. Heliyon. 2023 Nov 14;9(11): e22317. doi: 10.1016/j.heliyon. 2023.e22317. PMID: 38053869; PMCID: PMC10694316.
1 Discente do Curso Superior de Bacharelado em Fisioterapia da Universidade da Amazônia Campus Gentil e-mail: miahsantos69@gmail.com
2 Discente do Curso Superior de Bacharelado em Fisioterapia da Universidade da Amazônia Campus Gentil e-mail: joaodereck32@gmail.com
3 Discente do Curso Superior de Bacharelado em Fisioterapia da Universidade da Amazônia Campus Gentil e-mail: gaby.alves1208@gmail.com
4 Coorientador do Curso Superior de Bacharelado em Fisioterapia da Universidade da Amazônia Campus Gentil e-mail: thiagosobral20@gmail.com
5 Docente do Curso Superior de Bacharelado em Fisioterapia da Universidade da Amazônia Campus Gentil. Mestre em Farmacologia e Bioquímica (PPGFARMABIO/UFPA). e-mail: axell.ti20@gmail.com
