REGISTRO DOI: 10.5281/zenodo.10273262
Mariah Tavares Barreto1
Lara Martini Siqueira Rodrigues Almeida1
Leticia Pedra Ferreira de Vasconcelos Rangel1
Barbara Tavares Barreto2
Liz Eyer2
Paula Eyer2
Luiz Henrique Guedes Moretz-sohn2
Palavras-chaves:
Miocardiopatia periparto; miocardiopatia dilatada; insuficiência cardíaca
Introdução:
A cardiomiopatia periparto é uma doença caracterizada por uma disfunção sistólica ventricular esquerda que surge entre o último trimestre da gravidez e o período pós-parto precoce, em mulheres previamente saudáveis. É uma doença rara, de etiologia desconhecida, que acomete mulheres em idade reprodutiva e sua incidência está relacionada ao ciclo gravídico-puerperal. Parece associar-se à interação fisiológica da gestação e do puerpério com fatores inflamatórios, infecciosos, genéticos, hormonais e metabólicos. A gravidez atua sobre as doenças do coração ao provocar modificações no organismo materno que repercutem sobre sua função cardiovascular e que podem agravar sua morbidade hemodinâmica, agravamento esse observado em 30 a 50% das gestantes cardiopatas nas classes funcionais III e IV, situação que conduz a mãe ao óbito em 25 a 50%.⁵ Já as gestantes classificadas na classe I e II evoluem habitualmente de forma satisfatória. ⁵
Metodologia:
As informações foram obtidas por meio de revisão do prontuário do paciente, entrevista com o paciente e seus pais, registro fotográfico dos métodos diagnósticos aos quais o paciente foi submetido e revisão da literatura.
Relato do caso:
Paciente feminina, 31 anos, negra, casada, do lar, natural e procedente de Campos dos Goytacazes. Foi diagnosticada há cerca de um ano e meio com Miocardiopatia Dilatada Periparto, com início dos sintomas após 15 dias da última gestação, além de hipertensão e depressão pós-parto. Classificada funcionalmente pela New York Heart Association em III após ecocardiograma apresentar fração de ejeção de 23%, com aumento das cavidades esquerdas, disfunção sistólica grave de VE por hipocinesia difusa, insuficiência mitral moderada a grave por dilatação do anel, insuficiência aórtica e tricúspide leves com PSAP estimada em 45mmHg, além de derrame pericárdico leve sem sinais de restrição diastólica.
Iniciou uso regular de Furosemida, Digoxina, Carvedilol, Enalapril e Espironolactona.
Em sua história fisiológica, G4P4A0, todos os partos normais e sem intercorrências, negando outras patologias atuais ou prévias.
Em maio de 2018 deu entrada na UPA apresentando quadro infeccioso sugestivo de broncopneumonia, por apresentar episódios de febre, tosse produtiva com secreção esverdeada. Queixava-se de dor precordial intensa em queimação e em repouso, com duração de aproximadamente uma hora, irradiando para hemitórax direito e associada, por vezes, a náuseas. Relatava ortopneia, dispneia em repouso e tosse paroxística noturna. Ao exame, apresentava-se anasarcada, ausculta respiratória com murmúrio vesicular diminuído em ambas as bases e roncos em hemitórax direito. Optou-se por início de antibioticoterapia com Levofloxacina (VO) e otimização sintomática, com melhora dos sintomas.
Foi transferida para o Hospital Escola Álvaro Alvim, onde apresentou melhora clínica, sem episódios de febre, com aspecto mucóide da secreção orotraqueal, melhora da dispneia com o uso de diuréticos, eupneica em ar ambiente, regressão do edema facial e membros inferiores.
Durante sua evolução, apresentou sopro sistólico ++/6+ predominantemente em foco tricúspide; exame abdominal revelando fígado palpável 3cm abaixo do rebordo costal direito (hepatimetria=13 cm). Foi constatado proteinúria de 835,2 mg/24h e hipoalbuminemia, levando ao uso de albumina por dois dias.
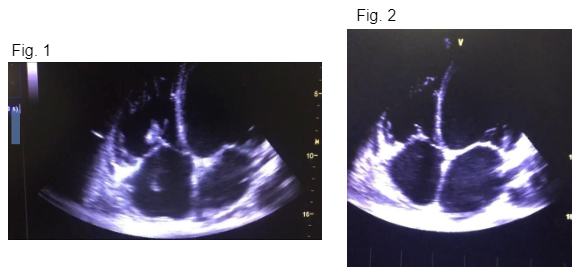
Realizado ecocardiograma com Doppler durante internação, constatando redução da fração de ejeção para 18% e alteração da relação entre o fluxo de enchimento rápido e o fluxo de contração atrial (fluxo mitral); veia cava inferior distendida e não variando com movimento respiratório e válvula mitral com aspecto de pinheiro tombado (fig. 1). Após uma semana de anticoagulação plena com heparina de baixo peso molecular, foi realizado outro ecocardiograma transtorácico, no qual não foi evidenciada a presença do trombo na válvula mitral (fig.2).
A paciente evoluiu com descompensação hemodinâmica, apresentando ortopneia, oligúria e anasarca, sendo transferida para UTI para melhor manejo clínico. Optado por inicar dobutamina, por indicação da cardiologia. Uma tomografia computadorizada de tórax revelou derrame pleural volumoso à direita, sendo realizada toracocentese com saída de 1513 mL até então.
Após otimização de drogas vasodilatadoras e balanço hídrico negativo foi indicada suspensão da dobutamina. Paciente evoluiu com piora importante da função renal, dobrando o valor da creatinina em 24h, tornando-se necessário o retorno do inotrópico positivo.
No dia 21 de julho às 00:15, a paciente apresentou PCR em assistolia, evoluindo para ritmo FV durante manobras de RCP, que duraram 27 minutos com retorno de circulação espontânea. Nos cuidados pós PCR, paciente apresentava-se sedada (RASS -5), intubada sob ventilação mecânica invasiva (VMI), apresentando arritmia ventilatória, pupilas mióticas bilateralmente, em uso de dobutamina e lidocaína.
Após suspensão de sedação, sem sucesso na evolução do desmame ventilatório, optado por traqueostomizada e mantendo acoplada à VMI em modo PSV, apresentando quadro neurológico prejudicado, com abertura ocular espontânea, mas sem interação, e reflexos preservados. Solicitado eletroencefalograma, evidenciando baixa atividade elétrica. Foi realizado desmame da dobutamina, mantendo estabilidade hemodinâmica, sem piora da função renal.
Paciente seguiu internada, mantendo quadro clínico descrito, a espera de home care para alta hospitalar.
Discussão:
A etiopatogênese da Miocardiopatia Periparto (MPP) continua indefinida. As causas mais consideradas são: miocardite viral, causa genética, imunológica, resposta inadequada ao estresse hemodinâmico da gestação, ativação de citoquinas inflamatórias, tocólise prolongada ou efeito deletério da prolactina 16 kDa, que provoca apoptose celular.
Outros fatores de risco associados ao desenvolvimento da doença são: idade materna avançada (> 35 anos), multiparidade (> 3 partos), gestação multifetal, pré-eclâmpsia/eclâmpsia ou hipertensão gestacional, cor negra.¹
No caso em questão não houve uso de tocolíticos, ou quaisquer intercorrências gestacionais.¹ O componente étnico relatado predispõe em 15 vezes o aumento do risco para deselvolvimento de MPP.³
Outros fatores que devem ser levados em consideração são deficiência de selênio, uso de cocaína, persistência das alterações fisiológicas da gestação (como hipertrofia ventricular transitória e remodelamento cardíaco) com diminuição excessiva da função ventricular esquerda. Estudos também sugerem como causa da MPP, a Miocardite.²
O papel da biópsia endomiocárdica permanece incerto, no entanto pode ser realizada na tentativa de esclarecer a causa da MPP.² Está indicada nas pacientes que não apresentam melhora com o tratamento convencional, nas primeiras semanas após o diagnóstico.¹ Evidencia infiltrado inflamatório, focos de necrose, hipertrofia e fibrose.²
Os achados eletrocardiográficos (ECG) incluem taquicardia sinusal, fibrilação atrial, anormalidades inespecíficas do segmento ST-T, baixa voltagem, hipertrofia ventricular esquerda. Ondas Q podem estar presentes. Os intervalos PR e QT podem estar prolongados.
A radiografia de tórax costuma evidenciar cardiomegalia, congestão pulmonar e/ou edema intersticial e derrame pleural², assim como no caso descrito. O ecocardiograma bidimensional revela aumento ventricular esquerdo com redução global da função ventricular sem hipertrofia, aumento do átrio esquerdo, regurgitação mitral e tricúspide e derrame pericárdico pequeno², corroborando com os resultados ecocardiográficos previamente citados da paciente em questão. Em casos que apresentam fatores de risco para doença arterial coronariana, deve-se realizar cineangiocoronariografia, a qual pode ser realizada no pré-parto, se necessário.²
As complicações mais frequentes da MPP são insuficiência cardíaca, tromboembolismo e arritmias. Os fenômenos tromboembólicos são frequentes pela hipercoagulabilidade da gestação associada à estase sanguínea dentro das câmaras cardíacas, favorecendo o surgimento de trombose intraventricular, sistêmica e pulmonar.²
A terapêutica não-farmacológica passa pela restrição de sal na dieta (<1,5 g/dia), pela restrição de fluidos em doentes com sobrecarga de volume, pela monitorização diária do peso, e por medições regulares da pressão arterial. A espironolactona está atualmente aprovada ela Academia Americana de Pediatria (AAP) para tratamento da IC durante o pós-parto.
Os IECAs e antagonistas dos receptores da angiotensina, apesar de diminuírem de forma significativa a mortalidade por IC na população geral, estão contraindicados em doentes grávidas com CMP. Contudo, de acordo com a AAP, o enalapril e o captopril podem ser administrados de forma segura durante a lactação.
A digoxina é relativamente segura tanto durante a gravidez como na lactação, desde que os seus níveis sejam mantidos no intervalo terapêutico.
Os nitratos e a hidralazina também constituem opções de tratamento relativamente seguras durante a gravidez e podem ser usados em combinação para reduzir a pós-carga.
Tem sido demonstrado que o metoprolol, o carvedilol e o bisoprolol reduzem o risco de arritmias ventriculares, morte súbita e a mortalidade total.⁴
A paciente se encontrava no período de pós-parto, fazendo uso de Digoxina, Furosemida, Carvedilol, Enalapril e Espironolactona, após o diagnóstico de ICC, durante acompanhamento ambulatorial.
Após seguimento na Unidade de Terapia Intensiva, foi necessário associação de outros fármacos para sua compensação hemodinâmica, como uso de inotrópicos (Dobutamina), vasodilatadores (Nitrato e Hidralazina) e drogas vasoativas como Noradrenalina.
Podemos citar como outras opções de tratamento, o balão intra-aórtico. É uma medida intermediária para o transplante cardíaco no insucesso do tratamento convencional. O transplante cardíaco é o tratamento aceitável quando a terapia padrão falha; resulta em sobrevida similar àquela de pacientes transplantadas devido a cardiomiopatia dilatada.²
Apesar de indicação para transplante cardíaco, o tratamento específico não foi instituído por condições clínicas e evolução desfavoráveis do quadro, com acometimento neurológico após PCR.
Paciente seguiu internada em enfermaria com suporte clínico, aguardando liberação de Home-care para possível alta hospitalar.
Conclusão:
A partir do caso relatado, foi possível concluir que a miocardiopatia periparto é uma condição rara, e sua etiologia ainda é de difícil elucidação. Desenvolve-se, geralmente, do último trimestre de gestação até o período periparto precoce, principalmente na vigência dos fatores de risco anteriormente relatados no caso. Dentre estes, aqueles classificados funcionalmente em III e IV pela NYHA apresentam evolução desfavorável, assim como no caso relatado. O tratamento indicado por sua vez provavelmente não mudaria seu desfecho, devido à relação direta existente entre o pior prognóstico e essa forma de envolvimento cardíaco.
Referências bibliográficas
1: OLIVEIRA F. et al.; Cardiomiopartia periparto, Rev Med Minas Gerais 2012; 22 (Supl 5): S25-S27.
2: ROMBALDI A. et al.; Cardiomiopatia periparto, Revista da Sociedade de Cardiologia do Rio Grande do Sul – Ano XIV nº 05 Mai/Jun/Jul/Ago 2005 Ano XIV nº 05 Mai/Jun/Jul/Ago 2005.
3: CARVALHO M., Cardiomiopatia periparto, Artigo de Revisão Bibliográfica -Mestrado Integrado em Medicina, Instituto de Ciências Biomédicas de Abel Salazar, Porto 2016.
4: CHAVES NETTO, Hermógenes; SÁ, R. A. M. Obstetrícia básica. 2.ed. São Paulo: Atheneu, 2007.
1Médico Clínica Geral
2Acadêmico de Medicina
