REGISTRO DOI: 10.5281/zenodo.10205263
Bruno Kauã Do Nascimento1
Orientador: Prof. Ms. Leandro Giorgetti2
RESUMO
A semaglutida, um composto farmacológico amplamente utilizado em contextos médicos e terapêuticos, tem sido objeto de crescente interesse devido à sua capacidade de modular processos bioquímicos e fisiológicos em organismos vivos. Este estudo busca investigar os mecanismos de ação da semaglutida e suas contraindicações associadas. A relevância desse tema reside na importância da compreensão abrangente dos efeitos da semaglutida para otimizar seu uso terapêutico e minimizar riscos à saúde. A metodologia incluiu uma revisão abrangente da literatura existente relacionada à semaglutida, bem como a análise de estudos clínicos e experimentais. Os resultados destacam a complexidade dos mecanismos de ação da semaglutida, revelando uma ampla gama de interações com sistemas biológicos. Além disso, identificaram-se várias contraindicações associadas ao seu uso, incluindo reações adversas e interações medicamentosas. A discussão enfatiza a necessidade de uma abordagem cuidadosa ao utilizar a semaglutida na prática clínica e enfoca a importância de uma supervisão médica adequada. Conclui-se que a pesquisa contínua é necessária para aprofundar nossa compreensão dos mecanismos de ação da semaglutida e identificar medidas de segurança aprimoradas para seu uso. Essas descobertas têm implicações significativas para a prática médica e apontam para futuras direções de pesquisa nesse campo em evolução.
Palavras-Chaves: Semaglutida. Mecanismos de Ação. Contraindicações.
ABSTRACT
Semaglutida, a widely used pharmacological compound in medical and therapeutic contexts, has garnered increasing interest due to its ability to modulate biochemical and physiological processes in living organisms. This study aims to investigate the mechanisms of action of semaglutida and its associated contraindications. The relevance of this topic lies in the importance of comprehensive understanding of the effects of semaglutida to optimize its therapeutic use and minimize health risks. The methodology included a comprehensive review of the existing literature related to semaglutida, as well as the analysis of clinical and experimental studies. The results highlight the complexity of semaglutida mechanisms of action, revealing a wide range of interactions with biological systems. Furthermore, contraindications associated with its use were identified, including adverse reactions and drug interactions. The discussion emphasizes the need for a cautious approach when using semaglutida in clinical practice and underscores the importance of proper medical supervision. It concluded that ongoing research required to deepen our understanding of the mechanisms of action of semaglutida and to identify enhanced safety measures for its use. These findings have significant implications for medical practice and point towards future research directions in this evolving field.
Keywords: Semaglutida. Mechanisms of Action. Contraindications.
1. Introdução
A diabetes mellitus tipo 2 (DM2) é uma condição crônica que afeta um número significativo de pessoas em todo o mundo, caracterizada por níveis elevados de glicose no sangue devido à resistência à insulina e à diminuição da capacidade do pâncreas de produzir insulina suficiente. A gestão adequada dessa condição é de extrema importância, uma vez que a falta de controle sobre os níveis de glicose sanguínea pode resultar em complicações graves, incluindo doenças cardiovasculares, danos renais, problemas oculares, neuropatia, problemas nos pés e até amputações (BAGGIO; DRUCKER, 2007).
Nesse contexto desafiador, a semaglutida emerge como uma abordagem inovadora no tratamento da DM2. A semaglutida pertence à classe de agonistas do receptor do peptídeo semelhante ao glucagon-1 (GLP-1), uma molécula que replica a ação do GLP-1, um hormônio natural do corpo envolvido na regulação dos níveis de açúcar no sangue. Este medicamento é administrado por meio de injeção subcutânea e está disponível em várias formulações, incluindo a semaglutida de ação prolongada, geralmente administrada uma vez por semana.
Este estudo visa explorar os mecanismos de ação da semaglutida e suas contraindicações associadas no contexto do tratamento da DM2 (PAULA, 2021).
A compreensão aprofundada desses aspectos é fundamental para otimizar a eficácia do tratamento, bem como para garantir a segurança dos pacientes. Através desta investigação, esperamos lançar luz sobre as implicações clínicas da semaglutida e destacar sua relevância na gestão da DM2, fornecendo assim uma contribuição valiosa para a área da saúde e da medicina.
Ademais, o objetivo geral desta monografia é analisar os mecanismos de ação da semaglutida e suas contraindicações associadas, a fim de fornecer uma compreensão abrangente do seu papel no tratamento da DM2 e seus impactos na saúde dos pacientes. Os objetivos Específicos pautam-se em, Investigar e descrever os mecanismos de ação da semaglutida, com foco na forma como essa molécula pertencente à classe de agonistas do receptor do peptídeo semelhante ao glucagon-1 (GLP-1) influencia os processos fisiológicos relacionados ao controle da glicose no sangue em pacientes com DM2; Identificar e analisar as contraindicações associadas ao uso da semaglutida, destacando os riscos potenciais, as interações medicamentosas e as reações adversas que podem ocorrer em pacientes com DM2 submetidos a esse tratamento; Avaliar as implicações clínicas da semaglutida no tratamento da DM2, considerando a eficácia no controle glicêmico, a melhoria da qualidade de vida dos pacientes e a minimização dos riscos de complicações associadas à doença (PAULA, 2021).
Assim, esses objetivos visam aprofundar o conhecimento sobre a semaglutida, permitindo uma análise abrangente de seus mecanismos de ação e das contraindicações relacionadas, bem como avaliar seu impacto clínico na gestão da DM2 (BASALAY; DAVIDSON; YELLON, 2019).
Sobre a justificativa do tema, nota-se que além do controle glicêmico, estudos clínicos também demonstraram que a semaglutida pode reduzir o risco de eventos cardiovasculares em pacientes com diabetes tipo 2 e risco cardiovascular elevado. É importante observar que a semaglutida não é adequada para todos os pacientes com DM2 e deve ser prescrita por um médico com base nas necessidades e histórico médico individuais. Além disso, como qualquer medicamento, a semaglutida pode ter efeitos colaterais, que devem ser discutidos com um profissional de saúde (BLUNDELL, 2017).
1.1 Metodologia
A metodologia adotada para este estudo se baseará em uma abordagem exploratória bibliográfica, com o propósito de analisar e sintetizar informações disponíveis na literatura científica relacionadas aos mecanismos de ação da semaglutida e suas contraindicações associadas no tratamento da DM2. Esse enfoque de pesquisa se revela fundamental para alcançar os objetivos propostos, pois permite uma análise detalhada do tema por meio de fontes já existentes e consolidadas na literatura científica.
A primeira etapa desse processo envolverá um levantamento minucioso da literatura disponível em diversas bases de dados acadêmicas, como PubMed, Scopus e Google Scholar, bem como em bibliotecas digitais de instituições de pesquisa de renome. Para direcionar efetivamente a pesquisa, foram definidas palavras-chave e termos de busca específicos, como “semaglutide,” “GLP-1 receptor agonists,” “mechanism of action,” “contraindications,” “type 2 diabetes,” entre outros, de modo a assegurar a abrangência necessária na coleta de informações.
Em seguida, os resultados obtidos serão submetidos a uma criteriosa seleção e triagem. Nesse processo, os estudos serão avaliados quanto à sua qualidade, relevância e aderência aos critérios de inclusão estabelecidos para esta pesquisa. Dentre as fontes de interesse, serão priorizados aqueles publicados em periódicos científicos, revisões sistemáticas e ensaios clínicos, sempre que disponíveis, a fim de garantir a confiabilidade das informações reunidas.
A terceira fase consistirá na análise crítica das fontes selecionadas, envolvendo a extração de informações pertinentes sobre os mecanismos de ação da semaglutida, bem como sobre as contraindicações associadas ao seu uso na DM2. Essas informações serão organizadas em categorias temáticas, possibilitando uma síntese coerente dos principais achados. Nesse processo, serão identificadas tendências, lacunas na pesquisa e questões em aberto que contribuirão para uma compreensão aprofundada do tema.
Com base nas informações obtidas nas etapas anteriores, será desenvolvida a monografia, seguindo uma estrutura padrão, que incluirá introdução, justificativa, referencial teórico, conclusão e palavras-chave em inglês. A redação do trabalho será realizada de forma cuidadosa e crítica, visando a assegurar a precisão e a coesão do conteúdo.
Por fim, o estudo será submetido a revisões minuciosas para garantir a qualidade e a formatação adequada de acordo com as normas acadêmicas, como a ABNT. Além disso, uma lista de referências bibliográficas completa será elaborada, seguindo as normas de citação apropriadas. Essa abordagem metodológica, centrada na pesquisa exploratória bibliográfica, oferece uma base sólida para a investigação aprofundada dos mecanismos de ação da semaglutida e suas contraindicações na DM2, contribuindo para o avanço do conhecimento em um tema de grande relevância na área da saúde (CONTE, 2014).
2. REVISÃO DE LITERATURA
2.1 Diabetes Mellitus tipo 2
O Diabetes Mellitus (DM) é uma doença endócrina caracterizada pela elevada glicemia em jejum e pós-prandial, resultante da menor sensibilidade à insulina e/ou reduzida secreção de insulina. Existem quatro classificações de DM, com a característica comum de manter os níveis de glicose acima do normal. O tratamento precoce é crucial para evitar complicações como doenças cardiovasculares, retinopatias, neuropatias e outras condições (BLUNDELL, 2017).
O DM tipo 2 está relacionado a fatores como sedentarismo e obesidade, e os genes desempenham um papel importante na suscetibilidade a essa doença. O gene da ECA (Enzima Conversora de Angiotensina) é considerado um candidato que influencia as respostas metabólicas (BASALAY; DAVIDSON; YELLON, 2019). Os polimorfismos desse gene (deleção ou inserção) afetam a atividade da ECA, o sistema renina-angiotensina e a pressão arterial. Diabéticos tipo 2 com o alelo D (deleção) apresentam maior pressão arterial e resistência à insulina. Além disso, a relação entre o polimorfismo do gene da ECA, diabetes tipo 2 e exercício físico ainda não está completamente esclarecida. No entanto, diversos estudos mostram que o exercício físico é benéfico para diabéticos tipo 2, reduzindo a glicemia e melhorando a função vascular.
Esta revisão de literatura aborda a fisiopatologia do DM tipo 2, as associações genéticas com o polimorfismo da ECA, o papel do exercício físico como tratamento não medicamentoso e as possíveis conexões entre as respostas ao exercício e os polimorfismos do gene da ECA (PAULA, 2021).
Além disso, o DM2 é uma condição crônica de saúde caracterizada por níveis elevados de glicose (açúcar) no sangue, devido à resistência à insulina e à diminuição da capacidade do pâncreas de produzir insulina em quantidades suficientes para manter a glicose sanguínea dentro dos limites saudáveis. É uma das formas mais comuns de diabetes, representando a grande maioria dos casos, e tende a se desenvolver em adultos, embora também possa afetar jovens (BLUNDELL, 2017).
A resistência à insulina é uma característica central do DM2, o que significa que as células do corpo têm dificuldade em responder adequadamente à insulina, o hormônio responsável por facilitar a entrada de glicose nas células para uso como energia. Consequentemente, o açúcar se acumula na corrente sanguínea, levando a níveis elevados de glicose no sangue, uma condição conhecida como hiperglicemia.
Existem vários fatores de risco associados ao DM2, incluindo predisposição genética, obesidade, estilo de vida sedentário, dieta inadequada, envelhecimento e histórico familiar da doença. A obesidade, em particular, desempenha um papel significativo na resistência à insulina e no desenvolvimento do DM2 (AMARAL, 2020).
Os sintomas podem incluir sede excessiva, micção frequente, fome constante, fadiga, visão turva, feridas que cicatrizam lentamente e infecções recorrentes. Muitas vezes, o DM2 pode ser assintomático por um longo período, o que ressalta a importância do diagnóstico precoce por meio de exames de glicose no sangue. O tratamento é abrangente e visa controlar os níveis de glicose no sangue, prevenir complicações e melhorar a qualidade de vida. As estratégias incluem mudanças no estilo de vida, como a adoção de uma dieta equilibrada, aumento da atividade física e perda de peso, quando necessário. Além disso, muitas vezes, medicamentos antidiabéticos orais ou insulina podem ser prescritos para ajudar a regular os níveis de glicose (AMARAL, 2020).
A prevenção do DM2 é uma prioridade, pois a doença está frequentemente relacionada a fatores de risco modificáveis, como obesidade e inatividade física. Programas de prevenção incluem educação sobre nutrição, promoção de exercícios físicos e aconselhamento sobre a importância da manutenção de um peso corporal saudável (CONTE,2014).
É essencial que as pessoas com essa doença mantenha um acompanhamento médico regular para controlar seus níveis de glicose no sangue, pressão arterial e outros fatores de risco, a fim de prevenir complicações a longo prazo, como doenças cardiovasculares, danos renais, problemas oculares, neuropatia e outros problemas de saúde associados ao diabetes. A gestão eficaz do DM2 requer um cuidadoso equilíbrio entre estilo de vida saudável, medicação e acompanhamento médico contínuo (CONTE,2014).
Partindo dessa premissa, a contexto nacional a incidência do DM2 no Brasil tem aumentado significativamente nas últimas décadas, refletindo uma tendência global de aumento na prevalência dessa condição. Esse aumento está associado a uma série de fatores, incluindo mudanças nos hábitos de vida, urbanização, envelhecimento da população e uma dieta menos saudável. O Quadro 1 e Quadro 2 apresentam uma análise de aspectos de incidência no país (AMARAL, 2020).
Quadro 1: Brasil, DM2.
Aspectos da Incidência do DM2 no Brasil Dados Prevalência Crescente Mais de 8% da população adulta é afetada. Diferenças Regionais Variação regional, maior em áreas urbanas. Fatores de Risco Obesidade, sedentarismo, má alimentação, histórico familiar e envelhecimento. Desafios de Diagnóstico Muitos casos permanecem subdiagnosticados. Impacto na Saúde Pública Aumento dos casos representa desafio para o sistema de saúde.
Fonte: IBGE,2020.
Quadro 2: Risco de acordo com Brunner.
Fatores de Risco para o Diabetes Mellitus tipo 2 (DM2) de Acordo com Brunner História familiar de diabetes (pais/irmãos) Obesidade (peso 20% acima do valor desejável ou IMC ≥ 27kg/m²) Raça/etnia (afrodescendentes, hispânicos, indígenas, orientais e nativos das Ilhas do Pacífico) Alterações dos valores da glicose em jejum ou comprometimento prévio da tolerância à glicose Hipertensão arterial (≥140/90mmHg) Dislipidemias Histórico de diabetes gestacional ou parto de RN >4,5kg
Fonte: Dias, 2019.
2.1.1 Tratamento Farmacológico
O tratamento do DM2 é uma abordagem multidisciplinar que envolve tanto medidas não farmacológicas quanto terapia medicamentosa. Abaixo, estão as diretrizes de tratamento farmacológico, divididas em primeira, segunda e terceira linhas, com base nas informações fornecidas.
a) Tratamento farmacológico: 1ª linha
Se uma pessoa com DM2 não alcançar a meta glicêmica em até três meses com as medidas não farmacológicas, a terapia preferencial é a adição de metformina ao plano terapêutico. A metformina é a primeira opção de tratamento devido ao seu perfil de segurança em longo prazo, efeito neutro ou redutor de peso, baixa incidência de hipoglicemias e sua capacidade de reduzir eventos macro vasculares, como infarto agudo do miocárdio e mortalidade (PAULA, 2021).
b) Tratamento farmacológico: 2ª linha
A maioria das pessoas com DM2 acabará necessitando da associação de um segundo fármaco devido à natureza progressiva da doença. Cerca da metade das pessoas que inicialmente respondem bem ao tratamento com metformina precisam de uma segunda medicação após cerca de dois anos. Quando as metas de controle não são alcançadas após três a seis meses de uso da metformina, pode-se associar uma sulfonilureia. As sulfonilureias podem também ser uma primeira escolha quando há perda de peso e níveis glicêmicos mais elevados, indicando secreção insuficiente de insulina.
c) Tratamento farmacológico: 3ª linha
Se o controle metabólico não for alcançado após o uso de metformina em associação com uma sulfonilureia por três a seis meses, uma terceira medicação deve ser considerada. Nesta fase, a insulina também é considerada, especialmente se os níveis de glicose no sangue estiverem acima de 300 mg/dL, principalmente se acompanhados de perda de peso, cetonúria e cetonemia. As classes de medicamentos que podem ser utilizadas nesta etapa incluem insulinas de ação intermediária ou longa. Recomenda-se o uso de insulina intermediária devido à longa experiência com seu uso e ao menor custo (AMARAL, 2020).
Essas estratégias de tratamento farmacológico no DM2 são baseadas em diretrizes clínicas e visam controlar efetivamente os níveis de glicose no sangue, prevenir complicações e melhorar a qualidade de vida das pessoas afetadas pela doença. A escolha do tratamento deve ser individualizada, levando em consideração as necessidades e características de cada paciente (BLUNDELL, 2017).
2.2 Descoberta da semaglutida
A semaglutida é um medicamento pertencente à classe dos agonistas do receptor do peptídeo semelhante ao glucagon-1 (GLP-1), utilizado no tratamento da DM2 e da obesidade. A descoberta e desenvolvimento da semaglutida representaram avanços significativos no campo da medicina e da terapia para essas condições de saúde (CONTE,2014).
É uma versão modificada do GLP-1, um hormônio natural do corpo que desempenha um papel fundamental na regulação dos níveis de glicose no sangue. O GLP-1 é secretado pelo intestino delgado após a ingestão de alimentos e estimula a liberação de insulina pelo pâncreas, reduzindo, assim, os níveis de glicose no sangue.
A descoberta da semaglutida e de outros análogos de GLP-1 é o resultado de décadas de pesquisa em endocrinologia e farmacologia. Essa pesquisa buscou entender melhor os mecanismos envolvidos na regulação da glicose e como eles poderiam ser aproveitados para o tratamento do DM2 e da obesidade (BASALAY; DAVIDSON; YELLON, 2019).
A grande vantagem da semaglutida e de medicamentos similares é que eles podem imitar a ação do GLP-1 no organismo, mesmo quando o hormônio natural está ausente ou não é eficaz o suficiente. A semaglutida é administrada por meio de injeção subcutânea e está disponível em várias formulações, incluindo versões de ação prolongada que podem ser administradas uma vez por semana, o que melhora a aderência ao tratamento (BAGGIO; DRUCKER, 2007).
Além de seu impacto na regulação da glicose, a semaglutida também tem demonstrado benefícios na perda de peso, tornando-a uma opção atraente para pacientes com DM2 que também enfrentam problemas de obesidade.
A revelação e o desenvolvimento da semaglutida exemplificam como a pesquisa contínua em medicina e ciências farmacêuticas pode levar ao desenvolvimento de terapias inovadoras e eficazes para condições médicas crônicas, como o DM2 e a obesidade. Esses avanços representam esperança para milhões de pessoas em todo o mundo que lutam com essas condições, oferecendo-lhes novas opções de tratamento e melhor qualidade de vida (PAULA, 2021).
Além disso, a investigação de terapias fundamentadas em GLP-1 para o tratamento da diabetes tipo 2, com um foco na otimização da conveniência do paciente, permitindo uma administração semanal, em contraposição às injeções diárias. Várias estratégias foram exploradas com o objetivo de desenvolver um GLP-1RA (Agonista do Receptor de GLP-1) que pudesse ser administrado uma vez por semana (OW) (AMARAL, 2020).
Inicialmente, a liberação sustentada foi uma das abordagens pioneiras submetidas a ensaios clínicos, resultando na aprovação da formulação de exenatida de liberação prolongada (ER). O taspoglutido, um GLP-1RA de origem humana, foi posteriormente avaliado em ensaios clínicos para administração semanal. O uso do aminoácido Aib8 foi empregado para proteger o taspoglutido da degradação mediada pelo DPP-IV (Inibidor de Peptidase Dipeptidil IV). Embora formulações de taspoglutido contendo cloreto de zinco, que facilitam a precipitação subcutânea, tenham demonstrado resultados promissores, a submissão para aprovação foi descontinuada devido a diversos casos de choque anafilático.
Outras estratégias exploradas incluíram a redução da depuração renal de compostos baseados em GLP-1 ou exendina, por meio da fusão covalente do peptídeo a proteínas plasmáticas de grande estabilidade, como a albumina (albiglutida) ou o domínio Fc de IgG (dulaglutida). Na Novo Nordisk, foi desenvolvida a abordagem de ligação reversível à albumina como estratégia para prolongar a ação dos análogos do GLP-1.
O principal desafio identificado anteriormente foi que a forte ligação à albumina afetava negativamente a potência dos compostos no receptor GLP-1R, devido à competição entre a ligação à albumina e a ligação ao receptor. A teoria sustentava que apenas a fração não ligada à albumina estaria disponível para ativar o GLP-1R. Assim, quanto maior a afinidade pela albumina, menor seria a fração circulante livre e ativa do peptídeo GLP-1. Isso foi observado com análogos da liraglutida, onde ácidos graxos mais longos, com alta afinidade pela albumina, resultaram em menor potência no GLP-1R.
Resultados semelhantes foram obtidos com o albiglutido, onde a ligação covalente do GLP-1RA à albumina exigia doses elevadas para obter eficácia clínica significativa. O albiglutido apresenta uma repetição em tandem de Gly8 GLP-1(7-36), projetada para melhorar a afinidade pelo GLP-1R ao aumentar a distância entre a albumina e o peptídeo GLP-1 distal. Além disso, a substituição do aminoácido (Ala8 para Gly8) protege o albiglutido da degradação do DPP-IV no N-terminal e a repetição em tandem é fundida ao terminal N da HSA para prolongar sua meia-vida, tornando-a adequada para administração semanal. No entanto, a potência do albiglutido foi significativamente reduzida em comparação com o exenatido devido a uma combinação da modificação Gly8 e da ligação covalente à HSA.
Ao desenvolver a semaglutida, o desafio era estabilizar um análogo do GLP-1 contra a eliminação do sistema para alcançar níveis plasmáticos adequados para o controle da glicemia após uma única dose semanal. Inicialmente, as descobertas com liraglutida em ensaios de GLP-1R in vitro e em modelos animais mostraram a dificuldade em encontrar um equilíbrio entre uma meia-vida plasmática longa e uma alta afinidade pelo GLP-1R na presença de albumina. Isso foi refletido na dose clínica relativamente alta de liraglutida em comparação com exenatida (PAULA, 2021).
Para resolver esse desafio, a estratégia adotada foi manter a estrutura peptídica semelhante a liraglutida e ao GLP-1 endógeno, com uma modificação apenas na posição 8, substituindo Ala por Aib, conhecido por resistir à clivagem pelo DPP-IV e ter alta afinidade pelo GLP-1R. A segunda parte da estratégia envolveu encontrar a combinação ideal de um ácido graxo com alta afinidade pela albumina, ligado ao GLP-1 por meio de um ligante químico compatível com água, garantindo alta potência do GLP-1R na presença de albumina. A Figura 1 resume esse processo.
Figura 1 – GLP-1R, mapa mental.
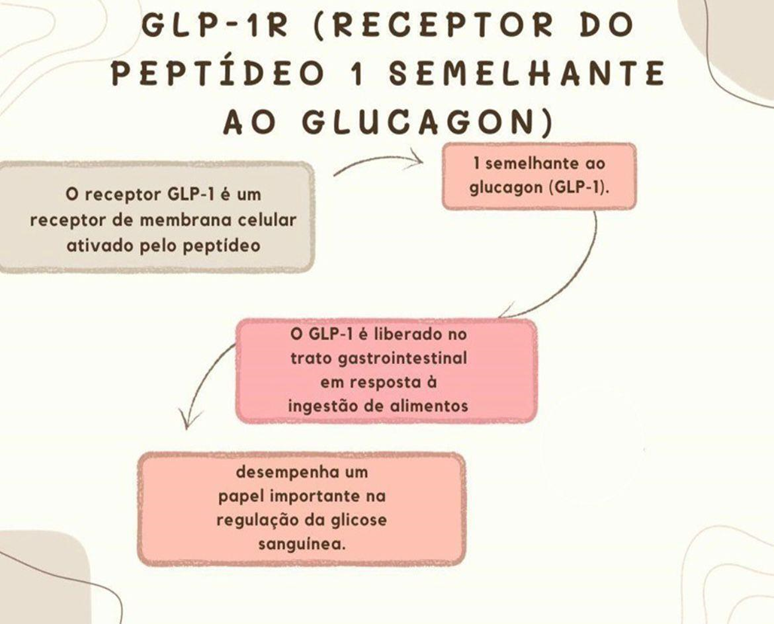
Fonte: Elaborado pelo Autor (2023).
Vários ácidos graxos e ligantes foram avaliados sistematicamente, e a introdução de ligantes “OEG” demonstrou resultar em alta potência do receptor e afinidade pela albumina. Para aumentar ainda mais a afinidade pela albumina, foram explorados diferentes comprimentos e tipos de ácidos graxos. Constatou-se que os diácidos graxos com um ácido graxo proximal para a ligação à amida e um ácido graxo distal foram eficazes em proporcionar alta ligação à albumina e potência no GLP-1R (PAULA, 2021).
2.3 Mecanismos de Ação da Semaglutida
Como já exposto, a semaglutida é um medicamento utilizado no tratamento da DM2 e da obesidade. Sua ação é baseada em sua capacidade de mimetizar o hormônio natural do corpo conhecido como GLP-1 (glucagon-like peptide 1), que desempenha um papel crucial na regulação dos níveis de glicose no sangue (DINEL, 2011). A semaglutida atua em vários mecanismos que ajudam a controlar a glicose sanguínea.
Ela atua sobre as células beta do pâncreas, estimulando a secreção de insulina. A insulina é um hormônio responsável por facilitar a entrada de glicose nas células do corpo, permitindo que ela seja utilizada como fonte de energia. Portanto, o aumento da secreção de insulina ajuda a reduzir os níveis elevados de glicose no sangue em pacientes com DM2 (DINEL, 2011).
A semaglutida também inibe a produção de outro hormônio, o glucagon, pelo pâncreas. O glucagon tem o efeito oposto da insulina, aumentando os níveis de glicose no sangue. A inibição do glucagon pela semaglutida contribui para a redução da glicose sanguínea em pacientes com DM2.
Ela retarda o esvaziamento gástrico, o que significa que os alimentos são digeridos e absorvidos mais lentamente no trato gastrointestinal. Isso ajuda a evitar picos de glicose no sangue após as refeições, uma vez que a glicose é liberada gradualmente na corrente sanguínea (ELIAS, 2003).
Na Ação no Sistema Nervoso Central tem efeitos no sistema nervoso central que reduzem o apetite e aumentam a sensação de saciedade. Isso pode levar à redução da ingestão de alimentos e à perda de peso, o que é benéfico para pacientes com DM2 que também enfrentam problemas de obesidade. Além de suas ações imediatas, a semaglutida tem demonstrado ter efeitos protetores nas células beta do pâncreas, as quais produzem insulina. Isso pode ajudar a preservar a função das células beta ao longo do tempo, retardando a progressão do DM2.
É importante notar que a semaglutida é frequentemente administrada por injeção subcutânea e está disponível em diferentes formulações, incluindo aquelas de ação prolongada que podem ser aplicadas uma vez por semana (DINEL, 2011). Sua ação é uma ferramenta valiosa no tratamento do DM2, ajudando a controlar os níveis de glicose no sangue e a melhorar a qualidade de vida dos pacientes afetados por essa condição. Os medicamentos atuam em vários órgãos do corpo, como aponta a Figura 2.
Figura 2 – Classificação de medicamentos.
Fonte: Elaborado pelo Autor (2023).
Além disso, a semaglutida também tem demonstrado benefícios na redução de eventos microvasculares, como infarto agudo do miocárdio e mortalidade, tornando-a uma opção terapêutica ainda mais atraente (ELIAS, 2003).
2.4 LGP1
O GLP-1, ou Peptídeo Semelhante ao Glucagon-1, é um hormônio natural produzido no trato gastrointestinal, principalmente nas células L localizadas no íleo e no cólon. Esse hormônio desempenha um papel fundamental na regulação dos níveis de glicose no sangue e no controle do apetite. O GLP-1 possui diversos mecanismos de ação que são vitais para o funcionamento do organismo, especialmente no que diz respeito à homeostase da glicose e à saciedade (DINEL, 2011).
O GLP-1 é principalmente produzido nas células L, que são células enteroendócrinas distribuídas ao longo do intestino, abrangendo o cólon, o íleo e as partes próximas do intestino delgado, em resposta à ingestão de alimentos. Este hormônio é derivado do gene do glucagon e suas formas bioativas consistem em uma cadeia de aminoácidos de 29 ou 30 unidades. Em condições de jejum ou quando não se está se alimentando, os níveis desse hormônio são baixos. Contudo, após a ingestão de alimentos, o GLP-1 entra em ação, estimulando as células beta do pâncreas para aumentar a secreção de insulina. Isso, por sua vez, promove a captação da glicose pelas células do corpo e inibe a secreção de glucagon (DUTHEIL, 2016).
Além das células β do pâncreas, o GLP-1R também é expresso no cérebro – hipófise, hipotálamo, tronco cerebral e córtex, no coração, rim, trato gastrointestinal (TGI), fibras aferentes vagais no TGI, na veia hepatoportal (veia porta hepática), fígado e no nervo vago (CANDEIAS, 2015). Seu efeito no metabolismo se dá por dois mecanismos principais: i) quando da elevação da glicemia, é liberado pelas células intestinais e atua no pâncreas, estimulando a secreção de insulina; ii) sua elevação pós-prandial também promove redução de apetite e redução da ingestão de alimentos, por ativação de neurônios anorexígenos no centro da saciedade no hipotálamo (DUTHEIL, 2016, p.16). A Figura 3:mostra os mecanismos pelos quais os agonistas de GLP-1 podem exercer efeitos fisiológicos no organismo
Figura 3 – Mecanismos de atuação dos agonistas de GLP-1.
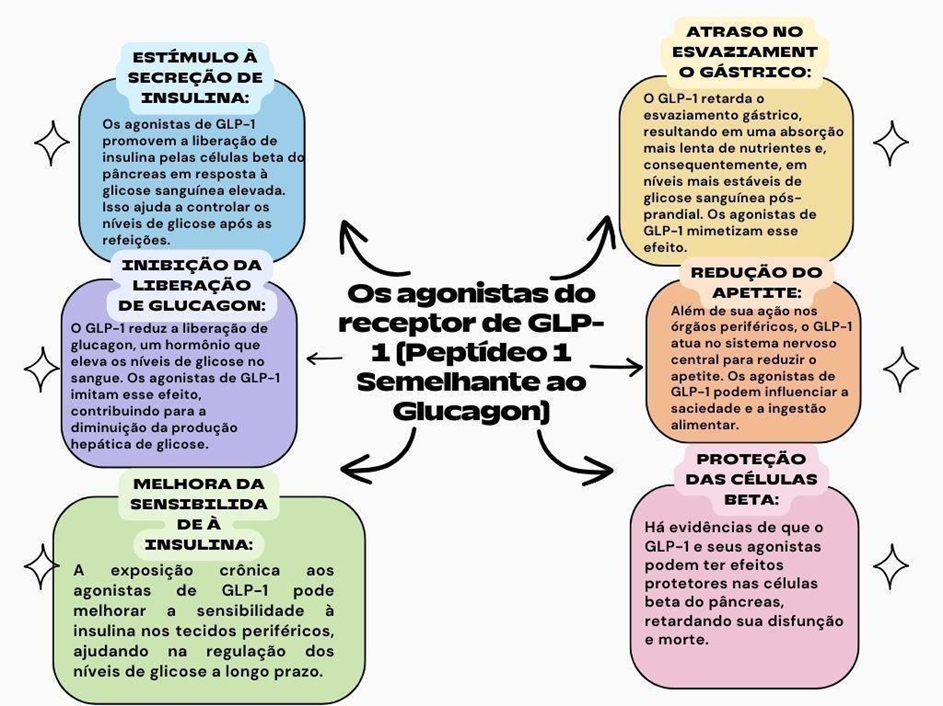
Fonte: Elaborado pelo Autor (2023).
2.5 Relação entre Obesidade e Prejuízo Cognitivo
A relação entre obesidade e prejuízo cognitivo é um tópico de crescente interesse na área da saúde, uma vez que a obesidade se tornou uma epidemia global. A obesidade é uma condição em que uma pessoa acumula um excesso de gordura corporal que pode ter um impacto significativo na saúde física e mental. Além dos riscos bem conhecidos para problemas de saúde, como diabetes tipo 2, doenças cardíacas e hipertensão (Quadro 3), a obesidade também tem sido associada a efeitos adversos sobre a função cognitiva (ELIAS, 2003).
Quadro 3. Fatores Relacionados à Obesidade e Prejuízo Cognitivo
Fator Descrição Inflamação Crônica A obesidade está associada a uma inflamação crônica de baixo grau no organismo devido à liberação de substâncias inflamatórias pelos depósitos de gordura. Essa inflamação pode afetar negativamente o cérebro, prejudicando a função cognitiva Resistência à Insulina A obesidade frequentemente está ligada à resistência à insulina, um problema no qual o corpo não responde eficazmente à insulina. A resistência à insulina tem sido associada a prejuízos na memória e no raciocínio Doenças Cardiovasculares A obesidade é um fator de risco para doenças cardiovasculares, como aterosclerose, que pode resultar em falta de oxigênio e nutrientes para o cérebro. Essa redução no suprimento sanguíneo cerebral pode levar a prejuízos cognitivos Estilo de Vida e Hábitos Alimentares Pessoas obesas frequentemente têm hábitos alimentares não saudáveis, que podem influenciar negativamente a função cerebral. Uma dieta rica em açúcares refinados e gorduras saturadas pode contribuir para prejuízos cognitivos. Depressão e Ansiedade A obesidade está associada a um maior risco de depressão e ansiedade. Essas condições psicológicas podem afetar a função cognitiva, especialmente a atenção e a memória. Impacto na Qualidade de Vida Prejuízos cognitivos devido à obesidade podem ter um impacto significativo na qualidade de vida. Isso pode dificultar a realização de tarefas diárias e o funcionamento social.
Fonte: Elaborado pelo Autor (2023).
A literatura científica tradicionalmente descreve os efeitos fisiológicos, metabólicos e, principalmente, cardiovasculares da obesidade. No entanto, estudos recentes têm demonstrado uma relação adicional com alterações no sistema nervoso central. O aumento do índice de massa corporal (IMC) está correlacionado com deficiências no aprendizado, na memória e nas funções cognitivas. A associação entre obesidade e comprometimento cognitivo, incluindo condições como a doença de Alzheimer, tem se tornado um tema de destaque na pesquisa. Evidências clínicas e estudos em modelos animais indicam que a obesidade e/ou dietas ricas em lipídios estão ligadas a déficits no aprendizado, na memória, nas funções motoras e, potencialmente, à atrofia cerebral (PAULA, 2021; ELIAS, 2003).
É importante destacar que a relação entre obesidade e prejuízo cognitivo é complexa e multifacetada. Ela não afeta todas as pessoas da mesma maneira, e outros fatores, como genética, idade e comorbidades, também desempenham um papel importante. No entanto, a conscientização sobre essa relação ressalta a importância de abordar a obesidade como uma preocupação de saúde abrangente, com o potencial de afetar não apenas o corpo, mas também a função cognitiva e a saúde mental. A promoção de um estilo de vida saudável, incluindo uma dieta equilibrada e a prática regular de exercícios, é fundamental para prevenir ou mitigar os riscos associados à obesidade (ELIAS, 2003).
2.6 Contraindicações da Semaglutida
A semaglutida, um medicamento inovador no tratamento da DM2 e da obesidade, tem se destacado devido aos seus mecanismos de ação singulares. Para entender completamente os benefícios e as contraindicações associadas a esse medicamento, é essencial considerar sua relação com o sistema GLP-1 e a maneira como afeta a glicose sanguínea e o peso corporal (DINEL, 2011).
O GLP-1, ou Peptídeo Semelhante ao Glucagon-1, é um hormônio natural produzido no trato gastrointestinal em resposta à ingestão de alimentos. Ele desempenha um papel crucial na regulação dos níveis de glicose no sangue, estimulando a secreção de insulina e inibindo o glucagon, outro hormônio que eleva a glicose sanguínea. Além disso, o GLP-1 retarda o esvaziamento gástrico e promove a saciedade, o que pode ajudar na redução da ingestão de alimentos.
A semaglutida é um agonista do receptor do GLP-1, o que significa que ela imita a ação desse hormônio natural. Quando administrada por injeção subcutânea, a semaglutida estimula a secreção de insulina, inibe o glucagon, retarda o esvaziamento gástrico e promove a saciedade, resultando na redução dos níveis de glicose no sangue e na perda de peso em pacientes com DM2 e obesidade (BAGGIO; DRUCKER, 2007).
Além disso, a semaglutida também demonstrou efeitos protetores nas células beta do pâncreas, retardando a progressão da DM2. No entanto, a semaglutida não é isenta de contraindicações. Ela é desaconselhada em casos de hipersensibilidade ao medicamento ou a qualquer um de seus componentes. Além disso, pessoas com histórico de pancreatite, distúrbios da tireóide, insuficiência renal grave e gestantes ou lactantes devem ter cautela e, em alguns casos, evitar o uso da semaglutida.
A compreensão dos mecanismos de ação da semaglutida e de suas contraindicações é fundamental para garantir um tratamento eficaz e seguro para pacientes com DM2 e obesidade. A avaliação individual de cada paciente, considerando seu histórico médico e suas condições de saúde atuais, é essencial para tomar decisões informadas sobre o uso desse medicamento inovador. Portanto, a parceria entre pacientes e profissionais de saúde desempenha um papel fundamental na gestão dessas condições de saúde complexas.
3. RESULTADOS E DISCUSSÕES
3.1 Resultados
Os mecanismos de ação da semaglutida envolvem a ativação dos receptores do GLP-1, que promove a regulação dos níveis de glicose no sangue, a redução do apetite e a perda de peso em pacientes com DM2 e obesidade. A semaglutida tem demonstrado eficácia na melhora do controle glicêmico, na redução de eventos cardiovasculares e na preservação das células beta do pâncreas, retardando a progressão da DM2.
A obesidade está associada a uma série de fatores que podem prejudicar a função cognitiva, incluindo inflamação crônica, resistência à insulina, doenças cardiovasculares, hábitos alimentares não saudáveis, depressão e ansiedade (ELIAS, 2003).
Os resultados destacam a importância dos mecanismos de ação da semaglutida no tratamento da DM2 e da obesidade. A ativação dos receptores do GLP-1 oferece uma abordagem inovadora para o controle da glicose sanguínea e a perda de peso, beneficiando os pacientes. A capacidade da semaglutida de preservar as células beta do pâncreas é particularmente relevante no tratamento da DM2, já que a deterioração dessas células é uma característica-chave da doença (BAGGIO; DRUCKER, 2007).
A discussão sobre os efeitos da obesidade na função cognitiva destaca a importância de reconhecer os riscos adicionais associados a essa condição. Os fatores como inflamação crônica e resistência à insulina podem contribuir para déficits cognitivos em pessoas obesas. A relação entre obesidade e comprometimento cognitivo, incluindo condições como a doença de Alzheimer, destaca a necessidade de estratégias de prevenção e tratamento para abordar tanto os aspectos físicos quanto cognitivos da obesidade (DINEL, 2011).
A discussão também enfatiza a importância da avaliação individual de pacientes que consideram o uso da semaglutida, levando em conta as contraindicações e os potenciais benefícios, a fim de tomar decisões informadas sobre o tratamento (BAGGIO; DRUCKER, 2007). Em resumo, os resultados e discussões destacam a relevância dos mecanismos de ação da semaglutida no contexto do tratamento da DM2 e da obesidade, ao mesmo tempo em que sublinham os riscos associados à obesidade para a função cognitiva. Abordar essas questões de maneira abrangente é essencial para a promoção da saúde e o bem-estar dos pacientes.
4. CONCLUSÕES
A pesquisa sobre os mecanismos de ação da semaglutida e suas contraindicações revela um campo complexo e em evolução no tratamento da DM2 e da obesidade. A semaglutida, como um agonista do receptor do GLP-1, demonstra potencial na melhora do controle glicêmico, na redução de eventos cardiovasculares e na preservação das células beta do pâncreas, oferecendo uma abordagem inovadora e promissora.
No entanto, é essencial destacar as contraindicações associadas à semaglutida, que incluem hipersensibilidade ao medicamento, histórico de pancreatite, distúrbios da tireoide, insuficiência renal grave e situações de gravidez ou amamentação. Essas contraindicações ressaltam a importância de uma avaliação cuidadosa por parte dos profissionais de saúde antes de prescrever o medicamento.
A pesquisa também destaca a relação entre obesidade e comprometimento cognitivo, enfatizando os riscos adicionais associados a essa condição, como inflamação crônica, resistência à insulina e doenças cardiovasculares. Isso demonstra a necessidade de abordagens de tratamento e prevenção abrangentes que considerem não apenas os aspectos físicos, mas também os cognitivos da obesidade.
Em suma, a pesquisa contínua é necessária para aprofundar nossa compreensão dos mecanismos de ação da semaglutida e identificar medidas de segurança aprimoradas para seu uso. Essas descobertas têm implicações significativas para a prática médica e apontam para futuras direções de pesquisa neste campo em constante evolução. A parceria entre pacientes e profissionais de saúde desempenha um papel fundamental na gestão das condições de DM2 e obesidade, garantindo um tratamento eficaz e seguro.
REFERÊNCIAS
AMARAL, A. B.; RESENDES, C.; SANTOS, A. M. Novos Antidiabéticos e Neuroproteção. Revista Portuguesa de Diabetes, v. 15, n. 1, p. 11-15, 2020. Disponível em http://www.revportdiabetes.com/wp-content/uploads/2020/05/RPD-Mar%C3%A7o-2020-Artigo-de-Revis%C3%A3o-p%C3%A1gs-11-15.pdf. Acesso em 23 nov. 2023.
BAGGIO, Laurie L.; DRUCKER, Daniel J. Biology of incretins: GLP-1 and GIP. Gastroenterology, v. 132, n. 6, p. 2131-2157, 2007. Disponível em http://www.glucagon.com/pdfs/BiologyofIncretinsGastro2007.pdf. Acesso em 23 nov. 2023.
BASALAY, Maryna V.; DAVIDSON, Sean M.; YELLON, Derek M. Neuroprotection in rats following ischaemia-reperfusion injury by GLP-1 analogues—liraglutide and semaglutide. Cardiovascular drugs and therapy, v. 33, p. 661-667, 2019. Disponível em https://link.springer.com/article/10.1007/s10557-019-06915-8. Acesso em 23 nov. 2023.
BLUNDELL, John et al. Effects of once‐weekly semaglutide on appetite, energy intake, control of eating, food preference and body weight in subjects with obesity. Diabetes, Obesity and Metabolism, v. 19, n. 9, p. 1242-1251, 2017. Disponível em https://dom-pubs.onlinelibrary.wiley.com/doi/pdf/10.1111/dom.12932. Acesso em 23 nov. 2023.
CANDEIAS, Emanuel Monteiro et al. Gut-brain connection: The neuroprotective effects of the anti-diabetic drug liraglutide. World journal of diabetes, v. 6, n. 6, p. 807, 2015. Disponível em https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4478577/. Acesso em 23 nov. 2023.
CONTE, Suélyn Carolina. Perspectivas de perda de peso com o uso de liraglutida: revisão da literatura. Brazilian Journal of Surgery & Clinical Research, v. 9, n. 1, 2014. Disponível em https://search.ebscohost.com/login.aspx?direct=true&profile=ehost&scope=site&authtype=crawler&jrnl=23174404&AN=101978558&h=0QNJLdizCIKuxR%2BhMTOopPp06eVvetFLpHuL4SyFUZVE8HpdIgJAri9plCynMe5lmdxtJun8%2B1RZHHmNfAc8Lg%3D%3D&crl=c. Acesso em 23 nov. 2023.
DINEL, Anne-Laure et al. Cognitive and emotional alterations are related to hippocampal inflammation in a mouse model of metabolic syndrome. PloS one, v. 6, n. 9, p. e24325, 2011. Disponível em https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0024325. Acesso em 23 nov. 2023.
DUTHEIL, Sophie et al. High-fat diet induced anxiety and anhedonia: impact on brain homeostasis and inflammation. Neuropsychopharmacology, v. 41, n. 7, p. 1874-1887, 2016. Disponível em https://www.nature.com/articles/npp2015357. Acesso em 23 nov. 2023.
ELIAS, M. F. et al. Lower cognitive function in the presence of obesity and hypertension: the Framingham heart study. International journal of obesity, v. 27, n. 2, p. 260-268, 2003. Disponível em https://www.nature.com/articles/802225. Acesso em 23 nov. 2023
PAULA, Gabriela Cristina et al. Hippocampal function is impaired by a short-term high-fat diet in mice: Increased blood–brain barrier permeability and neuroinflammation as triggering events. Frontiers in neuroscience, v. 15, p. 734158, 2021. Disponível em https://www.frontiersin.org/articles/10.3389/fnins.2021.734158/full. Acesso em 23 nov. 2023.
