REGISTRO DOI: 10.5281/zenodo.8090511
Isabella Alves Silva
José Dantas Torres Queiroz
Luís Eduardo Rodrigues Barbosa
Resumo: O linfoma não-Hodgkin de células B é uma neoplasia dos tecidos linfóides, cujo diagnóstico é feito através de critérios clínicos (sintomas B) e de exames complementares (biópsia e imunofenotipagem), sendo necessário a realização de tomografia por emissão de pósitrons (PET-CT), para determinação do estadiamento através dos sistemas Ann Arbor e Lugano. Além disso, o tratamento é feito com a administração da imunoterapia associada ao CHOP e à radioterapia de consolidação.
Palavras-Chave: Linfoma de Hodgkin, sintomas B, imunoterapia;
Summary: B-cell non-Hodgkin lymphoma is a neoplasm of lymphoid cells, whose diagnosis is made through clinical criteria (B symptoms) and complementary exams (biopsy and immunophenotyping), requiring the performance of positron emission tomography (PET- CT), for determination of staging using the Ann Arbor and Lugano systems. In addition, treatment is performed with the administration of immunotherapy associated with CHOP and consolidation radiotherapy.
Key words: lymphomaHodgkin, B symptoms, immunotherapy;
Resumen: El linfoma no Hodgkin de células B es una neoplasia de células linfoides, cuyo diagnóstico se realiza a través de criterios clínicos (síntomas B) y exámenes complementarios (biopsia e inmunofenotipado), requiriendo la realización de tomografía por emisión de positrones (PET-CT), para determinación de puesta en escena utilizando los sistemas de Ann Arbor y Lugano. Además, el tratamiento se realiza con la administración de inmunoterapia asociada a CHOP y radioterapia de consolidación.
Palabras clave: Linfoma de Hodgkin, síntomas B, inmunoterapia;
1.INTRODUÇÃO
Os linfomas são neoplasias malignas de células linfóides normais, que ocorrem predominantemente em tecidos linfóides, descritos pela primeira vez pelo médico inglês Thomas Hodgkin em 1832, sendo classificado de acordo com a morfologia em linfoma de
Hodgkin e linfoma não-Hodgkin (ARAÚJO et al.;2008). Segundo a Organização Mundial da Saúde (OMS), o LH é dividido em duas categorias principais, denominadas de linfoma nodular e de linfoma clássico, com predominância de células de Reed-Sternberg ou de células de Hodgkin (MACHADO et al.;2004), já o LNH é separado em linfoma de pequenas células – BURKITT e NÃO-BURKITT-, linfoma linfoblástico e linfoma de grandes células, podendo ocorrer em células B, células T e células natural-killer (ARAÚJO et al.;2008).
Dessa forma, o linfoma é um termo geral empregado para indicar um grupo constituído por várias doenças neoplásicas do sistema linfático, ocasionadas por meio da propagação clonal das células de defesa, com natureza desigual e diferenças estruturais. Além disso, constituem a patologia sanguínea mais frequente, sobretudo originadas de linfócitos B, correspondendo a aproximadamente 80% dos casos, associados a causas hereditárias, ambientais, infecciosas e imunológicas (ALENCAR; BELMONTE; ESPUCH, 2020).
Conforme análise de Barbosa et al. (2015), os linfomas são responsáveis por grande parte da mortalidade no Brasil e no mundo, em que as neoplasias são as principais causas de morte em países de primeiro mundo e a segunda maior origem de óbitos nos países em desenvolvimento. Em relação ao linfoma não-Hodgkin, trata-se de um dos cânceres hematológicos, que aumentou consideravelmente nas últimas décadas, tanto no Brasil, quanto no mundo. Sendo, o mais incidente entre os neoplasmas sanguíneos (COSTA; MELLO; FRIEDRICH, 2017).
Os linfomas não-Hodgkin de células B equivalem a 80% dos casos, enquanto que o restante envolve os linfócitos T, em que o primeiro grupo possui evolução mais rápida, agressiva e desordenada, representando grandes riscos à população (BARROS, 2021). No Brasil, foram diagnosticados 6.580 homens e 5.450 mulheres, totalizando 12.030 casos da doença que levaram 4.357 à morte em 2020, cujo percentual mais elevado condiz com os doentes do sexo masculino. Nos últimos 25 anos, houve a duplicação do número de casos de linfoma não-Hodgkin por motivos desconhecidos, principalmente, entre pessoas com mais de 60 anos (INCA, 2022). Portanto, o presente estudo tem como objetivo listar as medidas terapêuticas para as neoplasias de células B.
Em relação aos riscos quanto ao desenvolvimento dos linfomas não-Hodgkin, o Instituto Nacional do Câncer (2022) aponta que as pessoas com o sistema imune comprometido por diferentes fatores, tais como sequelas de doenças genéticas hereditárias, uso de drogas em decorrência de procedimentos de transplantes de órgãos e pessoas infectadas por HIV, são mais propensas a desenvolver essa doença. Ademais, os trabalhadores expostos a determinadas substâncias químicas, os operários do transporte em rodovias e ferrovias e os funcionários da indústria de borracha e de plástico são mais predispostos a desenvolverem a referida patologia.
O diagnóstico é feito a partir do exame clínico, em que é avaliado a presença de linfadenomegalia e de sintomas B (febre, hiperidrose noturna e perda de peso), além de exames complementares, como a biópsia e a imunofenotipagem, para identificar características histológicas e genéticas da linfadenopatia (ARAÚJO et al.;2008). Ademais, já foi comprovado a relação entre o desenvolvimento do linfoma não-Hodgkin com a presença de condições inflamatórias crônicas, tal qual síndrome de Sjogren, doença celíaca e artrite reumatoide, bem como a ação de alguns microrganismo, incluindo o vírus da herpes e da hepatite C e a bactéria Helicobacter pylori (AKANJI, 2006).
O estadiamento do linfoma não-Hodgkin é feito através do sistema Ann Arbor/Cotswolds, que classifica os pacientes em quatro categorias de acordo com a extensão e a disseminação da doença no organismo (ARAÚJO et al.;2008), segundo demonstrado na imagem 1. O estágio I acomete uma cadeia linfonodal ou uma estrutura linfóide (linfoma localizado), o estágio II acomete as cadeia linfonodais à direita do diafragma, o estágio III acomete as cadeias linfonodais dos dois lados do diafragma e o estágio IV acomete vários órgãos extra-linfáticos (linfoma disseminado). Ademais, também é avaliado a ausência (A) ou a presença (B) de sintomas sistêmicos, incluindo febre, sudorese noturna e perda de peso (INCA, 2021).
Imagem 1. Estadiamento de Ann Arbor
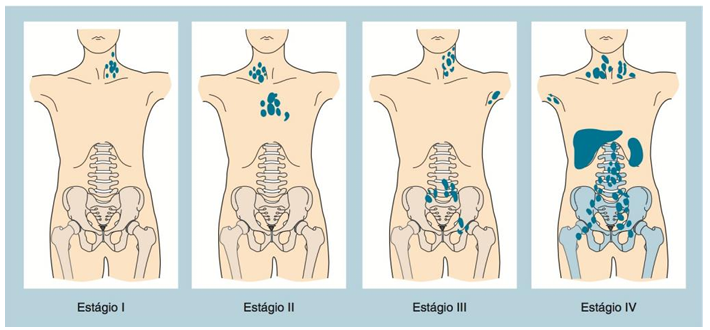
Fonte: Fundamentos de Hematologia de Hoffbrand (7° edição).
O sistema de Lugano é outra alternativa para estadiamento do LNH, separando os linfomas em doenças localizadas (estágios I, IE, II, IIE e II bulky) e doenças avançadas (estágios III e IV), conforme informado na tabela 1 (INCA, 2021). Dessa forma, os exames necessários para determinar a fase da doença são hemograma completo, função renal e hepática, desidrogenase lática (LDH), beta-2 microglobulina, cálcio, ácido úrico, eletroforese de proteínas, sorologias virais, biópsia de medula óssea e tomografia computadorizada de tórax, de abdome e de pelve, além de PET-CT com contraste (ARAÚJO et al.;2008).
Tabela 1. Classificação de Lugano.
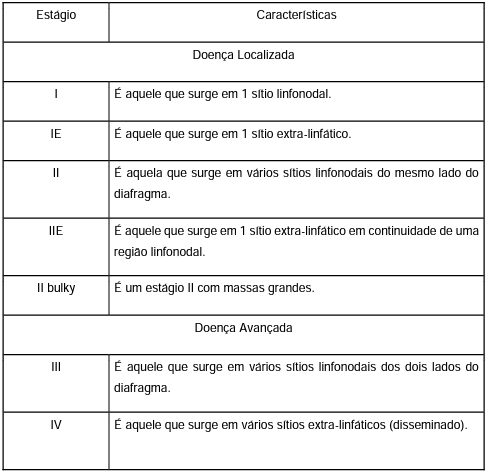
Fonte: INCA, 2021.
A classificação dos linfomas de células B é feita de acordo com a gravidade da neoplasia em baixo-grau, sendo composto por células pequenas e indolentes, grau intermediário, sendo composto por células grandes e difusas, e alto-grau, sendo composto pelos casos recidivantes (AKANJI, 2006). Em conclusão, o tratamento indicado é o uso dos fármacos ciclofosfamida, doxorrubicina, vincristina e prednisolona (CHOP), em conjunto com o rituximabe, cujo mecanismo de ação estimula a eliminação de células cancerígenas e a produção de células de defesa no organismo (PASQUALLETO; SORIANO; STUCHI, 2018).
O rituximabe é um anticorpo monoclonal quimérico desenvolvido para o tratamento de linfoma de células B maligno, denominado de anti-CD20, que induz a liberação de grânulos citotóxicos do sistema imune mediada pela apoptose celular, sendo utilizado na radioimunoterapia. Nesse procedimento, a radiação citotóxica derivada dos radioisótopos terapêuticos é depositada nos focos de neoplasia através do imunoconjugado de antiCD20, sem atingir os tecidos sadios (AKANJI, 2006).
Assim, a administração do CHOP pode ser feita de forma curativa ou paliativa em conjunto com tratamentos de quimioterapia, para as formas mais agressivas de LNH, e de radioterapia, para as formas menos agressivas de LNH, além do uso de procedimentos cirúrgicos e de transplante de medula óssea nas situações de risco iminente de vida e de recaídas (PASQUALLETO; SORIANO; STUCHI, 2018). O autotransplante de célulastronco hematopoiéticas após a aplicação de terapia sequencial de alta dose, devido a sensibilidade à quimioterapia de resgate (BALDISSERA et al. 2010). Ao final do processo, devem ser feitos exames físicos, laboratoriais e de imagem, para detectar eventos recidivantes (PASQUALLETO; SORIANO; STUCHI, 2018).
2.DESENVOLVIMENTO
A investigação diagnóstica é essencial no manejo terapêutico do linfoma não Hodgkin, que inclui exame físico (sintomas B), laboratoriais (hemograma, sorologia, imunofenotipagem e biópsia da medula óssea) e radiológicos/moleculares (tomografia, cintilografia e PET-CT), levando em consideração a apresentação patológica da doença.
Dessa forma, a NATIONAL COMPREHENSIVE CANCER NETWORK (NCCN), uma aliança sem fins lucrativos dos principais centros de câncer dedicados ao desenvolvimento de diretrizes e de recomendações no tratamento de câncer, fornece guidelines em diferentes idiomas para melhora da qualidade de vida dos pacientes oncológicos em todo o mundo. Em relação ao linfoma de células B, a terapia de primeira linha é determinada a partir do sistema de classificação de Lugano.
Os estágios I e II sem doença mesentérica extensa podem ser divididos em linfomas não-volumosos (<7,5cm) e volumosos (>7,5cm), tratados com 3 e 6 ciclos do RCHOP, respectivamente, podendo ser necessário a aplicação de radioterapia de consolidação (ISRT), para inibição do crescimento das células tumorais. Já os casos de estágio II com doença mesentérica extensa, III e IV, são realizados 6 ciclos do RCHOP, com novo estadiamento após 2-4 ciclos dos medicamentos.
Também é necessário realizar um reestadiamento com PET-CT após a terceira aplicação farmacológica, cujo resultado pode ser resposta completa ou parcial, sendo necessário mais 1-3 ciclos dos medicamentos ou ISRT, além de doença progressiva, que exige uma repetição da biópsia. Ao término do tratamento, o paciente deve realizar exames laboratoriais a cada 3-6 meses por 5 anos e exames de imagem a cada 6 meses por 2 anos, avaliando a remissão completa do linfoma e a presença de complicações pós tratamento. Ademais, a recidiva com menos de 12 meses é tratada com transplante ou ISRT, e a recidiva com mais de 12 meses é tratada com um receptor quimérico de antígeno denominado CAR-T (anti-C19).
No Brasil, segundo o Ministério da Saúde, os pacientes são classificados de acordo com o Índice de Prognóstico Internacional (IPI) em baixo risco, risco intermediário-baixo, risco intermediário-alto e alto risco, que inclui variáveis como idade >60anos, estágios III ou IV, acometimento de mais de uma sítio extranodal, performance status maior do que 2, dosagem sérica de desidrogenase láctica alta e diagnóstico prévio de síndrome da imunodeficiência adquirida (HIV/AIDS). Nesse ínterim, o tratamento para linfoma de células B só pode ser feito em pacientes maiores de 18 anos, que apresenta diagnóstico histopatológico positivo, cujos critérios de interrupção incluem grau de toxicidade, capacidade funcional do paciente ausência de resposta após o quarto ou oitavo ciclo e falta de aderência.
Assim, a primeira linha de tratamento inclui 6-8 ciclos de quimioterapia com ciclofosfamida (750 mg endovenosa), doxorrubicina (50 mg endovenosa), vincristina (1,4 mg endovenosa) e prednisona (40 mg via oral), associados com rituximabe (375 mg endovenosa) em um intervalo de 21 dias, sendo que a medicação deve ser suspensa após a quarta aplicação, quando não houver resposta completa. A escolha da segunda linha de tratamento é feita quando não há resposta até o quarto ciclo farmacológico, através da administração de fosfato de diidroxiacetona (DHAP), para identificar os candidatos no transplante autólogo de células tronco hematopoiéticas (casos recidivantes). Também pode ser utilizado terapia profilática a partir do fator estimulante de crescimento de colônias de granulócitos nos pacientes neutropênicos.
3. MATERIAIS E MÉTODOS
3.1 ABORDAGEM METODOLÓGICA
Foi realizada uma revisão sistemática da literatura sobre linfoma não-Hodgkin de células B, que permite identificar, analisar, compreender e sintetizar os resultados de estudos anteriores envolvendo a mesma temática. Dessa forma, houve a realização de um estudo atualizado e ampliado a partir de bases científicas, que pode resultar em uma conclusão inovadora.
3.2 INSTRUMENTOS E PROCEDIMENTOS PARA COLETA DE DADOS
As bases de dados utilizados na busca de literatura foram PubMed, Biblioteca Nacional de Medicina, Portal regional da biblioteca virtual em saúde – BVS e Biblioteca digital Scientific Electronic Library Online (SCIELO). Os descritores aplicados incluem Linfoma não-Hodgkin B and estágios da doença, Linfoma não-Hodgkin B and práticas terapêuticas e Linfoma não-Hodgkin B and avanços no tratamento.
3.2.1 Critérios de inclusão
Neste estudo, foram utilizados artigos publicados entre 2004 e 2022, gratuitos e na linguagem portuguesa e inglesa, com temáticas que atendem aos objetivos propostos na pesquisa.
3.2.2 Critérios de exclusão
Neste estudo, foram não foram utilizadas publicações em formato de teses, de dissertações, de livros, de artigos duplicados, de artigos oriundos de revisões bibliográficas, bem como literaturas oriundas de jornais eletrônicos, de blogs e de outros meios não condizentes às bases de dados acima selecionadas e destacadas.
4. CONCLUSÃO
A eficácia do manejo terapêutico do linfoma de Hodgkin de células B depende da realização do diagnóstico precoce e do estadiamento adequado, sendo a quimioterapia com RCHOP a primeira opção de tratamento no Brasil e em países europeus e norteamericanos. Contudo, os paciente diagnosticados com essa patologia só podem ser atendidos em centros hospitalares oncológicos com suporte tecnológico e multiprofissional, estrutura ambulatorial e hemoterapia, para obtenção de resultados satisfatórios, que pode forçar o paciente a procurar atendimento em outras cidades, aumento os gastos financeiros com alimentação, moradia e transporte.
Consequentemente, a regulamentação e a organização das redes assistenciais de atendimento ao paciente são feitas através do Cadastro Nacional dos Estabelecimentos de Saúde (CNES), que gerencia a autorização prévia dos procedimento, o monitoramento dos procedimento quimioterápicos e a análise dos percentuais do número de casos de LNH, além de ações de auditoria para verificar a compatibilidade do procedimento e do diagnóstico, a conformidade da prescrição e da administração dos medicamentos, a cobrança dos serviços executados e o grau de satisfação dos doentes.
Além disso, o Ministério da Saúde e as Secretarias de Saúde não fornecem medicamentos antineoplásicos diretamente aos hospitais ou usuários do Sistema Único de Saúde (SUS). Portanto, os hospitais credenciados e habilitados em oncologia são responsáveis pela entrega dos medicamentos oncológicos, sendo que o preço de cada ampola do imunoterápico rituximabe varia entre R$ 8800-11900 reais, dependendo da empresa farmacêutica e da concentração do princípio ativo, cujo acesso pode ser indisponível para paciente de baixo nível socioeconômico.
REFERÊNCIAS
ALMENZAR, B, N.; BELMONTE, M.J.M; ESPUCH, J.G. Linfomas. Elsevier, Espanha, vol.13, n.20, Novembro 2020, p. 1125-1132. Disponível em: https://www.sciencedirect.com/science/article/pii/S0304541220302687. Acesso em 30 jun. 2022.
AKANJI, Akinkunmi Ganiyu. Estudo de marcação com iodo-131 de anticorpo monoclonal anti-CD20 usado na terapia de linfoma não-Hodgkin. 2006. Tese de Doutorado. Master Dissertation.
BALDISSERA, Renata et al. O transplante de células-tronco hematopoéticas no tratamento dos linfomas não Hodgkin. Revista Brasileira de Hematologia e Hemoterapia, v. 32, p. 106-114, 2010.
BARBOSA, Sheyla Fernanda da Costa et al. Aspectos epidemiológicos dos casos de leucemia e linfomas em jovens e adultos atendidos em hospital de referência para câncer em Belém, Estado do Pará, Amazônia, Brasil. Rev. Pan – Amazônica de Saúde 2015; 6(1):43-50. Disponível em http://revista.iec.gov.br/submit/index.php/rpas/article/view/255. Acesso em 03 mai. 2022.
BARROS, Liziane. Linfoma Não Hodgkin: o que você precisa saber. Pebmed, 2021. Disponível em https://pebmed.com.br/linfoma-nao-hodgkin-o-que-voce-precisasaber/?msclkid=2979590dd05b11ecb23e594621a7c3bd. Acesso em 03 mai. 2022.
BRASIL. Ministério da Saúde. INCA Instituto Nacional de Câncer (Brasil). Tipos de câncer. Versão para profissionais da saúde. Disponível em https://www.inca.gov.br/tiposde-cancer/linfoma-nao-hodgkin. Acesso em 03 mai. 2022.
BRASIL. Portaria nº 956, de 26 de setembro de 2014. Protocolo Clínico e Diretrizes Terapêuticas do Linfoma Difuso de Grandes Células B. Ministério da Saúde e Secretaria de Atenção à Saúde. Disponível em: https://www.gov.br/saude/pt-br/assuntos/protocolosclinicos-e-diretrizes-terapeuticas-pcdt/arquivos/2014/ddt_linfomadifusob_26092014.pdf. Acesso em: 15 de março de 2023.
COSTA, Vanessa Indio do Brasil da; MELLO, Márcia Sarpa de Campos de; FRIEDRICH, Karen. Exposição ambiental e ocupacional a agrotóxicos e o linfoma não Hodgkin. Saúde debate – Rio de Janeiro, v. 41, n. 112, 2017. https://www.scielo.br/j/sdeb/a/gq7pCfbPYfCgvJqksVPCgzy/. Acesso em 03 mai. 2022.
ERCOLE; Flávia Falci; MELO, Laís Samara de; ALCOFORADO, Carla Lúcia Goulart Constant. Revisão integrativa versus revisão sistemática. REME, vol. 18.1, 2014. Disponível em http://www.reme.org.br/artigo/detalhes/9. Acesso em 08 mai. 2022.
FARIAS, Jener Gonçalves; CARNEIRO, Gleicy Gabriela V. S.; MACIEL, Anderson da Silva; MEIRELLES, Mayle; M. SANTOS, Jean Nunes. Linfoma não-Hodgkin de células B: relato de caso. Rev. Cir. Traumatol. Buco-Maxilo-fac., Camaragibe v.8, n.3, p. 25, 2008. Disponível em http://www.revistacirurgiabmf.com/2008/v8n3/3.pdf?msclkid=fa912c21d13011ec93e63dcfff 0604ef. Acesso em 03 mai. 2022.
FREITAG, Mateus Augusto; AMADUCCI, André; ORSO, Ivan Roberto Bonotto. Linfoma não-hodgkin de células b: relato de caso. Revista Thêma et Scientia – Vol. 9, no 1E, 2019 – Edição Especial Medicina. Disponível em https://www.sumarios.org/revista/th%C3%AAma-etscientia?msclkid=2dac9649d13811ec9c930cc98227b61d. Acesso em 03 mai. 2022.
HOFFBRAND, Victor; MOSS, Paul. Fundamentos em Hematologia de Hoffbrand. 7 ed. Porto Alegre: Artmed, 2018.
DE LIMA ARAÚJO, Luiz Henrique et al. Linfoma não-Hodgkin de alto grau-Revisão da literatura. Revista brasileira de cancerologia, v. 54, n. 2, p. 175-183, 2008.
Linfoma de Células B. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®), 2022. Disponível em: https://www.nccn.org/guidelines/guidelinesdetail?category=1&id=1480. Acesso em: 15 de março de 2023.
MACHADO, Mariana et al. Linfoma de Hodgkin–Conceitos actuais. Medicina Interna, v. 11, n. 4, p. 208, 2004.
PASQUALETTO, Francieli Carolini; DE MATTOS SORIANO, Lidiane Regi; STUCHI, Nathália Maciel Maniezzo. Novas condutas terapêuticas para o Linfoma não Hodgkin. Revista Eletrônica Acervo Saúde, v. 11, n. 2, p. e187-e187, 2019. INCA. Linfoma não Hodgkin: Estimativa de novos casos. [S. l.], 19 ago. 2021. Disponível em: https://www.inca.gov.br/tipos-de-cancer/linfoma-nao-hodgkin. Acesso em: 24 mar. 2022
Sistema Único de Saúde (SUS). Protocolo clínico e diretrizes terapêuticas do linfoma de hodgkin no adulto. Instituto Nacional de Câncer José Alencar Gomes da Silva (INCA).Disponível em: https://www.inca.gov.br/sites/ufu.sti.inca.local/files//media/document/informe-sus-oncojaneiro-2021_0.pdf. Acesso em: 03 de setembro de 2022.
