ACUTE HEART FAILURE (AHF): PROTOCOL FOR AVERAGE FIRST CARE UNIT COMPLEXITY
REGISTRO DOI: 10.5281/zenodo.8322813
Ana Luísa Silva Oliveira¹
Axel Felipe Câmara Pereira2, Bruno Angelo Silva3
Carlos Eduardo Lins Franca Piau4, Juliana Leles Costa5
Resumo
Objetivo: A insuficiência cardíaca aguda (ICA) é uma síndrome cardiovascular grave que pode levar a óbito. Este artigo propõe um protocolo para atendimento a pacientes com ICA em Unidades de Pronto Atendimento (UPA) de média complexidade. Portanto, este é um artigo que tem com objetivo de elaborar um protocolo para atendimento em quadros de Insuficiência Cardíaca Aguda (ICA) em pacientes internados em Unidades de Pronto Atendimento (UPA), de média complexidade, tal como a unidade Clarice Borges, do município de Barreiras. Metodologia: O protocolo foi desenvolvido com base nas diretrizes mais atualizadas da American Heart Association (AHA), da European Society of Cardiology (ESC) e da Sociedade Brasileira de Cardiologia (SBC), visando estabelecer condutas padronizadas por toda a equipe médica da UPA em pacientes suspeitos de ICA, levando em consideração a realidade do Sistema Único de Saúde (SUS) e os recursos, por vezes limitados, que o sistema oferece. Resultados e Conclusão: O diagnóstico da ICA é baseado na avaliação clínica, exames laboratoriais e exames de imagem. O tratamento visa aliviar os sintomas, otimizar a função cardíaca e prevenir complicações. Os medicamentos mais usados são diuréticos, inotrópicos positivos e vasodilatadores. Os pacientes também devem ser monitorados quanto aos sinais vitais, função renal e níveis de eletrólitos. O protocolo desenvolvido para UPA’s leva em consideração a realidade do Sistema Único de Saúde (SUS) e os recursos limitados que o sistema oferece. O protocolo é flexível e pode ser adaptado às circunstâncias específicas de cada local.
Palavras-chave: Descompensação Cardíaca. Falência Cardíaca. Insuficiência Cardíaca Aguda.
Abstract
Objective: Acute heart failure (AHF) is a serious cardiovascular syndrome that can be fatal. This article proposes a protocol for the care of patients with AHF in medium-complexity emergency care units (UPAs). Methodology: The protocol was developed based on the most up-to-date guidelines from the American Heart Association (AHA), the European Society of Cardiology (ESC), and the Brazilian Society of Cardiology (SBC). Results and Conclusions: The diagnosis of AHF is based on clinical evaluation, laboratory tests, and imaging studies. Treatment aims to relieve symptoms, optimize cardiac function, and prevent complications. The most commonly used medications are diuretics, inotropics, and vasodilators. Patients should also be monitored for vital signs, renal function, and electrolyte levels. The protocol developed for UPAs takes into account the reality of the Unified Health System (SUS) and the limited resources that the system offers. The protocol is flexible and can be adapted to the specific circumstances of each location.
Key-words: Heart Decompensation. Heart Failure. Acute Heart Failure.
1 INTRODUÇÃO
A Insuficiência Cardíaca Aguda (ICA) é uma síndrome clínica caracterizada pela incapacidade do coração de manter o débito cardíaco (DC) adequado para as necessidades metabólicas do organismo, (ALBUQUERQUE et al., 2015). Isso pode ocorrer devido a uma disfunção cardíaca estrutural ou funcional subjacente, uma síndrome com repercussões cardiovasculares imediatas, tendo sido disposta dentro de um curto período de tempo o qual fora caracterizado pelo início súbito ou pela rápida progressão de sinais e sintomas estruturados previamente como pertencentes à própria insuficiência cardíaca (IC), expondo assim a necessidade de uma intervenção em caráter de urgência, (DUTRA; GOMES, 2023).
No Brasil a IC permanece como diagnóstico inicial e fator de internação em pelo menos 200.833 casos durante o ano de 2018, 199.844 casos durante o ano de 2019 e exatos 169.485 casos durante o ano de 2020 segundo o DATASUS, perfazendo uma curva de melhora em números absolutos do desfecho comum que é essa síndrome cardiovascular, ainda que em 2017 tenha havido 190.000 casos de internações por ICA e o diagnóstico de IC seja compartilhado com outros 240.000 pacientes ao ano, (AGUIAR et al., 2022). A mesma pode decorrer de uma disfunção cardíaca aguda (sem a presença de diagnóstico prévio de IC), ou da exacerbação de um quadro crônico. É uma das principais causas de internação hospitalar no Brasil e no mundo, estando relacionada a um aumento da mortalidade e à necessidade de reinternação em curto e longo prazos, (BERTOLETTI, 2023).
A despeito dos avanços no tratamento da IC crônica, a incidência de internações por ICA vem aumentando, o que leva a um grave problema de saúde pública, com altíssimo custo para o sistema de saúde, (ALBUQUERQUE et al., 2015). De acordo com o estudo BREATHE (2023), primeiro registro brasileiro de ICA, evidenciou que as principais etiologias para a enfermidade foram: isquêmica (30%), hipertensiva (20%), dilatada idiopática (15%), valvar (12%) e doença de Chagas (11%). Os pacientes apresentaram alta taxa de mortalidade intra-hospitalar (13%) e baixa taxa de prescrição de medicamentos baseados em evidências.
A avaliação diagnóstica define não somente a presença ou não da ICA, mas fornece amplo entendimento etiopatogênico, fisiopatológico e hemodinâmico, que deve ser realizado nas primeiras duas horas após a admissão neste serviço, (BENJAMIN et al., 2018). A definição da conduta terapêutica será mais adequada para o controle dos distúrbios que estiverem associados à ICA.
As etapas de avaliação seguem uma lógica na construção do racional diagnóstico: presença ou não de IC aguda; modelo fisiopatológico de apresentação (aguda nova ou crônica agudizada); tipo de insuficiência cardíaca (ICFEp, ICFELr, ICFEr); definição do fator etiológico; presença do fator descompensador; perfil hemodinâmico e presença de comorbidades não cardiovasculares descompensada, (CRUZ et al., 2022).
A elaboração de um protocolo para atendimento em quadros de ICA nos pacientes internados na UPA, como no caso do município de Barreiras, na Unidade Clarice Borges (UPA) se faz necessário devido, à complexidade do quadro clínico e suas repercussões imediatas aos pacientes que ali permanecem, tal qual o fato de que nem sempre é possível à equipe responsável pelo mesmo, apresentar uma profissionalização referente à Cardiologia tendo sido outorgada de maneira prévia pelo Conselho Nacional de Saúde (CNS).
De tal modo, a então necessidade frente à realização e subsequente padronização estratificada por meio de um protocolo que busque estabelecer um fluxograma acessível a todo o corpo clínico do hospital é apresentada, otimizando o processo de diagnóstico e reduzindo o intervalo que define o início do manejo hospitalar para os mais diversos casos de ICA.
Nesse sentido, o presente artigo tem o objetivo de discutir sobre o diagnóstico para ICA e propor um manejo terapêutico para os pacientes internados com quadro de Insuficiência Cardíaca Aguda em Unidade de Pronto Atendimento, de média complexidade.
A abordagem terapêutica na insuficiência cardíaca aguda (ICA) é um processo complexo e fundamental para a evolução clínica do paciente. A escolha adequada do tratamento não apenas afeta diretamente a duração da permanência do paciente na unidade hospitalar, mas também tem implicações econômicas e impacto na evolução da descompensação, (FONTES-CARVALHO; LEITE-MOREIRA, 2011). Neste contexto, este estudo busca avaliar de forma abrangente os diferentes aspectos da terapia adotada para a ICA, considerando os benefícios clínicos, o custo associado a cada abordagem e as consequências na progressão da doença.
A seleção da terapia para ICA não se resume apenas à administração de medicamentos, mas envolve a aplicação de intervenções que abordam aspectos como oxigenação, controle hemodinâmico, administração farmacológica e uso de dispositivos, (NEVES et al., 2023). É crucial compreender como essas escolhas terapêuticas se correlacionam com o tempo de permanência do paciente na unidade hospitalar. Além disso, investigar a relação entre as opções terapêuticas e o custo associado a cada uma delas é de suma importância, considerando o panorama econômico da saúde.
Outro fator de relevância é avaliar como diferentes abordagens terapêuticas influenciam a evolução da descompensação da ICA. A variação na resposta ao tratamento pode ter impactos significativos na redução dos sintomas, estabilização clínica e prevenção de complicações. Portanto, esta pesquisa se propõe a analisar e comparar esses desdobramentos, a fim de fornecer informações cruciais para a tomada de decisões clínicas embasadas, otimização de recursos e melhoria nos resultados dos pacientes com ICA.
No decorrer deste estudo, serão exploradas as diferentes escolhas terapêuticas disponíveis para a ICA, considerando os benefícios clínicos, os aspectos econômicos envolvidos e o impacto na evolução da descompensação. A compreensão abrangente desses fatores contribuirá para uma visão mais precisa sobre as estratégias de tratamento mais eficazes e sustentáveis, visando o bem-estar dos pacientes e a otimização dos recursos hospitalares.
2 FUNDAMENTAÇÃO TEÓRICA
A insuficiência cardíaca aguda (ICA) é uma condição médica complexa e progressiva que envolve uma incapacidade cardíaca de bombear sangue de forma eficaz, resultando em sintomas como dispneia, fadiga e edema de membro inferiores, (WRITING COMMITTEE MEMBERS et al., 2016). A compreensão aprofundada dessa síndrome cardiovascular é crucial para o desenvolvimento de abordagens eficazes de diagnóstico e manejo.
A ICA é uma condição de saúde pública relevante, afetando milhões de pessoas em todo o mundo. No Brasil, a prevalência de IC é de aproximadamente 2 milhões de pacientes, e sua incidência é de aproximadamente 240.000 novos casos por ano (COMITÊ COORDENADOR DA DIRETRIZ DE INSUFICIÊNCIA CARDÍACA, 2018), ICA continua a ser uma das principais causas de hospitalização e morbidade em idosos e em pacientes com doenças cardiovasculares pré-existentes, (KANG et al., 2023).
Disfunção sistólica e/ou diastólica, remodelação ventricular, ativação neuro-hormonal e inflamatória, fazem parte dos mecanismos fisiopatológicos da ICA, esses processos contribuem para o enfraquecimento da bomba cardíaca e para a resposta compensatória inadequada, levando ao ciclo de agravamento da doença, (OLIVEIRA et al., 2022).
A ICA pode ser classificada em insuficiência cardíaca com fração de ejeção reduzida (ICFEr), onde a capacidade de bombeamento do coração está comprometida, e insuficiência cardíaca com fração de ejeção preservada (ICFEp), em que a disfunção diastólica é a característica predominante, (PONIKOWSKI et al., 2016). Doença arterial coronariana, hipertensão, doenças valvares e cardiomiopatias, são as etiologias predominantes da ICA, (SARTESCHI et al., 2019).
O diagnóstico requer uma avaliação clínica minuciosa, análise de sinais e sintomas, exames laboratoriais e de imagem. A quantificação de biomarcadores como BNP ou NT-proBNP desempenha um papel crucial na identificação da ICA e na diferenciação entre suas causas, (BUI; HORWICH; FONAROW, 2011).
O tratamento da ICA é multifacetado e envolve abordagens farmacológicas, mudanças no estilo de vida, intervenções não farmacológicas e, em casos graves, terapias invasivas como transplante cardíaco, (CARDOSO et al., 2023). Medicamentos como inibidores da enzima conversora de angiotensina (IECAs), betabloqueadores e diuréticos são frequentemente prescritos para aliviar sintomas e melhorar a função cardíaca, (FONTES-CARVALHO; LEITE-MOREIRA, 2011).
Apesar dos avanços no tratamento da ICA, ainda existem desafios significativos, como o aumento da prevalência em idosos, custos associados ao tratamento e a necessidade de abordagens personalizadas, (KOTECHA et al., 2016). Novas terapias, abordagens não farmacológicas e intervenções baseadas em tecnologia estão sendo exploradas para melhorar os resultados e a qualidade de vida dos pacientes com ICA, (RIBEIRO et al., 2016). Em suma, destaca-se a importância da compreensão abrangente da insuficiência cardíaca aguda. A análise da literatura existente não apenas fornece uma base para a pesquisa em andamento, mas também enfatiza a necessidade contínua de investigação e inovação para enfrentar os desafios associados a essa condição clínica complexa.
3 METODOLOGIA
Trata-se de uma pesquisa bibliográfica, um estudo observacional, analítico (transversal), com método qualitativo, em que utilizou as publicações em periódicos disponibilizados online para determinar qual a melhor escolha terapêutica para o tratamento de ICA.
Foi realizada uma busca bibliográfica incluindo as diretrizes de ICA da Sociedade Brasileira de Cardiologia (SBC), da American Heart Association (AHA) e da Sociedade Europeia de Cardiologia (ESC), por meio das fontes de busca constituídas pelos recursos eletrônicos nas seguintes bases de dados: Literatura Latino-Americana e do Caribe em Ciências da Saúde (LILACS), PUBMED, UpToDate e na biblioteca eletrônica Scientific Eletronic Library On-line (SciELO)
Os pesquisadores realizaram um levantamento bibliográfico no decorrer dos meses de julho à dezembro de 2022. Os descritores utilizados foram: Descompensação Cardíaca/Heart Decompensation OR Falência Cardíaca/Heart Failure OR Insuficiência Cardíaca Aguda/Acute Heart Failure. Salienta-se que os descritores supracitados se encontram nos Descritores em Ciências da Saúde (DeCS).
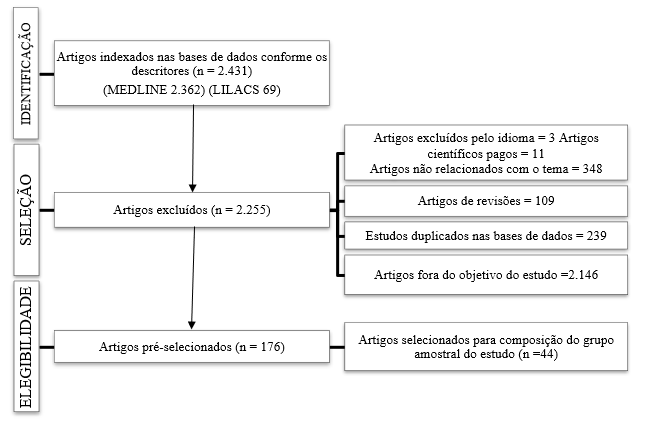
Após a identificação dos artigos, nas fontes de busca mencionadas, foram avaliados os títulos e resumos, de modo a selecioná-los (Figura 1). Tendo sido elencados os artigos que fizeram parte da amostra, que estão registrados em ficha própria contendo dados do periódico, base de dados, idioma, ano de publicação, objetivos, resultados e conclusões. Os resultados estão apresentados por meio de quadros que contemplem as principais características dos artigos utilizados na pesquisa.
Incluídos da pesquisa o material bibliográfico que contenham estudos com pacientes adultos (maiores de 18 anos), escritos em idioma inglês, espanhol e português, com o tema central de tratamento de ICA. As evidências deveriam ter sido publicadas entre os anos de 2017 e 2022. Artigos que cumpram os critérios de elegibilidade e com disponibilidade gratuita de todo o seu conteúdo na base de dados. Foram excluídos do presente estudo, os artigos duplicados em mais de uma base de dados, artigos que não discutem sobre o manejo e a eficácia na evolução do quadro.
4 RESULTADOS E DISCUSSÕES OU ANÁLISE DOS DADOS
4.1 CARACTERIZAÇÃO DO QUADRO CLÍNICO
4.1.1 Anamnese e Exame Físico
Antes de qualquer conduta, a identificação de risco imediato de morte deverá ser realizada e tratada em, no máximo, 30 minutos. Isso é determinante na evolução prognóstica intra-hospitalar destes pacientes, (COMITÊ COORDENADOR DA DIRETRIZ DE INSUFICIÊNCIA CARDÍACA, 2018).
A presença de qualquer um destes fatores de risco citados abaixo, torna o paciente elegível a uma vaga de UTI: Insuficiência Respiratória Aguda, Infarto Agudo do Miocárdio (IAM), Choque Cardiogênico, Edema Agudo de Pulmão (EAP), Taquiarritmia, Bradiarritmia, causas mecânicas agudas, Emergência Hipertensiva, Tromboembolismo Pulmonar (TEP), Acidente Vascular Cerebral (AVC), Confusão Mental e Desorientação, (AGUIAR et al., 2022).
O diagnóstico de ICA é feito baseado em sinais e sintomas clínicos e amparado por exames complementares. Dentro da anamnese devemos estabelecer se a IC é de origem recente ou uma doença crônica agudizada, assim como o provável fator causal e desencadeante, as comorbidades e os fármacos que vêm sendo utilizados, (ALBUQUERQUE et al., 2015).
As queixas mais comumente apresentadas pelos pacientes são: tosse, dispneia, fadiga e edema periférico; no entanto, a presença de ortopneia e dispneia paroxística noturna (DPN) são os sintomas mais sensíveis e específicos associados a ICA, (CARDOSO et al., 2023).
Entre os sinais de exame físico, aqueles com maior especificidade são a presença de terceira bulha e a turgência jugular em 45º, entretanto, a sensibilidade desses sinais é baixa e sua ausência não exclui o diagnóstico de IC, (CRUZ et al., 2022).
Segundo o Comitê Coordenador da Diretriz de Insuficiência Cardíaca de 2018, a ICA ainda deve ser classificada de acordo com cinco aspectos: síndrome clínica de apresentação (insuficiência ventricular esquerda, IC congestiva, choque cardiogênico e edema agudo de pulmão); tempo de evolução da doença (IC aguda nova ou crônica agudizada); tipo de disfunção ventricular (ICFEp − considerada FEVE ≥ 50%; ICFELr − com FEVE de 41% a 49%; e ICFEr – representada por FEVE ≤ 40%); perfil hemodinâmico (exame clínico avalia a presença de congestão ou baixo débito cardíaco, classificando o paciente em quatro categorias( Quadro 1); e de acordo com a classe funcional segundo a New York Heart Association (NYHA):
I – Não há limitação física. Cansaço aos grandes esforços. Ergometria > 6 METs;
II – Limitação física leve. Cansaço aos moderados esforços. Ergometria 4-6 METs;
III – Limitação física moderada. Cansaço aos pequenos esforços. Ergometria < 4 METs;
IV – Limitação física grave. Sintomas em repouso ou aos mínimos esforços. Não tolera ergometria.
Basicamente, os sintomas relacionados à ICA são devido à congestão pulmonar ou sistêmica (edema de membros inferiores, hepatomegalia, ascite) associados ou não à presença de baixo débito cardíaco (hipotensão arterial, alterações do nível de consciência, oligúria, pulso filiforme, extremidades frias) (COUCEIRO et al., 2023), (Quadro 2).
Quadro 1 Perfil hemodinâmico

Fonte: Comitê Coordenador da Diretriz de Insuficiência Cardíaca. Diretriz Brasileira de Insuficiência Cardíaca Crônica e Aguda. Arq Bras Cardiol. (Adaptado em 2022).

*Largura de pulso corresponde a pressão arterial sistólica – pressão arterial diastólica/ pressão arterial sistólica x 100. FR: frequência respiratória; PAS: pressão arterial sistólica.
Fonte: Comitê Coordenador da Diretriz de Insuficiência Cardíaca. Diretriz Brasileira de Insuficiência Cardíaca Crônica e Aguda. Arq Bras Cardiol. 2018; 111(3):436-539 (Adaptado em 2022).
É recomendada a utilização de alguns critérios, como por exemplo o de Framinghan (Quadro 3), para que se estabeleça o diagnóstico de ICA. Em seguida, após confirmação, se faz necessário a identificação dos fatores de descompensação, (COUCEIRO et al., 2023) (Quadro 4).

* Para o diagnóstico de insuficiência cardíaca: dois critérios maiores e um menor, ou um maior e dois menores. Para a utilização dos critérios menores é necessária a ausência de qualquer condição que possa justificar a presença de um dos critérios
Fonte: Comitê Coordenador da Diretriz de Insuficiência Cardíaca. Diretriz Brasileira de Insuficiência Cardíaca Crônica e Aguda. Arq Bras Cardiol. 2018; 111(3):436-539 (Adaptado em 2022).

IAM: infarto agudo do miocárdio; DDD: marca-passo dupla câmara; VVI: marca-passo unicameral; HAS: hipertensão arterial sistêmica.
Fonte: Comitê Coordenador da Diretriz de Insuficiência Cardíaca. Diretriz Brasileira de Insuficiência Cardíaca Crônica e Aguda. Arq Bras Cardiol. 2018; 111(3):436-539 (Adaptado em 2022).
4.2 OBTENÇÃO DE EXAMES COMPLEMENTARES
4.2.1 Eletrocardiograma
O eletrocardiograma (ECG) é uma ferramenta diagnóstica essencial na avaliação de pacientes com ICA. Por meio dele, podemos não só suspeitar da etiologia da IC bem como da causa da descompensação, (DANZMANN et al., 2023).
Na admissão do paciente, é necessária a monitorização completa do paciente, e avaliação eletrocardiográfico por meio do monitor, com confirmação posterior pelo ECG de taquiarritmias ou bradiarritmias, que demandem intervenção terapêutica imediata, (HEIDENREICH et al., 2022).
4.2.2 Radiografia de tórax
Deve ser realizada no leito e em pacientes de baixo risco, no gabinete nas projeções póstero-anterior e perfil. É um importante exame inicial no paciente dispneico que permite avaliar a área cardíaca (índice cardiotorácico > 0,5), a presença de sinais de congestão (cefalização da trama vascular pulmonar, linhas B de Kerley e derrame pleural), além de diferenciar ICA de doença pulmonar primária. Salienta-se, porém, que uma radiografia sem alterações não afasta congestão pulmonar, principalmente em pacientes com IC crônica agudizada, (MCMURRAY et al., 2014).
4.2.3 Ecocardiograma Transtorácico
O ecocardiograma transtorácico (ECOTT) é um exame essencial na avaliação de ICA e deve ser realizado em todos os pacientes dentro das primeiras 48 horas da admissão. Ele auxilia nas definições do fator etiológico, do grau da disfunção ventricular, da avaliação da congestão pulmonar e sistêmica, e da identificação de fator mecânico, importantes para o direcionamento precoce da terapêutica admissional, (AMBROSY et al., 2014).
4.2.4 Exames laboratoriais
Exames laboratoriais iniciais devem ser solicitados com intuito de identificar comorbidades e causas do episódio agudo. Solicita-se hemograma, proteína C-reativa, glicemia de jejum, função renal (ureia e creatinina), eletrólitos (sódio, potássio, magnésio), transaminases, proteínas totais e frações, bilirrubinas, função tireoidiana, ferro sérico, ferritina, gasometria venosa e lactato, (ACCORSI et al., 2023).
O peptídeo natriurético (BNP) também deve utilizado de rotina para avaliação diagnóstica admissional em pacientes com dispneia, pois apresentam alto valor preditivo de IC quando analisados de forma isolada ou quando associados ao exame clínico e radiológico do tórax, (ALEXSANDER et al., 2022).
Níveis de BNP inferior a 100pg/mL deixam o diagnóstico de IC improvável, enquanto que níveis muito elevados, superiores a 500pg/mL tornam o diagnóstico de IC provável. Vários fatores clínicos podem elevar o peptídeo natriurético, reduzindo seu valor preditivo positivo. Portanto, níveis de BNP na faixa entre 100 a 500pg/mL necessitam de correlação clínica para confirmação de ICA, (KOTECHA et al., 2016).
Pacientes em uso de sacubitril-valsartana têm a acurácia diagnóstica do peptídeo natriurético diminuída1, pois a inibição da neprilisina pelo sacubritil promove elevação nos níveis séricos do BNP, mas não do NT-proBNP, (ACCORSI et al., 2023).
4.3 DIAGNÓSTICO DE INSUFICIÊNCIA CARDÍACA COM FRAÇÃO DE EJEÇÃO PRESERVADA (ICFEP), INSUFICIÊNCIA CARDÍACA COM FRAÇÃO DE EJEÇÃO LEVEMENTE REDUZIDA (ICFELR) E INSUFICIÊNCIA CARDÍACA COM FRAÇÃO DE EJEÇÃO REDUZIDA (ICFER)
4.3.1 Insuficiência Cardíaca Com Fração De Ejeção Preservada (ICFEP)
Inicialmente, procuramos por sinais e sintomas de IC; comorbidades associadas tais como obesidade, hipertensão, diabetes mellitus, idade avançada, fibrilação atrial; exames complementares. A suspeita de ICFEp está igual ou maior que 50%, sem a presença de valvopatia ou isquemia importante, e com pelo menos um fator de risco típico, (PETERSEN et al., 2021).
Em seguida, deve ser avaliado a presença de remodelamento cardíaco, disfunção diastólica, sinais de congestão e níveis elevados de BNP. A ausência desses critérios, pode considerar o descarte do diagnóstico, devendo-se atentar para outras causas. Caso todos estes parâmetros estejam presentes, o diagnóstico é confirmado. Necessário portanto, a solicitação de parecer para a equipe de cardiologia da unidade, (PONIKOWSKI et al., 2016).
4.3.2 Insuficiência Cardíaca Com Fração De Ejeção Levemente Reduzida (ICFELR)
Caracterizado pela FEVE entre 41 e 49%, com peptídeos natriuréticos elevados e com presença de alterações estruturais e/ou disfunção diastólica ao ecocardiograma transtorácico, (WRITING COMMITTEE MEMBERS et al., 2016).
4.3.3 Insuficiência Cardíaca Com Fração De Ejeção Reduzida (ICFER)
Definido pela FEVE inferior ou igual a 40% associado a níveis elevados dos peptídeos natriuréticos e à presença de alterações estruturais e disfunção diastólica ao ecocardiograma transtorácico, (WRITING COMMITTEE MEMBERS et al., 2016).
4.4 ABORDAGEM TERAPÊUTICA
4.4.1 Suporte Clínico
No manejo inicial do paciente com ICA deve-se realizar a avaliação da via aérea para assegurar oxigenação e ventilação adequadas, incluindo oximetria de pulso contínua. Não é recomendado a administração de rotina de suplementação de oxigênio na ausência de hipóxia, (ALBUQUERQUE et al., 2015).
Na presença de desconforto respiratório (frequência respiratória > 25mpm, SATO2 < 90%, batimento de asa de nariz, uso de musculatura acessória), iniciar suplementação de O2 com o uso de cateter nasal, (CORREIA; MESQUITA, 2022). Caso não haja melhora, deve-se trocar o dispositivo para máscara de Venturi ou com reservatório, evoluindo para VNI (ventilação não-invasiva) e para IOT (Intubação Orotraqueal) conforme a necessidade, (HOTTA et al., 2022).
Avaliar a hemodinâmica e manter monitorização cardíaca contínua, além de assegurar um acesso endovenoso. Para pacientes com congestão pulmonar (perfil B e C), orientar repouso relativo, realizar controle diário do peso e da diurese (caso necessário, realizar sondagem vesical de demora), manter restrição hidrossalina e elevar a cabeceira, (GROSSMAN, 2023).
4.5 ABORDAGEM TERAPÊUTICA CONFORME FRAÇÃO DE EJEÇÃO DO VENTRÍCULO ESQUERDO (FEVE)
4.5.1 ICFER
Nesta afecção específica, existem alguns fármacos que modificam o curso da doença, agindo diretamente na morbimortalidade dos pacientes. Dentre estes medicamentos encontram-se os Inibidores da Enzima Conversora de Angiotensina (IECA) e os Bloqueadores dos Receptores de Angiotensina (BRA), os Inibidor do Receptor da Angiotensina e Neprisilina (INRA), os antagonistas da aldosterona e os betabloqueadores, (FONTES-CARVALHO; LEITE-MOREIRA, 2011).
Os IECAs e os BRAs não devem ser utilizados nos casos de hipotensão arterial sintomática. Seu uso é indicado como manutenção da terapia utilizada cronicamente. Suas doses devem ser diminuídas ou a medicação suspensa no caso de hipotensão, insuficiência renal aguda ou hipercalemia. Iniciar ou reiniciar quando paciente se manter estável, (WRITING COMMITTEE MEMBERS et al., 2016).
Os INRAs poderão ser utilizados em substituição aos IECAs / BRAs em pacientes descompensados. Este é aceitável e seguro quando a Taxa de Filtração Glomerular (TFG) for maior que 30mL/min. Caso o paciente esteja utilizando IECA, é necessário a descontinuação do seu uso por 36 horas antes de iniciar os INRAs, (SÁNCHEZ-MARTELES; RUBIO GRACIA; GIMÉNEZ LÓPEZ, 2016).
Como a aldosterona pode ser produzida independentemente do sistema renina-angiotensina, seus efeitos adversos não são completamente inibidos, mesmo com o uso máximo de IECA / BRA. Assim, os antagonistas da aldosterona (também chamados antagonistas do receptor de mineralocorticoides) são utilizados particularmente em pacientes com sintomas moderados a graves ou com sinais de IC, destaca-se a espironolactona, (CRUZ et al., 2022). Eles reduzem mortalidade, incluindo por morte súbita, pacientes com FEVE < 35%, IC crônica ou ICA complicada por IAM. Seu uso deve ser descontinuado em caso de hipercalemia (K > 5,5mEq/L) ou creatinina maior que 2,5mg/dL, (COUCEIRO et al., 2023).
Os betabloqueadores mostraram benefício ao seu uso a longo prazo. Estes não devem ser iniciados durante os episódios de descompensação aguda, sendo usados apenas naqueles pacientes que já realizavam tratamento crônico com a medicação, (KANG et al., 2023).
Em casos de descompensação moderada/severa e hipotensão, a dose deve ser diminuída ou a medicação suspensa. Nos casos de congestão pulmonar importante ou necessidade de inotrópicos, a droga deve ser sempre suspensa. Deve-se iniciar ou reiniciar seu uso apenas quando o paciente estiver compensado, (NEVES et al., 2023).
Os Inibidores do SGLT2 (Dapaglifozina e Empaglifozina) são que possuem efeitos sobre o miocárdio e a vasculatura. Mostraram prevenir o início da IC em pacientes com DM 2. Ambos mostraram melhora de sintomas e de qualidade de vida, além de reduzir progressão da piora da função renal (quando TFG ≥ 20mL/min), hospitalização e mortalidade em pacientes com ICFEr em uso de terapia tripla otimizada (IECA/BRA/INRA, betabloqueador e antagonista da aldosterona). O benefício foi semelhante em pacientes com e sem diabetes, (BUI; HORWICH; FONAROW, 2011).
A hidralazina associada ao mono/dinitrato de isossorbida pode auxiliar pacientes intolerantes aos IECA / BRA (em geral, em virtude de disfunção renal significativa), embora o benefício a longo prazo dessa combinação seja limitado, (DANZMANN et al., 2023). Nos pacientes negros, quando acrescentada ao tratamento convencional, essa combinação mostrou reduzir as taxas de mortalidade e hospitalização e melhorar a qualidade de vida. Como vasodilatadores, esses fármacos melhoram a hemodinâmica, reduzem a regurgitação valvar e aumentam a capacidade de esforço, sem provocar comprometimento renal significativo, (HEIDENREICH et al., 2022).
A Ivabradina atua diminuindo a frequência cardíaca, age em receptores cardíacos localizados no nó sinoatrial; portanto, não possui outros efeitos cardíacos e não são úteis naqueles pacientes que estão fora do ritmo sinusal. Este fármaco está aprovado para uso em pacientes com ICFEr sintomático, em ritmo sinusal e FC > 70 bpm, apesar da terapia medicamentosa otimizada, (MOZAFFARIAN et al., 2016).
A digoxina causa um fraco inotropismo positivo, reduz a atividade simpática, bloqueia o nó AV, reduz a vasoconstrição e melhora o fluxo sanguíneo renal. Não traz benefícios para a sobrevida, porém, auxilia no controle dos sintomas, reduzindo a probabilidade de internação em pacientes com ICFEr. Sua escolha terapêutica é reservada para pacientes com sintomas significativos, apesar do tratamento triplo otimizado, (SÁNCHEZ-MARTELES; RUBIO GRACIA; GIMÉNEZ LÓPEZ, 2016).
A amiodarona está indicada para controle de frequência cardíaca naqueles pacientes portadores de FA de alta resposta ventricular refratários ao uso de betabloqueadores e digitálicos em dose otimizada, (COMITÊ COORDENADOR DA DIRETRIZ DE INSUFICIÊNCIA CARDÍACA, 2018).
A anticoagulação plena com heparina não fracionada (HNF) ou heparina de baixo peso molecular (HBPM) está indicada em pacientes com: FA, trombo intracavitário ou prótese valvar mecânica. A anticoagulação profilática estará indicada nos demais casos, (MCDONAGH et al., 2021).
A Terapia com ressincronização cardíaca (TRC) pode aliviar os sintomas e reduzir internações por IC. Está indicada em pacientes sintomáticos com FEVE ≤ 35%, ritmo sinusal e bloqueio de ramo esquerdo (BRE). Quando QRS ≥ 150ms, indicação classe I. Se QRS entre 120 e 149ms, indicação classe IIa, (PONIKOWSKI et al., 2014). O Cardiodesfibrilador Implantável (CDI) está indicado para aqueles pacientes com boa expectativa de vida que tiverem taquicardia ventricular sustentada sintomática ou fibrilação ventricular ou sintomáticos com FEVE inferior a 30%, principalmente coronariopatas, (OLIVEIRA et al., 2022).
4.5.2 ICFELR
Nestes pacientes a terapêutica deve se pautar na manutenção do uso da terapia tripla otimizada associada ou não com a anticoagulação, seja ela plena ou profilática, (AMBROSY et al., 2014).
4.5.3 ICFE melhorada
Caracterizada por FEVE com aumento de 10% em pacientes com FEVE pregressa reduzida, atingindo taxas acima de 40%. Há indicação da manutenção da terapêutica modificadora de prognóstico utilizada no tratamento da ICFEr, (HOTTA et al., 2022).
4.5.4 ICFEP
Nestes pacientes devemos tratar as comorbidades tais como: hipertensão arterial sistêmica (HAS), FA e DAC para evitar a progressão da IC. Além disso, é necessário proceder a investigação de condições potencialmente reversíveis, como por exemplo, cardiomiopatias infiltrativas e restritivas. O uso de diuréticos está indicado para redução de sintomas, (SARTESCHI et al., 2019).
A ICA é uma doença responsável por grande número de internações e custos ao sistema de saúde. Seu tratamento precoce e de maneira padronizada reduz a morbimortalidade, melhorando a qualidade de vida do paciente, bem como sua sobrevida, (AGUIAR et al., 2022).
Portanto, o objetivo deste protocolo é o de uniformizar as condutas nos casos suspeitos de ICA. O protocolo será publicado em modo digital, em plataformas que facilitem o acesso pela equipe médica, de forma rápida e efetiva, no momento da avaliação do paciente com suspeita de ICA, (DUTRA; GOMES, 2023).
5 CONCLUSÃO/CONSIDERAÇÕES FINAIS
A ICA é uma doença responsável por grande número de internações e custos ao sistema de saúde. Seu tratamento precoce e de maneira padronizada reduz a morbimortalidade, melhorando a qualidade de vida do paciente, bem como sua sobrevida.
Portanto, o objetivo deste protocolo é o de uniformizar as condutas nos casos suspeitos de ICA. O protocolo será publicado em modo digital, em plataformas que facilitem o acesso pela equipe médica, de forma rápida e efetiva, no momento da avaliação do paciente com suspeita de ICA. A identificação e tratamento rápidos do risco imediato de morte são cruciais para a evolução prognóstica intra-hospitalar de pacientes com insuficiência cardíaca aguda (ICA). A presença de fatores de risco como insuficiência respiratória aguda, infarto agudo do miocárdio, choque cardiogênico, entre outros, torna um paciente elegível para uma vaga na UTI. O diagnóstico da ICA se baseia em sinais clínicos, anamnese detalhada e exames complementares.
Os sintomas mais comuns incluem tosse, dispneia, fadiga e edema periférico, com ortopneia e dispneia paroxística noturna sendo indicativos sensíveis e específicos. A classificação da ICA considera aspectos clínicos, tempo de evolução, disfunção ventricular, perfil hemodinâmico e classificação funcional. A avaliação por exames como radiografia de tórax, ecocardiograma transtorácico e níveis de peptídeo natriurético auxilia na confirmação do diagnóstico.
O manejo inicial envolve avaliação da via aérea, monitorização cardíaca, controle da congestão pulmonar, restrição hidrossalina e oxigenação adequada. O uso de medicamentos, como inibidores da enzima conversora de angiotensina (IECA), bloqueadores dos receptores de angiotensina (BRA), inibidores do receptor da angiotensina e neprisilina (INRA), betabloqueadores e outras terapias específicas, é crucial para reduzir os sintomas e melhorar o prognóstico.
A individualização do tratamento com base na situação clínica do paciente é essencial, considerando comorbidades, resposta aos medicamentos e potenciais interações medicamentosas. O papel do ecocardiograma transtorácico, dos exames laboratoriais e do monitoramento contínuo não pode ser subestimado na tomada de decisões terapêuticas adequadas.
Em última análise, a abordagem multidisciplinar, o diagnóstico preciso e a terapia personalizada são cruciais para melhorar a qualidade de vida e a sobrevida dos pacientes com insuficiência cardíaca aguda.
REFERÊNCIAS
COMITÊ COORDENADOR DA DIRETRIZ DE INSUFICIÊNCIA CARDÍACA. Diretriz Brasileira de Insuficiência Cardíaca Crônica e Aguda. Arq Bras Cardiol. 2018; 111(3):436-539
ACCORSI, T. A. D. et al. Emergências Relacionadas à Doença Valvar Cardíaca: Uma Revisão Abrangente da Abordagem Inicial no Departamento de Emergência. Arquivos Brasileiros de Cardiologia, v. 120, p. e20220707, 19 jun. 2023.
AGUIAR, Y. M. et al. Perfil epidemiológico das internações e óbitos por doenças cardiovasculares no nordeste do Brasil antes e durante a pandemia do Covid-19. Research, Society and Development, v. 11, n. 14, p. e590111436850, 7 nov. 2022.
ALBUQUERQUE, D. C. DE et al. I Registro Brasileiro de Insuficiência Cardíaca – Aspectos Clínicos, Qualidade Assistencial e Desfechos Hospitalares. Arquivos Brasileiros de Cardiologia, v. 104, p. 433–442, jun. 2015.
ALEXSANDER, R. et al. Análise Epidemiológica por Insuficiência Cardíaca no Brasil. Brazilian Medical Students, v. 6, n. 9, 12 abr. 2022.
AMBROSY, A. P. et al. The Global Health and Economic Burden of Hospitalizations for Heart Failure. Journal of the American College of Cardiology, v. 63, n. 12, p. 1123–1133, abr. 2014a.
AMBROSY, A. P. et al. The Global Health and Economic Burden of Hospitalizations for Heart Failure. Journal of the American College of Cardiology, v. 63, n. 12, p. 1123–1133, abr. 2014b.
BENJAMIN, E. J. et al. Heart Disease and Stroke Statistics—2018 Update: A Report From the American Heart Association. Circulation, v. 137, n. 12, 20 mar. 2018.
BERTOLETTI, O. Boas Práticas em Cardiologia – Uma Lição a Partir dos Indicadores de Desempenho. Arquivos Brasileiros de Cardiologia, v. 120, p. e20230033, 7 abr. 2023.
BUI, A. L.; HORWICH, T. B.; FONAROW, G. C. Epidemiology and risk profile of heart failure. Nature Reviews Cardiology, v. 8, n. 1, p. 30–41, jan. 2011.
CARDOSO, A. F. et al. Trombose Tardia de Prótese Biológica em Posição Mitral com Apresentação com Obstrução Significativa e Insuficiência Cardíaca Aguda. Arquivos Brasileiros de Cardiologia, v. 120, p. e20220481, 3 abr. 2023.
CORREIA, E. T. DE O.; MESQUITA, E. T. Novidades e Reflexões sobre o Tratamento Farmacológico da Insuficiência Cardíaca com Fração de Ejeção Preservada. Arquivos Brasileiros de Cardiologia, v. 119, p. 627–630, 12 set. 2022.
COUCEIRO, S. M. et al. Neuromodulação Vagal Auricular e sua Aplicabilidade em Pacientes com Insuficiência Cardíaca e Fração de Ejeção Reduzida. Arquivos Brasileiros de Cardiologia, v. 120, p. e20220581, 15 maio 2023.
CRUZ, I. O. et al. Telemonitoramento da Insuficiência Cardíaca – A Experiência de um Centro. Arquivos Brasileiros de Cardiologia, v. 118, p. 599–604, 7 fev. 2022.
DANZMANN, L. C. et al. Sobrevida em 10 Anos de Pacientes com Insuficiência Cardíaca com FEVE 40-59%: Uma Classificação Fenotípica Viável? Arquivos Brasileiros de Cardiologia, v. 120, p. e20210772, 13 fev. 2023.
DUTRA, G.; GOMES, B. A Relação NUS/Cr Confere Pior Prognóstico em Todos os Espectros de Fração de Ejeção? Arquivos Brasileiros de Cardiologia, v. 120, p. e20230107, 7 abr. 2023.
FONTES-CARVALHO, R.; LEITE-MOREIRA, A. Insuficiência cardíaca com fração de ejeção preservada: combater equívocos para uma nova abordagem. Arquivos Brasileiros de Cardiologia, v. 96, n. 6, p. 504–514, jun. 2011.
GROSSMAN, G. Cardiologia Nuclear na Otimização da Terapia de Ressincronização: Quo Vadis? Arquivos Brasileiros de Cardiologia, v. 120, p. e20230136, 7 abr. 2023.
HEIDENREICH, P. A. et al. 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure. Journal of the American College of Cardiology, v. 79, n. 17, p. e263–e421, maio 2022.
HOTTA, V. T. et al. Análise Crítica e Limitações do Diagnóstico de Insuficiência Cardíaca com Fração de Ejeção Preservada (ICFEp). Arquivos Brasileiros de Cardiologia, v. 119, p. 470–479, 11 jul. 2022.
KANG, Y. et al. Relação entre a Razão Nitrogênio Ureico/Creatinina e Prognóstico de Insuficiência Cardíaca em Todo o Espectro da Fração de Ejeção. Arquivos Brasileiros de Cardiologia, v. 120, p. e20220427, 3 abr. 2023.
KOTECHA, D. et al. Heart Failure With Preserved Ejection Fraction and Atrial Fibrillation. Journal of the American College of Cardiology, v. 68, n. 20, p. 2217–2228, nov. 2016.
MCDONAGH, T. A. et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. European Heart Journal, v. 42, n. 36, p. 3599–3726, 21 set. 2021.
MCMURRAY, J. J. V. et al. Angiotensin–Neprilysin Inhibition versus Enalapril in Heart Failure. New England Journal of Medicine, v. 371, n. 11, p. 993–1004, 11 set. 2014.
MOZAFFARIAN, D. et al. Heart Disease and Stroke Statistics—2016 Update: A Report From the American Heart Association. Circulation, v. 133, n. 4, 26 jan. 2016.
NEVES, A. P. L. et al. Lesão miocárdica e complicações cardiovasculares na COVID-19: estudo de coorte em pacientes graves e críticos. Revista Brasileira de Terapia Intensiva, v. 34, p. 443–451, 3 mar. 2023.
OLIVEIRA, G. M. M. D. et al. Estatística Cardiovascular – Brasil 2021. Arquivos Brasileiros de Cardiologia, v. 118, n. 1, p. 115–373, 19 jan. 2022.
PETERSEN, L. C. et al. Sobrevida de Pacientes com Insuficiência Cardíaca Aguda e Fração de Ejeção Intermediária em um País em Desenvolvimento – Estudo de Coorte no Sul do Brasil. Arquivos Brasileiros de Cardiologia, v. 116, n. 1, p. 14–23, 27 jan. 2021.
PONIKOWSKI, P. et al. Heart failure: preventing disease and death worldwide: Addressing heart failure. ESC Heart Failure, v. 1, n. 1, p. 4–25, set. 2014.
PONIKOWSKI, P. et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC)Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. European Heart Journal, v. 37, n. 27, p. 2129–2200, 14 jul. 2016.
RIBEIRO, A. L. P. et al. Cardiovascular Health in Brazil: Trends and Perspectives. Circulation, v. 133, n. 4, p. 422–433, 26 jan. 2016.
ROSSI NETO, J. M.; CASADEI, C.; FINGER, M. A. Revista SOCESP – INSUFICIÊNCIA CARDÍACA AGUDA. Disponível em: <https://socesp.org.br/revista/edicoes/revista-socesp-v30-n2-2020-30-2/insuficiencia-cardiaca-aguda-761/>. Acesso em: 26 ago. 2023.
SÁNCHEZ-MARTELES, M.; RUBIO GRACIA, J.; GIMÉNEZ LÓPEZ, I. Fisiopatología de la insuficiencia cardiaca aguda: un mundo por conocer. Revista Clínica Española, v. 216, n. 1, p. 38–46, jan. 2016.
SARTESCHI, C. et al. Predictors of Post-Discharge 30-Day Hospital Readmission in Decompensated Heart Failure Patients: Predictors of post-discharge 30-day readmission. International Journal of Cardiovascular Sciences, 2019.
WRITING COMMITTEE MEMBERS et al. 2016 ACC/AHA/HFSA Focused Update on New Pharmacological Therapy for Heart Failure: An Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America. Circulation, v. 134, n. 13, 27 set. 2016.
1Discente do Curso Superior de Medicina do Centro Universitário Uninassau, Campus Barreiras – BA e-mail: analuiso@icloud.com
2 Discente do Curso Superior de Medicina do Centro Universitário Uninassau, Campus Barreiras – BA e-mail: axelipe@gmail.com
3 Discente do Curso Superior de Medicina do Centro Universitário Uninassau, Campus Barreiras – BA e-mail: brunoangelo06@hotmail.com
4 Docente do Curso Superior de Medicina do Centro Universitário Uninassau, Campus Barreiras – BA. e-mail: dudu_lins7@hotmail.com
5 Docente do Curso Superior de Medicina do Centro Universitário Uninassau, Campus Barreiras – BA. e-mail: profajulianaleles@gmail.com
