INCIDENCE OF LEUKEMIA IN DOWN SYNDROME PATIENTS
REGISTRO DOI: 10.5281/zenodo.11107129
Andrielle Lima Do Nascimentoa, Laryssa Cavalcante de Sousa Silvab, Talita da Silva Souzac, Orientadora: Renata Ruoco Loureirod.
RESUMO
A Síndrome de Down (SD) é uma condição genética caracterizada pela presença de um cromossomo extra, resultando em três cópias do cromossomo 21. Essa alteração ocorre devido a um erro na distribuição dos cromossomos durante a divisão celular dos gametas. Por outro lado, a Leucemia Linfoide Aguda (LLA) é um tipo de câncer sanguíneo que se desenvolve na medula óssea, afetando os linfócitos, células brancas do sangue. A relação entre a leucemia e a SD tem sido constantemente analisada, e as causas que levam as crianças com SD a desenvolverem leucemia em uma frequência maior do que aquelas sem essa alteração cromossômica têm sido objeto de estudo. Estatísticas mostram que aproximadamente 1 em cada 150 crianças com SD serão diagnosticadas com leucemia, enquanto somente uma em cada 3.500 crianças sem essa síndrome desenvolverá a doença. O primeiro estudo sobre a associação entre a SD e a leucemia foi conduzido há mais de 75 anos. Desde então a literatura afirma que, aproximadamente 90% dos casos, são identificadas mutações no gene GATA1, cuja função desempenha um papel importante na hematopoiese, especialmente na formação de eritrócitos e plaquetas.
Descritores: Síndrome de Down, Leucemia, GATA1, criança.
ABSTRACT
Down Syndrome is a genetic condition characterized by the presence of an extra chromosome, resulting in three copies of chromosome 21. This alteration occurs due to an error in the distribution of chromosomes during the cell division of gametes. On the other hand, Acute Lymphoid Leukemia (ALL) is a type of blood cancer that develops in the bone marrow, affecting lymphocytes, white blood cells. The relationship between leukemia and Down’s Syndrome has been constantly analyzed, and the causes that lead children with Down’s Syndrome to develop leukemia at a higher rate than those without this chromosomal alteration have been the subject of study. Statistics show that approximately one in 150 children with Down’s Syndrome will be diagnosed with leukemia, while only one in 3,500 children without this syndrome will develop the disease. The first study on the association between Down Syndrome and leukemia was conducted more than 75 years ago. Since then, the literature states that in approximately 90% of cases, mutations are identified in the GATA1 gene, which plays an important role in hematopoiesis, especially in the formation of erythrocytes and platelets.
Descriptors: Down Syndrome, Leukemia, GATA1, child.
INTRODUÇÃO
Acredita-se que a trissomia do cromossomo 21 seja um fator predisponente ao câncer, uma vez que muitas crianças com Síndrome de Down (SD) já nascem com uma condição conhecida como Leucemia Transitória ou Doença Megaloblástica Transitória, sendo a incidência de Leucemia Linfoblástica Aguda (LLA) cerca de 33 vezes mais elevada nesta população 1,2..
A Leucemia é um tipo de câncer maligno que atinge os leucócitos e a SD é a trissomia do cromossomo 21, ambas são ligadas à causas genéticas 1, 2.
A relação entre essas patologias é as mutações no gene GATA1 que estão identificadas em 90% dos casos de Síndrome de Down. Esse gene é um fator de transcrição de células do sangue essencial na maturação dos eritrócitos, megacariócitos, eosinófilos e mastócitos e está localizado no cromossomo X. Sua associação com o cromossomo extra e mutação ocasiona a perda de capacidade de transcrição, o que impulsiona os estudos sobre a relação dessas patologias1.
O objetivo do trabalho é analisar a relação entre a Síndrome de Down e o desenvolvimento de leucemia em crianças, investigando os fatores genéticos, biológicos e clínicos que contribuem para essa maior suscetibilidade
JUSTIFICATIVA
O tema deste trabalho foi selecionado devido a uma curiosidade desenvolvida em conjunto e o interesse de dissertar entre a alteração genética de crianças com SD e a leucemia, de modo que a literatura sobre o tema é escassa.
MÉTODOS
Foi utilizado o método de revisão de literatura, utilizando livros e as bases de dados SciELO e PubMed, a plataforma Google Acadêmico também foi consultada para coleta de artigos, foram coletados preferencialmente artigos entre os anos 2000 e 2023, com a extração de informações de artigos sobre o que é SD, quais as suas características, o que é leucemia, qual tipo acomete o SD, ensaios clínicos etc.
DESENVOLVIMENTO
O que é Síndrome de Down
O termo “síndrome” significa um conjunto de sinais e sintomas observáveis e “Down” é o sobrenome do médico pediatra inglês John Langdon Down, que realizou a primeira descrição da síndrome em 18663,4. Em seu estudo, a fim de caracterizar etnicamente os tipos de deficiências mentais, John classificou como “idiotia mongólica” pessoas com fissura palpebral obliqua, baixa estatura, déficit intelectual e nariz plano3,4. Down acreditava que a condição que agora chamamos de SD era um retorno a um tipo racial mais primitivo, ao reconhecer nas crianças afetadas uma aparência oriental, Down criou o termo “mongolismo” e chamou a condição, inadequadamente de “idiota mongolóide”3,4. Hoje sabe-se que as implicações raciais são incorretas e por essa razão e por causa das conotações étnicas negativas dos termos mongol, mongolóide e mongolismo, devem ser evitados3,4.
Em 1958, Jérôme Lejeune e sua equipe descobriram a presença do cromossomo 21 extra nas pessoas com SD classificando assim como uma alteração genética, que até então eram descritas apenas por suas características físicas5.
Síndrome de Down (SD) ou trissomia do cromossomo 21 é uma cromossopatia, onde ocorre uma alteração genética causada pela presença de um cromossomo a mais, onde o paciente apresenta três cromossomos 215. Essa alteração é caracterizada por um erro na distribuição dos cromossomos nas células durante a divisão celular dos gametas, acarretando embriões acometidos5. As pessoas acometidas com essa alteração possuem assim 47 cromossomos em suas células ao invés de 46 5.
Há descrito na literatura três tipos de trissomia do cromossomo 21 (SD), que não implicam no grau de desenvolvimento das pessoas acometidas, com exceção do mosaicismo que, por não afetar todas as células, apresentando um menor comprometimento no desenvolvimento global do indivíduo, por tratar-se de um caso pouco expressivo6. A trissomia simples acomete cerca de 95% dos casos de SD, e resulta da não-disjunção do par 21 que ocorre no momento da divisão celular, conforme ilustrado na figura 16

O mosaicismo acomete cerca de 2% dos casos de pacientes com SD, ocorre quando o indivíduo apresenta dois materiais genéticos distintos, comprometendo assim apenas parte das células, sendo assim algumas células possuem 46 cromossomos e outras 47; conforme modelo ilustrado na figura 26
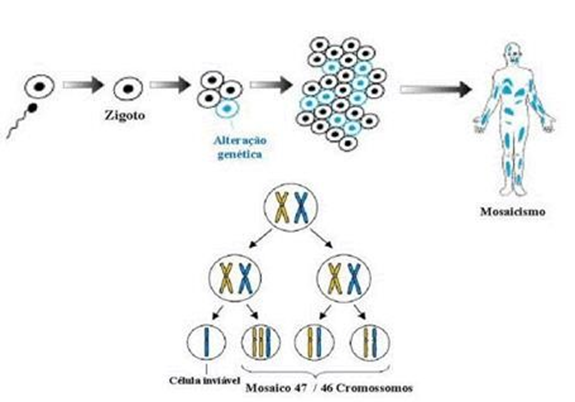
A translocação, que também é pouco expressiva acomete cerca de 2% dos casos de pacientes com SD, o cromossomo extra do par 21 fica “grudado” em outro cromossomo e, apesar do indivíduo ter 46 cromossomos, ele se torna portador da SD. Diante dos três casos descritos este é o único caso em que a SD pode ser hereditária9.
Os indivíduos afetados pela SD sofrem atrasos cognitivos e podem apresentar também alguns problemas genéticos3; tais como anomalias digestivas com o estreitamento duodenal, constipação, hipotonia muscular, cardiopatias congênitas, sinusite, bronquite, asma crônica, extremidades encurtadas, com mãos e pés chatos, Doença de Alzheimer; calcificação de gânglio basal e epilepsia e hipotireoidismo3.
As pessoas com SD apresentam também alguns traços típicos3; como cabelo liso e fino, olhos com linha ascendente e dobras da pele nos cantos internos, nariz pequeno e um pouco “achatado”, rosto arredondado, orelhas pequenas, baixa estatura, pescoço curto e grosso, flacidez muscular, mãos pequenas com dedos curtos, prega palmar única, o sistema imunológico um pouco debilitado e uma maior tendência a desenvolver câncer, mais especificamente a leucemia, que ocorre porque 1 em cada 150 crianças com SD desenvolvem problemas na produção dos leucócitos, as células responsáveis por combater vírus e bactérias no organismo. Nos primeiros três anos de vida, a leucemia mielóide aguda (LMA) é a forma mais comum. Depois, aproximadamente 80% dos casos são de leucemia linfocítica (LLA)3.
Diagnóstico de Síndrome de Down (SD)
O diagnóstico da SD, pode ser realizado ainda durante a gestação, entre os métodos utilizados está o ultrassom morfológico, que é capaz de rastrear possíveis marcadores como a transluscência nucal (realizado entre 11 e 14 semanas de gestação); o NIPT é um teste utilizado durante o pré natal, sendo um método não invasivo, realizado através da coleta de sangue para avaliar os riscos de algumas alterações cromossômicas; o cariótipo com banda G , é um teste genético capaz de diagnosticar alterações cromossômicas, realizado por meio de fotografia dos cromossomos que compõe o DNA humano, podendo ser feito a partir de qualquer célula que contenham um núcleo (principalmente os linfócitos); o PGT-A, realizado através da análise de uma amostra de DNA nas células embrionárias pela técnica de amplificação completa do genoma (WGA) e sequenciamento de nova geração na plataforma ION Torrent; a Biópsia de Vilo Corial (BVC) é um procedimento invasivo realizado através da coleta de fragmentos da placenta, esse exame é realizado a partir de 12 semanas de gestação, também pode ser realizado a amniocentese (ambos exames são realizados apenas quando os marcadores de transluscência nucal é maior a 3,5 mm, quando existe risco de cromossomopatias já identificada em exames não invasivos e malformação fetal já identificada na ecografia) (ThermoFisher) 9.
Leucemia e definições
A leucemia é uma patologia hematopoiética caracterizada pela proliferação desordenada e bloqueio maturativo das células de origem mieloides ou granulocíticas da medula óssea10,13,14. Sendo o resultado de alterações citogenéticas associadas a possíveis fatores que a predispõe como: fatores genéticos e congênitos, radiações, agentes químicos e fármacos (como benzeno e agentes alquilantes), vírus oncogênicos (human T-lymphotropic vírus type I [HTLV-I] causando leucemia das células T do adulto), hábitos individuais prejudiciais à saúde, convívio em situações de estresse ou de queda de resistência física, exposição frequente a substâncias tóxicas e a predisposição de adquirir doenças virais10,14.
Para fins didáticos e diagnóstico, as leucemias são classificadas conforme o tipo celular envolvido, grau de maturação da célula e características citogenéticas, classificandoas como mielóide e linfocítica e níveis agudo e crônico. 10,14.
A leucemia mieloide aguda (LMA) é caracterizada pelo crescimento desordenado dos blastos que são as células jovens de origem mieloide representando cerca de 15-20% de diagnóstico da infância e 80% de adultos11,13. É categorizada desde LMA-M0 até LMA-M7 de acordo com a classificação imunofenotípica das características da população blástica em maior volume13.
Já a leucemia mieloide crônica (LMC) possui células alteradas que funcionam apropriadamente, resultando em um curso inicial da doença ameno, entretanto, a maioria dos pacientes passam pela fase acelerada que sucede o aumento de blastos na medula óssea e no sangue periférico11. É adquirida pela presença de uma mutação onde ocorre translocação recíproca e balanceada entre os braços longos dos cromossomos 9 e 22, intitulado como cromossomo Philadelphia (Ph) 10,11,15.
A leucemia linfoide aguda (LLA) é descrita como a produção descontrolada de blastos de características linfoide, ocorrendo o acúmulo de células jovens, bloqueando a produção normal de glóbulos vermelhos, brancos e plaquetas11,16.
A doença acomete, em sua maioria, crianças menores de 15 anos com pico de incidência dos dois aos cinco anos de idade16,17. Os fundamentos sobre as causas da LLA podem ser uma soma de fatores, como danos cromossômicos secundários à exposição por agentes químicos ou físicos, informações genéticas virais transmitidas às células progenitoras susceptíveis e o que está sendo evidenciado neste trabalho através de pesquisas bibliográficas: Anormalidades genéticas hereditárias, como SD que pode predispor a LLA17.
Os sinais e sintomas da LLA são muito parecidos aos da LMA, como perda de massa corporal, anemia, neutropenia, trombocitopenia e infiltração dos tecidos por células, vômitos e dor de cabeça sugestivos de envolvimento do sistema nervoso 11,16,17.
A leucemia linfoide crônica (LLC) constituem-se em linfócitos B previamente expostos a antígenos, ou seja, provavelmente imunocompetentes12. É mais frequente em pacientes de faixa etária elevada18.
É uma doença clinicamente heterogênea, onde existem dois extremos de prognóstico18. Um tardo que durante muitos anos pode ser controlado com pouco ou nenhum tratamento e outro apresenta rápida evolução, e de difícil controle terapêutico12. Para esse tipo de caracterização de risco desta doença é por marcadores, que têm forte implicações na evolução e no tipo de tratamento a ser escolhido18.
Leucemia em pacientes portadores de Síndrome de Down (SD)
Crianças com SD têm uma probabilidade maior de desenvolver leucemia em comparação as crianças não portadoras da síndrome19. As alterações genéticas estão altamente correlacionadas com a incidência de casos de Leucemia19. De acordo com a literatura, esse prognóstico se deve a uma fusão que inclui a porção 5’ do gene TEL no cromossomo 12 e a região codificante do gene AML1 no cromossomo 21, onde essa fusão inibe a atividade transcricional medida por AML1, resultando em alteração na capacidade de diferenciação e reestruturação das células hematopoiéticas19.
As razões para esse risco elevado não são completamente compreendidas, mas algumas hipóteses incluem: alterações genéticas: a trissomia do cromossomo 21 em si pode levar a alterações genéticas adicionais que aumentam o risco de leucemia, contribuindo diretamente e funcionalmente para a sua transformação maligna19; suscetibilidade imunológica: a SD pode afetar o sistema imunológico, tornando os indivíduos mais suscetíveis a infecções e possivelmente ao desenvolvimento de leucemia20; exposição a fatores ambientais: alguns fatores ambientais, como exposição a produtos químicos tóxicos ou radiação, podem desempenhar um papel no desenvolvimento da leucemia em pessoas com SD20. As células precursoras hematopoiéticas também podem ser uma das causas que levam a incidência de leucemia nesses pacientes, onde através da hematopoiese ocorre a maturação das células sanguíneas23. Neste momento, existe um processo regulado por uma expressão coordenada de fatores de transcrição, os quais são ativados ou inibidos em casos normais23. No caso de intercorrências ou desregulação nesse processo as células sanguíneas são alteradas, ocasionando mudanças em suas funções e podendo gerar uma transformação maligna23.
Em cerca de 90% dos casos observam-se mutações no gene GATA1, gene que desempenha um papel crítico na produção de células sanguíneas, especificamente na formação de glóbulos vermelhos (eritrócitos) e plaquetas20. O gene GATA1 codifica uma proteína chamada fator de transcrição GATA1s, que regula a expressão de outros genes envolvidos na diferenciação e maturação das células sanguíneas devido a isso, esse gene pode desempenhar um papel na predisposição de indivíduos com SD a certos distúrbios sanguíneos, como a leucemia, esse distúrbio ocorre conforme o modelo apresentado na figura 320.
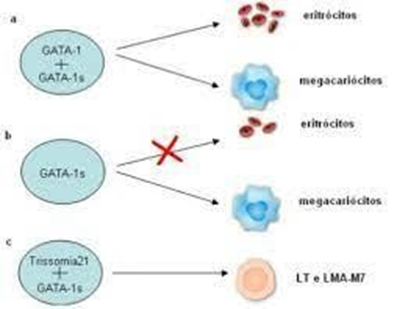
Também existem os casos de Leucemia Transitória da Síndrome de Down (LT-SD), que consiste em uma forma rara de leucemia que afeta principalmente crianças com SD, sendo considerada uma complicação especifica dessa condição genética24. Doença mieloproliferativa de carácter transitório e com mielopoese anormal em recém-nascidos portadores de SD24.
Seus sintomas geralmente incluem anemia, infecções recorrentes, fadiga, palidez, distúrbios de coagulação com sangramento, insuficiência cardíaca e até mesmo derrames24. O diagnóstico pode ser realizado mediante imunofenotipagem de sangue periférico, pois na LT-SD pode haver uma contagem elevada de células megacarioblásticas24. Além disso, os níveis de hemoglobina e plaquetas podem estar diminuídos24. Em grande parte dos casos à leucemia transitória desaparece nos primeiros meses de vida e a maioria dos portadores são assintomáticos, entretanto em alguns essa doença pode avançar para a morte fetal ou perinatal24.
Os resultados no tratamento da leucemia nestes pacientes têm gerado avanço significativo e mostra um nível de recuperação semelhantes aos pacientes sem SD21. Entretanto as intercorrências e morbidade associadas a quimioterapia se mostra maior nos pacientes com SD devido a maior incidência de toxicidades em casos de LLA SD 21.
CONSIDERAÇÕES FINAIS
A associação dentre a SD e leucemia é crucial para que os pacientes portadores de SD sejam monitorados de perto para detectar precocemente qualquer sinal de leucemia, levando melhor gerenciamento na percepção dos sintomas como fadiga persistente, infecções recorrentes e sangramento fácil e condução de diagnósticos como exame de sangue, imunofenotipagem, mielograma e entre outros.
Diante do quadro é importante aumentar a conscientização sobre o assunto entre profissionais de saúde, famílias e cuidadores. Isso pode levar a uma detecção mais precoce e a um melhor gerenciamento da condição, melhorando assim os resultados para os pacientes.
O entendimento dos mecanismos subjacentes à associação entre SD e leucemia continua a ser uma área de pesquisa ativa. Novos avanços na genética e na biologia molecular podem eventualmente levar a estratégias de prevenção mais eficazes ou tratamentos direcionados para essa população de pacientes.
Referências bibliográficas
- Lyra YC, Leite JB. ASSOCIAÇÃO ENTRE LEUCEMIA E SÍNDROME DE DOWN: REVISÃO SISTEMÁTICA. Rev. Saber Digital [Internet]. 22º de janeiro de 2020 [citado 28º de abril de 2024];12(2):77-90. Disponível em: https://revistas.faa.edu.br/SaberDigital/article/view/795.
- VIANA. R. C. et al. leucemia linfoblástica aguda em crianças com síndrome de down: uma revisão da literatura sobre os aspectos biológicos e genéticos, Revista Eletrônica da Fainor, Vitória da Conquista, v.8, n.2, p.66-78, jul./dez. 2015
- SIEGFRIED, 1993, p. 48 e 49.
- Moreira, Lília MA, El-Hani, Charbel N e Gusmão, Fábio AF. A síndrome de Down e sua patogênese: considerações sobre o determinismo genético. Brazilian Journal of Psychiatry
- Rev. AMRIGS ; 57(1): 5-8, jan.-mar. 2013. taArtigo em Português | LILACS | ID: lil686150Biblioteca responsável.
- SIEGFRIED, 1993, p. 48 e 49.
- Genética Thompson & Thompson.
- FAMERP,2006.
- Shwartzman, J. S.(2003) Síndrome de Down. São Paulo: Memnon/ Mackenzie.
- MMF dos Santos, GP de Jesus, LP Ferreira, R Ferreira – 2019 – portal.unisepe.com.br
- N Hamerschlak – Jornal de Pediatria, 2008 – SciELO Brasil.
- Garicochea B. Patogênese da leucemia linfóide crônica. Rev Bras Hematol Hemoter [Internet]. 2005Oct;27(4):241–6. Available from: https://doi.org/10.1590/S151684842005000400005.
- Martins SLR, Falcão RP. A importância da imunofenotipagem na Leucemia Mielóide Aguda. Rev Assoc Med Bras [Internet]. 2000Jan;46(1):57–62. Available from: https://doi.org/10.1590/S0104-42302000000100009.
- Silva GC da, Pilger DA, Castro SM de, Wagner SC. Diagnóstico laboratorial das leucemias mielóides agudas. J Bras Patol Med Lab [Internet]. 2006Apr;42(2):77–84. Available from: https://doi.org/10.1590/S1676-24442006000200004.
- Bollmann PW, Giglio A del. Chronic myeloid leukemia: past, present, future. einstein (São Paulo) [Internet]. 2011Apr;9(2):236–43. Available from: https://doi.org/10.1590/S167945082011RB2022.
- Cavalcante MS, Santana Rosa IS, Torres F. Leucemia linfoide aguda e seus principais conceitos. Rev Cient Fac Educ e Meio Ambient [Internet]. 15º de dezembro de 2017 [citado 28º de abril de 2024];8(2):151-64. Disponível em: https://revista.unifaema.edu.br/index.php/Revista-FAEMA/article/view/578.
- Leite EP, Muniz MTC, Azevedo A da CAC de, Souto FR, Maia ÂCL, Gondim CM da F, et al.. Fatores prognósticos em crianças e adolescentes com Leucemia Linfóide Aguda. Rev Bras Saude Mater Infant [Internet]. 2007Oct;7(4):413–21. Available from: https://doi.org/10.1590/S1519-38292007000400009.
- Barros JC. Leucemia linfocítica crônica & visão geral. Rev Bras Hematol Hemoter [Internet]. 2009Jul;31(4):215–. Available from: https://doi.org/10.1590/S151684842009000400003.
- (Chauffaille M de LLF. LLA em portadores de Síndrome de Down e TEL/AML1(ETV6/RUNX1). Rev Bras Hematol Hemoter [Internet]. 2009;31(5):305–6).
- (WEBB, D. K. H. Optimizing Therapy for Myeloid Disorders of Down Syndrome. British Journal of Haematology v. 131, p. 3-7, 2005).
- (Maloney KW. Acute lymphoblastic leukaemia in children with Down syndrome: an updated review. Br J Haematol. 2011).
- (DA SILVA P. H. et al. Hematologia laboratorial: Teoria e Procedimentos. 1ª ed. São Paulo: Artmed, 2015).
- (Hematology, Transfusion and Cell Therapy, v.45, Supplement 4, 2023).
- https://repositorio.uniceub.br/jspui/bitstream/prefix/13068/1/21506932.pdf.
a: Graduanda do curso de Biomedicina do Centro Universitário das Faculdades Metropolitanas Unidas – FMU/Brasil.
b: Graduanda do curso de Biomedicina do Centro Universitário das Faculdades Metropolitanas Unidas – FMU/Brasil.
c: Graduanda do curso de Biomedicina do Centro Universitário das Faculdades Metropolitanas Unidas – FMU/Brasil.
d: Orientadora, Biomédica, Docente de Biomedicina do Centro Universitário das Faculdades Metropolitanas Unidas – FMU/Brasil.
