COMPARATIVE STUDY OF THE SIDE EFFECTS OF CANNABIDIOL AND OTHER DRUGS IN THE TREATMENT OF EPILEPSY OF THE DRAVET SYNDROME TYPE
ESTUDIO COMPARATIVO DE LOS EFECTOS SECUNDARIOS DEL CANNABIDIOL Y OTRAS DROGAS EN EL TRATAMIENTO DE LA EPILEPSIA TIPO SÍNDROME DE DRAVET
REGISTRO DOI: 10.69849/revistaft/cl10202411171227
Igor da Silva Oliveira1
Vanessa Kelly Amador Ramos2
Sleimann Augusto El souki Cerbino3
George Luiz Pereira Dias4
Fábio José Coelho de Souza Júnior5
Daniel Carvalho de Meneses
Resumo
Introdução. A Síndrome de Dravet é uma doença neurológica complexa que inicia nos primeiros meses de vida, devido uma mutação no genes SCN1A; Essa síndrome é farmacorresistente e precisa de medicamentos específicos para que não haja agravo no desenvolvimento das crianças. O canabidiol é um fitocanabinoides extraído da planta Cannabis Sativa que age como modulador no sistema endocanabinoide. Objetivo. Comparar os fármacos convencionais com o canabidiol, seus efeitos colaterais e a qualidade de vida dos pacientes depois do uso do Canabidiol. Método. Trata-se de uma revisão integrativa da literatura. As fontes utilizadas foram: Pubmed, ScienceDirect e SCIELO. As buscas foram pelos descritores: Canabidiol, Síndrome de Dravet, epilepsia, mutação no gene SCN1A, eficácia do CBD, mecanismo de ação, fármacos convencionais. Resultados. Dos 64 artigos selecionados, 26 tiveram como resultado a diminuição significativa da frequência das crises, 6 não obtiveram resultados favoráveis do uso do canabidiol no tratamento de epilepsia, 12 apresentaram como resultado a longo prazo a eficácia do uso, 12 apresentaram como resultado o benefício do uso do canabidiol em crianças com Síndrome de Dravet, e 8 apresentaram uma melhora na qualidade de vida Conclusão. é notório o avanço significativo que o canabidiol vem trazendo para os pacientes com Síndrome de Dravet, devolvendo a qualidade de vida tanto para os paciente, quanto aos seus cuidadores. Mas é necessário que mais estudos sejam desenvolvidos, principalmente a longo prazo.
Unitermos. Epilepsia; efeitos colaterais; canabidiol
Abstract
Introduction: Dravet Syndrome is a complex neurological disorder that begins in the first months of life due to a mutation in the SCN1A gene. This syndrome is pharmacoresistant and requires specific medications to prevent worsening in the development of these children. Cannabidiol is a phytocannabinoid extracted from the Cannabis sativa plant that acts as a modulator in the endocannabinoid system. Objective: To compare conventional drugs with cannabidiol, their side effects, and the quality of life of patients after using cannabidiol. Method: This is an integrative literature review. The sources used were PubMed, ScienceDirect, and SCIELO. The searches were conducted using the descriptors: Cannabidiol, Dravet Syndrome, epilepsy, SCN1A gene mutation, CBD efficacy, mechanism of action, conventional drugs. Results: Of the 64 selected articles, 26 reported a significant reduction in seizure frequency; 6 did not yield favorable results regarding the use of cannabidiol in epilepsy treatment; 12 showed long-term efficacy of cannabidiol use; 12 reported benefits of cannabidiol use in children with Dravet Syndrome; and 8 indicated an improvement in quality of life. Conclusion: There is significant progress that cannabidiol has brought to patients with Dravet Syndrome, improving the quality of life for both patients and their caregivers. However, more studies, especially long-term, need to be conducted.
Keywords: Epilepsy; side effects; cannabidiol.
Resumen.
Introducción. El Síndrome de Dravet es una enfermedad neurológica compleja que comienza en los primeros meses de vida, debido a una mutación en el gen SCN1A. Este síndrome es farmacorresistente y necesita medicamentos específicos para evitar un deterioro en el desarrollo de estos niños. El cannabidiol es un fito cannabinoide extraído de la planta Cannabis Sativa que actúa como modulador en el sistema endocannabinoide. Objetivo. Comparar los fármacos convencionales con el cannabidiol, sus efectos secundarios y la calidad de vida de los pacientes después del uso del cannabidiol. Método. Se trata de una revisión integrativa de la literatura. Las fuentes utilizadas fueron: Pubmed, ScienceDirect y SCIELO. Las búsquedas se realizaron con los descriptores: Cannabidiol, Síndrome de Dravet, epilepsia, mutación en el gen SCN1A, eficacia del CBD, mecanismo de acción, fármacos convencionales. Resultados. De los 64 artículos seleccionados, 26 mostraron una disminución significativa en la frecuencia de las crisis, 6 no obtuvieron resultados favorables del uso del cannabidiol en el tratamiento de la epilepsia, 12 presentaron como resultado a largo plazo la eficacia del uso, 12 evidenciaron el beneficio del uso del cannabidiol en niños con Síndrome de Dravet, y 8 mostraron una mejora en la calidad de vida. Conclusión. Es notable el avance significativo que el cannabidiol ha traído para los pacientes con Síndrome de Dravet, devolviendo la calidad de vida tanto a los pacientes como a sus cuidadores. Sin embargo, es necesario que se realicen más estudios, especialmente a largo plazo.Unitermos. Epilepsia; efectos secundarios; cannabidiol.
INTRODUÇÃO
A epilepsia é uma doença neurológica que causa crises convulsivas, conhecidas como crises epilépticas, que consequentemente interfere no desenvolvimento cognitivo, psicológico, motor e neurológico (Beghi; Giussani, 2018). De acordo com a Organização Mundial da Saúde (OMS), aproximadamente 50 milhões de pessoas em todo o mundo são portadoras dessa doença, no entanto, em grande maioria se encontram em países desenvolvidos (OMS, 2024)
Dentre os vários tipos de epilepsia, destaca-se a Síndrome de Dravet, também conhecida como Epilepsia Mioclônica Grave da Infância. Essa síndrome é rara e grave, acometendo crianças nos primeiros meses de vida. O tratamento é realizado com medicamentos, porém, na maioria dos casos, os fármacos convencionais não têm se mostrado eficazes (Scheffer et al., 2019).
A Síndrome de Dravet é classificada como uma encefalopatia epiléptica devido às frequentes convulsões que comprometem o neurodesenvolvimento da criança. Portanto as crises podem ser classificadas como clônicas, tônicas-clônicas, mioclônica generalizadas ou fragmentadas, tônicas e não convulsivas, e em todos os estágios, elas não respondem ao tratamento medicamentoso e vem acompanhada por distúrbios de comportamento, hiperatividade, impulsividade e transtorno do espectro autista (Madan et al., 2021; Lagae et al., 2018).
A síndrome ocorre devido a mutações nos genes SCN1A (2q24.3), que codificam a subunidade alfa 1 uma proteína chamada canal de sódio voltagem-dependente (Shmuely et al., 2020). Essa proteína desempenha um papel crucial na formação do cérebro e, quando ocorrem alterações nesse gene, a comunicação entre os neurônios é perturbada. Esse desequilíbrio na função neuronal leva aos primeiros sinais da síndrome, que incluem convulsões febris, ou seja, causadas por mínima mudança de temperatura. No entanto, ao longo do tempo, as convulsões começam a ocorrer sem a presença de febre, manifestando-se como pequenos choques (Brunklaus et al., 2012).
As bases fisiopatológicas da síndrome de Dravet envolvem alterações no funcionamento dos canais de sódio presentes nos neurônios, a principal causa identificada em 80% dos pacientes com SD é uma mutação genética de novo (não herdadas) que codifica a subunidade alfa-1 do gene SCN1A do canal de sódio dependente de voltagem NAV 1.1. Esses canais são importantes para a excitabilidade de células como os neurônios, impactando no potencial de ação, resultando em disparos descontrolados nos neurônios do ácido gama-aminobutírico (GABAérgicos). O diagnóstico é feito clinicamente, e em casos de dúvida, testes genéticos são recomendados (Chopra P, Isom LL, 2014).
Essa disfunção dos canais de sódio leva a uma hiperexcitabilidade dos neurônios, interferindo na função de outros neurotransmissores, como o ácido gama-aminobutírico
(GABA) que é responsável por inibir a atividade dos neurônios, resultando nas convulsões características da síndrome de Dravet, atraso no desenvolvimento e problemas neurológicos associados (Hernandez et al ., 2017).
Os tratamentos geralmente recomendados para crises convulsivas incluem o uso de anticonvulsivantes como o valproato de sódio em primeira linha, seguido pelo estiripentol e clobazam como segunda linha e Canabidiol como terceira linha. Em casos em que essas opções não surtem resultados esperados, podem ser considerados medicamentos como topiramato e dieta cetogênica como quarta linha de tratamento (Devinsky et al., 2014). No entanto, é importante ressaltar que os resultados terapêuticos desses medicamentos podem ser insatisfatórios e ainda podem causar efeitos colaterais indesejáveis. Portanto, existe uma necessidade premente de novas abordagens terapêuticas que possam controlar de forma mais efetiva as crises convulsivas (Lagae et al., 2018).
A cannabis contém mais de 100 compostos químicos chamados de canabinoides, sendo o THC (tetra-hidrocanabinol) e o CBD (canabidiol) os mais conhecidos. O THC é responsável pelos efeitos psicoativos da maconha, enquanto o CBD não causa esses efeitos e tem sido amplamente estudado por seus potenciais efeitos medicinais; CBD e THC são dois fitocanabinoides mais estudados na planta da cannabis, que interagem com o sistema endocanabinoide do corpo humano (Shohami E et al., 2011).
O CBD, diferente do THC, é uma substância fitocanabinoide, não alucinógena, extraída principalmente das flores e folhas da planta e possui uma afinidade baixa pelos receptores canabinoides endógenos CB1 e CB2, atuando como um modulador alostérico negativo do receptor CB1 e como um antagonista/agonista inverso do receptor CB2, o que justifica em parte a ausência de efeitos psicoativos deste canabinoide e seus mecanismos de ação anticonvulsivantes, são amplamente estudados (Matos et al., 2017).
No Brasil, a planta foi trazida por escravos nas embarcações portuguesas em meados de 1500, esse período foi marcado pelo descobrimento do Brasil; e a disseminação desta planta se deu após os escravos apresentarem aos índios, aos quais passaram a cultivá-las . Em 1830 no Rio de Janeiro, houve a primeira proibição que tornou ilegal o uso da cannabis para qualquer fim; caso o contrário a pessoa séria presa por 3 dias, além de pagar multa ( Martins, 2023).
No entanto, foi no século XX que a utilização medicinal da cannabis começou a enfrentar desafios. Com a proibição global das drogas, principalmente a partir da Convenção Única sobre Entorpecentes de 1961, muitos países passaram a restringir severamente o uso da cannabis, inclusive para fins medicinais. Essa proibição afetou negativamente a pesquisa científica sobre os benefícios potenciais da planta e limitou o acesso das pessoas aos seus poderes terapêuticos. (Saad, 2013).
Mesmo com todas as diversidades que rondavam em torno da Cannabis Sativa medicinal, o cientista israelense Raphael Mechoulam, continuou a sua pesquisa e se tornou pioneiro na identificação e isolamento de dois principais compostos da cannabis, o THC (delta-9-tetrahidrocanabinol) que é uma substância classificada como psicoativo e o canabidiol (CBD), na década de 1960. Mechoulam também descobriu o sistema endocanabinoide no corpo humano, que é fundamental para a regulação de muitos processos fisiológicos (Matos et al., 2017).
O sistema endocanabinoide é dividido em duas classes, as endógenas que são os endocanabinoides produzidos pelo organismos e são responsáveis pelo controle das funções do organismo como o humor, dor e apetite e as exógenas chamados fitocanabinoides que são os canabinoides externos, como o THC e CBD dentre outros, presentes na planta Cannabis Sativa (Fonseca et al., 2013; Matos et al, 2017).
O mecanismo de ação dos canabinoides foi elucidado na década de 90 pelo Dr. Raphael Mechoulam, após a descoberta de 2 ligantes endógenos: Anandamida (ananda-que significa prazer) e a 2-AG (2-aeachidonoyl glicerol) são neurotransmissores que desempenham um grande papel no SNC (Shohami et al ., 2011).
Os canabinoides endógenos, como a anandamida e 2AG interagem com os receptores CB1 e CB2 resultando em uma variedade de efeitos farmacológicos. A anandamida é um agonista parcial do CB2, mas também se liga ao CB1, gerando efeitos analgésicos, ansiolíticos e antidepressivos; o 2-araquidonoilglicerol é um agonista total do receptor CB2 e suas ações modulam a plasticidade sináptica dos processos de aprendizagem e memória. A produção e degradação desses canabinoides são regulados por enzimas específicas GABA e Glutamato (Fonseca et al ., 2013).
A ativação dos receptores canabinoides leva à inibição da liberação de neurotransmissores excitatórios e à modulação da excitabilidade neuronal. Isso pode ter um impacto significativo na supressão da dor, já que o sistema endocanabinoide está envolvido na regulação da transmissão da dor e da excitabilidade neuronal (Fonseca, 2013).
Atentando para a problemática, o objetivo deste estudo é fazer uma análise comparativa dos efeitos colaterais dos fármacos de primeiras linhas, contrapondo ao uso terapêutico do CBD isolado. Tendo em vista que pacientes portadores dessa síndrome são farmacorresistentes ao tratamento medicamentoso convencional e analisar a eficácia e segurança do uso do Canabidiol, como forma terapêutica para o tratamento da Síndrome de Dravet; já que há um enfrentamento decorrentes da resistência aos fármacos utilizados atualmente; explorar os estudos clínicos sobre mudanças na qualidade de vida dessas crianças.
MÉTODO
Neste artigo, apresentamos uma revisão integrativa da literatura que consiste em uma pesquisa e análise ampla de estudos científicos, artigos, publicações e outros recursos relevantes relacionados aos medicamentos utilizados para a Síndrome de Dravet, seus efeitos adversos, com ênfase no tratamento terapêutico utilizando o Canabidiol. Essa pesquisa seguiu a organização a partir de uma adaptação das etapas descritas por Witthemore e Knaf (2005) e Donato (2019), conforme descrito abaixo.
Identificação do problema e formulação da questão da pesquisa.
Foi realizada uma busca em bases de dados através da estratégia PICO, representada na tabela 1.
Desenvolvimento da estratégia de pesquisa e identificação das fontes de dados.
Tabela 1 – Estratégia PICO e determinação da pergunta de pesquisa

A metodologia consiste em construir um protocolo de pesquisa, com definição dos objetivos e descritores a serem utilizados. Foi realizada uma busca em bases de dados como PUBMED, SCIELO e ScienceDirect, utilizando os descritores relacionados ao tema.
Os estudos encontrados foram avaliados quanto à sua relevância e adequação aos objetivos da pesquisa. Os estudos selecionados foram então analisados criticamente, considerando sua metodologia, resultados e conclusões, coletadas informações relevantes dos estudos selecionados, como dados demográficos, indicações terapêuticas, eficácia, efeitos colaterais, entre outros. Por fim, os dados foram organizados e sintetizados de forma a responder aos objetivos da pesquisa. Portanto, as pesquisas realizadas foram as seguintes:
Figura 1: Fluxograma da metodologia das pesquisas
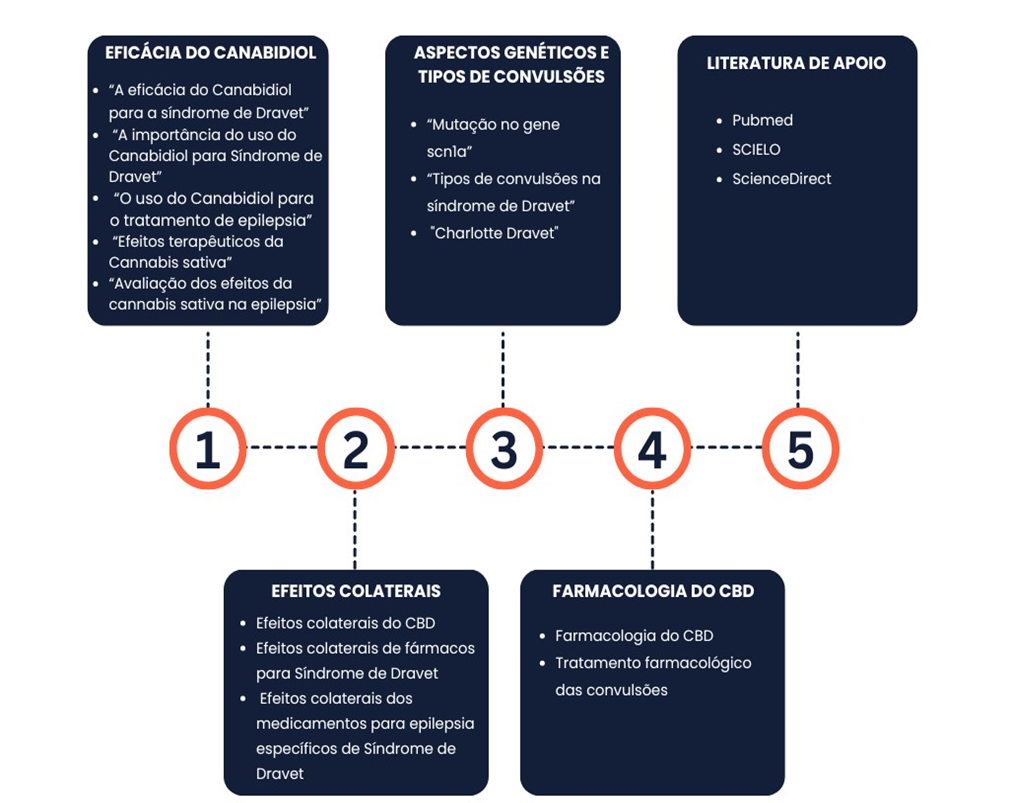
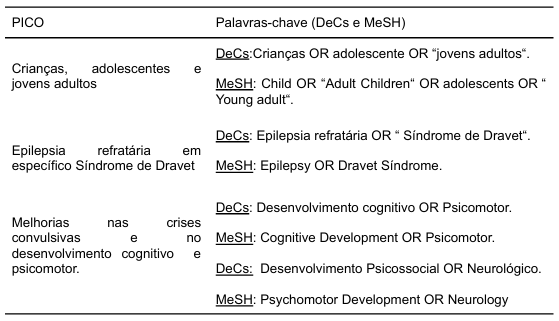
Tabela 2– Metodologia de busca de acordo e palavra-chave
Definição dos critérios de inclusão e exclusão de artigos.
Os artigos utilizados foram publicados no período entre 2010 a 2024, considerando os estudos escritos em português do Brasil, espanhol e inglês.
Essa metodologia foi utilizada com o objetivo de realizar uma pesquisa abrangente e atualizada sobre o uso do Canabidiol no tratamento da Síndrome de Dravet e seus efeitos terapêuticos, em artigos publicados na íntegra e levando em consideração estudos científicos nas bases de dados confiáveis e demais recursos relevantes no campo da saúde.
Coleta de dados, análise e apresentação dos resultados da revisão.
Para assegurar a robustez das conclusões, foi submetido os dados extraídos a uma análise de consistência, onde foi verificado a homogeneidade e a relevância das informações coletadas. Foi concedida atenção especial às limitações dos estudos analisados, bem como às implicações para pesquisas futuras.
RESULTADOS
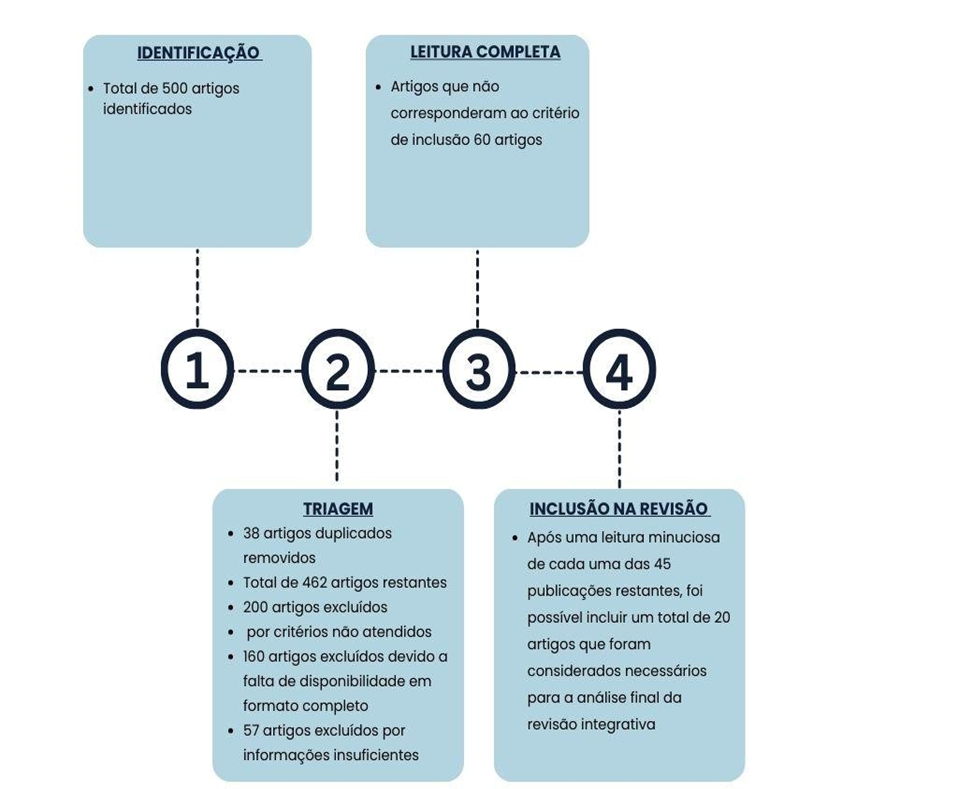
Na fase de Identificação, após uma busca extensiva nas bases de dados mais relevantes, com o objetivo de assegurar uma cobertura ampla e variada da literatura, coletamos um total de 500 artigos relacionados ao intuito da pesquisa, as estratégias de buscas resultaram na identificação de 300 publicações na base Pubmed, 150 na base ScienceDirect e 50 na base SCIELO; Essas publicações foram minuciosamente revisadas, e por concordância entre os revisores;
Além do mais, apenas foram considerados para esta análise estudos originais, revisões sistemáticas e meta-análises, a fim de assegurar a relevância e a atualidade dos dados. Durante a fase de seleção, uma triagem inicial foi realizada, que envolveu a leitura de títulos e resumos das publicações. Nesta etapa, foram descartados estudos que não atendiam aos critérios estabelecidos previamente. Como resultado, 38 publicações duplicadas foram removidas, deixando um total de 462 artigos como candidatos para a próxima fase de avaliação.
O processo de triagem foi rigoroso e contemplou a exclusão de artigos redundantes, aplicando criteriosamente os critérios de inclusão e exclusão, o que levou à eliminação de 200 publicações que não se adequaram aos padrões estabelecidos, com base na análise dos títulos e resumos; enquanto 160 foram afastados devido à falta de disponibilidade em formato completo acessível para revisão.
Outros 57 artigos foram eliminados por apresentarem informações insuficientes, como a ausência de dados empíricos relevantes para a pesquisa, revisões não sistemáticas e a falta de acesso ao texto completo. Registros que discutiam condições neurológicas distintas das de interesse, como esquizofrenia, epilepsia em geral e Parkinson, também foram excluídos do processo. Adicionalmente, documentos que apresentavam metodologias inadequadas ou que não forneciam informações suficientes para uma avaliação completa dos resultados foram considerados inelegíveis.
Por meio desse rigoroso processo de triagem, após uma leitura minuciosa de cada uma das 45 publicações restantes, foi possível incluir um total de 20 artigos que foram considerados necessários para a análise final da revisão integrativa, garantindo que a revisão abarcasse as publicações mais relevantes e significativas para o tema em questão.
Figura 2- Fluxograma do procedimento de escolha das produções
Diversos estudos têm relatado melhorias significativas nos sintomas relacionados à epilepsia após o uso de canabidiol. Por exemplo, um estudo conduzido por Devinsky et al. (2017) demonstrou que o uso de uma formulação de CBD resultou em uma redução considerável na frequência das crises em pacientes com síndromes epilépticas refratárias, como a síndrome de Dravet e a síndrome de Lennox-Gastaut. A pesquisa revelou que até 44% dos pacientes experimentaram uma redução de 50% ou mais na frequência das convulsões. Esses achados não apenas reforçam a eficácia do CBD, mas também destacam sua capacidade de melhorar a qualidade de vida dos pacientes.
Abaixo, apresentação em quadro demonstrativo de todos os artigos extraídos e selecionados para este trabalho.
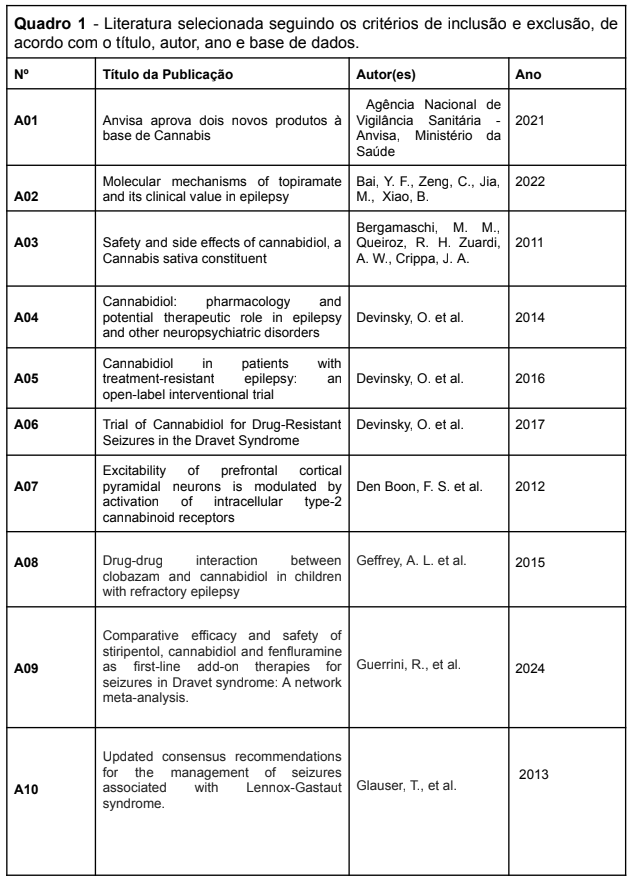
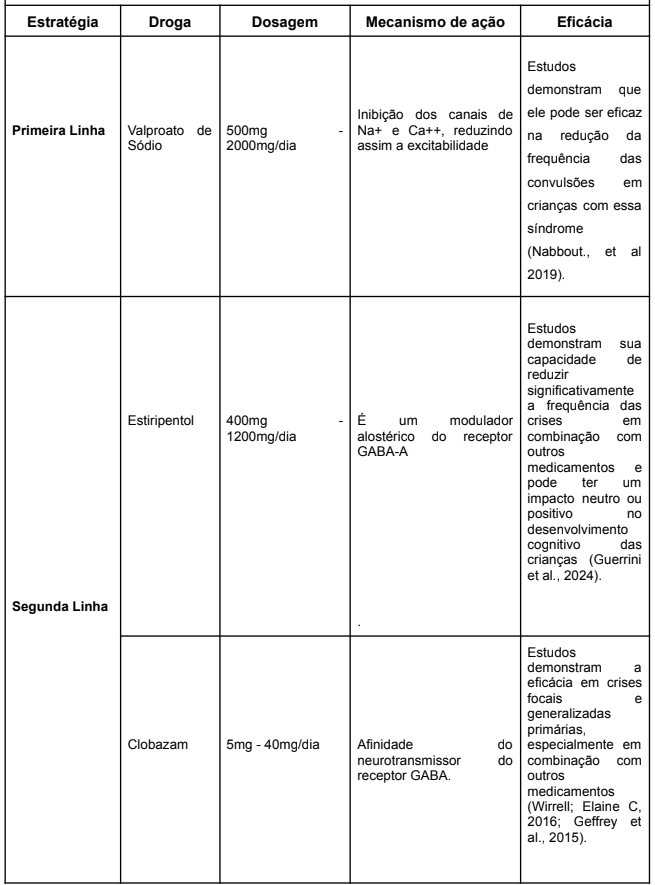
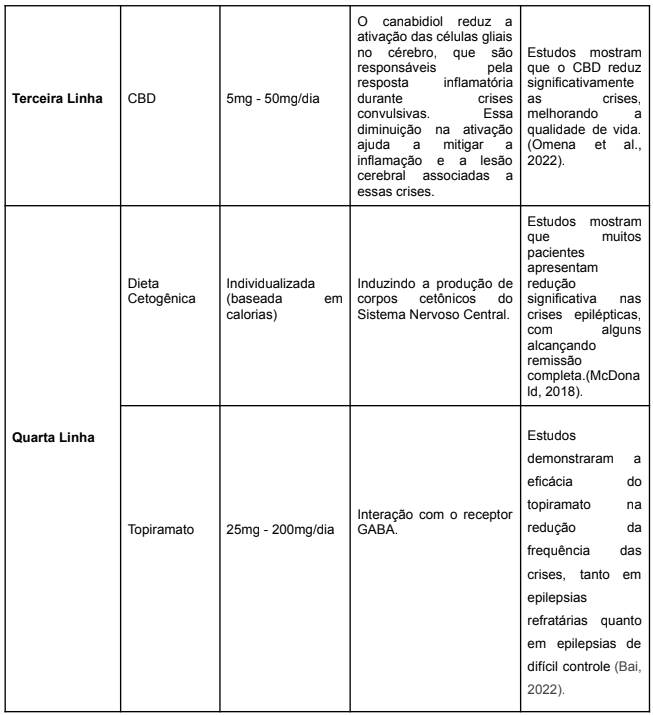
Eficácia clínica dos fármacos para Síndrome de Dravet
A análise da eficácia dos fármacos no tratamento da síndrome de Dravet, se torna cada vez mais criteriosa e expressa avanços significativos na abordagem terapêutica da condição por se tratar de uma síndrome complexa e devastadora.

No ensaio clínico duplo-cego conduzido por Devinsky et al. (2017), a evidência de uma redução significativa das convulsões em pacientes com epilepsia refratária em comparação com o placebo é crucial. Esse tipo de estudo é considerado o padrão ouro na pesquisa clínica, pois minimiza viés e oferece uma avaliação robusta da eficácia do tratamento. A validação de que o CBD pode reduzir a frequência das crises é um avanço significativo para pacientes que não respondem a outros tratamentos convencionais.
Complementar a essa perspectiva, a revisão sistemática e meta-análise realizada por Devinsky et al. (2014) revela um cenário mais amplo, abordando não apenas a epilepsia, mas também outras condições como ansiedade, dor crônica e inflamação. O auto-relato de melhora nos sintomas de ansiedade indica que o CBD pode ter um papel potencial na melhoria da qualidade de vida, além de sua função no controle das crises epilépticas. Essa multifuncionalidade do CBD sugere que ele poderia ser um recurso valioso na terapia de condições coexistentes, que frequentemente afetam pacientes com epilepsia.
O estudo de caso de Devinsky et al. (2016) focado na síndrome de Dravet, discorre sobre melhorias nas convulsões e no comportamento geral dos pacientes tratados com CBD. Este achado é particularmente importante, visto que a síndrome de Dravet é desafiadora no manejo clínico, e opções de tratamento eficazes são limitadas. A experiência positiva relatada sugere que o CBD pode oferecer esperança para famílias que enfrentam essa difícil condição.
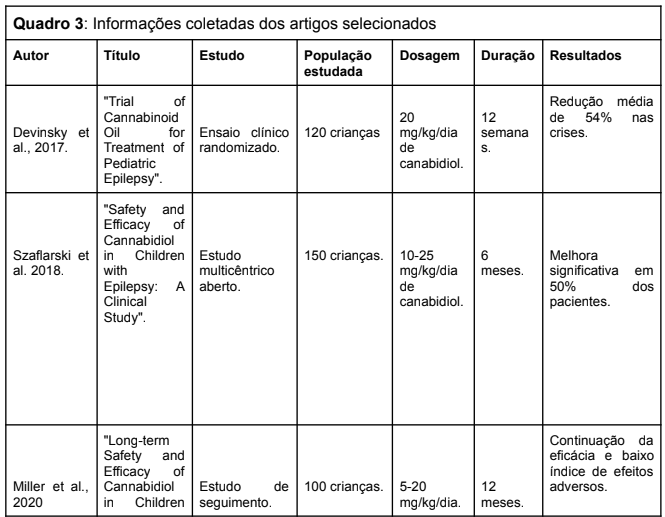

Tabela 3: Comparação dos efeitos colaterais do Canabidiol para com os fármacos convencionais.
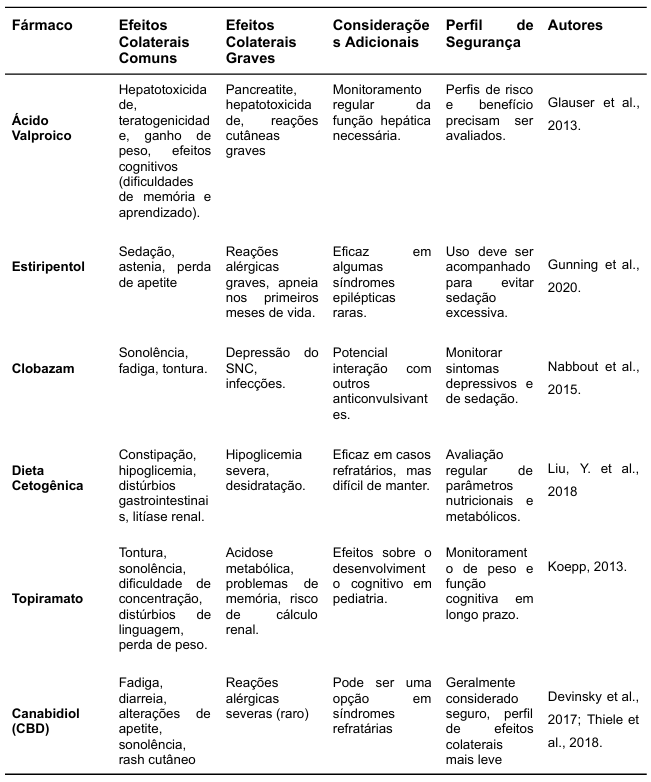
Esses estudos mostram que enquanto os fármacos anticonvulsivantes tradicionais podem estar associados a uma gama mais ampla de efeitos colaterais, o canabidiol tem um perfil de efeitos adversos que, em muitos casos, é considerado mais manejável.
DISCUSSÃO
A epilepsia refratária continua sendo um desafio significativo na prática clínica. Em um contexto onde os medicamentos antiepilépticos tradicionais muitas vezes apresentam limitações, seja pela ineficácia ou pelos efeitos colaterais adversos; o canabidiol (CBD) surge como uma alternativa promissora. A crescente evidência em torno da eficácia e do perfil de segurança do CBD chama a atenção para a necessidade de uma análise crítica sobre seu papel no manejo da epilepsia resistente a fármacos.
A eficácia dos tratamentos com fármacos convencionais não é uniforme, dependendo de fatores individuais e genéticos; o que reforça a necessidade de novas abordagens terapêuticas; A síndrome de Dravet é notoriamente refratária a muitos dos medicamentos antiepilépticos tradicionais (Thiele et al., 2019).
O Canabidiol é um composto farmacológico presente na planta Cannabis Sativa L, encontrada em alta concentração nas plantas fêmeas, essa substância é extraída das flores; não possui características psicoativas, por ter baixa afinidade com os receptores CB1 e CB2 ou seja, não age principalmente via receptor canabinoide, mas sim por diferentes mecanismos moleculares; por esse motivo o CBD não causa efeitos de alteração do estado mental. Além disso, o CBD apresenta baixa toxicidade e alta tolerabilidade em seres humanos, o que significa que é bem aceito pelo organismo e pode ser utilizado com segurança (Franco, 2021).
O mecanismo de ação do CBD é complexo e desafiador, mas envolve a inibição da enzima FAAH (amida hidrolase de ácidos graxos) responsável pela degradação do endocanabinoide anandamida. Isso resulta em um aumento dos níveis de anandamida, que é conhecida por ter efeitos analgésicos e anti-inflamatórios (Den Boon et al., 2012). O CBD é capaz de modular um efeito de um ligante ortostérico, agindo como um alostérico negativo do receptor CB1, diminuindo a ação de excitabilidade e como um antagonista/agonista inverso dos receptores CB2, bloqueando ou reduzindo a resposta aos impulsos desordenados. Isso significa que o CBD pode ativar esses receptores de maneira diferente da ação normal dos endocanabinoides, potencialmente produzindo efeitos anti-inflamatórios e imunomoduladores (Treves et al., 2021).
O CBD também pode atuar em outros sistemas de sinalização, como o receptor de serotonina 5-HT1A, envolvidos na modulação da ansiedade e da depressão, o que justifica suas propriedades ansiolíticas. É capaz, de ativar os receptores de vaniloides TRPV1, canais iônicos que integram vários estímulos nociceptivos, incluindo a dor e os reflexos protetores o que esclarece o efeito do CBD no alívio da dor e no receptor GPR5, ele atua também no CB1, através das micróglias que estão localizadas no SNC responsáveis por processo inflamatório, o CBD inibe transmissões sinápticas bloqueando canais de cálcio e potássio, reduzindo significativamente as crises convulsivas; Essa ação multifacetada do CBD pode contribuir para seus efeitos terapêuticos, incluindo redução da ansiedade, modulação da dor e potencial neuroprotetor (Gomes et al., 2012).
Estudos clínicos demonstraram que o Canabidiol pode reduzir significativamente a frequência e a gravidade das convulsões em pacientes com essas síndromes, melhorando sua qualidade de vida e proporcionando um maior controle dos sintomas (Hilal-Dandan, 2015).
Quanto às dosagens, a literatura sugere que o tratamento com CBD deve ser individualizado. A dosagem frequentemente utilizada em estudos varia, mas muitos indicam que doses eficazes podem ser alcançadas em intervalos que vão de 5 a 20 mg/kg/dia. Além disso, a forma de administração também pode influenciar a eficácia do tratamento. O uso de produtos com espectro completo (full spectrum), que contêm não apenas canabidiol, mas também outros canabinoides e terpenos, tem sido sugerido para potencializar os efeitos terapêuticos. O chamado “efeito entourage” sugere que a combinação dos componentes presentes na planta tem um impacto sinérgico, potencializando os benefícios e minimizando os efeitos adversos (Devinsky et al., 2017).
O Canabidiol está revolucionando o tratamento de convulsões refratárias, proporcionando uma nova esperança para pacientes e suas famílias. É um exemplo de como a pesquisa científica e a inovação farmacêutica podem trazer benefícios significativos para a saúde pública (Franco, 2021).
O estudo observacional de Porter et al. (2021) sobre pacientes em tratamento para dor crônica destaca a redução significativa do sono e da qualidade de vida ao iniciar o tratamento com CBD. Embora este estudo não se concentre exclusivamente na epilepsia, é importante destacar que muitos pacientes com epilepsia enfrentam não apenas as crises convulsivas, mas também a dor crônica e a sonolência, que podem ser efeitos colaterais decorrentes dos medicamentos utilizados no tratamento. Essa combinação de condições pode impactar significativamente a qualidade de vida desses indivíduos. Assim, a inclusão do CBD na abordagem terapêutica pode proporcionar um alívio adicional e uma melhora geral no bem-estar dos pacientes.
Em comparação com fármacos tradicionais, o CBD apresenta um perfil de segurança mais favorável. Embora os efeitos adversos do CBD possam incluir fadiga, diarreia e mudanças no apetite, sua gravidade é frequentemente menor do que os efeitos colaterais associados a antiepilépticos clássicos, que são conhecidos por induzir sérios comprometimentos funcionais ao longo do tratamento (Tzadok et al., 2022). Isso representa um ponto significativo ao considerar o tratamento a longo prazo.
Além disso, o CBD não parece causar efeitos colaterais graves, como intoxicação, dependência ou overdose. Em estudos pré-clínicos e clínicos, doses muito altas de CBD foram bem toleradas sem efeitos colaterais significativos; No entanto, é importante ressaltar que o CBD pode interagir com outros medicamentos, especialmente aqueles metabolizados pelo sistema enzimático do fígado. Portanto, é importante que os pacientes informem seus médicos sobre o uso de CBD para evitar interações medicamentosas indesejadas (Bergamaschi et al., 2011).
O organograma apresentado abaixo aborda os efeitos colaterais dos tratamentos para a Síndrome de Dravet. Ele está estruturado em quatro linhas de tratamento diferentes, cada uma com suas respectivas opções terapêuticas e os efeitos adversos associados.
Organograma 1: Drogas anticonvulsivantes para Síndrome de Dravet
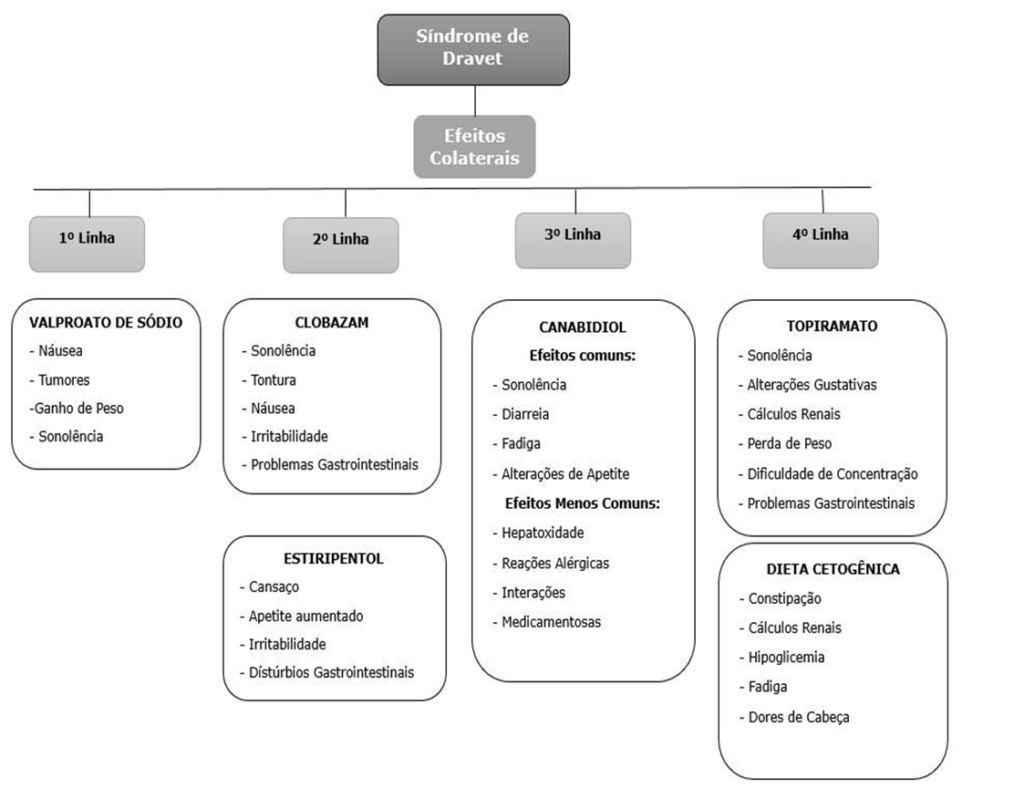
1ª Linha: Valproato de Sódio.
Os efeitos listados incluem náusea, tumores, ganho de peso e sonolência. O Valproato de Sódio é um anticonvulsivante comum, mas seu uso pode estar associado a sérios efeitos colaterais, exigindo monitoramento contínuo.
2ª Linha: Clobazam e Estiripentol.
Efeitos como, sonolência, tontura, náuseas, irritabilidade e problemas gastrointestinais são relatados; Ele é um benzodiazepínico utilizado frequentemente para manejo de crises, mas apresenta uma gama de efeitos colaterais que podem afetar a qualidade de vida do paciente e o Estiripentol é utilizado em associação a outros medicamentos, e seus efeitos podem impactar a adesão ao tratamento.
3ª Linha: Canabidiol.
Os efeitos comuns incluem sonolência, diarreia, fadiga e alteração do apetite, O Canabidiol é um dos principais tratamentos emergentes para epilepsias refratárias, mas seu uso pode resultar em efeitos adversos notáveis.
Efeitos Menos Comuns incluem hepatotoxicidade, reações alérgicas e interações medicamentosas. Esses efeitos, embora menos frequentes, exigem atenção devido ao potencial de comprometimento hepático.
4ª Linha: Topiramato e Dieta Cetogênica.
Topiramato, entre os efeitos colaterais estão sonolência, alterações gustativas, O Topiramato, um dos anticonvulsivantes mais utilizados, deve ser administrado com cautela devido à variedade de possíveis efeitos adversos.
Dieta Cetogênica, os efeitos colaterais associados incluem constipação, cálculos renais, hipoglicemia, fadiga e dores de cabeça. Essa dieta é frequentemente considerada para pacientes com epilepsia resistente a tratamentos convencionais, mas seus efeitos na saúde geral precisam ser monitorados.
Regulamentação do Canabidiol no Brasil
No Brasil, a regulamentação tem evoluído nos últimos anos. Em 2015, a Agência Nacional de Vigilância Sanitária (ANVISA) autorizou a importação de produtos à base de CBD para tratamento de epilepsia e outras condições de saúde. Em 2019, a ANVISA aprovou a resolução de n• 2.113 que permitiu o uso do medicamento, porém como uso terapêutico e sob prescrição médica, desde que contivessem uma concentração máxima de 0,2% de THC ou até mesmo o CBD isolado (Matos, 2017).
Essas regulamentações visam garantir o acesso seguro e legal ao Canabidiol para pacientes que se beneficiem do seu uso, ao mesmo tempo em que protegem contra a utilização abusiva ou recreativa da substância. Para que ocorra a importação do medicamento é necessário uma consulta médica, onde será prescrito o uso de Canabidiol; em seguida é necessário que seja feito o cadastro na ANVISA, preenchendo o formulário eletrônico e físico, declaração de responsabilidade válida por um ano (podendo ser renovado após expiração do prazo). Após o envio correto das documentações, cabe a ANVISA fazer a análise dos mesmo para autorizar a importação. Dada a presente aprovação, será enviada por e-mail a autorização para o produto, que deverá ser apresentado junto ao medicamento sempre que transportado. Esse importação pode ser feita por pessoa física ou intermediada a instituições correlacionadas a área da saúde, sendo proibida a importação para revenda no Brasil. A chegada do Canabidiol no Brasil é passada por fiscalização no aeroporto e sua retirada é permitida mediante a apresentação da receita médica, junto a autorização da ANVISA (Agência Nacional de Vigilância Sanitária).
A dosagem de canabidiol pode variar conforme a condição médica tratada, a resposta individual de cada paciente e a forma de uso. Geralmente, as doses iniciais de CBD podem variar de 5 a 10 mg por dia, podendo ser aumentadas gradativamente, conforme necessário e indicado por um profissional de saúde. A dosagem deve sempre ser orientada por um médico especializado, levando em consideração as particularidades e individualidade de cada paciente (Devinsky et al., 2014).
O canabidiol puro não contém tetrahidrocanabinol (THC), que é o principal canabinoide psicoativo da planta Cannabis. No entanto, muitos produtos no mercado brasileiro são formulados com extratos da planta inteira, que podem conter quantidades mínimas de THC. No Brasil, a legislação permite que produtos à base de canabidiol contenham até 0,2% de THC, o que, em geral, não é suficiente para provocar efeitos psicoativos.
O indicado para pacientes com Síndrome de Dravet é o CBD isolado, pois em um estudo de caso seriado, os pesquisadores observaram que o CBD é geralmente bem tolerado, com efeitos colaterais leves a moderados, o que é crucial considerando que muitos pacientes com síndrome de Dravet são crianças (Devinsky et al., 2016).
As análises realizadas indicam a importância em compreender os benefícios e riscos dos medicamentos tradicionais para que continuem a desempenhar um papel importante no tratamento das epilepsias fármacos resistente, levando sempre em consideração por outro, a crescente evidência sobre a eficácia e o perfil de segurança do canabidiol, por oferecer uma alternativa valiosa, especialmente para casos refratários. É imperativo que futuras pesquisas continuem a explorar o potencial do CBD em regimes de tratamento e comparem sistematicamente sua eficácia e segurança com os fármacos convencionais. A individualização do tratamento, que leva em conta tanto a resposta clínica quanto os efeitos colaterais, deve ser um princípio orientador na prática clínica, impulsionando avanços nas opções terapêuticas para pacientes que enfrentam epilepsia.
CONCLUSÕES
As informações colhida nos estudos apresentam um avanço significativo em pacientes com a Síndrome de Dravet ao utilizarem o CBD como um meio terapêutico, apesar das dificuldades enfrentadas pela não aceitação que perdura em alguns países, mas com a necessidade por um tratamento com menos efeitos colaterais, hoje é cada vez mais presente a inclusão do CBD principalmente em pacientes fármacos resistentes. Entretanto, a jornada de tratamento para esses pacientes é repleta de desafios, tanto no que diz respeito à aceitação social quanto à implementação clínica.
Os pacientes que convivem com a Síndrome de Dravet frequentemente enfrentam um cenário de dificuldades sociais e emocionais. A natureza imprevisível das convulsões pode limitar sua participação em atividades cotidianas e afetar seu desenvolvimento educacional e social. Além disso, o estigma associado às condições epilépticas pode levar a sentimentos de exclusão e solidão, impactando negativamente sua autoestima e bem-estar emocional.
Muitos pacientes com Síndrome de Dravet apresentam resistência aos tratamentos convencionais, o que pode levar a um sentimento de frustração e desespero, tanto para os pacientes quanto para os cuidadores. A alteração contínua das medicações na busca por um controle mais eficaz das crises pode promover uma sensação de instabilidade.
O sofrimento emocional também é um fator crítico. As convulsões frequentes podem ser uma fonte de estresse, e os pacientes podem experimentar ansiedade e depressão. O apoio psicológico é muitas vezes necessário, mas pode ser difícil de encontrar. As crises epilépticas podem levar a limitações em atividades cotidianas, como a prática de esportes, a participação em eventos escolares ou encontros sociais. Isso pode resultar em isolamento e dificuldades de interação social para a criança, além de preocupações constantes dos pais.
A qualidade de vida dos pacientes com Síndrome de Dravet, assim como de suas famílias, pode ser profundamente afetada por diversos fatores:
Como dependência de cuidado, embora muitas crianças precisam de atenção e acompanhamento constantes, o que pode sobrecarregar os cuidadores e criar estresse familiar. Isso pode limitar a liberdade e a qualidade de vida dos cuidadores. As dificuldades financeiras: O tratamento contínuo e os cuidados especiais geralmente implicam em custos elevados, que podem causar problemas econômicos nas famílias. A educação, as dificuldades de aprendizagem podem ser uma consequência das convulsões ou dos efeitos dos medicamentos. A falta de adequação nas escolas para lidar com as necessidades específicas dessas crianças pode resultar em um acesso limitado à educação de qualidade. A falta de acesso a tratamentos inovadores, embora existam terapias mais recentes, como a cannabis medicinal e outros medicamentos emergentes, nem sempre há acesso a essas opções, ou elas podem ser extremamente caras.
Diante desse cenário, é fundamental que haja uma maior conscientização sobre a Síndrome de Dravet e sobre os benefícios do uso do CBD, bem como a promoção de políticas de saúde que garantam não apenas o acesso a tratamentos apropriados, mas também o suporte psicológico e social para esses pacientes e suas famílias. Com um tratamento eficaz e a inclusão de suporte abrangente, é possível melhorar significativamente a qualidade de vida dessas pessoas, permitindo-lhes alcançar um desenvolvimento mais pleno e uma integração social mais satisfatória, e para que isso acontece de forma segura, é necessário um estudo a longo prazo do Canabidiol, para que ele não seja somente usado como forma terapêutica, e sim como um fármaco de primeira linha para Síndrome de Dravet. E que este medicamento possa chegar de forma gratuita em famílias em condições econômicas hipossuficientes.
Com base na análise realizada sobre a Síndrome de Dravet e o uso do CBD como uma estratégia terapêutica, pode-se afirmar que os objetivos deste trabalho foram, em grande parte, alcançados. A pesquisa demonstrou não apenas a eficácia potencial do canabidiol no controle das convulsões em pacientes resistentes a tratamentos convencionais, mas também iluminou as dificuldades enfrentadas por essas famílias no que se refere à aceitação social, ao estigma associado à epilepsia e à luta por acesso a cuidados adequados.
Portanto, ao enfatizar a relevância de conscientização e inclusão de apoio abrangente, este estudo contribui para um melhor entendimento da Síndrome de Dravet e propõe caminhos concretos para a melhoria da qualidade de vida desses pacientes. A integração do CBD como uma terapia de primeira linha e seu acesso gratuito para famílias de baixa renda também aparece como um objetivo desejável e necessário, evidenciando uma necessidade premente de mudança nas políticas de saúde. Em resumo, o trabalho não apenas elucidou a situação atual, mas também apresentou propostas concretas para o avanço no tratamento e a promoção do bem-estar dos pacientes e de suas famílias
REFERÊNCIAS
- Agência Nacional de Vigilância Sanitária – Anvisa. Anvisa aprova dois novos produtos à base de Cannabis (endereço na internet). Ministério da Saúde, 2021(Acessado em: 23/09/2024). Disponível em:https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2021/anvisa-registra-doisnovos-produtos-a-base-de-cannabis
- Bai, Y. F., Zeng, C., Jia, M., & Xiao, B. (2022). Molecular mechanisms of topiramate and its clinical value in epilepsy. Seizure, 98, 51–56. https://doi.org/10.1016/j.seizure.2022.03.024
- Bergamaschi, M. M., Queiroz, R. H., Zuardi, A. W., & Crippa, J. A. (2011). Safety and side effects of cannabidiol, a Cannabis sativa constituent. Current drug safety,6(4), 237–249. https://doi.org/10.2174/157488611798280924
- Bergamaschi, M. M., Queiroz, R. H., Chagas, M. H., de Oliveira, D. C., De Martinis, B. S., Kapczinski, F., Quevedo, J., Roesler, R., Schröder, N., Nardi, A. E., Martín-Santos, R., Hallak, J. E., Zuardi, A. W., & Crippa, J. A. (2011). Cannabidiol reduces the anxiety induced by simulated public speaking in treatment-naïve social phobia patients. Neuropsychopharmacology : official publication of the AmericanCollege of Neuropsychopharmacology, 36(6), 1219–1226. https://doi.org/10.1038/npp.2011.6
- Beghi, E., & Giussani, G. (2018). Aging and the Epidemiology of Epilepsy. Neuroepidemiology, 51(3-4), 216–223. https://doi.org/10.1159/000493484
- Brunklaus, A., Ellis, R., Reavey, E., Forbes, G. H., & Zuberi, S. M. (2012). Prognostic, clinical and demographic features in SCN1A mutation-positive Dravet syndrome. Brain : a journal of neurology, 135(Pt 8), 2329–2336. https://doi.org/10.1093/brain/aws151
- Chopra, R., & Isom, L. L. (2014). Untangling the dravet syndrome seizure network: the changing face of a rare genetic epilepsy. Epilepsy currents, 14(2), 86–89. https://doi.org/10.5698/1535-7597-14.2.86
- Devinsky, O., Cilio, M. R., Cross, H., Fernandez-Ruiz, J., French, J., Hill, C., Katz, R., Di Marzo, V., Jutras-Aswad, D., Notcutt, W. G., Martinez-Orgado, J., Robson, P. J., Rohrback, B. G., Thiele, E., Whalley, B., & Friedman, D. (2014). Cannabidiol: pharmacology and potential therapeutic role in epilepsy and other neuropsychiatric disorders. Epilepsia, 55(6), 791–802. https://doi.org/10.1111/epi.12631
- Devinsky, O., Marsh, E., Friedman, D., Thiele, E., Laux, L., Sullivan, J., Miller, I., Flamini, R., Wilfong, A., Filloux, F., Wong, M., Tilton, N., Bruno, P., Bluvstein, J., Hedlund, J., Kamens, R., Maclean, J., Nangia, S., Singhal, N. S., Wilson, C. A., … Cilio, M. R. (2016). Cannabidiol in patients with treatment-resistant epilepsy: an open-label interventional trial. The Lancet. Neurology, 15(3), 270–278. https://doi.org/10.1016/S1474-4422(15)00379-8
- Devinsky, O., Cross, J. H., & Wright, S. (2017). Trial of Cannabidiol for Drug-Resistant Seizures in the Dravet Syndrome. The New England journal of medicine, 377(7), 699–700. https://doi.org/10.1056/NEJMc1708349
- Den Boon, F. S., Chameau, P., Schaafsma-Zhao, Q., van Aken, W., Bari, M., Oddi, S., Kruse, C. G., Maccarrone, M., Wadman, W. J., & Werkman, T. R. (2012). Excitability of prefrontal cortical pyramidal neurons is modulated by activation of intracellular type-2 cannabinoid receptors. Proceedings of the National Academy ofSciences of the United States of America, 109(9), 3534–3539. https://doi.org/10.1073/pnas.1118167109
- Franco, V., Bialer, M., & Perucca, E. (2021). Cannabidiol in the treatment of epilepsy: Current evidence and perspectives for further research. Neuropharmacology, 185, 108442.https://doi.org/10.1016/j.neuropharm.2020.108442
- Fonseca, B. M., Costa, M. A., Almada, M., Correia-da-Silva, G., & Teixeira, N. A. (2013). Endogenous cannabinoids revisited: a biochemistry perspective. Prostaglandins & other lipid mediators, 102-103, 13–30. https://doi.org/10.1016/j.prostaglandins.2013.02.002
- Fonseca, B. M., Costa, M. A., Almada, M., Soares, A., Correia-da-Silva, G., & Teixeira, N. A. (2013). O Sistema Endocanabinóide–uma perspetiva terapêutica. Acta Farmacêutica Portuguesa, 2(2), 37-44.Available from. Citado em. 20 de set 2024. Disponivel em:https://actafarmaceuticaportuguesa.com/index.php/afp/article/view/5/105
- Gomes, F. V., Reis, D. G., Alves, F. H., Corrêa, F. M., Guimarães, F. S., & Resstel, L. B. (2012). Cannabidiol injected into the bed nucleus of the stria terminalis reduces the expression of contextual fear conditioning via 5-HT1A receptors. Journal of psychopharmacology (Oxford, England), 26(1), 104–113. https://doi.org/10.1177/0269881110389095
- Geffrey, A. L., Pollack, S. F., Bruno, P. L., & Thiele, E. A. (2015). Drug-drug interaction between clobazam and cannabidiol in children with refractory epilepsy. Epilepsia, 56(8), 1246–1251. https://doi.org/10.1111/epi.13060
- Glauser, T., Ben-Menachem, E., Bourgeois, B., et al. . “Updated consensus recommendations for the management of seizures associated with Lennox-Gastaut syndrome.” Epilepsia, vol.54, n3, pág 397-403, 2013.
- Guerrini, R., Chiron, C., Vandame, D., Linley, W., & Toward, T. (2024). Comparative efficacy and safety of stiripentol, cannabidiol and fenfluramine as first-line add-on therapies for seizures in Dravet syndrome: A network meta-analysis. Epilepsia open, 9(2), 689–703. https://doi.org/10.1002/epi4.12923
- Gunning, B., et al. “Scottish Epilepsy Research Group. Stiripentol effect on patients with drug-resistant epilepsy.” Seizure, vol. 78, pág. 33-37, 2020.
- Hernandez, C. C., Kong, W., Hu, N., Zhang, Y., Shen, W., Jackson, L., Liu, X., Jiang, Y., & Macdonald, R. L. (2017). Altered Channel Conductance States and Gating of GABAA Receptors by a Pore Mutation Linked to Dravet Syndrome. eNeuro, 4(1), ENEURO.0251-16.2017. https://doi.org/10.1523/ENEURO.0251-16.2017
- Hilal-Dandan, R., & Brunton, L. (2015). Manual de farmacologia e terapêutica deGoodman & Gilman. AMGH Editora. Disponível em.https://books.google.com.br/books?hl=pt-BR&lr=&id=ofidBgAAQBAJ&oi=fnd&pg=PT2&dq=Manual+de+farmacologia+e+terap%C3%AAutica+de+Goodman+%26+Gilman&ots=TfO8wqmepx&sig=KnBAt57bZVpti1fFRRtpBs4pCA8#v=onepage&q=Manual%20de%20farmacologia%20e%20terap%C3%AAutica%20de%20Goodman %20%26%20Gilman&f=false
- Koepp, M. J. “Topiramate.” Pharmacological Reviews, vol. 65, n.3, pág 723-745, 2013.
- Lagae, L., Brambilla, I., Mingorance, A., Gibson, E., & Battersby, A. (2018). Quality of life and comorbidities associated with Dravet syndrome severity: a multinational cohort survey. Developmental medicine and child neurology, 60(1), 63–72. https://doi.org/10.1111/dmcn.13591
- LIU, Y., et al. “The ketogenic diet for the treatment of epilepsy: A systematic review.” Neurotherapeutics, vol.15, n.4, pág. 823-835, 2018.
- Madan Cohen, J., Checketts, D., Dunayevich, E., Gunning, B., Hyslop, A., Madhavan, D., Villanueva, V., Zolnowska, M., & Zuberi, S. M. (2021). Time to onset of cannabidiol treatment effects in Dravet syndrome: Analysis from two randomized controlled trials. Epilepsia, 62(9), 2218–2227. https://doi.org/10.1111/epi.16974
- MATOS, R. L., Spinola, L. A., Barboza, L. L., Garcia, D. R., França, T. C., & Affonso, R. S. (2017). O uso do canabidiol no tratamento da epilepsia. RevistaVirtual de Química,9(2),786814.http://static.sites.sbq.org.br/rvq.sbq.org.br/pdf/v9n2a24.pdf
- Martins, D. D. A., & Posso, I. D. P. (2023). Legislação atual sobre cannabis medicinal. Histórico, movimentos, tendências e contratendências no território brasileiro. BrJP.https://doi.org/10.5935/2595-0118.20230026-pt
- Miller, I., Scheffer, I. E., Gunning, B., Sanchez-Carpintero, R., Gil-Nagel, A., Perry, M. S., Saneto, R. P., Checketts, D., Dunayevich, E., Knappertz, V., & GWPCARE2 Study Group (2020). Dose-Ranging Effect of Adjunctive Oral Cannabidiol vsPlacebo on Convulsive Seizure Frequency in Dravet Syndrome: A Randomized Clinical Trial. JAMA neurology, 77(5), 613–621. https://doi.org/10.1001/jamaneurol.2020.0073
- McDonald, Tanya J W, and Mackenzie C Cervenka. “Ketogenic Diets for Adult Neurological Disorders.” Neurotherapeutics : the journal of the American Society forExperimental NeuroTherapeutics vol. 15,4 (2018): 1018-1031. doi:10.1007/s13311-018-0666-8
- Nabbout, R., et al. “Clobazam: a review of its efficacy and safety in children with epilepsy.” Expert Opinion on Pharmacotherapy, vol. 16, n.6, pág. 853-865, 2015.
- OMENA, Beatriz Lucas et al. A eficácia do canabidiol no tratamento da Epilepsia. Research, Society and Development, v. 11, n. 16, p. e71111638057-e71111638057, 2022.
- Porter, B., Marie, B. S., Milavetz, G., & Herr, K. (2021). Cannabidiol (CBD) Use by Older Adults for Acute and Chronic Pain. Journal of gerontological nursing, 47(7), 6–15. https://doi.org/10.3928/00989134-20210610-02
- Shmuely, S., Surges, R., Helling, R. M., Gunning, W. B., Brilstra, E. H., Verhoeven, J. S., Cross, J. H., Sisodiya, S. M., Tan, H. L., Sander, J. W., & Thijs, R. D. (2020).Cardiac arrhythmias in Dravet syndrome: an observational multicenter study. Annals of clinical and translational neurology, 7(4), 462–473. https://doi.org/10.1002/acn3.51017
- Shohami, E., Cohen-Yeshurun, A., Magid, L., Algali, M., & Mechoulam, R. (2011).Endocannabinoids and traumatic brain injury. British journal of pharmacology, 163(7), 1402–1410. https://doi.org/10.1111/j.1476-5381.2011.01343.x
- Scheffer, I. E., & Nabbout, R. (2019). SCN1A-related phenotypes: Epilepsy and beyond. Epilepsia, 60 Suppl 3, S17–S24. https://doi.org/10.1111/epi.16386
- Saad, L. G. (2013). ” Fumo de negro”: a criminalização da maconha no Brasil (c.1890-1932). Citado em: 10/05/2024. Disponivel em: https://repositorio.ufba.br/handle/ri/13691
- Szaflarski, J. P., Bebin, E. M., Cutter, G., DeWolfe, J., Dure, L. S., Gaston, T. E., Kankirawatana, P., Liu, Y., Singh, R., Standaert, D. G., Thomas, A. E., Ver Hoef, L. W., & UAB CBD Program (2018). Cannabidiol improves frequency and severity of seizures and reduces adverse events in an open-label add-on prospective study.Epilepsy & behavior : E&B, 87, 131–136. https://doi.org/10.1016/j.yebeh.2018.07.020
- Thiele, E., Marsh, E., Mazurkiewicz-Beldzinska, M., Halford, J. J., Gunning, B., Devinsky, O., Checketts, D., & Roberts, C. (2019). Cannabidiol in patients with Lennox-Gastaut syndrome: Interim analysis of an open-label extension study. Epilepsia, 60(3), 419–428. https://doi.org/10.1111/epi.14670
- Thiele, E. A., et al. “Cannabidiol in Patients with Drug-Resistant Epilepsy: The Expanded Access Investigative Study.” Epilepsy & Behavior, vol. 86, pág. 131-135, 2018.
- Treves, N., Mor, N., Allegaert, K., Bassalov, H., Berkovitch, M., Stolar, O. E., & Matok, I. (2021). Efficacy and safety of medical cannabinoids in children: a systematic review and meta-analysis. Scientific reports, 11(1), 23462. https://doi.org/10.1038/s41598-021-02770-6
- Tzadok, M., Hamed, N., Heimer, G., Zohar-Dayan, E., Rabinowicz, S., & Ben Zeev, B. (2022). The Long-Term Effectiveness and Safety of Cannabidiol-Enriched Oil in Children With Drug-Resistant Epilepsy. Pediatric neurology, 136, 15–19. https://doi.org/10.1016/j.pediatrneurol.2022.06.016
- Wirrell E. C. (2016). Treatment of Dravet Syndrome. The Canadian journal of neurological sciences. Le journal canadien des sciences neurologiques, 43 Suppl 3, S13–S18. https://doi.org/10.1017/cjn.2016.249
- 37.ORGANIZAÇÃO MUNDIAL DA SAÚDE. Epilepsia. Genebra: Organização Mundial da Saúde, 2024 (Acessado: 01/09/2024). Disponível em:(https://www.who.int/mental_health/management/epilepsy/en/);. Acesso em: 29 set. 2024.
- Whittemore, R., & Knafl, K. (2005). The integrative review: updated methodology.Journal of advanced nursing, 52(5), 546–553. https://doi.org/10.1111/j.1365-2648.2005.03621.x45.
- Wirrell, E. C., Hood, V., Knupp, K. G., Meskis, M. A., Nabbout, R., Scheffer, I. E., Wilmshurst, J., & Sullivan, J. (2022). International consensus on diagnosis and management of Dravet syndrome. Epilepsia, 63(7), 1761–1777. https://doi.org/10.1111/epi.17274
1Graduando em Biomedicina, Faculdade Cosmopolita. Belém-PA, Brasil. Orcid: https://orcid.org/0009-0003-1462
2Graduanda em Biomedicina, Faculdade Cosmopolita. Belém-PA, Brasil. Orcid: https://orcid.org/0009-0006-3626-5424
3Graduado em Biomedicina
4Graduado em Administração, com habilitação em sistema de informação, especialista em Gestão de T.i e mestre de administração
5Formado pela universidade federal do Pará Mestre em farmacologia pela universidade de São Paulo Doutorando em farmacologia – bioquímica pela universidade federal do Pará
