REGISTRO DOI: 10.69849/revistaft/ni10202503270717
Letícia Dos Santos De Lima; Maria Isabel Do Nascimento De Carvalho; Thainá De Jesus Almeida Fernandes; Orientador: Rafaella De Carvalho Cardoso
1. Resumo
Este trabalho aborda a eficácia dos bioestimuladores de colágeno no tratamento da lipodistrofia ginóide (celulite), uma condição multifatorial que afeta principalmente mulheres devido à influência hormonal e predisposição genética. A revisão discute os mecanismos fisiopatológicos da celulite, incluindo alterações na derme, microcirculação e tecido adiposo, bem como as diferentes classificações clínicas da condição. Dentre os tratamentos analisados, destacam-se os bioestimuladores de colágeno, como o ácido poli-L-lático (PLLA) e a hidroxiapatita de cálcio (HaCa).O estudo reforça a importância dos bioestimuladores como alternativa minimamente invasiva para o tratamento da lipodistrofia ginóide, destacando sua relevância no campo da biomedicina estética e sugerindo a necessidade de pesquisas adicionais para aprimorar protocolos de aplicação e otimizar os resultados clínicos.
Palavras chaves: Bioestimuladores de colágeno,Lipodistrofia ginóide, Ácido poli-L-láctico (PLLA), Hidroxiapatita de cálcio (HaCa).
2. Introdução
A Lipodistrofia Ginóide, vulgarmente conhecida como celulite, é uma condição multifatorial que afeta cerca de 80 a 90% das mulheres (Luebberding et al., 2015). Sua prevalência no gênero feminino se destaca pelos altos níveis do hormônio estrogênio, ao contrário dos homens, que o possuem em baixa quantidade (Gabriel et al., 2023). Ela está presente no tecido cutâneo e adiposo, resultando em uma modificação da estrutura da derme, além de provocar alterações na microcirculação e nos adipócitos. Normalmente, incidem nas regiões que acumulam gordura com mais facilidade, como os glúteos, coxas, barriga e quadris, devido a influência do hormônio feminino (estrogênio), causando insatisfação em muitas mulheres (SBD).
Apesar de sua histopatologia ser de origem desconhecida, algumas teorias que buscam explicá-la. Uma delas a descreve como um edema crônico no tecido conjuntivo, provocando fibrose tecidual (Terranova et al, 2006). Outra sugere que a lipodistrofia ginóide é o resultado de uma alteração microcirculatória, caracterizada pela compressão do sistema venoso e linfático. Por fim, uma última teoria baseia-se no posicionamento perpendicular dos septos interlobulares do tecido subcutâneo (Gabriel et al., 2023).
Devido ao acúmulo de gordura, as células adipócitas hipertrofiam, e as alterações na microcirculação aumentam a pressão dos adipócitos, comprimindo os vasos, tornando as paredes dos capilares frágeis, aumentando sua permeabilidade e acumulando líquido (Cunha et al, 2015). A drenagem linfática na região diminui e ocorre a redução dos restos metabólitos, o endurecimento das fibras do tecido conjuntivo, provoca a tração da pele em direção à parte inferior do tecido, formando o aspecto casca de laranja. Devido ao aumento da fibrogênese e da deposição de colágeno, o número de cordões de colágeno subdérmicos (septos) é reduzido em áreas de celulite e dispostos perpendicularmente à superfície da pele (Gabriel et al., 2023).
Figura 1: Hipoderme e tecido adiposo subcutâneo
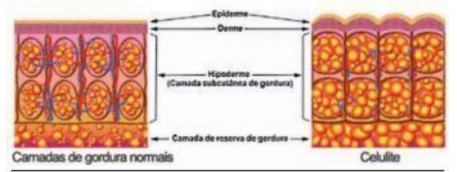
Sua classificação foi desenvolvida de maneira qualitativa através de imagens e avaliações clínicas. Segundo Guirro & Guirro (2004), os graus são divididos em grau I: Visível apenas em compressão e contração muscular, grau II: Depressões visíveis sem compressão, grau III: Alterações observadas sem contrações ou qualquer decúbito, aspecto de casca de noz, muita fibrose presente, grau IV: Nódulos e fibroses mais visíveis, palpáveis e dolorosos (Guirro & Guirro., 2004).
A Lipodistrofia Ginóide provém de uma interação complexa entre fatores genéticos, estruturais e hormonais, envolvendo alterações no tecido conjuntivo subcutâneo e a disposição da gordura corporal (Sadick, 2019).
O uso de Bioestimuladores de colágeno, surgiu como uma alternativa para o tratamento da Lipodistrofia Ginóide, esses, conhecidos como ácido poli-L-lático, policaprolactona e a hidroxiapatita de cálcio, atuando de forma inflamatória controlada, estimulando assim a produção intrínseca de colágeno (Rho et al, 2018).
O objetivo dos bioestimuladores de colágeno, é melhorar a aparência da pele, firmeza e sustentação. Atuando na camada mais profunda, restaurando volume perdido, contorno facial e corporal de forma sutil e natural, bioestimulando o colágeno novo, ativando os fibroblastos e aumentando a produção do colágeno. Podem ser classificados pela sua duração e a absorção pelo organismo, e são considerados semipermanentes (Borges FS & Scorza FA, 2016).
Ácido poli-L-lático (PLLA), são micropartículas que são biodegradáveis e absorvíveis, sua fórmula química estrutural é CH3-CH(OH)-COOH e tem o lactato como a forma ionizada (Franzen et al, 2013). De acordo com a International Union of Pure and Applied Chemistry (IUPAC), é conhecido como ácido cido α-hidroxipropanóico ou acido2- hidroxipropanóico. A degradação gradual do Ácido poli-L-láctico é biocompatível e metabolizada naturalmente pelo organismo.
Carreadas através de um gel de carboximetilcelulose sódica. Seu mecanismo de ação é o estímulo da neocolagênese, após a aplicação, suas micropartículas atraem os macrófagos que falham na fagocitose dessas partículas, formando um amontoado de células, que dão origem ao que conhecemos por célula gigante ou multinuclear (células inflamatórias), linfócitos e fibroblastos.
Os estudos mais recentes mostram a eficiência do bioestimulador de colágeno a base de policaprolactona (PCL) no mercado, ainda não foi encontrado muitos estudos sobre o uso deste para fins estéticos corporais (Kim Ja et al, 2015). Seu mecanismo se dá no reparo tecidual de forma imediata, criando uma lesão que desencadeia o processo de reparo e formação de colágeno tipo 1 a longo prazo (Galadari H et al, 2015).
Hidroxiapatita de cálcio (CaHa), produzido pelo corpo humano, sendo comumente presente em tecido ósseo. É biocompatível, promove um processo inflamatório controlado. Foi relatado em um estudo revisado pelo Centro Universitário FAI –UCEFF Itapiranga, o efeito volumizador da CaHa. Isso se dá pela rápida expressão de volume após aplicação do produto, o gel carreador se dissolve em 2/3 meses, promovendo uma resposta fibroblástica, estimulando colágeno por 18 meses e atuando como sustentador. O estudo Centro ressaltou que embora os efeitos sejam iguais aos demais bioestimuladores, o PLLA e o PCL têm a duração maior que a hridroxiapatita de cálcio (Miranda LHS, 2015).
O objetivo deste trabalho é analisar a eficácia, segurança, metodologias abordadas, efeitos adversos, efeitos esperados no tratamento da Lipodistrofia Ginóide com o uso do Ácido poli-L-lático.
3. Metodologia
Trata-se de um artigo de revisão narrativa de literatura, a partir dos resultados da busca em bases de dados como PubMed, Scientific Electronic Library Online (Scielo) e Biblioteca Virtual em Saúde (BVS), utilizando-se os descritores ácido poli-l-lático; fibroedema gelóide; celulite; bioestimulador de colágeno; celulite; tratamentos corporais, e seus correspondentes em língua inglesa.
Os artigos incluídos no presente estudo compreendiam estudos de casos, casos clínicos e revisões bibliográficas integrativas e sistemáticas publicadas a partir de 2013, disponíveis em meios digitais e na íntegra, em língua portuguesa ou inglesa. Resumos publicados em anais de congressos, artigos em pré-prints, livros, publicações em linguagem não adotada nos critérios de inclusão foram textos excluídos e não compuseram o repertório para elaboração desta presente obra.
4. Desenvolvimento
O Brasil ocupa o terceiro lugar mundial em procedimento não cirúrgico injetáveis, segundo dados da International Society of Aeshtetic plastic surgery (ISAPS (2020). O que reflete a crescente demanda por soluções estéticas e a importância de regulamentar a atuação dos profissionais da área, como biomédicos estetas.
O processo de envelhecimento, é um dos responsáveis por disfunções estruturais morfológicas e funcionais pois ocorre em qualquer camada do órgão, em decorrência de uma redução significativa de fibroblastos, comprometendo a produção de colágeno permitindo o surgimento e aumento da flacidez, aumentando outras disfunções estéticas. Ademais, a síntese de colágeno e elastina diminui em 1% ao ano levando à uma desorganização estrutural e funcional da derme (camada mais profunda da pele). Por conseguinte, a pele apresenta-se mais fina, enrugada, desidratada, frágil (Chaudhary et al., 2020).
O aumento do interesse pela estética glútea é uma preocupação real a essa condição multifatorial, a relação cintura-quadril de 0,6 a 0,65 em mulheres (Wong ww et al., 2016) e 0,85 em homens são parâmetros essenciais para o estabelecimento de uma abordagem estética adequada (Nteli Chatzioglou G et al., 2019). Em decorrência dos aumentos de intercorrências em procedimentos cirúrgicos em glúteos, o tratamento com bioestimulo de colágeno passou a ser considerado uma boa alternativa para corrigir depressões e FEG, além de proporcionar volume através do espessamento dérmico (Sandoval MHL., 2020).
O ácido poli- L -láctico, é um polímero sintético, biocompatível e biodegradável, tem sido usado com segurança em várias aplicações clínicas nas últimas décadas. O PLLA comercialmente injetável na forma de micropartículas, tem sido usado como volumizador no tratamento de lipoatrofia em pacientes com HIV. Ele também tem várias aplicações na engenharia de tecidos, melhorando a proliferação e a adesão celular. Pode ser categorizado como um preenchedor estimulatório, pois estimula a síntese e a deposição de tecido fibroso e colágeno. O colágeno é um dos componentes mais significativos da matriz extracelular e benéfico para a fisiologia normal. É também o componente estrutural do corpo humano (J. Funct. Biomater. 2020).
O PLLA é o estimulador de colágeno de longa duração de ação após várias sessões necessárias de tratamento, assim como o intervalo entre as sessões tem um papel fundamental para obter um resultado ótimo e duradouro. A justificativa para a necessidade de outras sessões foi documentada pela primeira vez em um artigo (Bauer U et al., 2011). Isso permitirá que o efeito da estimulação de colágeno ocorra e evite sobrecorreção. O bioestimulador a base de PLLA é usado também para aumento de volume, contorno corporal, flacidez, cicatrizes, celulite e estrias. Sendo ele o primeiro bioestimulador de colágeno aprovado na estética em 1999 na Europa e em 2004 nos EUA (Goldberg D et al., 2013). Seu uso foi se expandindo pelo mundo, associado a bons resultados estéticos a longo prazo graças ao seu efeito. Acredita-se que o mecanismo de ação seja uma estimulação de uma reação de corpo estranho caracterizada pelo aumento de macrófagos, mastócitos e linfócitos. Esse influxo leva à degradação lenta do produto aumentando a atividade fibroblástica e neocolagênese gradual (J. Cosmet. Laser Ther. 2018).
Figura 2: Amostras de pacientes
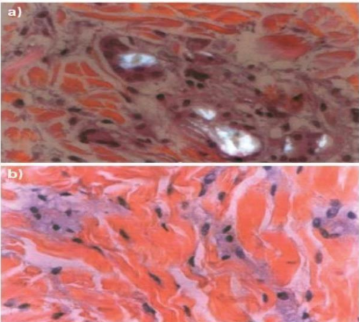
A Hidroxiapatita de cálcio (CaHa), tem se mostrado promissora na área estética devido à sua excelente aceitação pelo organismo e eficácia comprovada em diversos tratamentos. Trata- se de uma substância biodegradável e biocompatível, amplamente encontrada nos ossos e dentes humanos. No contexto estético, a hidroxiapatita é manipulada em forma esférica e diluída para atuar como bioestimulador de colágeno e agente preenchedor (Zerbinati et al., 2017; Saragoça et al., 2023).
Uma das principais vantagens desse material está na sua capacidade de ser absorvida de forma natural reduz o risco de rejeição pelo organismo, além de induzir a formação de fibroblastos, a CaHa também proporciona aumento de volume, dependendo do método de preparo e aplicação, quando mais diluída, menor será seu efeito volumizador, e isso permitirá uma estimulação controlada e personalizada conforme a necessidade do paciente (Saragoça et al., 2023).
A CaHa é comumente utilizada na biomedicina estética devido as suas propriedades únicas, sua estrutura cristalina, semelhante ao tecido ósseo, confere alta compatibilidade com o organismo e minimiza a ocorrência de reações adversas. Além disso, a substância estimula a produção de colágeno, proporcionando efeito lifting e melhorando a elasticidade da pele, com resultados naturais e duradouros (Abbud et al., 2021).
O processo de produção de CaHa envolve etapas rigorosas para garantir sua pureza e qualidade, utilizando fosfato de cálcio e água como componentes primordiais da sua composição. A reação química entre esses elementos é realizada sob condições controladas para promover a cristalização ideal (Haddad et al., 2017). A aplicação de hidroxiapatita de cálcio é realizada através de técnicas especificas, tal como injeções subcutâneas, utilizando cânulas e agulhas adequadas, no contorno corporal, é utilizado no realce de áreas como glúteos, coxas, abdômen, contribuindo para a modelagem do corpo e a melhora da aparência de irregularidades, como a fibro edema ginóide (De Oliveira et al., 2017).
A eficácia e segurança da CaHa forma evidenciadas por estudos clínicos, bem como a alta taxa de satisfação entre os pacientes. Quando comparado a outros bioestimuladores de colágeno como o ácido poli-L-lático e a policaprolactona, a CaHa exibe vantagens significativas em termos de resultados e segurança (Alves et al., 2024; Guida e Gladari., 2024).
O gel transportador distribuiu uniformemente as microesferas de CaHa, porporção 1:1 e se dissipando gradativamente, deixando as microesferas no local injetado, estimulando a neocolagenese por ativação de fibroblastos (Berlim AL et al., 2020). Segundo estudo histomorfológico clínico o HaCa estimula por longos 9 meses a produção de colágeno proporcionando aumento de volume e ação duradoura (Marmur et al., 2013).
Em um outro estudo realizado em animais, os resultados exibidos foram de um crescimento de colágeno novo ocorrendo na 4° semana após a injeção e permanecendo em ritmo estimulatório por 12 meses pelo menos. Sendo possível visualizar ao redor das microesferas a deposição de novo colágeno por média de 12 a 18 meses de duração, em alguns casos por 24 meses após injeção (Bass L S et al., 2010)
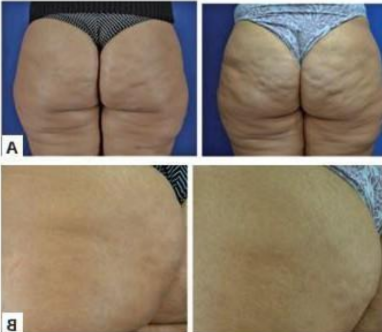
Figura 3: Antes de depois CaHa
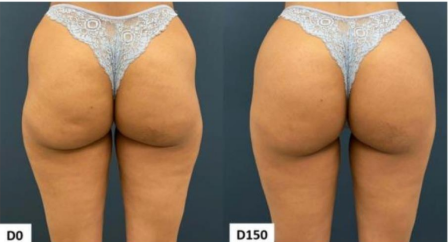
Resultados estéticos prée 150 dias pós-tratamento com injeção de Hidroxilapatita de Cálcio (TEODORO et al., 2023).
CaHa está associada a um perfil de segurança alto e bem estabelecido, é muito eficaz para diversas áreas de tratamento em tecidos moles (Pavicic., 2013). Tornando-o único considerado no mercado que repõe imediatamente o volume perdido e estimula colágeno natural da pele para resultados duradouros. Suas características de alta elasticidade e viscosidade, combinadas com a capacidade de formação de colágeno novo são únicas e lhe proporciona grande versatilidade, o que fez com que a CaHa evoluísse no campo estético de um agente preenchedor para um agente que pode ser usado para tratamento facial e corporal (Tzikas T L et al., 2008)
Como todo procedimento injetável esta suscetível a intercorrências, o uso da CaHa abre um alerta a intercorrência mais comum em sua aplicação, a formação de nódulos. Devido sua aplicação ser em tecido subdérmico e subcutâneo, regiões altamente moveis, permite que o produto se aglomere suas partículas mais facilmente. A região nodular ocorre logo após a aplicação e são completamente resolvidas com injeção de soro fisiológico e massagem vigorosa (Voigts R et al., 2010). Em síntese a CaHa representa uma alternativa promissora na biomedicina estética, com aplicações versáteis, efeitos positivos e excelente aceitação clínica. Apesar de possíveis reações adversas, estas podem ser minimizadas com adoção de protocolos adequados, consolidando-a como uma ferramenta eficaz.
Figura 4: Mecanismo de reação do corpo a um biomaterial
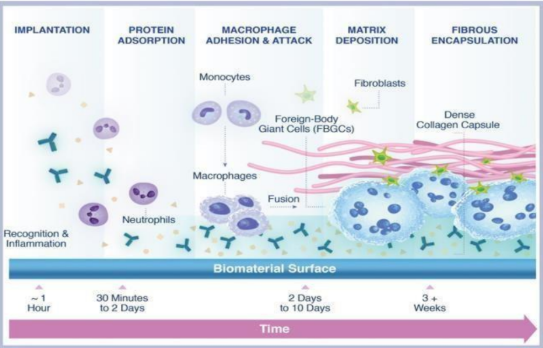
Com o envelhecimento, perda ou aumento de peso, ocorre a perda da elasticidade da pele e a perda de volume na área devido à redução de gordura subcutânea glútea, tornando-se menos firme, levando a flacidez das nádegas, e o aumento de gordura leva ao espessamento dos septos subcutâneos comprimindo os vasos e comprometendo a circulação, causando zonas elevadas dividindo a projeção da gordura subjacente à superfície da pele. Sadick N também relatou em seu estudo chamado “tratamento para celulite”, que as depressões e reentrâncias estão associadas ao aumento da espessura dos septos fibrosos, vistos em ressonância magnética.
Em pratica a administração do PLLA deve ser feita sob a musculatura, dentro da camada subcutânea, uma zona chamada de triangulo do perigo precisa ser corretamente identificada (Lin Mj et al 2020). Diversos resultados satisfatórios foram relatados em relatos de casos, revisões retrospectivas, estudos clínicos e prática clínica, através do tratamento da lipodistrofia ginóide com PLLA na região glútea e de coxas proporcionando um volume e melhorando o aspecto da FEG (Swearingen et al., 2021).
A anatomia da musculatura do glúteo é constituída por três camadas, sendo elas glúteo máximo, médio e mínimo, suas funções incluem extensão, abdução do quadril, rotação medial e lateral. Inervados pelos nervos glúteo inferior e superior, por ele também passa o nervo ciático. O glúteo máximo, é uma lâmina espessa e plana de músculo que se inclina da pélvis para baixo, através da nádega, a 45°, enquanto o glúteo médio tem forma de leque com seu terço posterior localizado reentrante ao glúteo máximo. O glúteo mínimo é o ínfimo e mais interno dos músculos, situado sob a cobertura do glúteo médio, com suas bordas anteriores situadas de ponta a ponta, da origem à inserção (Keith L. et al., 2013)
Figura 5: Anatomia dos glúteos
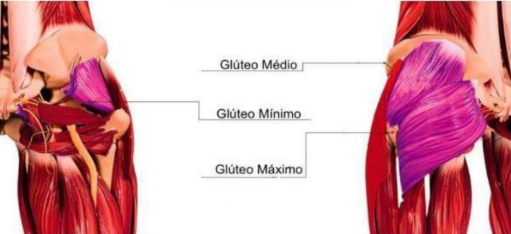
Á cima do glúteo se encontra o tecido subcutâneo, se trata de uma região maleável, vascularizada. Composta por adipócitos, separados por septos fibrosos. Nela podemos localizar folículos pilosos, glândulas sebáceas, coberta pela derme. Sua função é fornecer a conexão entre derme e estruturas móveis abaixo dela, protege o organismo de choques e ajuda no controle da temperatura. Sua espessura tende a ser diferente de acordo com a região, sexo e idade (Kashiwabara K. et. al,2019)
A derme, é uma estrutura mais espessa contendo vasos e nervos. Dividida em papilar e reticular, sendo papilar superficial a camada superior mais fina. A derme reticular profunda, como o nome já diz é a camada mais profunda, mais espessa. Contém uma vasta quantidade de vasos sanguíneos e fibras de colágeno que fornecem resistência à tração da pele.
O tecido conjuntivo fibroelástico, composto principalmente de colágeno, está contido nessa camada, assim como os fibroblastos.
A região papilar superficial é a camada superior mais fina, comedido de tecido conjuntivo frouxo que se liga ao tecido conjuntivo da epiderme. Ela compõe-se em matriz extracelular e fibroblastos. Os fibroblastos também secretam fibronectina e ácido hialurônico. A derme superficial também contém vasos sanguíneos, linfáticos, células epiteliais, pequenos músculos e neurônios. ( Lotfollahi Z., 2024).
A epiderme é dividida em cinco camadas em regiões inferiores das mãos e pés. Já nas outras partes podemos contar com apenas quatro sendo eles, estrato basal, estrato espinhoso, estrato granuloso e córneo. (Lotfollahi Z.,2024).
Figura 6: Hipoderme e tecido adiposo subcutâneo
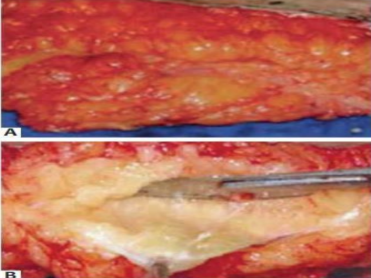
Segundo o estudo realizado por Cunha et al. (2016) com objetivo de avaliar a eficácia e segurança do uso do ácido poli-L-lático (PLLA) no tratamento de celulite e flacidez. A pesquisa envolveu 14 mulheres com idades entre 27 e 37 anos, apresentando celulite grau II e flacidez na região glútea. O protocolo incluiu duas aplicações de PLLA, com intervalos de 45 dias entre as sessões. Cada frasco do produto foi previamente diluído em 9 ml de água destilada e 2 ml de lidocaína, garantindo maior conforto. As aplicações foram realizadas na interface entre a derme profunda e a hipoderme superficial, utilizando pontos marcados em quadrantes de 2 cm². Após cada aplicação, foi realizada uma massagem vigorosa para distribuir uniformemente o produto, minimizando riscos.
Os resultados foram avaliados seis meses após a última aplicação, considerando critérios clínicos, ultrassonográficos e fotos, 78% afirmaram melhorias moderadas ou significativas, houve aumento mensurável na espessura da pele tratada, os efeitos adversos foram leves e temporários, como hematomas e dor em alguns pontos de aplicação, que desapareceram em poucos dias. As descobertas indicam que o PLLA é uma técnica minimamente invasiva e eficaz para o tratamento da celulite, com resultados duradouros devido ao estímulo de colágeno. O produto declarado é seguro, desde que aplicado por profissionais especializados, respeitando a técnica correta e as ofertas recomendadas.
Figura 7: Antes e depois PLLA
Outro estudo relevante realizado por Swearingen et al. (2021) indicou que a aplicação de PLLA na região glútea e nas coxas resultou em uma melhora no volume e no contorno da área tratada, além de uma redução nas depressões características da celulite. A avaliação ultrassonográfica também revelou um aumento mensurável na espessura da pele tratada, corroborando a eficácia do PLLA em melhorar a textura da pele e reduzir a visibilidade da celulite.
No entanto, o estudo de Ketelhut, P.F.A.M. et al. 2024 destaca a necessidade de mais pesquisas para consolidar as provas científicas do uso do PLLA no tratamento da celulite. Pesquisas sistemáticas e ensaios clínicos de maior escala poderiam contribuir para a definição de protocolos padronizados e para a confirmação de sua eficácia em variados cenários clínicos. Seria útil realizar estudos comparativos entre o PLLA e outras formas de tratamento para entender melhor os benefícios e restrições dessa estratégia.
Em síntese, o ácido poli-L-láctico é um progresso notável no combate à celulite, proporcionando uma estratégia segura, eficiente e de longa duração para pacientes que buscam aprimorar a aparência da pele. A sua habilidade de alterar o tecido subcutâneo e promover a formação de colágeno o qualifica como um agente de transformação.
5. Conclusão
A compreensão do mecanismo de ação dos bioestimuladores de colágeno, sua técnica de aplicação e os impactos na estrutura da pele são fundamentais para a formulação de protocolos eficazes e cientificamente embasados no tratamento da lipodistrofia ginóide. A celulite, predominantemente presente na região glútea, promove alterações na derme, microcirculação e tecido adiposo, resultando em irregularidades visíveis na pele. Os bioestimuladores de colágeno, como o ácido poli-L-láctico (PLLA) e a hidroxiapatita de cálcio (HaCa), demonstraram ser alternativas seguras e eficazes para a melhora da qualidade da pele e redução da flacidez.
O PLLA atua de maneira progressiva, promovendo bioestimulação de longa duração e um aumento gradual da espessura dérmica, resultando em um efeito natural e duradouro. Já a HaCa, além de proporcionar um efeito volumizador inicial, induz a neocolagênese, melhorando a textura e sustentação da pele.
A revisão de literatura evidencia que esses bioestimuladores representam um avanço significativo na biomedicina estética, destacando-se como opções minimamente invasivas no tratamento da lipodistrofia ginóide. Seus efeitos positivos na estimulação de colágeno e na melhora do aspecto da pele reforçam sua relevância como alternativa terapêutica, consolidando seu papel na busca por soluções estéticas eficazes e seguras. No entanto, ressalta-se a necessidade de estudos adicionais para aprimorar protocolos e garantir resultados cada vez mais satisfatórios e individualizados.
6. Referências
AARESTRUP, B.J. Histologia Essencial. Rio de Janeiro: Guanabara Koogan, 2012. AZULAY, R.D. Dermatologia. Rio de Janeiro: Guanabara Koogan; 2013. 1022p.
BRASIL. Ministério da Saúde. Secretaria de Políticas de Saúde. Departamento de Atenção Básica. Dermatologia na Atenção Básica / Ministério da Saúde, Secretaria
ACÚRCIO, A.R.; RODRIGUES, L.M. Os Ritmos da Vida – Uma Visão Atualizada da Cronobiologia Aplicada. Revista Lusófona de Ciências e Tecnologia da Saúde, v.6, n.2, p.216- 234, 2009.
ADDOR, F. A. S.; AOKI, V. Barreira cutânea na dermatite atópica. An. Bras. Dermatol., v.85, n.2, p. 184-194, 2010.
BASS LS, Smith S, Busso M, McClaren M. Hidroxiapatita de cálcio (Radiesse) para tratamento de sulcos nasolabiais: resultados de segurança e eficácia a longo prazo. Aesthet Surg J. 2010; 30:235–238. DOI: 10.1177/1090820X10366549.
BAUER U, Graivier MH. Otimizando a administração de ácido poli-L-láctico injetável para aumento de tecidos moles: a justificativa para três sessões de tratamento. Pode J Plast Surg. 2011; 19(3): e22–27. DOI:10.1177/229255031101900311
BAUER, U.; et al. “Long-term results of poly-L-lactic acid for the treatment of facial volume loss.” Journal of Drugs in Dermatology, v. 10, n. 7, p. 762-765, 2011.
BERLIM AL, Hussain M, Goldberg DJ. Preenchedor de hidroxiapatita de cálcio para rejuvenescimento facial: análise histológica e imuno-histoquímica. Dermatol Surg. 2008; 34(Suppl 1): S64–S67. DOI: 10.1111/j.1524-4725.2008. 34245.x
BRITO, Josy Q. A.; SILVA, Ana Paula O. Estudo de Caso Sobre os Efeitos da Radiofrequência no Tratamento do Fibro Edema Gelóide. Id on Line Revista Multidisciplinar e de Psicologia, Abrilde 2017, vol.11, n.35, p.32-41. ISSN: 1981-1179.
CAMATTA CP, BarrosoGP. Análisecomparativateóricaentreosbioestimuladores de colágeno injetáveis.2022.
CHUMMY S. Sinnatamby. Anatomia de Last. ISBN: 9780702033940-Flores D, Umpire D, Sampaio M, Cresswell M,
COLEMAN KM, Voigts R, DeVore DP, Termin P. Coleman WP 3rd. Neocolagênese após injeção de composição de hidroxiapatita de cálcio em modelo canino. Dermatol Surg. 2008; 34(Suppl 1): S53–S55. DOI: 10.1111/j.1524-4725.2008.34243. x.
CUNHA MG, CUNHA ALG, MACHADO CA. Fisiopatologia da lipodistrofia ginoide. Surg Cosmet Dermatol 2015;7(2):98-103.
CUNHA, M.; et al. “Efficacy and safety of poly-L-lactic acid for cellulite treatment.” Journal of Cosmetic Dermatology, v. 15, n. 2, p. 120-125, 2016.
DURAIRAJ, Kay, BAKER Omer, YAMBAO Monalea, LINNEMANN-HEAT, Jacob; Shirinyan Ani. Safety and Efficacy of Diluted Calcium Hydroxylapatite for the Treatment of Cellulite Dimpling on the Buttocks: Results from an Open-Label, Investigator-Initiated, SingleCenter, Prospective Clinical Study. Aesthetic Plastic Surgery, 10.1007/s00266-023-03815-z, vol. 48, n. 9, 1797-1806, 2024.
Goldberg D, Guana A, Volk A, Daro-Kaftan E. Estudo de braço único para a caracterização da resposta do tecido humano ao ácido poli-L-láctico injetável. Dermatol Surg. 2013; 39(6):915– 922. DOI:10.1111/dsu.12164
GOLDBERG, D. J.; et al. “Poly-L-lactic acid for facial volume restoration and improvement skin texture.” Dermatologic Surgery, v. 39, p. 1354-1360, 2013.
KEITH L. Moore, Arthur F. Dalley, AMR Agur. Anatomia Clinicamente Orientada. ISBN: 9781451119459 –
KETELHUT P. F. A. M., Silva, R. V. da, Buchalla, M. S., & Braga, J. S. da S. (2024). REVOLUÇÃO ESTÉTICA: O ÁCIDO POLI-L-LÁCTICO REDEFININDO PADRÕES DA HARMONIZAÇÃO GLÚTEA. Revista Ibero-Americana De Humanidades, Ciências E Educação, 10(10), 5768–5782. https://doi.org/10.51891/rease.v10i10.16419
LIN MJ, Dubin DP, Khorasani H. Ácido poli-L-láctico para aumento glúteo minimamente invasivo. Dermatol Surg. 2020; 46(3):386–394. DOI:10.1097/DSS.00000000000001967
LIN MJ, Dubin DP, Goldberg DJ, Khorasani H. Práticas no uso e reconstituição do ácido poli- L-láctico. JDD. 2019; 18(9):880–886.
LOGHEM JV, Yutskovskaya YA, Werschler WP. Hidroxiapatita de cálcio: mais de uma década de experiência clínica. J Clin Dermatol Estético. 2015; 8(1):38–49.
LOWE, NJ Otimizando o uso do ácido poli-l-láctico. J. Cosmet. Laser Ther. 2008, 10, 43–46.
MARMUR ES, Phelps R, Goldberg DJ. Achados clínicos, histológicos e microscópicos eletrônicos após injeção de um preenchedor de hidroxiapatita de cálcio. J Cosrnet Laser Ther. 2004; 6:223–226. DOI: 10.1080/147641704100003048.
MENDONÇA, A. M. da S.; PÁDUA, M. de.; RIBEIRO, A. P.; MILANI, G. B.; & JOÃO, S. M. A. Confiabilidade intra e interexaminadores da fotogrametria na classificação do grau de lipodistrofia ginóide em mulheres assintomáticas. Fisioterapia e Pesquisa, vol. 16, n. 2, pp-102– 106, 2009. https://doi.org/10.1590/S1809-29502009000200002.
NOGUEIRA, I. C. da C.; SILVA, N. C. S. da. Applicability of collagen biostimulators (poly- llactic acid and calcium hydroxyapatite) in dermal filler in off-face areas of the body. Research, Society and Development, [S. l.], vol. 11, n. 8, p. e47411831181, 2022. DOI: 10.33448/rsdv11i8.31181.
NTELI Chatzioglou G, Govsa F, Bicer A, Ozer MA, Pinar Y. Atratividade física: análise dos padrões das nádegas para o planejamento do tratamento do contorno corporal. Surg Radiol Anat. 2019; 41(1):133–140. DOI:10.1007/s00276-018-2083-4
PATHRIA M. US e RNM da anatomia do tendão pélvico e condições patológicas.Radiographics. 2022;42(5):1433-56. doi:10.1148/rg.220055
PAVICIC T. Enchimento de hidroxiapatita de cálcio: uma visão geral da segurança e tolerabilidade. J Drogas Dermatol. 2013; 12:996–1002.
RAY, Subarna, and Hang T. Ta. 2020. “Investigating the Effect of Biomaterials Such as Poly-(L-
Lactic Acid) Particles on Collagen Synthesis In Vitro: Method Is Matter” Journal of Functional Biomaterials 11, no. 3: 51. https://doi.org/10.3390/jfb11030051
REVIVA / Revista do Centro Universitário FAI –UCEFF / Itapiranga –SC. vol. 2, n.1, jun. 2022 ISSN 2965-0232.
REVIVA / Revista do Centro Universitário FAI –UCEFF / Itapiranga –SC. vol. 3, n. 2, 2024 ISSN 2965-0232
SADICK Neil, Treatment for cellulite, International Journal of Women’s Dermatology, volume 5, Issue 1, 2019, Pages 68-72, ISSN 2352-6475, https://doi.org/10.1016/j.ijwd.2018.09.002.
SADICK N. Tratamento para celulite. Int J Womens Dermatol. 2019; 5(1):68–72. DOI: 10.1016/j.ijwd.2018.09.002
SANDOVAL MHL. Ácido poli-L-láctico para a área glútea. In: Costa AD, editor. Procedimentos estéticos minimamente invasivos: um guia para dermatologistas e cirurgiões plásticos. Publicação Internacional Springer; 2020:543–547. DOI:10.1007/978-3-319-78265-2_76
Sociedade Brasileira de Dermatologia (SBD), Celulite | Biblioteca Virtual em Saúde MS (saude.gov.br), https://bvsms.saude.gov.br/celulite /
SBD. Sociedade Brasileira de Dermatologia. Conheça a Pele. 2015
SurgCosmetDermatol2016;8(4)322-7. DOI:http://dx.doi.org/10.5935/scd1984 – 8773.20168404 Aplicação de ácido poli-l-lático para o tratamento da flacidez corporal
SWEARINGEN A, Medrano K, Ferzli G, Sadick N, Arruda S. Estudo randomizado, duplo-cego e controlado por placebo de ácido poli-L-láctico para tratamento de celulite nas extremidades inferiores. JDD. 2021; 20(5):529–533. DOI:10.36849/JDD.5380
SWEARINGEN, J.; et al. “Poly-L-lactic acid for the treatment of cellulite and skin laxity.” Journal of Cosmetic Laser Therapy, v. 23, n. 1, p. 55-60, 2021.
TERRANOVA F, Berardesca E, Maibach H. Cellulite: nature and aetiopathogenesis. Int J Cosmet Sci. 2006; 28:157-67.
TZIKAS TL. Um resumo de 52 meses dos resultados usando hidroxiapatita de cálcio para aumento de tecidos moles faciais. Dermatol Surg. 2008; 34(Suppl 1): S9–S15. DOI: 10.1111/j.1524-4725.2008.34237. x.
VOIGTS R, DeVore DP, Grazer JM. Dispersão de acúmulos de hidroxiapatita de cálcio na pele: estudos em animais e práticas clínicas. Dermatol Surg. 2010; 36:798–803.
WONG WW, Motakef S, Lin Y, Gupta SC. Redefinindo as nádegas ideais: uma análise populacional. PlastReconstrSurg. 2016;137(6):1739–1747. DOI:
