REGISTRO DOI: 10.69849/revistaft/ch102025005101638
Davi Rogienfisz Mendes¹; Emily Rocha Miranda¹; Gabriela de Andrade Palhares¹; Jordana Cristina Brito Rodrigues¹; Mariana Lavier Correa Batista Silva¹; Vitor Hugo Simões Lima¹; Welington Nunes Silva1; Renato Resende Mundim2
Resumo
A diarreia aguda é uma das principais causas de morbidade e mortalidade em crianças menores de cinco anos, especialmente em países de baixa e média renda. Embora a terapia de reidratação oral (TRO) represente o pilar do tratamento, abordagens adjuvantes como a suplementação com zinco e o uso de probióticos vêm ganhando destaque. Este estudo realizou uma revisão narrativa da literatura para avaliar a eficácia dessas intervenções no manejo da diarreia aguda em pacientes pediátricos. Foram selecionados 12 estudos publicados entre 2015 e 2025, com foco na associação entre zinco, probióticos e desfechos clínicos relevantes. A suplementação com zinco demonstrou reduzir significativamente a duração e a gravidade da diarreia, sobretudo em populações desnutridas. Já os probióticos apresentaram efeitos variados, com destaque para cepas específicas como Saccharomyces boulardii e Lactobacillus rhamnosus GG, que mostraram capacidade de reduzir a duração dos sintomas. No entanto, a eficácia dos probióticos é estirpe-dependente e influenciada por fatores como dose, tempo de início da administração e características da população. Conclui-se que o uso combinado de zinco e probióticos pode trazer benefícios adicionais ao tratamento da diarreia aguda, desde que utilizado de forma criteriosa e baseada em evidências.
Palavras-chave: diarreia aguda. zinco. probiótico. pediatria.
1 INTRODUÇÃO
A diarreia aguda representa um importante problema de saúde pública na pediatria, configurando-se como uma das principais causas de morbidade e mortalidade em crianças menores de cinco anos em escala global (LAHIRI et al., 2022). Embora a mortalidade associada ao quadro seja menos frequente em países de alta renda, o impacto econômico e a sobrecarga nos serviços de saúde continuam sendo expressivos (LO VECCHIO et al., 2016). Nos países em desenvolvimento, entretanto, a diarreia aguda permanece como um desafio crítico, comumente relacionada a condições de saneamento inadequadas e ao acesso restrito a serviços de saúde (LAHIRI et al., 2022).
Do ponto de vista fisiopatológico, a diarreia aguda resulta, principalmente, de um desequilíbrio entre os processos de absorção e secreção de fluidos no trato gastrointestinal. Esse distúrbio culmina na eliminação de fezes com consistência reduzida e/ou aumento da frequência evacuatória — geralmente três ou mais episódios em um período de 24 horas (LAHIRI et al., 2022). Diversos agentes etiológicos podem estar envolvidos, com destaque para infecções virais, bacterianas e parasitárias, que comprometem a integridade da mucosa intestinal e prejudicam a absorção de água e eletrólitos (FLOREZ et al., 2018).
A terapia de reidratação oral (TRO) constitui o pilar do tratamento da diarreia aguda, sendo reconhecida mundialmente como a principal estratégia para prevenção da desidratação (LAHIRI et al., 2022). Além disso, a manutenção da alimentação habitual, com realimentação precoce, é fortemente recomendada. O uso de antibióticos, por sua vez, deve ser criterioso e reservado para casos específicos com suspeita ou confirmação de etiologia bacteriana (LO VECCHIO et al., 2016).
Nesse contexto, o zinco e os probióticos vêm sendo estudados como terapias adjuvantes no manejo da diarreia aguda infantil. A suplementação com zinco tem demonstrado reduzir tanto a duração quanto a gravidade dos episódios, especialmente em crianças desnutridas ou com idade superior a seis meses (LAHIRI et al., 2022). Os probióticos, por sua vez, favorecem a restauração da microbiota intestinal, competem com microrganismos patogênicos e modulam a resposta imune local (FLOREZ et al., 2018).
Diante desse panorama, torna-se pertinente revisar a literatura científica disponível sobre a eficácia dessas intervenções. O presente estudo tem como objetivo analisar as evidências sobre o uso de zinco e probióticos no tratamento da diarreia aguda em crianças.
FUNDAMENTAÇÃO TEÓRICA OU REVISÃO DA LITERATURA
A diarreia aguda continua figurando entre as principais causas de morbimortalidade infantil, especialmente em países em desenvolvimento. O manejo clínico adequado visa à prevenção da desidratação, à redução da duração dos sintomas e à mitigação de complicações. Diversas estratégias terapêuticas têm sido empregadas, sendo algumas amplamente consolidadas e outras ainda em fase de avaliação (MARAGKOUDAKI et al., 2018).
A terapia de reidratação oral (TRO) é amplamente reconhecida como a principal intervenção terapêutica para a diarreia aguda em crianças, devido à sua comprovada eficácia na correção dos distúrbios hidroeletrolíticos e na prevenção da desidratação (LO VECCHIO et al., 2016). Mesmo em quadros moderados, estudos demonstram que a TRO pode ser tão eficaz quanto a reidratação intravenosa, com a vantagem de reduzir riscos relacionados ao uso de acessos venosos e diminuir o tempo de hospitalização (RAWASHDEH et al., 2022).
A suplementação com zinco, recomendada pela Organização Mundial da Saúde, constitui uma abordagem relevante, sobretudo em contextos de risco nutricional elevado (FLOREZ et al., 2018). O mineral atua na regeneração da mucosa intestinal e na modulação da resposta imune, contribuindo para a diminuição da gravidade e da duração dos episódios diarreicos. Entretanto, sua eficácia pode ser influenciada pelo estado nutricional da criança e pelas características epidemiológicas da população (RAWASHDEH et al., 2022).
Os probióticos têm se consolidado como adjuvantes terapêuticos promissores. Determinadas cepas, como Saccharomyces boulardii e Lactobacillus reuteri, assim como combinações contendo zinco, demonstraram eficácia na redução da duração da diarreia (FLOREZ et al., 2018). Em contrapartida, outras cepas, como Bacillus clausii, ou combinações de Lactobacillus rhamnosus e L. acidophilus, não apresentaram benefícios clínicos significativos, ressaltando a importância da escolha criteriosa da cepa probiótica (RAWASHDEH et al., 2022).
A esmectite, um silicato natural de alumínio e magnésio com propriedades adsorventes, tem sido estudada como opção complementar. Meta-análises indicam sua capacidade de reduzir tanto a duração da diarreia quanto o volume fecal (FLOREZ et al., 2018). Contudo, seu uso isolado mostrou-se menos eficaz em comparação a combinações com zinco (RAWASHDEH et al., 2022). Além disso, seu uso em crianças menores de dois anos é desaconselhado pela Agência Nacional Francesa para a Segurança de Medicamentos e Produtos de Saúde, devido ao risco de contaminação por chumbo. (RAWASHDEH et al., 2022).
O racecadotril, um inibidor da encefalinase com ação antissecretora, tem demonstrado resultados positivos na redução do volume e da duração da diarreia (GUTIÉRREZ-CASTRELLÓN et al., 2014). Estudos em rede (network meta-analyses) apontam o racecadotril como superior a outros adjuvantes, como probióticos e esmectite (RAWASHDEH et al., 2022). Diretrizes da ESPGHAN/ESPID recomendam seu uso como complemento à TRO (GUTIÉRREZ-CASTRELLÓN et al., 2014).
Antieméticos, como a ondansetrona, podem ser utilizados em crianças com mais de seis meses de idade que apresentem vômitos persistentes. Uma única dose é capaz de reduzir falhas na TRO, bem como a necessidade de hospitalização e reidratação intravenosa (MARAGKOUDAKI et al., 2018). No entanto, seu uso rotineiro não é recomendado, sendo indicado apenas em situações específicas conforme as diretrizes internacionais (RAWASHDEH et al., 2022).
Os antidiarreicos inibidores da motilidade, como a loperamida, são contraindicados na maioria dos casos pediátricos devido ao risco de agravamento clínico e à ausência de eficácia comprovada (LO VECCHIO et al., 2016).
Em relação à alimentação, recomenda-se a manutenção da dieta habitual e a realimentação precoce. O uso de fórmulas isentas de lactose pode ser considerado em casos hospitalares com suspeita de intolerância secundária, mas não deve ser adotado rotineiramente em contextos ambulatoriais (RAWASHDEH et al., 2022; LO VECCHIO et al., 2016). Da mesma forma, a diluição do leite não demonstrou benefícios clínicos comprovados (RAWASHDEH et al., 2022).
Os prebióticos, embora teoricamente benéficos por estimularem o crescimento de bactérias comensais, não apresentaram superioridade em relação ao tratamento padrão em revisões sistemáticas recentes (RAWASHDEH et al., 2022).
Por fim, apesar do reconhecido papel imunológico da vitamina A e de outros suplementos micronutricionais, as evidências disponíveis não indicam benefícios consistentes na redução da duração da diarreia (FLOREZ et al., 2018).
Dessa forma, a TRO permanece como a intervenção mais eficaz, segura e acessível no manejo da diarreia aguda pediátrica. A suplementação com zinco e o uso de probióticos selecionados podem oferecer benefícios adicionais, especialmente em cenários específicos. O emprego de terapias complementares, como o racecadotril e a esmectite, deve ser avaliado com base nas evidências científicas e no perfil clínico individual. Assim, o tratamento da diarreia aguda requer uma abordagem fundamentada em evidências e adaptada às necessidades de cada criança (FLOREZ et al., 2018).
2 METODOLOGIA
Este estudo consiste em uma revisão narrativa da literatura, com o objetivo de avaliar a eficácia da suplementação de zinco e do uso de probióticos no manejo da diarreia aguda em pacientes pediátricos.
A pesquisa bibliográfica foi realizada na base de dados PubMed, utilizando os seguintes descritores: (“Zinc” OR “Zinc supplementation”) AND (“Probiotics” OR “Lactobacillus” OR “Saccharomyces boulardii”) AND (“Acute diarrhea” OR “Acute gastroenteritis”) AND (“Pediatrics” OR “Children”). Os termos foram combinados por meio dos operadores booleanos “AND” e “OR”, com busca de publicações nos idiomas inglês, espanhol e português.
A busca inicial resultou na identificação de 18 artigos. Os critérios de inclusão adotados foram: publicações entre os anos de 2015 e 2025, artigos disponíveis nos idiomas especificados e estudos que abordassem de forma direta a relação entre a suplementação de zinco, o uso de probióticos e a diarreia aguda em crianças. Os critérios de exclusão incluíram: artigos que abordavam apenas um dos dois elementos de intervenção (zinco ou probióticos) sem discutir sua associação com a diarreia aguda.
Após a leitura completa dos textos, 6 artigos foram excluídos por não atenderem aos critérios previamente estabelecidos, resultando em 12 artigos selecionados para compor a base teórica da presente revisão.
3 RESULTADOS E DISCUSSÕES
O Quadro 1 apresenta uma síntese dos principais artigos incluídos nesta revisão narrativa, destacando título, ano de publicação, autores e objetivos centrais de cada estudo analisado.
Quadro 1 – Características dos Artigos Revisados
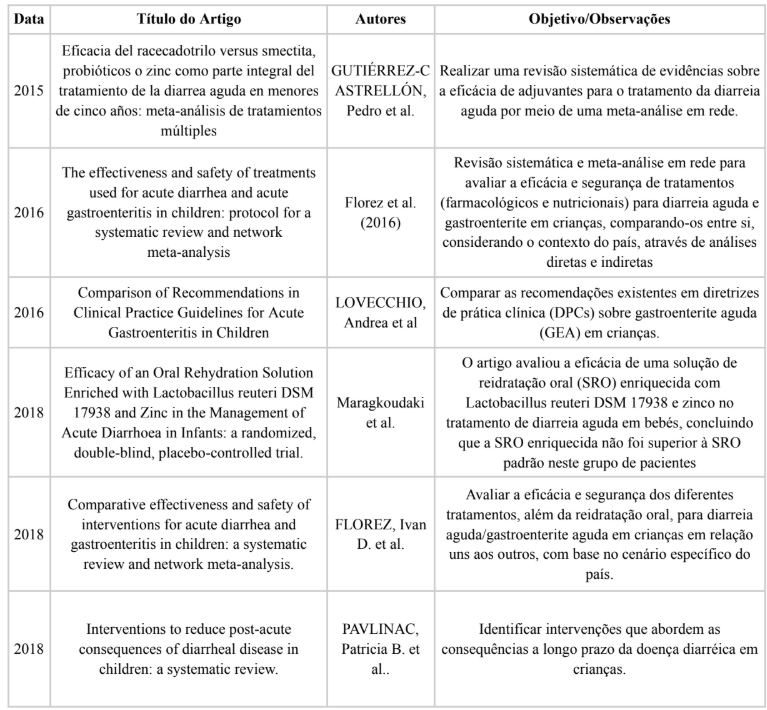
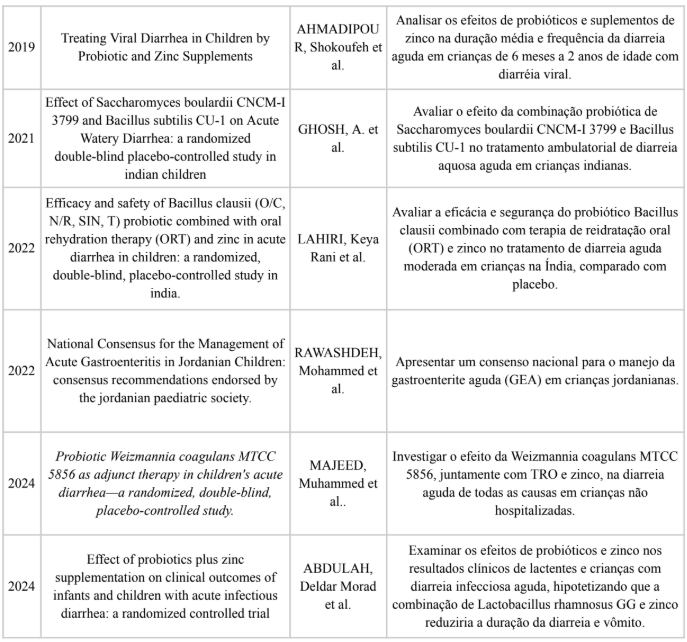
Fonte: Autoria própria
3.1 Suplementação de Zinco
A suplementação com zinco desempenha um papel importante no tratamento da diarreia aguda em crianças, especialmente em países em desenvolvimento onde a deficiência de zinco é comum. A Organização Mundial da Saúde (OMS) e o Fundo das Nações Unidas para a Infância (UNICEF) recomendam o uso de zinco oral como um tratamento adjuvante à solução de reidratação oral (SRO) para crianças com diarreia aguda por 10 a 14 dias (MARAGKOUDAKI et al., 2018).
Estudos demonstraram que a suplementação com zinco pode reduzir a duração e a gravidade dos episódios de diarreia. Uma revisão sistemática incluiu 33 estudos com 10.841 crianças de 1 mês a 5 anos de idade com diarreia aguda ou persistente, incluindo disenteria (ABDULAH et al., 2024). A suplementação com zinco conseguiu reduzir a duração média da diarreia em quase meio dia em crianças com mais de 6 meses de idade e diminuir o número de crianças com diarreia persistente até o sétimo dia (ABDULAH et al., 2024). O efeito foi ainda maior em pacientes com sinais de desnutrição, reduzindo a duração da diarreia em cerca de um dia (ABDULAH et al., 2024). Além disso, a suplementação com zinco tem se mostrado eficaz na redução do número de crianças com diarreia persistente até o sétimo dia (MARAGKOUDAKI et al., 2018).
Acredita-se que o zinco atue em vários níveis, incluindo a melhora da absorção de água e eletrólitos pelo intestino, a regeneração do epitélio intestinal, o aumento dos níveis de enzimas da borda em escova dos enterócitos e o reforço dos mecanismos imunológicos, o que contribui para uma resolução mais rápida da diarreia (MARAGKOUDAKI et al., 2018).
A dosagem recomendada de zinco varia entre 10 mg e 20 mg por dia (RAWASHDEH et al., 2022). Em alguns estudos, doses de 2 mg/kg/dia também foram utilizadas (PAVLINAC et al., 2018). A suplementação geralmente é administrada por um período de 10 a 14 dias. (RAWASHDEH et al., 2022)
É importante notar que a eficácia do zinco pode variar de acordo com a idade da criança e o contexto. Alguns estudos não encontraram efeitos significativos da suplementação de zinco na duração da diarreia em crianças com menos de 6 meses de idade. Nesse sentido, a pesquisa de Lahiri et al. (2022), conduzida na Índia, não identificou diferença significativa na eficácia de probióticos e o placebo, sendo que ambos os grupos receberam TRO e zinco.
Além disso, a eficácia do zinco parece ser mais pronunciada em países em desenvolvimento onde a prevalência de deficiência de zinco é maior. Em países de alta renda, o benefício da suplementação de zinco pode ser menos evidente em crianças bem nutridas. Dessa forma, Lo Vecchio et al. (2016) observaram que a recomendação de zinco é mais frequente em diretrizes de países de baixa renda, enquanto em países de alta renda seu uso não é sistematicamente preconizado em crianças sem deficiência do mineral.
Em comparação com outros tratamentos adjuvantes, um estudo sugere que, em alguns casos, a eficácia do zinco pode ser maior do que a de probióticos na redução da persistência da diarréia. Assim, Ahmadipour et al. (2019) verificaram que o zinco demonstrou maior eficácia do que os probióticos no tratamento da diarreia viral aguda em crianças iranianas. Por outro lado, Abdulah et al. (2024) observaram que crianças que receberam probióticos mais zinco se recuperaram mais rapidamente da gastroenterite em comparação com aquelas que receberam apenas probióticos.
Embora a suplementação com zinco seja geralmente segura, alguns estudos relataram vômitos como um possível efeito colateral (FLOREZ et al., 2018). No entanto, a ocorrência de complicações associadas ao zinco parece ser menor em comparação com outros tratamentos, como os probióticos, em alguns estudos (AHMADIPOUR et al., 2019).
3.2 Probióticos
Os probióticos são microrganismos vivos que sobrevivem no trato gastrointestinal e, quando ingeridos em quantidades apropriadas, conferem um benefício à saúde do hospedeiro. Eles têm sido amplamente estudados e utilizados como terapia adjuvante no tratamento da diarreia aguda em crianças (ABDULAH et al., 2024).
Meta-análises demonstraram que certas estirpes de probióticos, em doses adequadas, exercem efeitos anti diarreicos em crianças (GHOSH et al., 2021). Na meta-análise conduzida por Szajewska et al. em 2007, mostrou-se que a administração de probióticos em crianças com diarreia infecciosa aguda reduziu significativamente o risco de gastroenterite com duração superior a 3 dias em comparação com o placebo, e observou uma redução significativa na duração média da diarreia nos pacientes tratados com probióticos versus placebo (–14,4 horas) (LAHIRI et al., 2022). Outra meta-análise de 2002 indicou que a diferença na duração da diarreia foi entre 13 a 26 horas quando Saccharomyces boulardii ou Lactobacillus GG foram usados sozinhos em comparação com o placebo (GHOSH et al., 2021). Uma revisão de 82 estudos clínicos sobre os efeitos dos probióticos na diarreia aguda observou que a duração da hospitalização foi, em média, menor nos grupos probióticos do que nos grupos controle, embora os resultados fossem altamente heterogêneos (MAJEED et al., 2024).
No entanto, nem todos os estudos e meta-análises mostram resultados positivos para todos os probióticos. O estudo de Arora et al. (2021) observou uma recuperação mais rápida com a administração precoce de uma combinação de S. boulardii e B. subtilis (GHOSH et al., 2021). Um estudo com Lactobacillus rhamnosus GG sozinho ou em combinação com Lactobacillus helveticus não se mostrou eficaz na resolução da diarreia ou na melhoria do vômito em crianças pequenas com gastroenterite (PAVLINAC et al., 2018).
Vários estudos investigaram estirpes específicas de probióticos. O Saccharomyces boulardii tem sido extensivamente estudado mundialmente em diferentes grupos etários de crianças com diarreia aquosa aguda, com estudos a revelarem uma diminuição significativa de aproximadamente 24 horas na duração da diarreia, bem como na consistência e frequência das fezes (ABDULAH et al., 2024). Um estudo com S. boulardii também estabeleceu uma redução de 50% no número de episódios durante o período de acompanhamento de dois meses subsequentes em comparação com o controle tratado apenas com SRO e suporte nutricional (GHOSH et al., 2021). Bacillus subtilis CU1 demonstrou ação antidiarreica em modelos experimentais, possivelmente através do aumento da capacidade do cólon para absorver água (MAJEED et al., 2024). Uma combinação probiótica contendo S. boulardii CNCM-I 3799 e esporos de B. subtilis CU-1 mostrou-se eficaz na redução da duração da diarreia quando administrada dentro de 48 horas após o início da diarreia num estudo em crianças indianas (GHOSH et al., 2021).
As diretrizes da Organização Mundial da Saúde e da Sociedade Europeia de Doenças Infecciosas Pediátricas recomendam o tratamento ativo com estirpes probióticas específicas, em conjunto com SRO e suplementação de zinco, para reduzir a duração e a frequência das fezes na diarreia (GHOSH et al., 2021). Nesse sentido, em 2014, a ESPGHAN e a Sociedade Norte-Americana de Gastroenterologia, Hepatologia e Nutrição Pediátrica (NASPGHAN) recomendaram S. boulardii e Lactobacillus GG no tratamento de crianças com gastroenterite aguda como adjuvantes da terapia de reidratação (GHOSH et al., 2021). Em 2020, a recomendação atualizada do grupo de trabalho da ESPGHAN e da NASPGHAN consideraria novas evidências literárias sistemáticas para uma determinada estirpe probiótica se houvesse pelo menos dois ensaios clínicos randomizados bem desenhados e de alta qualidade para qualquer estirpe que apresentasse benefícios no tratamento da gastroenterite aguda (GHOSH et al., 2021).
É importante notar que o efeito probiótico é estirpe-específico e a sua eficácia e segurança precisam de ser estabelecidas individualmente. Além disso, fatores como dose, tempo de administração e características da população estudada podem influenciar os resultados. Alguns estudos sugerem que a administração precoce de probióticos, dentro das primeiras 24 a 48 horas do início da diarreia, pode ser mais eficaz (MAJEED et al., 2024).
A seleção de probióticos deve considerar a estirpe específica, a dosagem adequada e o contexto clínico do paciente, e mais estudos são necessários para definir melhor o papel dos probióticos no tratamento da diarreia aguda em diferentes populações e contextos (RAWASHDEH et al., 2022)
4 CONSIDERAÇÕES FINAIS
O presente estudo teve como objetivo analisar, por meio de uma revisão narrativa da literatura científica, a eficácia da suplementação com zinco e do uso de probióticos como terapias adjuvantes no tratamento da diarreia aguda em pacientes pediátricos. Com base na análise de doze estudos relevantes, publicados entre 2015 e 2025, foi possível observar que ambas as intervenções apresentam potencial benefício clínico quando utilizadas de maneira adequada, considerando-se fatores como idade da criança, estado nutricional, cepas específicas utilizadas e contexto socioeconômico.
No que se refere ao zinco, a suplementação oral mostrou-se eficaz na redução da duração e gravidade da diarreia, principalmente em crianças desnutridas e com mais de seis meses de idade. O mineral atua favorecendo a regeneração da mucosa intestinal, fortalecendo a imunidade local e promovendo a absorção de água e eletrólitos, o que contribui para uma recuperação mais rápida. A recomendação de sua utilização pela OMS e pelo UNICEF reforça sua importância terapêutica, especialmente em países de baixa renda, onde a deficiência nutricional é mais prevalente. No entanto, sua eficácia é menos evidente em populações bem nutridas e em contextos de alta renda, o que indica a necessidade de uso contextualizado.
Em relação aos probióticos, os efeitos terapêuticos foram mais variáveis, dependendo principalmente da estirpe utilizada, da dose administrada e do tempo de início da intervenção. Cepas como Saccharomyces boulardii e Lactobacillus rhamnosus GG mostraram resultados mais consistentes na redução da duração da diarreia e no número de evacuações diárias. Por outro lado, outras cepas não apresentaram benefícios clínicos significativos, o que evidencia a necessidade de maior rigor na seleção dos probióticos utilizados. Além disso, a administração precoce, preferencialmente nas primeiras 24 a 48 horas de início do quadro diarreico, parece estar associada a melhores resultados.
Conclui-se, portanto, que a terapia de reidratação oral deve permanecer como o tratamento padrão para a diarreia aguda em crianças, mas que a suplementação com zinco e o uso de probióticos selecionados podem desempenhar papel complementar relevante. O sucesso dessas intervenções, no entanto, depende de sua aplicação baseada em evidências, respeitando as particularidades de cada população e as diretrizes clínicas vigentes. Estudos adicionais, com metodologias robustas e aplicados a diferentes realidades socioeconômicas, são necessários para aprofundar o conhecimento sobre a eficácia dessas abordagens e promover práticas clínicas mais eficazes e seguras no manejo da diarreia aguda pediátrica.
REFERÊNCIAS
ABDULAH, Deldar Morad et al. Effect of probiotics plus zinc supplementation on clinical outcomes of infants and children with acute infectious diarrhea: a randomized controlled trial. Clinical And Experimental Pediatrics, [S.L.], v. 67, n. 4, p. 203-212, 15 abr. 2024. Korean Pediatric Society. http://dx.doi.org/10.3345/cep.2023.01340.
AHMADIPOUR, Shokoufeh et al. Treating Viral Diarrhea in Children by Probiotic and Zinc Supplements. Pediatric Gastroenterology, Hepatology & Nutrition, [S.L.], v. 22, n. 2, p. 162, 2019. The Korean Society of Pediatric Gastroenterology, Hepatology and Nutrition. http://dx.doi.org/10.5223/pghn.2019.22.2.162.
FLOREZ, Ivan D. et al. Comparative effectiveness and safety of interventions for acute diarrhea and gastroenteritis in children: a systematic review and network meta-analysis. Plos One, [S.L.], v. 13, n. 12, p. 0207701, 5 dez. 2018. Public Library of Science (PLoS). http://dx.doi.org/10.1371/journal.pone.0207701.
FLOREZ, Ivan D. et al. The effectiveness and safety of treatments used for acute diarrhea and acute gastroenteritis in children: protocol for a systematic review and network meta-analysis. Systematic Reviews, [S.L.], v. 5, n. 1, p. 1-1, 20 jan. 2016. Springer Science and Business Media LLC. http://dx.doi.org/10.1186/s13643-016-0186-8.
GHOSH, Apurba et al. Effect of Saccharomyces boulardii CNCM-I 3799 and Bacillus subtilis CU-1 on Acute Watery Diarrhea: a randomized double-blind placebo-controlled study in indian children. Pediatric Gastroenterology, Hepatology & Nutrition, [S.L.], v. 24, n. 5, p. 423, 2021. The Korean Society of Pediatric Gastroenterology, Hepatology and Nutrition. http://dx.doi.org/10.5223/pghn.2021.24.5.423.
GUTIÉRREZ-CASTRELLÓN, Pedro et al. Eficacia del racecadotrilo versus smectita, probióticos o zinc como parte integral del tratamiento de la diarrea aguda en menores de cinco años: meta-análisis de tratamientos múltiples. Gaceta Médica de México, Mexico, v. 151, n. 2015, p. 329-337, jun. 2014.
LAHIRI, Keya Rani et al. Efficacy and safety of Bacillus clausii (O/C, N/R, SIN, T) probiotic combined with oral rehydration therapy (ORT) and zinc in acute diarrhea in children: a randomized, double-blind, placebo-controlled study in india. Tropical Diseases, Travel Medicine And Vaccines, [S.L.], v. 8, n. 1, p. 1-1, 10 abr. 2022. Springer Science and Business Media LLC. http://dx.doi.org/10.1186/s40794-022-00166-6.
LOVECCHIO, Andrea et al. Comparison of Recommendations in Clinical Practice Guidelines for Acute Gastroenteritis in Children. Journal Of Pediatric Gastroenterology And Nutrition, [S.L.], v. 63, n. 2, p. 226-235, ago. 2016. Wiley. http://dx.doi.org/10.1097/mpg.0000000000001133
MAJEED, Muhammed et al. Probiotic Weizmannia coagulans MTCC 5856 as adjunct therapy in children’s acute diarrhea—a randomized, double-blind, placebo-controlled study. Frontiers In Pediatrics, [S.L.], v. 11, n. 1, p. 1-1, 10 jan. 2024. Frontiers Media SA. http://dx.doi.org/10.3389/fped.2023.1338126.
MARAGKOUDAKI, Maria et al. Efficacy of an Oral Rehydration Solution Enriched with Lactobacillus reuteri DSM 17938 and Zinc in the Management of Acute Diarrhoea in Infants: a randomized, double-blind, placebo-controlled trial. Nutrients, [S.L.], v. 10, n. 9, p. 1189, 1 set. 2018. MDPI AG. http://dx.doi.org/10.3390/nu10091189.
PAVLINAC, Patricia B. et al. Interventions to reduce post-acute consequences of diarrheal disease in children: a systematic review. Bmc Public Health, [S.L.], v. 18, n. 1, p. 1-1, 1 fev. 2018. Springer Science and Business Media LLC. http://dx.doi.org/10.1186/s12889-018-5092-7.
RAWASHDEH, Mohammed et al. National Consensus for the Management of Acute Gastroenteritis in Jordanian Children: consensus recommendations endorsed by the jordanian paediatric society. International Journal Of Pediatrics, [S.L.], v. 2022, p. 1-11, 30 ago. 2022. Wiley. http://dx.doi.org/10.1155/2022/4456232.
1Discente do Curso Superior de Medicina do Centro Universitário do Planalto Central Apparecido dos Santos (UNICEPLAC);
2Docente do Curso Superior de Medicina do Centro Universitário do Planalto Central Apparecido dos Santos (UNICEPLAC). Mestrando em Ensino de Ciência e Saúde pela Universidade do Grande Rio (UNIGRANRIO)
