REGISTRO DOI: 10.5281/zenodo.10801601
José Carlos Bedran
Orientadora Profa. Dra. Creusa Sayuri Tahara Amaral
Coorientadora Profa. Dra. Eliane Trovatti
RESUMO
Este trabalho tem o objetivo de desenvolver um fitomedicamento com propriedades regenerativas, em nova forma de administração tópica para tratamento de prurido anal e doença hemorroidária. Para isso, foi realizada uma pesquisa bibliográfica sobre inovações no tratamento tópico de doenças anorretais. A partir de consultas a bases de dados nacionais e internacionais, foi possível definir as melhores vias de atuação no desenvolvimento do produto do ponto de vista farmacológico, médico e biotecológico. Como metodologia foi utilizado o Design Science Research (DSR), que é um método aplicado em pesquisas tecnológicas, cujo principal objetivo é a produção de artefatos. Assim, o DSR é um método que apoia a criação de novos conhecimentos por meio de pesquisas aplicadas. O desenvolvimento deste projeto utiliza-se também do conceito de inovação aberta, como uma estratégia do programa de pós-graduação na consolidação de um habitat de inovação. Assim, o projeto contou com a parceria e colaboração para o desenvolvimento do fármaco. A identificação do problema surgiu pela experiência clínica do autor, no tratamento de doenças anorretais, que sucedeu as primeiras propostas dos fitoterápicos a serem utilizados na formulação e também na sua forma de administração. Os testes iniciais do medicamento foram realizados com o suporte da farmacotécnica e da tecnologia farmacêutica em conjunto com a parceria e colaboração com uma empresa de manipulação de fármacos. A partir de uma formulação selecionada pelas boas propriedades, foram realizados testes para validação do produto, os testes de qualidade do produto, como estabilidade, fixação, e viscosidade, obtendo-se um resultado positivo, com o alcance da composição e consistência ideais, estabilidade relativa estipulada e embalagem determinada. Realizou-se testes de estabilidade da formulação. Como um importante resultado da pesquisa, foi realizado o depósito de patente de invenção para o produto desenvolvido, cuja novidade é um processo para obtenção de composição fitofarmacêutica líquida, cujos componentes possuem peptídeos de crescimento epitelial, auxiliando numa cicatrização mais rápida, tendo sua administração tópica realizada por pulverização (frasco de spray).
Palavras-chave: Fitoterápico. Prurido anal. Novas formas farmacêuticas. Design Science Research.
ABSTRACT
This work aims to present the development of a phytotherapeutic drug with regenerative properties, in a new form of topical administration for the treatment of anal pruritus and hemorrhoidal disease. For this purpose, a bibliographic research on innovations in the topical treatment of anorectal diseases was carried out. From national and international databases, it was possible to define the best ways to develop the product from a pharmacological, medical and biotechnological point of view. The methodology used was Design Science Research (DSR), which is a method applied in technological research, which main objective is the production of artifacts. Thus, DSR is a method that supports the creation of new knowledge through applied research. The development of this project also uses the concept of open innovation, as a strategy of the graduate program in the consolidation of an innovation habitat. Hence, the project relied on partnership and collaboration for the development of the drug. The identification of the problem arose from the author’s clinical experience, in the treatment of anorectal diseases, which succeeded the first proposals of phytotherapic drugs to be used in the formulation and also its form of administration. The initial tests of the drug were carried out with the support of pharmacotechnology and famaceutical technology in conjunction with the partnership and collaboration with a drug handling company. Starting with a formulation selected for its good properties, tests were performed for product validation, the product quality tests, such as stability, fixation, and viscosity, obtaining a positive result, with the achievement of the ideal composition and consistency, stipulated relative stability, and determined packaging. Stability tests of the formulation were performed. As an important result of the research, an invention patent was deposited for the developed product, which novelty is a process for obtaining a liquid phytopharmaceutical composition, containing peptides for epithelial growth, helping faster healing, with topical administration by spraying (spray bottle).
Keywords: Phytotherapy. Anal pruritus. New pharmaceutical forms. Design Science Research.
1 INTRODUÇÃO
Segundo o Guia 2020 da Interfarma, Associação da Indústria Farmacêutica de Pesquisa, o cenário de inovação na saúde e em pesquisa clínica no Brasil não está entre os melhores. Mesmo com diversos indicadores que apontariam o Brasil na direção do protagonismo global, considerando que o país é a 9ª maior economia do mundo, de acordo com o Fundo Monetário Internacional (FMI), o Brasil ocupa a 66ª posição no ranking mundial de inovação dentre 169 países. Quanto à quantidade de pesquisas, o Brasil ocupa a 25ª colocação no ranking mundial (BRASIL OCUPA…, 2020). Algumas das áreas de destaque no cenário brasileiro de pesquisa na área da saúde são: infectologia, vacinas, oftalmologia, doenças cardiovasculares, doenças autoimunes e inflamatórias, oncologia, entre outras (INTERFARMA, 2020).
Em média, um medicamento pode necessitar de cerca de 10 anos entre o início dos estudos em laboratório e o seu lançamento. Isso porque o processo de desenvolvimento compreende quatro fases de estudos antes do lançamento. São feitos testes em laboratório, seguidos por três fases de pesquisa clínica com pacientes voluntários, para investigar eficácia e segurança do tratamento. Mesmo depois de lançados, os estudos não cessam, já que os efeitos adversos de longo prazo devem ser avaliados (BRASIL OCUPA…, 2020).
Na economia, o mercado farmacêutico brasileiro, que engloba as vendas de todos os laboratórios instalados no Brasil, chegou a R$ 102,8 bilhões em 2019. O valor representa um crescimento de 11,4% em comparação ao ano anterior. O aumento mais significativo ocorreu no chamado mercado institucional, formado por governos, clínicas e hospitais, que corresponde a R$ 33,7 bilhões. Já o varejo farmacêutico, em que 75% das compras são realizadas pelo público final, respondeu por R$ 69 bilhões das vendas em 2019. Seu aumento foi de 53% nos últimos quatro anos. Essa alta se justifica por várias razões, entre o envelhecimento da população e a oferta de novos tratamentos (BRASIL OCUPA…, 2020).
O déficit na balança comercial de medicamentos no Brasil tem registrado constante aumento nos últimos anos, chegando a mais de R$ 6 bilhões em 2019. Uma das principais medidas para reverter esse cenário seria a criação de um ambiente favorável à pesquisa clínica, com celeridade para avaliação de pedidos de estudos, integração entre governos, universidades e iniciativa privada, fomento à inovação e ao empreendedorismo. A pesquisa científica no setor farmacêutico resulta em tratamentos inovadores aos pacientes, conhecimento aos profissionais de saúde e investimentos ao país (BRASIL OCUPA…, 2020).
Segundo a Sociedade Brasileira de Coloproctologia (SBCP, 2016), aproximadamente metade das pessoas na idade adulta tem ou já tiveram algum sintoma relacionado à doença hemorroidária. De acordo com o Tratado de cirurgia do CBC (2015 a doença hemorroidária (DH) está presente em aproximadamente 50% das pessoas com mais de 50 anos, o que corresponde a 7,9% da população feminina e a 5,6% da população masculina do Brasil, de acordo com dados do IBGE (2020), totalizando uma estimativa de pouco mais de 27 milhões de pessoas com DH.
Dados do Instituto Nacional do Câncer, com relação ao Brasil, estimam cerca de 20.540 casos de câncer de cólon e reto a cada ano, entre o triênio de 2020-2022, entre homens e mulheres, sendo estimado uma média de 19,64 casos novos a cada 100 mil homens e 19,03 para cada 100 mil mulheres (INCA, 2020). A estimativa mundial aponta a ocorrência de 1 milhão de novos casos entre homens e cerca de 800 mil entre as mulheres, sendo o mais incidente dentre os cânceres entre os homens e o segundo mais frequente entre as mulheres (INCA, 2020 apud BRAY et al. 2018; FERLAY et al., 2018).
O tratamento das doenças anorretais, como hemorroidas e fissuras anais, é normalmente clínico para a maioria dos pacientes. Mudanças no estilo de vida, como maior consumo de fibras e ingestão de líquidos e higienização adequada da região, são essenciais na prevenção e no tratamento dessas doenças. Medicamentos tópicos são uma opção terapêutica efetiva e segura para o tratamento conservador das afecções anorretais, pois causam alívio rápido dos sintomas e da dor associados à doença hemorroidária, à fissura anal, ao prurido local e no pós-operatório de cirurgias proctológicas (SOBRADO, 2014).
Atualmente no Brasil, os medicamentos disponíveis para tratamento e alívio de sintomas de doença hemorroidária são comprimidos (como Venaflon, Daflon e Velunid), que atuam na circulação sanguínea e na resistência das veias hemorroidárias, atenuando os sintomas internos e externos; pomadas (como Hemovirtus, Proctyl e Ultraproct) e supositórios (como Ultraproct e Proctyl), ambos com ações vasoconstrictoras, analgésicas e anti-inflamatórias (SALLES, 2019). O banho de assento e a almofada ortopédica também são recomendados. Para o prurido anal, as pomadas anestésicas já mencionadas também são indicadas, além de pomadas antifúngicas em casos de micoses, remédios para vermes em casos de infestação e talco antisséptico com óxido de zinco (BEZERRA, 2020).
A região perianal, composta por ânus, canal anal e reto, pode ser acometida por um vasto número de doenças. A doença hemorroidária é a mais comum delas. Hemorroidas são varicosidades das veias do plexo hemorroidário, frequentemente complicadas por inflamação, trombose e sangramento (CRUZ et al., 2006). As hemorroidas podem ser externas (varizes ou pelotas de sangue e são visíveis na borda do ânus) ou internas (localizadas acima do esfíncter anal, com sintomas mais agudos) (BRASIL, 2017).
Outras doenças anorretais encontradas por meio de exame proctológico são: (1) lesões cutâneas (câncer de pele perianal, condilomas, úlceras, dermatopatias, prurido anal, proctites e destruição anal e perianal); (2) lesões da mucosa do canal anal (fissura, hipertrofia de papilas anais, criptite, proctite, câncer transicional); (3) tumores duros subcutâneos (gânglios, nódulos fibróticos, granulomas, hematomas, massas tumorais benignas e malignas); (4) tumores macios subcutâneos (abscessos, cistos, lipomas, hematomas); (5) infiltrações enduradas fazendo corpo com a pele (doença de Crohn, hidroadenite supurativa, infiltração carcinomatosa); (6) lesões anorretais inespecíficas (doença de Crohn, retocolite ulcerativa idiopática); (7) lesões anorretais específicas (tuberculose, esquistossomose, actino e blastomicose, amebíase); (8) estenoses anais (por fissuras, cirúrgicas, carcinomatosas); (9) orifícios e trajetos fistulosos (fístulas perianais e anorretais, específicas e inespecíficas); (10) anormalidades com o tônus anal (hipertonia, hipotonia, atonia); (11) invasão do ânus e períneo por doenças que vêm do reto (tumores retais); (12) comprometimento anal de doenças sistêmicas (diabete, pênfigo, linfoma); e (13) doenças dermatológicas que podem comprometer as regiões anal e perianal e doenças intestinais que podem apresentar lesões cutâneas próximas dessas regiões (CRUZ et al., 2006).
Algumas doenças são diagnosticadas após inspecção e por manobras apalpatórias e de esforço, pois são exteriorizadas pelo ânus. Podem ser: hemorróidas internas, prolapsos e procidências retais, pólipos, papilas anais hipertrofiadas, tumores vilosos prolapsados (CRUZ et al., 2006). Os sintomas dessas doenças geralmente se manifestam como: constipação, incontinência fecal e dor anorretal (WALD et al., 2014).
Novas tecnologias para o tratamento tópico de doenças anorretais são encontradas em outros países como o Perinal (medicamento em forma de spray), disponível para países do Reino Unido (DERMAL LABORATORIES, 2019) e o Proctofoam (medicamento em forma de espuma). Ciência, tecnologia e inovação auxiliam na transformação do modo de vida das pessoas, pela oferta de novos tratamentos para doenças ou pela oferta de novos produtos de consumo, para o trabalho, etc. Nesse processo, a ciência não utiliza as práticas de tentativa e erro e a inovação não ocorre em rompantes de inspiração. Uma abordagem, que vem se mostrando vantajosa no desenvolvimento de inovações e novas tecnologias é a inovação aberta (open innovation). Segundo Chesbrough (2003) essa estratégia vem sendo usada por empresas, que buscam solucionar problemas e desafios, utilizando profissionais fora de seu quadro de funcionários e/ou outras empresas para, em um processo de parceria, para criarem produtos e serviços mais inovadores em menor tempo e com mais chances de sucesso.
No Brasil, a inovação aberta tem sido feita de várias formas: 1) corporate venture (aceleração de startups), em que grandes empresas investem em startups e programas de inovação, se inovando ao mesmo tempo em que as startups tem acesso a recursos, mentoria e ganha experiência no mercado; 2) estrutura de inovação criada dentro da empresa: abertura de espaços onde a startup possa atuar e desenvolver suas ideias, como espaços coworkings; 3) eventos de inovação promovidos pelas empresas, como os hackathons, em que os promotores desse tipo de maratona buscam solucionar problemas encontrados pela empresa, podem, ainda, haver a oferta de prêmios para as melhores soluções (OPEN INNOVATION…, 2020).
Ainda assim, no Brasil, constata-se que a inovação aberta está em processo de difusão, e ainda falta melhor compreensão dos preceitos da inovação aberta pelas empresas do setor industrial e do setor de serviços. Os principais desafios para o uso dessa tecnologia no país estão relacionados ao aspecto jurídico, da cultura do mercado e regulamentações, pressões para crescimento e aumento de receita (BUSSMANN, 2020).
A abordagem de inovação aberta também tem sido usada por instituições acadêmicas, principalmente para consolidar as parcerias com as indústrias (PEDRINHO et al., 2020), devido à dificuldade de se desenvolver conhecimento e tecnologia suficientes para gerar inovar, a partir de uma única instituição. Assim, é comum que pesquisadores acadêmicos estabeleçam parcerias entre laboratórios da mesma unidade e entre universidades parceiras. Contudo, as parcerias com empresas para a realização de parte da pesquisa, ainda são incomum, mas devem se tornar um importante modelo para a inovação (PEDRINHO et al., 2020).
Dado o contexto, a abordagem de inovação aberta, pode ser utilizada como modelo para o codesenvolvimento de novos tratamentos, como o desenvolvimento de um medicamento para o tratamento de doenças anorretais, que seja eficiente e possa ser desenvolvido em menos tempo.
1.1 Objetivos
Este trabalho tem o objetivo de desenvolver uma formulação farmacêutica fitoterápica com propriedades curativas e nova forma de administração tópica para tratamento de prurido anal e doença hemorroidária.
Os objetivos específicos são:
– Identificar medicamentos fitoterápicos, bem como sua composição (princípio ativo, solvente, formas de uso etc.) para o tratamento de patologias anorretais;
– Identificar novos mecanismos e abordagens para tratamentos tópicos de patologias anorretais;
– Propor um processo (dentro dos moldes da inovação aberta) para as formulações identificadas.
1.2 Justificativa
Os sintomas de prurido anal podem persistir mesmo quando todas as causas subjacentes tiverem sido tratadas. A condição tende a ser recidivante ou crônica e é exacerbada por coçar e esfregar a área, levando à liquenificação e infecção bacteriana ou fúngica secundária.
O tratamento tópico pode precisar ser repetido ao longo do dia, e as formulações antipruríticas, anti-inflamatórias e anestésicas existentes são inconvenientes, pois precisam ser aplicadas manualmente, são geralmente oleosas e tocar a pele pode desencadear o desejo de esfregar a área de coceira.
Esta pesquisa se justifica pela alta incidência de doença hemorroidária na população (brasileira e mundial), com estimativa de que chegue a atingir 4,4% da população mundial (aproximadamente 50% da população adulta com mais de 50 anos) (ROBERTSON, 2019), e, também, pela limitação na forma de aplicação dos fármacos existentes no Brasil, sendo, em sua maioria, de administração manual, como pomadas, o que leva ao objetivo deste trabalho, que consiste no desenvolvimento de um medicamento fitoterápido de pulverição, utilizando um frasco spray.
A escolha por um medicamento fitoterápico se deu porque a fitoterapia apresenta eficácia e baixo custo operacional, tendo sua garantia asegurada pela ANVISA, que padroniza sua quantidade e qualidade através da purificação de microrganismos e substâncias estranhas e o Brasil apresenta uma vasta riqueza de biomas e vegetais. Tal variedade, associada à diversidade étnico-cultural, fornece um amplo uso de plantas e vegetais com finalidade medicinal, unindo a cultura tradicional e o uso fitoterápico dessas plantas. Segundo Esteves et al. (2020) “Fatores como o fácil acesso a essas plantas e a compatibilidade cultural são de extrema relevância para o progresso no uso dos medicamentos fitoterápicos, conferindo um excelente custo-benefício para tal prática”.
Esse trabalho se trata de uma pesquisa que envolve múltiplas áreas, com interações entre a medicina, farmacologia, tecnologia farmacêutica e biotecnologia, como mostrado na Figura 1.
Figura 1. Intersecções das áreas da pesquisa.
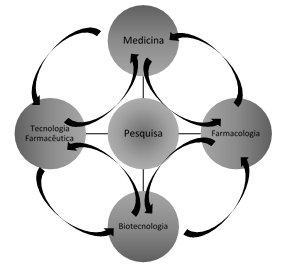
Unindo essas áreas, com novas tecnologias e métodos que estão surgindo, trazemos a Inovação Aberta (Open Innovation), que também tem sido usada por instituições de ensino, principalmente na relação com indústrias, visto que há dificuldade de se criar conhecimento e tecnologia suficientes para inovar dentro de uma única instituição. Esse modelo, escolhido para o desenvolvimento deste trabalho, envolve uma parceria entre instituições de pesquisa, empresas e licenciamento de patentes visando a promoção de inovações, através da criação de novos produtos, serviços ou modelos de negócios.
Se comparadas às empresas de países de primeiro mundo, as empresas brasileiras brasileiras ofertam diferentes níveis de desenvolvimento tecnológicos. Um caminho alternativo para uma economia emergente como a do Brasil é a rede de codesenvolvimento, que consiste em um mecanismo de acesso a recursos complementares, quando enfatizadas em estratégias de inovação aberta.
2 FUNDAMENTAÇÃO TEÓRICA
2.1 Farmacologia
Segundo o Dicionário de Substâncias Farmacêuticas Comerciais, princípio ativo (também chamado de insumo farmacêutico ativo, farmoquímico e fármaco) é a substância que deverá exercer efeito farmacológico e pode ser obtido por:
processos extrativos, nos reinos animal (ex. heparina), mineral (ex. cloreto de sódio) e vegetal (ex. rutina). Podem, ainda, ser obtidos por síntese química (ex. omeprazol), por processos biotecnológicos clássicos, como fermentativos (ex. penicilina) e enzimáticos (ex. amoxicilina). Podem ser obtidos ainda por processos biotecnológicos modernos (ex. alfainterferona) (PEREIRA, 2013).
Após extensa pesquisa em documentos da Anvisa e na Farmacopeia Brasileira, chegamos aos seguintes achados:
1. A Anvisa autoriza o uso de dois fármacos como medicamentos tópicos para a região anal: succinato sódico de hidrocortisona e cloridrato de lidocaína. Como fator biotecnológico, pensou no uso de fitoterápicos; busca na Farmacopeia Brasileira resultou em dois fitoterápicos: a babosa (Alloe vera) e a castanha-da-Índia (Aesculus hippocastanum L.).
2. A castanha-da-Índia é uma planta da família Hippocastanaceae, cujas castanhas são usadas no tratamento de algumas doenças. Seu uso é indicado no alívio da dor e prurido associados a hemorroidas, no entanto, quando as patologias são graves, seu uso tem sido previamente excluído por médicos (BRASIL, 2019; CASTANHA-DA-ÍNDIA, 2014).
3. As sementes da castanha-da-Índia contêm de 3 a 10% de escina (uma substância saponina presente em alguns vegetais, responsável pela formação de espuma), à qual são atribuídas atividades antidematogênica, anti-inflamatória e venotônica. Além da escina, constituintes da semente incluem flavonoides (0,2–0,3%), esteróis, cumarinas, taninos e óleos essenciais (VENOCUR® FIT, 2004).
4. A castanha-da-Índia usada como fármaco atua na redução da atividade das enzimas lisossomais, cuja quantidade aumenta no corpo humano quando ocorrem desordens venosas crônicas, “inibindo a desagregação do glicocálix (mucopolissacarídeos) na região da parede dos capilares”. A redução da permeabilidade vascular causa alívio dos sintomas comuns de insuficiência venosa, como a sensação de dor e de peso nas pernas, edema, câimbras e prurido (BLUMENTHAL et al., 2000).
5. A escina tem absorção rápida por administração oral, e tem meia-vida de absorção de 1 h aproximadamente. Porém essa substância sofre alta taxa de metabolismo de primeira passagem, resultando em uma biodisponibilidade de apenas 1,5% (CASTANHA-DA-ÍNDIA, 2014).
6. A Aloe vera L., nome popular de babosa, erva-babosa, erva-de-azebre, caraguatá e caraguatá-de-jardim, da família Liliaceae, possui ligninas e polissacarídeos que restituem os líquidos perdidos, reparando os tecidos de dentro para fora nas queimaduras (sol e fogo), fissuras, cortes, ralados, esfolados e perdas de tecidos ao penetrar profundamente nas três camadas da pele. A Aloe vera tem ação similar a dos esteroides, como a cortisona, mas sem seus efeitos colaterais. No entanto, essa planta não foi usada nos testes, pois estudos demonstram que a castanha-da-Índia apresenta maior eficiência para pruridos em geral (ALOE VERA, 2011).
Cabe elucidar, agora, as diferenças entre alopatia e fitoterapia, para que fiquem claros os motivos que fizeram a pesquisa seguir por este caminho e não por aquele.
2.1.1 Princípio ativo alopático
Medicina alopática é um termo usado para a medicina moderna ou convencional. Outros nomes para a medicina alopática incluem: medicina convencional, medicina ocidental, medicina ortodoxa ou biomedicina. A medicina alopática também é chamada de alopatia. É um sistema de saúde no qual médicos, enfermeiros, farmacêuticos e outros profissionais da saúde são licenciados para praticar e tratar sintomas e doenças. O tratamento alopático é feito com medicamentos, cirurgia, radiação, outras terapias e procedimentos (IFTIKHAR, 2019).
A palavra “alopático” vem do grego “allos“, que significa “outro”, “diferente”, e “pathos“, que significa “sofrimento”. Essa palavra foi cunhada pelo médico alemão Samuel Hahnemann nos anos 1800. Ela se refere aproximadamente ao tratamento de um sintoma com seu oposto, como é feito com frequência na medicina convencional. Por exemplo, a constipação pode ser tratada com um laxante (IFTIKHAR, 2019).
A medicina alopática é bastante diferente hoje do que era no século XIX. A medicina moderna ou convencional trabalha para tratar sintomas e doenças. Mas ela também ajuda a prevenir doenças e moléstias. Os médicos alopáticos podem se especializar em medicina preventiva. O cuidado profilático é o tratamento para evitar que uma doença ocorra. É usado em uma variedade de campos da medicina convencional (IFTIKHAR, 2019).
Os cuidados preventivos na medicina alopática incluem: vacinações para prevenir doenças graves que ameaçam a vida de bebês, crianças e adultos; antibióticos profiláticos para prevenir infecções após uma cirurgia, ferida ou corte muito profundo; cuidados pré-diabetes para ajudar a prevenir o diabetes; medicamentos para pressão arterial para ajudar a prevenir complicações graves como doenças cardíacas e acidentes vasculares cerebrais; programas de educação para prevenir o desenvolvimento de questões de saúde comuns a populações em risco, como doenças cardíacas, câncer e diabetes (IFTIKHAR, 2019).
2.1.2 Princípio ativo fitoterápico
Já a fitoterapia (do grego “therapeia” = tratamento, e “phyton” = vegetal) é o estudo das plantas medicinais e suas aplicações na cura das doenças. A fitoterapia envolve preparações de plantas inteiras como chá de framboesa (Rubus idaeus) ou extrato de semente de castanha-da-Índia (Aesculus hippocastanum), que se acredita, através do processo de “sinergia”, serem mais eficazes do que a soma de suas partes. É essa ênfase no material vegetal inteiro, em vez de ingredientes químicos individuais, que diferencia a fitoterapia da apropriação e fabricação sintética pela medicina convencional dos compostos ativos das plantas (ABDULLA, 1999).
2.2 Desenvolvimento tecnológico em fitomedicamentos
O desenvolvimento de um fitofármaco, ou seja, a transformação de uma planta em um produto tecnicamente elaborado, implica a utilização de operações de transformação tecnológica. A complexidade do processo e o número de operações dependem do nível de transformação requerido, que pode ser simples, como a preparação de chás, ou bem maior, quando o objetivo é obter frações purificadas como a obtenção de fitofármacos.
Uma vez desenvolvida, a formulação passará pelos estudos de estabilidade e validação. Esses estudos seguem a regulamentação geral estabelecida para medicamentos pela ANVISA. Orientações específicas para fitoterápicos e produtos tradicionais fitoterápicos são detalhados em Instruções Normativas como a IN 04/2014.
Para a produção de um fitofármaco ou fitoterápico uma série de exigências de padronização devem ser cumpridas (detalhadas no Quadro 1).
Quadro 1. Exigências de padronização de fitofármacos e fitoterápicos
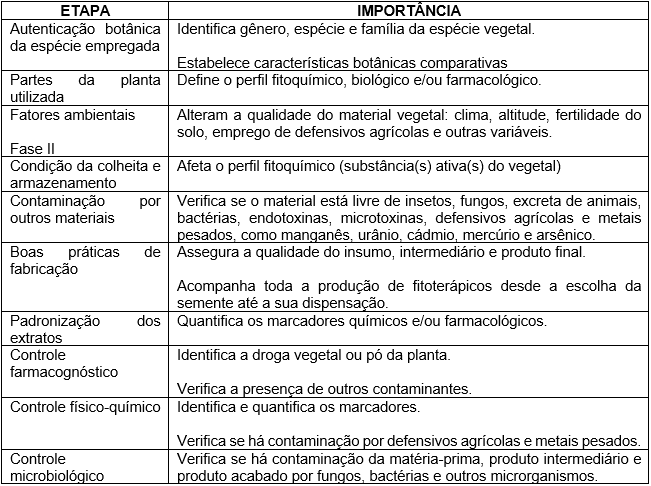
Para a área da saúde, a padronização do fitoterápico é fundamental para se estabelecer a prescrição de forma racional e segura, além de permitir o início do processo de industrialização.
A Fiocruz (2018) apresenta um estudo que descreve os entraves e dificuldades que devem ser superados, como mostra o Quadro 2.
Quadro 2. Desafios, entraves e dificuldades na pesquisa, desenvolvimento e produção de medicamentos da biodiversidade
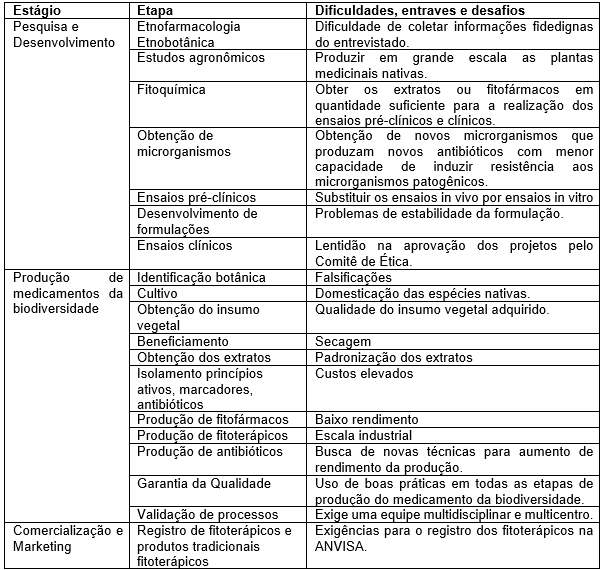
A transformação de uma planta em medicamento visa sua preservação e integridade química e farmacológica, para que sua utilização seja garantida. Para atingir esses objetivos, a sua produção requer estudos prévios relativos a aspectos botânicos, agronômicos, fitoquímicos, farmacológicos, toxicológicos e de desenvolvimento de metodologias tecnológicas e analíticas.
O processo de desenvolvimento de um novo fitofármaco compreende etapas ilustradas na Figura 3. Esse procedimento já é bem consolidado na prática, tanto nas farmácias de manipulação, como nas indústrias do fitoterápicos.
Figura 3. Desenvolvimento de fitofármaco
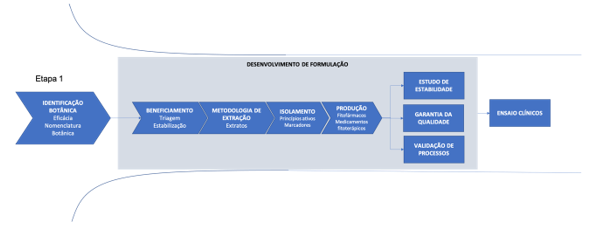
Fonte: Autoria própria.
2.3 Desenvolvimento de formas farmacêuticas
Os medicamentos chegam ao público consumidor em uma determinada forma. Para se chegar a esse formato, designado de forma farmacêutica, há um longo processo de investigação e um rigoroso processo de produção. O tipo de formulação está diretamente relacionado com a forma de administração do fármaco. De acordo com a Farmacopeia Brasileira, forma farmacêutica é:
o estado final de apresentação dos [insumos farmacêuticos ativos vegetais] IFAV após uma ou mais operações farmacêuticas executadas, com a adição ou não de excipientes apropriados, a fim de facilitar a sua utilização e obter o efeito terapêutico desejado, com características apropriadas a uma determinada via de administração. (FARMACOPEIA BRASILEIRA, 2018)
As formas farmacêuticas podem ser:
– Sólidas: adesivo, anel, barra, bastão, cápsula (dura, dura de liberação prolongada, dura de liberação retardada, mole, mole de liberação prolongada, mole de liberação retardada), comprimido (de liberação modificada, de liberação prolongada, efervescente, mastigável, orodispersível, para colutório, para solução, para suspensão, revestido, revestido de liberação prolongada, revestido de liberação retardada), dispositivo intrauterino, filme, glóbulo, goma de mascar, granulado (efervescente, para solução, para suspensão, revestido, revestido de liberação prolongada, revestido de liberação retardada), implante, pastilha (dura, gomosa), pó (aerossol, efervescente, liofilizado para solução injetável, liofilizado para suspensão injetável, liofilizado para solução injetável de liberação prolongada, para colutório, para solução, para solução injetável, para solução para infusão, para suspensão, para suspensão injetável, para suspensão injetável de liberação prolongada), rasura, sabonete, supositório e tablete.
– Líquidas: emulsão (aerossol, gotas, injetável, para infusão, spray), esmalte, espuma, líquido, óleo, sabonete líquido, solução (colutório, colutório spray, elixir, aerossol, de liberação prolongada, gotas, injetável, para diluição, para diluição injetável, para diluição para colutório, para diluição para infusão, para infusão, para irrigação, spray), suspensão (aerossol, de liberação prolongada, de liberação retardada, gotas, injetável, injetável de liberação prolongada, spray), xampu e xarope.
– Semissólidas: creme, emplastro, gel, pomada e pasta.
– Gasosas: gás.
A base das formulações farmacêuticas é composta por três categorias: veículos e excipientes, adjuvantes e ativos (CARESATTO E OLIVEIRA, 2019).
Veículos e excipientes são substâncias inertes responsáveis pela estabilidade do produto final, além de completar sua massa ou volume. Também carregam os princípios ativos para o órgão-alvo sem alterar a função do ativo. A diferença entre ambos é que os veículos são líquidos e os excipientes são sólidos ou semissólidos (ALLEN JR.; POPOVICH; ANSEL, 2013; CARVALHO, 2014).
Os componentes adjuvantes são aqueles que podem realizar ação modificadora (não são consideradas princípios ativos, mas alteram as características da base. Exemplos: umectantes, tensoativos e espessantes) ou corretiva (melhoram a aceitação do produto pelo consumidor, corrigindo cor e aroma através de corantes e fragrâncias e assegurando a vida útil através dos conservantes) (ALLEN JR.; POPOVICH; ANSEL, 2013; CARVALHO, 2014).
Por fim, os princípios ativos são responsáveis pela ação específica da aplicação do fármaco, cujas substâncias são destacadas nos rótulos dos produtos (ALLEN JR.; POPOVICH; ANSEL, 2013; CARVALHO, 2014).
As vias de administração das formulações farmacêuticas são: bucal, capilar, dermatológica, epidural, inalatória, inalatória por via nasal, inalatória por via oral, intra-arterial, intra-articular, intradérmica, intramuscular, intratecal, intrauterina, intravenosa, irrigação, nasal, oftalmológica, oral, otológica, retal, subcutânea, sublingual, transdérmica, uretral e vaginal (BRASIL, 2011).
Para desenvolvimento do fármaco, então, buscou-se primeiro conhecer os possíveis mecanismos de aplicação, ou seja, as embalagens primárias, uma vez que a intenção é sua dispersão sem contato manual com a região.
Para a escolha da embalagem deve-se considerar o material que está em contato com a forma farmacêutica e o material que está em contato com o meio externo, nessa ordem. O grau de transparência (âmbar, opaco, transparente e translúcido) refere-se à capacidade de visualização externa da embalagem para todos os casos.
Assim, as embalagens primárias podem ser: ampola (de plástico translúcido, de plástico transparente, de vidro âmbar, de vidro transparente), aplicador preenchido (de plástico opaco, de plástico transparente), bisnaga (de alumínio, de alumínio/plástico opaco, de plástico/alumínio opaco, de plástico opaco, de plástico transparente), blíster (de alumínio/alumínio, de alumínio/plástico âmbar, de alumínio/plástico opaco, de alumínio/plástico translúcido, de alumínio/plástico transparente), bolsa (de plástico transparente), bombona (de plástico opaco, de plástico translúcido), carpule (de vidro transparente), cilindro (de alumínio, de metal), envelope (de alumínio, de alumínio/papel, de alumínio/plástico, de papel, de plástico opaco), estojo (de plástico), flaconete (de plástico âmbar, opaco ou transparente, de vidro âmbar, opaco ou transparente), frasco (de alumínio, de plástico âmbar, opaco, translúcido ou transparente, de vidro âmbar, opaco ou transparente), frasco-ampola (de plástico transparente, de vidro âmbar ou transparente), frasco-aplicador (plástico âmbar, opaco, translúcido ou transparente, de vidro âmbar, opaco ou transparente), frasco de transferência (de vidro âmbar ou transparente), frasco-gotejador (de plástico âmbar, opaco, translúcido ou transparente, de vidro âmbar, opaco ou transparente), frasco spray (de plástico âmbar, opaco, translúcido ou transparente, de vidro âmbar, opaco ou transparente), lâmina (de alumínio, de papel), pote (de metal, de plástico âmbar, opaco, translúcido ou transparente, de vidro âmbar, opaco ou transparente), seringa preenchida (de plástico âmbar ou transparente, de vidro âmbar ou transparente), strip (de alumínio, de alumínio/papel, de alumínio/plástico, de papel, de plástico opaco), tubo (de alumínio, de plástico) (BRASIL, 2011).
Encontrou-se, assim, dois tipos de administração do fitofármaco na forma farmacêutica líquida em spray: aerossol e pulverizador.
2.3.1 Aerossol
Aerossol é um sistema de partículas líquidas ou sólidas distribuídas uniformemente em estado finamente dividido através de um gás, geralmente ar. As partículas de aerossóis, como o pó, desempenham um papel importante no processo de precipitação, fornecendo os núcleos sobre os quais ocorre a condensação e o congelamento (AEROSOL…, 2020).
Propelente é qualquer gás, líquido ou sólido cuja expansão possa ser utilizada para transmitir movimento a outra substância ou objeto. Nas embalagens aerossóis, os gases comprimidos, como o óxido nitroso, o dióxido de carbono e muitos hidrocarbonetos halogenados, são utilizados como propulsores. O propulsor pode permanecer na forma gasosa (óxido nitroso ou dióxido de carbono), ou pode liquefazer-se sob pressão. Os produtos alimentares, como as natas batidas artificiais, são movidos por óxido nitroso ou dióxido de carbono; os produtos não alimentares, como os cosméticos, inseticidas, tintas e produtos farmacêuticos, eram anteriormente dispensados da ajuda de hidrocarbonetos fluorados. Devido à ameaça que se crê ser colocada à camada de ozono da Terra por propulsores halogenados, estes foram proibidos em muitos países, exceto para utilizações essenciais como alguns medicamentos, pesticidas, lubrificantes e produtos de limpeza para equipamento eléctrico ou eletrônicos (PROPELLANT…, 2019).
Embalagem aerossol é qualquer embalagem, geralmente uma lata de metal ou uma garrafa de plástico, concebida para dispensar o seu conteúdo líquido como uma névoa ou espuma. Este tipo de recipiente foi desenvolvido em 1941 pelo químico americano Lyle D. Goodhue e outros para a distribuição de inseticidas. Desde então, uma grande variedade de produtos, desde desinfetantes a chantilly, tem sido embalada em recipientes aerossóis (AEROSOL…, 2013).
Solvente é uma substância, normalmente um líquido, em que outros materiais se dissolvem para formar uma solução. Os solventes polares (por exemplo, a água) favorecem a formação de íons; os não polares (por exemplo, os hidrocarbonetos) não o fazem. Os solventes podem ser predominantemente ácidos, predominantemente básicos, ambos ou nenhum. Os compostos orgânicos utilizados como solventes incluem compostos aromáticos e outros hidrocarbonetos, álcoois, ésteres, éteres, cetonas, aminas e hidrocarbonetos nitrados e halogenados. As suas principais utilizações são como meios de síntese química, como produtos de limpeza industriais, em processos de extração, em produtos farmacêuticos, em tintas, tintas de impressão, vernizes e lacas (SOLVENT…, 2019).
Spray é um equipamento de emissão que, sob pressão, emite a substância armazenada misturada com o gás (ou ar). Um aerossol é a mistura de dois líquidos, sendo um deles o produto em si – creme de barbear, desodorante, tinta ou inseticida – e o outro o propelente, uma substância capaz de impulsionar o produto para fora. Entre outras palavras, o spray é o recipiente, o equipamento utilizado para emissão do aerossol (AEROSSOL…, 2022).
Segundo o art. 4º da Lei Brasileira nº. 6360/766 que dispõe sobre a vigilância sanitária a que ficam sujeitos os medicamentos, as drogas, os insumos farmacêuticos e correlatos, cosméticos, saneantes e outros produtos: “os produtos destinados ao uso infantil não poderão conter substâncias cáusticas ou irritantes, terão embalagens isentas de partes contundentes e não poderão ser apresentados sob a forma de aerossol” (BRASIL, 2017).
2.3.2 Pulverizador
Figura 4. Sistema de pulverização
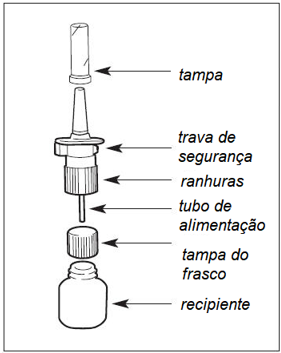
A pulverização, por outro lado, funciona quando mantida em qualquer direção. O recipiente é ecológico em relação à camada de ozono. Não é um aerossol e não contém quaisquer propelentes potencialmente irritantes (PERINAL…, 2019). A Figura 4 representa as partes de um sistema de pulverização.
Como já dito anteriormente, não há no mercado brasileiro a forma de aplicação de medicamentos para tratamento de prurido anal de uso tópico. Atualmente, há apenas pomadas e supositórios, sendo o medicamento Perinal (com pulverizador) encontrado apenas em países da Europa. Assim, verifica-se a importância e a necessidade de desenvolver esse produto, dadas as vantagens de manuseio e aplicação, além da oportunidade de negócio vislumbrada.
3 METODOLOGIA
A classificação das pesquisas ocorre com base em seus objetivos gerais e podem ser exploratórias, descritivas e explicativas. Essa classificação é útil para se delinear os conceitos iniciais da pesquisa. Este trabalho foi desenvolvido a partir de aspectos da pesquisa exploratória, cujo “objetivo principal é o aprimoramento de ideias” (Gil 2002, p. 41), utilizando também da pesquisa bibliográfica e do método de pesquisa Design Science Research, que se detalha na subseção seguinte.
3.1 Design Science Research
Design Science Research é um método de pesquisa orientado à solução de problemas. O método busca o entendimento do problema e, então, o desenvolvimento de artefatos que permitam contribuir para a solução do problema ou transportá-lo para estados melhores ou desejáveis. Os artefatos podem ser classificados em: constructos, modelos, métodos, instanciações (MARCH; SMITH, 1995; MARCH; STOREY, 2008).
No método Design Science Research é preciso estabelecer a relação entre conhecimento técnico e o conhecimento científico, entre tecnologia e ciência, entre artefato e teoria. Bayazit (2004), define Design Science Research como um método que operacionaliza e fundamenta a pesquisa, quando o objetivo é obter um artefato, a partir do estudo, pesquisa e investigação do artificial. Assim, uma característica do método Design Science Research é sua orientação à solução de problemas, não necessariamente a solução ideal, mas uma que se adeque ao contexto. A criação de um artefato, a partir desse método, é o principal meio pelo qual se pode gerar novos conhecimentos baseados em experiências práticas.
Para auxiliar na condução do método Design Science Research, foram propostas algumas etapas (VAISHNAVI; KUECHLER; PETTE ,2004), ilustradas na Figura 5.
Figura 5. Ciclo para aplicação do Design Science Research
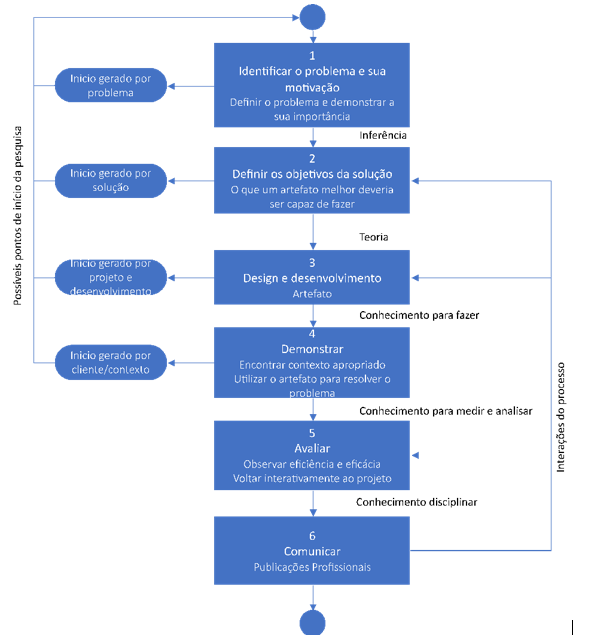
Fonte: Adaptado de VAISHNAVI; KUECHLER; PETTE (2004)
1) Problema: O processo do Design Research inicia quando o pesquisador busca solucionar um problema, é a condição inicial de pesquisa. E para isso é necessário entender a natureza do problema, o contexto, as potencialidades e as limitações para que seja possível compreender o ambiente em que o problema está inserido.
2) Solução: É preciso ter conhecimento sobre o problema e o contexto, compreender o problema, especialmente suas causas e consequências, para se pensar em possíveis soluções. Esse conhecimento pode ser obtido de uma revisão de literatura, de estudos empíricos anteriores, de estudos exploratórios ou de especialistas no domínio.
3) Desenvolvimento: A etapa do desenvolvimento é a efetiva construção do artefato pelo pesquisador, podendo ser um artefato ou um conjunto deles para solucionar o problema proposto.
4) Demonstração: A etapa de demonstração apresenta ações para que o artefato possa ser analisado e testado de acordo com as condições contextuais estabelecidas para validação.
5) Avaliação: Nesta etapa busca-se avaliar a eficiência e eficácia do artefato.
6) Comunicação: A etapa de comunicação é o fim de um ciclo de pesquisa. Consiste na formalização do processo e na sua comunicação à comunidade acadêmica e de profissionais.
3.2 Etapas de pesquisa
As etapas propostas para o desenvolvimento do trabalho seguiram o método do Design Science Research, em 6 etapas, e da Open Innovation. A Figura 5, na seção anterior, ilustra os passos da DSR.
Cabe ressaltar que o Design Science Research não é equivalente com ao método pesquisa-ação. A maior diferença é que este último prevê que as soluções partam das necessidades presentes na realidade dos pesquisados e não somente dos pesquisadores, ou seja, “o pesquisador participa ativamente para mudar uma determinada realidade, mas não define qual o problema a ser resolvido e não estabelece as prioridades” (FREITAS JUNIOR et al., 2016, p. 25).
O termo design neste método significa “o conhecimento sob a forma de técnicas e métodos para a execução do mapeamento das necessidades para a criação do artefato que satisfaça um conjunto de requisitos funcionais” (MACHADO et al., 2013, p. 4). Busca-se conceber os artefatos para solucionar uma dificuldade ou exigência, já que eles são “a interface entre o ambiente externo e a situação em que devem funcionar, incluindo todas as leis naturais que regem o seu funcionamento, o ambiente interno, a substância e a organização do artefato em si” (MACHADO et al., 2013, p. 4). Em outras palavras, o desenvolvimento de um artefato é o elemento pelo qual se consegue criar novos conhecimentos através de pesquisas aplicadas, embora ele não seja, obrigatoriamente, o principal resultado do Design Science Research. Outros resultados relevantes são:
– Oportunidades para a pesquisa interdisciplinar, pois os problemas visados necessitam de diferentes tipos de conhecimentos;
– Adesão dos sujeitos de pesquisa (ex.: coordenação de curso, alunos) pelo caráter aplicado da pesquisa, que pode gerar inovação no ambiente pesquisado;
– Possibilidade de coletar dados por diferentes fontes e de diferentes tipos (tanto qualitativos quanto quantitativos);
– Riqueza dos dados, baseados na observação da ¨vida real¨;
– Riqueza da aprendizagem por parte dos pesquisadores envolvidos (contato com a realidade);
– Flexibilidade do método, pela avaliação contínua do processo de pesquisa, os conhecimentos são gerados ao longo do processo e não só ao final; e,
– O artefato gerado pode ser aprimorado e aplicado na prática novamente. (MACHADO et al., 2013, p. 13)
Etapa 1 – identificação do problema a ser solucionado. Ocorrência de alta incidência de doença hemorroidária, não só na população brasileira, como a nível mundial e, no Brasil, os produtos existentes para seu tratamento são limitados em forma de aplicação e conteúdo (sendo, em sua maioria, alopáticos). E é neste ponto que foi identificado o problema a ser solucionado.
Etapa 2 – visa o encontro da solução do problema. Foi realizada uma revisão da literatura e das teorias existentes. De acordo com Gil (2002) a pesquisa bibliográfica é feita a partir de materiais, geralmente impressos, denominados “fontes bibliográficas”, que podem ser: livros, dicionários, enciclopédias, anuários, almanaques e publicações periódicas, como jornais e revistas científicas. Tal revisão foi realizada buscando por teorias e métodos já existentes visando a busca por uma solução para o desenvolvimento do novo produto.
Assim, buscou-se informação a respeito dos mecanismos de ação de princípios ativos, composição de medicamentos, métodos farmacológicos existentes atualmente e inovações biotecnológicas no tratamento de patologias anorretais. Para isso, foram usadas informações encontradas em livros (como a Farmacopeia Brasileira) e demais produções acadêmicas publicadas em jornais e revistas especializados em plataformas como: SciELO, Science Direct, Web of Science, PubMed, BDTD, ETD, entre outras.
As buscas iniciais de artigos e outras fontes com os temas de interesse desta pesquisa foram feitas em língua portuguesa e inglesa (para dar abrangência à pesquisa) com as principais palavras-chave conhecidas sobre o tema. A partir deste trabalho, construiu-se uma string de busca para elaboração de pesquisa bibliográfica. É importante que a revisão seja bem executada e confiável, realizada de forma de fácil compreensão. String de busca é o termo que se adota para realizar levantamentos, como por exemplo: (hemorro* OR perianal*) AND (pomada* OR creme*) AND (anestésico OR alívio).
A busca resultou em vários temas, que foram divididos em: (i) tipos de mecanismos de aplicação do fármaco, (ii) formulações dos fármacos liberados atualmente, (iii) inovações biotecnológicas, que serão discutidos em Resultados.
No ambiente tecnológico é comum que as pesquisas sejam de natureza aplicada. Porém as metodologias usadas tendem a ser tradicionais, “emprestadas das ciências sociais e naturais, as quais não compartilham da mesma natureza dos problemas e das soluções das pesquisas da área das engenharias e tecnológicas” (FREITAS JUNIOR et al., 2016, p. 25). O que vem a ser um problema, já que o desenvolvimento de tecnologias não é apenas a aplicação do conhecimento científico, pois os resultados não partem necessariamente de proposições e/ou teorias amplas, mas muitas vezes da busca de soluções para problemas pontuais e específicos, relacionados ao desenvolvimento de “artefatos”, bem como seu planejamento, operação, ajuste, manutenção e monitoramento (FREITAS JUNIOR et al., 2016).
Assim, conceitualiza-se “artefato” não apenas como um objeto, mas também como uma modificação de sistemas naturais (como o desvio do curso de um rio), artificiais, sociais (como a escalação de um time de futebol), de serviços (como os procedimentos médicos) (FREITAS JUNIOR et al., 2016).
Deve-se ter em mente que o resultado de pesquisas aplicadas pressupõe a criação de algo novo. Logo, “o tipo de conhecimento empregado é do tipo prescritivo, específico, peculiar ou tácito” (FREITAS JUNIOR et al., 2016, p. 25). As informações que dão embasamento a ela são originárias de exigências técnicas, econômicas ou culturais que o artefato deve satisfazer.
Etapa 3 – desenvolvimento do produto, feito em conjunto com uma farmácia de manipulação, parceira na realização do presente trabalho. Testes do produto, como a testagem de princípios ativos, testes com fitoterápicos (biotecnologia) e testes de solubilidade e consistência. Os testes seguem as regulamentações para medicamentos da ANVISA.
Etapa 4 – testes do produto, com a testagem in vitro e de segurança.
Etapa 5 – levantamento estatístico da eficácia e o desenvolvimento do produto em escala laboratorial.
A etapa 6 – depósito de patente (já realizado) e futura publicação de um artigo científico em revista especializada.
Sobre o modelo de inovação aberta, ele “já vem sendo utilizado pela indústria farmacêutica brasileira pelo menos desde os anos 2000” (VASCONCELOS, 2018, p. 23), foi a base para o codesenvolvimento da formulação do fitofármaco, considerando o estabelecimento de uma parceria, estratégica para o trabalho proposto. O acordo de parceria foi realizado com uma pequena empresa da área farmacêutica (farmácia de manipulação), com conhecimento e experiência para apoiar e colaborar com o desenvolvimento da formulação.
Devido à pandemia do COVID-19, que dificultou o desenvolvimento de pesquisas que necessitam de experimentação laboratorial, encontramos no modelo de inovação aberta, a possibilidade de agilizar e otimizar o desenvolvimento da forma farmacêutica por meio de parceria com uma farmácia de manipulação.
3.3 Desenvolvimento do produto
As empresas do século 21 estão participando de um processo de mudança nos modelos de negócio, que deixa a estratégia de especialização extrema e parte para estratégias de colaboração e parcerias. A indústria farmacêutica do século passado exemplifica bem esse fenômeno. Com o avanço de pesquisas e desenvolvimento de novas tecnologias nas áreas da ciência, tornou-se difícil e oneroso para que as empresas mantivessem um P&D totalmente especializado em sua área de atuação. Uma nova estratégia tornou-se necessária e fez com que as empresas começassem a dividir e compartilhar seus P&Ds, dividir pesquisas com outras empresas, com Institutos de Ciência e Tecnologia (ICTs) e com pesquisadores individuais, incorporando novos conhecimentos especializados de cada parceiro, e juntos criarem inovação.
Sobre as pesquisas com ingredientes naturais, essa estratégia faz ainda mais sentido. Uma empresa isolada, além de não deter o conhecimento e recursos necessários para desenvolver um novo extrato, um novo óleo essencial, acaba representando um volume pequeno para o produtor agrícola e para a indústria que faz a transformação da massa vegetal em um ingrediente natural. Essa estratégia pode beneficiar toda a cadeia de produção, pois o codesenvolvimento é uma estratégia sustentável que deve abarcar um número crescente de empresas.
Em P&D, principalmente na indústria, existem procedimentos que são a base para o desenvolvimento de produtos seguros e que tenham a qualidade esperada pelas empresas, pelos órgãos regulatórios e pelo mercado consumidor. Na área farmacêutica, o processo de desenvolvimento de uma nova droga é geralmente longo e requer grande investimento financeiro, além de estrutura de laboratórios e recursos humanos qualificados. Esses procedimentos são os testes de bancada, de planta-piloto e industriais (OS PROCESSOS…, 2021).
Testes de bancada são a primeira fase do processo de criação de produto farmacológico. Utilizam-se de equipamentos simples, como balanças, liquidificadores, batedeiras e fornos domésticos, e são feitos quando se quer desenvolver protótipos rápidos, realizar ajustes rápidos e observações de funcionalidades básicas. Por outro lado, não servem para definição de processos, avaliação de funcionalidades e teste de shelf life. Os pesquisadores de bancada sabem que existem impurezas que serão resíduos na produção em escala fabril, o que não se sabe é a quantidade, as características e como esses resíduos terão que ser tratados (LEONHARDT, 2017; WOOD-BLACK, 2014).
Em seguida, vêm os testes de planta-piloto, que produzem em menor escala, porém com razoável precisão, através de processos encontrados na planta fabril. Servem para definir processos, protótipos adequados e entendem melhor as funcionalidades, mas não são adequados para medições exatas de processo, shelf life e avaliação de embalagens. A planta-piloto fornece dados essenciais para a construção, compreensão e operação do processo em escala fabril (LEONHARDT, 2017; WOOD-BLACK, 2014).
Os testes industriais são feitos para reproduzir as condições reais pelas quais o produto irá passar quando se tornar um produto em comercialização. Servem para avaliação completa das funcionalidades, shelf life, treinar produção e qualidade e verificar o projeto, e não servem para definir formulação ou comparar ingredientes (LEONHARDT, 2017; WOOD-BLACK, 2014).
Após essas três etapas, o produto passa para a fase de produção/qualidade, onde será feito o acompanhamento do produto (LEONHARDT, 2017; WOOD-BLACK, 2014).
Sobre a criação de produtos farmacêuticos, o processo é dividido em duas grandes fases: 1) descoberta (ou fase pré-clínica) e 2) desenvolvimento (ou fase clínica). Na primeira fase, faz-se inicialmente a concepção do projeto e a abordagem da pesquisa através de a) identificação e validação de alvos (biologia, bioquímica, genômica e bioinformática); b) desenvolvimento de ensaios biológicos; c) estudos de biologia estrutural (GUIDO; ANDRICOPULO; OLIVA, 2010; NAHAS, 2013).
Após, é feita a identificação de compostos-líderes: a) triagem biológica automatizada; b) identificação de compostos bioativos; c) síntese orgânica; d) estudos de química medicinal; e) estudos de relação entre estrutura e atividade (GUIDO; ANDRICOPULO; OLIVA, 2010; NAHAS, 2013).
Em seguida, faz-se a otimização de compostos-líderes: a) estudos in vitro/in vivo; b) aumento da potência/afinidade; c) avaliação de propriedades farmacocinéticas (ADME) e toxicológicas; escalonamento; d) seleção de compostos otimizados (GUIDO; ANDRICOPULO; OLIVA, 2010; NAHAS, 2013).
Já na fase de desenvolvimento, são feitos estudos em humanos, com provas de segurança e de eficácia, efeitos adversos, determinação da dose, entre outros, diferenciando-se basicamente pelo número de participantes em cada fase: Fase 1 (20 a 80 indivíduos sadios), Fase 2 (200 a 300 pacientes), Fase 3 (1.000 a 3.000 pacientes). Ficando a Fase 4 reservada para o registro do novo fármaco nos órgãos competentes, como ANVISA, FDA, etc. (GUIDO; ANDRICOPULO; OLIVA, 2010; NAHAS, 2013).
4 DESENVOLVIMENTO PARA A FORMA FARMACÊUTICA
Dentre os objetivos desta pesquisa, esta seção irá tratar do desenvolvimento da formulação farmacêutica fitoterápica com propriedades curativas e de nova forma de administração tópica para tratamento de prurido anal e doença hemorroidária e como cada fitofármaco foi especialmente escolhido, testado e ajustado para que, de maneira harmônica e eficiente, resultassem numa formulação fitoterápica de aplicação realizada por pulverização (frasco spray).
A parceria com a farmácia de manipulação reduziu o tempo de desenvolvimento do produto, uma vez que várias competências foram incorporadas ao projeto, sem que fosse necessário o investimento de tempo e recursos financeiros para a preparação das formulações. A partir da parceria, novas rotas de formulação foram avaliadas, como uso de extratos vegetais, peptídeos de crescimento epitelial, substitutos dos princípios ativos convencionais.
Abaixo são descritos os materiais selecionados para os testes de bancada, após reuniões entre os pesquisadores da Universidade e a farmacêutica responsável, bem como descritas como foram analisadas e inseridas as rotas biotecnológicas do produto.
4.1 Seleção do material e preparação dos fitofármacos
4.1.1 Veículos
Como veículos foram usados, nas cinco fases da formulação, água deionizada, EDTA dissódico, triglicerídeos de ácido cáprico/caprílico e etoxidiglicol (Transcutol, Sigma-Aldrich).
Os triglicerídeos do ácido cáprico/caprílico (TACCs) são excelentes solventes de princípios ativos devido à sua composição estrutural. São recomendados como substitutos do óleo mineral, usado como veículo ou diluente, por ser também inerte (TRIGLICÉRIDES…, 2021).
O transcutol P é um solubilizante que pode aumentar a liberação dos ativos de produtos de uso tópico sejam formulações aquosas, géis, emulsões, cremes e pomadas. Sua performance multifuncional possibilita a solubilização de diversos ativos, melhora absorção dérmica e pode reduzir o potencial de absorção sistêmica da droga por formar uma barreira na pele onde o ativo fica depositado para liberação gradativa. É indicado para formulações de uso tópico, retal e vaginal (TRANSCUTOL P).
Seu princípio ativo é o etoxidiglicol: solubilizante de alta pureza, excelente perfil de segurança e compatível com a grande maioria das formulações. Aumenta a eficácia da formulação e, também, em diferente uso, pode auxiliar na redução da oleosidade de protetores solares (TRANSCUTOL P).
4.1.2 Adjuvantes
Como adjuvantes foram usados o conservante fenoxietanol/parabenos (Phenochem, Sharon Laboratories); o aglutinante goma xantana; os silicones DC 200-350, DC 9040 e DC 245; copolímeros de VP/acriloildimetiltaurato de amônio (Aristoflex AVC), emulsificante baseado na tecnologia Double Gel Network (Emulfeel SSC Plus, Chemyunion) e o conservante hidroxitolueno butilado (BHT, C15H24O).
4.1.2.1 Copolímero de VP/acriloildimetiltaurato de amônio
O copolímero de VP/acriloildimetiltaurato de amônio faz a caracterização de polímeros sintéticos utilizados, normalmente, como agentes espessantes em fórmulas à base de água ou na estabilização de emulsões, como cremes ou loções, principalmente fórmulas leves sem emulsificantes. O Copolímero de VP/acriloildimetiltaurato de amônio acumula géis claros na água, com um comportamento de fluxo diferente (GLOSSÁRIO…, 2021).
4.1.2.2 Emulsificante
O Emulfeel SSC Plus possui estruturação lipídica em presença de surfactantes e polímero. Emulsionante baseado em uma tecnologia que proporciona estruturação das fases lipídica e aquosa e suporta até 30% de carga oleosa. Estabiliza filtros solares. Proporciona versatilidade na criação de texturas viscosas ou fluidas, além de garantir sensoriais leves ou ricos e filme residual aveludado. Pode ser empregado em processos a frio ou a quente e ser usado com emulsionante principal ou coemulsionante. Não possui óleo mineral.
Emulsões com diversas texturas e sensoriais, tais como: cremes, loções, séruns e manteigas, contendo filtros e pigmentos como é o caso de protetor solar e BB creams. A incorporação pode ser a frio ou a quente, em que o ingrediente é preferencialmente disperso na fase oleosa seguido da sua dispersão na fase aquosa.
Benefícios:
– Diversas aplicações cosméticas para a formação de emulsões O/A.
– Permite a adição de altas concentrações de fase oleosa (até 30% p/p) em emulsões cosméticas;
– Pode ser usado como único espessante/estabilizante da formulação de produtos com FPS em processo a frio;
– Segurança clínica, dermatológica e oftalmológica comprovadas.
A concentração sugerida para uso como emulsionante principal é de 3 a 7%; como coemulsionante é de 0,5 a 3% (EMULFEEL® SSC Plus, 2021).
4.1.2.3 Bigel
Géis são definidos como materiais sólidos ou semissólidos em estado coloidal; por exemplo, uma solução de gelatina em água. Entretanto, na indústria cosmética e farmacêutica, o termo gel é interpretado de uma maneira mais ampla. Seguindo essa definição, muitos produtos que não são suspensões coloidais verdadeiras são chamados de géis para melhorar o apelo ao consumidor. O sistema bigel é uma dispersão de um gel oleoso em um gel aquoso, estabilizado por um sistema livre de surfactante, o que o torna menos irritativo. O bigel consiste em uma associação sinérgica de polímeros de etilcelulose com emolientes, em que a etilcelulose presente na interface óleo–água estabiliza as gotículas e previne floculação e coalescência. A estabilidade do bigel é comparável a das emulsões, e pode ser usado para criar uma vasta gama de produtos (MITURA; SIONKOWSKA; JAISWAL, 2020).
Nos produtos cosméticos atuais, os ácidos graxos essenciais atuam como excelentes emolientes, umectantes, reequilibrantes do manto hidrolipídico e a sua utilização é altamente benéfica na preparação cosmética. O óleo de canola, por exemplo, possui alto conteúdo de esteróis e tocoferóis, apresentando propriedades anti-inflamatórias e fotoprotetoras, sendo um ingrediente bioativo natural para formulações anti‑idade (MITURA; SIONKOWSKA; JAISWAL, 2020).
O bigel é um gel de fase oleosa que melhora a absorção do produto pela pele. Estabelecendo‑se as características do produto e as especificações que devem ser mantidas, devem ser realizados testes corriqueiros de controle de qualidade. Nas propriedades químicas, cada ingrediente ativo deve manter a sua integridade e a atividade indicada na embalagem, dentro de certos limites especificados, enquanto nas físicas observa‑se como os produtos se apresentam após sua fabricação. Essas características devem ser verificadas nos estudos de estabilidade, realizados de acordo com o objetivo que se pretende alcançar. Os estudos de estabilidade devem observar os seguintes critérios (SANTOS et al., 2010):
1. Pré‑formulação ou amostra: Seleção, de forma adequada, dos componentes de um produto, concentração, processo de fabricação, material de embalagem, entre outros. Sua finalidade é alcançar a composição quali‑quantitativa do produto, definir as características físico‑químicas, o processo de fabricação e qual será a embalagem final adequada.
2. Determinação da vida útil: quando se pretende estabelecer o período de tempo no qual um produto de composição definida, procedimento de fabricação estabelecido, numa embalagem determinada, é capaz de conservar suas características químicas, físicas e microbiológicas.
Os estudos da estabilidade de produtos cosméticos fornecem informações que indicam o grau de estabilidade relativa de um produto, nas variadas condições a que possa estar sujeito, desde sua fabricação até o término de sua validade. Essa estabilidade é relativa, pois varia com o tempo e em função de fatores que aceleram ou retardam alterações nos parâmetros do produto. Modificações dentro de limites determinados podem não configurar motivo para reprovar o produto. A sequência sugerida de estudos (preliminares, acelerados e de prateleira) tem por objetivo avaliar a formulação em etapas, buscando indícios que levem a conclusões sobre sua estabilidade (BRASIL, 2004).
4.1.3 Princípios ativos
Os princípios ativos utilizados foram: peptídeos de fator de crescimento transformador (TGF): B3, AFGF, BFGF, óleo de framboesa, óleo de buriti, ácido glicirrízico e castanha-da-Índia (BRASIL, 2019).
4.1.3.1 Castanha-da-Índia
A castanha-da-Índia atua aliviando os sintomas característicos da insuficiência venosa, como a sensação de dor e de peso nas pernas, inchaço, cãibras e prurido. Proporciona aumento da resistência vascular periférica e melhora do retorno do fluxo venoso (CASTANHA-DA-ÍNDIA, 2014).
4.1.3.2 Óleo de framboesa
O óleo de framboesa é indicado no auxílio do tratamento de peles secas e com descamação; como coadjuvante na prevenção de dermatites, psoríase, no tratamento de ferimentos cutâneos como úlceras e queimaduras, prevenção de gengivite, tratamento de estrias, peles inflamadas. Usado em produtos para pele sensível, formulações antienvelhecimentos, óleos de massagem, protetor solar, produtos faciais e corporais, pós-peeling. A combinação dos Ômegas 3, 6 e 9 no óleo de framboesa proporcionam a redução dos efeitos do stress oxidativo na pele, promovem a restauração da função barreira e regeneram a pele lesionada. Foi observado que o Óleo de Framboesa é útil em aplicações de filtros solares devido à absorbância de raios UVA e UVB. E refresca a pele após a exposição ao sol. Toxicidade e contraindicações não foram encontradas nas literaturas consultadas (BUSHMAN et al., 2004; OOMAH et al., 2000).
4.1.3.3 Óleo de buriti
O óleo extraído da polpa apresenta composição graxa rica em ácidos graxos insaturados (ácidos palmítico e oleico); alto teor de carotenoides, comportando-se como uma das fontes mais ricas em provitamina A; alta concentração de tocoferóis com excelente atividade antioxidante e alta estabilidade oxidativa. O óleo de buriti aumenta a elasticidade e diminui o ressecamento da pele exposta à radiação solar; auxilia na regeneração dos lipídeos da camada córnea e aumento de FPS devido ao seu alto teor de β caroteno. Testes clínicos mostraram que a adição de 5% de óleo de buriti em uma formulação de protetor solar acarretou em um acréscimo de cerca de 20% no FPS (fator de proteção solar) final do produto, quando comparado a outro sem a adição de do óleo. É indicado para formulações cosméticas anti-aging, produtos solares e pós-solares, fortalecedores capilares, produtos para cabelos tingidos e danificados, sabonetes líquidos em barra ou shower gel, cremes, loções e emulsões para a pele (ÓLEO DE BURITI…, 1996).
4.1.3.4 Peptídeos de crescimento epitelial
Devido à dificuldade de liberação pelos órgãos responsáveis dos componentes hidrocortisona e lidocaína para testes de formulações bem como para uma futura produção do novo medicamento, que neste caso só poderia ocorrer por meio de uma indústria farmacêutica, pensou-se na substituição desses componentes por fitoterápicos com efeito similar.
Em discussão preliminar com a farmacêutica responsável pela formulação dos primeiros testes, foi sugerido por ela não limitar o desenvolvimento do fármaco à Farmacopeia Brasileira, mas usar a padronização dela com extratos vegetais. Por se tratar de medicamento para tratamento de feridas e reconstituição da pele, foi avaliado o uso de peptídeos com nanofator de crescimento.
O fator de crescimento epidérmico (EGF) é uma proteína que estimula o crescimento e a diferenciação celular ao se ligar ao seu receptor, o EGFR. O EGF humano é 6-k Da e tem 53 resíduos de aminoácidos e três ligações dissulfeto intramoleculares. O EGF foi originalmente descrito como um peptídeo secretado encontrado nas glândulas submaxilares de camundongos e na urina humana. Desde então, o EGF foi encontrado em muitos tecidos humanos, incluindo a glândula submandibular (glândula submaxilar) e a glândula parótida. Inicialmente, o EGF humano era conhecido como urogastrona.
4.1.1.4 Extrato de glicirriza como substituto à hidrocortizona
Assim, ficou determinado que o extrato de glicirriza substituiria a hidrocortisona. O extrato de glicirriza é um fitoterápico proveniente da raiz do alcaçuz (Glycyrrhiza glabra) e tem demonstrado atividade antiinflamatória, melhora de problemas gastrointestinais, antioxidante, antialérgico, laxativo, distúrbios das vias respiratórias e detoxificante (IBERO MAGISTRAL, 2019). O alcaçuz é um ingrediente importante nos óleos medicinais contra epilepsia, paralisia, reumatismo e doença hemorrágica (KAUR et al., 2013).
4.1.3 Resultados
4.2 Teste de formulações
4.2.1 Farmacotécnica da formulação com óleo de framboesa
Procedimento de preparo:
1. Em recipiente com capacidade adequada, a fase 1 (água deionizada, EDTA dissódico, Phenochem) foi pesada e solubilizada.
2. Após pulverizar sobre o sistema principal o Aristoflex AVC, aguardou-se até sua completa hidratação. Em seguida, a fase 1 foi agitada em alta rotação até formação de um gel.
3. Dispersou-se a goma xantana sobre o sistema principal em alta rotação.
4. Em recipiente com capacidade adequada, pesou-se toda a fase 2 (Emulfeel SSC Plus, triglicerídeo de ácido cáprico/caprílico, BHT e óleo de framboesa), que foi, em seguida, aquecida a 50 °C.
5. Verteu-se a lentamente a fase 2 sobre a 1, sob agitação de 1000 rpm.
6. Em recipiente com capacidade adequada, toda fase 3 (TGF B3, AFGF, BFGF) foi pesada e solubilizada. Em seguida, foi adicionada lentamente.
7. Fase 4: em recipiente com capacidade adequada, pesou-se extrato de glicirriza, solubilizado em Transcutol, e adicionado à solução principal.
8. Em seguida, adicionou-se tintura de castanha-da-Índia.
9. Fase 5: em recipiente com capacidade adequada, misturou os silicones, DC 200-350, DC 9040 e DC 245, e adicionou-se à solução principal.
10. Após a homogeneização de todas as fases, o peso final foi conferido e, se necessário, deve-se completar com água o volume perdido por evaporação durante todo o processo.
Calculou-se o rendimento de acordo com a formulação: Aristoflex AVC (0,2%); EDTA dissódico (0,1%); Emulfeel SSC plus (2%); triglicerídeos de ácido cáprico/caprílico (3%); Phenochem (0,2%); DC 200-350 (5%); DC 9040 (3%); DC 245 (1%); extrato de glicirriza (1%); AFGF (1%); BFGF (1%); TGF b3 (1%) óleo de framboesa (3%); tintura de castanha-da-Índia (3%); Transcutol (10%); BHT (0,05%); Agua deionizada QSP (50 mL) e goma xantana (0,2%).
4.2.2 Farmacotécnica da formulação com óleo de buriti
Procedimento de preparo:
1. Em recipiente com capacidade adequada, pesou-se toda fase 1 (água deionizada, EDTA dissódico, Phenochem) e solubilizar.
2. Após pulverizar sobre o sistema principal o Aristoflex AVC, e aguardar até sua completa hidratação. Em seguida, agitado em alta rotação até formação de um gel.
3. Dispersar a goma xantana sobre o sistema principal em alta rotação.
4. Em recipiente com capacidade adequada, pesou-se toda fase 2 (Emulfeel SSC Plus, triglicerídeo de ácido cáprico/caprílico, BHT e óleo de buriti) e aquecido a 50° C.
5. Verteu-se a lentamente a fase 2 sobre a 1, sob agitação de 1000 rpm.
6. Em recipiente com capacidade adequada, toda fase 3 (TGF B3, AFGF, BFGF) foi pesada e solubilizada. Em seguida, foi adicionada lentamente.
7. Fase 4: em recipiente com capacidade adequada, pesou-se ácido glicirrízico, solubilizado em Transcutol, e adicionado à solução principal.
8. Em seguida, adicionou-se tintura de castanha-da-Índia.
9. Fase 5: em recipiente com capacidade adequada, misturou os silicones, DC 200-350, DC 9040 e DC 245, e adicionou-se à solução principal.
10. Após a homogeneização de todas as fases, o peso final foi conferido e, se necessário, deve-se completar com água o volume perdido por evaporação durante todo o processo.
5 RESULTADO FINAL
Após a realização de todos os procedimentos, obteve-se a formulação ideal do fitofármaco e sua forma inovadora de aplicação, por pulverização, realizada através do frasco spray e, também, realização de depósito de patente. Os resultados finais também convergiram na produção de um artigo científico, cuja publicação em revista especializada será realizada no futuro.
6 CONCLUSÃO
O medicamento consiste de uma composição fitofarmacêutica líquida à base de castanha-da-índia, óleo de framboesa e óleo de buriti, com peptídeos de crescimento epitelial. Sua administração tópica é realizada por pulverização e tem por objetivo auxiliar no tratamento e cicatrização de doenças anorretais. A inovação obtida encontra-se na forma (líquida) e no mecanismo de aplicação do produto (frasco de spray), assim como em sua formulação, que contém princípios ativos fitoterápicos, peptídeos de crescimento epitelial, auxiliando numa cicatrização mais rápida.
De acordo com o método Design Science Research, encontra-se faltante a testagem clínica em humanos e algumas partes integrantes relacionadas à comunicação. Visto que a publicação deste trabalho, em si, já faz parte desta última etapa, não se realizaram a publicação científica (artigo encontra-se concluído, porém, ainda não publicado) e a comunicação voltada aos profissionais da área.
A parceria com a farmácia de manipulação seguiu os moldes do codesenvolvimento, explicitado no trabalho de Spina et al. (2002), em que o relacionamento com a empresa parceira seguiu as contingências a serem atendidas e, em conjunto com a inovação aberta foi essencial para que, no cenário restritivo e incerto que a pandemia do COVID-19 trouxe, a pesquisa seguisse e culminasse em sua conclusão, com o depósito de patente feito e um artigo a ser publicado no futuro.
O produto resultante da pesquisa da pesquisa, uma nova formulação para medicamento de tratamento hemorroidário e de pruridos anais, que inova em sua aplicação por pulverização (frasco spray), sem nome ou marca associada, torna evidente o potencial a ser explorado da biodiversidade brasileira em produzir inovações, que podem direcionar pesquisar, que tenham impacto na melhoria da saúde da população. Assim, este trabalho também contribui para que outras pesquisas, com medicamentos baseados em plantas, possam ser desenvolvidas.
REFERÊNCIAS
ABDULLA, S. Phytotherapy – good science or big business? Nature, 1999. https://doi.org/10.1038/news990513-8
OS PROCESSOS de inovação na indústria de ingredientes. AI Aditivos | Ingredientes, 2021. Disponível em: https://aditivosingredientes.com/upload_arquivos/202107/2021070472461001626983356.pdf. Acesso em: 02 fev. 2022.
AEROSOL CONTAINER. Encyclopædia Britannica. Encyclopædia Britannica, Inc. 2013. Disponível em: https://www.britannica.com/technology/aerosol-container. Acesso em: 4 ago. 2021.
AEROSSOL e Spray. GGUS. DEPI. Unicamp, 2022. Disponível em: http://www.ggus.depi.unicamp.br/?page_id=2096. Acesso em: 2 fev. 2022.
ALLEN JUNIOR., L. V.; POPOVICHM N. G.; ANSEL, H. C. Formas Farmacêuticas e Sistemas de Liberação de Fármacos. 9. ed. Porto Alegre: Artmed, 2013.
ALOE VERA L. Piracicaba: Florien. 2011. Bula. Disponível em: http://florien.com.br/wp-content/uploads/2016/06/ALOE-VERA.pdf. Acesso em: 3 ago. 2021.
BARNEY, J. Firm Resources and Sustained Competitive Advantage. Journal of Management, v. 17, n. 1, p. 99-120, 1991. https://doi.org/10.1177/014920639101700108
BAYAZIT, N. Investigating design: A review of forty years of design research. Design Issues, v. 20, n. 1, p. 16-29, Disponível em: https://www.ida.liu.se/~steho87/desres/bayazit.pdf
BELL, M. N.; PAVITT, K. The development of technological capabilities. In: HAQUE, I.-U.; BELL, M. N. (ed.). Trade, Technology and International Competitiveness. Washington: World Bank, 1995. p. 69-101.
BEZERRA, C. Principais causas e tratamentos para coceira no ânus. Tua Saúde [Internet]. 2020. Disponível em: https://www.tuasaude.com/coceira-no-anus/. Acesso em: 29 abr 2020.
BLUMENTHAL, M.; GOLDBERG, A.; BRINCKMANN, J. Herbal Medicine: Expanded Commission E Monographs. Austin: American Botanical Council, Boston, 2000.
BOISOT, M.; CHILD, J. From Fiefs to Clans and Network Capitalism: Explaining China’s Emerging Economic Order. Administrative Science Quarterly, v. 41, n. 4, p. 600-628, 1996. https://doi.org/10.2307/2393869
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Vocabulário Controlado de Formas Farmacêuticas, Vias de Administração e Embalagens de Medicamentos. Brasília: Anvisa, 2011. Disponível em: http://www.atfmaster.com.br/vocabulario_medicamentos.pdf. Acesso em: 4 ago. 2021
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). 2004. Instrução Normativa 04/2014. Dispõe sobre o processo de contratação de Soluções de Tecnologia da Informação pelos órgãos integrantes do Sistema de Administração dos Recursos de Tecnologia da Informação – SISP do Poder Executivo Federal. Disponível em: https://www.gov.br/governodigital/pt-br/legislacao/IN42014Completa.pdf. Acesso em: 4 ago. 2021.
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Nota técnica nº 02/2018/GHCOS/DIARE/ANVISA. 2017. Disponível em: https://www.gov.br/anvisa/pt-br/setorregulado/regularizacao/cosmeticos/notas-tecnicas/produtos-na-forma-de-spray-continuo-bag-on-valve-ou-bov-para-o-publico-infantil#:~:text=Segundo%20o%20Art.,cosm%C3%A9ticos%2C%20saneantes%20e%20outros%20produtos%3A&text=15%3A%20%E2%80%9COs%20produtos%20infantis%20n%C3%A3o,sob%20a%20forma%20de%20aerossol%E2%80%9D. Acesso em: 4 ago. 2021.
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Documentos de instrução. 2017. Disponível em: https://www9.anvisa.gov.br/peticionamento/sat/Consultas/ConsultaAssuntoCheckList.asp?pCoAssunto=150&sArea=Medicamento. Acesso em: 12 mar. 2021.
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Farmacopeia Brasileira. 6. ed. Brasília: Ministério da Saúde, 2019. Disponível em: https://www.gov.br/anvisa/pt-br/assuntos/farmacopeia/farmacopeia-brasileira. Acesso em: 2 fev. 2022.
BRASIL OCUPA 25ª posição no ranking mundial de pesquisas clínicas. Medicina S/A, 2020. Disponível em: https://medicinasa.com.br/brasil-pesquisas-clinicas/. Acesso em: 3 ago. 2021.
BUSHMAN, B. S.; PHILLIPS, B.; ISBELL, T.; OU, B.; CRANE, J. M.; KNAPP, S. J. Chemical composition of caneberry (Rubus spp.) seeds and oils and their antioxidant potential. Journal of Agricultural and Food Chemistry, v. 52, n. 26, p. 7982-7987, 2004. https://doi.org/10.1021/jf049149a
BUSSMANN, L. A. S. Open innovation: the case of small and new financial technology firms in Brazil. Tese (doutorado CDAE) – Fundação Getulio Vargas, Escola de Administração de Empresas de São Paulo, São Paulo, 2020. Disponível em: https://bibliotecadigital.fgv.br/dspace/handle/10438/29791. Acesso em: 4 ago. 2021.
CARESATTO, C.; OLIVEIRA, F. A. A. Farmacotécnica alopática e homeopática: do conhecimento à realização. São Paulo: Senac, 2019.
CASTANHA-DA-ÍNDIA. Herbarium Laboratório Botânico. 2014. Bula. Disponível em: http://200.199.142.163:8002/FOTOS_TRATADAS_SITE_14-03-2016/bulas/2686.pdf. Acesso em: 4 ago. 2021.
CHESBROUGH, H. W.; VANHAVERBEKE, W.; WEST, J. Novas fronteiras em inovação aberta. São Paulo: Blucher, 2017.
CHESBROUGH, H. W. Open innovation: the new imperative for creating and profiting from technology. Cambridge: Harvard Business School Press, 2003.
CHESBROUGH, H. W.; TEECE, D. J. When is virtual virtuous? Harvard Business Review, Brighton, v. 74, n. 1, p. 65-73, 1996.
COHEN, W. M.; LEVINTHAL, D. A. Absorptive Capacity: A New Perspective on Learning and Innovation. Administrative Science Quarterly, v. 35, n. 1, p. 128-152, 1990. https://doi.org/10.2307/2393553
CONFORTO, E. C.; AMARAL, D. C.; SILVA, S. L. Roteiro para revisão bibliográfica sistemática: aplicação no desenvolvimento de produtos e gerenciamento de projetos. In: CONGRESSO BRASILEIRO DE GESTÃO DE DESENVOLVIMENTO DE PRODUTO, 8, 2011, Porto Alegre. Anais […]. Porto Alegre: CBGDP, 2011.
CRUZ, G. M. G.; SANTANA, J. L.; SANTANA, S. K. A. A.; FERREIRA, R. M. R. S.; NEVES, P. M.; FARIA, M. N. Z. Doenças anais concomitantes à doença hemorroidária: revisão de 1.122 pacientes. Revista Brasileira de Coloproctologia, v. 26, n. 3, p. 369-376, 2006. Disponível em: http://www.jcol.org.br/pdfs/26_4/01.pdf. Acesso em: 27 abr 2020.
CUPANI, A. La peculiaridade del conocimiento tecnológico. Scientiæ Studia, v. 4, n. 3, p. 353-71, 2006. Disponível em: https://www.scielo.br/j/ss/a/STXgdYmmHXL4Qjcb5xYqrDm/?format=pdf&lang=es. Acesso em: 4 ago. 2021.
DUTRÉNIT, G. The transition from building‐up innovative technological capabilities to leadership by latecomer firms. Asian Journal of Technology Innovation, v. 15, n. 2, p. 125-149, 2007. https://doi.org/10.1080/19761597.2007.9668640
EMULFEEL® SSC PLUS. Prospector [Internet]. 2021. Disponível em: https://www.ulprospector.com/en/na/PersonalCare/Detail/6823/640878/Emulfeel-SSC-Plus. Acesso em: 4 ago. 2021.
ESTEVES, C. O.; RODRIGUES, R. M.; MARTINS, A. L D.; VIEIRA, R. A.; BARBOSA, J. L.; VILELA, J. B. S. Medicamentos fitoterápicos: Prevalência, vantagens e desvantagens de uso na prática clínica e perfil e avaliação dos usuários. Revista de Medicina, v. 99, n. 5, p. 463-472, 2020. https://doi.org/10.11606/issn.1679-9836.v99i5p463-472
FIGUEIREDO, P. N. Gestão da inovação: conceitos, métricas e experiências de empresas no Brasil. Rio de Janeiro: LTC, 2009.
FIOCRUZ CAMPUS VIRTUAL. Dificuldades, entraves e desafios da cadeia produtiva de Medicamentos da Biodiversidade. Fiocruz [Internet]. 2021. Disponível em: https://mooc.campusvirtual.fiocruz.br/rea/medicamentos-da-biodiversidade/dificuldades_entraves_e_desafios_da_cadeia_produtiva_de_medicamentos_da_biodiversidade.html. Acesso em: 4 ago. 2021.
FORTICAL: calcitonin salmon spray, metered Physicians Total Care, Inc. Medlibrary, 2010. Disponível em: https://medlibrary.org/lib/rx/meds/fortical/. Acesso em: 2 ago. 2021.
FREITAS JUNIOR, V.; CECI, F.; WOSZEZENKI, C. R.; GONÇALVES, A. L. Design Science Research Methodology Enquanto Estratégia Metodológica para a Pesquisa Tecnológica. Revista Espacios, v. 38, n. 6, p. 25, 2017. Disponível em: https://www.revistaespacios.com/a17v38n06/17380625.html. Acesso em: 4 ago. 2021.
GIL, A. C. Como elaborar projetos de pesquisa. 4. ed. São Paulo: Atlas, 2002.
GLOSSÁRIO de ingredientes. Nívea, 2021. Disponível em: https://www.nivea.com.br/sobre-nos/sustentabilidade-nivea/glossario-ingredientes. Acesso em: 4 ago. 2021.
GUIDO, R. V. C.; ANDRICOPULO, A. D.; OLIVA, G. Planejamento de fármacos, biotecnologia e química medicinal: aplicações em doenças infecciosas. Estudos Avançados, v. 24, n. 70, 2010. https://doi.org/10.1590/S0103-40142010000300006
IBERO MAGISTRAL. Alcaçuz extrato seco: Fitoterápico. 2019. Disponível em: https://www.iberomagistral.com.br/Arquivos/Insumo/arquivo-090506.pdf. Acesso em: 21 jan. 2022.
IFTIKHAR, N. What Is Allopathic Medicine? Healthline, 2019. Disponível em: https://www.healthline.com/health/allopathic-medicine. Acesso em: 2 ago. 2021.
INTERFARMA (Associação da Indústria Farmacêutica de Pesquisa). Guia 2020 Interfarma. 2020. Disponível em: https://www.interfarma.org.br/app/uploads/2020/12/2020_VD_JAN.pdf. Acesso em: 4 ago. 2021.
INSTITUTO NACIONAL DO CÂNCER (INCA). Síntese de Resultados e Comentários – Estimativa 2020. [Internet]. 2020. Disponível em: https://www.inca.gov.br/estimativa/sintese-de-resultados-e-comentarios. Acesso em: 4 ago. 2021.
KAUR, R.; KAUR, H.; DHINDSA, A. S. Glycyrrhiza glabra: a phytopharmacological review. International Journal of Pharmaceutical Sciences and Research, v. 4, n. 7, p. 2470-2477, 2013. https://doi.org/10.13040/IJPSR.0975-8232.4(7).2470-77
LEONHARDT, C. Qual a diferença entre testes de bancada, planta-piloto e industrial? Sra. Inovadeira [Internet]. 2017. Disponível em: https://srainovadeira.com.br/diferenca-testes-bancada-planta-piloto-industrial/. Acesso em: 4 ago. 2021.
MARCH, S. T.; SMITH, G. Design and natural science research on information technology. Decision Support Systems, v. 15, n. 4, p. 251-266, 1995.
MARCH, S. T.; STOREY, V. C. Design science in the information systems discipline: an introduction to the special issue on design science research. MIS Quarterly, v. 32, n. 4, p. 725-730, 2008.
MACHADO, L.; FREITAS JUNIOR, J. C. S.; KLEIN, A. Z.; FREITAS, A. S. A Design Research como método de pesquisa de Administração: Aplicações práticas e lições aprendidas. In XXXVII Encontro da ANPAD, 2013. Anais […]. Rio de Janeiro. Disponível em: http://www.anpad.org.br/diversos/down_zips/68/2013_EnANPAD_EPQ748.pdf. Acesso em: 4 ago. 2021.
NAHAS, T. As fases da pesquisa clínica. Ciência da mídia [Internet]. 2013. Disponível em: https://ciencianamidia.wordpress.com/2013/12/16/as-fases-da-pesquisa-clinica/. Acesso em: 4 ago. 2021.
NOOTEBOOM, B. Innovation and inter-firm linkages: new implications for policy. Research Policy, v. 28, p. 793–805, 1999. Disponível em: https://research.rug.nl/en/publications/innovation-and-inter-firm-linkages-new-implications-for-policy. Acesso em: 4 ago. 2021.
ÓLEO DE BURITI. Mapric. Bula. 1996. Disponível em: https://mapric.com.br/pdf/Boletim924_01092014-09h17.pdf. Acesso em: 4 ago. 2021.
OOMAH, D. B.; LADET, S.; GODFREY, D., V.; LIANG, J.; GIRARD, B. Characteristics of raspberry (Rubus idaeus L.) seed oil. Food and Chemistry, v. 69, n. 2, p.187-193, 2000. https://doi.org/10.1016/S0308-8146(99)00260-5
OPEN INNOVATION no Brasil: panorama e cenário atual. Distrito [Internet]. 2020. Disponível em: https://distrito.me/open-innovation-quais-startups-podem-me-ajudar/. Acesso em: 4 ago. 2021.
PEDRINHO, G. C.; CARVALHO, D. N.; TEIXEIRA, C. S.; LEZANA, Á. G. R. Universidade e o ecossistema de inovação: revisão estruturada de literatura. Revista de Gestão e Tecnologia, v. 10, n. 1, p. 1-23, 2020. Disponível em: https://dialnet.unirioja.es/servlet/articulo?codigo=7774806. Acesso em: 4 ago. 2021.
PEFFERS, K.; TUUNANEN, T; ROTHENBERGER, M. A.; CHATTERJEE, S. A Design Science Research Methodology for Information Systems Research. Journal of Management Information Systems, v. 24, n. 3, p.45-77, 2007.
PEREIRA, O. Á. Dicionário de Substâncias Farmacêuticas Comerciais. Rio de Janeiro: Abiquif, 2013. Disponível em: https://www.labnetwork.com.br/wordpress/wp-content/uploads/2014/03/subst%C3%A2ncias-farmac%C3%AAuticas2.pdf. Acesso em: 2 ago. 2021.
PERINAL Cutaneous Spray. Hitchin: Dermal Laboratories Limited, 2020. Bula. Disponível em: https://www.medicines.org.uk/emc/product/3762/smpc. Acesso em: 08 abr. 2020.
PITASSI, C. Inovação aberta na perspectiva das empresas brasileiras de base tecnológica: proposta de articulação conceitual. Revista de Administração e Inovação, v. 9, n. 3, p. 77-102, 2012.
PRAHALAD, C. K.; HAMEL, G. The Core Competence of the Corporation. Harvard Business Review, 1990. Disponível em: https://hbr.org/1990/05/the-core-competence-of-the-corporation. Acesso em: 2 ago. 2021.
PROPELLANT. Encyclopedia Britannica, Inc., 2019. Disponível em: https://www.britannica.com/science/propellant. Acesso em: 4 ago. 2021.
ROBERTSON, S. Epidemiology of Hemorrhoids. News Medical Life Science [Internet]. 2019. Disponível em: https://www.news-medical.net/health/Epidemiology-of-Hemorrhoids.aspx#:~:text=Worldwide%2C%20the%20overall%20prevalence%20of,is%20estimated%20to%20be%204.4%25. Acesso em: 18 jan. 2022.
SALLES, R. Remédios para tratar hemorroida: supositório, pomada, cuidados caseiros e mais. Ativo Saúde [Internet]. 2019. Disponível em: https://www.ativosaude.com/saude/remedios-para-hemorroida/. Acesso em: 29 abr. 2020.
SANTOS, I. N. S. D. G.; QUEIROZ, S. C.; LUTOSA, S. R.; BENEVIDES, G. Bi – gel: desenvolvimento de um novo conceito de cosméticos sem emulsionante. Infarma-Ciências Farmacêuticas, v. 22, n. 1-4, p. 61-66, 2010.
SOBRADO, C. W. Tratamento tópico das doenças anorretais. Revista Brasileira de Medicina, v. 71, n. 1-2, 2014.
SOCIEDADE BRASILEIRA DE COLOPROCTOLOGIA (SBCP). 2016. Disponível em: https://sbcp.org.br/. Acesso em: 4 ago. 2021.
SOLVENT. Encyclopedia Britannica, Inc. 2019. Disponível em: https://www.britannica.com/science/solvent-chemistry. Acesso em: 4 ago. 2021.
SPINA, G.; VERGANTI, R.; ZOTTERI, G. A model of co-design relationships: definitions and contingencies. International Journal of Technology Management, v. 23, n. 4, 2002. https://doi.org/10.1504/IJTM.2002.003012
TRANSCUTOL P: Solubilizante. Presidente Prudente: Botica Magistral. Bula. Disponível em: http://sistema.boticamagistral.com.br/app/webroot/img/files/transcutol%20p.pdf. Acesso em: 10 mar. 2021.
TRIGLICÉRIDES de ácido cáprico/caprílico – (TCM). Maian Food [Internet]. 2021. Disponível em: https://maian.com.br/en/services/triglicerides-de-acido/. Acesso em: 4 ago. 2021.
VASCONCELOS, L. O. B. P. Inovação aberta e propriedade intelectual no segmento de fitoterápicos. 2018. Monografia (Especialização) – Instituto de Tecnologia em Fármacos – Farmanguinhos. Pós-Graduação em Gestão da Inovação em Fitomedicamento, Rio de Janeiro, 2018. Disponível em: https://www.arca.fiocruz.br/bitstream/icict/34914/2/luis_otavio_barreto_portella_de.pdf. Acesso em: 4 ago. 2021.
VAISHNAVI, V.; KUECHLER, B.; PETTE, S. Design science research in information systems. Association for informations systems, 2004. Disponível em: http://desrist.org/design-research-in-information-systems/. Acesso em: 20 jan. 2022.
VENOCUR® FIT. Abbott Laboratórios do Brasil. 2004. Bula. Disponível em: https://dam.abbott.com/pt-br/documents/pdfs/nossas-bulas/v/BU%2004_Venocur%20fit_paciente.pdf. Acesso em: 4 ago. 2021.
WALD, A.; BHARUCHA, A. E.; COSMAN, B. C.; WHITEHEAD, W. E. ACG clinical guideline: management of benign anorectal disorders. The American Journal of Gastroenterology, v. 109, n. 8, p. 1141-1157, 2014. https://doi.org/10.1038/ajg.2014.190
WOOD-BLACK, F. Considerations for Scale-Up – Moving from the Bench to the Pilot Plant to Full Production. In: M. K. Moore, E. B. Ledesma. Academia and Industrial Pilot Plant Operations and Safety. Washington: ACS, 2014. https://doi.org/10.1021/bk-2014-1163.ch003
