CORRELATION OF DIABETES MELLITUS WITH DEMENTIA SYNDROMES IN THE ELDERLY
REGISTRO DOI: 10.5281/zenodo.10155720
Bruna Caroline Ribeiro Beltrão1
Karla Emília Lima da Silveira1
Maria Fernanda Araujo de Miranda1
Thiago de Souza Lopes Araújo2
RESUMO
Introdução: O envelhecimento pode ser estudado através dos prismas da senescência e senilidade; este último corresponde a condições que acometem o indivíduo no decorrer da vida, ocasionado por processos fisiopatológicos como o diabetes mellitus (DM). Segundo dados de 2021 da Federação Internacional de Diabetes (IDF), cerca de 537 milhões de adultos entre 20 e 79 anos vivem com DM. Esta condição foi associada pelo The World Alzheimer Report (WAR) ao risco de várias formas de demência. Objetivos: O objetivo deste estudo foi realizar uma revisão sistemática da literatura, a fim de compreender a correlação entre o DM e o aparecimento das síndromes demenciais na população idosa. Metodologia: Realizou-se a busca por publicações através da combinação dos descritores “diabetes mellitus”, “demência” e “idoso” com o operador booleano AND, no intervalo de tempo de 2017 a 2022. Resultados e discussão: Os artigos avaliados encontraram uma associação entre o DM e o desenvolvimento de demência e/ou um pior funcionamento cognitivo com o decorrer da idade, estando associados ou não a outras doenças como hipertensão. Conclusão: Os danos associados à progressão da demência no cérebro e as anormalidades na sinalização insulínica parecem estar intimamente conectadas com a formação de placas senis, demonstrando que qualquer desbalanço na atividade insulínica pode acarretar danos cerebrais e desencadear processos neurodegenerativos.
Palavras-chave: Diabetes Mellitus; Demência; Idoso.
Abstract
Introduction: Aging can be studied through the perspectives of senescence and senility; the latter corresponds to conditions that affect individuals throughout their lives, caused by pathophysiological processes such as diabetes mellitus (DM). According to 2021 data from the International Diabetes Federation (IDF), around 537 million adults aged 20 to 79 live with DM. This condition has been associated by The World Alzheimer Report (WAR) with the risk of several forms of dementia. Objectives: The objective of this study was to carry out a systematic review of the literature, in order to understand the correlation between DM and the appearance of dementia syndromes in the elderly population. Methodology: A search for publications was carried out by combining the descriptors “diabetes mellitus”, “dementia” and “elderly” with the boolean operator AND, in the time range from 2017 to 2022. Results: The articles evaluated found an association between DM and the development of dementia and/or worse cognitive functioning with age, whether or not associated with other diseases such as hypertension. Conclusion: The damage associated with the progression of dementia in the brain and abnormalities in insulin signaling appear to be closely connected with the formation of senile plaques, demonstrating that any imbalance in insulin activity can lead to brain damage and trigger neurodegenerative processes.
Keywords: Diabetes Mellitus; Insanity; Elderly.
INTRODUÇÃO
A expectativa de vida dos brasileiros teve um aumento significativo na última década. Segundo dados do IBGE (2018) a população com mais de 60 anos era de 25,4 milhões no ano de 2012 e em cinco anos houve um incremento de 4,8 milhões de novos idosos, um crescimento de 18% neste grupo etário, que tem se tornado cada vez mais representativo no Brasil. Ademais, as mulheres são maioria expressiva nesse grupo, com 16,9 milhões (56%), enquanto os homens são 13,3 milhões (44%).1 O processo de envelhecimento é construído pelo prisma da história a partir de crenças, atitudes e valores socioculturais de uma sociedade. No entanto, ainda é relacionado às perspectivas negativas, como incapacidade e dependência, anulando o valor do sujeito.2
O processo de envelhecimento pode ser estudado por meio de dois conceitos bastante abordados na atualidade: senescência e senilidade. O primeiro está ligado a todas as mudanças que ocorrem no organismo humano no decorrer do tempo, sem estar relacionado a patologias, correspondendo às alterações fisiológicas naturais do envelhecimento. A exemplo da senescência tem-se o surgimento de cabelos brancos ou sua queda, a perda da elasticidade da pele, o aparecimento de rugas, perda de massa muscular e diminuição da estatura. Já o segundo conceito é definido como condições que acometem o indivíduo no decorrer da vida, ocasionado por processos fisiopatológicos, tais como hipertensão arterial sistêmica, diabetes mellitus (DM), insuficiência renal, insuficiência cardíaca e outras.2
O aumento da expectativa de vida reflete no crescimento das doenças crônicas e degenerativas que afetam principalmente os idosos, como DM e síndromes demenciais, e, diante do aumento dessas doenças, haverá um grande desafio para o sistema de saúde pública nacional, visto que, com o decorrer da idade maior é a necessidade de cuidados especializados e consequente redução da participação social, podendo afetar negativamente o período de senescência. Com isso, é necessária maior atenção por parte dos Órgãos Públicos, sobretudo, no que tange Atenção Primária à Saúde, a fim de estabelecer estratégias para monitorar doenças que podem acometer os idosos de forma frequente e tornar o atendimento mais ágil e inclusivo.2
Segundo dados da Federação Internacional de Diabetes (IDF), cerca de 537 milhões de adultos entre 20 e 79 anos vivem com DM, numa proporção de 1 em cada 10 pessoas. A estimativa é que esse número se eleve para 643 milhões no ano de 2030 e 783 milhões em 2045.3 O cálculo do total de portadores de DM (20-79 anos) no Brasil em 2017 era de 12,5 milhões, o equivalente a quase 6% da população brasileira. Na comunidade idosa, a prevalência de DM é de 16,1%. O aumento da prevalência do diabetes no Brasil e no mundo deriva de fatores diversos, como a rápida urbanização, transição nutricional, estilo de vida sedentário, excesso de peso, crescimento e envelhecimento populacional, bem como a maior sobrevida de indivíduos com DM. Dessa maneira, com a maior quantidade de indivíduos diabéticos tem-se uma associação com a elevação de taxas de hospitalizações e utilização dos serviços de saúde, bem como maior incidência de doenças e eventos cerebrovasculares, cegueira, insuficiência renal e amputações de membros inferiores, proporcionando maior sobrecarga aos serviços de saúde.4
Em 2014, o The World Alzheimer Report (WAR) concluiu que o DM em idade avançada, e possivelmente meia-idade, está associado a um risco aumentado de várias formas de demência. Esta, por sua vez, afetou 47 milhões de pessoas em todo o mundo em 2015, 60% das quais em países de baixa e média renda. Em 2030, estima-se que esse número chegará a 75 milhões. Embora a demência seja mais comum em pessoas idosas, ela não é uma parte natural do processo de envelhecimento.5
A demência é uma doença caracterizada pelo declínio cognitivo envolvendo um ou mais domínios (linguagem, aprendizagem, cognição social, função físico-perceptivo-motora, concentração e memória). O déficit deve representar um declínio de um nível anterior de funcionamento e ser grave o suficiente para interferir na performance diária e na independência do ser humano. A demência mais comum entre os idosos é a decorrente da doença de Alzheimer (DA), que responde por 60 a 80% dos casos. A porcentagem geral de demência está aumentando à medida que a população envelhece. Com o envelhecimento populacional e o aumento da conscientização sobre a DA e outras síndromes demenciais de início tardio, os profissionais da saúde devem estar preparados para avaliar o comprometimento cognitivo da população e questionar sobre o declínio funcional de cada pessoa para evitar falhas no reconhecimento das demências.6
Assim, observa-se uma relação entre DM e demência, que logo podem ser vistas como acometimentos que atingem grande parcela da população, principalmente os idosos. As disfunções características do DM como fator de risco para o comprometimento cognitivo em indivíduos idosos, representam uma lacuna potencial no campo científico, já que, as pesquisas sobre esse tema assumem uma postura dicotômica. Portanto, objetiva-se com esse estudo analisar a correlação entre o Diabetes Mellitus e o aparecimento das síndromes demenciais na população idosa, bem como suas possíveis complicações.
METODOLOGIA
Este trabalho configura-se como uma revisão integrativa qualitativa de caráter explicativo. Segundo Marconi (2022), a revisão bibliográfica é essencial para delimitar a linha limítrofe da pesquisa que se pretende desenvolver, considerando uma visão científica. Elaborada de acordo com o material já produzido como artigos, livros, e teses, a pesquisa bibliográfica possui aspecto exploratório, uma vez que proporciona uma maior proximidade com o assunto, aprimoramento de ideias ou descoberta de intuições.7 Nesse viés, é preciso retratar os tópicos principais, autores, palavras, periódicos e fontes de dados preliminares.
Realizou-se a busca por publicações através da combinação dos descritores “diabetes mellitus”, “demência” e “idoso” com o operador booleano AND, no intervalo de tempo de 2017 a 2022. Foram preferidas as referências obtidas em bases de dados científicas como: Scientific Electronic Library Online (SCIELO), Literatura Latino-americana e do Caribe em Ciências da Saúde (LILACS), PUBMED, Google Acadêmico, bem como o uso de literaturas clássicas, como livros e documentações oficiais do Ministério da Saúde.
Desse modo, após a leitura dos títulos dos trabalhos e aplicação dos critérios de elegibilidade, conforme a Figura 1, foi realizada a seleção dos artigos que melhor se aplicam ao problema estudado. Após essa etapa foi feita a leitura dos resumos e escolhidos artigos que correspondem ao tema pretendido neste trabalho.
Figura 1 – Fluxograma e critérios de seleção e inclusão dos trabalhos.
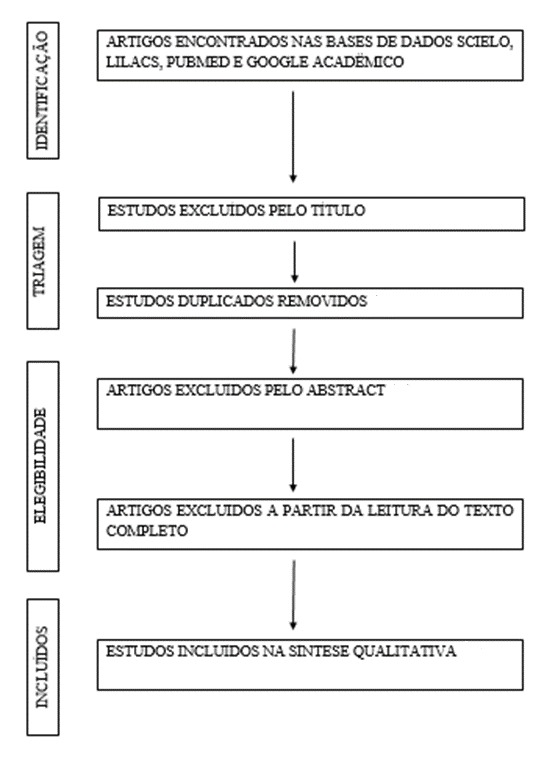
Fonte: Autoria própria
RESULTADOS
Após a seleção dos artigos incluídos na avaliação, esses foram os principais resultados obtidos:
Tabela 1 – Demonstrativo dos artigos que integram a revisão sistemática
DISCUSSÃO
O objetivo do presente estudo foi realizar uma revisão sistemática da literatura, a fim de compreender a correlação entre o Diabetes Mellitus e o aparecimento das síndromes demenciais na população idosa, bem como as consequências decorrentes dessa associação.
O envelhecimento populacional ocorre de modo acelerado no Brasil e com esse aumento da expectativa de vida, as doenças crônicas não transmissíveis (DCNT), como a DM e a demência, evidenciam-se como importante obstáculo para a saúde pública, no que tange a sua relação com a alta morbidade que originam. Essas enfermidades podem causar sérios graus de inaptidão que impactam tanto os hábitos de vida como o bem-estar do sujeito. Números acerca da morbimortalidade por DM manifestam a relevância da doença como um obstáculo de saúde pública na sociedade brasileira, sendo que cerca de 20% da população idosa possui DM, apresentando altas taxas de morte prematura, incapacidade funcional, perda muscular acelerada e patologias coexistentes.8
Ainda, em 2002, as DCNT foram responsáveis por quase 60% das mortes. Cerca de 80% dos idosos têm pelo menos uma doença crônica e 50% têm duas ou mais. Dentre as doenças não transmissíveis relacionadas ao envelhecimento, a demência se destaca como a principal causa de disfunção e qualidade da vida em idosos. Segundo a OMS, mais de 35 milhões de pessoas em todo o mundo sofriam de alguma forma de demência, em 2012, e esse número pode triplicar e alcançar mais de 115 milhões até 2050.8
Segundo Louis et al. a demência é caracterizada por um declínio na inteligência, que pode ser acompanhado por um declínio na independência e no funcionamento social ou ocupacional diário. Vários domínios cognitivos podem ser afetados, principalmente, em diferentes tipos de demência, incluindo memória, orientação, abstração, capacidade de aprendizado, percepção visuoespacial, função da linguagem, prática construtiva e funções executivas superiores, como planejamento, organização e sequenciamento de atividades. Porém, a demência muitas vezes não é diagnosticada na presença de dano de domínio único, exigindo danos significativos em pelo menos dois domínios e um declínio significativo na execução de tarefas em casa ou no trabalho.9
Desse modo, a classificação mais útil da demência atualmente é baseada na patogênese da doença. Por meio de correlações clínico-patológicas, hoje é possível estabelecer um diagnóstico específico ao longo da vida de um indivíduo com acurácia de 75% a 85%. É importante reconhecer que mesmo com uma excelente história clínica, exame e estudos auxiliares, a patogênese no diagnóstico clínico de demência não terá sensibilidade ou especificidade perfeitas. As demências são melhores categorizadas em etiologia como endócrinas, metabólicas, cerebrovasculares, inflamatórias, infecciosas, estruturais ou neurodegenerativas. A última categoria é caracterizada pela ausência das etiologias supracitadas. A causa mais comum de demência entre idosos é a doença neurodegenerativa. Eles incluem a doença de Alzheimer, demência com corpos de Lewy, demência frontotemporal e demência vascular.9
Primeiramente, a doença de Alzheimer, com perda de forma proeminente da memória e da linguagem, constitui a forma mais frequente de demência no indivíduo idoso, por cerca de 80% do número total de pacientes em séries de necropsia, clínicas ou populacionais. Na concepção estrutural, essa afecção caracteriza-se por dano temporal e parietal. Em nível molecular, configura-se como “amiloidopatia”, já que a particularidade mais específica consiste em depósitos anormais de β-amiloide em placas, além da proteína tau hiperfosforilada menos específica, evidente em emaranhados neurofibrilares.9
Já a demência com corpos de Lewy constitui a segunda causa mais frequente de demência no indivíduo idoso. Ela é caracterizada, clinicamente, pela presença de corpos de Lewy tanto em regiões corticais como em áreas subcorticais do encéfalo. A sua sintomatologia inclui: declínio cognitivo progressivo, alucinações visuais recorrentes, flutuação no estado cognitivo e sinais parkinsonianos.20 Observa-se maior sensibilidade a efeitos indesejáveis de medicamentos neurolépticos e a resposta a medicações inibidoras da acetilcolinesterase é geralmente boa. Do ponto de vista patológico, a presença de corpos de Lewy com composição molecular principalmente de alfassinucleína levou ao termo sinucleinopatia.9,18
Ademais, em alguns cérebros de pacientes com demência com corpos de Levy, corpos de Lewy podem coexistir com placas senis e emaranhados neurofibrilares, estruturas que são abundantes na doença de Alzheimer, e nos cérebros de pacientes mais velhos sem demência.21 No entanto, a descoberta dos corpos de Levy não se limita à demência com corpos de Levy: podemos observá-los em menor grau no processo de senescência e na doença de Alzheimer. Ela também é encontrada nos encéfalos de demência com corpos de Lewy: perda regional de neurônios; microvacuolação (alterações semelhantes a esponjas); perda de sinapses; anormalidades neuroquímicas; e deficiências de neurotransmissores.9,19
Já as demências frontotemporais representam um grupo molecularmente heterogêneo de doenças degenerativas caracterizadas pela degeneração dos lobos frontal e temporal. A degeneração frontotemporal geralmente se apresenta na década de 50 e é responsável por 5 a 10 por cento dos casos. Em casos típicos, as manifestações incluem distúrbios comportamentais do tipo frontal (desinibição, apatia, inconveniência social, transtorno obsessivo-compulsivo) e distúrbios de linguagem.22 A patologia molecular deste grupo de doenças pode ser amplamente dividida entre aquelas envolvendo a proteína tau e aquelas envolvendo a proteína TDP-43 (TAR 43 DNA-binding protein), com papéis menores para as proteínas FUS, CHMP3 ou VCP.9
E ainda, doença cerebrovascular é atualmente considerada uma das principais causas de demência. Síndromes de demência de infarto estratégico, demência de múltiplos infartos, doença isquêmica grave da substância branca (doença de Binswanger ou demência arteriosclerótica subcortical) e encefalopatia hemorrágica podem causar demência.23 O AVC agudo é uma causa comum de comprometimento cognitivo, mas não se manifesta como demência progressiva; de fato, os déficits cognitivos são acompanhados por déficits neurológicos focais agudos, ou podem ser seguidos por um curso contínuo com lesões marcadas e incapacidade.9
Além disso, vale ressaltar que, a predominância de DM é estimulada por uma complexa relação de fatores socioeconômicos, demográficos, ambientais, genéticos e comportamentais. Elevações progressivas na adesão de modos de vida pouco saudáveis e a crescente urbanização respondem de forma relevante pelo crescimento da incidência e prevalência do diabetes no Brasil. Complicações crônicas podem expressar nos pacientes com diabetes, sobretudo nos idosos, já no momento do diagnóstico.10
Convém lembrar que, o processo de envelhecimento, sobretudo, a senilidade está acompanhada de patologias que aumentam esse processo de degeneração do organismo. A exemplo disso, tem-se a DM2, a qual está muito relacionada a um risco maior de morte prematura, a maior associação com outras comorbidades e, principalmente, com as grandes síndromes geriátricas, sendo importante salientar os prejuízos em relação à capacidade funcional, autonomia e qualidade de vida, o que a configura como uma afecção de alto impacto, com repercussões sobre o sistema de saúde, família e o próprio idoso acometido.11
Enquanto isso, a diabetes tipo 2 é responsável por 90 a 95% de todos os casos de diabetes no mundo. Os fatores de risco associados são obesidade, hipertensão arterial e dislipidemia, sedentarismo, diagnóstico precoce de diabetes ou diabetes gestacional, histórico familiar e o aumento da idade. Na maioria das vezes, a doença é assintomática ou oligossintomática, por um longo período e situações como a cetoacidose diabética, que pode ser comum na DM1 em indivíduos não diagnosticados, raramente ocorre na DM2, pois ainda há produção de insulina, mesmo que sua ação seja diminuída. Dessa forma, nos estágios iniciais da doença o paciente pode não perceber os sintomas clássicos, permitindo que a doença siga seu curso. No entanto, uma vez instaurada a hiperglicemia os pacientes correm o risco de desenvolver complicações crônicas.3,4
Logo, as principais complicações relacionadas ao diabetes são categorizadas em distúrbios micro e macrovasculares, os quais resultam em retinopatia, nefropatia, neuropatia periférica, doenças coronarianas e cerebrovasculares e doença arterial periférica. Além disso, a incidência de outras doenças crônicas, como a hipertensão arterial, aumenta em indivíduos diabéticos.21
Para tanto, o alto risco no desenvolvimento da DM2 em idosos advém da combinação da influência genética, estilo de vida e envelhecimento, os quais contribuem para a hiperglicemia através da diminuição da capacidade secretória das células β e da já citada intolerância periférica à insulina. Esses fatores são característicos do envelhecimento por si só, mas a exposição crônica à hiperglicemia e a toxicidade glicêmica pioram a resistência à insulina e prejudicam mais ainda as células pancreáticas.12,16
Além disso, pacientes idosos frequentemente sofrem de outras comorbidades geriátricas que contribuem para um aumento da fragilidade. A diabetes, que, isoladamente, constitui alto fator de risco cardiovascular e cerebrovascular, acrescenta um peso a mais a esta conta, podendo provocar graves limitações como artropatias, cegueira e a possibilidade de amputações nos membros inferiores. Ademais, o idoso diabético, em comparação com o não diabético, está mais sujeito à polifarmácia, doença renal crônica, perda funcional (fraqueza muscular, debilidade de marcha, fraturas, ferimentos graves, etc.) problemas cognitivos e queda, desgastando a saúde física e mental do indivíduo.13
Nesse ínterim, a ADA (2021), traz algumas das condições geriátricas mais comuns que podem ser agravadas pelo diabetes, entre elas a sarcopenia, depressão e disfunção cognitiva.14 A sarcopenia, caracterizada pela perda de massa muscular própria do avanço da idade é acelerada no quadro de DM, tornando o paciente mais propenso a quedas e fraturas, impondo uma modificação de seu estilo de vida e maior dependência. Esse quadro está intimamente ligado ao desenvolvimento de depressão, comprometimento cognitivo e um risco 1,6 maior de demência futura. 12,14
Assim, conforme uma meta-análise realizada por Gudala e colaboradores acerca do risco de demência em indivíduos com diabetes, houve um aumento de 73% no risco de todos os tipos de demência, 56% em Alzheimer e 127% em demências vasculares, correlacionado ao risco inerente de doenças cerebrovasculares causadas pelo DM. Alguns dos mecanismos mencionados foram os efeitos tóxicos da hiperglicemia, resistência à insulina do cérebro, formação de produtos finais de glicação avançada (AGE) e competição pela enzima degradante de insulina (IDE) resultando em degradação reduzida de β amilóide.15,17
Dessa forma, como mostrado nos dados supracitados, a DM e a demência são patologias que fazem parte do processo de senilidade humana, levando-se a observar uma notória associação destas e suas consequências a curto e longo prazo para o paciente, com prejuízos de cunho fisiológico, social e familiar.
CONCLUSÃO
O objetivo do presente estudo foi realizar uma revisão sistemática qualitativa de caráter explicativo a fim de analisar a correlação entre o diabetes Mellitus e a demência na população idosa, esclarecendo ao público sobre as complicações neurológicas dos pacientes com diabetes. Tal revisão foi elaborada por meio da leitura dos títulos dos trabalhos e aplicados os critérios de inclusão e exclusão, selecionando os artigos que melhor se aplicam ao problema estudado.
Muitos fatores contribuem para a disfunção neurocognitiva, os danos associados à progressão da demência no cérebro, as anormalidades na sinalização insulínica, a resistência à insulina e as alterações metabólicas parecem estar intimamente conectadas com a formação de Placas Senis a partir do acúmulo de β-amilóide e de emaranhados neurofibrilares provenientes da hiperfosforilação da proteína Tau, acarretando em inflamação, lesão neurológica, alterações estruturais e declínio cognitivo, uma vez que a insulina, além de atuar no metabolismo da glicose cerebral e mobilização de GLUT4 para captação de glicose, é capaz de modificar a plasticidade sináptica, facilitar o crescimento de neuritos, ter efeitos neuroprotetores e é responsável pela modulação cognitiva. Portanto, qualquer desbalanceamento na atividade da insulina pode acarretar uma complicação nos mecanismos de reparação, crescimento e diferenciação celulares e, tendo como consequência, desencadeamento dos processos neurodegenerativos.
Os estudos envolvendo a correlação entre DM2 e demência são recentes, e mais estudos são necessários com a finalidade de aprofundar o conhecimento desta condição. Nesse viés, um melhor entendimento da fisiopatologia pode oferecer uma oportunidade de gerar terapias que previnem a progressão da doença e melhoram a qualidade de vida dos pacientes.
REFERÊNCIAS
1. Número de idosos cresce 18% em 5 anos e ultrapassa 30 milhões em 2017. Agência de Notícias [Internet]. Agência de Notícias – IBGE. 2018 [citado2022 Set 5]. Disponível em: https://agenciadenoticias.ibge.gov.br/agencia-noticias/2012-agenciadenoticias/noticias/20980-numero-de-idosos-cresce-18-em-5-anos-e-ultrapassa-30-milhoesem-2017.
2. Freitas, Elizabete Viana de. Tratado de geriatria e gerontologia. 4ª edição. Rio de Janeiro: Guanabara Koogan, 2017.
3. International Diabetes Federation. IDF Diabetes Atlas. 10th edition, 2021 [Internet]. Disponível em: www.diabetesatlas.org.
4. BRASIL. Diretrizes da Sociedade Brasileira de Diabetes 2019-2020. Brasília: Sociedade Brasileira de Diabetes, 2019. 491 p. ISBN: 978-85-93746-02-4.
5. Martin Prince, Emiliano Albanese, Maëlenn Guerchet, Matthew Prina. World Alzheimer Report 2014. Dementia and Risk Reduction: An analysis of protective and modifiable risk factors. [Research Report] Alzheimer’s Disease International. 2014. ffhal-03495430f.
6. Da Silva FG, Da Silva LAM, Oliveira KSM, Vieira JL, Delfino VDFR, Nascimento AG et al. Risco de doença de alzheimer em idosos com diabetes mellitus tipo 2: uma revisão sistemática. Braz. J. Develop. 2021 Aug. 13;7(8):80491-508.
7. Marconi, Marina de, A. e Eva Maria Lakatos. Metodologia Científica. 8ª edição. Minha Biblioteca: Grupo GEN, 2022.
8. Santos C de S dos, Bessa TA de, Xavier AJ. Fatores associados à demência em idosos. Ciência & Saúde Coletiva. 2020 Feb;25(2):603–11.
9. LOUIS, Elan D.; MAYER, Stephan A.; ROWLAND, Lewis P. Merritt. Tratado de Neurologia, 13ª edição. Rio de Janeiro: Grupo GEN, 2018. E-book. ISBN 9788527733908.
10. Francisco, Priscila Maria Stolses Bergamo et al. Diabetes mellitus em idosos, prevalência e incidência: resultados do Estudo Fibra. Revista Brasileira de Geriatria e Gerontologia, v. 25, 2022.
11. Ramos R de SP da S, Marques AP de O, Ramos VP, Borba AK de OT, Aguiar AMA de, Leal MCC. Fatores associados ao diabetes em idosos atendidos em um ambulatório especializado em gerontologia-geriatria. Revista Brasileira de Geriatria e Gerontologia. 2017 maio [citado 2021 jan 9]; 20(3):363–73. Disponível a partir de: https://www.scielo.br/pdf/rbgg/v20n3/1809-9823-rbgg-20-03-00363.pdf. doi.org/10.1590/1981-22562017020.160145
12. Vilar L. Endocrinologia Clínica. (7ª edição). Rio de Janeiro, Guanabara Koogan: Grupo GEN; 2020.
13. Nguyen, H. T. T. et al. Health-related quality of life in elderly diabetic outpatients in Vietnam. Dovepress p. 1347-1354, 2018.
14. American Diabetes Association. Standards of Medical Care in Diabetes-2021 Abridged for Primary Care Providers. Clin Diabetes. 2021 Jan;39(1):14-43. doi: 10.2337/cd21-as01. PMID: 33551551; PMCID: PMC7839613.
15. Gudala K, Bansal D, Schifano F, Bhansali A. Diabetes mellitus and risk of dementia: A meta-analysis of prospective observational studies. J Diabetes Investig. 2013 Nov 27;4(6):640-50. doi: 10.1111/jdi.12087. Epub 2013 Apr 26. PMID: 24843720; PMCID: PMC4020261.
16. Abdelhafiz, AH, and AJ Sinclair. Metabolic phenotypes explain the relationship between dysglycaemia and frailty in older people with type 2 diabetes. Journal of diabetes and its complications vol. 36,4. 2022 Feb; 108144. doi:10.1016/j.jdiacomp.
17. Hadley, Gina et al. “Cognitive decline and diabetes: a systematic review of the neuropathological correlates accounting for cognition at death.” Journal of neurology, neurosurgery, and psychiatry vol. 93,3 (2022): 246-253. doi:10.1136/jnnp-2021-328158
18. Li, Lily et al. “Diabetes Mellitus Increases Risk of Incident Dementia in APOEɛ4 Carriers: A Meta-Analysis.” Journal of Alzheimer’s disease: JAD vol. 74,4 (2020): 1295-1308. doi:10.3233/JAD-191068
19. Li, Xiao-Ying et al. “Midlife Modifiable Risk Factors for Dementia: A Systematic Review and Meta-analysis of 34 Prospective Cohort Studies.” Current Alzheimer research vol. 16,14 (2019): 1254-1268. doi:10.2174/1567205017666200103111253
20. Mohanannair Geethadevi, Gopisankar et al. “Multi-domain prognostic models used in middle-aged adults without known cognitive impairment for predicting subsequent dementia.” The Cochrane database of systematic reviews vol. 6,6 CD014885. 2 Jun. 2023, doi:10.1002/14651858.CD014885.pub2.
21. Niermeyer, Madison A. “Cognitive and gait decrements among non-demented older adults with Type 2 diabetes or hypertension: a systematic review.” The Clinical neuropsychologist vol. 32,7 (2018): 1256-1281. doi:10.1080/13854046.2017.1414306.
22. Papunen, Sanna et al. “The association between diabetes and cognitive changes during aging.” Scandinavian journal of primary health care vol. 38,3 (2020): 281-290. doi:10.1080/02813432.2020.1802140
23. You, Yue et al. “The prevalence of mild cognitive impairment in type 2 diabetes mellitus patients: a systematic review and meta-analysis.” Acta diabetologica vol. 58,6 (2021): 671-685. doi:10.1007/s00592-020-01648-9.
1 Acadêmica do Curso de Graduação em Medicina pelo Instituto de Educação Superior do Vale do Parnaíba (IESVAP), Parnaíba, Piauí.
2 Professor, Doutor do Curso de Graduação em Medicina pelo Instituto de Educação Superior do Vale do Parnaíba (IESVAP), Parnaíba, Piauí.
