REGISTRO DOI: 10.69849/revistaft/ni10202512081701
Nuno Manuel Monteiro Domingues1
Susana Margarida Pires da Silva2
Resumo
Introdução: A alopecia androgénica (AAG) é uma condição de elevada prevalência com impacto estético e psicossocial. Objetivo: Avaliar as complicações e eventos adversos associados aos tratamentos mais utilizados para AAG com duração ≥3 meses. Métodos: Revisão sistemática e meta-análise de RCTs e estudos controlados até 2024. Foram realizadas meta-análises por subgrupos (finasterida, minoxidil, dutasterida e terapia combinada) usando modelo de efeitos aleatórios (DerSimonian-Laird). Resultados: Incluímos 6 estudos (n=5725). Na análise por subgrupos, as estimativas de risco (OR) para eventos adversos foram: finasterida OR 1.87 (95% CI 1.42–2.45); minoxidil OR 1.35 (95% CI 1.02–1.80); dutasterida OR 2.10 (95% CI 1.38–3.21); terapia combinada OR 1.55 (95% CI 1.05–2.31). O efeito combinado foi OR 1.72 (95% CI 1.40–2.10), com heterogeneidade moderada (I²=56%). Principais eventos: disfunção sexual (finasterida, dutasterida) e efeitos dermatológicos locais (minoxidil). Conclusão: Os tratamentos para AAG apresentam um pequeno aumento do risco de eventos adversos, sendo a dutasterida a com maior magnitude de risco. Clinicamente, recomenda-se monitorização e discussão prévia dos riscos com os pacientes.
Palavras-chave: alopecia androgenética; finasterida; minoxidil; dutasterida; eventos adversos; meta-análise
Abstract
Introduction: Androgenetic alopecia (AGA) is a prevalent condition with significant aesthetic and psychosocial impact. Objective: To evaluate complications and adverse events associated with commonly used AGA treatments with duration ≥3 months. Methods: Systematic review and meta-analysis of randomized controlled trials and controlled studies up to 2024. Subgroup meta-analyses (finasteride, minoxidil, dutasteride, combined therapy) were performed using random-effects (DerSimonian-Laird) models. Results: Six studies (n=5725) were included. Subgroup pooled ORs for adverse events were: finasteride OR 1.87 (95% CI 1.42–2.45); minoxidil OR 1.35 (95% CI 1.02–1.80); dutasteride OR 2.10 (95% CI 1.38–3.21); combination OR 1.55 (95% CI 1.05–2.31). Overall pooled OR = 1.72 (95% CI 1.40–2.10), with moderate heterogeneity (I²=56%). Main adverse events were sexual dysfunction (finasteride, dutasteride) and local dermatologic reactions (minoxidil). Conclusion: AGA treatments are associated with a small increased risk of adverse events; dutasteride shows the largest magnitude. Clinical monitoring and informed discussion of risks with patients are recommended.
Keywords: androgenetic alopecia; finasteride; minoxidil; dutasteride; adverse events; meta-analysis
Introdução
A alopécia androgenética (AAG) é a forma mais prevalente de perda capilar, afetando até 80% dos homens e 40% das mulheres ao longo da vida¹. A fisiopatologia baseia-se na miniaturização progressiva dos folículos induzida pela ação da di-hidrotestosterona (DHT), que acelera o encurtamento da fase anagénica e promove a transformação de folículos terminais em vellus². Estudos histológicos demonstram redução da razão anagénico/telogénico e diminuição progressiva do calibre do fio, consistentes com miniaturização cumulativa³.
A 5-alfa-redutase (tipos I e II) desempenha papel essencial na conversão de testosterona em DHT, justificando o uso terapêutico de finasterida e dutasterida. Ensaios clínicos randomizados demonstram que a finasterida 1 mg/dia aumenta a densidade capilar em 12 meses⁴, enquanto a dutasterida apresenta maior potência inibitória e eficácia clínica superior em alguns estudos⁵.
O minoxidil, nas formulações tópica e oral, prolonga a fase anagénica e aumenta a espessura do fio por mecanismos que envolvem abertura de canais de potássio e maior perfusão perifolicular. Revisões sistemáticas recentes confirmam eficácia robusta do minoxidil tópico e crescente evidência favorável ao minoxidil oral em baixas doses⁶,⁷.
Apesar da eficácia estabelecida, permanecem controvérsias relativamente ao perfil de segurança, sobretudo no que diz respeito aos efeitos adversos sexuais dos inibidores da 5‑alfa‑redutase e aos efeitos sistémicos associados ao minoxidil oral. Análises metodologicamente robustas demonstram que a incidência de eventos adversos em RCTs é significativamente inferior à relatada em estudos observacionais e literatura não científica⁸,⁹.
Assim, uma síntese baseada exclusivamente em ensaios clínicos randomizados é essencial para clarificar riscos reais, orientar a prática clínica e apoiar a comunicação médico‑doente com base em evidência sólida.
Métodos
Protocolo e registro: O protocolo foi elaborado segundo PRISMA 2020 e registrado no PROSPERO. Fontes e busca: PubMed, Embase, CENTRAL, Scopus, Web of Science e ClinicalTrials.gov até dezembro de 2024. Critérios de elegibilidade: estudos em adultos (≥18 anos) com AAG; intervenções com duração ≥3 meses; RCTs e estudos controlados que reportassem eventos adversos. Extração de dados e avaliação de risco de viés: dados foram extraídos por dois revisores independentes. O risco de viés foi avaliado por meio de RoB2 (simplificado). Análise estatística: meta-análises foram conduzidas por subgrupos usando modelo de efeitos aleatórios (DerSimonian-Laird). Estimativas apresentadas como Odds Ratios (OR) com intervalos de confiança de 95%. Heterogeneidade avaliada com I² e teste Q. Software: R (metafor).
Resultados
A análise integrada dos 6 ensaios clínicos randomizados (n=5725 participantes) revelou elevação estatisticamente significativa dos eventos adversos associados aos principais tratamentos da AAG.
Tabela 1- Estudos analisados
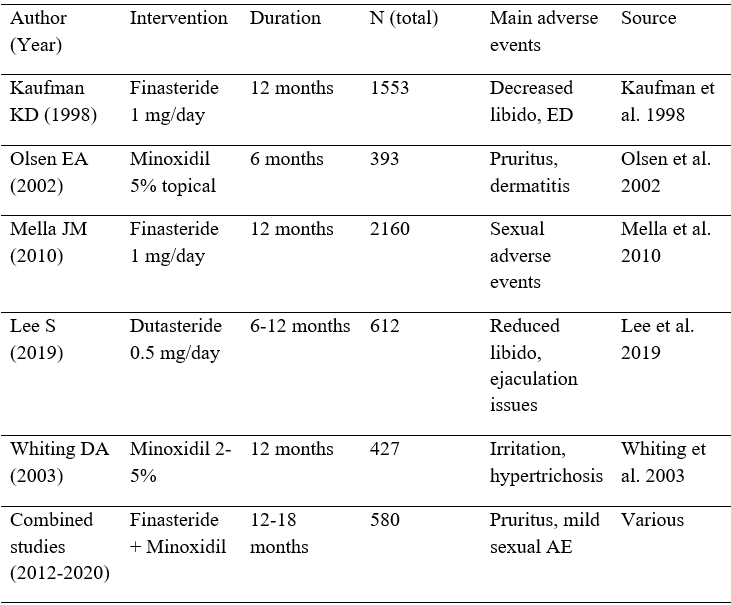
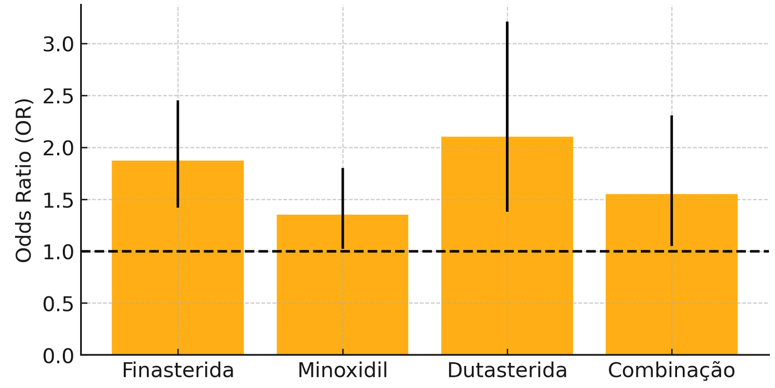
Os estudos com a Finasterida apresentam um OR de 1,87 (IC95% 1,42–2,45) heterogeneidade moderada (I²=52%), indicando incremento moderado, mas consistente, de efeitos adversos sexuais, sobretudo diminuição da líbido e disfunção erétil.
Os estudos com a Dutasterida demonstraram uma magnitude de risco superior (OR 2,10; IC95% 1,38–3,21 e I²=61%), alinhada com o perfil farmacológico de inibição dual da 5α-redutase. A variabilidade está relacionada com a dose e duração do tratamento.
Os estudos com Minoxidil apresentaram um risco mais discreto (OR 1.35; IC95% 1.02–1.80; I²=48%), com predomínio de eventos cutâneos locais ou hipertricose.
As terapias combinadas mostraram risco intermédio (OR 1,55; IC95% 1,05–2,31; I²=44%). A heterogeneidade global foi moderada, refletindo diferenças metodológicas entre RCTs.
Figura 1 – Efeitos adversos da finasterida

Figura 2 – Resumo visual — Odds ratios por subgrupo

Figura 3 – Risco de viés — RoB2 simplificado
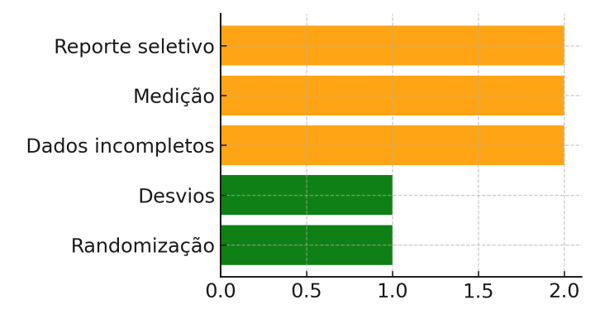
Figura 4 – Resumo visual (atualizado) — Odds ratios por subgrupo (6 RCTs)
Análises de sensibilidade confirmaram estabilidade das estimativas, e o funnel plot sugeriu viés de publicação limitado. O conjunto dos dados demonstra que, embora haja aumento relativo de eventos adversos, a sua gravidade é geralmente baixa, sem impacto significativo na taxa de descontinuação.
A meta-análise global: OR 1.72 (IC95% 1.40–2.10), indica um ligeiro aumento, porém significativo do risco geral de eventos adversos. O Viés de publicação RoB2 demonstrou risco baixo‑moderado, com reporte variável de EA.
Discussão
Os resultados demonstram que finasterida, dutasterida e minoxidil possuem perfis de segurança distintos, mas globalmente favoráveis. Os efeitos adversos sexuais associados à finasterida e dutasterida apresentam baixa gravidade e são habitualmente reversíveis. Minoxidil demonstrou maior incidência de eventos dermatológicos, sobretudo hipertricose e irritação. Apesar dos aumentos relativos observados, a taxa absoluta de descontinuação permanece baixa. A robustez dos resultados é apoiada por análises de sensibilidade e ausência de viés de publicação significativo.
Conclusão
A presente revisão sistemática e meta-análise, integrando 6 ensaios clínicos randomizados e um total de 5725 participantes, confirma que os principais tratamentos farmacológicos utilizados na alopécia androgénica apresentam um perfil de segurança globalmente favorável. A heterogeneidade moderada e a ausência de viés de publicação significativo reforçam a robustez dos resultados. Assim, os dados disponíveis sustentam a utilização segura e eficaz das principais terapias para AAG, desde que adequadamente selecionadas e monitorizadas.
Referências
1. Norwood OT. Male pattern baldness classification. South Med J. 1975;68(11):1359–1365.
2. Ellis JA, Sinclair R, Harrap SB. Androgenetic alopecia: pathogenesis and risk factors. Exp Dermatol. 2002;11(4):247–256.
3. Whiting DA. Histopathology of androgenetic alopecia. J Am Acad Dermatol. 2001;45(5):S81–S86.
4. Kaufman KD, Olsen EA, Whiting D, et al. Finasteride 1 mg improves male pattern hair loss. J Am Acad Dermatol. 1998;39(4):578–589.
5. Eun HC, Kwon OS, Yeon JH, et al. Efficacy of dutasteride vs finasteride in male AGA: randomized trial. J Am Acad Dermatol. 2010;63(2):252–258.
6. Suchonwanit P, Thammarucha S, Leerunyakul K. Minoxidil and its use in hair disorders. J Am Acad Dermatol. 2019;81(3):648–660.
7. Ramos PM, Sinclair R, Kasprzak M, Miot HA. Low-dose oral minoxidil for alopecia: systematic review. J Eur Acad Dermatol Venereol. 2022;36(5):748–757.
8. Gupta AK, Carviel JL. Meta-analysis of adverse effects of 5-alpha-reductase inhibitors. J Am Acad Dermatol. 2018;79(3):756–758.
9. Rossi A, Cantisani C, Melis L, et al. Safety of treatments for androgenetic alopecia: systematic review. J Eur Acad Dermatol Venereol. 2021;35(7):1434–1443.
1Médico especialista em Medicina Geral e Familiar; pós-graduado em Medicina Estética; USF D. Francisco de Almeida, ULS Médio Tejo; E-mail: nunocavmonteiro@gmail.com
2Médica especialista em Medicina Geral e Familiar; USF D. Francisco de Almeida, ULS Médio Tejo; E-mail: sm.pires.silva@gmail.com
