REGISTRO DOI: 10.69849/revistaft/ni10202410280705
Beatriz De Amorim Salazar; Fernanda Ribeiro Galindo Ortega; Iliane Da Cruz Kalschne; Orientadora: Prof. Ms. Taiana Caira Barbosa Galves
RESUMO
O Diabetes mellitus é definido como uma doença crônica não transmissível (DCNT), sendo uma síndrome caracterizada por hiperglicemia persistente, resultante de distúrbios metabólicos, podendo ocorrer devido à destruição das células beta produtoras de insulina ou à resistência à ação insulínica. O aumento da glicose plasmática, ocorre devido à defeitos na secreção e/ou ação da insulina produzida pelo pâncreas, podendo ser subdividida em três tipos principais: Diabetes mellitus tipo 1 (autoimune), Diabetes mellitus tipo 2 (resistente à insulina) e o Diabetes mellitus gestacional. O Diabetes é caracterizado por múltiplas complicações, agudas e crônicas (divididas em microvasculares e macrovasculares), que constituem uma causa importante de mortalidade precoce. As complicações crônicas microvasculares, são associadas às lesões específicas ocasionadas pela dificuldade da passagem do sangue para o endotélio. Essa obstrução ocorre devido a hiperglicemia crônica que desencadeia a inflamação endotelial, resultando em uma produção de produtos de glicolisação avançada, levando ao estresse oxidativo, tendo inflamação e o aparecimento de microtrombos, dificultando essa passagem. Já as complicações macrovasculares, além da hiperglicemia, estão também relacionadas a problemas como a dislipidemia, hipertensão arterial sistêmica e ao tabagismo. Tais fatores podem levar ao acidente vascular encefálico, ao infarto agudo do miocárdio e a doença arterial obstrutiva periférica. Este trabalho propõe uma revisão crítica da literatura existente sobre as complicações crônicas do Diabetes mellitus tipo 2, destacando medidas de rastreio, prevenção e tratamento. Conclui-se ser essencial o conhecimento técnico e clínico sobre a fisiopatologia e alternativas de intervenção para o cuidado imediato e integral dos pacientes com Diabetes mellitus tipo 2, bem como a prevenção de suas complicações crônicas.
Palavras-chave: Complicações. Diabetes. Crônica.
ABSTRACT
Diabetes mellitus is defined as a chronic non-communicable disease (NCD), being a syndrome characterized by persistent hyperglycemia, resulting from metabolic disorders, which may occur due to the destruction of insulin-producing beta cells or resistance to insulin action. The increase in plasma glucose occurs due to defects in the secretion and/or action of insulin produced by the pancreas, and can be subdivided into three main types: Type 1 Diabetes mellitus (autoimmune), Type 2 Diabetes mellitus (insulin resistant) and Diabetes gestational mellitus. Diabetes is characterized by multiple complications, acute and chronic (divided into microvascular and macrovascular), which constitute an important cause of early mortality. Chronic microvascular complications are associated with specific injuries caused by difficulty in passing blood to the endothelium. This obstruction occurs due to chronic hyperglycemia that triggers endothelial inflammation, resulting in the production of advanced glycolysis products, leading to oxidative stress, inflammation and the appearance of microthrombi, making this passage difficult. Macrovascular complications, in addition to hyperglycemia, are also related to problems such as dyslipidemia, systemic arterial hypertension and smoking. Such factors can lead to stroke, acute myocardial infarction and peripheral arterial obstructive disease. This work proposes a critical review of the existing literature on the chronic complications of Type 2 Diabetes mellitus, highlighting screening, prevention and treatment measures. It is concluded that technical and clinical knowledge about the pathophysiology and alternative interventions is essential for the immediate and comprehensive care of patients with Type 2 Diabetes mellitus, as well as the prevention of its chronic complications.
Key words: Complications. Diabetes. Chronic.
1. INTRODUÇÃO
O Diabetes mellitus (DM) é uma síndrome caracterizada por hiperglicemia persistente, resultante de distúrbios metabólicos, podendo ocorrer devido à destruição das células beta produtoras de insulina ou à resistência à ação insulínica (LEE; PARK; CHOI, 2021). No mundo, nos últimos 30 anos, a prevalência tem aumentado progressivamente, mais que triplicando o número de doentes (“Organização Pan-Americana da Saúde”, 2022), estimando-se que um a cada 11 indivíduos têm Diabetes, sendo destes, 90% o tipo II da doença (NEVES et al., 2023).
Dados divulgados na décima edição do Atlas do Diabetes, da Federação Internacional de Diabetes, mostram que 537 milhões de pessoas têm Diabetes no mundo, com número de mortes que ultrapassa 4 milhões por ano. A Federação projeta que até o ano de 2045, 700 milhões de indivíduos terão a doença (MAGLIANO; BOYKO; IDF DIABETES ATLAS 10TH EDITION SCIENTIFIC COMMITTEE, 2021).
O Panorama do Diabetes da OPAS (Organização Pan-Americana da Saúde) nas Américas, publicado em 2022, estima que ao menos 62 milhões de pessoas vivem com Diabetes nas Américas, no entanto, cerca de 40% das pessoas não sabem que têm a doença, tornando o número muito maior. Se as tendências atuais continuarem, o número de pessoas com Diabetes na região poderá chegar a 109 milhões até 2040 (Panorama of Diabetes in the Americas, 2022).
De acordo com a Sociedade Brasileira de Diabetes, existem atualmente, no Brasil, mais de 13 milhões de pessoas vivendo com a doença, representando cerca de 6,9% da população nacional (ARAUJO et al., 2023), com estimativas de mais de 23 milhões no ano de 2045 (MAGLIANO; BOYKO; IDF DIABETES ATLAS 10TH EDITION SCIENTIFIC COMMITTEE, 2021). O Brasil ocupa a quinta colocação no número de pessoas com DM no mundo, apresentando uma prevalência de aproximadamente 8% (Panorama of Diabetes in the Americas, 2022).
A DM acomete não só adultos, mas também crianças e adolescentes, sendo a DM do tipo 1 a segunda doença crônica mais presente na infância, caracterizando cerca de 500 mil crianças e adolescentes com DM1 no mundo (CASTRO et al., 2021).
O Diabetes mellitus é definido como uma doença crônica não transmissível (DCNT), caracterizada pelo aumento da glicose plasmática, devido à defeitos na secreção e/ou ação da insulina produzida pelo pâncreas, podendo ser subdividida em três tipos principais: DM tipo 1 (autoimune), DM tipo 2 (resistente à insulina) e o DM gestacional (COSTA; MOREIRA, 2021).
O DM tipo 1 é considerado de origem autoimune, ocorrendo devido à presença de anticorpos contra epítopos que atacam as células beta-pancreáticas, gerando uma destruição parcial ou total destas células, prejudicando assim, a produção/secreção de insulina (COSTA; MOREIRA, 2021). Os autoanticorpos geralmente associados à Diabetes tipo 1 são aqueles que visam a insulina (anticorpos anti-insulina), a descarboxilase de ácido glutâmico de 65 kDa (anticorpos antiGAD65), a proteína 2 associada ao insulinoma (anticorpos anti-IA 2) ou o transportador de zinco 8 (anticorpos anti-ZNT8) (SILVA-NUNES, 2018).
Este tipo tem uma forte predisposição genética. Entre a população geral, o risco de desenvolver Diabetes tipo 1 é de 0,4%. Apesar disso, se Diabetes tipo 1 estiver presente em irmãos, na mãe ou no pai, o risco de desenvolver a doença é de 6-7%, de 1,3-4% e de 6-9%, respectivamente, cerca de 50% da hereditariedade é representada pela região do antígeno leucocitário humano (HLA), no cromossomo 6p21. O maior risco de doença está ligado aos haplótipos de HLA classe II, em particular os haplótipos DR4-DQ8 e DR3-DQ2. (SILVA-NUNES, 2018).
Já no DM tipo 2, existem dois mecanismos fundamentais em sua geração, a resistência à insulina (RI) e a subsequente e progressiva disfunção da célula beta, na qual interagem múltiplas vias de sinalização de diferentes órgãos, que devido a fatores externos e internos são alteradas (JEREZ FERNÁNDEZ et al., 2022).
A RI é uma condição em que as células-alvo da insulina não respondem adequadamente a ela, o que reduz a incorporação de glicose no músculo e no tecido adiposo. Ocorre devido uma falha na via de sinalização da insulina, que pode ser causada por mutações ou modificações pós-traducionais do receptor ou do IRS (substrato do receptor da insulina) ou de moléculas na via da insulina alteradas (JEREZ FERNÁNDEZ et al., 2022).
Quanto aos danos nas células beta-pancreáticas, se incluem: dano induzido pela leptina e resistina – o aumento da leptina tem a capacidade de induzir a apoptose nas células beta, pois inibe a síntese de insulina, aumenta as reações inflamatórias e gera estresse oxidativo; lipotoxicidade – As células beta respondem de maneira bifásica ao acúmulo anormal de lipídios; glucotoxicidade – o excesso de glicose intracelular produz diminuição na síntese e secreção de insulina (JEREZ FERNÁNDEZ et al., 2022).
A DM gestacional ocorre quando não há o aumento adequado da produção de insulina nas gestantes. Esse distúrbio metabólico é definido como qualquer nível de intolerância a carboidratos, resultando em hiperglicemia variável, diagnosticada durante a gestação, em geral sendo revertida para tolerância normal no período pósparto, mas que pode permanecer após o nascimento (REIS; VIVAN; GUALTIERI, 2019).
Além disso, há ainda outras condições, referidas como pré-Diabetes, que são assim classificadas quando a glicemia em jejum se encontra alterada em níveis maior que 100 mg/dl e menor que 126 mg/dl e quando a tolerância à glicose se apresenta diminuída (CASTRO et al., 2021).
Os tipos 1 e 2 da DM são mais frequentes, porém variam em aspectos como idade e prevalência, a DM1 (antigamente chamada de Diabetes juvenil ou insulinodependente) acomete principalmente crianças e adolescentes, já a DM2, ocorre principalmente em adultos e possui maior prevalência, sendo responsável por cerca de 90% dos casos de DM (CASTRO et al., 2021; NEVES et al., 2023).
O quadro de DM geralmente se apresenta assintomático, no entanto, os principais sintomas são chamados de 4 “polis”, sendo eles, a poliúria (produção excessiva de urina), a polidipsia (sede excessiva), a polifagia (ingestão excessiva de alimentos) e a perda de peso (CASTRO et al., 2021). Além disso, o Diabetes é caracterizada por múltiplas complicações, agudas e crônicas (divididas em microvasculares e macrovasculares), que constituem uma causa importante de mortalidade precoce (CASTRO et al., 2021; CORTEZ et al., 2015).
Dentre as complicações agudas estão a hipoglicemia, o estado hiperglicêmico hiper osmolar e a cetoacidose diabética. Já as crônicas incluem as complicações microvasculares: retinopatia, nefropatia, neuropatias e macrovasculares: cardiopatia isquêmica, doença cerebrovascular e vascular periférica. As degenerativas mais frequentes são o infarto agudo do miocárdio, a arteriopatia periférica, o acidente vascular cerebral e a microangiopatia (CORTEZ et al., 2015; FONSECA; RACHED, 2019).
Todas as complicações se relacionam ao tempo de doença, onde a aguda tem a manifestação de seus sintomas de forma mais imediata, e a crônica resulta de uma manifestação dos seus sintomas após anos de evolução da doença, e que se relacionam diretamente a um controle glicêmico inadequado (FONSECA; RACHED, 2019).
As complicações crônicas microvasculares, são associadas às lesões específicas ocasionadas pela dificuldade da passagem do sangue para o endotélio. Essa obstrução ocorre devido a hiperglicemia crônica que desencadeia a inflamação endotelial, resultando em uma produção de produtos de glicolisação avançada, levando ao estresse oxidativo, tendo inflamação e o aparecimento de microtrombos, dificultando essa passagem (CASTRO et al., 2021).
A nefropatia diabética é a principal causa de insuficiência renal crônica dialítica, sendo responsável por 44% dos casos de hemodiálise. Nos casos de cegueira adquirida, a retinopatia diabética é a principal causa entre 20 e 74 anos de idade. E a neuropatia diabética e as complicações vasculares em membros inferiores são as principais causas de amputação não traumáticas, além de possuir maior prevalência para complicação crônica, podendo atingir cerca de 40% dos pacientes com DM (CASTRO et al., 2021; FONSECA; RACHED, 2019).
Já as complicações macrovasculares, além da hiperglicemia, estão também relacionadas a problemas como a dislipidemia, hipertensão arterial sistêmica e ao tabagismo. Tais fatores podem levar ao acidente vascular encefálico, ao infarto agudo do miocárdio e a doença arterial obstrutiva periférica (CASTRO et al., 2021).
Para o tratamento da DM, o principal objetivo é a normalização dos níveis glicêmicos e metabólico, prevenindo também as complicações. O tratamento envolve medicação, e mudanças no estilo de vida, que incluem hábitos alimentares saudáveis e a prática de atividade física (CASARIN et al., 2022).
Dentre as medicações utilizadas, temos os antidiabéticos orais e a insulinoterapia. Os antidiabéticos orais são classificados de acordo com o seu mecanismo de ação em, fármacos que estimulam a secreção pancreática de insulina (sulfonilureias e glinidas), aqueles que diminuem a absorção de glicídios (inibidores das alfaglicosidases), os que diminuem a produção hepática de glicose (biguanidas) e aqueles que aumentam o uso periférico da glicose (glitazonas) (CASARIN et al., 2022).
Já a insulinoterapia, existem algumas opções para uso como, a insulina regular (de ação rápida), NPH (de ação intermediária), insulinas análogas de ação ultrarrápida, de ação prolongada e as insulinas biossimilares da glargina (CASARIN et al., 2022). Os antidiabéticos orais são utilizados geralmente para regular os níveis de glicemia, por pessoas com DM2 e em alguns casos raros e específicos sendo usados para a DM1 e, a insulinoterapia, com a aplicação intramuscular de insulina exógena, é utilizada em ambos tipos de DM que possuem resistência insulínica ou comprometimento nas células beta pancreáticas (BOAS; FOSS-FREITAS; PACE, 2014; CASARIN et al., 2022).
Objetivos
1.2.1 Objetivos Gerais
Neste estudo objetivou-se descrever a evolução do DM tipo 2, destacando as complicações crônicas, como causa impacto a população doente, a alta morbimortalidade e o comprometimento da qualidade de vida dos usuários.
2. METODOLOGIA
Trata-se de uma revisão narrativa de literatura, de caráter amplo e se propõe a descrever o desenvolvimento de determinado assunto, sob o ponto de vista teórico ou contextual, mediante análise e interpretação da produção científica existente.
Para alcançar o objetivo de descrever a evolução do DM tipo 2, destacando as complicações crônicas, como causa impacto a população doente, a alta morbimortalidade e o comprometimento da qualidade de vida dos usuários, fo acessada a Biblioteca Virtual em Saúde (BVS) nas bases de dados Literatura LatinoAmericana e do Caribe em Ciências da Saúde (LILACS) e na biblioteca SciELO – Scientific Electronic Library Online.
Por meio da busca avançada, realizada em junho de 2024, utilizando-se os termos delimitadores de pesquisa, Diabetes and Complicações and Crônica como descritores para o levantamento de dados nos últimos 40 anos. Este processo envolveu atividades de busca, identificação, fichamento de estudos, mapeamento e análise.
3. REFERENCIAL TEÓRICO
ANATOMIA E FISIOLOGIA DO DIABETES MELLITUS TIPO 2
3.1.1 Anatomia do Pâncreas
O nome pâncreas deriva do grego ‘pan’ que significa ‘todo’ e ‘creas’ que significa ‘carne’. Em situações normais, nos humanos, consiste em um órgão com aproximadamente 100 gramas, medindo de 14 a 25 cm e com volume de 72.4 ± 25.8 cm3 (ATKINSON et al., 2020; SLACK, 1995).
O órgão está conectado ao duodeno pela ampola de Vater, onde o ducto pancreático principal se une ao ducto biliar comum. No ser humano, os termos cabeça, pescoço, corpo e cauda são usados para designar regiões do órgão de proximal a distal (Figura 1).
Figura 1. Principais características anatômicas do pâncreas humano.
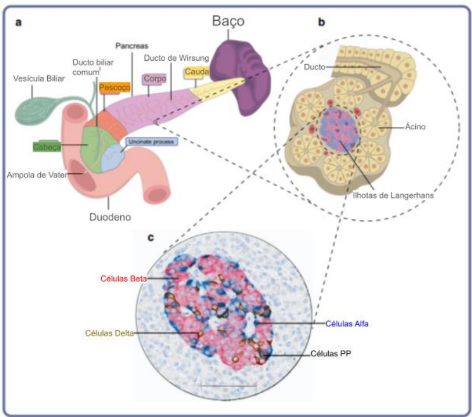
Fonte: ATKINSON et al., 2020 (modificado pelos autores).
O pâncreas é um órgão com dupla função, composto por células exócrinas responsáveis pela secreção de enzimas digestivas no lúmen gastrointestinal e por células endócrinas que se encontram nas ilhotas de Langherans e são fundamentais para a produção de hormonas reguladoras de processos metabólicos. As células do pâncreas que produzem essas enzimas digestivas são as células acinares, derivadas da palavra latina ‘acinus’, que significa uva, pois são agregados celulares que formam feixes semelhantes a cachos de uvas, as células acinares constituem quase 85% do pâncreas, estão dispostos em ácinos e sintetizam e secretam enzimas ativas em proteínas, gorduras e carboidratos digestão, incluindo tripsina, lipase e amilase (ATKINSON et al., 2020; ROMACIUC, 2017).
Em adultos, as ilhotas de Langherans representam 1-2% da massa pancreática total, localizadas entre os aglomerados de células acinares, e são constituídos maioritariamente por células β (beta) (60-80%) que são responsáveis pela secreção de insulina, por células α (alfa) (20-30%) produtoras de glucagon, células δ (delta) responsáveis pela secreção de somatostatina (5-15%) e, células do polipeptídio pancreático (PP) (Figura 1). As ilhotas de Langherans são inervados por fibras nervosas autónomas, sendo que a enervação parassimpática do nervo vago estimula a libertação de insulina, enquanto a enervação por parte do sistema simpático adrenérgico inibe a produção de insulina e estimula a secreção de glucagon, assim, as funções das ilhotas são reguladas por sinais iniciado por nervos autônomos, metabólitos circulantes (por exemplo, glicose, aminoácidos e corpos cetônicos), hormônios circulantes e hormônios locais (parácrinos) (ATKINSON et al., 2020; ROMACIUC, 2017).
O pâncreas compõe um órgão de extrema importância na patogênese do Diabetes, como por exemplo o desenvolvimento pós-pâncreas, produção anormal de insulina, muitos aspectos da biossíntese de insulina nas ilhotas beta pancreáticas, déficits na produção de insulina (MARSHALL, 2020). Estudos demonstram que no DM2, o volume do pâncreas variou de 20,8 a 99,7 cm3, mostrando uma diminuição do tamanho do pâncreas, a morfologia irregular e o aumento no teor de gordura quando com a patologia (MACAULEY et al., 2015).
O Diabetes é um distúrbio do metabolismo dos carboidratos, caracterizado pela incapacidade do corpo de produzir quantidade suficiente ou responder adequadamente à insulina. Além disso, a secreção desregulada de glucagon pelas células alfa é uma característica fundamental de Diabetes tipo 1 e tipo 2. Portanto, a importância do pâncreas se dá pelo fato que ele secreta os dois principais hormônios, glucagon e insulina, que desempenham um papel central na regulação do metabolismo energético (ATKINSON et al., 2020).
A seguir, abordaremos as modificações ocorridas no pâncreas no caso da DM tipo 2.
3.1.1.1 Aumento da deposição de substância amiloide
As células β, secretoras de insulina, possuem a capacidade de adaptação à demanda metabólica, no entanto, a resposta adaptativa das células beta não é ilimitada e quando falha, surge o Diabetes tipo 2. Em contraste com o DM tipo 1, que apresenta mudanças na morfologia das ilhotas e na infiltração imunológica, não há nenhum estereótipo na histologia do pâncreas no Diabetes tipo 2 (ATKINSON et al., 2020).
Uma característica histológica que apresenta é a deposição de amiloide, um agregado de proteína extracelular derivado do IAPP (amilina ou peptídeo ilhota amiloide). Embora a amiloide das ilhotas esteja presente em algumas ilhotas da maioria dos indivíduos com Diabetes tipo 2, seu papel causal na patogênese do Diabetes não foi estabelecido. Além disso, não é um marcador histológico definitivo, uma vez que uma fracção significativa de indivíduos com Diabetes tipo 2 não tem amiloide nos seus ilhéus, embora estes depósitos possam estar presente nas ilhotas de indivíduos euglicêmicos e, também, daqueles com Diabetes tipo 1 (ATKINSON et al., 2020).
3.1.1.2 Redução da massa de células β
Outra característica pancreática observada em alguns estudos, é a redução da massa de células β (ATKINSON et al., 2020).. Estudos de autópsia descobriram que a massa de células beta pancreáticas em indivíduos com Diabetes tipo 2 apresentaram ser cerca de 60% da massa normal (WESTERMARK et al., 1987), achados semelhantes foram obtidos de amostras pancreáticas de doadores de órgãos (CLARK et al., 1990).
Contudo, a causa e efeito ainda não podem ser determinados, pois, a massa de células β apresenta grande variabilidade no nascimento e infância, além da determinação longitudinal dessas células ainda não ser possível. O declínio de tais células durante o curso do DM tipo 2 pode ser devido a predisposição genética, ou escolhas de estilo de vida e glicotoxicidade associada, ou ainda, indivíduos nascidos com uma pequena massa de ilhotas serem mais propensos a desenvolver o DM2 (ATKINSON et al., 2020).
3.1.1.3 Aumento de gordura pancreática
Uma característica frequentemente, embora não consistentemente, relatada do pâncreas no Diabetes tipo 2 é o seu aumento no teor de gordura (ATKINSON et al., 2020). A esteatose hepática é uma característica comum na obesidade e na resistência à insulina. Portanto, não é surpreendente que a esteatose também ocorra no pâncreas; na verdade, a esteatose pancreática ocorre simultaneamente em mais de dois terços dos indivíduos com Diabetes tipo 2 (ATKINSON et al., 2020; LEE et al., 2009). Uma possibilidade é que, nos estágios iniciais da doença, a esteatose pancreática pode contribuir para um declínio da função, mas uma vez que o Diabetes evidente ocorre, vários fatores deletérios, como aumento da inflamação e do estresse oxidativo, desempenham um papel muito mais determinante do que o conteúdo lipídico pancreático (ATKINSON et al., 2020; GUGLIELMI; SBRACCIA, 2018).
3.1.2 Anatomia do Sistema Cardiovascular
3.1.2.1 Coração
O coração é dividido em quatro cavidades, duas direitas (átrio direito e ventrículo direito) e duas esquerdas (átrio esquerdo e ventrículo esquerdo). O lado direito do coração recebe o sangue pouco oxigenado vindo da circulação sistêmica pelas veias cavas superior e inferior, e o bombeia através da artéria pulmonar para os pulmões, onde será oxigenado. O sangue retorna, então, para o átrio esquerdo através das veias pulmonares, dirige-se ao ventrículo esquerdo, e, por meio da artéria aorta, volta à circulação sistêmica). Portanto, átrios são responsáveis por receber o sangue, enquanto os ventrículos, em bombeá-lo para os demais tecidos e órgãos do corpo (BRANCO et al., 2018).
Existem quatro valvas cardíacas, duas atrioventriculares (AV), tricúspide e mitral, e duas semilunares (SL), pulmonar e aórtica. Entre o AD e VD está a valva tricúspide e entre AE e VE está a valva mitral. As AV evitam o refluxo de sangue dos ventrículos para os átrios durante a sístole ventricular e as SL evitam o refluxo de sangue da aorta e das artérias pulmonares durante a diástole ventricular (BRANCO et al., 2018).
Para que seu funcionamento ocorra corretamente e ritmicamente, o coração apresenta um ciclo cardíaco, que é iniciado através de um potencial de ação no nodo sinusal, situado na parede lateral superior do AD, que se difunde rapidamente até o feixe atrioventricular, e a partir dele para os ventrículos. O ciclo é composto por três eventos básicos: contrações, relaxamento e o enchimento (BRANCO et al., 2018; MAIA; SA, 1988).
3.1.2.2 Artérias
As artérias são as responsáveis por levar o sangue do coração aos outros tecidos, as artérias maiores (de grande calibre) se dividem em artérias menores, as arteríolas, que se dividem em capilares. Com essa progressiva redução de tamanho, há a redução também do diâmetro dos vasos, espessura de suas paredes, pressão em seu interior e na velocidade em que o sangue atravessa (RODRIGUES, 2021).
3.1.3 Anatomia dos Olhos
O globo ocular é constituído por três camadas concêntricas, sendo a mais externa formada pela córnea e a esclera. A camada média ou vascular é formada pela coroide, corpo ciliar e íris, e a camada interna ou sensorial, pela retina. A esclera ou “branco dos olhos” é uma camada fibrosa. Nela, os músculos extraoculares se inserem para mover o olho. A córnea corresponde à parte transparente dos olhos, permitindo a visualização da íris e da pupila. A córnea e o cristalino são as lentes que focalizam a imagem na retina. Qualquer alteração na transparência dessas estruturas trará prejuízos à formação da imagem e consequente baixa acuidade visual (AV) (GRAZIANO; LEONE, 2005).
A luz entra no olho através da pupila, e a imagem é focada na retina, através das lentes do olho. Nesta, a luz é transformada em impulso elétrico pelos fotorreceptores (cones e bastonetes) e transmitida ao cérebro através das células bipolares e ganglionares. São os axônios das células ganglionares que constituem o nervo óptico. Antes de chegar ao lobo occipital, onde estes estímulos são decodificados, as células ganglionares fazem sinapse no corpo geniculado lateral (GRAZIANO; LEONE, 2005).
3.1.4 Anatomia dos Rins
Os rins são órgãos pares, em forma de grão de feijão, coloração marromavermelhada, situados em região retroperitoneal. os quais realizam a maior parte das funções de excreção, filtrando o sangue e recolhendo deste os resíduos metabólicos de todas as células do corpo. Os rins são recobertos pelo peritônio e circundados por uma massa de gordura e de tecido areolar frouxo. Cada rim tem cerca de 11,25 cm de comprimento, 5 a 7,5 cm de largura e um pouco mais que 2,5 cm de espessura (PIROG et al., 2012).
Embora os rins constituam menos de 0,5 % do total da massa do corpo, recebem de 20 a 25 % do débito cardíaco em repouso, por meio das artérias renais (direita e esquerda), que são dois grandes troncos que se originam da artéria aorta abdominal, ao nível do disco intervertebral entre a primeira e a segunda vértebra lombar (PIROG et al., 2012).
3.2 FISIOPATOLOGIA DO DIABETES MELLITUS TIPO 2
O Diabetes tipo 2 (DM2) é uma doença metabólica complexa primariamente causado por dois fatores principais: a reduzida secreção de insulina pelas células β pancreáticas e a resistência periférica dos tecidos a esse hormônio, que serão descritos com maiores detalhes nos próximos tópicos (OLIVEIRA et al., 2023; ROMACIUC, 2017).
3.2.1 Disfunção das Células β
A disfunção das células β foi associada, primeiramente, à apoptose destas células. No entanto, estudos mais recentes sugerem que interações entre fatores ambientais e diferentes vias moleculares da biologia celular possam estar envolvidas. Foram propostos vários mecanismos que induzem a apoptose das células β, tais como a glicolipotoxicidade, a deposição de polipeptídio amiloide dos ilhéus pancreáticos (IAPP) nas células β, o stress oxidativo, stress do retículo endoplasmático, a disfunção mitocondrial, a libertação de citocinas inflamatórias e a disfunção da autofagia (OLIVEIRA et al., 2023; ROMACIUC, 2017).
A glicotoxicidade é uma das hipóteses para essa disfunção, causada pela hiperglicemia, que desencadeia vários mecanismos oxidativos, libertando espécies reativas de oxigênio e azoto, que por sua vez vão provocar stress oxidativo nas células β, tendo como consequência a disfunção e a apoptose das mesmas. Essas espécies reativas de oxigênio interferem negativamente na síntese e secreção de insulina, visto que diminuem a expressão dos principais fatores de transcrição, PDX1 (pancreatic and duodenal homeobox 1) e MafA, que regulam a expressão genética de vários fatores relacionados às células β, inclusive a insulina (ROMACIUC, 2017).
A lipotoxicicidade também surge na presença de hiperglicemia, a absorção progressiva de ácidos graxos livres e um defeito no metabolismo destes nas células β tem como consequência a deposição de lipídios nas ilhotas de Langherans, contribuindo para o declínio da secreção de insulina na DMT2. A glicolipotoxicidade é sustentada por vários estudos e experiências, que demonstraram que uma infusão aguda de glicose e uma elevada carga lipídica interfere com o funcionamento normal das células β. Além disso, a redução aguda da glicolipotoxicidade com intervenção a tratamentos intensivos com insulina e com uma restrição energética induz a restauração significativa da função das células β (OLIVEIRA et al., 2023; ROMACIUC, 2017).
3.2.2 Resistência à Insulina
O tecido adiposo modula o metabolismo pela liberação de ácidos graxos livres, como glicerol, citocinas pró-inflamatórias, quimiocinas e hormônios, incluindo a leptina e a adiponectina. O aumento da maioria desses ácidos compromete a ação da insulina nos órgãos-alvo, atuando principalmente na sua cascata de sinalização, levando à Resistência à Insulina (RI) (CASTANHOLA; PICCININ, 2020).
A resistência à insulina é um fator predisponente significativo para o desenvolvimento da DM2, sendo considerado a principal causa desta patologia. A RI caracteriza-se pela deficiência na absorção de glicose nos tecidos sensíveis à insulina, principalmente no tecido muscular esquelético, tecido adiposo e fígado (CASTANHOLA; PICCININ, 2020; ROMACIUC, 2017).
Para um indivíduo ser considerado resistente à insulina tem de apresentar vários critérios, como hiperinsulinemia e hiperglicemia em jejum, aumento da hemoglobina glicada (HbA1c), hiperglicemia pós-prandial, dislipidemia, tolerância à glicose alterada e tolerância à insulina diminuída, aumento da produção de glicose hepática, perda da primeira fase de secreção da insulina e aumento dos marcadores inflamatórios no plasma (ROMACIUC, 2017).
3.3 COMPLICAÇÕES CRÔNICAS
Na DM as alterações vasculares são divididas em duas categorias: microvasculares, principal causa de morte em pacientes com o tipo 1, e macrovasculares, principal causa em pacientes com o tipo 2. O acometimento microvascular está relacionado aos pequenos vasos, capilares e arteríolas, ocorrendo principalmente pelo espessamento da membrana basal capilar (acomete os rins, levando a nefropatia diabética, o sistema vascular sistêmico, entre outros). Já o comprometimento macro vascular é essencialmente uma forma acelerada da aterosclerose, sendo responsável pela alta incidência de doenças cardiovasculares, que são responsáveis pelos maiores índices de mortalidade nessa população, e incluem o infarto do miocárdio, o acidente vascular cerebral e a gangrena periférica (VIANA; RODRIGUEZ, 2011).
Os pacientes com DM do tipo 2 têm uma propensão duas a quatro vezes maior de morrer por doença cardíaca em relação a não diabéticos, e quatro vezes mais chance de ter doença vascular periférica (DVP) e acidente vascular cerebral (AVC), além disso, o DM do tipo 2 também é apontado como uma das principais causas de cegueira entre adultos com idade de 20 a 74 anos. Em alguns levantamentos, após 15 anos do diagnóstico de DM do tipo 2, a retinopatia diabética (RD) esteve presente em 97% dos usuários de insulina e em 80% dos não usuários. A prevalência de doença renal varia de 10% a 40% e a de neuropatia, de 60% a 70%4 (SCHEFFEL et al., 2004).
Entre os fatores envolvidos na etiologia das complicações crônicas do DM do tipo 2, destacam-se a hiperglicemia, a hipertensão arterial sistêmica, a dislipidemia e o tabagismo. Além destes, outros fatores de risco não convencionais têm sido descritos, como, a disfunção endotelial, estado pré-trombótico e inflamação (SCHEFFEL et al., 2004).
A seguir, abordaremos com mais detalhes as principais complicações presentes no DM tipo 2.
3.3.1 Disfunção Endotelial e Doenças Cardiovasculares
A hiperglicemia e o aumento da glicose intracelular induzem a ativação da via dos polióis, a formação de produtos finais de glicação avançada, o estresse oxidativo, as anormalidades lipídicas, e a ativação da proteína quinase C (PKC). Essas situações geram um estado inflamatório persistente, dano osmótico, alteração da função de proteínas e fatores de transcrição, além de dano ao DNA celular, que associado ao acometimento na micro e na macro vasculatura representa a base da patogênese das complicações diabéticas (GOMES; SILVA; SPINETI, 2013).
Um dos mecanismos fisiopatológicos das complicações macrovasculares do DM inclui a ativação do sistema renina-angiotensina (SRA), que é acompanhado por um estado pró-inflamatório/pró-fibrótico, envolvendo remodelamento vascular e do miocárdico em animais (GOMES; SILVA; SPINETI, 2013).
O endotélio normal, capaz de secretar óxido nítrico (NO), prostaciclina (PGI2) e fator hiperpolarizante, é responsável pela manutenção do tônus vascular, regulação da agregabilidade plaquetária e da coagulação, modulação da fibrinólise, dissolução de trombos intravasculares formados e modulação da inflamação através da regulação da adesão e ativação de leucócitos e de quimiocinas. Lesões endoteliais promovidas pelo DM, hipercolesterolemia e outros fatores de risco para aterosclerose causam uma redução na síntese e secreção desses fatores protetores e estas alterações propiciam um estado pró-constritor, pró-inflamatório e próagregante ao vaso sanguíneo. Em decorrência da ativação do endotélio para um estado pró-aterogênico ocorre antes das alterações estruturais na microcirculação, alterações na reatividade microvascular, além disso, a hiperglicemia está também associada ao aumento na secreção de endotelina, o mais potente vasoconstrictor conhecido (AGUIAR; VILLELA; BOUSKELA, 2007).
A aterosclerose é uma doença multifatorial e sua aceleração em pacientes com Diabetes pode ser explicada por várias condições, incluindo hiperglicemia, aumento do estresse oxidativo, produtos de glicação avançada, dislipidemia, desequilíbrio autonômico, hiperinsulinemia, marcadores inflamatórios e variáveis genéticas. Condições como o Diabetes, obesidade e resistência insulínica são associadas a um processo inflamatório subclínico caracterizado por aumento de expressão de citocinas produzidas pelo tecido adiposo, principalmente o visceral, macrófagos ativados e outras células (GOMES; SILVA; SPINETI, 2013; VIANA; RODRIGUEZ, 2011).
Mediadores inflamatórios, tais como TNF-α, interleucina-1 (IL-1), IL-6, leptina, resistina, MCP-1, inibidor do ativador do plasminogénio-1 (PAI-1), proteína C-reativa (PCR), fibrinogênio, angiotensina, visfatina, retinol-bindingprotein-4 e adiponectina estão envolvidos em vias de sinalização da insulina e perpetuação da resposta inflamatória. Essas citocinas estão envolvidas no processo inflamatório crônico da parede de vasos, promovendo o acúmulo de lípidos com consequente desenvolvimento de aterosclerose e das doenças cardiovasculares (GOMES; SILVA; SPINETI, 2013; VIANA; RODRIGUEZ, 2011).
O risco relativo de morte devido a complicações vasculares é três vezes maior nos pacientes com DM do que na população restante com as doenças cardiovasculares (DCVs), sendo responsáveis por até 80% dos óbitos em portadores de DM (TSCHIEDEL, 2014).
3.3.2 Nefropatia
A nefropatia diabética (ND) é uma complicação crônica do Diabetes que afeta 20% a 30% das pessoas com Diabetes mellitus tipo 1 (DM1) ou DM2, sendo responsável por aproximadamente metade dos novos casos de insuficiência renal nos indivíduos em diálise e tendo sido associada a um aumento significativo da mortalidade, principalmente cardiovascular (CASTRO et al., 2017; TSCHIEDEL, 2014).
A nefropatia diabética apresenta-se em três estágios evolutivos, estágios baseados na excreção urinária de albumina (EUA): nefropatia incipiente ou fase de microalbuminúria (EUA entre 30-300mg/24h ou 20-200mg/min), nefropatia clínica ou fase de macroalbuminúria (por EUA superior a 300mg/24h ou 200mg/min) e insuficiência renal terminal (uremia) (MURUSSI et al., 2003; TSCHIEDEL, 2014).
O Diabetes provoca alterações estruturais características na histologia renal. As mais precoces ocorrem ao nível do glomérulo e caracterizam-se pelo espessamento da membrana basal glomerular e do mesângio, devido à acumulação de matriz extracelular, o que conduz ao aumento inicial do volume renal, contrariamente a outras formas de patologia renal crônica em que o volume renal se encontra diminuído (exceto na amiloidose e na doença do rim poliquístico) (ANTÃO; GALLEGO; CALDEIRA, 2007; MURUSSI et al., 2003).
Estudos sugerem que a hiperglicemia, a presença em circulação de complexos glicosilados e a ativação de biomarcadores inflamatórios estão envolvidos na ND. A hiperglicemia é responsável pela hiper filtração renal que por sua vez induz o aumento da pressão capilar glomerular. Esta promove a proliferação celular regulada pela libertação do fator de crescimento TGF-α (mediação da hipertrofia e divisão celular e do processo de fibrose renal, através da estimulação da produção de colágeno e fibronectina) (ANTÃO; GALLEGO; CALDEIRA, 2007).
Os produtos glicosilados, resultantes da ligação da glicose a proteínas no rim, também contribuem para a lesão renal, através da estimulação de fatores promotores de fibrose. A glomerulosclerose no Diabetes é caracterizada pelo espessamento da membrana basal glomerular, esclerose mesangial difusa e nodular, arteriosclerose hialina, micro aneurismas e também alterações a nível tubular e intersticial. As alterações estruturais são mais heterogêneas em portadores de DM2, com micro ou microalbuminúria (ANTÃO; GALLEGO; CALDEIRA, 2007; MURUSSI et al., 2003).
O comprometimento glomerular no DM inicia-se, geralmente, cinco a 10 anos depois da evolução do Diabetes, apresentando um aumento de incidência após 15 anos de doença, portanto o rastreamento deve ser iniciado logo ao diagnóstico em pessoas com DM2, uma vez que 7% delas já têm microalbuminúria nesse momento, e se a macroalbuminúria estiver ausente, a análise deve ser repetida anualmente, tanto no DM1 quanto no DM2 (TSCHIEDEL, 2014).
O tratamento da ND deve ser realizado precocemente, a fim de se evitar a progressão da doença e, também, porque a redução da albuminúria diminui o risco de eventos cardiovasculares Quando a microalbuminúria se estabelece, deve-se iniciar o bloqueio do sistema renina-angiotensina com inibidor da enzima de conversão da angiotensina (iECA) (TSCHIEDEL, 2014).
3.3.3 Retinopatia
A retinopatia diabética (RD) é uma das complicações mais comuns do Diabetes e estima-se que 80% dos pacientes diabéticos apresentarão algum grau de RD após 25 anos da doença. Entre 5 e 8% dos pacientes cegos no mundo o são em decorrência de RD. Apesar do avanço no controle metabólico e de terapias oculares cada vez mais efetivas, a RD ainda é uma das principais causas de cegueira no Brasil e no mundo, tendo grande impacto socioeconômico (ZELANIS et al., 2015). No DM2 a RD já está presente em 21% dos indivíduos recém-diagnosticados e pode atingir 60% dos pacientes após 20 anos de doença (TSCHIEDEL, 2014).
Os seguintes fatores têm sido relacionados com uma evolução mais desfavorável da doença retiniana: idade (pior na fase pré-puberal), duração da doença, raça (pior na negra), sexo (mais severa em mulheres), hipertensão arterial sistêmica e controle glicêmico (ramos). A nefropatia diabética (ND) também aparece, como um fator de associação a RD. Estudos mostram a incidência conjunta das duas moléstias (CASTRO et al., 2017).
Os níveis séricos elevados de glicose induzem a uma série de anormalidades bioquímicas e celulares na retina, que podem provocar as alterações vasculares encontradas na RD. Como exemplo, aumento na atividade da via dos polióis, glicação não-enzimática de proteínas, estresse oxidativo e ativação da proteína kinase C pela síntese de diacilglicerol. Entretanto, o exato mecanismo, ou o conjunto de mecanismos pelos quais a hiperglicemia leva à retinopatia, ainda não foi completamente descrito (BOSCO et al., 2005).
Pode-se classificar a RD em retinopatia não proliferativa (RDNP) e proliferativa (RDP), a retinopatia diabética não proliferativa pode ser classificada em leve, moderada ou grave e caracteriza-se pela presença de micro aneurismas, micro hemorragias, exsudatos duros e algodonosos e a progressão da doença causa diminuição da perfusão capilar, com várias hemorragias intrarretinianas, alterações no calibre venoso e anormalidades microvasculares intrarretinianas (TSCHIEDEL, 2014).
Já quando há o aparecimento de neovasos, induzidos pela isquemia retiniana, identifica a retinopatia diabética como proliferativa. O edema macular diabético (EMD), outro evento importante do Diabetes, é mais frequente no DM2 e, nesta fase, a pessoa ainda pode enxergar bem, mas a visão já está agudamente ameaçada. A detecção precoce e o tratamento a laser do edema macular clinicamente significativo são essenciais na prevenção da perda permanente da visão (TSCHIEDEL, 2014).
O controle glicêmico tem um papel importante na atenuação do aparecimento e da progressão da retinopatia diabética, onde para cada redução de 1% dos níveis de hemoglobina glicada A1c e de 10mmHg da pressão arterial ocorre uma diminuição de 37% e 13%, respectivamente, do risco de evolução para qualquer complicação microvascular. A principal forma de tratamento da RD é a foto coagulação a laser, que pode ser realizada em vários padrões, dependendo das alterações encontradas na retina (TSCHIEDEL, 2014).
3.3.4 Neuropatia
A neuropatia diabética (NeD) é a complicação tardia mais frequente do Diabetes e pode ser evidenciada no DM2, muitas vezes no momento do diagnóstico, constitui um grupo heterogêneo de manifestações clínicas ou subclínicas, que acometem o sistema nervoso periférico (SNP) com a presença de sintomas e/ou sinais de disfunção dos nervos periféricos em diabéticos, após a exclusão de outras causas o comprometimento do sistema nervoso periférico (NASCIMENTO; PUPE; CAVALCANTI, 2016; TSCHIEDEL, 2014).
A patogênese da NeD ainda não está totalmente compreendida, e diferentes teorias tentam explicar a etiologia da doença, um dos mecanismos mais estudados abrange a insuficiência microvascular com redução no fluxo sanguíneo neural. Ela é resultante da isquemia absoluta ou relativa dos vasos endo neurais e epi neurais, que leva ao espessamento da membrana basal, à diminuição do fluxo sanguíneo e a alterações da permeabilidade vascular. Isso acarreta disponibilidade reduzida de óxido nítrico e excesso de formação de espécies reativas de oxigênio, que favorecem a produção de peroxinitrito, um potente agente oxidante pró-inflamatório e tóxico às células endoteliais (TSCHIEDEL, 2014).
É uma das manifestações clínicas mais frequentes, afetando entre 40% e 50% dos indivíduos com DM2, que abrange um grupo de alterações relacionadas ao envolvimento estrutural e funcional de fibras nervosas sensitivas, motoras e autonômicas, que podem ser reversíveis ou permanentes. Clinicamente, manifestam-se de formas muito variáveis, desde síndromes dolorosas graves, agudas, secundárias a oscilações glicêmicas, até formas assintomáticas. Além disso, entre os pacientes com NeD, aproximadamente 20% apresentam dor neuropática, implicando em redução significativa da qualidade de vida e capacidade funcional (NASCIMENTO; PUPE; CAVALCANTI, 2016; TSCHIEDEL, 2014).
A NeD constitui fator de risco importante para úlceras, deformidades, amputações de MMII (membros inferiores) e para o desenvolvimento de outras complicações microvasculares. Ainda, aumenta as taxas de internações hospitalares e mortalidade cardiovascular em pacientes diabéticos devido ao acometimento autonômico (NASCIMENTO; PUPE; CAVALCANTI, 2016).
A polineuropatia sensitivo-motora difusa simétrica periférica constitui sua forma clínica mais frequente, apresentando-se geralmente de maneira assintomática e, pode ser de fibras finas, grossas ou mistas. Os sinais e sintomas são parestesia, dor (queimação, pontada, choque ou agulhada) em pernas e pés, hiperestesia (dor ao toque de lençóis e cobertores), diminuição ou perda da sensibilidade tátil (fibras grossas), térmica ou dolorosa (fibras finas), perda dos reflexos tendinosos profundos, fraqueza e perda da motricidade distal, úlceras nos pés. No entanto, menos da metade dos pacientes apresenta algum tipo de sintoma neuropático, sendo na maioria das vezes sintomas sensitivos. (NASCIMENTO; PUPE; CAVALCANTI, 2016; TSCHIEDEL, 2014).
Já a neuropatia autonômica caracteriza- -se por função pupilar anormal (diminuição do diâmetro pupilar no escuro), disfunção sudomotora (anidrose, intolerância ao calor, boca seca, sudorese gustatória), disfunção geniturinária (bexiga neurogênica, disfunção erétil, ejaculação retrógrada, disfunção sexual feminina), disfunção gastrintestinal (atonia de vesícula biliar, dismotilidade esofagiana, gastroparesia, constipação, diarreia e incontinência fecal), disfunção cardiovascular (taquicardia em repouso, intolerância a exercícios, hipotensão ortostática, isquemia miocárdica silenciosa) e disfunção metabólica (hipoglicemia despercebida) (TSCHIEDEL, 2014).
Na mononeuropatia focal, os nervos mais comumente acometidos são: ulnar, radial, mediano, femoral e peroneiro. Na neuropatia craniana os nervos mais comumente acometidos são os pares cranianos III, IV, VI e VII (TSCHIEDEL, 2014).
3.4 SINAIS E SINTOMAS
A hiperglicemia no DM2 geralmente se desenvolve de forma gradual e, nos estágios iniciais, não é suficiente para promover os sintomas clássicos, permanecendo a doença não diagnosticada por vários anos (ANDRADE, 2003).
Os primeiros sintomas do Diabetes estão relacionados aos efeitos diretos da concentração sérica alta de glicose, no caso, quando esta é superior a 160 a 180 mg/dl, a glicose passa para a urina, esses primeiros sintomas são definidos como “4 P’s”. Quando essa concentração aumenta ainda mais, os rins excretam uma maior quantidade de água para diluir a grande quantidade de glicose perdida. Consequentemente, o indivíduo com Diabetes elimina grandes volumes de urina (poliúria), o que acarreta uma sede anormal (polidipsia). Devido a perda excessiva de calorias pela urina, o indivíduo começa a perder peso, acarretando a uma frequente sensação de fome excessiva (polifagia). No início, os aumentos da micção e da sede são discretos e pioram gradualmente ao longo de semanas ou meses (ANDRADE, 2003; LUCENA, 2007).
Outros sintomas incluem a visão borrada, sonolência, náusea e a diminuição da resistência durante o exercício. Além disso, os indivíduos com Diabetes mal controlados são mais suscetíveis às infecções, por causa da gravidade do déficit de insulina (LUCENA, 2007).
A cetoacidose é rara na DM2, que ocorre quando a concentração sérica de açúcar se torna muito alta (frequentemente excedendo 1000 mg/dl), normalmente decorrente da sobreposição de algum estresse (p. ex. infecção) ou de drogas, o indivíduo pode apresentar uma desidratação grave, a qual pode acarretar confusão mental, sonolência, convulsões e uma condição denominada coma hiperglicêmico hiper osmolar não-cetótico (LUCENA, 2007).
3.5 DIAGNÓSTICO
O diagnóstico do Diabetes é estabelecido quando o indivíduo apresenta concentração sérica anormalmente alta de glicose. Baseia-se fundamentalmente nas alterações da glicose plasmática de jejum ou após uma sobrecarga de glicose por via oral (GROSS et al., 2002; LUCENA, 2007).
Os critérios diagnósticos se dão pela glicose plasmática de jejum (8 horas), nos pontos de jejum e de 2h após sobrecarga oral de 75g de glicose (teste oral de tolerância à glicose TOTG) e na medida da glicose plasmática casual (Tabela 1)(GROSS et al., 2002).
Tabela 1. Diagnóstico de DM e alterações da tolerância à glicose de acordo com valores de glicose plasmática (mg/dl).

Existem outros testes laboratoriais relacionados ao controle de DM2 e acompanhamento de possíveis complicações, como:
– Avaliação de risco de doenças coronária e aterosclerótica: Colesterol Total, Colesterol HDL, Colesterol LDL.
– Avaliação da função renal: Ureia, Creatinina.
– Avaliação do metabolismo lipídico: Triglicérides.
3.6 TRATAMENTO
Atualmente, o tratamento do DM2 visa manter o controle glicêmico adequado, seja com dieta hipocalórica, aumento da prática de exercícios físicos ou uso de medicações (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000).
3.6.1 Dieta
A dieta é um dos pontos fundamentais no controle e tratamento do DM, que deve ter como objetivos, fornecer energia através dos nutrientes para manter ou melhorar o estado nutricional do indivíduo; manter e/ou reduzir a glicemia próxima aos níveis adequados, através de uma alimentação balanceada com a insulina e/ou hipoglicemiantes orais, e; atingir os níveis adequados de lipídios séricos, reduzindo o risco de morbidades associadas como as doenças cardiovasculares (BERTONHI, 2018).
A alimentação do diabético deve ser individualizada de acordo com as necessidades calóricas diárias, atividade física e hábitos alimentares. Em um indivíduo não diabético, o gasto calórico calculado é de cerca de 30 a 40 calorias/kg/dia, já no caso de um indivíduo portador de DM2 e obeso (o que ocorre em 85 a 90% dos casos) é necessário diminuir o valor calórico diário em 15 a 30% ou mais (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000).
Quanto a quantidade de macros, recomenda-se que o teor dos carboidratos da dieta, seja de 50 a 60% do total de calorias, além disso, deve ser incentivado o consumo de alimentos ricos em fibras, 20 a 35g por dia, as quais estão presentes nos legumes, raízes e tubérculos. O teor de proteínas deve ser entre 10 e 20% do total das calorias, uma vez que a dieta rica em proteínas e a hiperglicemia podem aumentar a taxa de filtração glomerular (em pacientes com nefropatia, recomenda-se 0,6 a 0,8 g/kg de peso de proteína ou menos). O teor de gorduras deve ser menor do que 30% do total de calorias da dieta, evitando-se as gorduras saturadas, de procedência animal, além das exceções vegetais, a do coco e a do dendê. A ingestão de colesterol deve ser menor que 300mg por dia. Recomenda-se 10% de gordura poli-insaturada (óleo de soja, milho, arroz) e 10% de gordura monoinsaturada (óleo de oliva, canola, etc.) e 10% ou menos de gordura saturada (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000).
Apenas essa mudança, já reduziria três dos fatores de risco para doença cardiovascular, a obesidade, a dislipidemia (presente em cerca de um terço dos diabéticos) e a hipertensão arterial (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000).
3.6.2 Exercícios Físicos
O exercício melhora a sensibilidade à insulina, diminui a hiperinsulinemia, aumenta a captação muscular de glicose, melhora o perfil lipídico e a hipertensão arterial, além da sensação de bem-estar físico e psíquico decorrente, além de também contribuir para a perda de peso (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000). O programa de treinamento físico acompanhado por profissionais qualificados, são extremamente recomendadas para as pessoas com Diabetes tipo 2, principalmente os exercícios de resistência, garantindo benefícios ao controle da glicemia, pressão arterial, lipídios e risco cardiovascular e minimizando lesões (SANTOS et al., 2021).
3.6.3 Hipoglicemiantes Orais, Anti-hiperglicemiantes e Sensibilizadores da Ação de Insulina
A prescrição de medicamentos para a DM2, geralmente ocorre quando com a dieta e o aumento da atividade física não foram capazes de obter um bom controle, ou seja, glicemias de jejum e pós prandial e hemoglobina glicosilada próximos aos níveis normais (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000).
Dentre os medicamentos utilizados para o tratamento do Diabetes mellitus tipo 2, temos:
– Sulfonilureias: agem estimulando as células β pancreáticas a secretar mais insulina pela inibição do canal de K+ sensível ao ATP, que provoca uma despolarização e ativa os canais de Ca++ levando a uma exocitose da insulina armazenada e aumenta a concentração plasmática da mesma; Tempos disponíveis: 1ª geração (Clorpropamida), 2ª geração, (glibenclamida, gliclazida e glipizida) e 3ª geração (glimepirida) (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000; ZANETTI et al., 2007).
– Meglitinidas: possuem o mesmo mecanismo de ação da sulfonilureias, mas estimulam a secreção prandial de insulina, ou seja, na presença de alimento (ZANETTI et al., 2007).
– Biguanidas: melhora a captação da glicose pelas células, melhorando a afinidade entre a insulina e seu receptor pelo aumento da atividade da proteinocinase dependente de AMP (AMPK). Temos disponíveis a metformina e a fenformina, sendo a primeira mais utilizada, pela menor frequência de efeitos colaterais (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000; ZANETTI et al., 2007).
– Tiazolinedionas: atuam na redução da resistência à insulina, no aumento do transporte de glicose e ainda tem efeito na melhora do perfil lipídico. Temos disponíveis a rosiglitazona e pioglitazona (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000).
– Inibidores da α glicosidase: retardam a absorção de glicose, reduzindo a glicemia pós-prandial São exemplos dessa classe acarbose e miglitol. (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000).
– Insulina: A insulinoterapia é realizada no paciente diabético tipo 2 num estágio avançado da doença, onde as células β pancreáticas já estão muito comprometidas (ARAÚJO; BRITTO; PORTO DA CRUZ, 2000).
3.7 ACOMPANHAMENTO
A DM2 não afeta todos os grupos populacionais igualmente. Há diferenças de acordo com sexo, status socioeconômico e etnia, sendo que grupos desfavoráveis economicamente estão mais expostos a experimentar dificuldades na adoção de estilo de vida saudável, isso provavelmente causado por determinantes sociais (VELOSO et al., 2020).
O acompanhamento de pessoas com diagnóstico de DM deve ser realizado, prioritariamente, pela Atenção Primária à Saúde (APS). A APS é considerada a porta de entrada para o sistema de saúde, por constituir nível próprio de atendimento (RADIGONDA et al., 2016).
Os profissionais de saúde devem incentivar os usuários a buscarem atendimento o mais precocemente possível, identificando possíveis sequelas e/ou intercorrências e incentivando a adesão ao tratamento (VELOSO et al., 2020). O acompanhamento periódico desses indivíduos, mediante ações de prevenção, identificação, manejo e controle desses agravos e suas complicações, tem como maior objetivo evitar internações hospitalares e reduzir a mortalidade por doenças cardiovasculares (RADIGONDA et al., 2016).
3.8 RASTREIO
Um rastreio, geralmente, é um processo em duas fases, onde a primeira corresponde à seleção, na população em geral, das pessoas com maior risco de doença; a segunda consiste na determinação dos níveis de glicemia desses indivíduos. A seleção, na primeira fase, pode ser feita quer através da pesquisa de fatores de risco de Diabetes pela aplicação de um questionário/score, são considerados fatores de risco: excesso de peso e obesidade, obesidade central ou visceral, idade (≥45 anos se europeus e ≥35 anos se de outra origem/região do mundo), vida sedentária, história familiar de Diabetes, em primeiro grau, Diabetes gestacional prévia, história de doença cardiovascular prévia: doença cardíaca isquêmica, doença cerebrovascular e doença arterial periférica, hipertensão arterial, dislipidemia, intolerância à glicose em jejum e diminuição da tolerância à glicose, prévias e o consumo de fármacos que predisponham à Diabetes (MARTINS et al., 2009).
O Quadro I contém os critérios Clássicos de Rastreio de Wilson e Jungner, adaptados pela Organização Mundial de Saúde:
Quadro I. Critérios para rastreio de Diabetes e Pré-Diabetes na população assintomática, não grávida. Adaptados das recomendações da ADA e USPSTF


Fonte: adaptado de AMERICAN DIABETES ASSOCIATION, 2009; MARTINS et al., 2009; SHEEHY; COURSIN; GABBAY, 2009; U.S. PREVENTIVE SERVICES TASK FORCE, 2008.
4. CONCLUSÃO
A partir deste trabalho, foi possível concluir que se faz essencial o conhecimento técnico e clínico sobre a fisiopatologia e alternativas de intervenção para o cuidado imediato e integral dos pacientes com Diabetes mellitus tipo 2, bem como a prevenção de suas complicações crônicas.
REFERÊNCIAS BIBLIOGRÁFICAS
AGUIAR, L. G. K. DE; VILLELA, N. R.; BOUSKELA, E. A microcirculação no Diabetes: implicações nas complicações crônicas e tratamento da doença. Arquivos Brasileiros de Endocrinologia & Metabologia, v. 51, p. 204–211, mar. 2007.
AMERICAN DIABETES ASSOCIATION. Standards of medical care in Diabetes-2009. Diabetes Care, v. 32 Suppl 1, n. Suppl 1, p. S13-61, jan. 2009.
ANDRADE, E. A. DE. Efeitos fisiológicos da atividade física suave e rotineira sobre os diversos sinais e sintomas do Diabetes Mellitus-Tipo 2. 2003.
ANTÃO, C. F.; GALLEGO, R.; CALDEIRA, J. Complicações renais da Diabetes Mellitus. Revista Portuguesa de Medicina Geral e Familiar, v. 23, n. 5, p. 577–94, 1 set. 2007.
ARAÚJO, L. M. B.; BRITTO, M. M. DOS S.; PORTO DA CRUZ, T. R. Tratamento do Diabetes mellitus do tipo 2: novas opções. Arquivos Brasileiros de Endocrinologia & Metabologia, v. 44, p. 509–518, dez. 2000.
ARAUJO, L. R. et al. Dados Epidemiológicos do Diabetes Mellitus no Brasil. Sociedade Brasileira de Diabetes, , 2023. Disponível em: <https://profissional.Diabetes.org.br/wp-content/uploads/2023/06/DadosEpidemiologicos-SBD_comT1Dindex.pdf>. Acesso em: 2 abr. 2024
ATKINSON, M. A. et al. Organisation of the human pancreas in health and in Diabetes. Diabetologia, v. 63, n. 10, p. 1966–1973, 1 out. 2020.
BERTONHI, L. G. Diabetes Mellitus tipo 2: aspectos clínicos, tratamento e conduta dietoterápica. mar. 2018.
BOAS, L. C. G.-V.; FOSS-FREITAS, M. C.; PACE, A. E. Adesão de pessoas com Diabetes mellitus tipo 2 ao tratamento medicamentoso. Revista Brasileira de Enfermagem, v. 67, p. 268–273, abr. 2014.
BOSCO, A. et al. Retinopatia diabética. Arquivos Brasileiros de Endocrinologia & Metabologia, v. 49, p. 217–227, abr. 2005.
BRANCO, V. G. C. et al. SEMIOLOGIA DO APARELHO CARDIOVASCULAR. ANATOMIA E FISIOLOGIA. Cadernos da Medicina – UNIFESO, v. 1, n. 1, 25 abr. 2018.
CASARIN, D. E. et al. Diabetes mellitus: causas, tratamento e prevenção. Brazilian Journal of Development, v. 8, n. 2, p. 10062–10075, 2022.
CASTANHOLA, M. E.; PICCININ, A. FISIOPATOLOGIA DA DIABETES E MECANISMO DE AÇÃO DA INSULINA REVISÃO DE LITERATURA. IX JORNACITEC – Jornada Científica e Tecnológica. Anais… Em: IX JORNACITEC – JORNADA CIENTÍFICA E TECNOLÓGICA. 30 set. 2020. Disponível em: <http://www.jornacitec.fatecbt.edu.br/index.php/IXJTC/IXJTC/paper/view/2154>. Acesso em: 9 abr. 2024
CASTRO, M. B. DE et al. Fatores de risco para retinopatia diabética: uma revisão. Revista de Patologia do Tocantins, v. 4, n. 3, p. 66–72, 26 set. 2017.
CASTRO, R. M. F. DE et al. Diabetes mellitus e suas complicações – uma revisão sistemática e informativa/ Diabetes mellitus and its complications – a systematic and informative review. Brazilian Journal of Health Review, v. 4, n. 1, p. 3349–3391, 20 fev. 2021.
CLARK, A. et al. Islet amyloid polypeptide in diabetic and non-diabetic Pima Indians. Diabetologia, v. 33, n. 5, p. 285–289, 1 maio 1990.
CORTEZ, D. N. et al. Complicações e o tempo de diagnóstico do Diabetes mellitus na atenção primária. Acta Paulista de Enfermagem, v. 28, p. 250–255, jun. 2015.
COSTA, B. B. DA; MOREIRA, T. A. Principais aspectos fisiopatológicos e clínicos presentes no Diabetes mellitus tipo I (autoimune). Research, Society and Development, v. 10, n. 14, p. e153101421773–e153101421773, 29 out. 2021.
FONSECA, K. P.; RACHED, C. D. A. Complicações do Diabetes mellitus. International Journal of Health Management Review, v. 5, n. 1, 2019.
GOMES, M. B.; SILVA, A. T. K.; SPINETI, P. P. M. Diabetes mellitus e coração: um continuum de risco Quais os alvos contemporâneos de tratamento e como alcançálos? Revista Hospital Universitário Pedro Ernesto (TÍTULO NÃO-CORRENTE), v. 12, 20 ago. 2013.
GRAZIANO, R. M.; LEONE, C. R. Problemas oftalmológicos mais freqüentes e desenvolvimento visual do pré-termo extremo. Jornal de Pediatria, v. 81, p. S95– S100, mar. 2005.
GROSS, J. L. et al. Diabetes Mellitus: Diagnosis, Classification and Glucose Control Evaluation. Arquivos Brasileiros de Endocrinologia & Metabologia, v. 46, p. 16– 26, fev. 2002.
GUGLIELMI, V.; SBRACCIA, P. Type 2 Diabetes: Does pancreatic fat really matter? Diabetes/Metabolism Research and Reviews, v. 34, n. 2, p. e2955, 2018.
JEREZ FERNÁNDEZ, C. I. et al. Fisiopatología y alteraciones clínicas de la Diabetes mellitus tipo 2: revisión de literatura. NOVA publ. cient, p. [39]-[39], 2022.
LEE, J. S. et al. Clinical implications of fatty pancreas: Correlations between fatty pancreas and metabolic syndrome. World Journal of Gastroenterology, v. 15, n. 15, p. 1869–1875, 21 abr. 2009.
LEE, S.-H.; PARK, S.-Y.; CHOI, C. S. Insulin Resistance: From Mechanisms to Therapeutic Strategies. Diabetes & Metabolism Journal, v. 46, n. 1, p. 15–37, 30 dez. 2021.
LUCENA, J. B. DA S. Diabetes mellitus tipo 1 e tipo 2. Monografia]. São Paulo (SP): Centro Universitário das Faculdades Metropolitanas Unidas, 2007.
MACAULEY, M. et al. Altered Volume, Morphology and Composition of the Pancreas in Type 2 Diabetes. PLOS ONE, v. 10, n. 5, p. e0126825, 7 maio 2015.
MAGLIANO, D. J.; BOYKO, E. J.; IDF DIABETES ATLAS 10TH EDITION SCIENTIFIC COMMITTEE. IDF DIABETES ATLAS. 10th. ed. Brussels: International Diabetes Federation, 2021.
MAIA, I. G.; SA, R. M. D. S. Anatomia e eletrofisiologia do coraçao: Anatomia e eletrofisiologia do coraçao. Journal of Cardiac Arrhythmias, v. 1, n. 1, p. 9–17, 1988.
MARSHALL, S. M. The pancreas in health and in Diabetes. Diabetologia, v. 63, n. 10, p. 1962–1965, 1 out. 2020.
MARTINS, V. et al. Rastreio de Diabetes Mellitus Tipo 2. Revista Portuguesa de Diabetes, v. 4, n. 4, p. 156–162, 2009.
MURUSSI, M. et al. Diabetic nephropathy in type 2 Diabetes mellitus: risk factors and prevention. Arquivos Brasileiros de Endocrinologia & Metabologia, v. 47, n. 3, p. 207–219, jun. 2003.
NASCIMENTO, O. J. M. DO; PUPE, C. C. B.; CAVALCANTI, E. B. U. Neuropatia diabética. Revista Dor, v. 17, p. 46–51, 2016.
NEVES, R. G. et al. Complicações por Diabetes mellitus no Brasil: estudo de base nacional, 2019. Ciência & Saúde Coletiva, v. 28, p. 3183–3190, 10 nov. 2023.
Número de pessoas com Diabetes nas Américas mais do que triplica em três décadas, afirma relatório da OPAS – OPAS/OMS |. Disponível em: <https://www.paho.org/pt/noticias/11-11-2022-numero-pessoas-com-Diabetes-nasamericas-mais-do-que-triplica-em-tres-decadas>. Acesso em: 2 abr. 2024.
OLIVEIRA, M. S. et al. Diabetes Mellitus tipo 2 – uma revisão abrangente sobre a etiologia, epidemiologia, fisiopatologia, diagnóstico e tratamento. Brazilian Journal of Health Review, v. 6, n. 5, p. 24074–24085, 6 out. 2023.
Panorama of Diabetes in the Americas. [s.l.] Pan American Health Organization, 2022. Disponível em: https://iris.paho.org/handle/10665.2/56643.
PIROG, G. et al. ANATOMIA RENAL. Revista Ciências da Saúde Unisantacruz, v. 1, n. 01, 2012.
RADIGONDA, B. et al. Avaliação do acompanhamento de pacientes adultos com hipertensão arterial e ou Diabetes melito pela Estratégia Saúde da Família e identificação de fatores associados, Cambé-PR, Brasil, 2012. Epidemiologia e Serviços de Saúde, v. 25, p. 115–126, mar. 2016.
REIS, M. G. V.; VIVAN, R. H. F.; GUALTIERI, K. DE A. Diabetes mellitus gestacional: aspectos fisiopatológicos materno-fetais. Revista Terra & Cultura: Cadernos de Ensino e Pesquisa, v. 35, n. 69, p. 32–45, 18 out. 2019.
RODRIGUES, T. M. DE A. Aula 16 – Sistema Cardiovascular. Em: Elementos da Anatomia Humana. [s.l: s.n.]. p. 247–286.
ROMACIUC, M. Diabetes Mellitus Tipo 2 como Doença Inflamatória: anatomia, fisiopatologia e terapêutica. 2017.
SANTOS, G. DE O. et al. Exercícios físicos e Diabetes mellitus: Revisão / Physical exercises and Diabetes mellitus: Review. Brazilian Journal of Development, v. 7, n. 1, p. 8837–8847, 22 jan. 2021.
SCHEFFEL, R. S. et al. Prevalência de complicações micro e macrovasculares e de seus fatores de risco em pacientes com Diabetes melito do tipo 2 em atendimento ambulatorial. Revista da Associação Médica Brasileira, v. 50, p. 263–267, set. 2004.
SHEEHY, A. M.; COURSIN, D. B.; GABBAY, R. A. Back to Wilson and Jungner: 10 Good Reasons to Screen for Type 2 Diabetes Mellitus. Mayo Clinic Proceedings, v. 84, n. 1, p. 38–42, jan. 2009.
SILVA-NUNES, J. Fisiopatologia da Diabetes mellitus tipo 1 e tipo 2 (100 perguntas chave na Diabetes). 1 mar. 2018.
SLACK, J. M. W. Developmental biology of the pancreas. Development, v. 121, n. 6, p. 1569–1580, 1 jun. 1995.
TSCHIEDEL, B. Complicações crônicas do Diabetes. v. 102, n. 5, 2014.
U.S. PREVENTIVE SERVICES TASK FORCE. Screening for type 2 Diabetes mellitus in adults: U.S. Preventive Services Task Force recommendation statement. Annals of Internal Medicine, v. 148, n. 11, p. 846–854, 3 jun. 2008.
VELOSO, J. et al. Perfil clínico de portadores de Diabetes Mellitus em acompanhamento multiprofissional em saúde. Revista Cuidarte, v. 11, n. 3, dez. 2020.
VIANA, M. R.; RODRIGUEZ, T. T. Complicações cardiovasculares e renais no Diabetes mellitus. http://www.portalseer.ufba.br/index.php/cmbio/issue/current/showToc, 2011.
WESTERMARK, P. et al. Islet amyloid polypeptide-like immunoreactivity in the islet B cells of Type 2 (non-insulin-dependent) diabetic and non-diabetic individuals. Diabetologia, v. 30, n. 11, p. 887–892, 1 nov. 1987.
ZANETTI, M. L. et al. Evolução do tratamento de pacientes diabéticos utilizando o protocolo staged Diabetes management. Acta Paulista de Enfermagem, v. 20, p. 338–344, set. 2007.
ZELANIS, S. K. et al. Achados de fundoscopia em pacientes com Diabetes mellitus atendidos no Hospital Nossa Senhora da Conceição. Clinical and biomedical research. Porto Alegre, 2015.
