TRATAMENTO HIV/TUBERCULOSIS CO-INFECTION: CHALLENGES IN PATIENT’S ADHERENCE TO TREATMENT
COINFECCIÓN VIH / TUBERCULOSIS: RETOS EN LA ADHESIÓN AL TRATAMIENTO
REGISTRO DOI: 10.69849/revistaft/th10249281214
Diêgo da Silva Fernandes1
Hermínio Oliveira Medeiros2
Resumo
Objetivo: Compreender o que influencia na não-adesão ao tratamento da co-infecção HIV/Tuberculose. Método: Pesquisa descritiva com revisão integrativa de artigos. Resultados: Poucos pacientes co-infectados utilizão medicação e os óbitos por HIV/Tuberculose aumentaram nos últimos anos. A co-infecção HIV/Tuberculose possui um tratamento longo, com grande quantidade de medicamentos e diversos efeitos colaterais, dificultando a adesão. Fatores como preconceito, falta de acesso a informação e condições de vida precárias aumentam a taxa de abandono. Conclusão: É necessária uma proximidade maior com os co-infectados, incentivar a busca por tratamento e fazer acompanhamento para garantir uma boa adesão. Descritores: HIV, tuberculose e tratamento.
Abstract
Objective: To understand what influences non-adherence to treatment of HIV / tuberculosis co-infection. Method: Descriptive research with integrative review of articles. Results: Few co-infected patients use medication and deaths from HIV / tuberculosis have increased in recent years. HIV / Tuberculosis co-infection has a long treatment, with a large amount of drugs and several side effects, making adherence difficult. Factors such as prejudice, lack of access to information and poor living conditions increase the dropout rate. Conclusion: Closer proximity to co-infected people is needed, encourage the search for treatment and follow up to ensure good adherence. Descriptors: HIV, tuberculosis and treatment.
Resumen
Objetivo: Comprender lo que influye en la no adhesión al tratamiento de la coinfección VIH / Tuberculosis. Método: Investigación descriptiva con revisión integrativa de artículos. Resultados: Pocos pacientes coinfectados usan medicamentos y las muertes por VIH / tuberculosis han aumentado en los últimos años. La coinfección por VIH / tuberculosis tiene un tratamiento prolongado, con una gran cantidad de medicamentos y varios efectos secundarios, lo que dificulta la adherencia. Factores como el prejuicio, la falta de acceso a la información y las malas condiciones de vida aumentan la tasa de deserción. Conclusión: Se necesita un contacto más cercano con las personas coinfectadas, fomentar el tratamiento y seguimiento para asegurar una buena adherencia. Descritores: VIH, tuberculosis y tratamiento.
1. INTRODUÇÃO
A AIDS (Síndrome da Imunodeficiência Adquirida) é uma doença causada por meio da infecção pelo Vírus da Imunodeficiência Humana (HIV) e atinge o sistema imunológico, principalmente os Linfócitos T-CD4, levando a sua destruição gradual (MINISTÉRIO DA SAÚDE, 2018). Portadores de HIV ou apresentando a AIDS, devido a sua resposta imunológica deficiente, têm uma maior chance de serem infectados por doenças oportunistas como, por exemplo, a tuberculose. A tuberculose é uma doença causada pelo Mycobacterium tuberculosis ou também conhecido como bacilo de Koch, é uma patologia infecciosa que pode ser transmitida a partir da eliminação dos bacilos por via respiratória (GASPAR et al., 2016).
De acordo com a OMS (2012): “O risco de indivíduos com HIV desenvolverem a tuberculose é de 20 a 37 vezes maior do que pacientes não infectados pelo HIV” e para Viveiros et al., (2012), nesses pacientes as probabilidades de uma tuberculose latente evoluir para um quadro de tuberculose ativa variam de 5 a 10%. A taxa de mortalidade em pacientes co-infectados por tuberculose-HIV está aumentando quando é comparada a pacientes que são HIV negativos. “A presença do HIV alerta para a transformação da tuberculose de uma doença endêmica para epidêmica” (GASPAR et al., 2016).
O diagnóstico e tratamento precoce do HIV com antirretrovirais durante o tratamento da tuberculose aumentam as chances de cura desta em até 90%, aumentando também o tempo de sobrevida do paciente. Porém, no período de seis meses é onde se ocorre maior abandono do tratamento dos tuberlostáticos e/ou dos antirretrovirais, fazendo com que a resistência aos medicamentos seja desenvolvida (FILHO, 2012).
Mesmo com uma alta probabilidade de cura da tuberculose em pessoas vivendo com HIV/AIDS (PVHA), muitos pacientes desistem do tratamento sucumbindo à doença. O objetivo deste trabalho é compreender os fatores que influenciam na não-adesão ao tratamento da co-infecção HIV/Tuberculose.
2. MÉTODO
O presente trabalho trata-se de uma pesquisa do tipo descritiva realizando uma revisão integrativa de dados disponibilizados em plataformas de dados científicos online.
A revisão integrativa determina o conhecimento atual sobre uma temática específica, já que é conduzida de modo a identificar, analisar e sintetizar resultados de estudos independentes sobre o mesmo assunto, contribuindo, pois, para uma possível repercussão benéfica na qualidade dos cuidados prestados ao paciente (SOUZA et al., 2010).
Foram empregados os descritores “HIV, tuberculose e tratamento”, encontrados no DECS da Bireme, juntamente com o operador booleano “and”. Os bancos de dados utilizados foram a Biblioteca Virtual em Saúde (BVS), Scientific Eletronic Library Online (SciELO) e Periódicos Capes. A pergunta norteadora para seleção dos artigos foi: “Por que os pacientes têm dificuldade na adesão do tratamento da co-infecção HIV/Tuberculose?”. Os portais do Ministério da Saúde, Conselho Federal de Farmácia e da Organização Mundial da Saúde também serviram como base para a pesquisa por meio de livretos, guias básicos, manuais técnicos e cartilhas de dados epidemiológicos. A partir da definição dos descritores, aplicaram-se os seguintes critérios de inclusão: artigos relacionados ao tratamento da co- infecção de HIV/Tuberculose, no idioma Português, disponibilizados de forma gratuita e publicados no período de 2012-2018.
Os critérios de exclusão para rejeição de artigos foram: artigos em outros idiomas, disponibilizados de forma não gratuita e publicados em anos anteriores a 2012 e artigos não relacionados com o tema proposto. Os artigos foram selecionados entre os dias 15/03/2019 e 30/03/2019.
Além do levantamento bibliográfico, realizou-se neste trabalho, uso de dados secundários encontrados no SINAN (Sistema de Informação de Agravos de Notificação), SVS (Secretaria de Vigilância em Saúde), SIM (Sistema de Informação sobre Mortalidade) e DIAHV (Departamento de Vigilância Prevenção e Controle das IST, do HIV/Aids e das Hepatites Virais). Os dados utilizados são referentes aos anos 2012, 2016 e 2017 e foram apresentados no texto por meio de gráficos.
3. RESULTADOS
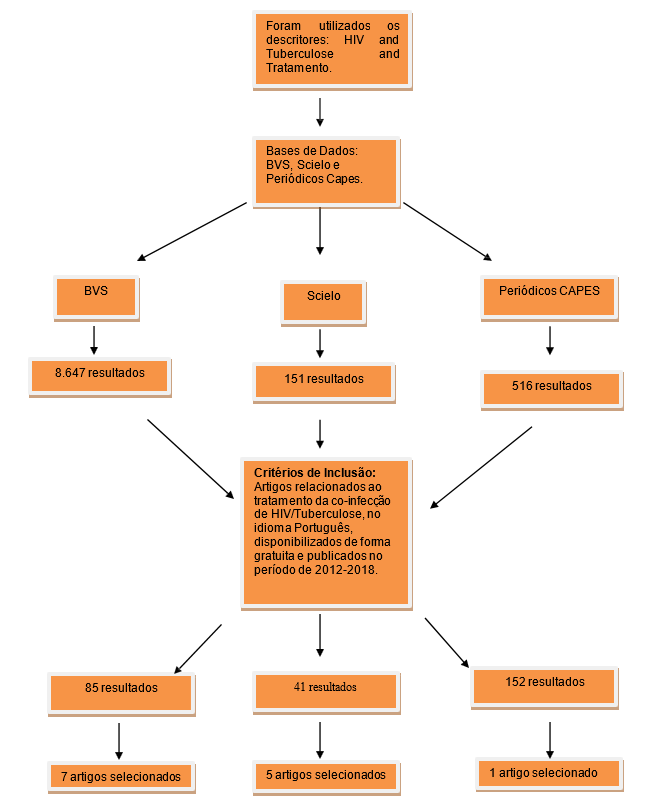
A partir da utilização dos descritores nas bases de dados e seguindo os critérios de inclusão e exclusão, obteve-se um total de 13 artigos (Figura 1), publicados em 11 diferentes revistas relacionadas à área da saúde (Quadro 1).
Figura 1. Organograma
Quadro 1. Relação de artigos encontrados nos bancos de dados por ano de publicação e revistas em que foram publicados
Título do Artigo Publicação Revista Tratamento da Tuberculose em Situações Especiais 2012 Revista Pulmão Tuberculose em Situações Especiais: HIV, Diabetes Mellitus e Insuficiência Renal 2012 Revista Pulmão Avaliação do acesso ao tratamento de Tuberculose por co-infectados ou não pelo Vírus da imunodeficiência humana 2012 Revista da Escola de Enfermagem da USP Pacientes vivendo com hiv/aids e co-infecção tuberculose: Dificuldades associadas à adesão ou ao abandono do tratamento 2012 Revista gaúcha de enfermagem, Adesão ao rastreio e tratamento da tuberculose em doentes infetados com o vírus da imunodeficiência humana 2013 Revista Portuguesa de Pneumologia Prova tuberculínica: o controle da tuberculose em pacientes infectados pelo vírus da imunodeficiência humana (HIV) 2015 Revista Semina: Ciências Biológicas e da Saúde, Os significados da comorbidade para os pacientes vivendo com TB/HIV: repercussões no tratamento 2015 Physis Revista de Saúde Coletiva Controle da Tuberculose em pessoas vivendo com HIV/AIDS 2016 Revista Latino-Americana de Enfermagem Fatores sociais, clínicos e de adesão em co- infectados por HIV/Tuberculose: estudo descritivo 2016 Online Brazilian Journal of Nursing Análise temporal dos casos notificados de tuberculose e de co-infecção tuberculose-HIV na população brasileira no período entre 2002 e 2012 2016 Jornal Brasileiro de Pneumologia Adesão aos antirretrovirais em pessoas com co-infecção pelo vírus da imunodeficiência 1 humana e tuberculose 2016 Revista Latino-Americana de Enfermagem Sobrevida de pacientes com AIDS e co- infecção pelo bacilo da tuberculose nas regiões Sul e Sudeste do Brasil 2017 Revista Ciência & Saúde Coletiva Infecção latente por tuberculose entre pessoas com HIV/AIDS, fatores associados e progressão para doença ativa em município no Sul do Brasil 2017 Cad. Saúde Pública 2017
Quando classificados em acordo com a base de dados utilizada (Quadro 2), observa-se que a plataforma BVS apresentou o maior número de artigos, com o total de 7 artigos publicados na temática. Na plataforma Scielo, após os critérios aplicados, encontrou-se 5 artigos, enquanto no periódico CAPES, 1 artigo.
Quadro 2. Relação do número de artigos publicados por base de dados
Base de dados Nº de artigos publicados BVS 7 Periódicos CAPES 1 Scielo 5
Em seguida, após a seleção dos artigos, procedeu-se a verificação do Qualis de cada revista cujo os artigos foram selecionados para esta pesquisa (Quadro 3). Os 13 artigos selecionados são provenientes de 11 diferentes revistas, das quais 2 possuem Qualis A2, 4 possuem Qualis B1, 3 com Qualis B2 e 2 com Qualis B3.
Quadro 3. Relação de Qualis das revistas nas quais foram publicados os artigos encontrados
Revista ISSN Qualis Cad. Saúde Pública 0102-311X B1 Jornal Brasileiro de Pneumologia 1806-3713 B1 Online Brazilian Journal of Nursing 1676-4285 B1 Physis Revista de Saúde Coletiva 0103-7331 B2 Pulmão RJ 2176-2465 B3 Revista Ciência & Saúde Coletiva 1413-8123 B2 Revista da Escola de Enfermagem da USP 0080-6234 A2 Revista Gaúcha de Enfermagem 0102-6933 B1 Revista Latino-Americana de Enfermagem 1518-8345 B3 Revista Portuguesa de Pneumologia 0873-2159 B2 Revista Semina: Ciências Biológicas e da Saúde 1676-5435 A2
Fonte: Plataforma Sucupira
Além dos artigos, foram selecionadas cartilhas de indicadores epidemiológicos disponibilizadas no site do Ministério da Saúde, como os Protocolos Clínicos e Diretrizes Terapêuticas (PCDTs), Boletins Epidemiológicos de HIV e os Panoramas da Tuberculose no Brasil.
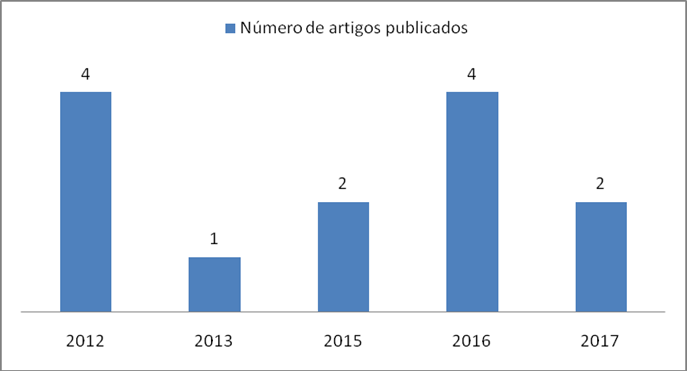
Organizando os artigos por ano publicado, nota-se que os anos de 2012 e 2016 possuem uma maior freqüência de publicações que os demais anos analisados (Gráfico 1).
Grafico1. Relação do número de artigos encontrados por ano de publicação
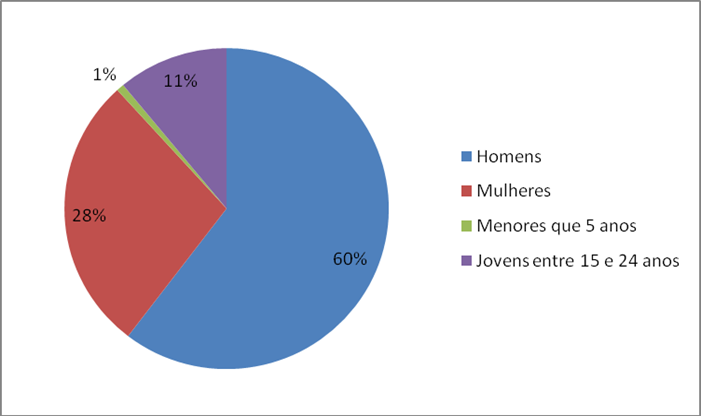
Os resultados apresentados tanto pelos artigos selecionados quanto pelos dados disponibilizados no SINAN, mostram que a incidência do HIV no Brasil se dá em sua grande maioria na população masculina com o equivalente a 60% dos casos, seguido por 28% representando as mulheres, 11% de jovens entre 15 e 24 anos e 1% de crianças menores que 5 anos (Gráfico 2).
Grafico2. Percentual de infectados por HIV no Brasil no ano de 2016
Fonte: Sinan/MS
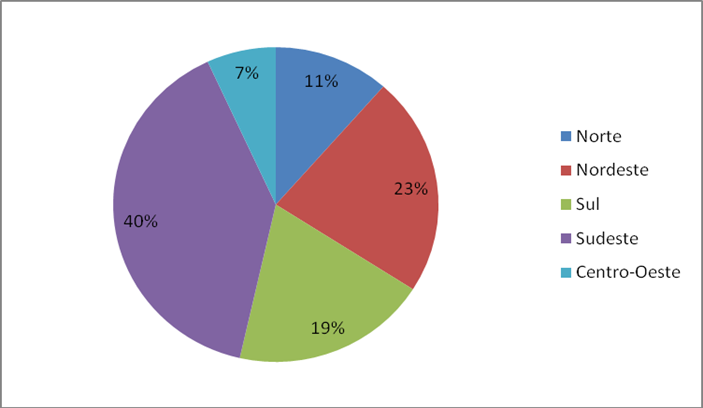
Se analisarmos o número de casos de HIV notificados no Sinan no ano de 2016 (Gráfico 3), por região, observa-se que a região Sudeste lidera com 40% do total de casos notificados, seguida pela região Nordeste (23%), Sul (19%), Norte (11%) e Centro-Oeste (7%).
Gráfico 3. Percentual de infectados por HIV por região do Brasil no ano de 2016
Fonte: Sinan/MS
Houve também um aumento exacerbado nos casos de HIV notificados no país num curto período de tempo. No ano de 2012 o número de casos girava em torno de 14.000 pessoas infectadas. Já em 2017 verifica-se um total de aproximadamente 43.000 pessoas infectadas (Gráfico 4).
Gráfico 4: Notificações de casos de HIV no Brasil entre os anos 2012 e 2017.
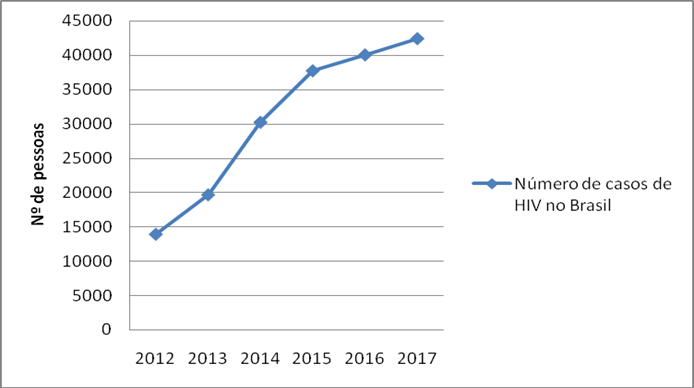
Fonte: MS/SVS/Departamento de Vigilância, Prevenção e Controle das IST, do HIV/AIDS e das Hepatites Virais, apud, Secretaria de Vigilância em Saúde (Adaptado).
Já a tuberculose apresentou uma queda, a nível nacional, na incidência de novos casos entre os anos de 2012 e 2016. Em 2012 o número total de notificações no SINAN era de 71.755 pessoas infectadas, e em 2016 esse número caiu para 70.086 pessoas infectadas. Porém, as regiões Norte e Sudeste obtiveram um aumento nesse número, sendo de 7.293 para 7.889 pessoas infectadas na região Norte e de 32.190 para 32.361 pessoas infectadas na região Sudeste. Já no ano de 2017 ocorreu um aumento considerável, atingindo o total de 73.070
pessoas infectadas em todo o Brasil. Novamente, as regiões Norte e Sudeste apresentaram aumento no número de pessoas infectadas, atingindo, respectivamente, 8.429 e 33.996 casos. (Gráfico 5). Vale destacar que estudos comprovaram que a incidência de tuberculose é maior em locais com baixo IDH, e os estados da região Norte possuem um dos menores IDHs do Brasil (SANTOS ET AL, 2016).
Quanto a região Sudeste, há uma relação muito forte entre cidades populosas e a incidência de tuberculose. A alta taxa de desemprego, grandes aglomerados de pessoas e distribuição desigual de renda também contribuem para a disseminação da tuberculose pois, com um grande número de pessoas muito próximas, o contato com o agente patológico é aumentado (PELISSARI E QUIJANO, 2017).
Mesmo com a queda, o agravante da situação são os portadores de HIV não tratados que possuem maior tendência de contrair tuberculose, e em alguns casos a testagem para HIV em pacientes com tuberculose é negligenciada. De todos os casos de tuberculose notificados no Brasil, foram solicitados teste para HIV de 81,8% dos pacientes. Destas solicitações, 76,3% foram realizadas e 9,4% dos resultados foram positivos para co-infecção (Gráfico 6). A região Nordeste fica por último nas solicitações de teste para HIV, sendo 73,4% de pedidos, 65,9% de testes realizados e 10,1% de resultados positivos para co-infecção. Já a região Sul lidera quanto ao número de solicitações com um total de 90,4%, 87,5% de realizações e 16,1% de confirmações de co-infecção.
Gráfico 5. Comparativo no número de novos casos de tuberculose notificados nos anos de 2012, 2016 e 2017.
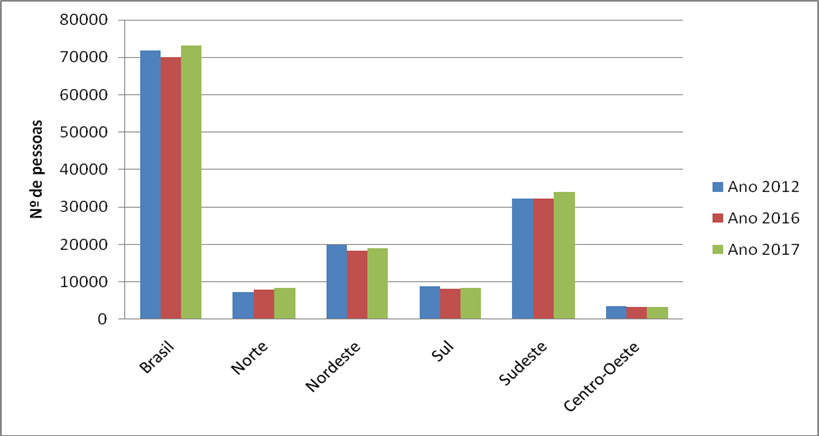
Fonte: Sinan/MS
Gráfico 6. Percentual de realizações de testes para HIV em pacientes com tuberculose, 2016
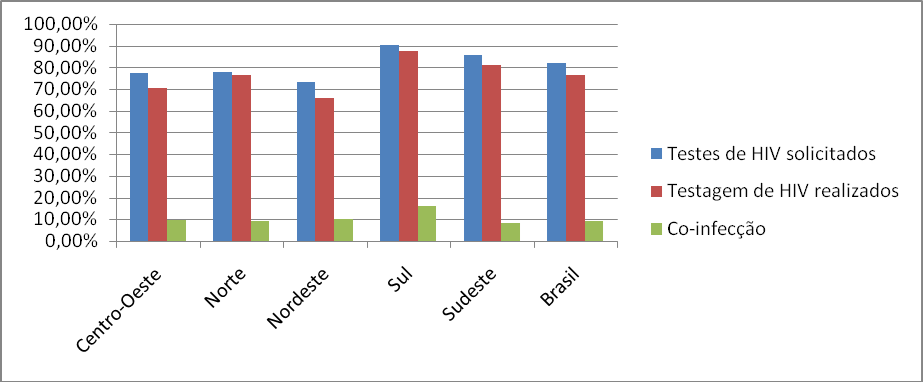
Fonte: Sinan/MS
Dentre os co-infectados por HIV/TB notificados no SINAN em 2016, nem todos estão fazenco uso de TARV (Terapia antirretroviral) (Gráfico 7). Dos 2.580 co-infectados residentes na região Sudeste, aproximadamente 926 estão em uso de TARV. Na região Nordeste, dos 1.491 co-infectados, aproximadamente 600 fazem uso da medicação. Essas atitudes pode acarretar num maior índice de mortalidade dessa população.
Gráfico 7. Relação de co-infecção HIV/Tb e uso de TARV, 2016
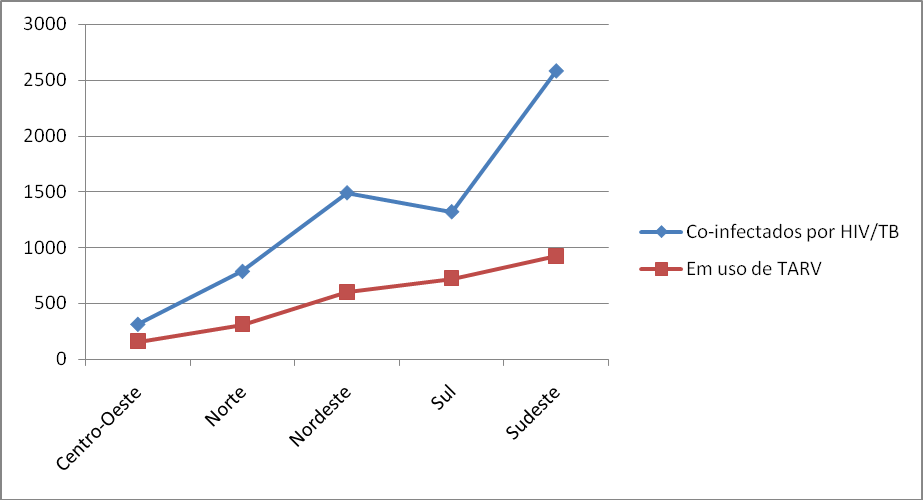
Fonte: Sinan. Base de dados de maio de 2017, apud, Secretaria de Vigilância em Saúde (Adaptado)
Mesmo se tratando de uma doença que já possui cura, a tuberculose é a maior causadora de óbitos em pacientes portadores de HIV (Gráfico 8). Do total de mortes com tuberculose como causa básica no país, notificados no SINAN, 65% eram portadores de HIV.
As doenças do aparelho circulatório estavam relacionadas a 7,4% dos óbitos, as neoplasias giraram em torno de 7%, doenças do aparelho respiratório com 4,9%, doenças do aparelho digestivo em torno de 4,2% e outras causas aproximadamente 11,5%.
Os casos de co-infecção HIV/tuberculose são uma grande preocupação devido as dificuldades relacionadas ao seu tratamento. Dados do SINAN indicam que no surgimento de novos casos de co-infecção em 2016 houve 49,1% de cura da tuberculose nos pacientes que seguiram corretamente o tratamento, porém, em casos de retratamento (pacientes portadores de HIV que se infectram novamente com tuberculose) os índices de cura da tuberculose foram de 35,8% (Gráfico 9). Um dado muito relevante visto nessa mesma época foi que do surgimento de novos casos de co-infecção 13,9% dos pacientes abandonaram o tratamento, enquanto nos casos de retratamento esse percentual de abandono subiu para 31,5%.
Gráfico 8. Percentual de óbitos que apresentaram tuberculose como causa básica, 2014
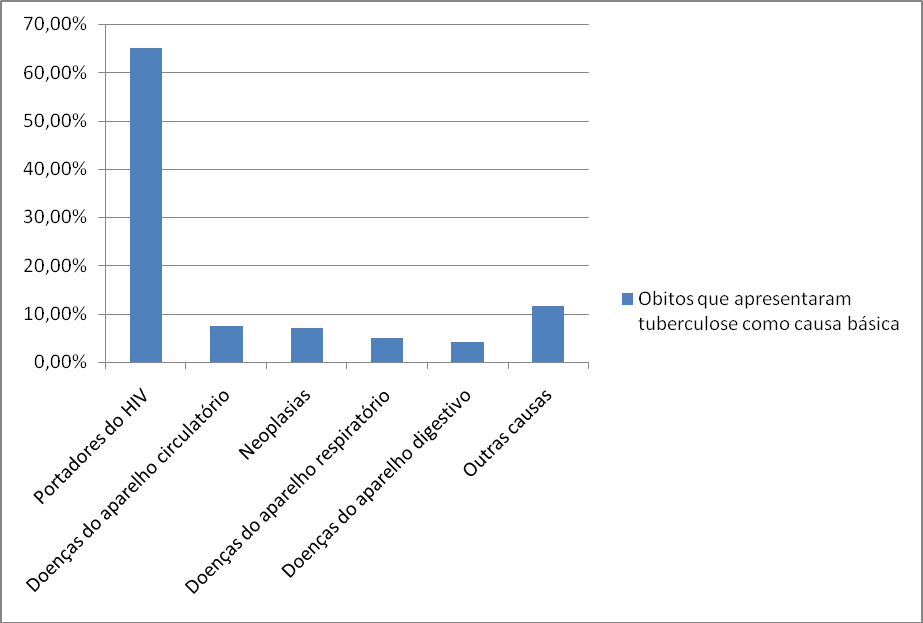
Fonte: SIM/MS e IBGE, apud, Secretaria de Vigilância em Saúde (Adaptado)
Gráfico 9. Desfechos dos casos de co-infecção HIV/Tb, 2016
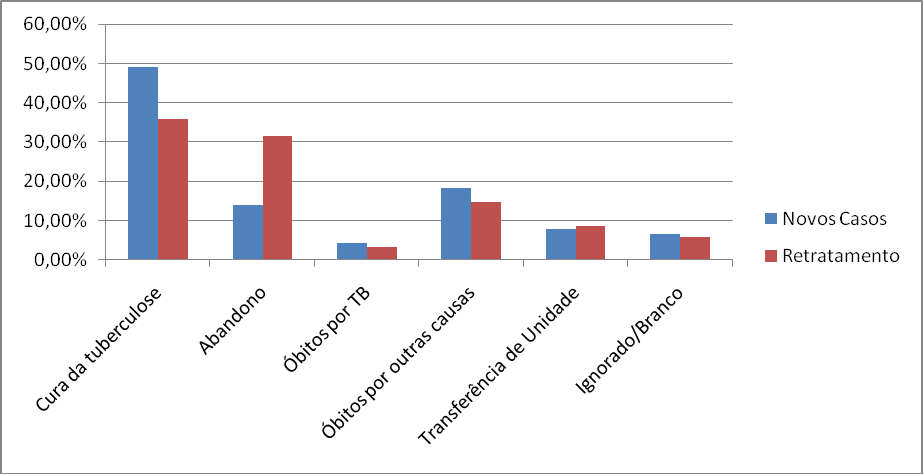
Fonte: Sinan, apud, Secretaria de Vigilância em Saúde (Adaptado)
4. DISCUSSÃO
Para um melhor entendimento, a construção narrativa está dividida em quatro capítulos. O Capítulo 1 diz respeito ao Vírus da Imunodeficiência Humana (HIV) no contexto histórico, patogenia, diagnóstico e tratamento. O Capítulo 2 trata da Tuberculose indicando sua patogênese, métodos de diagnóstico e tratamento. O Capítulo 3 cita a Co-infecção HIV/Tuberculose exemplificando o seu desenvolvimento, detecção e cuidados. Já o Capítulo 4 aborda as Intervenções Farmacêuticas e a adesão ao tratamento da Co-Infecção HIV/Tb, dando ênfase nas dificuldades durante o tratamento apontando os fatores clínicos e sociais para as mesmas.
Capítulo 1 – Vírus da Imunodeficiência Humana (HIV)
Segundo o Ministério da Saúde (2018), foi identificado pela primeira vez, no Brasil, no ano de 1980 na cidade de São Paulo, o primeiro caso do que viria a se chamar HIV. Em 1982 surgiu o primeiro nome para a nova doença, “Doença dos 5H, representando os homossexuais, hemofílicos, haitianos, heroinômanos (usuários de heroína injetável) e hookers (denominação em inglês para as profissionais do sexo)” (MINISTERIO DA SAÚDE, 2018). Ainda em 1982, descobriu-se que o HIV poderia ser transmitido por contato sexual, compartilhamento de seringas e nesse mesmo ano ocorreu o primeiro caso de HIV por meio da transfusão de sangue.
Entre os anos de 1983 e 1985 foi notificado no Brasil o primeiro caso de HIV numa pessoa do sexo feminino além do primeiro caso de transmissão vertical (de mãe para filho). Em 1985 surge o termo HIV (Human Immunodeficiency Virus), é liberado o primeiro teste para diagnóstico da doença e o governo federal cria a Portaria 236 de 2 de maio de 1985 que dispõe do controle da AIDS no país (MINISTERIO DA SAÚDE, 2018).
Nos anos de 1986 e 1987 os casos de HIV notificados no Brasil alcançam a faixa de 2.775 casos, sendo criado o Programa Nacional de DST e AIDS. Nesse período, a cidade de Porto Alegre (RS) ganha o primeiro centro de orientação sorológica do Brasil e a zidovudina começa a ser utilizada no tratamento de câncer e HIV. Neste mesmo período, o dia 1º de dezembro é escolhido como dia mundial da luta contra a AIDS.
No período de 1988 e 1991, a doença toma notoriedade com morte de brasileiros famosos devido quadro de AIDS. Logo, os casos de HIV no Brasil quadruplicam, o Sistema Único de Saúde (SUS) é criado, iniciando a distribuição de gratuita dos antirretrovirais, além do lançamento do primeiro antirretroviral da classe dos inibidores da transcriptase reversa, que daria inicio ao controle do vírus HIV no mundo. Dessa forma, reduzem-se consideravelmente os quadros de AIDS (MINISTERIO DA SAÚDE, 2018).
Com o avanço do entendimento sobre a doença, foi possível classificar biologicamente o vírus e elucidar seu ciclo compreendendo melhor a patogênese do vírus e permitindo o desenvolvimento de protocolos eficazes. Define-se, então, que o HIV se trata de um vírus pertencente ao gênero lentivírus, que são “uma família de retrovírus de mamíferos que estabelecem infecções persistentes crônicas, com instalação gradual dos sintomas clínicos” (GOODMAN AND GILMAN, 2012).
O vírus do HIV possui um tropismo controlado por uma proteína chamada gp160 que possui afinidade pelos receptores CD4 que se encontram nos linfócitos. Outra proteína denominada gp41 realiza a fusão da membrana do vírus com a membrana dos linfócitos humanos liberando no citoplasma da célula hospedeira o RNA viral, o qual produz uma cópia do DNA viral e começa um processo de replicação do vírus. O DNA viral migra para o núcleo e em seguida funde-se com o cromossomo do hospedeiro através da integrase viral. A partir desse momento, a célula infectada começa o seu processo de replicação e, ao mesmo tempo em que ocorre a transcrição do DNA do hospedeiro, ocorre também à transcrição do DNA viral integral acarretando na produção de proteínas e RNA virais. Estas proteínas se agrupam ao redor do RNA viral formando um nucleocapsídio que dará origem a novos vírus HIV, os quais brotam pela membrana celular destruindo o linfócito infectado, caem na corrente sanguínea e realizam o mesmo processo em outros linfócitos (GOODMAN AND GILMAN, 2012).
Por fim, a contagem de linfócitos T CD4+ do hospedeiro começa a sofrer um declínio constante, acompanhado de elevações nas concentrações plasmáticas de RNA do HIV. Quando a contagem periférica de células CD4 cai abaixo de 200 células/mm³, existe um risco cada vez maior de doenças oportunistas e, finalmente, de morte. (GOODMAN AND GILMAN, 2012)
O HIV, em pacientes não tratados, pode manifestar três fases distintas após a infecção, sendo elas a Infecção Aguda (que ocorre nas primeiras semanas), Latência Clínica (ocorrendo nos primeiros anos) e a AIDS (podendo surgir em até 10 anos) (MINISTÉRIO DA SAÚDE, 2018).
Na fase aguda há a replicação intensa do vírus HIV, o que leva ao decaimento dos linfócitos T-CD4 e aumento da CV-HIV (MINISTÉRIO DA SAÚDE, 2018). Por se tratar de uma infecção viral aguda há o surgimento de sintomas denominados Síndrome Retroviral Aguda (SRA)
Os principais achados clínicos de SRA incluem febre, cefaleia, astenia, adenopatia, faringite, exantema e mialgia. A SRA pode cursar com febre alta, sudorese e linfadenomegalia, comprometendo principalmente as cadeias cervicais anterior e posterior, submandibular, occipital e axilar. Podem ocorrer, ainda, esplenomegalia, letargia, astenia, anorexia e depressão. (MINISTÉRIO DA SAÚDE, 2018)
Durante a fase de Latência Clínica, geralmente há presença de linfadenopatia e plaquetopenia. Com a contagem de LT-CD4 reduzida é freqüente o surgimento de infecções bacterianas como, por exemplo, a tuberculose e podendo progredir para infecção atípica. Um importante marcador para infecção grave é a presença de candidíase oral e com a progressão da infecção é comum o surgimento de sintomas constitucionais como febre, cefaléia, diarréia crônica e fadiga (MINISTÉRIO DA SAÚDE, 2018).
Na AIDS, a contagem do LT-CD4 se encontra bem abaixo de 200 cel/mm³ e ocorrem freqüentes infecções oportunistas (neurotoxoplasmose, meningite criptocócica e tuberculose pulmonar disseminada) e neoplasias (sendo o Sarcoma de Kaposi a mais comum) (MINISTÉRIO DA SAÚDE, 2018).
Além das infeccoes e das manifestacoes nao infecciosas, o HIV pode causar doenças por dano direto a certos orgaos ou por processos inflamatorios, tais como miocardiopatia, nefropatia e neuropatias, que podem estar presentes durante toda a evolucao da infeccao pelo HIV. (MINISTÉRIO DA SAÚDE, 2018)
O diagnostico de HIV é feito a partir da detecção de anticorpos anti-HIV, e no Brasil segue os critérios estabelecidos pela Portaria Nº59/2003 do Ministério da Saúde.
De acordo com a Portaria Nº59/2003, “… para o diagnóstico laboratorial da infecção pelo HIV, é exigido o cumprimento rigoroso dos procedimentos seqüenciados, agrupados em
três etapas.” Sendo elas a Triagem Sorológica por meio de testes rápidos os quais, tendo resultado positivo, levarão a uma investigação mais ampla por meio da Confirmação Sorológica. Nesta, realiza-se um imunoensaio em paralelo ao teste de Imunofluorescência Indireta para o HIV-1 (IFI/HIV-1) ou ao teste de Imunoblot para HIV e, se ainda restarem dúvidas quanto ao resultado, realiza-se o teste de Western blot para HIV-1 (WB/HIV-1) (MINISTERIO DA SAUDE, 2003).
Para que os testes sejam capazes de detectar os anticorpos anti-HIV é necessário ter passado o período da janela diagnóstica, que se refere ao “…tempo decorrido entre a infecção e o aparecimento ou detecção de um marcador da infecção, seja ele RNA viral, DNA proviral, antígeno p24 ou anticorpo” (MINISTÉRIO DA SAÚDE, 2013).
Levando em conta que a incidência de infecção por HIV tem aumentado consideravelmente nos últimos anos (de aproximadamente 14.000 casos notificados em 2012 passou para aproximadamente 43.000 casos em 2017) o seu tratamento é essencial para o bem estar do paciente e evitar o surgimento de novos casos. O tratamento é feito por meio da utilização de antirretrovirais (ARV), sendo eles os Inibidores da Transcriptase Reversa Análogos de Nucleosídeos (ITRN), Inibidores da Transcriptase Reversa Não Análogos de Nucleosídeos (ITRNN), Inibidores de Protease (IP), Inibidores de Protease com Reforço de Ritonavir (IP/r) e Inibidor de Integrase (INI) (MINISTÉRIO DA SAÚDE, 2018).
Para Silva et al., (2014) “A partir de 1996, com a introdução dos antirretrovirais (ARV), os portadores de HIV/ Aids passam a conviver com uma doença crônica, que não tem cura, mas tem tratamento”. Essa introdução dos ARVs ajudou na redução da morbi- mortalidade e aumento da expectativa de vida de pessoas vivendo com o HIV (PVHIV) (SILVA et al, 2014).
A recomendação de inicio precoce da TARV considera, além dos claros benefícios relacionados a redução da morbimortalidade em PVHIV, a diminuição da transmissão da infecção, o impacto na redução da tuberculose – a qual constitui principal causa infecciosa de óbitos em PVHIV no Brasil e no mundo – e a disponibilidade de opções terapêuticas mais cômodas e bem toleradas. (MINISTERIO DA SAUDE, 2018)
O protocolo para o inicio do tratamento do HIV é feito a partir da combinação de ARVs, sendo, atualmente, “dois ITRN/ITRNt associados a uma outra classe de antirretrovirais (ITRNN, IP/r ou INI)” (MINISTERIO DA SAUDE, 2018). No Brasil, a medicação utilizada segue um esquema (Quadro 4) para TARV inicial preferencial disposto no Protocolo Clinico e Diretrizes Terapêuticas (PCDT). A primeira linha de tratamento para adultos é a utilização combinada de tenofovir 300mg e lamivudina 300mg (em co- formulação) associado à dolutegavir 50mg sendo administrados 1 vez ao dia. Nos casos de co-infecção que não tenham critérios de gravidade, a recomendação é a utilização de tenofovir 300mg juntamente com lamivudina 300mg e efavirenz 600mg 1 vez ao dia. Já pacientes co- infectados com critérios de gravidade (como baixa contagem de células CD4, internados ou que possuam alguma outra doença oportunista) a indicação é a utilização de tenofovir 300mg e lamivudina 300mg associados à raltegravir 400mg 1 vez ao dia.
Quadro 4. Esquema de TARV inicial para adultos. TDF= tenofovir; 3TC= lamivudina; DTG= dolutegravir; EFV= efavirenz; RAL= raltegravir; DFC= dose fixa combinada.
Situação Terapia Antirretroviral Dose Diária Adultos em inicio de tratamento TDF/3TC + DTG (300mg/300mg) ”2×1” + 50mg 1x/dia Co-infecção HIV/Tb sem critérios de gravidade TDF/3TC/EFV (300mg/300mg/600mg) -DFC 1x/dia Co-infecção HIV/Tb com um ou mais critérios de gravidade abaixo citados: LT-CD4+ <100 células/mm³ Presença de outra infecção oportunista Necessidade de internação hospitalar/doença grave Tuberculose disseminada TDF/3TC + RAL (300mg/300mg) “2×1” 1x/dia + 400mg 12/12h
Fonte: DIAHV/SVS/MS, apud, Ministério da Saúde, 2018¹ (Adaptado)
Em alguns casos especiais, são utilizados tratamentos de forma alternativa (Quadro 5). Pacientes que possuem intolerância ao dolutegravir podem fazer o uso de efavirenz em seu lugar. Caso haja contra-indicação ao uso de tenofovir, é recomendado o uso de abacavir desde que o paciente apresente resultado negativo a presença do antígeno HLA-B*5701. Nos pacientes co-infectados por HIV/Tuberculose e que tenham intolerância ao uso de tenofovir e abacavir, deve-se substituir por zidovudina caso o teste para a presença do antígeno HLA- B*5701 dê positivo.
Quadro 5. Recomendação de TARV inicial para adultos. ABC= abacavir; AZT= zidovudina; HLA-B*5701= antígeno leucocitário humano responsável por sensibilidade ao abacavir.
Intolerância ou contra-indicação ao DTG Substituir o DTG por EFV Contraindicação ao TDF Substituir o TDF por ABC caso teste HLA- B*5701 der resultado negativo Intolerância ao EFV na co-infecção HIV/Tb Substituir o TDF por AZT caso teste HLA- B*5701 der resultado positivo ou paciente ter intolerância ao ABC
Fonte: DIAHV/SVS/MS, apud, Ministério da Saúde, 2018¹ (Adaptado)
O Brasil conta com diversas leis (nacionais e regionais) em defesa dos portadores do vírus HIV, dentre elas a Declaração dos Direitos Fundamentais da Pessoa Portadora do Vírus da AIDS instituída em 1989 (UNAIDS, 2017). Destaca-se a Lei nº 12.984, de 2 de junho de 2014 que “Define o crime de discriminação dos portadores do vírus da imunodeficiência humana (HIV) e doentes de AIDS”.
No setor regional, alguns estados como Goiás, Minas Gerais, Espírito Santo e Rio de Janeiro possuem penalizações em casos de discriminação a PVHIV (Pessoas vivendo com HIV) datados anteriormente a publicação da legislação em âmbito nacional (UNAIDS, 2017). Além das leis antidiscriminação, PVHIV possuem proteções garantidas em lei no ambiente de trabalho, previdência social, transporte e tratamento. São assegurados a PVHIV o auxilio doença e aposentadoria por invalidez de acordo com a Instrução Normativa INSS/PRES nº 45, de 06 de agosto de 2010, isenção do imposto de renda de acordo com o Art. 6º, XIV, da Lei nº 7.713, de 22 de dezembro de 1988 e tratamento de acordo com a Lei nº 9.313, de 13 de novembro de 1996 (UNAIDS, 2017).
O Ministério da Saúde (2018) disponibilizou uma atualização do Protocolo Clínico e Diretrizes Terapêuticas Manejo da Infecção pelo HIV em Adultos (PCDT) que “… tem por principal objetivo oferecer recomendações atualizadas para prevenção da transmissão, tratamento da infecção e melhoria da qualidade de vida das pessoas vivendo com HIV (PVHIV)”. Com a inclusão do PCDT, houve uma padronização de diagnóstico e terapia para o HIV além de maior acesso a informação. Não somente para adultos, são viabilizados diversos protocolos clínicos com constantes atualizações para crianças e adolescentes, profilaxia pré-exposição (PReP), gestantes dentre outras. (MINISTÉRIO DA SAÚDE, 2018).
Capítulo 2 – Tuberculose
A tuberculose é uma doença antiga, que foi descoberta por um biologista chamado Robert koch, o descobrimento foi feito no ano de 1882, porém, também houveram achados de ossos pré-históricos humanos na Alemanha e registros que foram datados há 8000 Antes de Cristo que diziam a respeito da sintomatologia da doença. Como a tuberculose era uma doença desconhecida pelos povos, se tinha a crença de que quem estava infectado foi castigado, mas Hipocrates desmistificou a crença da população mostrando que a tuberculose era uma doença natural, em XXX Antes de Cristo, na Grécia (MINISTÉRIO DA SAÚDE, 2015).
A tuberculose começou ser entendida nos séculos XXII e XVIII , quando houve o surgimento da anatomia, assim recebeu o nome que se tem hoje. No Brasil, em 1920, houve a reforma de Carlos Chagas, onde se deu origem ao Departamento Nacional de Saúde Pública e com isto o estado começou a estar presente no combate a tuberculose, tendo então a criação da Inspetoria de Profilaxia da Tuberculose. Na década seguinte (1930) surgiram alguns avanços relacionados ao combate da patologia, como a invenção da vacina BCG, da baciloscopia, abreugrafia, do pneumotórax e de algumas outras cirurgias torácicas. Na década de 1940 foi feita a descoberta da quimioterapia antibiótica, tendo comprovação da eficácia durante as décadas de 1950 e 1960, após esta descoberta o tratamento passou a ser ambulatorial e deixou de ser feito sem internações, assim dando fim aos sanatórios. Na década de 1990 achava-se que a doença tivesse sido controlada, mas então se começou a observar o grande crescimento da infecção de tuberculose associada aos casos de paciente infectados pelo vírus da imunodeficiência humana (MINISTÉRIO DA SAÚDE, 2015).
A tuberculose é uma patologia causada pelo Mycobacterium tuberculosis, ou também conhecido como bacilo de koch, é uma doença grave, mas que tem cura. A transmissão da tuberculose ocorre através da inalação de aerossóis que são eliminados dos pacientes contaminados pela patologia, esses aerossóis são eliminados através da fala, de espirros e também da tosse. A tuberculose possui a forma pulmonar e também a forma extrapulmonar, que esta relacionada a outros órgãos do corpo (MINISTÉRIO DA SAÚDE, 2018).
De acordo com Ministério da Saúde (2011), a tuberculose pulmonar pode ser apresentada de três formas: a primária, pós primaria ou secundaria e miliar. A forma primaria normalmente é a que mais acomete a população, é mais comumente ocorrer em crianças. Têm-se como sintomas: febre baixa, irritabilidade e sudorese noturna. A forma pós-primária pode acometer a população em qualquer idade, mas ocorrem comumente em adulto jovem e adolescente e os principais sintomas são: tosse produtiva ou seca, febre vespertina, expectoração com sangue ou não, sudorese noturna, anorexia. Nos locais que se tem uma alta taxa de tuberculose, qualquer paciente que chegue à unidade de saúde reclamando de tosse deve ser investigado para o diagnóstico ou exclusão da tuberculose. A forma miliar é a forma mais grave da tuberculose, esta forma ocorre em 10% dos pacientes soropositivos, que estão na fase de imunossupressão, a tuberculose miliar é mais comum em pacientes jovens adultos e em crianças; os principais sintomas são: febre, emagrecimento, perda da força física, tosse, no exame físico pode se encontrar hepatomegalia, podem ocorrer algumas alterações no sistema nervoso central e também alterações cutâneas. As formas extrapulmonares da tuberculose podem ocorrer em vários órgãos do corpo humano, os seus sintomas e sinais vão variar de acordo com o órgão afetado. Normalmente os pacientes que tem a forma extrapulmonar são as pessoas com o vírus da imunodeficiência humana (HIV) ou pacientes com imunossupressão.
As principais formas de tuberculose extrapulmonar diagnosticadas no Brasil são a pleural, ganglionar e meningoencefálica. A tuberculose pleural acomete a população jovem e os sintomas mais comuns são o emagrecimento, febre, tosse seca. Ela pode se apresentar parecida com a pneumonia bacteriana aguda. Para diagnostico se faz o exame histopatológico do fragmento pleural e também é feito a baciloscopia, e cultura do liquido pleural. Tuberculose ganglionar periférica é a forma que mais acomete a população que é soropositiva, mas também acomete pessoas com idade abaixo aos quarenta anos e crianças.
Os sinais e sintomas são: aumento assimétrico das cadeias granglionares cervical anterior e posterior, que é indolor e assimétrico, em pacientes com o HIV o aumento ganglionar pode ocorrer bilateralmente, quando feito o exame físico, os gânglios podem estar amolecidos ou endurecidos. Para diagnóstico é feito o aspirado do liquido, biopsia do gânglio, podem ser feitos exames histopatológicos e bacteriológicos também (MINISTÉRIO DA SAÚDE, 2011). A tuberculose meningoencefálica é mais comum é pacientes HIV positivos do que nos pacientes que não são infectados pelo vírus da imunodeficiência humana, a meningite basal exsudativa é mais comum em crianças com idade inferior aos seis anos, ela pode se subaguda ou crônica. Os sintomas variam da forma subaguda pra a crônica, na subaguda pode correr cefaléia holocraniana, vômitos, anorexia, alterações de comportamento, febre com associação a dor abdominal, rigidez na nuca que pode ocorrer por volta de duas semanas ou mais. Na forma crônica, o paciente pode sentir cefaleia durante semanas, podem ocorrer pares cranianos, assim podendo ser diagnosticado como meningite crônica, podem se formar tuberculomas, muitas vezes a febre não é presente nestes casos. Outra forma extra pulmonar é a tuberculose pericárdica e ela se apresenta normalmente na forma subaguda tendo como
principais sintomas: dor torácica, tosse seca e dispneia, mas também pode ocorrer emagrecimento, tonteira, edema nos membros inferiores, febre, dor no hipocôndrio e também o aumento do volume abdominal. Tuberculose óssea ocorre normalmente em crianças ou em pessoas com quarenta a cinquenta anos, esta forma atinge comumente as articulações coxofemorais e articulações dos joelhos e principalmente a coluna vertebral, mas também podem acometer outros ossos do corpo. A tuberculose de coluna causa dores na lombar e dor quando se é apalpado e sudorese noturna, ela acomete a coluna torácica, baixa e a lombar (MINISTÉRIO DA SAÚDE, 2011).
Apesar de ter cura, a tuberculose ainda é considerada um problema de saúde pública, e mesmo sendo menos comum hoje do que há alguns anos atrás (de 71.755 pessoas infectadas em 2012, caiu para 70.086 em 2016 de acordo com o SINAN), a doença ainda é preocupante para a saúde publica, pois é uma patologia transmissível. A tuberculose pode estar ligada ou não as condições de vida do paciente, como por exemplo: pacientes com baixa qualidade de vida, pobreza, moradores de rua, pessoas privadas da liberdade, má distribuição de renda e também pacientes contaminados pelo vírus da imunodeficiência humana tem mais chances de se contaminar com a tuberculose (MAGNABOSCO et al.,2016).
Segundo Seiscento (2012) em alguns ambientes como domiciliar e em locais de serviço a saúde devem obter medidas preventivas para a não transmissão da tuberculose, tais como eles: triagem de casos, a separação dos casos que são infectantes dos casos não infectantes, a investigação na unidade de saúde de pacientes com tosse, evitar a internação prolongada de pacientes infectados pelo HIV. Mas também é necessário ter cuidados ambientais, e com materiais de proteção individual como: uso de mascaras pelos pacientes que estão infectados nas unidades de saúde, o cuidado com a ventilação do local onde se encontram os pacientes.
De acordo com o Ministério da Saúde, (2018) o sistema único de saúde (SUS) fornece o tratamento da tuberculose. Este tratamento tem o tempo mínimo de seis meses, e é um tratamento que tem a preferência de tratamento diretamente observado (TDO). O tratamento diretamente observado tem a função de aproximar o paciente do profissional de saúde, assim ajudando o paciente na adesão correta do tratamento. O paciente deve ser sempre orientado sobre o tratamento da tuberculose e sobre os efeitos adversos que ele pode ter, o paciente deve ser orientado sobre os benefícios do tratamento e o uso regular da medicação. “São utilizados quatro fármacos para o tratamento dos casos de tuberculose que utilizam o esquema básico: rifampicina, isoniazida, pirazinamida e etambutol” (MINISTÉRIO DA SAÚDE, 2018).
O paciente deve ser aconselhado pelos profissionais da saúde a não interromper o tratamento, mesmo que nas primeiras semanas tenham alguma melhora, o tratamento deve ser feito no mínimo seis meses e só deve ser interrompido pelo medico, o profissional deve informar ao paciente q a desistência do tratamento ira piorar a sua condição de saúde e deixara a tuberculose resistente ao tratamento (MINISTERIO DA SAUDE, 2018).
Capítulo 3: Co-infecção HIV/Tuberculose
Segundo Gaspar et al., (2016) “A presença do HIV alerta para a transformação da tuberculose de uma doença endêmica para epidêmica.” Pacientes HIV positivos tem um risco maior de contrair a tuberculose do que as pessoas que são HIV negativas. A tuberculose tem um grande índice de mortalidade em pacientes infectados com o HIV (aproximadamente 65% dos óbitos por HIV tem a tuberculose como causa básica), isso representa um desafio grande para o controle mundial da tuberculose. A chance de um paciente HIV positivo contrair a tuberculose é muito grande, pois os pacientes com o vírus da imunodeficiência humana são normalmente imunologicamente deficientes (LEMOS ET AL., 2016).
Em 2011, entre os casos de TB notificados no SINAN (71 mil), cerca de 10% apresentavam coinfecção TB/HIV, sendo 6% a taxa de letalidade relacionada à sobreposição de ambas infecções. (MAGNABOSCO et al., 2016)
Melo, Donalísio e Cordeiro (2017) constataram em sua pesquisa que pacientes co- infectados por tuberculose e HIV possuem uma sobrevida muito menor em relação aos não co-infectados, girando em torno de aproximadamente 60 meses de sobrevida. Por essa razão, pacientes que são HIV positivos devem passar por um rastreio para saber se estão contaminados com tuberculose. Nesse sentido, o sistema público de saúde oferece um guia básico que é classificado com: por que, quando, onde e como fazer o rastreio. O guia possui a divisão do diagnostico da tuberculose ativa em PVHIV que expõe o quanto é importante o diagnostico da tuberculose e o inicio rápido do tratamento (SEE-SP, 2017).
Para todos os pacientes que são HIV positivos deve-se sempre se atentar sobre a manifestação dos seguintes sinais e sintomas: febre, tosse, perda de peso e sudorese noturna, pois são sintomas típicos da tuberculose. O paciente soro positivo deve ser acompanhado pelas unidades de saúde e a atenção a esses sintomas deve acontecer em todas as visitas ou consultas, caso haja presença destes sintomas, o mesmo deve ser encaminhado para atendimento médico a fim de avaliação (SEE-SP, 2017).
Mesmo tendo a tosse constante como principal indicativo de tuberculose, Damásio et al., (2016) destaca “…a necessidade dos profissionais de saúde atentarem para o rastreamento
de formas não pulmonares da tuberculose, que também são preditores de mau prognóstico e necessitam de tratamento oportuno.”
Quando se inicia uma consulta e há suspeita de tuberculose é preciso solicitar alguns exames específicos para o diagnostico, dentre eles: raio-x do tórax, teste rápido de detecção da doença, baciloscopia, cultura para micobacteria, ultrassonografia e/ou tomografia computadorizada.
O rendimento da baciloscopia direta de escarro pode ser inferior à apresentada por pacientes não infectados pelo HIV, principalmente em pacientes imunossuprimidos, nos quais a presença de cavidades pulmonares pode ser menos observada. Preconiza-se a realização de cultura e a identificação da micobactéria em pacientes infectados pelo HIV com o objetivo de aumentar a chance de confirmação do diagnóstico e a realização de testes de sensibilidade às drogas. (SEISCENTOS, 2012)
Quanto há infecção latente da tuberculose em pessoas que vivem com HIV o tratamento é importante, pois diminui o risco de tuberculose ativa. Nos novos casos de co- infecção registrados em 2016 no SINAN, 49,1% dos pacientes que iniciaram o tratamento precocemente se curaram da tuberculose.
Todos os pacientes que são portadores do HIV devem ser investigados nas consultas ou visitas a unidades de saúde realizando os seguintes exames para o diagnostico: o raio x de tórax, prova tuberculínica (PPD), contagem de CD4 (SEE-SP, 2017). De acordo com Santos et al., (2017) a prova tuberculínica (PT) é utilizada para o diagnostico de infecção latente por tuberculose em pessoas que vivem com HIV/AIDS.
A PT utilizada para o diagnóstico de ILTB deve ser analisada de forma criteriosa nos indivíduos infectados pelo HIV. Quando resultado positivo, investigar TB doença e, quando negativo, avaliar o número de linfócitos TCD4+ e a possibilidade de alergia cutânea. Nestes casos, há a recomendação de repetir o teste após a reconstituição imune e, em se mantendo negativo, repeti-lo anualmente. (MONTEIRO et al., 2015)
Não somente devem-se realizar exames para tuberculose em pacientes portadores de HIV quanto é de suma importância a realização de testagem para HIV em pacientes infectados com tuberculose. Os dados do SINAN mostram que no ano de 2016, dos pacientes infectados por tuberculose no Brasil, foram solicitados testagem para HIV de 81,8% deles. Destes, 76,3% foram realizados e 9,4% obtiveram resultado positivo para a co-infecção. Assim, fica evidente que em ambos os casos (tuberculose e HIV) são necessários testes para triagem de co-infecção.
É de extrema importância que o paciente tenha uma boa adesão ao tratamento tanto da tuberculose quando do HIV/AIDS, pois o tratamento irá controlar as infecções. O tratamento do HIV é ininterrupto, pois a doença ainda não tem cura, mas pode ser controlada; já o tratamento da tuberculose pode variar de seis a nove meses dependendo do tipo de tuberculose que o paciente possui (LEMOS et al, 2016). Porém, os dados apontam que grande parte dos co-infectados não estão em uso dos TARVs. Só em 2016, dos 6.501 casos notificados no SINAN apenas 2.717 faziam uso da medicação.
A SEE-SP, (2017) instrui que o tratamento de infecção latente da tuberculose deve ser feito com isoniazida de 10mg/hg no dia, com a dosagem de no máximo 300mg ao dia, o tratamento vai durar de 6 a 9 meses. Para o tratamento de tuberculose ativa o tratamento é mais intenso. “Para pacientes em uso de antirretrovirais no momento do diagnóstico da TB, a TARV não deve ser interrompida, e sim apenas ajustada, quando necessário.”
Idealmente, o tratamento da TB deve ser feito com esquema básico, utilizando-se os comprimidos combinados de rifampicina, isoniazida, pirazinamida e etambutol (RHZE). Observar sempre ajuste da dose conforme peso do paciente. (SEE-SP, 2017).
Há a possibilidade de efeitos adversos e também de interação medicamentosa, o que pode favorecer o sofrimento do paciente, bem como a desistência ao tratamento (MIRANDA, 2012). No ano de 2016, dos novos casos de tuberculose registrados no SINAN, 13,9% abandonaram o tratamento. Já para pacientes que estavam em retratamento esse percentual aumentou para 31,5%, o que alerta para que os profissionais de saúde tenham uma maior atenção com esses pacientes.
Capítulo 4: Intervenções Farmacêuticas e a adesão ao tratamento da Co-Infecção HIV/Tb
De acordo com Filho et al., (2012) os pacientes que são co-infectados pelo vírus da imunodeficiência humana e a tuberculose têm vários motivos para não adesão do tratamento. “As doenças TB e HIV são historicamente estigmatizadas e o impacto negativo gera conseqüências drásticas de abandono do tratamento e elevadas taxas de mortalidade” (RODRIGUES et al., 2012). Alguns pacientes têm dificuldade para tomar as medicações na hora certa e às vezes confundem um medicamento com outro, outros pacientes deixam de fazer o uso da medicação por causa dos efeitos colaterais, mas também tem aqueles pacientes que não usam a medicação por estar consumindo bebida alcoólica ou ate mesmo utilizando drogas ilícitas. A não adesão do tratamento acarreta a resistência das patologias, assim dificultando o tratamento quando o paciente volta à unidade de saúde (FILHO et al., 2012).
As dificuldades que influenciam a não-adesão e o abandono do tratamento de TB em pessoas vivendo com HIV/AIDS incluem o baixo nível educacional e socioeconômico, os hábitos de vida prejudiciais à saúde, a falta de recursos para alimentação e locomoção, o uso de álcool e outras drogas, a história de não-adesão anterior, os efeitos adversos da medicação, a não-aceitação do diagnóstico, a melhora dos sintomas e a ausência de conhecimento sobre a evolução clínica e importância do tratamento. (FILHO et al., 2012)
Conviver com as duas doenças é um processo difícil e alguns fatores são importantes para uma melhor adesão ao tratamento. Silva et al., (2014) constatou em sua pesquisa a influência de fatores sociais no agravo dessa comorbidade, como a pobreza, dificuldades em relação a família e principalmente a discriminação por parte da sociedade.
Silva et al., (2014) destaca o quão imprescindível é o apoio da família durante o tratamento, sendo considerada um ambiente seguro para preservação da identidade. Além do apoio familiar, a religiosidade tem grande influência no estimulo a não desistência do tratamento e busca por uma melhor qualidade de vida, pois, a fé da pessoa lhe dá esperança pra suportar as adversidades.
Os profissionais da saúde têm um papel fundamental no acompanhamento de pacientes conviventes com co-infecção HIV/Tb. Dentre eles, pode-se destacar o profissional Farmacêutico que, dentro de suas atribuições e leis vigentes, pode executar determinadas tarefas capazes de auxiliar no rastreio e numa melhor adesão ao tratamento da co-infecção HIV/Tb.
De acordo com a Resolução Nº 585 de 29 de agosto de 2013 do Conselho Federal de Farmácia (CFF), que regulamenta as atribuições clínicas do farmacêutico, o mesmo “…tem o dever de contribuir para a geração, difusão e aplicação de novos conhecimentos que promovam a saúde e o bem-estar do paciente, da família e da comunidade.”
Dentre as atribuições exercidas pelo farmacêutico que podem intervir nos cuidados aos pacientes portadores de co-infecção HIV/Tb, destacam-se o Acompanhamento Farmacoterapêutico, Educação em Saúde, Dispensação, Revisão de Farmacoterapia e o Rastreamento em Saúde. As intervenções são preconizadas pelo CFF com a finalidade de garantir, não só ao paciente, mas também a família e sociedade em geral, uma saúde de qualidade (CONSELHO FEDERAL DE FARMÁCIA, 2013).
O passo inicial nos cuidados a saúde é a prevenção da co-infecção. O profissional farmacêutico deve estar inserido em programas que orientem a população quanto a métodos de profilaxia a patologias. O Conselho Federal de Farmácia, (2013) destaca a importância de orientar quanto a mudanças nos hábitos de vida, informações sobre as doenças e fatores de risco. Em pacientes saudáveis é necessário precaver que haja contração de HIV, pois assim os riscos de uma co-infecção são reduzidos. Neste caso, o farmacêutico deve conscientizar a população sobre os métodos de prevenção existentes para o HIV, como o uso de preservativos e, em casos especiais, o uso de Profilaxia Pré-Exposição (PrEP) e Profilaxia Pós-Exposição (PEP). A PrEP consiste no uso de ARVs antes de se expor a uma situação considerada de risco para contração de HIV. Já a PEP é o uso de ARVs após exposição a uma situação de risco (MINISTÉRIO DA SAÚDE, 2018).
Tanto a PrEP quanto a PEP são fornecidas de forma gratuita pelo SUS desde que os pacientes se enquadrem nas populações consideradas de risco, como por exemplos “gays ou outros homens que fazem sexo com homens (HSH); pessoas trans e trabalhadores(as) do sexo” (MINISTÉRIO DA SAÚDE, 2018). Além dessa população, outras situações especiais têm direito ao uso profilático dos ARVs como, por exemplo, pessoas que freqüentemente não fazem uso de preservativo em suas relações tanto vaginais quanto anais; se expôs a uma relação desprotegida com paciente portador do vírus HIV que não está em tratamento ou quem apresenta repetidamente quadros de IST’s (Infecções sexualmente transmissíveis) (MINISTÉRIO DA SAÚDE, 2018).
Se tratando da tuberculose, a primeira linha de prevenção é a vacinação.
A vacina BCG (Bacilo Calmette-Guérin) é utilizada desde a década de 1920 como medida preventiva complementar no controle da tuberculose. A vacina previne especialmente as formas graves da doença, como TB miliar e meníngea na criança. É uma das mais utilizadas em todo mundo e sua incorporação nos programas de imunização teve impacto na redução da mortalidade infantil por TB em países endêmicos. (MINISTÉRIO DA SAÚDE, 2019)
Segundo a SEE-SP (2017), a tuberculose está relacionada às condições de vida da população, seja por viver em situações de pobreza, casas mal-ventiladas ou muitas pessoas compartilhando o mesmo quarto. Devido a isso, melhorar as condições de vida das pessoas é uma forma de prevenção, além do uso de quimioprofilaxia (SEE-SP, 2017).
A quimioprofilaxia é a administração de medicamento para tuberculose por um determinado período de tempo em pacientes que são considerados de risco para contração da doença, como por exemplo, recém-nascidos que freqüentam ambiente foco do bacilo; menores de 15 anos que não receberam vacina BCG e que vivem em foco contaminante; população indígena exposta a risco de contaminação e imunodeprimidos (MINISTÉRIO DA SAÚDE, 2004).
O rastreamento em saúde é o segundo passo nos cuidados ao paciente, pois se trata da “…identificação de indivíduos com doenças que ainda não foram diagnosticadas” (CONSELHO FEDERAL DE FARMACIA, 2013). Deste modo, pacientes que apresentem sintomas que caracterizem HIV ou tuberculose são encaminhados para exames complementares e avaliação.
A partir da identificação do problema de saúde, o farmacêutico pode agir monitorando o tratamento do paciente por meio da dispensação (repassando informações importantes sobre as medicações garantindo uma utilização segura), revisão de farmacoterapia (avaliando a prescrição a fim de aperfeiçoar a adesão das medicações), educação em saúde (orientando o paciente quanto ao seu estado de saúde para que o mesmo tenha autonomia com o controle da enfermidade) e o acompanhamento farmacoterapêutico (serviço pelo qual o farmacêutico acompanha de perto o tratamento, avaliando a efetividade das medicações e a evolução do quadro clínico) (CONSELHO FEDERAL DE FARMACIA, 2013).
O farmacêutico não tem somente o papel de fornecer o medicamento prescrito, mas também tem a função de acolher o paciente e atender suas dúvidas (CONSELHO FEDERAL DE FARMÁCIA, 2017). Seu papel na adesão do tratamento da co-infecção HIV/Tb é de extrema importância, pois é uma patologia com tratamento complexo e com uma maior quantidade de medicamentos, além do maior número de reações adversas e interações medicamentosas (Quadro 6).
Dentre as reações adversas mais comuns, se destacam a diarréia, náuseas, vômitos, tontura e dor abdominal. Alguns medicamentos como a isoniazida e a pirazinamida têm como reação comum a capacidade de causar danos hepáticos, o que acarreta num grande desafio para o tratamento.
Quadro 6: Efeitos adversos dos medicamentos utilizados para tratamento de HIV e Tuberculose.
Fármaco Efeitos Adversos Rifampicina Comuns: diarréia, náuseas, vômito, urina com a cor marrom ou avermelhada. Raras: rubor facial, erupção cutânea, insuficiência hepática, hemorragias gengivais, febre, pancreatite, tontura, cefaléia, calafrios, tremores, respiração ofegante, dores musculares. Isoniazida Comuns: náuseas, dor no estomago, febre, erupção cutânea púrpura, vômitos e neuropatia periférica e hepatite (comumente em pessoas acima de 35 anos) Raras: descordenação motora, contração muscular, convulsões, dor epigástrica. Pirazinamida Comuns: vômitos, mal estar, anorexia e lesão hepática grave. Raras: astralgia, urticária e aumento do acido úrico. Etambutol Comuns: vômito, dor abdominal, anorexia, náuseas. Raras: ataxia, dificuldade de concentração, tontura. Abacavir (ziagenavir) Comuns: dores de cabeça, vômito, náuseas, anorexia, letargia ou fadiga, erupção cutânea, Raras: eritema multiforme, pancreatite e acidose lática. Zidovudina Comuns: insônia, cefaléia intensa e náuseas. Raras: dispnéia, tremores, rinite, hemorragia nasal,sinusite, faringite. Efavirenz Comuns: náuseas, diarréia. Raras: coordenação anormal, vertigem, confusão, reações alérgicas. Raltegravir Comuns: náuseas, diarréia, astenia, fadiga, tontura. Raras: dor abdominal, gastrite, boca seca, flatulência, insônia, ansiedade. Lamivudina Comuns: dores de cabeça, náuseas, dor abdominal, distúrbios musculares, febre, fadiga, alopecia. Raras: pancreatite, acidose lática, aumento de amilase sérica. Dolutegravir (tivicay) Comuns: cefaléia, náuseas, diarréia, tontura, ansiedade, vomito, desconforto abdominal, prurido, fadiga Raras: hipersensibilidade, síndrome de reconstituição imune, hepatite. Tenofovir Comuns: tonturas, diarréia, náuseas, erupção cutânea Raras: febre, dor nas costas, flatulência.
Fonte: ANVISA (Agência Nacional de Vigilância Sanitária)
Ter um bom relacionamento com os pacientes e falar de forma clara e simples para o entendimento da forma correta do uso da medicação e das posologias certas evitando erros no tratamento, é essencial. O paciente precisa confiar no profissional para que a comunicação seja mais tranqüila. Transmitir conhecimento para o paciente sobre os malefícios do abandono do tratamento ajuda no processo de adesão (MINISTÉRIO DA SAÚDE, 2010).
A promoção a saúde auxilia o paciente no tratamento e o profissional deve influenciar no correto uso da medicação, ajudando na posologia, nas possíveis causas de toxicidade, organizando os medicamentos nos horários corretos e ajudando na identificação das medicações para que não ocorra troca dos comprimidos. O farmacêutico deve monitorar a frequência do paciente na busca das medicações e caso ele falhe o farmacêutico deve procura o paciente para que a medicação seja entregue e usada (MINISTÉRIO DA SAÚDE, 2010).
5. CONCLUSÃO
Os resultados apresentados no presente estudo demonstram o HIV é um vírus com alta capacidade de trazer danos consideráveis ao portador por se tratar de um imunodepressor. Quando não tratado, o paciente fica susceptível a doenças oportunistas, destacando-se a tuberculose.
Mesmo se tratando de uma doença que possui cura, a tuberculose juntamente com o HIV é um grande problema de saúde publica. Os fatores associados à infecção por tuberculose estão relacionados a alta taxa de desemprego, distribuição desigual de renda e aglomerados populacionais.
A co-infecção HIV/TB possui um alto índice de cura da tuberculose nos novos casos, porém, em retratamentos, os índices de abandono são extremamente altos. A baixa adesão ao tratamento se dá tanto por fatores sociais e econômicos quanto por fatores associados ao próprio tratamento. A grande quantidade de medicamentos e os efeitos colaterais dos mesmos estão diretamente ligados a desistência do tratamento. Mesmo o tratamento sendo distribuído de forma gratuita, as condições de vida do paciente também influenciam na adesão do tratamento, como por exemplo, a dificuldade de locomoção do paciente para unidade de saúde (levando em consideração que nem todos tem fácil acesso a transporte). Os fatores sociais ligados a não adesão do tratamento incluem o a má convivência com a família e principalmente o preconceito (que leva a pessoa a não buscar aconselhamento médico e assim evitando o diagnóstico precoce).
O farmacêutico, como profissional de saúde, tem papel fundamental no rastreio e acompanhamento de pacientes co-infectados por HIV/TB. Participar de campanhas de prevenção a IST’s e tuberculose é uma das primeiras iniciativas no processo de cuidado a saúde. O projeto de educação em saúde sexual por meio da distribuição de preservativos, conscientização quanto ao uso de PrEP e PEP e aconselhamento quanto a realização periódica de exames diminuem as chances de infecção por HIV. Quanto à tuberculose, incentivar a vacinação (vacina BCG) e orientar quanto à existência de quimioprofilaxia, os cuidados em casa e evitar grandes aglomerações.
Por se tratar do profissional dos medicamentos, o farmacêutico deve estar atento aos pacientes em tratamento. Ter um bom relacionamento com o paciente e levar informações sobre o tratamento e os efeitos colaterais são de grande importância.
6. REFERÊNCIAS
MIRANDA, Silvana S. Tratamento de tuberculose em casos especiais. Disponível em: < http://pesquisa.bvsalud.org/brasil/resource/pt/lil-661992>. Acesso em:20/04/2019.
FILHO, Manoel Pereira de Souza et. al. Pacientes vivendo com HIV/AIDS e coinfecção tuberculose: dificuldades associadas á adesão ou abando do tratamento. Disponível em:<http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1983- 14472012000200020&lang=en>. Acesso em: 20/04/2019.
DAMASIO, Gabriela Souza et. al. Fatores sociais, clínicos e de adesão em coinfectados por HIV/Tuberculose: estudo descritivo. Disponível em:<http://pesquisa.bvsalud.org/brasil/resource/pt/biblio-967863>. Acesso em: 21/04/2019.
MAGNABOSCO, Gabriela Tavares et. al. Controle da Tuberculose em pessoas vivendo com HIV/Aids. Disponível em: <http://pesquisa.bvsalud.org/brasil/resource/pt/biblio- 960918>. Acesso em 21/04/2019.
MELO, Marcio Cristiano; DONALISIO, Maria Rita; CORDEIRO, Ricardo Carlos. Sobrevida de pacientes com AIDS e coinfecção pelo bacilo da tuberculose nas regiões Sul e Sudeste do Brasil. Disponível em: <http://pesquisa.bvsalud.org/brasil/resource/pt/biblio- 890185>. Acesso em 21/04/2019.
VIVEIROS, F et.al. Adesão ao rastreio e tratamento da tuberculose em doentes infetados com o vírus da imunodeficiência humana. Disponível em: < https://www.journalpulmonology.org/pt-adesao-ao-rastreio-e-tratamento-articulo- S0873215913000329 > . Acessado em 06/05/2019.
GASPAR, Renato Simões et al. Análise temporal dos casos notificados de tuberculose e de coinfecção tuberculose-HIV na população brasileira no período entre 2002 e 2012. Disponível em: < http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1806- 37132016000600416&lng=en&tlng=en> . Acessado em 06/05/2019.
RODRIGUES, Ana Maria da Silveira et al. Avaliação do acesso ao tratamento de tuberculose por coinfectados ou não pelo vírus da imunodeficiência humana. Disponível em: < http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0080- 62342012000500018&lang=en >. Acessado em 06/05/2019.
MONTEIRO, Ariane Thaise Alve et al. Prova tuberculínica: o controle da tuberculose em pacientes infectados pelo vírus da imunodeficiência humana (HIV). Disponível em: < http://pesquisa.bvsalud.org/brasil/resource/pt/lil-770851>. Acessado em 06/05/2019.
SEISCENTOS, Márcia. Tuberculose em Situações Especiais: HIV, Diabetes Mellitus e Insuficiência Renal. Disponível em: < http://pesquisa.bvsalud.org/brasil/resource/pt/lil- 662002>>. Acessado em 08/05/2019.
LEMOS, Larissa de Araújo et al. Adesão aos antirretrovirais em pessoas com coinfecção pelo vírus da imunodeficiência humana e tuberculose. Disponível em: < http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0104- 11692016000100324&lang=pt> . Acessado em 08/05/2019.
SANTOS, Danielle Talita dos et al. Infecção latente por tuberculose entre pessoas com HIV/AIDS, fatores associados e progressão para doença ativa em município no Sul do Brasil. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0102- 311X2017000805008&lang=pt>. Acessado em 06/05/2019.
SILVA, Jacqueline Barbosa et al. Os significados da comorbidade para os pacientes vivendo com TB/HIV: repercussões no tratamento. Disponível em: < http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0103- 73312015000100209&lang=pt> . Acessado em 06/05/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Boletim Epidemiológico – Aids e DST Jul. 2015/Jun. 2016. Brasília, Ano V- Nº 01, edição 2016. Disponível em: < http://www.aids.gov.br/pt-br/pub/2016/boletim-epidemiologico-de-aids-2016>. Acessado em: 07/07/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Boletim Epidemiologico Coinfecção TB-HIV no Brasil: panorama epidemiológico e atividades colaborativas. Brasília, edição 2017. Disponível em:< http://www.aids.gov.br/pt-br/pub/2017/coinfeccao-tb- hiv-no-brasil-panorama-epidemiologico-e-atividades-colaborativas-2017>. Acessado em: 07/07/2019.
UNAIDS. Legislação brasileira e o HIV. Brasília, edição 2017. Disponível em: < https://unaids.org.br/wp-content/uploads/2015/06/2018_01_18_Legislacao_Br_HIV-1.pdf>.Acessado em: 08/07/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Manual Técnico Para o Diagnóstico da Infecção Pelo HIV. Brasília, edição 2013. Disponível em: < http://bvsms.saude.gov.br/bvs/publicacoes/manual_tecnico_diagnostico_infeccao_hiv.pdf>.Acessado em: 08/07/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Boletim Epidemiológico Implantação do Plano Nacional pelo Fim da Tuberculose como Problema de Saúde Pública no Brasil: primeiros passos rumo ao alcance das metas. Brasília, Volume 49, Nº 11, edição 2018. Disponível em: < https://portalarquivos2.saude.gov.br/images/pdf/2018/marco/26/2018-009.pdf>. Acessado em: 08/07/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Panorama da tuberculose no Brasil: indicadores epidemiológicos e operacionais. Brasília, 1ª edição, 2014. Disponível em:<http://bvsms.saude.gov.br/bvs/publicacoes/panorama%20tuberculose%20brasil_2014.pd f.>. Acessado em: 19/07/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Panorama da tuberculose no Brasil: a mortalidade em números. Brasília, 1ª edição, 2016. Disponível em: <http://bvsms.saude.gov.br/bvs/publicacoes/panorama_tuberculose_brasil_mortalidade.pdf>. Acessado em: 19/07/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Panorama da tuberculose no Brasil. São Paulo, 2018. Disponível em: < http://www.saude.sp.gov.br/resources/cve-centro-de-vigilancia-epidemiologica/areas-de- vigilancia/tuberculose/eventos/tb18_forum_panorama_tb_no_brasil.pdf>. Acessado em: 19/07/2019.
WHO, World Health Organization. Política de la OMS sobre actividades de colaboración TB/VIH: guías para programas nacionales y otros interesados directos. Edição única, 2012. Disponível em: < https://www.who.int/tb/publications/2012/tb_hiv_policy_9789241503006/es/>. Acessado em: 06/05/2019.
BRASIL. Secretaria de Estado da Saúde de São Paulo. Guia Básico para Prevenção, Diagnóstico e Tratamento da Tuberculose em Pessoas Vivendo com HIV. São Paulo, edição única, 2017. Disponível em: <http://www.saude.sp.gov.br/resources/crt/publicacoes/publicacoes- download/guiabasicotbhiv.pdf>. Acessado em: 07/09/2019.
BRASIL. Conselho Federal de Farmácia. Serviços farmacêuticos diretamente destinados ao paciente, à família e à comunidade: contextualização e arcabouço conceitual. Brasília, edição única, 2016. Disponível em: < http://www.cff.org.br/userfiles/Profar_Arcabouco_TELA_FINAL.pdf>. Acessado em: 08/07/2019.
GOODMAN & GILMAN. As Bases Farmacológicas da Terapêutica. Porto Alegre, 12ª edição, p. 1623-1625, ano 2012.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Manual de Recomendações para o Controle da Tuberculose no Brasil. Brasília, 2ª edição atualizada, 2011. Disponível em: < http://bvsms.saude.gov.br/bvs/publicacoes/manual_recomendacoes_controle_tuberculose_bra sil_2_ed.pdf>. Acessado em: 10/09/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Protocolo Clínico e Diretrizes para Profilaxia Pré-Exposição (PrEP) de Risco à Infecção pelo HIV. Brasília, 1ª edição, 2018. Disponível em: < http://www.aids.gov.br/pt-br/pub/2017/protocolo-clinico-e- diretrizes-terapeuticas-para-profilaxia-pre-exposicao-prep-de-risco>. Acessado em: 19/09/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Protocolo Clínico e Diretrizes Terapêuticas HIV/Aids para Manejo da Infecção pelo HIV em Adultos. Brasília, 1ª edição, 2018. Disponível em: < http://www.aids.gov.br/pt-br/pub/2013/protocolo- clinico-e-diretrizes-terapeuticas-para-manejo-da-infeccao-pelo-hiv-em-adultos>. Acessado em: 19/09/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Protocolo Clínico Diretrizes Terapêuticas para Profilaxia Pós-Exposição (PEP) de Risco à Infecção pelo HIV, IST e HV. Brasília, 1ª edição, 2018. Disponível em: <http://www.aids.gov.br/pt- br/pub/2015/protocolo-clinico-e-diretrizes-terapeuticas-para-profilaxia-pos-exposicao-pep-de- risco>. Acessado em: 20/09/2019.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Protocolo de Assistência Farmacêutica em DST/HIV/Aids. Brasília, 1ª edição, 2010. Disponível em: < http://www.aids.gov.br/pt-br/pub/2010/protocolo-de-assistencia-farmaceutica-em-dsthivaids- 2010>. Acessado em: 18/09/2019.
SANTOS, Vitor Gomes et al. Avaliação de IDH e dos quantitativos de incidência de tuberculose e de HIV nos Estados da região norte do Brasil. Disponível em:<http://www.sbmt.org.br/medtrop2016/wpcontent/uploads/2016/12/8274Avaliac%CC%A7a%CC%83o-de-IDH-e-dos-quantitativos-de-incide%CC%82ncia-de-tuberculose-e-de-HIV- nos-Estados-da-regia%CC%83o-norte-do-Brasil.pdf>. Acessado em: 15/10/2019.
PELISSARI, Daniele Maria; QUIJANO, Fredi Alexander Diaz. Household crowding as a potential mediator of socioeconomic determinants of tuberculosis incidence in Brazil.Disponível em: <https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0176116>. Acessado em: 15/10/2019.
1 Farmacêutico Generalista, Faculdade do Futuro, joaovictorcordeirodias10@gmail.com
2 Farmacêutico, Doutor em Saúde Pública, Faculdade do Futuro, herminiofar@gmail.com
