REGISTRO DOI: 10.5281/zenodo.10642208
1Rafael André Ferreira
2Ludmilla Ferreira De Assis
3Reinaldo Reis Pimentel
4Ana Clara Fernandes De Souza
5Pollyanne Nunes Bonfim Gouvêa
6Fabiane De Carvalho Silva
7Fabio Oliveira De Souza
8Geisiane Barbosa De Bastos
9Murillo Monteiro De Oliveira
10Ricardo Viana Velloso
Resumo: A bacitracina, um antibiótico polipeptídico cíclico, destaca-se por sua singularidade quanto aos mecanismos de ação e pelo fato de atuar inibindo a síntese da parede celular bacteriana e a produção de proteínas, apresentando eficácia contra diversas bactérias gram-positivas e alguns gram-negativos. Sua estabilidade é aprimorada pela presença de Zn2+, e seu uso tópico é comum em pomadas para tratar lesões cutâneas leves. O estudo baseia-se em revisões bibliográficas, as quais versam sobre a síntese da bacitracina, seus mecanismos de ação e aplicações clínicas, abordando a evolução histórica do medicamento, desde sua descoberta em 1945 até os dias atuais. A metodologia incluiu buscas em fontes como Scielo, PubMed e Google Acadêmico realizados durante o segundo semestre de 2023. No referencial teórico, são discutidas as fases críticas do desenvolvimento desse medicamentos, destacando a importância da pesquisa pré-clínica, desenvolvimento clínico e revisão regulatória, enfatizando as indicações da bacitracina como pomada, por exemplo, para tratar cortes, arranhões e queimaduras, além de pneumonia e empiema em lactentes. O mecanismo de ação da bacitracina envolve sua absorção pela pele, inibindo a transferência de mucopeptídeos para a parede celular bacteriana e, assim, impedindo a replicação do microrganismo. O medicamento atua também como inibidor de proteases e enzimas envolvidas na função da membrana celular e sua administração ocorre de por via tópica, oftálmica ou intramuscular. Quanto aos efeitos adversos, destaca-se a possibilidade de dermatite de contato alérgica e reações anafiláticas. A bacitracina é classificada como categoria C na gravidez, sendo necessária precaução. Contraindicações incluem hipersensibilidade e cuidados durante a aplicação em infecções virais ou fúngicas. Por fim, o artigo conclui alertando sobre o aumento do uso da bacitracina e seus potenciais efeitos adversos, enfatizando a necessidade de monitoramento cuidadoso, especialmente em casos de administração intramuscular, destacando a importância da conscientização dos profissionais de saúde sobre possíveis reações alérgicas, incentivando a leitura de rótulos por parte dos pacientes.
Palavras-chave: bacitracina, antimicrobianos, antibacterianos, síntese de medicamentos.
Abstract: Bacitracin, a cyclic polypeptide antibiotic, stands out for its uniqueness in mechanisms of action, inhibiting bacterial cell wall synthesis and protein production, demonstrating efficacy against various gram-positive and some gram-negative bacteria. Its stability is enhanced by the presence of Zn2+, and its topical use is common in ointments for treating minor skin injuries. The study is based on literature reviews covering bacitracin synthesis, mechanisms of action, and clinical applications, addressing the historical evolution of the drug from its discovery in 1945 to the present day. The methodology involved searches in sources such as Scielo, PubMed, and Google Scholar conducted during the second semester of 2023. In the theoretical framework, critical phases of drug development are discussed, emphasizing the importance of preclinical research, clinical development, and regulatory review, highlighting bacitracin indications, such as ointment use for treating cuts, scratches, burns, as well as pneumonia and empyema in infants. Bacitracin’s mechanism of action involves skin absorption, inhibiting the transfer of mucopeptides to the bacterial cell wall, thus preventing microbial replication. The drug also acts as a protease inhibitor and affects enzymes involved in membrane function, with administration occurring topically, ophthalmically, or intramuscularly. Regarding adverse effects, attention is drawn to the possibility of allergic contact dermatitis and anaphylactic reactions. Bacitracin is classified as category C in pregnancy, requiring caution. Contraindications include hypersensitivity and application in viral or fungal infections. Lastly, the article concludes by warning about the increasing use of bacitracin and its potential adverse effects, emphasizing the need for careful monitoring, especially in cases of intramuscular administration, and stressing the importance of healthcare professionals’ awareness of possible allergic reactions while encouraging patients to read labels.
Keywords: bacitracin, antimicrobials, antibacterials, drug synthesis.
1 INTRODUÇÃO
A literatura sobre os mecanismos bioquímicos de ação de medicamentos indica que, dos antibióticos em uso clínico, a bacitracina tem características singulares pela demanda de concentrações bacteriostáticas mínimas e por possuir um modo de ação duplo.
Por um lado, em comum com a penicilina e a cicloserina, a bacitracina suprime a síntese das paredes celulares bacterianas. Por exemplo, o medicamento faz com que o Staphylococcus aureus lise (CRAWFORD & ABRAHAM, 1957), forme protoplastos (ABRAHAM, 1957), acumule nucleotídeos de uridina (ABRAHAM & NEWTON, 1958; PARK, 1958, 1960) e seja incapaz de incorporar aminoácidos radioativos em mucopeptídeos de parede celular (PARK, 1958; MANDELSTAM & ROGERS, 1959).
Por outro lado, em associação com o cloranfenicol, a bacitracina impede que o S. aureus sintetize proteínas como β-galactosidase (CREASER, 1955; GALE & FOLKES, 1955) e α-hemolisina (HINTON & ORR, 1960). No entanto, a bacitracina não impede que o S. aureus incorpore lisina radioativa na proteína celular e nem inibe a biossíntese da proteína M por estreptococos (PARK, 1960).
A estabilidade térmica e de armazenamento da bacitracina é aprimorada pela presença de uma concentração equimolar de Zn2+ (GROSS, 1954), e a ação antibacteriana do medicamento é potencializada pela presença desse íon (WEINBERG, 1959).
Além disso, a bacitracina pode ser utilizada como uma pomada antibiótica tópica amplamente utilizada tanto por profissionais de saúde quanto pelo público em geral para tratar lesões cutâneas leves, incluindo cortes, arranhões e queimaduras (WRONG NM et al., 1951). A bacitracina pode ser usada como uma pomada de agente único ou em combinação, como uma pomada de terapia tripla, com polimixina B e neomicina. Esta última pode ser encontrada sem receita médica em farmácias locais. Esta trabalho esboça as indicações, mecanismo de ação, administração segura, efeitos adversos e contraindicações ao usar a bacitracina (SCHALOCK PC, ZUG KA, 2005).
Nesse sentido se faz necessária a presente abordagem por situar os achados relevantes em relação à síntese do fármaco antimicrobiano bacitracina, os mecanismos de ação e aplicação clínica, e importantes aspectos farmacológicos de relevância desse medicamento sintético no cenário terapêutico, além dos avanços científicos convergentes com as possibilidades de melhorias nas tecnologias de produção de medicamentos antimicrobianos.
Destaque-se, por fim, a exploração da evolução da síntese da bacitracina desde sua introdução como parte das primeiras drogas antimicrobianas até os dias atuais. Discutiremos também a importância desse medicamento antimicrobiano o qual é um dos mais utilizados na prática clínica, focando na sua estrutura, função e características mais relevantes.
2 METODOLOGIA
O estudo foi elaborado a partir de dados obtidos por meio de revisões bibliográficas. A revisão da literatura foi realizada durante o segundo semestre de 2023 por meio de pesquisa em livros e revistas científicas e em sites de busca como Scielo, PubMed e Google Acadêmico. Ao todo foram selecionados 40 trabalhos para revisão sistemáticas os quais podem ser consultados no decorrer do texto ou na sessão “referências”. Foram realizadas buscas utilizando o descritor “bacitracina” com ênfase em seus princípios de ação, características químicas, estruturais e farmacológicas, interações e principais indicações. Foram também destacadas informações como implicações clinicas e efeitos adversos.
3 REFERENCIAL TEÓRICO E DISCUSSÃO
3.1 Indicações
A bacitracina é um antibiótico polipeptídico cíclico (figura 01) usado para prevenir e tratar infecções em feridas, tratar pneumonia e empiema em lactentes, e para tratar infecções na pele e nos olhos (SCHALOCK PC, ZUG KA, 2005).
A bacitracina apresentada como pomada antibiótica tópica tem sido amplamente utilizada por profissionais de saúde e pelo público em geral para tratar lesões cutâneas leves, como cortes, arranhões e queimaduras (SCHALOCK PC, ZUG KA, 2005; JOHNSON BA, ANKER H, MELENEY FL., 1945).
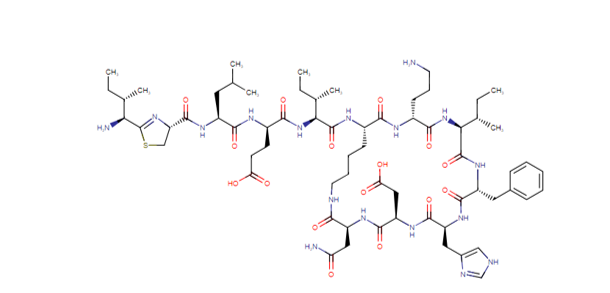
Figura 1: Estrutura química da bacitracina (disponível em https://go.drugbank.com/structures/DB00626/, acesso em 01/11/2023).
A bacitracina foi descoberta em 1945 a partir de uma lesão na perna de uma menina americana de sete anos chamada Margaret Tracey. Os detritos coletados de sua ferida cultivaram isolados de vários polipeptídeos cíclicos relacionados produzidos por um membro do grupo Bacillus subtilis. Essa descoberta deu origem ao nome único, bacitracina (STONE KJ, STROMINGER JL., 1975; CRONIN H, MOWAD C., 2009).
A agencia que administra e fiscaliza a produção de alimentos e medicamentos dos Estados Unidos, a FDA (sigla em inglês para “Food and Drug Administration”), aprovou o uso da bacitracina em 1948 para a prevenção e tratamento a curto prazo de infecções cutâneas localizadas agudas e crônicas. A bacitracina também pode ser administrada com menos frequência como medicação parenteral por meio de injeção intramuscular (IM) para o tratamento sistêmico de pneumonia estreptocócica infantil e empiema (GIGLIOTTI F, 1984; SHETH VM, WEITZUL S, 2008).
A bacitracina desempenha um papel crucial na promoção da cicatrização e prevenção de infecções em feridas cutâneas. Sua aplicação é frequentemente indicada para tratar desde pequenos cortes e arranhões até feridas cirúrgicas, proporcionando um ambiente propício para o processo de cicatrização. Além disso, é empregada como medida preventiva em lesões cutâneas, protegendo contra a invasão de bactérias gram-positivas. A eficácia da bacitracina a torna uma escolha comum para profissionais de saúde na busca por cuidados adequados e seguros para a pele, desempenhando um papel significativo na manutenção da integridade cutânea e na prevenção de complicações infecciosas. (CRONIN H, MOWAD C., 2009).
3.2 Mecanismo de Ação
A bacitracina é uma mistura de vários antibióticos polipeptídicos cíclicos intimamente relacionados que possuem propriedades tanto bacteriostáticas quanto bactericidas, dependendo da concentração do medicamento e da suscetibilidade do microrganismo (LEACHMAN SA, REED BR., 2006; SHETH VM, WEITZUL S, 2008).
Muitas bactérias gram-positivas, incluindo Staphylococcus spp., Streptococcus spp., Corynebacterium spp., Clostridium spp. e Actinomyces spp., são suscetíveis à bacitracina. Alguns organismos gram-negativos, como Neisseria spp., também apresentam suscetibilidade; no entanto, a maioria dos organismos gram-negativos é resistente (MURASE JE, HELLER MM, BUTLER DC, 2014).
A bacitracina é prontamente absorvida através da pele desnudada, queimada ou granulada e atua evitando a transferência de mucopeptídeos para a parede celular de vários microorganismos. Isso inibe subsequentemente a síntese da parede celular bacteriana e, em última instância, a replicação bacteriana. A bacitracina também atua como inibidor de proteases e outras enzimas envolvidas na alteração da função da membrana celular bacteriana (LEACHMAN SA, REED BR., 2006; SHETH VM, WEITZUL S., 2008).
A bacitracina inibe a síntese da parede celular bacteriana ao prevenir a desfosforilação do transportador de fosfolipídeo P-P que conecta os precursores de peptidoglicano da parede celular à membrana celular, levando à lise celular bacteriana (figura 02) (JONES RN et al., 2006).
3.3 Administração
A bacitracina está disponível em três vias diferentes nos Estados Unidos: tópica, oftálmica e parenteral por meio de injeção intramuscular (IM).O uso mais comum é como um agente tópico aplicado diretamente na ferida ou área infectada. Também pode ser administrado como uma pomada oftálmica tópica para tratar infecções oculares superficiais envolvendo a conjuntiva e a córnea, utilizando uma formulação especificamente fabricada para uso ocular (BONOMO RA et al., 2007).
Antes da aplicação tópica, a pele deve ser limpa suavemente com sabão neutro e água. Em seguida, uma quantidade suficiente de pomada deve ser aplicada para cobrir a área afetada, e um curativo estéril pode ser usado para cobrir a ferida. Isso ajuda na cicatrização da ferida e previne uma maior contaminação do local da ferida (KATZ BE, FISHER AA, 1987; BONOMO RA et al., 2007).
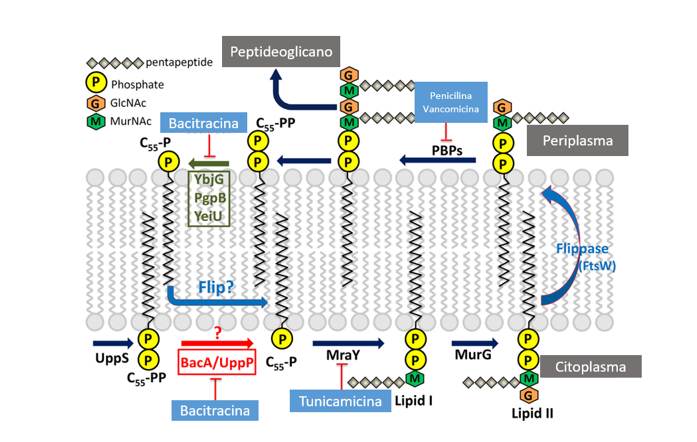
Figura 02: Visão esquematizada do mecanismo de ação da bacitracina. A bacitracina inibe a biossíntese de bactoprenol (C55-isoprenil fosfato) e, consequentemente do peptidoglicano na parede celular por meio da formação de um complexo em presença de dois cátions bivalentes. Assim, há inibição de precursores da parede celular e também a desfosforilação do carreador fosfolipídio.
NOTA: De modo geral as proteínas UppS sintetizam C 55 -PP, que é desfosforilado para monofosfato C55-P pela fosfatase BacA/UppP. Posteriormente, os açúcares-pentapeptídeo são transferidos para C 55 -P pelas enzimas MraY e MurG, produzindo respectivamente lipídeo I e lipídeo II. O lipídeo II é então transportado para o periplasma via flipase (FtsW) para a montagem do peptidoglicano pelas proteínas ligadoras de penicilina (PBPs). Por fim, o peptidoglicano é transferido para a cadeia de peptidoglicano, e o C 55 -P é invertido de volta para o citoplasma para repetir o ciclo após ser desfosforilado pelas enzimas YbjG, PgpB ou YeiU. O ponto de interrogação azul indica que atualmente não se sabe como as moléculas de C 55 -P desfosforiladas no periplasma retornam ao citoplasma na via de reciclagem. O ponto de interrogação vermelho indica que a função de BacA/UppP no compartimento citosólico ou no espaço periplasmático ainda não está clara. Antibióticos ativos na parede celular incluem Bacitracina, que forma um complexo dependente de metal com C55 -PP e inibe sua desfosforilação. Tunicamicina inibe a transferência do precursor do peptidoglicano (fosfo-MurNAc-pentapeptídeo) para o C55 -PP. Vancomicina inibe a síntese da parede celular ligando-se aos dois resíduos de D-Ala no final das cadeias de pentapeptídeo. Penicilina e moenomicina A (MmA) inibem as proteínas ligadoras de penicilina (Adaptado de Chang HY et al., 2014).
3.4 Efeitos Adversos
Ao ser usado topicamente como pomada única ou como parte de uma pomada em terapia tripla, a bacitracina e os componentes de sua formulação podem causar dermatite de contato alérgica, que pode levar a uma reação anafilática ou anafilaxia. Além disso, é possível ocorrer febre, urticária, coceira, inchaço nos lábios e rosto, dificuldade para respirar, náusea e vômito de forma rara (SARYAN JA, DAMMIN TC, BOURAS AE, 1998; LEVIN HS, KAGAN BM, 1968).
É importante salientar que a bacitracina é classificada como categoria C de risco na gravidez e que não foram realizados grandes estudos sobre o uso de bacitracina tópica durante a gravidez ou lactação. Até o momento, não há evidências que sugiram um aumento no risco de desenvolvimento fetal adverso com o uso tópico de bacitracina (KOCH R, DONNELL G, 1957; SOOD A, TAYLOR JS, 2003).
Além disso, as formas tópicas e oftálmicas de bacitracina geralmente resultam em absorção mínima através da pele e são consideradas de baixo risco para o lactente. Apenas cremes ou géis solúveis em água devem ser aplicados no tecido mamário para evitar a exposição do lactente ao parafina mineral por meio da lambedura (TAYLOR JS, 2003).
Na tabela a seguir estão elencados os principais eventos adversos decorrente do uso da bacitracina bem como precauções necessárias para se garantir a segurança na administração desse antibiótico.
Tabela 01: Principais informações e medidas quanto à administração segura de bacitracina.
Eventos Considerações Efeitos colaterais comuns: Reações nefrotóxicas (toxicidade renal), incluindo albuminúria, cilindrúria e azotemia; Náusea e vômito; Coceira; Discrasias sanguíneas; Transpiração; Reações no local da injeção (dor, queimação, inchaço); Erupções cutâneas. Efeitos colaterais graves: Frequência miccional aumentada; Presença de sangue na urina; Dor na região lombar; Dor ao urinar. Nefrotoxicidade: Pode haver insuficiência renal devido à necrose tubular e glomerular (evitar o uso simultâneo com outros medicamentos nefrotóxicos, por exemplo, estreptomicina, gentamicina, canamicina, polimixina B, colistina, neomicina, anfotericina B). Contraindicações: Qualquer tipo de hipersensibilidade à bacitracina e motivo de contraindicação. Via de administração: Não administrar por via intravenosa (pode ocorrer tromboflebite grave). Gravidez e Lactação: Seu uso é limitado (com prescrição rigorosa) em neonatos com pneumonia ou empiema causados por cepas suscetíveis de estafilococos, quando antibióticos menos tóxicos não seriam eficazes.
3.5 Contraindicações
A bacitracina tópica é contraindicada em qualquer pessoa com hipersensibilidade à bacitracina e/ou a qualquer um dos componentes de sua formulação. Pacientes com hipersensibilidade conhecida à neomicina também podem ser sensíveis à bacitracina. A aplicação de bacitracina em uma infecção ou ferida causada por uma infecção viral ou fúngica pode aumentar o risco de desenvolvimento de bactérias resistentes a medicamentos (SPRING S, PRATT M, CHAPLIN A., 2012).
Taylor J.S. (2003) afirma, que uso de bacitracina tópica é recomendado apenas para lesões cutâneas leves e não deve ser utilizado em áreas extensas do corpo, recomendando a realização de uma consulta médica antes de usar bacitracina tópica em casos de lesões graves, como queimaduras, feridas profundas, ferimentos por perfuração ou mordidas de animais.
3.6 Toxicidade
De acordo com Zug K.A. e colaboradores (2006) não há menção de toxicidade com o uso tópico de bacitracina como pomada única ou parte de uma pomada de terapia tripla.
No entanto, a administração intramuscular (IM) foi associada à nefrotoxicidade e insuficiência renal devido à necrose tubular e glomerular. Consequentemente, é necessário monitoramento cuidadoso com o uso IM de bacitracina. A função renal deve ser avaliada antes, durante e após a administração IM. A ingestão diária ideal de fluidos e a produção urinária dos pacientes devem ser acompanhadas de perto para evitar lesões renais (SPRING S, PRATT M, CHAPLIN A., 2012)
O uso simultâneo de estreptomicina, canamicina, polimixina E e neomicina deve ser evitado, uma vez que esses medicamentos também são conhecidos por serem nefrotóxicos (ZUG KA et al., 2006).
4 CONCLUSÃO
A bacitracina, ao longo de sua trajetória na farmacologia, consolidou-se como uma ferramenta valiosa no arsenal terapêutico para o tratamento de infecções bacterianas. Este estudo oferece uma análise abrangente desde a descoberta inicial da bacitracina até suas aplicações clínicas e considerações farmacológicas. A significância clínica da bacitracina é inegável, respaldada por sua prescrição frequente devido à sua eficácia no combate a uma variedade de patógenos bacterianos.
A bacitracina atua inibindo a síntese de peptidoglicano, uma abordagem que a torna particularmente eficaz contra bactérias Gram-positivas. Ao longo deste estudo, abordamos aspectos como sua farmacocinética, mecanismo de ação e potenciais efeitos adversos, oferecendo uma visão holística de seu perfil terapêutico.
Além disso, o papel da bacitracina nas práticas médicas contemporâneas é enfatizado, destacando seu uso em pomadas tópicas para prevenção de infecções em feridas e procedimentos dermatológicos. A evolução constante da pesquisa na busca por melhores formulações e compreensão mais aprofundada de seu impacto clínico reitera a importância contínua da bacitracina no tratamento eficaz de infecções bacterianas.
Em resumo, a bacitracina continua a desempenhar um papel fundamental na terapêutica, representando uma opção confiável no tratamento de infecções. Sua relevância e versatilidade reforçam sua posição como uma ferramenta essencial na prática clínica, contribuindo significativamente para o controle e manejo de infecções bacterianas em diversas condições médicas.
5 REFERÊNCIAS
- ABRAHAM E. P. 1957 Biochemistry of Some Peptide and Steroid Antibiotics. New York: John Wiley and Sons, Inc;
- ABRAHAM E. P., NEWTON G. G. F. 1958; Structure and function of some sulphur-containing peptides. CIBA Foundation Symposium on amino acids and peptides with antimetabolic activity. Wolstenholme G. W. S., O’Connor C. M. London: J. and A. Churchill, Ltd;
- BONOMO RA, VAN ZILE PS, LI Q, SHERMOCK KM, MCCORMICK WG, KOHUT B. Topical triple-antibiotic ointment as a novel therapeutic choice in wound management and infection prevention: a practical perspective. Expert Rev Anti Infect Ther. 2007 Oct;5(5):773-82. 12.
- BOUKOUVALA F. et al., “Computer-Aided Flowsheet Simulation of a Pharmaceutical Tablet Manufacturing Process Incorporating Wet Granulation,” J. Pharm. Innov., vol. 8, no. 1, pp. 11–27, Jan. 2013.
- BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Resolução da Diretoria Colegiada – RDC n° 17, de 16 de abril de 2010, dispõe sobre Boas Práticas de fabricação de Medicamentos. Diário Oficial da União, Poder Executivo, Brasília, DF, 17 de abr. 2010b.
- BRASIL. O que devemos saber sobre medicamentos? Cartilha da Agência Nacional de Vigilância Sanitária (Anvisa). São Paulo, 104 p, 2010a.
- CARON S.,THOMSON N. M., “Pharmaceutical process chemistry: Evolution of a contemporary data-rich laboratory environment,” J. Org. Chem., vol. 80, no. 6, pp. 2943–2958, 2015.
- CHANG HY, CHOU CC, HSU MF, WANG AH. Proposed carrier lipid-binding site of undecaprenyl pyrophosphate phosphatase from Escherichia coli. J Biol Chem. 2014 Jul 4;289(27):18719-35. doi: 10.1074/jbc.M114.575076. Epub 2014 May 22. PMID: 24855653; PMCID: PMC4081917.
- CRAWFORD K., ABRAHAM E. P. 1957; The synergistic action of cephalosporin C and benzylpenicillin against a penicillinase-producing strain of Staphylococcus aureus. J. gen. Microbiol. 16:604.
- CREASER E. H. 1955; The induced (adaptive) biosynthesis of β-galactosidase in Staphylococcus aureus. J. gen. Microbiol. 12:288
- CRONIN H, MOWAD C. Anaphylactic reaction to bacitracin ointment. Cutis. 2009 Mar;83(3):127-9.
- GALE E. F., FOLKES J. P. 1955; The assimilation of amino-acids by bacteria. 21. The effect of nucleic acids on the development of certain enzymatic activities in disrupted staphylococcal cells. Biochem. J. 59:675
- GIGLIOTTI F, HENDLEY JO, MORGAN J, MICHAELS R, DICKENS M, LOHR J. Efficacy of topical antibiotic therapy in acute conjunctivitis in children. J Pediatr. 1984 Apr;104(4):623-6.
- GROSS H. M. 1954; Zinc bacitracin in pharmaceutical preparations. Drug. Cosmet. Ind. 75:612.
- HINTON N. A., ORR J. H. 1960; The effect of antibiotics on the toxin production of Staphylococcus aureus. Antibiot. & Chemother. 10:758
- JOHNSON BA, ANKER H, MELENEY FL. Bacitracin: a new antibiotic produced by a member of the b. subtilis group. Science. 1945 Oct 12;102(2650):376-7.
- JONES RN, LI Q, KOHUT B, BIEDENBACH DJ, BELL J, TURNIDGE JD. Contemporary antimicrobial activity of triple antibiotic ointment: a multiphased study of recent clinical isolates in the United States and Australia. Diagn Microbiol Infect Dis. 2006 Jan;54(1):63-71.
- KATZ BE, FISHER AA. Bacitracin: a unique topical antibiotic sensitizer. J Am Acad Dermatol. 1987 Dec;17(6):1016-24.
- KOCH R, DONNELL G. Staphylococcic infections in children. Calif Med. 1957 Nov;87(5):313-6.
- LEACHMAN SA, REED BR. The use of dermatologic drugs in pregnancy and lactation. Dermatol Clin. 2006 Apr;24(2):167-97.
- LEE S. L. et al., “Modernizing Pharmaceutical Manufacturing: from Batch to Continuous Production,” J. Pharm. Innov., vol. 10, no. 3, pp. 191–199, 2015.
- LEVIN HS, KAGAN BM. Antimicrobial agents: pediatric dosage, routes of administration and preparation procedures for parenteral therapy. Pediatr Clin North Am. 1968 Feb;15(1):275-90.
- MANDELSTAM J., ROBERS H. J. 1959; The incorporation of amino acids into the cell-wall mucopeptide of staphylococci and the effect of antibiotics on the process. Biochem. J. 72:654.
- MURASE JE, HELLER MM, BUTLER DC. Safety of dermatologic medications in pregnancy and lactation: Part I. Pregnancy. J Am Acad Dermatol. 2014 Mar;70(3):401.e1-14; quiz 415.
- PARK J. T. 1958; Inhibition of cell-wall synthesis in Staphylococcus aureus by chemicals which cause accumulation of wall precursors. Biochem. J. 70:2
- PARK J. T. 1960; Inhibition of synthesis of bacterial muco-peptides or protein by certain antibiotics and its possible significance for microbiology and medicine. Antimicrobial Agents Annual 1960338 New York: Plenum Press, Inc.
- SARYAN JA, DAMMIN TC, BOURAS AE. Anaphylaxis to topical bacitracin zinc ointment. Am J Emerg Med. 1998 Sep;16(5):512-3.
- SCHALOCK PC, ZUG KA. Bacitracin. Cutis. 2005 Aug;76(2):105-7.
- SHETH VM, WEITZUL S. Postoperative topical antimicrobial use. Dermatitis. 2008 Jul-Aug;19(4):181-9.
- SIMON L. L. H., et al., “Assessment of recent process analytical technology (PAT) trends: A multiauthor review,” Org. Process Res. Dev., vol. 19, no. 1, pp. 3–62, 2015.
- SOOD A, TAYLOR JS. Bacitracin: allergen of the year. Am J Contact Dermat. 2003 Mar;14(1):3-4.
- SPRING S, PRATT M, CHAPLIN A. Contact dermatitis to topical medicaments: a retrospective chart review from the Ottawa Hospital Patch Test Clinic. Dermatitis. 2012 Sep-Oct;23(5):210-3.
- STEENSMA M. et al., “Modelling and experimental evaluation of reaction kinetics in reactive extraction for chiral separation of amines, amino acids and amino-alcohols,” Chem. Eng. Sci., vol. 62, no. 5, pp. 1395–1407, Mar. 2007.
- STONE KJ, STROMINGER JL. Mechanism of action of bacitracin: complexation with metal ion and C 55 -isoprenyl pyrophosphate. Proc Natl Acad Sci U S A. 1971 Dec;68(12):3223-75.
- WEGNER J, CEYLAN S., KIRSCHNING A., “Flow Chemistry – A Key Enabling Technology for (Multistep) Organic Synthesis,” Adv. Synth. Catal., vol. 354, no. 1, pp. 17–57, Jan. 2012.
- WEINBERG E. D. 1957; The mutual effects of antimicrobial compounds and metallic cations. Bad. Rev. 21:46.
- WEINBERG E. D. 1959; Enhancement of bacitracin by metallic ions of group IIB. Antibiotics Annual 1958–1959924 Welch H., and Marti-Ibanez F. New York: Medical Encyclopedia, Inc.
- WRONG NM, SMITH RC, HUDSON AL, HAIR HC. The treatment of pyogenic skin infections with bacitracin ointment. Treat Serv Bull. 1951 Jun;6(6):257-61.
- YU L. X., “Pharmaceutical Quality by Design: Product and Process Development, Understanding, and Control,” Pharm. Res., vol. 25, no. 4, pp. 781–791, 2008.
- ZUG KA, WARSHAW EM, FOWLER JF, MAIBACH HI, BELSITO DL, PRATT MD, SASSEVILLE D, STORRS FJ, TAYLOR JS, MATHIAS CG, DELEO VA, RIETSCHEL RL, MARKS J. Patch-test results of the North American Contact Dermatitis Group 2005-2006. Dermatitis. 2009 May-Jun;20(3):149-60.
1Biomédico pelo Centro Universitário UNA – MG, Mestre em Bioquímica e Imunologia pela Universidade Federal de Minas Gerais – UFMG, Doutorando em Educação pela Universidad Internacional Iberoamericana – Porto Rico (EUA), Especialista em Analises Clinicas e Microbiologia pela Faculdade Venda Nova do Imigrante – ES (FAVENI – ES);
2Biomédica pela Universidade Paulista (UNIP), Aluna do curso de Pós-Graduação Lato Sensu em Hematologia Clínica e Banco de Sangue, Hemoterapia e Terapia Celular pelo Instituto Monte Pascoal – GO;
3Biólogo pela Faculdade Araguaia – GO (UniAraguaia), Aluno do curso de Pós-Graduação Lato Sensu em Microbiologia Aplicada ao Laboratório Clínico pelo Instituto Monte Pascoal – GO;
4Enfermeira pela Faculdade Padrão – GO, Especialista em UTI e Urgência e Emergência pela Faculdade Afirmativo – MT;
5Acadêmica do curso de Nutrição pelo Centro Universitário Leonardo da Vinci (UNIASSELVI);
6Acadêmica do curso de Biomedicina pelo Centro Universitário Leonardo da Vinci (UNIASSELVI); Técnica em Enfermagem pelo Instituto de Técnologia e Educação de Goiás – GO (ITEG);
7Biomédico pela Pontifícia Católica de Goiás – GO (PUC-GO), Mestre em Genética Pontifícia Católica de Goiás – GO (PUC-GO);Especialista em Gestão e Biossegurança em Estética e Cosmética pela Universidade Estadual de Goiás – GO (UEG);
8Biomédica pela Universidade Paulista (UNIP), Aluna do curso de Pós-Graduação Lato Sensu em Hematologia Clínica e Bioinformática pela Faculdade Unyleya – DF;
9Biomédico pela Universidade Paulista (UNIP), Aluno do curso de Pós-Graduação Lato Sensu em Hematologia Clínica e Banco de Sangue, Hemoterapia e Terapia Celular pelo Instituto Monte Pascoal – GO;
10Licenciado em Letras pela Universidade Candido Mendes – RJ, Doutor em Educação pela Universidade São Francisco – SP (USF) Mestre em Educação pela Universidade Estadual de Minas Gerais – MG (UEMG), Especialista em Ensino da Língua Portuguesa pela Universidade Candido Mendes – RJ.
Instituição: 1,2,4,6,7,8Unidade de Pronto Atendimento 24 horas (UPA 24 horas) / Secretaria Municipal de Saúde do Município de Senador Canedo – GO; 2,3,9Instituto Monte Pascoal – GO; 1,5,6Centro Universitário Leonardo da Vinci (UNIASSELVI); 10Universidade Federal de Minas Gerais – MG (UFMG).
