AUTOMATION IN THE PHARMACEUTICAL INDUSTRY
REGISTRO DOI: 10.5281/zenodo.11570176
Gaspar Silveira Martins Da Cruz Junior1; Wesley Henrique Lima Nogueira2; Renaldo José Feitosa; Marcidis Humberto Carneiro3; Márcio José Dias4
Resumo
Este estudo explora o impacto da automação avançada na indústria farmacêutica, enfocando especialmente nos tempos de produção e na conformidade regulatória. Aborda-se a utilização de tecnologias de automação cruciais para o processo produtivo, buscando compreender como essas contribuem tanto para a eficiência operacional quanto para a adesão às normativas regulatórias. Uma metodologia de revisão da literatura foi empregada para sintetizar as pesquisas existentes, oferecendo uma visão abrangente das tendências atuais, dos desafios e das oportunidades na aplicação da automação no setor. A busca foi realizada em bases de dados acadêmicas e científicas renomadas, utilizando descritores específicos e operadores booleanos para refinar as buscas, focando em publicações entre 2019 e 2029. A seleção de literatura incluiu artigos originais de pesquisa, revisões e diretrizes regulatórias que discutiram o uso da automação e seu impacto na indústria. Os resultados indicam que a automação não apenas acelera a produção, mas também fortalece a conformidade com as regulamentações, embora haja barreiras econômicas, técnicas e regulatórias que desafiam sua implementação completa. As conclusões ressaltam a necessidade de estratégias adaptativas para superar esses obstáculos, destacando o papel transformador da automação na melhoria contínua dos padrões de produção e regulatórios na indústria farmacêutica.
Palavras-chave: Automação Industrial. Indústria Farmacêutica. Tecnologia de Automação.
1 INTRODUÇÃO
A automação está transformando a maneira como as indústrias farmacêuticas operam, adotando máquinas para realizar tarefas repetitivas e cruciais. Essa mudança vem ocorrendo em um ritmo rápido, impulsionada pelo aumento dos padrões regulatórios, que estão mais rigorosos do que nunca. Implementar funções automatizadas é uma maneira eficaz para as empresas manterem-se atualizadas com as constantes alterações nas normas regulatórias. Historicamente, a adoção de novas tecnologias que substituem o trabalho manual tem sido uma prática comum em várias indústrias, apesar da resistência de sindicatos e comunidades preocupadas com o impacto no emprego (Arden et al., 2021).
Recentemente, houve um aumento dramático no uso de sistemas de visão computacional para garantia de qualidade, o que pode levar a uma mudança de pessoal. Avanços significativos em hardware e software levaram a melhorias notáveis. Esta tecnologia não só proporciona flexibilidade e precisão, mas também reduz custos, permitindo maior produtividade sem sacrificar a qualidade. Hoje em dia, estes sistemas são concebidos como componentes essenciais dos processos farmacêuticos, permitindo a monitorização contínua e em tempo real da qualidade do produto (Silva et al., 2020).
A indústria de automação evoluiu para incluir sistemas sofisticados, como robótica avançada e inteligência artificial (IA). Os robôs agora são usados para tarefas complexas, como manuseio de materiais perigosos e fabricação com maior precisão. Além disso, a IA e o aprendizado de máquina estão sendo usados para analisar grandes quantidades de dados para otimização, previsão de demanda e otimização. Esta tecnologia não só aumenta a eficiência, mas também permite a inovação na investigação e no desenvolvimento de novos medicamentos (Silva; Resende; Amorim, 2020).
A integração de automação de processos e sistemas de informação, como Enterprise Resource Planning (ERP) e Manufacturing Execution System (MES), inaugura uma nova era de transparência e controle sobre os resultados da indústria farmacêutica. Os sistemas de propriedade permitem monitorar o ritmo real de produção, capacidades de pesquisa múltipla e eficiência de recursos. Um poderoso avaliador e capacidade imediata e inabalável de tomar decisões baseadas em dados, melhorando a gestão da cadeia de suprimentos e a eficácia operacional (Bhatnagar, 2020).
Entretanto, a adoção da automação na indústria farmacêutica não vem sem desafios. Questões como a segurança cibernética, a necessidade de profissionais qualificados para operar e manter tecnologias avançadas e a conformidade com regulamentações rigorosas são obstáculos significativos. Além disso, o alto custo inicial de implementação pode ser uma barreira para pequenas e médias empresas (Lima; Gomes, 2021).
Apesar desses desafios, o futuro da automação na indústria farmacêutica é promissor. A busca contínua por maior eficiência, qualidade e segurança dos produtos farmacêuticos impulsiona a inovação e o investimento em novas tecnologias. À medida que a automação se torna mais acessível e as soluções tecnológicas evoluem, espera-se que a indústria farmacêutica continue a se beneficiar dessas transformações, oferecendo medicamentos mais seguros, de alta qualidade e acessíveis a uma população global crescente (Arden et al., 2021).
Estes avanços tecnológicos, que combinarão sistemas robóticos com soluções de inteligência artificial, permitirão processos de fabrico mais rápidos e precisos, reduzindo significativamente o tempo necessário para produtos farmacêuticos e outros produtos químicos. Ao mesmo tempo, a precisão e os custosos recursos de monitoramento oferecidos pela automação melhoram a adesão à medida que padrões regulatórios rigorosos são definidos, minimizando riscos de qualidade e garantindo maior segurança aos motoristas. Esses nove novos recursos não apenas aceleram o lançamento de produtos críticos, mas também fortalecem a garantia de conformidade com os padrões internacionais de saúde, representando ou satisfazendo Seu Requisito de Continuidade Melhoria Contínua e Regulamentação (Ghosh et al., 2020).
Este estudo teve como objetivo descrever o impacto da automação avançada nos tempos de produção e na conformidade regulatória na indústria farmacêutica. Foi dado foco em identificar as tecnologias de automação cruciais para o processo produtivo, entender como contribuem para a eficiência e a conformidade regulatória, e examinar os desafios para sua implementação, incluindo barreiras econômicas, técnicas e regulatórias. Esta abordagem direta visa oferecer uma visão clara sobre a influência da automação na eficiência produtiva e na aderência às normativas do setor farmacêutico.
2 FUNDAMENTAÇÃO TEÓRICA OU REVISÃO DA LITERATURA
O desenvolvimento da automação na indústria tem sido um dia de mudanças contínuas e disruptivas, marcado por décadas de desenvolvimento de produtos e atividade tecnológica desde o projeto das primeiras máquinas e linhas de montagem introduzidas durante a revolução industrial até os sofisticados sistemas de controle baseados em inteligência artificial e robótica atuais e mexer e não focar em tarefas simples (Coito et al., 2020).
Com o passar do tempo, a integração de sistemas de controle computadorizados e a robótica elevaram a automação a novos patamares, permitindo uma precisão inédita, flexibilidade na produção e capacidade de resposta rápida às mudanças de demanda do mercado. Esta evolução não apenas acelerou a produção, mas também abriu caminho para níveis sem precedentes de qualidade e personalização de produtos (Solfa, 2022).
Nos últimos anos, algumas indústrias registaram uma melhoria dramática na automação com o advento da Indústria 4.0, caracterizada pela combinação de digital, físico e biotecnologia. A utilização de big data, conectividade, análise avançada e aprendizagem automática estão a transformar a disrupção do local de trabalho, permitindo processos automatizados que podem ser melhor automatizados em tempo real. A maquinação moderna abre agora desde a aquisição da matéria-prima até à entrega do produto final, redefinindo o conceito de eficiência e abrindo novas oportunidades para uma maior sustentabilidade da inovação e modelos de negócio disruptivos. Algumas empresas estão a caminhar para um futuro onde a automação não só define a produtividade e a eficiência, mas também permite maior flexibilidade e flexibilidade, respondendo às crescentes exigências de crescimento e flexibilidade num mundo de atividades em rápida mudança (Kern et al., 2019).
No que diz respeito à indústria farmacêutica, a automação introduziu inovações revolucionárias e enfrenta desafios regulamentares da indústria. Esta mudança começou há décadas, com a introdução gradual de tecnologia que automatizou, padronizou e acelerou tarefas rotineiras. Hoje, abundam tecnologias como robótica avançada, sistemas de controle em tempo real e inteligência artificial, cada uma desempenhando um papel importante na otimização do tempo de produção e na garantia da conformidade com os regulamentos regulamentares (Hole; Hole; Mcfalone-Shaw, 2021).
O impacto destas tecnologias reduziu significativamente o tempo de produção, permitindo que produtos farmacêuticos e outros produtos farmacêuticos chegassem ao mercado mais rapidamente. Através de exemplos concretos e estudos de caso, é possível ao supervisor não só acelerar automaticamente a produção, mas também elevar os padrões de qualidade e segurança. Além disso, a conformidade é aprimorada pela precisão e rastreabilidade que a automação proporciona, facilitando a documentação de documentos e procedimentos de conformidade conforme rígidas diretrizes internacionais. (Klose et al., 2019).
A integração de sistemas automatizados no chão de fábrica tem possibilitado um controle de qualidade mais rigoroso, redução significativa dos tempos de produção e uma maior consistência nos produtos finais. Tecnologias como robótica avançada, sistemas de visão computacional e análise de dados em tempo real permitem uma monitoração e ajuste precisos dos processos produtivos, garantindo a aderência estrita às normativas regulatórias. Essa precisão é crucial na indústria farmacêutica, onde a qualidade e a segurança do produto são de suma importância. Além disso, a automação facilita a rastreabilidade completa dos lotes de produção, desde as matérias-primas até o produto acabado, melhorando a capacidade de resposta a qualquer questão de qualidade ou segurança que possa surgir (Mishra; Dash; Mishra, 2020).
A automação tem um impacto profundo e promissor na cadeia de abastecimento e na logística da indústria farmacêutica, garantindo que os medicamentos sejam produzidos e distribuídos de forma eficiente e dentro do prazo. Por exemplo, a utilização de um sistema de embalagem automatizado reduz o erro humano e aumenta a velocidade de embalagem, garantindo a autenticidade do produto durante a entrega. Estas eficiências operacionais traduzem-se em custos mais baixos e numa maior satisfação do cliente à medida que os produtos chegam ao mercado de forma mais rápida e fiável, promovendo assim não só tendências tecnológicas na indústria farmacêutica, mas também o desenvolvimento regulatório mais eficiente (Silva; Resende; Amorim, 2020).
Os benefícios da automação se estendem além da eficiência de produção e conformidade regulatória. Eles incluem a melhoria da segurança dos trabalhadores, a redução dos erros humanos e o aumento da qualidade dos produtos farmacêuticos. No entanto, a implementação de tais tecnologias não está isenta de desafios. As empresas farmacêuticas enfrentam obstáculos econômicos, técnicos e de integração de sistemas que podem dificultar a adoção da automação. Questões regulatórias específicas também surgem, particularmente no que diz respeito à validação de sistemas automatizados e à adesão a normas internacionais (Klose et al., 2019).
As implicações dessa evolução são profundas. A automação não apenas melhora a eficiência operacional e a conformidade regulatória, mas também promove a competitividade e a inovação dentro do setor farmacêutico. Ao final, a adoção contínua de automação tem o potencial de melhor atender às crescentes necessidades de saúde em todo o mundo. Esta revisão literária não apenas destaca a importância crítica da automação para a indústria farmacêutica moderna, mas também aponta para a necessidade de pesquisa contínua que acompanhe a rápida evolução tecnológica e suas implicações para a fabricação de produtos farmacêuticos (Mishra; Dash; Mishra, 2020).
2.1 SIGNIFICADO DA AUTOMAÇÃO NAS INDÚSTRIAS FARMACÊUTICAS
As indústrias farmacêuticas produzem milhões de tipos de medicamentos, e todos eles devem ser examinados minuciosamente para garantir a segurança antes de serem enviados fora da instalação. A maioria dos fabricantes utiliza sistemas automatizados para executar uma variedade de tarefas, incluindo o processamento de cápsulas, frascos e recipientes; fornecedor de formas farmacêuticas e seus respectivos recipientes; e assim por diante. Todas as operações automatizadas são monitoradas por uma central de computação. As centrais de informática monitorarão eficazmente todos os componentes essenciais do processo para garantir que a qualidade dos produtos permaneça consistente (Bhatnagar, 2020).
As máquinas de envase automatizadas também podem encher recipientes, frascos e cápsulas com eficácia. Eles são capazes de inspecionar o nível de recipientes e frascos cheios e rejeitar efetivamente itens não preenchidos (BOGDAN; DOMBROWSKI, 2019).
Tais sistemas automatizados podem ser usados para executar tais tarefas em instalações de produção em larga escala. Os sistemas automatizados são tão avançados que a preocupação da equipe de QA/QC é praticamente eliminada. Os lotes com problemas de conformidade são registrados continuamente na memória da máquina, tornando-se fácil identificar todos os lotes com problemas de conformidade (Bach; 2019).
Nesse contexto, devido ao fato de que medicamentos personalizados são muito eficazes no tratamento de vários tipos de doenças, a indústria médica percebeu a importância desses produtos. A automação é extremamente importante para que os medicamentos pessoais sejam uma realidade e realizem seu potencial. Sistemas mais sofisticados podem permitir uma pesquisa de medicamentos mais eficaz e mais rápida. A combinação ideal de medicamentos e dosagens pode ser encontrada por meio do uso de diversas tecnologias computacionais contemporâneas. A adoção de medicamentos personalizados é difícil em um mundo com uma população tão diversa, e com os métodos atuais, o conceito de medicamentos personalizados pode ser considerado inviável (Ranebennur et al., 2023).
Por exemplo, cada pessoa no planeta é única devido à sua composição genética diversificada. Por esta razão, os cuidados médicos de que necessitam também serão diferentes. Ferramentas automatizadas podem gerenciar dados geneticamente complicados e auxiliar a divisão de P&D no desenvolvimento de estratégias de tratamento eficazes. Primeiro, serão agrupados indivíduos com composição genética semelhante e, em seguida, o foco será o desenvolvimento de medicamentos adaptados a cada um deles. Os futuros desenvolvimentos tecnológicos permitirão a produção de medicamentos adaptados ao nível de tolerância aos medicamentos de cada paciente. Dependendo da quantidade desejada, os procedimentos de produção podem ser simplesmente otimizados para produzir produtos farmacêuticos em concentrações variadas (Kern et al., 2019).
Devido às limitações inerentes aos processos de produção convencionais/atuais, diferentes concentrações de medicamentos não podem ser produzidas conforme necessário. Atualmente, antes de ser liberado para o próximo lote com concentração alterada, um ciclo de produção deve completar seu todo. Quando e quando necessário, dispositivos automatizados serão eficientes na regulação dos parâmetros do processo para gerar a concentração necessária de medicamentos nas quantidades necessárias. Portanto, esse benefício específico da automação só pode ser usado para criar medicamentos personalizados para pacientes em todo o mundo (Mak; Wong; Pichika, 2023).
A indústria farmacêutica utiliza extensivamente a robótica para uma variedade de operações de produção, pesquisa e triagem de medicamentos. A maioria das ferramentas analíticas é automatizada, o que simplifica processos analíticos trabalhosos. Há uma diminuição significativa na carga de trabalho do departamento de CQ. quando há uma produção maior. Os sistemas automatizados podem auxiliar o departamento analítico caso este não consiga receber seus resultados no prazo. Dispositivos automatizados e robóticos são incorporados para permitir testes e amostragem imediatos em lotes. A probabilidade de perder lotes seria bastante baixa devido aos testes em andamento (Bach, 2019).
Todos os resultados dos testes são mantidos ou tratados corretamente graças ao design dos sistemas analíticos. Como a maioria dos sistemas nunca altera os dados, eles cumprem os regulamentos da FDA relativos à integridade dos dados. Um sistema de HPLC totalmente automatizado, por exemplo, pode coletar amostras, analisá-las e enviar os resultados para um computador central por conta própria. A assistência de uma equipe de CQ não é necessária neste caso. Nesse sentido, a robótica e os sistemas automatizados têm o potencial de influenciar significativamente as operações laboratoriais da indústria farmacêutica (GHOSH et al., 2020).
Nesse sentido, os robôs industriais têm uma vida útil muito longa antes de sofrerem qualquer mau funcionamento tecnológico. Tudo o que será necessário é manutenção regular e uma fonte de energia contínua. Como resultado, estes procedimentos contínuos podem ajudar financeiramente as indústrias. Existem limitações em exigir que os humanos trabalhem em horários prolongados, como o bem-estar físico e mental dos trabalhadores. No entanto, isso não é um problema com máquinas. Todas as máquinas funcionarão bem e sem problemas por longos períodos de tempo com manutenção adequada. Isto pode ser imediatamente responsabilizado pela taxa de desemprego. É imperativo que os fabricantes e reguladores investiguem este elemento, pois a comunidade trabalhadora preferiria que isso não ocorresse. As economias também podem ser afetadas por isso (Arden et al., 2021).
Javaid et al., (2021) destaca que são inúmeros sensores integrados que conseguem detectar as variáveis dos processos em cada etapa, garantindo que as operações ocorram em um sistema controlado e com poucos erros. Como os sistemas automatizados são tão avançados, eles podem até registrar ou desligar caso seja encontrado um lote que não esteja em conformidade. Os sistemas automatizados são equipados com sensores posicionados por toda parte para permitir o monitoramento contínuo da variação do processo. Por outro lado, esses dados são enviados ao computador, que os utiliza para analisá-los e depois decide o que fazer, como rejeitar lotes ou desligar o sistema. A intervenção humana nestas situações será mínima porque a sua única responsabilidade seria garantir o funcionamento dos diferentes sistemas envolvidos.
Às vezes, as indústrias combinam todos os seus sistemas vitais, incluindo unidades de tratamento de ar, sistemas WFI, sistemas de vapor puro e sistemas de produção. Isto é bom porque permite o controle de todos os atributos relacionados à qualidade. A equipe é notificada caso haja algum tipo de problema em algum sistema. Estes sistemas integrados são cruciais para a produção de produtos parenterais, etc., onde é necessária extrema cautela porque mesmo um pequeno desvio das especificações pode afetar a qualidade do produto final (Javaid; Haleem, 2019).
2.2 TECNOLOGIAS DE AUTOMAÇÃO UTILIZADAS NA INDÚSTRIA FARMACÊUTICA
O uso dessas tecnologias na indústria farmacêutica tem sido classificado globalmente de acordo com o nível organizacional em que são utilizadas, seja em funções administrativas, no design de produtos e processos integrados, no planejamento de produção ou no controle deste (Javaid et al., 2021).
O primeiro grupo a ser destacado trata-se da gestão de tecnologias que ajudam a integrar os departamentos funcionais da empresa. Estas incluem planejamento de requisitos de materiais (MRP), planejamento de recursos materiais (MRPII), just in time (JIT), tecnologia de grupo (GT), inteligência artificial (IA), troca eletrônica de dados (EDI) (Al-Amin et al., 2023; Hossain et al., 2022).
Já o grupo dois refere-se à tecnologias que apoiam as operações da planta para o design, planejamento e controle de processos e produtos. Este grupo inclui design assistido por computador (CAD), design e esboços assistidos por computador (CADD), engenharia assistida por computador (CAE), monitoramento de processos assistido por computador e planejamento de processos assistido por computador (CAPP) (TARASOV et al., 2022).
O grupo três trata-se de tecnologias baseadas em computadores que são utilizadas diretamente nas plantas para produzir, manipular e transportar materiais e produtos. Aqui se encontram robôs, máquinas de visão artificial, máquinas de controle numérico (CNC), controladores lógicos programáveis (PLC), manipuladores automatizados de materiais, sistemas automatizados de transporte (AGVS), sistemas automatizados de armazenamento e recuperação (AR/AS) (ZHANG et al., 2019).
Os sistemas de transporte automatizado entre cada uma das etapas do processo, como áreas de armazenamento, embalagem e expedição, são utilizados para movimentação de material dentro das instalações de produção, o que permite a criação de uma planta farmacêutica de produção completamente automatizada que requer mínima participação de trabalhadores no chão de fábrica (GOHAR; NENCIONI, 2021).
De acordo com o conceito de JIT, o uso de veículos guiados automaticamente (AGV) facilita o transporte de contêineres com granel ou recipientes com materiais em processo e componentes de embalagem para onde são necessários. Isso elimina áreas de armazenamento temporário ou de trânsito e melhora o processo de fluxo e trajetórias de materiais na planta (RANEBENNUR et al., 2023).
Recipientes de dimensões padronizadas são utilizados para transportar e misturar pós secos e granulados entre várias etapas do processo, assim como para armazená-los em comprimidos e enchê-los em cápsulas. As características de manipulação automatizada para transferência e ajuste às máquinas de processo, carga e descarga, estações de recepção, lavagem de recipientes e mistura de material foram simplificadas graças a este avanço. Os recipientes podem ser equipados com etiquetas de identificação permanentes, que permitem a verificação automatizada por meio de códigos de barras para identificar e rastrear os recipientes na planta, aumentando a segurança em caso de confusão e/ou contaminação cruzada entre lotes (DOULGKEROGLOU et al., 2020).
Sendo assim, os AGVs transportam os recipientes com materiais para a estação de trabalho ao longo de rotas predefinidas onde estão localizados. A estação de selagem automática é ativada para garantir um ajuste perfeito entre a descarga e o recipiente onde é recebido. Neste tipo de indústria, o conceito de automação em ilhas de produção é desenvolvido ao colocar as máquinas de processo em salas limpas específicas e conectá-las através de descargas por gravidade e retorno por vácuo a recipientes dedicados para descarga e recebimento, respectivamente (Doulgkeroglou et al., 2020).
Cada ilha de produção automatizada pode estar equipada com um controlador lógico programável (PLC), que supervisiona o processo e o controle automatizado de outros PLCs do grupo. O PLC principal fornece o controle direto da comunicação no sistema de planta de processo. Todo o processo de produção é gerenciado por este sistema, que também controla diretamente os sistemas PLC de baixo nível, ajudando a integrar e organizar todas as operações de produção (Namekar; Yadav, 2020).
Um sistema de gerenciamento e controle de processos (PMCS) controla diretamente os AGVs e os computadores do armazém, emitindo blocos de ordens de transporte e requisitos de planejamento de produção. Também permite planejar e implementar requisitos de produção, armazenar dados de produção, programas de processamento em lotes, rastreamento de materiais na planta e identificação e verificação de todas as etapas do processo (Arden et al., 2021).
Finalmente, as Boas Práticas de Manufatura Automatizada (GAMP) foram desenvolvidas como resultado do conceito de qualidade que caracteriza esse tipo de produção. O GAMP orienta os fornecedores de sistemas automatizados em seu desenvolvimento e manutenção e fornece diretrizes para os usuários sobre os aspectos relacionados ao pessoal, validações e garantia de qualidade do software e documentação necessária para apoiar as validações (Hole et al., 2021).
2.3 INTELIGÊNCIA ARTIFICIAL UTILIZADAS NO DESENHO INTEGRADO DE PRODUTOS E PROCESSOS
As tecnologias de inteligência artificial (IA) são desenvolvimentos de software cujo objetivo é incorporar o conhecimento de um domínio em um sistema de computador para realizar tarefas em áreas específicas, que normalmente são realizadas por humanos altamente treinados no assunto. Esses sistemas devem interpretar a informação de um especialista humano em termos de sua linguagem e transformá-la em variáveis computacionais; além disso, têm a capacidade de tomar decisões e chegar a resultados e conclusões semelhantes às de um especialista humano (Kolluri et al., 2022).
A tendência atual é o Design Integrado de Produto e Processo (IPPD), que concretiza as necessidades da sociedade em soluções na forma de produtos, incluindo o desenvolvimento abrangente de um produto desde a percepção de sua necessidade no mercado até a criação dos primeiros protótipos funcionais deste. A forma como a informação gerada em cada etapa será processada é importante ao aplicar essa ideia ao design (VORA et al., 2023).
O desenvolvimento de um novo medicamento busca um sistema de entrega estável, baseado nas formas farmacêuticas conhecidas. O processo começa com a definição de uma ideia, expressa em termos de parâmetros de design, e termina com a criação de uma ou mais formulações que atendam aos requisitos (PATEL; SHAH, 2022).
As alternativas no campo da automação, como sistemas especialistas, redes neurais e algoritmos genéticos, facilitam o trabalho dos designers ao avançar na atividade de desenvolvimento de produtos dentro de uma planta de produção. Sistemas especialistas são programas de computador que auxiliam na tomada de decisões com base no conhecimento de especialistas no assunto. Este software desenvolvido consiste em um motor de inferência que extrai e manipula informações armazenadas no banco de dados e simula o processo de resolução de problemas (Bhattamisra et al., 2023).
As redes neurais artificiais são programas de software que se baseiam no comportamento dos neurônios biológicos para imitar o processo de aprendizagem humano. Uma unidade neuronal recebe uma ou mais entradas e então gera uma saída. Os neurônios são organizados em uma arquitetura de rede, que consiste em várias camadas de neurônios. Nesta arquitetura de rede, a saída de cada neurônio é a entrada de outro neurônio na próxima camada. O “algoritmo de treinamento” é utilizado para treinar redes neurais (Koromina; Pandi; Patrinos, 2019).
As redes neurais são úteis para modelar as relações não lineares entre variáveis dependentes e independentes, tornando-as úteis em campos como a pré-formulação e a formulação de medicamentos, onde a complexidade das variáveis dificulta a resolução rápida dos problemas de desenvolvimento (Colombo, 2020).
As redes neurais têm muitas vantagens, incluindo a capacidade de lidar com aplicações do mundo real, a facilidade de aprendizado e adaptação, a capacidade de generalizar, a alta tolerância a falhas, a rapidez e a eficiência, a flexibilidade e a manutenção fácil. Os algoritmos genéticos, uma técnica de otimização eficaz, são usados em processos cíclicos, nos quais uma sequência de operações é executada rapidamente para buscar o nível ótimo. Quando são utilizados algoritmos genéticos para a otimização, estabelece-se uma função de “desejabilidade” que fornece a solução ótima para um projeto de formulação específico (Mirmozaffari et al., 2022).
Os algoritmos genéticos podem usar algoritmos estocásticos, que buscam as condições que melhor satisfazem uma função específica. São rápidos e eficientes, e podem encontrar o ponto global mínimo e máximo dentro de um conjunto de dados. Ao iniciar o processo de seleção natural e combinar várias funções, produzem resultados que se aproximam dos melhores valores (Patel; Shah, 2022).
No modelamento e otimização de formulações de produtos, a interação entre as redes neurais e os algoritmos genéticos permite, inicialmente, criar um modelo através de redes neurais, que pode ser consultado ou usado para experimentos condicionais “se”. O uso de algoritmos genéticos para otimizar o modelo permite encontrar a melhor formulação dentro de uma ampla gama de possibilidades.
3 METODOLOGIA
Neste estudo, adotou-se uma metodologia de revisão sistemática da literatura para investigar o impacto da automação avançada nos tempos de produção e na conformidade regulatória na indústria farmacêutica. A metodologia visou sintetizar as pesquisas existentes sobre o tema, proporcionando uma compreensão abrangente das tendências, desafios e oportunidades na aplicação da automação nesse setor específico.
Para garantir a relevância e a precisão da busca por literatura, foram utilizados descritores específicos, tais como “automação na indústria farmacêutica”, “impacto da automação nos tempos de produção”, “automação e conformidade regulatória” e “tecnologias de automação em farmacêutica”. Esses termos foram empregados tanto isoladamente quanto em combinação, utilizando-se operadores booleanos AND e OR para refinar as buscas.
A pesquisa foi conduzida em bases de dados acadêmicas e científicas de renome, incluindo PubMed, SciElo e Google Academico, além de bases de dados específicas do setor farmacêutico, como a International Pharmaceutical Abstracts e a base de dados da Food and Drug Administration (FDA). O foco esteve em trabalhos publicados entre 2019 e 2029, período que permitiu captar as tendências mais atuais no uso da automação na indústria farmacêutica.
Foram incluídos artigos originais de pesquisa, revisões, estudos de caso e diretrizes regulatórias que discutiram o uso da automação e seu impacto na indústria, limitando-se a documentos em inglês, espanhol ou português. Foram excluídos editoriais, comentários e cartas ao editor sem dados de pesquisa originais, trabalhos não relacionados diretamente ao tema, não acessíveis integralmente ou publicados fora do intervalo de tempo definido.
O procedimento de seleção iniciou com a análise de títulos e resumos para determinar a relevância em relação aos objetivos da pesquisa. Em seguida, os textos completos dos artigos pré-selecionados foram examinados detalhadamente para assegurar o cumprimento dos critérios de inclusão. A Figura 1 sintetiza a metodologia utilizada.
Figura 1 – Esquema metodológico adota neste estudo.

Este método sistemático possibilitou a coleta e análise de informações atuais e pertinentes sobre as implicações da automação para a indústria farmacêutica, abrangendo as inovações tecnológicas, os desafios encontrados e as oportunidades emergentes neste campo vital.
4 RESULTADOS E DISCUSSÕES
Com base na metodologia adotada, identificamos os 10 estudos mais pertinentes para este trabalho. O Quadro 1 abaixo resume as informações-chave desses estudos selecionados.
Quadro 1 -Artigos selecionados que atendem ao tema proposto.
AUTORES ANO TÍTULO PERIÓDICO ARDEN, N. Sarah et al. 2021 Industry 4.0 for pharmaceutical manufacturing: Preparing for the smart factories of the future International Journal of Pharmaceutics BHATNAGAR, Nitu 2020 Role of robotic process automation in pharmaceutical industries Springer International Publishing BHATTAMISRA, Subrat Kumar et al. 2023 Artificial intelligence in pharmaceutical and healthcare research Big Data and Cognitive Computing DOULGKEROGLOU, Meletios-Nikolaos et al. 2020 Automation, monitoring, and standardization of cell product manufacturing Frontiers in Bioengineering and Biotechnology GHOSH, Rajesh et al. 2020 Automation opportunities in pharmacovigilance: an industry survey Pharmaceutical Medicine HOLE, Glenn; HOLE, Anastasia S.; MCFALONE-SHAW, Ian 2021 Digitalization in pharmaceutical industry: What to focus on under the digital implementation process? International Journal of Pharmaceutics: X KERN, Simon et al. 2019 Flexible automation with compact NMR spectroscopy for continuous production of pharmaceuticals Analytical and bioanalytical chemistry RANEBENNUR, Raksha et al. 2023 Development of Automated Quality Assurance Systems for Pharmaceutical Manufacturing: A Review Journal of Coastal Life Medicine VORA, Lalitkumar K. et al. 2023 Artificial intelligence in pharmaceutical technology and drug delivery design Pharmaceutics MISHRA, Sushruta; DASH, Anuttam; MISHRA, Brojo Kishore 2020 An insight of Internet of Things applications in pharmaceutical domain Academic Press
Um dos pontos fortes analisando o Quadro 1 é a diversidade temática que ele abrange, desde a inteligência artificial e a automação robótica até o monitoramento de processos, oferecendo uma visão detalhada de como as tecnologias estão sendo aplicadas na indústria. Além disso, a atualidade dos artigos, que majoritariamente datam de 2020 a 2023, é essencial em um campo em rápida evolução como o da automação tecnológica, garantindo que o conteúdo seja relevante e contemporâneo.
A Figura 2 descreve também o volume de artigos publicados por ano, permitindo avaliar como a área tem avançado em número de estudos,
Figura 2 – Volume de artigos publicados por ano.
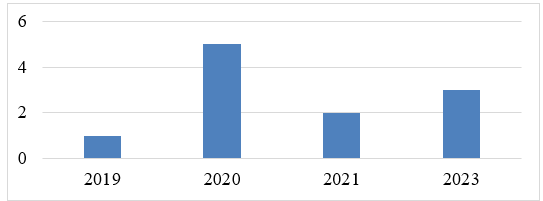
Em 2019, observamos apenas uma publicação, indicando um interesse inicial talvez mais modesto nesta área específica. No entanto, em 2020, houve um salto significativo para cinco artigos, possivelmente refletindo um crescente interesse motivado por necessidades emergentes, como as impostas pela pandemia de COVID-19, que exigiu processos mais eficientes e seguros. Em 2021, o número de publicações caiu para dois, sugerindo uma possível consolidação das pesquisas anteriores.
Em 2023, o número aumentou novamente para três publicações, indicativo de um amadurecimento das tecnologias de automação ou a emergência de novos desafios que demandaram inovações adicionais. Este padrão de publicação ilustra não só o crescimento da área mas também suas flutuações anuais, que podem estar alinhadas a ciclos de financiamento, mudanças nas prioridades de pesquisa ou respostas a desafios industriais específicos.
No estudo de ARDEN, N. Sarah et al. (2021), os autores discutem o avanço da Indústria 4.0 na fabricação farmacêutica, destacando a preparação para as fábricas inteligentes do futuro. Este trabalho oferece uma visão sobre como as tecnologias digitais estão sendo incorporadas para melhorar a eficiência e a produtividade, possibilitando assim um novo paradigma de fabricação personalizada e flexível na indústria farmacêutica (ARDEN, N. Sarah et al., 2021).
Bhatnagar (2020) aborda de forma detalhada a integração da automação de processos robóticos nas indústrias farmacêuticas. Seu estudo destaca não apenas a capacidade desta tecnologia de acelerar os processos de produção, mas também de aprimorar a precisão e a aderência às rigorosas normas regulatórias. Além disso, ele evidencia como a automação pode reduzir significativamente os custos operacionais e os erros humanos em ambientes que demandam alto grau de conformidade.
Por outro lado, Bhattamisra et al. (2023) investigam o impacto revolucionário da inteligência artificial na pesquisa farmacêutica e de saúde. O estudo revela que a IA não só tem a capacidade de prever tendências de doenças, mas também de otimizar as composições dos medicamentos e personalizar os tratamentos. Este trabalho ilustra claramente o potencial transformativo da inteligência artificial, enfatizando seu papel crucial no desenvolvimento de novas terapias que podem ser adaptadas às necessidades individuais dos pacientes.
Doulgkeroglou et al. (2020) conduziram um estudo abrangente sobre automação, monitoramento e padronização na produção de produtos celulares. A pesquisa ressalta a crucialidade dos sistemas automatizados em assegurar a uniformidade e a qualidade em processos altamente especializados e delicados, que são fundamentais na fabricação de bioprodutos. O estudo enfatiza que a automação não apenas facilita a eficiência operacional, mas também é vital para manter os elevados padrões de segurança e eficácia requeridos neste campo avançado da biotecnologia.
No mesmo ano, Ghosh et al. (2020) exploraram as possibilidades de automação em farmacovigilância através de um levantamento meticuloso. O estudo ilumina o modo como a automação pode elevar tanto a eficiência quanto a precisão na monitoração de eventos adversos, um componente vital para garantir a segurança dos pacientes e cumprir com as normativas regulatórias. A pesquisa argumenta que a integração da automação nesses processos não apenas otimiza a coleta e análise de dados, mas também reforça os mecanismos de resposta rápida frente a possíveis complicações farmacológicas.
Hole et al. (2021) apresentaram uma análise aprofundada sobre a digitalização na indústria farmacêutica, focando especialmente nos desafios do processo de implementação digital. O estudo sublinha a importância de desenvolver uma estratégia clara e bem definida para a digitalização das operações farmacêuticas. Ao detalhar essa necessidade, os autores argumentam que uma abordagem focada é essencial para maximizar os benefícios das tecnologias emergentes, facilitando assim uma transição suave para sistemas mais eficientes e inovadores que podem impulsionar significativamente a produtividade e a competitividade no setor (Hole, Glenn et al., 2021).
Por outro lado, Simon et al. (2019) exploraram a implementação de uma automação flexível através do uso de espectroscopia de RMN compacta na produção contínua de medicamentos. Este método inovador promove uma adaptabilidade substancial e uma eficiência aprimorada nos processos de fabricação, exemplificando como tecnologias específicas podem revolucionar a produção farmacêutica. O estudo destaca como essas inovações não apenas aumentam a produtividade, mas também melhoram a qualidade dos produtos farmacêuticos, demonstrando o potencial transformador dessas tecnologias no setor (Kern, Simon et al., 2019).
No estudo de Hole et al. (2021), a digitalização na indústria farmacêutica é analisada com um enfoque particular nos desafios associados ao processo de implementação digital. Este artigo ressalta a importância crítica de estabelecer uma estratégia clara e bem definida para digitalizar operações, argumentando que uma abordagem meticulosamente planejada é fundamental para aproveitar ao máximo as tecnologias emergentes. Os autores enfatizam que, ao adotar tais estratégias, as empresas farmacêuticas podem não só melhorar a eficiência operacional, mas também fortalecer sua capacidade de inovar e manter a competitividade no mercado (Hole, Glenn et al., 2021).
Simon et al. (2019) investigam a aplicação de automação flexível utilizando espectroscopia de RMN compacta na produção contínua de medicamentos. O estudo ilustra como essa abordagem proporciona uma adaptabilidade e eficiência excepcionais aos processos de fabricação, enfatizando o potencial de tais inovações tecnológicas para revolucionar a indústria farmacêutica. Os autores destacam que essa técnica não apenas melhora a produção, mas também eleva os padrões de qualidade dos produtos, demonstrando o impacto transformador da tecnologia na melhoria contínua dos processos farmacêuticos (Kern, Simon et al., 2019).
A Internet das Coisas (IoT) tem o potencial de revolucionar a eficiência operacional ao conectar equipamentos e sistemas, melhorando significativamente a monitoração de processos e a implementação de manutenção preditiva. Esse avanço tecnológico permite não apenas um acompanhamento mais preciso das operações em tempo real, mas também antecipa necessidades de manutenção antes que falhas ocorram, reduzindo tempo de inatividade e custos. Este aumento na eficiência operacional é destacado no estudo de Mishra, Sushruta et al. (2020), demonstrando como a IoT pode ser um recurso valioso na otimização contínua de processos industriais.
Ao analisar a convergência de tecnologias na indústria farmacêutica, ARDEN, N. Sarah et al. (2021) e Hole et al. (2021) apresentam perspectivas complementares e, ao mesmo tempo, contrastantes. ARDEN e colaboradores destacam o potencial das fábricas inteligentes em transformar a produção farmacêutica através da Indústria 4.0, enfatizando a customização e flexibilidade dos processos. Em contrapartida, e Hole et al. (2021) focam nos desafios da digitalização, sublinhando a necessidade de uma estratégia clara para implementação tecnológica eficaz. Ambos os estudos ressaltam a importância da inovação tecnológica, mas Hole et al. (2021) oferecem um olhar crítico sobre as barreiras práticas que podem impedir a realização dessas visões futurísticas.
Por outro lado, a comparação entre os estudos de Bhatnagar (2020) e Doulgkeroglou et al. (2020) revela uma tensão interessante entre a eficiência operacional e a qualidade do produto final. Bhatnagar (2020) argumenta vigorosamente que a automação de processos robóticos pode acelerar a produção e reduzir erros, enquanto Doulgkeroglou e colaboradores enfatizam que a automação deve também garantir a qualidade e a segurança em processos especializados de fabricação de bioprodutos. Essa dialética entre velocidade e segurança ressalta um equilíbrio delicado necessário na adoção de novas tecnologias na indústria farmacêutica.
Enquanto isso, a interseção das abordagens de Bhattamisra et al. (2023) e Simon et al. (2019) ilustra a expansão do papel da tecnologia na personalização e na inovação de processos. Bhattamisra e colaboradores destacam como a inteligência artificial pode revolucionar o desenvolvimento de terapias personalizadas através da previsão e otimização de fórmulas, enquanto Simon e equipe mostram como a automação flexível, como a espectroscopia de RMN, pode ajustar dinamicamente a produção para atender demandas variáveis. Ambos os estudos sugerem um futuro em que a personalização e a eficiência não são mutuamente exclusivas, mas sim complementares na otimização da produção farmacêutica (Bhattamisra et al., 2023; Simon et al., 2019).
Ghosh et al. (2020) e Mishra, Sushruta et al. (2020) fornecem uma visão integrada sobre como diferentes formas de automação podem reforçar a segurança e a eficácia na indústria farmacêutica. Ghosh e sua equipe discutem como a automação em farmacovigilância pode aprimorar a monitoração de eventos adversos, enquanto Mishra e colaboradores exploram como a IoT pode ser empregada para aprimorar a manutenção preditiva e a monitoração de processos. Essas abordagens, embora distintas, convergem na ideia de que a tecnologia pode e deve ser utilizada para aumentar a segurança operacional e a confiabilidade do processo produtivo.
O contraste entre os estudos de Kern et al. (2019) e todos os outros discutidos anteriormente ressalta uma faceta crucial da inovação tecnológica na indústria farmacêutica: enquanto muitos estudos focam em aspectos específicos da produção ou monitoramento, Kern e sua equipe oferecem uma visão holística da produção, propondo uma integração completa da automação para não apenas melhorar a produção, mas também elevar os padrões de qualidade dos produtos farmacêuticos. Este estudo serve como um lembrete de que, para uma verdadeira transformação na indústria farmacêutica, a integração de tecnologias deve ser abrangente e bem orquestrada (Kern, Simon et al., 2019).
5 CONCLUSÃO
A partir do objetivo proposto neste estudo, que foi descrever o impacto da automação avançada nos tempos de produção e na conformidade regulatória na indústria farmacêutica, observou-se que a implementação de tecnologias automatizadas contribui substancialmente para a redução dos tempos de produção. Este aprimoramento nos processos produtivos não só acelera a fabricação, mas também permite uma maior consistência e repetibilidade, elementos cruciais para aumentar a eficiência operacional e atender à crescente demanda do mercado.
Os dados coletados demonstram que a automação desempenha um papel fundamental na melhoria da conformidade regulatória. Com sistemas automatizados, a precisão dos processos é aprimorada, reduzindo erros humanos e assegurando que os padrões regulatórios rigorosos sejam cumpridos de forma mais eficaz. Este aspecto é particularmente importante em um setor altamente regulado como o farmacêutico, onde a aderência às normas é diretamente ligada à segurança e eficácia dos produtos.
Portanto, conclui-se que a automação na indústria farmacêutica não apenas otimiza a produção, mas também reforça o cumprimento das regulamentações, garantindo produtos de alta qualidade. A continuidade na adoção e evolução das tecnologias de automação é essencial para sustentar esses benefícios e continuar a impulsionar inovações que respondam às necessidades tanto dos consumidores quanto das autoridades regulatórias.
REFERÊNCIAS
AL-AMIN, Md et al. History, Features, Challenges, and Critical Success Factors of Enterprise Resource Planning (ERP) in The Era of Industry 4.0. European Scientific Journal, ESJ, v. 19, n. 6, p. 31, 2023.
ARDEN, N. Sarah et al. Industry 4.0 for pharmaceutical manufacturing: Preparing for the smart factories of the future. International Journal of Pharmaceutics, v. 602, p. 120554, 2021.
ARDEN, Sarah et al. Industry 4.0 for pharmaceutical manufacturing: Preparing for the smart factories of the future. International Journal of Pharmaceutics, v. 602, p. 120554, 2021.
BACH, Ina. Practical Guide for Microbiological QA/QC of Non‐sterile Pharmaceuticals Manufacturing for EU. Pharmaceutical Microbiological Quality Assurance and Control: Practical Guide for Non‐Sterile Manufacturing, p. 505-518, 2019.
BHATNAGAR, Nitu. Role of robotic process automation in pharmaceutical industries. In: The International Conference on Advanced Machine Learning Technologies and Applications (AMLTA2019) 4. Springer International Publishing, 2020. p. 497-504.
BHATNAGAR, Nitu. Role of robotic process automation in pharmaceutical industries. In: The International Conference on Advanced Machine Learning Technologies and Applications (AMLTA2019) 4. Springer International Publishing, 2020. p. 497-504.
BHATTAMISRA, Subrat Kumar et al. Artificial intelligence in pharmaceutical and healthcare research. Big Data and Cognitive Computing, v. 7, n. 1, p. 10, 2023.
BOGDAN, Andrew R.; DOMBROWSKI, Amanda W. Emerging trends in flow chemistry and applications to the pharmaceutical industry. Journal of medicinal chemistry, v. 62, n. 14, p. 6422-6468, 2019.
COITO, Tiago et al. A middleware platform for intelligent automation: An industrial prototype implementation. Computers in industry, v. 123, p. 103329, 2020.
COLOMBO, Stefano. Applications of artificial intelligence in drug delivery and pharmaceutical development. In: Artificial intelligence in healthcare. Academic Press, 2020. p. 85-116.
DOULGKEROGLOU, Meletios-Nikolaos et al. Automation, monitoring, and standardization of cell product manufacturing. Frontiers in Bioengineering and Biotechnology, v. 8, p. 811, 2020.
GHOSH, Rajesh et al. Automation opportunities in pharmacovigilance: an industry survey. Pharmaceutical Medicine, v. 34, p. 7-18, 2020.
GOHAR, Ali; NENCIONI, Gianfranco. The role of 5G technologies in a smart city: The case for intelligent transportation system. Sustainability, v. 13, n. 9, p. 5188, 2021.
HOLE, Glenn; HOLE, Anastasia S.; MCFALONE-SHAW, Ian. Digitalization in pharmaceutical industry: What to focus on under the digital implementation process?. International Journal of Pharmaceutics: X, v. 3, p. 100095, 2021.
HOLE, Glenn; HOLE, Anastasia S.; MCFALONE-SHAW, Ian. Digitalization in pharmaceutical industry: What to focus on under the digital implementation process?. International Journal of Pharmaceutics: X, v. 3, p. 100095, 2021.
HOSSAIN, Tanjim et al. History, Features, Challenges and Critical Success Factors of ERP in the ERA of Industry 4.0. ESI Preprints, v. 12, p. 493-493, 2022.
JAVAID, Mohd et al. Significance of sensors for industry 4.0: Roles, capabilities, and applications. Sensors International, v. 2, p. 100110, 2021.
JAVAID, Mohd; HALEEM, Abid. Industry 4.0 applications in medical field: A brief review. Current Medicine Research and Practice, v. 9, n. 3, p. 102-109, 2019.
KERN, Simon et al. Flexible automation with compact NMR spectroscopy for continuous production of pharmaceuticals. Analytical and bioanalytical chemistry, v. 411, p. 3037-3046, 2019.
KERN, Simon et al. Flexible automation with compact NMR spectroscopy for continuous production of pharmaceuticals. Analytical and bioanalytical chemistry, v. 411, p. 3037-3046, 2019.
KLOSE, Anselm et al. Orchestration requirements for modular process plants in chemical and pharmaceutical industries. Chemical Engineering & Technology, v. 42, n. 11, p. 2282-2291, 2019.
KOLLURI, Sheela et al. Machine learning and artificial intelligence in pharmaceutical research and development: a review. The AAPS journal, v. 24, p. 1-10, 2022.
KOROMINA, Maria; PANDI, Maria-Theodora; PATRINOS, George P. Rethinking drug repositioning and development with artificial intelligence, machine learning, and omics. Omics: a journal of integrative biology, v. 23, n. 11, p. 539-548, 2019.
LIMA, Faíque Ribeiro; GOMES, Rogério. Conceitos e tecnologias da Indústria 4.0: uma análise bibliométrica. Revista Brasileira de Inovação, v. 19, p. e0200023, 2021.
MAK, Kit-Kay; WONG, Yi-Hang; PICHIKA, Mallikarjuna Rao. Artificial intelligence in drug discovery and development. Drug Discovery and Evaluation: Safety and Pharmacokinetic Assays, p. 1-38, 2023.
MAK, Kit-Kay; WONG, Yi-Hang; PICHIKA, Mallikarjuna Rao. Artificial intelligence in drug discovery and development. Drug Discovery and Evaluation: Safety and Pharmacokinetic Assays, p. 1-38, 2023.
MIRMOZAFFARI, Mirpouya et al. An integrated artificial intelligence model for efficiency assessment in pharmaceutical companies during the COVID-19 pandemic. Sustainable Operations and Computers, v. 3, p. 156-167, 2022.
MISHRA, Sushruta; DASH, Anuttam; MISHRA, Brojo Kishore. An insight of Internet of Things applications in pharmaceutical domain. In: Emergence of pharmaceutical industry growth with industrial IoT approach. Academic Press, 2020. p. 245-273.
NAMEKAR, Swapnil Arun; YADAV, Rishabh. Programmable Logic Controller (PLC) and its applications. International Journal of Innovative Research in TechnologY (IJIRT), v. 6, n. 11, p. 372-376, 2020.
PATEL, Veer; SHAH, Manan. Artificial intelligence and machine learning in drug discovery and development. Intelligent Medicine, v. 2, n. 3, p. 134-140, 2022.
RANEBENNUR, Raksha et al. Development of Automated Quality Assurance Systems for Pharmaceutical Manufacturing: A Review. Journal of Coastal Life Medicine, v. 11, p. 1855-1864, 2023.
SILVA, Adriano R. et al. Estudos da Implementação da Técnica de Gerenciamento OEE em uma Indústria Farmacêutica. Revista Processos Químicos, v. 14, n. 28, p. 221-231, 2020.
SILVA, Felipe; RESENDE, David; AMORIM, Marlene. Um estudo sobre a aplicação dos conceitos e elementos da indústria 4.0 na produção de biomedicamentos. Revista Produção Online, v. 20, n. 2, p. 493-520, 2020.
SOLFA, Federico Del Giorgio. Impacts of cyber security and supply chain risk on digital operations: evidence from the pharmaceutical industry. International Journal of Technology, Innovation and Management (IJTIM), v. 2, n. 2, p. 18-32, 2022.
TARASOV, Oleksandr et al. Development of Integrated CAD/CAE Systems Based on Parameterization of the Simulated Process. In: Conference on Integrated Computer Technologies in Mechanical Engineering–Synergetic Engineering. Cham: Springer Nature Switzerland, 2022. p. 679-691.
VORA, Lalitkumar K. et al. Artificial intelligence in pharmaceutical technology and drug delivery design. Pharmaceutics, v. 15, n. 7, p. 1916, 2023.
ZHANG, Mu et al. Towards automated safety vetting of plc code in real-world plants. In: 2019 IEEE Symposium on Security and Privacy (SP). IEEE, 2019. p. 522-538.
1Discente do Curso Superior de xxxxxxxxxxxxxxxxx do Instituto xxxxxxxxxxxxxxx Campus xxxxxx e-mail: nome@provedor.com.br
2Docente do Curso Superior de xxxxxxxxxxxxx do Instituto xxxxxxxxx Campus xxxxxxxxxxx. Mestre em xxxxx (PPGMAD/UNIR). e-mail: nome@provedor.com.br
3Docente do Curso Superior de Tecnologia em Automação Industrial da FATEC SENAI Roberto Mange – Anápolis/Goiás. Eng. de Controle e Automação (UNIP). Especialista em Engenharia de Produção (UEG). e-mail: marcidishc.senai@fieg.com.br
4Docente do Curso Superior de Tecnologia em Automação Industrial da FATEC SENAI Roberto Mange – Anápolis/Goiás. Eng. de Controle e Automação (UNIP). Especialista em Engenharia de Produção (UEG). Mestre em Engenharia Agrícola (PPGEA-UEG). Doutorando em Ciências Ambientais (PPGSTMA – UniEVANGÉLICA. e-mail: marciodias.senai@fieg.com.br.
