Analysis of the Market Complaint Flow in the Pharmaceutical Industry
REGISTRO DOI: 10.5281/zenodo.10201281
Wallace Barbosa dos Santos1
Leandro Giorgetti2
Resumo
As reclamações de mercado são notificações de defeito apresentado por algum produto, pós comercialização e quando já em posse do consumidor final. As indústrias farmacêuticas devem estar cientes de que a correta tratativa do fluxo de reclamações de mercado pode promover a qualidade e gerar um aumento significativo da confiança e satisfação dos consumidores com relação aos seus produtos. Para isto, a adoção de medidas como estabelecer um fluxo de recebimento destas notificações, o seguimento das ferramentas do Sistema de Gestão da Qualidade para investigação de Não Conformidades assim como para proposição e execução de ações CAPA, verificação contínua e indicadores de qualidade, e análise de tendência devem ser tomadas. Estas ações, quando em conformidade com as legislações vigentes e seguidas através de um plano de ação pré-determinado por procedimentos operacionais internos, pode garantir a mitigação de riscos de recall de produtos e a extensão de defeitos que gerem novos registros de reclamações.
Palavras-chave: Reclamações de mercado. Sistema de Gestão da Qualidade. Indicadores. Indústria farmacêutica. Não Conformidades.
Abstract
Market complaints are notifications of defects presented by a product, after marketing and when already in the possession of the final consumer. Pharmaceutical companies must be aware that the correct handling of the flow of market complaints can promote quality and generate a significant increase in consumer confidence and satisfaction with their products. To this end, the adoption of measures such as establishing a flow of receipt of these notifications, the monitoring of the tools of the Quality Management System for the investigation of Non-Conformities as well as for the proposition and execution of CAPA actions, continuous verification and quality indicators, and trend analysis must be taken. These actions, when in compliance with current legislation and followed through an action plan predetermined by internal operating procedures, can ensure the mitigation of product recall risks and the extent of defects that generate new records of complaints.
Keywords: Market complaints. Quality Management System. Indicators. Pharmaceutical industry. Non-conformities.
1 INTRODUÇÃO
No contexto da indústria farmacêutica, o processo de fabricação de medicamentos deve ser feito com base nas normas de Boas Práticas de Fabricação, estabelecidas pela agência regulatória, e garantidas pela Garantia da Qualidade. O cumprimento das normas de Boas Práticas de Fabricação, e consequentemente o padrão de qualidade, deve estar diretamente relacionado com a baixa frequência de desvios ocorridos durante e após o processo de fabricação (Braga, 2007).
Reclamações de Mercado são notificações de defeito apresentados por algum produto, quando este já em posse do consumidor. O setor da Garantia da Qualidade é responsável por registrar e investigar essas ocorrências buscando a melhoria contínua do processo de fabricação, aplicando ferramentas de ação corretiva e preventiva (CAPA), para que não haja reincidências nos próximos lotes fabricados.
Levando em consideração a alta competitividade das indústrias e o aumento de demanda na produção de medicamentos, eleva-se os riscos inerentes ao processo, fazendo-se necessário uma análise da utilização das ferramentas de qualidade para resolução de problemas ligados a desvios potencialmente geradores de reclamações de mercado e recall de produtos. O sistema da qualidade, parte da Garantia da Qualidade, deve ser fundamental como mecanismo de promover e garantir a qualidade do produto fabricado, visando a diminuição de potenciais riscos levados ao consumidor, monitorando os índices de reclamações e desvios através de KPIs (Key Performance Indicators) (Veluchuri, Adhikari & Indukuri, 2020).
Dito isso, o objetivo desta revisão literária é analisar os métodos e ferramentas do Sistema de Gestão da Qualidade aplicados à tratativa de Reclamações de Mercado em indústrias farmacêuticas para minimizar a incidência de registros de reclamações que apresentem impacto na qualidade do produto fabricado e/ou distribuído.
2 METODOLOGIA
Foi realizada uma revisão de literatura sobre Reclamações de Mercado e Garantia da Qualidade com a base de dados do Google Scholar e Scielo. Para encontrar os artigos que melhor correspondiam ao tema pesquisado, foram utilizados os seguintes termos em inglês: Market Complaints, Quality Management System, Quality Assurance, Deviations, Key Performance Indicators. Quando a pesquisa foi realizada em português os mesmos termos foram apenas traduzidos.
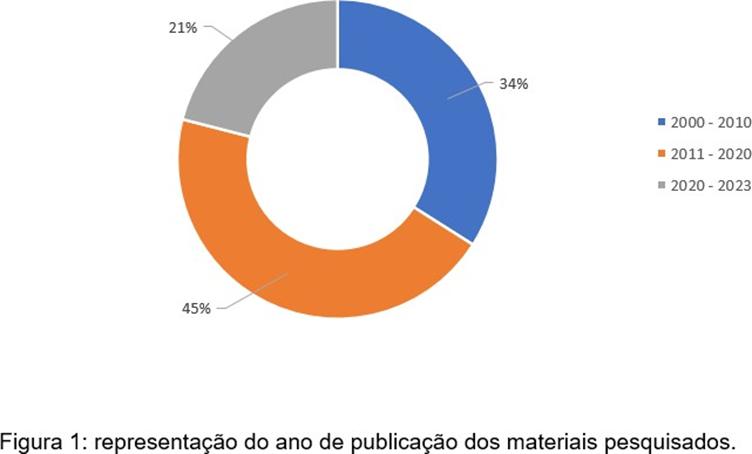
Os critérios para a seleção dos artigos encontrados nessa revisão foram, em ordem: textos escritos em inglês que continham definições de termos ligados a Reclamações de Mercado e Sistema de Gestão da Qualidade, e dados relacionados ao fluxo de tratativa de Reclamações de Mercado na indústria farmacêutica. Quando as informações pesquisadas não foram encontradas em artigos em inglês os mesmos termos foram pesquisados em português. No total, foram analisados 10 materiais, utilizados como fonte para esta revisão, e os respectivos anos de publicação constam no gráfico a seguir:
Ano de Publicação dos Materiais-Fonte
3 RESULTADOS E DISCUSSÕES OU ANÁLISE DOS DADOS
3.1 Fluxo Correto de Reclamações de Mercado
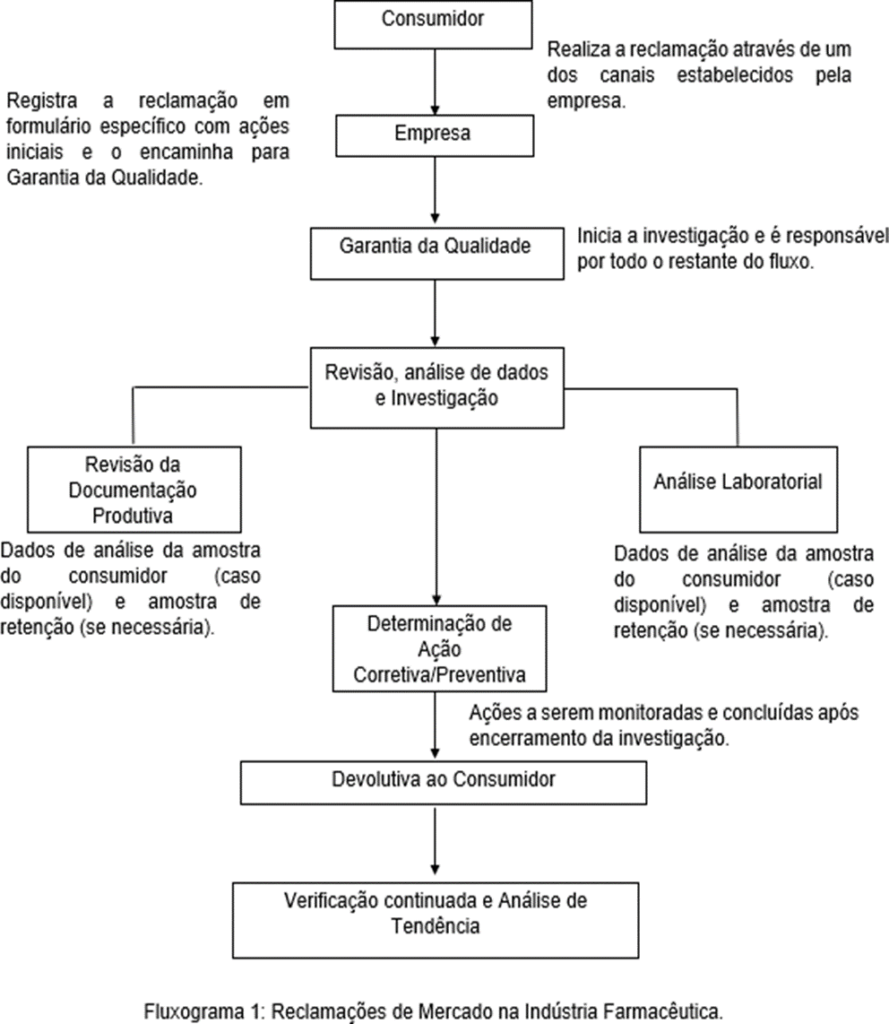
3.1.1 Recebimento de Reclamações
A indústria deve estabelecer um canal de comunicação com o consumidor afim de receber suas sugestões, dúvidas e reclamações relacionadas aos produtos fabricados e/ou comercializados. Através dos canais, as reclamações devem ser encaminhadas para Garantia da Qualidade, que é responsável por analisar, investigar, e se necessário, propor ações frente aos defeitos reclamados (Braga, 2007).
As reclamações, previamente ao envio para Garantia da Qualidade, devem ser registradas em formulário que contenha informações básicas sobre o reclamante, como: nome, endereço e contato. Além destas, devem ser registradas informações acerca do produto, como: nome do produto, número do lote, data de validade e fabricação, descrição em detalhes da reclamação e demais informações que sejam julgadas necessárias (Shashikant, Gurmeet & Nayan, 2018).
3.1.2 Investigação de Reclamações
Segundo a norma Resolução da Diretoria Colegiada da ANVISA nº 658 de 30 de março de 2022, em seu artigo 328 ressalta que “todas as reclamações devem ser documentadas e avaliadas visando a identificação se representam um possível desvio de qualidade ou outro problema”, e este papel cabe à Garantia da Qualidade (ANVISA, 2022).
O uso de um sistema de gerenciamento adequado deve garantir que os registros sejam avaliados e que ações corretivas e preventivas (CAPA) apropriadas sejam propostas e executadas para eliminar a causa raiz identificada. O Sistema de Gestão da Qualidade é importante para ajudar a melhorar a qualidade do produto e processos, inclusive de reclamações de mercado, para alcançar, consequentemente, maior satisfação dos consumidores (Boltic et al., 2010).
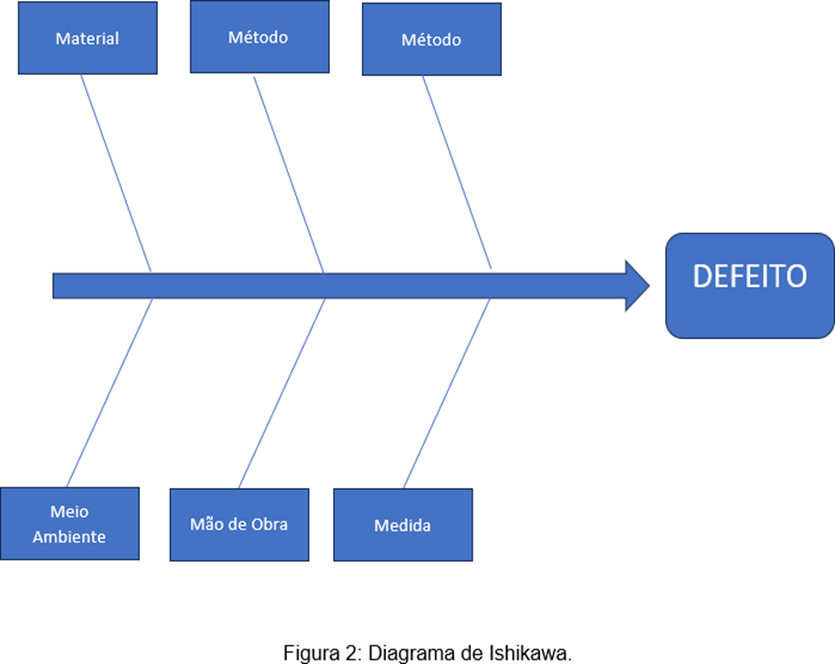
A investigação de registros deve seguir os conceitos e ferramentas de qualidade, como diagrama de Ishikawa. Este é apenas um exemplo de método que visa a análise e solução dos problemas reportados em reclamações de mercado.
A ferramenta diagrama de Ishikawa deve ser utilizada de forma a separar as possíveis causas do problema reportado, dividindo-as em 6 categorias: Máquina, Mão de Obra, Método, Medida, Meio Ambiente e Material. Com essa divisão, uma análise holística deve ser realizada relacionando os itens citados a seus possíveis impactos como causadores do defeito reclamado.
Para investigação de desvios e possíveis não conformidades é indispensável o uso de ferramentas de qualidade, como diagrama de Ishikawa. Estas ferramentas permitem organizar, distribuir e analisar dados de forma a obter a melhor interpretação destes, resultando em uma conclusão mais precisa da reclamação (Amorim & Garcia-Amoedo, 2021).
Associado ao uso de ferramentas de qualidade, para a investigação de registros de reclamações de mercado deve-se utilizar da verificação da documentação produtiva do lote reclamado (em busca de possíveis não conformidades geradas durante o processo de fabricação/armazenamento/distribuição do lote) e análise laboratorial da amostra do consumidor ou de retenção (se disponível/se necessária) para verificar a conformidade do processo, sob responsabilidade da empresa, e da unidade reclamada pelo consumidor.
Ao concluir a investigação, com dados obtidos através da utilização de uma ou mais ferramentas da qualidade, análise da documentação produtiva e amostras do consumidor e/ou de retenção, a reclamação deve ser classificada de uma das seguintes possibilidades:
Reclamação confirmada: quando a ferramenta da qualidade ou análise da documentação produtiva ressaltam uma fragilidade do processo que possa ocasionar o defeito reclamado, ou quando se obtém da análise da amostra um resultado OOS (resultado fora de especificação).
Reclamação não confirmada: quando a ferramenta da qualidade ou análise da documentação produtiva não ressaltam qualquer sinal de fragilidade do processo que possa resultar no defeito reclamado, quando a análise da amostra não resulta em dados Out-Of- Specification. Entretanto, em casos que se obtém da análise da amostra do consumidor um resultado OOS, mas que este resultado é claramente proveniente de uma má utilização/armazenamento do produto pelo consumidor, o registro também deve ser classificado com reclamação não confirmada. Para estes casos, deve-se avaliar a gravidade do defeito reclamado, se representa um risco grave à saúde dos consumidores, e se, portanto, é necessário seguir com o processo de recall (recolhimento) do lote afetado (Braga, 2007).
Reclamação suspeita de falsificação: quando a amostra apresenta indícios de falsificação/violação. Por exemplo: quando uma substância estranha é adicionada ao produto, mudando suas características físico-químicas. Reclamações relacionadas à suspeita de falsificação devem ser tratadas com atenção especial. Ao confirmar a relação de uma reclamação a uma falsificação, a unidade jurídica da empresa e as autoridades competentes devem ser notificadas (Shashikant, Gurmeet & Nayan, 2018).
3.1.3 Ações Corretiva-Preventiva (CAPA Plan)
Plano CAPA representa uma melhoria do processo utilizado para sanar a ocorrência investigada, agindo como ação corretiva, ou mitigar e eliminar o risco de extensão e novos casos envolvendo o defeito investigado na reclamação, agindo como ação preventiva (Shashikant, Gurmeet & Nayan, 2018).
Toda reclamação classificada como confirmada, de preferência, exige a implementação de um plano CAPA. Uma ação apropriada deve ser proposta a depender da natureza da reclamação e se houve a identificação de uma tendência durante a investigação, e neste caso, as ações propostas devem ser avaliadas por uma equipe multidisciplinar afim de determinar a necessidade de aplicação da ação a mais de um lote.
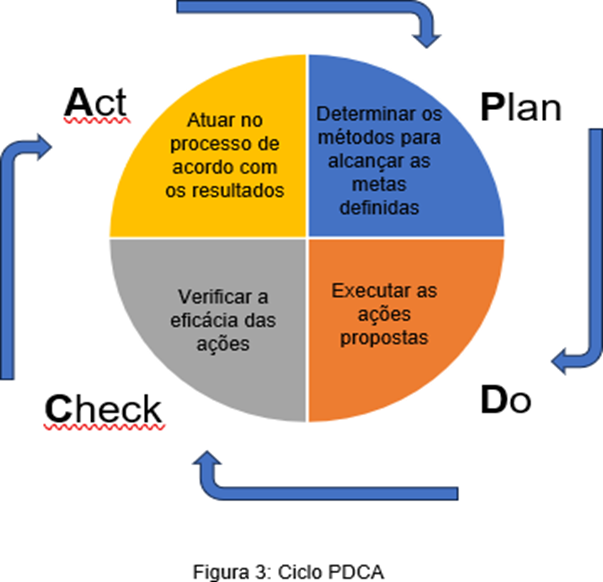
O ciclo PDCA é uma importante ferramenta da qualidade para implementação do plano CAPA pois tem como premissa o planejamento (to plan), a execução (to do), a verificação (to check) e a ação (to act). Essas ações, nesta ordem, garantem que sejam tomadas medidas adequadas que visem a melhoria do processo e a mitigação de riscos de qualidade a um ou mais lotes alvo do plano ação estabelecido (Ishnia, Purba & Debora, 2020).
3.1.4 Devolutiva ao Consumidor
Ao término e classificação da reclamação, o consumidor deve receber uma devolutiva que retrate os métodos de conclusão do registro de reclamação e o resultado da investigação, assim como as implicações do defeito caso a reclamação apresente uma confirmação do defeito reclamado. Para casos de reclamações não confirmadas que representem um defeito originado pela má utilização do produto, a empresa deve notificar o cliente de forma a orientá-lo sobre o correto manuseio e utilização do produto para que se mitigue a incidência de reclamações futuras relacionadas ao defeito reclamado, mesmo que não seja necessária qualquer tomada de ação interna, como implementação de plano CAPA. Com relação a reclamações que envolvem falsificação/violação, o cliente deve ser notificado assim como ocorre a notificação para casos de reclamações confirmadas, porém o departamento de Assuntos Jurídicos deve também receber a notificação para que este possa avaliar a necessidade de tomada de ações legais.
Para todos os casos, em especial para aqueles em que o consumidor forneceu sua amostra para análise e investigação, é recomendado que a empresa forneça uma unidade do produto de forma gratuita como forma de suprir a ausência do produto durante a tratativa da reclamação. Esta ação pode contribuir para um marketing positivo, estabelecer confiança com os clientes e, consequentemente, elevar o nível de satisfação dos consumidores (Braga, 2007).
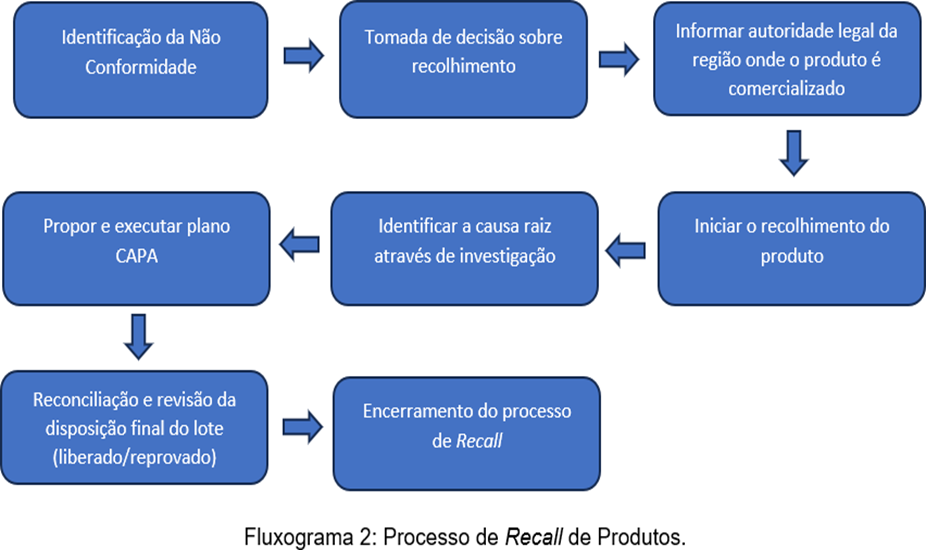
3.1.5 Recall de Produtos
Um recall significa o recolhimento de todo ou parte de um lote disponível no mercado após constatação de que este pode estar em inconformidade com as legislações vigentes no país em que é comercializado ou se este pode implicar em agravos à saúde dos consumidores. Para que seja realizado um recolhimento, deve-se avaliar a gravidade do defeito encontrado e seu potencial risco à integridade dos clientes. Os recalls estão frequentemente associados às investigações de reclamações de mercado, que evidenciam reações adversas à saúde ou falhas de produção que resultam em unidades fabricadas que não cumprem com os requisitos legais, como falha de rotulagem por exemplo (Veluchuri, Adhikari & Indukuri, 2020).
Os recolhimentos são classificados em 3 tipos:
Classe I de recall: situação em que a exposição ao produto pode, razoavelmente, ocasionar em uma reação adversa grave ou agravos à condição clínica do consumidor, incluindo seu falecimento.
Classe II de recall: situação em que a probabilidade de reações adversas oriundas da utilização do produto recolhido pode ser controlada, e que estas reações representam efeitos temporários ou clinicamente reversíveis.
Classe III de recall: situação em que a utilização do produto recolhido não causa reações adversas perceptíveis (Shashikant, Gurmeet & Nayan, 2018).
Independentemente da classe do recall, uma estratégia pré-definida deve ser estabelecida para garantir que toda a parcela defeituosa seja recolhida, de forma a evitar a extensão dos defeitos e reclamações reportadas. Esta estratégia deve garantir que o produto seja recolhido a nível de consumidor e varejo. Para isto, deve-se utilizar de ferramentas de comunicação massiva, como noticiários e imprensa especializada, e informações médico- científicas, como repasse da notificação por meio de médicos e profissionais da saúde (Veluchuri, Adhikari & Indukuri, 2020).
3.1.6 Verificação Continuada e KPIs para Reclamações
Os KPIs (Indicadores Chave de Performance) em indústrias farmacêuticas são utilizados de forma a avaliar o desempenho da empresa e monitorar a qualidade de seus produtos. Estes KPIs são definidos através de indicadores que retratam as estatísticas “em tempo real” dos valores envolvidos no processo de tratativa de reclamações de mercado (Staron et al., 2016).
Os indicadores podem ser classificados nos seguintes tipos:
Indicadores estratégicos: indicam o desempenho dos dados relacionados a meta de qualidade proposta.
Indicadores de eficiência: indicam a relação entre o resultado de qualidade obtido e o gasto necessário.
Indicadores de eficácia: indicam o nível de qualidade relacionado a satisfação dos consumidores com seus produtos.
Indicadores de impacto: indicam as consequências das ações tomadas para que se resulte na qualidade determinada.
Indicadores de capacidade: indicam a capacidade de um processo relacionado às saídas produzidas por unidade de tempo (Palmeira, 2014).
Portanto, os KPIs permitem verificar as ações tomadas pelo fluxo de tratativa de reclamações de mercado, sua eficácia, eficiência e a satisfação dos consumidores alcançada (Staron et al., 2016).
3.1.7 Análise de Tendência de Reclamações de Mercado
Periodicamente, relatórios devem ser elaborados para avaliar as ações propostas em cada investigação de reclamação e para determinar se há uma tendência de defeitos que podem representar sinais de falhas em processos da empresa.
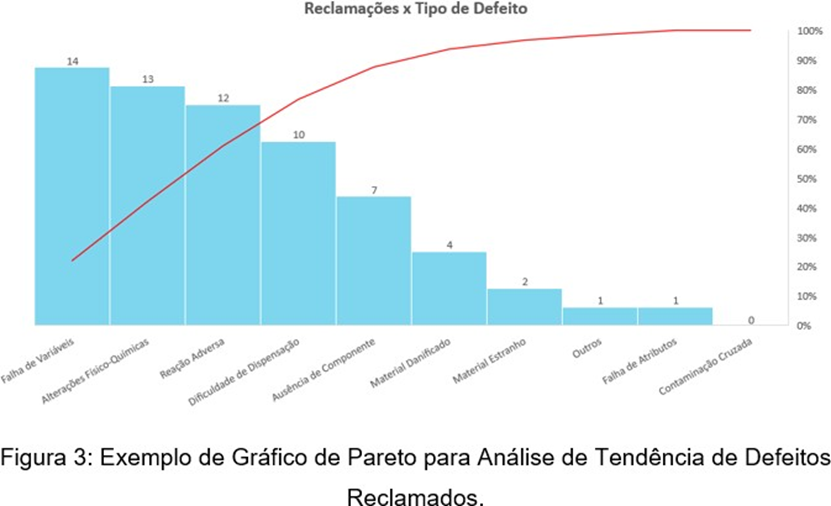
O conteúdo dos relatórios deve conter informações relacionadas a quantidade de reclamações recebidas em determinado período pré-estabelecido, quantos casos foram classificados como confirmados e quantos representam suspeitas de falsificação/violação, os principais produtos alvos de reclamações e as principais causas das reclamações classificadas de acordo com a ferramenta da qualidade utilizada na investigação de cada um dos registros. Para elaboração dos relatórios é recomendado o uso de gráficos, de barra simples ou de linha de Pareto, que demonstram visualmente as informações necessárias para identificação de tendências (Palmeira, 2014).
4 CONCLUSÃO/CONSIDERAÇÕES FINAIS
Esta revisão bibliográfica sobre o fluxo de reclamações de mercado na indústria farmacêutica ressalta que há uma forma correta de realizar as devidas tratativas a respeito de queixas dos clientes.
O fluxo correto, evidenciado ao longo desta revisão, pode contribuir com uma melhor promoção da qualidade dos produtos comercializados, diminuindo a frequência de desvios pós liberação dos lotes e, consequentemente, o alcance da confiança e satisfação dos consumidores.
REFERÊNCIAS
BRAGA, Glaucia. Complaint Handling in Pharmaceutical Companies. The Quality Assurance Journal, volume 11, issue 1. 2007.
VELUCHURI, ADHIKARI & INDUKURI. An Overview on Pharmaceutical Drug Recalls. The Pharmaceutical and Chemical Journal, 7(1):16-22. 2020.
SHASHIKANT, GURMEET & NAYAN. Handling of Market Complaints and Recalls, Revi- ew of FDA-483 FORM. Asian Journal of Pharmaceutical, Research and Development, 6 (3):55-59. 2018.
BRASIL. Resolução RDC 658 de 30 de março de 2022, que dispões sobre as diretrizes de Boas Práticas de Fabricação de Medicamentos. 2022.
BOLTIC et. al. Measuring the performance of quality assurance processes: pharmaceutical industry deviation management case study. Accreditation Quality Assurance (2010) 15:629–636. 2010.
PFEIFER et al. Integrating six sigma with quality management systems. The TQM Magazi- ne, volume 16, number 4, 2004, 241-249. 2004.
AMORIM & GARCIA-AMOEDO. Aplicação de Ferramentas da Qualidade em um desvio de qualidade na indústria farmacêutica: um estudo de caso. Infarma, Ciências Farmacêuticas, volume 33, 345-351. 2021.
PALMEIRA, Aline. Ferramentas de Qualidade no Gerenciamento de Reclamações de Merca- do na Indústria Farmacêutica. Acta de Ciências e Saúde, Número 03 Volume 02, 109-131. 2014.
ISNIAH, PURBA & DEBORA. Plan do check action (PDCA) method: literature review and research issues. Jurnal Sistem dan Manajemen Industri, volume 4, number 1, 72-81. 2020.
STARON et. al. A Key Performance Indicator Quality Model and Its Industrial Evaluation. Joint Conference of the International Workshop on Software Measurement and the In- ternational Conference on Software Process and Product Measurement, 170-179. 2016.
Wallace Barbosa dos Santos – Discente do Curso Superior de Farmácia da Escola de Ciências da Saúde, da Universidade Anhembi-Morumbi Campus Centro-Mooca1
Leandro Giorgetti – Docente do Curso Superior de Farmácia do da Escola de Ciências da Saúde, da Universidade Anhembi- Morumbi Campus Centro-Mooca. Mestre em Fármacos e Medicamentos (FCF/USP)2
