COMPARATIVE ANALYSIS OF PH INCREASE IN ROOT CANALS OF THREE BRANDS OF CALCIUM HYDROXIDE USED IN BRAZILIAN ENDODONTICS
REGISTRO DOI: 10.69849/revistaft/th10249051509
Pedro Foeppel Meireles1
Antônio Henrique Braitt2
Kaique Richard Cabral1
Larisse Andrade Veloso1
Leandro Machado Silva Souza1
RESUMO
Introdução: O hidróxido de cálcio desempenha importante papel em diversas áreas da odontologia, sendo encontrado em formato de pasta, onde são utilizadas e misturadas duas diferentes pastas, ou em formato de pó. Na endodontia, este material pode ser utilizado para proteção do complexo dentina-polpa, utilizando o seu formato pasta-pasta; aplicação direta na polpa, em formato de pó, na tentativa de gerar dentina reparadora, evitando assim a realização do tratamento endodôntico; como também para medicação intracanal, na intenção de eliminar as bactérias presente no conduto radicular. Quando o paciente apresenta alguma lesão de cárie extensa, onde a destruição chegou à polpa dentária, é necessário que seja feito o tratamento endodôntico. Entretanto, as bactérias presentes na doença cárie podem trazer severas infecções, sendo necessário um material capaz de eliminar todos microrganismos do canal radicular. Para que essa desinfecção ocorra, o hidróxido de cálcio precisa apresentar um pH alcalinizado, pois quando o pH do meio está alto, as atividades bacterianas são inibidas. Objetivo: O objetivo deste trabalho é avaliar as marcas encontradas no mercado brasileiro da endodontia que apresentam um pH adequado, ou seja, alcalinizado, para exercer atividade antibacteriana. Conclusão: Com este trabalho espera-se avaliar quais marcas de hidróxido de cálcio apresentam melhor alcalinização, para assim, auxiliar no momento da escolha de compra para utilização durante um tratamento endodôntico.
Palavras Chaves: Endodontia; Hidróxido de Cálcio; Tratamento Endodôntico
ABSTRACT
Introduction: Calcium hydroxide plays an important role in several areas of dentistry, being found in paste format, where two different pastes are used and mixed, or in powder format. In endodontics, this material can be used to protect the dentin-pulp complex, using its paste-paste format; direct application in the pulp, in powder format, in an attempt to generate repairing dentin, thus avoiding the performance of endodontic treatment; as well as for intracanal medication, with the intention of eliminating the bacteria present in the root canal. When the patient has an extensive caries lesion, where the destruction has reached the dental pulp, it is necessary to carry out endodontic treatment. However, the bacteria present in caries disease can bring severe infections, requiring a material capable of eliminating all microorganisms from the root canal. For this disinfection to occur, calcium hydroxide needs to have an alkalized pH, because when the pH of the medium is high, bacterial activities are inhibited. Goal: The objective of this study is to evaluate the brands found in the Brazilian endodontics market that have an adequate pH, that is, alkalized, to exert antibacterial activity. Conclusion: With this work, it is expected to evaluate which brands of calcium hydroxide present better alkalinization, in order to assist in the choice of purchase for use during endodontic treatment.
Key Words: Endodontics, Calcium Hydroxide, Endodontic Treatment.
INTRODUÇÃO:
O hidróxido de cálcio foi introduzido na Odontologia pelo alemão Bernhard W. Hermann (Würzburg) em 19201, com uma Tese de doutorado em Ciências Naturais.
Entretanto coube a Rhoner, em 1940, o primeiro trabalho histológico em dentes humanos que demonstrou, após pulpotomia e obturação dos canais com Calxyl, a formação de barreira mineralizada no ápice radicular2.
Durante muitos anos o Calxyl (pasta de hidróxido de cálcio) não encontrou o necessário reconhecimento na Alemanha. Entretanto, resultados promissores foram obtidos em clínicas universitárias de outros países, como na Suíça, fundamentados por investigações científicas.
Holland, no Brasil, estudou e posteriormente descreveu em sua tese de doutorado o mecanismo de ação biológica do hidróxido de cálcio em tecido conjuntivo (polpas dentais de cães)3. Em 1994 e 1995 Estrela et al4,5 discutiram o provável mecanismo de ação dessa substância sobre os microrganismos.
Estrela6 acredita que seu representativo destaque, entre os fármacos endodônticos, expressa-se devido a importantes propriedades, entre as quais a inibição de enzimas bacterianas a partir da ação em nível de membrana citoplasmática, a qual conduz ao efeito antimicrobiano e a ativação enzimática tecidual, que motiva o efeito mineralizador, observada a partir de sua ação sobre a fosfatase alcalina
O hidróxido de cálcio nada mais é do que a cal hidratada, altamente utilizada na construção civil7,8. Ele é composto pela ligação entre um cátion de cálcio e dois ânions de hidróxido, com um pH 12,6, pouco solúvel em água obtida a partir da calcinação (aquecimento) do carbonato de cálcio, até sua transformação em óxido de cálcio (Cal viva). Com a hidratação do óxido de cálcio chega-se ao hidróxido de cálcio. A reação entre este e o gás carbônico leva à formação do carbonato de cálcio. Assim, sua fórmula química é conhecida como Ca(OH)2.
REVISÃO DA LITERATURA:
Shetty et al9 estudaram a variação de pH no meio circundante após o uso de dois veículos diferentes de hidróxido de cálcio – solução salina (aquoso), propilenoglicol (viscoso) e hidróxido de cálcio contendo pontos de guta percha durante um período de 7 dias como medicamento intracanal. Em sessenta pré-molares de raízes únicas foram removidas as coroas na junção cemento-esmalte, limpos e modelados até a lima #40, divididos aleatoriamente em 4 grupos. Um controle e três experimentais. No grupo controle I os canais radiculares foram deixados vazios. Nos grupos experimentais – o grupo II foi preenchido com Ca(OH)2 + solução salina, o grupo III foi preenchido com Ca(OH)2 + propilenoglicol e o grupo IV os canais radiculares foram preenchidos com pontos de hidróxido de cálcio. Os acessos coronais foram selados com 3mm de Cavit G e todas as superfícies da raiz foram cobertas com 3 demãos em verniz ungueal. As amostras foram então colocadas em frascos herméticos contendo 2ml de água destilada. Os frascos foram mantidos em estufa e o pH do meio circundante foi medido com um pHmetro digital após 1,3,5 e 7 dias, respectivamente. Houve diferença estatisticamente significante (p<0,05) entre os grupos experimentais durante o período de observação. No dia 1, um pH elevado foi registrado pelos grupos de hidróxido de cálcio e salina e um pH mais baixo pelo grupo propileno. Nos dias 3 e 5, o pH máximo foi registrado pelo grupo propilenoglicol e o mínimo pelos pontos hidróxido de cálcio e grupos salina. No 7º dia, o pH de todos os grupos havia caído, com o propilenoglicol registrando o pH máximo, seguido pelos pontos salina e, por último, hidróxido de cálcio. Dentro das limitações deste estudo, concluíram que um veículo viscoso é melhor entre outros veículos, a pasta de hidróxido de cálcio de propilenoglicol proporcionou a maior liberação de 7 dias de íons hidroxila.
Ferreira et al10 analisaram o aumento do pH na superfície radicular externa após o uso de diferentes pastas de hidróxido de cálcio (Calen, hidróxido de cálcio associado à clorexidina gel a 2%, hidróxido de cálcio associado à solução salina) com e sem EDTA como agente quelante antes da aplicação tópica da medicação intracanal. Cem dentes extraídos de raiz única foram limpos e modelados. Eles foram divididos aleatoriamente em seis grupos experimentais (n = 15) e um grupo controle (n = 10), de acordo com a medicação a ser utilizada. Os dentes foram mantidos imersos em solução salina e as medidas de pH foram verificadas semanalmente com o auxílio de um pHmetro. Verificou-se o aumento do pH na primeira semana em quase todos os grupos. Apenas os grupos em que Ca(OH)2 foi associado ao gel de clorexidina a 2% apresentaram evolução significativa no aumento do pH ao longo do tempo (p = 0,0116). O uso de EDTA não resultou em maiores valores de pH (p = 0,2278). Concluiram que o pH aumentou em todas as associações utilizadas; que a clorexidina gel a 2% permitiu o aumento gradual do pH ao longo do tempo; e que a remoção da camada de esfregaço não influenciou no aumento do pH.
Em condições de elevado pH (baixa concentração de íons H+) a atividade enzimática das bactérias é inibida11. O mecanismo de ação do hidróxido de cálcio se dá através da liberação de íons hidroxila, necessário para aumentar o pH, tornando o meio inapropriado para a sobrevivência dos microrganismos. O hidróxido de cálcio promove dois tipos de efeitos sobre a bactéria: inibição do crescimento ou inibição da reprodução. Estes efeitos envolvem a interferência na síntese da parede celular, alteração da permeabilidade da membrana citoplasmática, interferência na síntese proteica ou alteração na replicação cromossômica, gerando a morte dos microrganismos.
Os valores das porcentagens de íons hidroxila e íons cálcio, nos períodos de 7, 30, 45 e 60 dias, indicaram maior liberação iônica para pastas com veículos hidrossolúveis aquosos (solução fisiológica e anestésica), quando comparado aos valores da pasta com veículo hidrossolúvel viscoso (Propilenoglicol 400)12.
Özcelik et al13compararam a tensão superficial de misturas de hidróxido de cálcio com vários veículos (glicerina, solução de Ringer, salina isotônica e solução anestésica). Os resultados expressaram diferenças significantes entre os veículos isolados e as combinações de hidróxido de cálcio. A menor tensão superficial foi observada no grupo cujo veículo foi a solução anestésica.
Tronstad et al14 analisaram a difusão de íons hidroxila do hidróxido de cálcio através dos túbulos dentinários e o possível aumento do pH nos tecidos. Os resultados mostraram que a colocação de hidróxido de cálcio no canal radicular pode influenciar as áreas de reabsorção, impossibilitar a atividade osteoclástica e o processo de reparação.
MATERIAIL E MÉTODO
O efeito do elevado pH do hidróxido de cálcio (12.6), influenciado pela liberação de íons hidroxila, é capaz de alterar a integridade da membrana citoplasmática da bactéria através de injúrias químicas aos componentes orgânicos e transporte de nutrientes, ou por meio da destruição de fosfolipídios ou ácidos graxos insaturados da membrana citoplasmática, observado pelo processo de peroxidação lipídica, sendo esta na realidade, uma reação de saponificação5.
Foram medidos o pH de três marcas de hidróxido de cálcio encontrados no Brasil: Ultracal XS®, hidróxido de cálcio PA® fabricado pela Biodinâmica e Dycal®.
Leonardo et al15 em 1976, avaliaram o hidróxido de cálcio associado a um veículo viscoso, na busca de uma pasta que fosse acessível ao clínico e que tivesse condições clínicas satisfatórias para o momento do seu emprego.
Uma pasta semelhante foi fabricada pela Ultradent e lançada no Mercado. As pastas comerciais avaliadas foram: Ultracal XS® (Ultradent Products, Inc., Indaiatuba, SP, Brasil) composta por Hidróxido de Cálcio 35%, numa solução aquosa com pH 12,5, acondicionado em seringa. Acompanha o produto seu respectivo Manual de Instruções de Uso, uma seringa onde está acondicionado o material e pontas aplicadoras (Navi Tip 29).
Outra amostra estudada foi o hidróxido de cálcio em forma de pó (PA – Pró-Análise), pela Biodinâmica Química e Farmacêutica (Paraná – Brasil) vez que o Hidróxido de Cálcio P.A. é um dos materiais mais aceitos atualmente para induzir a formação da dentina reparadora, apresentando propriedades imprescindíveis para materiais que atuam em procedimentos sobre a dentina possuindo excelente histo compatibilidade e estimula o tecido hospedeiro, favorecendo a reparação tecidual. Composição: Hidróxido de Cálcio P.A. (99 a 100,0%) em solução aquosa ou viscosa.
A terceira amostra foi o Dycal® fabricado pela Dentsply Sirona (Petrópolis – Brasil). Cimento à base de hidróxido de cálcio radiopaco quimicamente ativado. Indicação: Dycal® é indicado para o capeamento pulpar e forramento protetor da polpa coronária. Figura 1.
Figura 1. Marcas de hidróxido de cálcio utilizadas na pesquisa.
Foram utilizados 03 (três) dentes incisivos bovinos, nos quais foram modelados no comprimento de trabalho com um instrumento reciprocante W+File 40.05 (TDKaFILES, Curitiba, Brasil) sendo irrigado com 5 mL de solução salina (Arboreto, Juiz de Fora, Brasil). Figura 2.
Após a limpeza e modelagem foram realizadas as últimas irrigações, auferidos os pH de cada espécime, depois secos com cones de papel absorventes W+File #25 (TDKaFILE, Curitiba, Brasil), auferidos os pHs e preenchidos, cada um, com uma pasta de hidróxido de cálcio manipuladas de acordo com o fabricante utilizando uma placa de vidro e uma espátula de manipulação Cooperflex Prime, Marituba, Pará) e colocados no interior dos canais simulados com o auxílio de uma Broca Lentulo #25 (Dentsply Sirona, Bellagues, Suíça). 15 (quinze) dias depois novamente foram auferidos os pHs em cada um dos três espécimes, encontrando os seguintes resultados (pH):

Figura 2. Da esquerda para a direita. Solução fisiológica, W+File #40.05, espátula para manipulação, placa de vidro, broca Lentulo.
RESULTADOS
Três incisivos superiores bovinos foram cortados, no sentido transversal, há 15 mm do ápice radicular. Foram colocados em plataformas utilizadas no Endo – Centro de Estudos Endodônticos e foram modelados com um instrumento reciprocante W+File 40.05 (TDKaFILES, Curitiba, Brasil) e irrigados com solução fisiológica. Em seguida à limpeza e modelagem foram auferidos os os pHs de cada um. Figuras 3, 4 e 5.
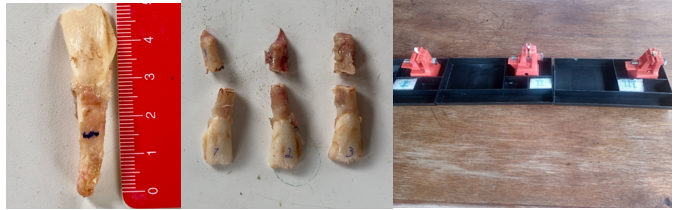
Figura 3: dente bovino. Figura 4: Dente bovino seccionado. Figura 5: Dentes bovinos colocados nas plataformas.
Os dentes foram numerados (I, II e III) e neles foi colocado uma amostra de hidróxido de cálcio e foram armazenados à temperatura ambiente por 15 dias. Após este tempo o hidróxido de cálcio foi removido e novamente auferido o pH, com o resultado que consta na tabela. Tabela 1.
Dente Antes Depois de 15 dias I 7,8 9,0 II 7,4 9,8 III 7,8 8,4 
Figura 6: Dente sendo modelado.
DISCUSSÃO.
Está estabelecido, sem sombra de dúvidas, que as bactérias desempenham um papel decisivo no desenvolvimento de lesões endodônticas. Consequentemente, um dos principais objetivos de uma endodontia bem-sucedida é a eliminação das bactérias do espaço do canal radicular e a remoção do substrato de que dependem16. Durante anos, uma infinidade de substâncias tem sido defendida para uso na terapia de canal. As origens históricas dos medicamentos remontam a tempos muito antigos. Scribonius, em 1045 d.C., escreveu sobre o uso de óleos e vinho na boca de pacientes com dor. Através da Idade Média há referências de uso de óleo de cravo e creosoto de madeira de faia como medicamentos. Infelizmente, a maioria desses medicamentos era inespecífica e por si só causava desconforto aos pacientes. Em tal situação, o hidróxido de cálcio emergiu como um potente medicamento intracanal17 desde que foi introduzido por Hermann no início do século 20.
Nerwich et al18 estudaram as mudanças de pH na dentina radicular de dentes humanos extraídos, por um período de tempo de 4 semanas, após a utilização do hidróxido de cálcio como medicação intracanal. Concluíram que esta substância requer de 1 a 7 dias para alcançar a dentina radicular externa e que, no terço cervical, observou-se valores mais altos de pH, quando comparado ao terço apical.
Segundo Holland3 no momento em que o hidróxido de cálcio entra em contato como tecido, ocorre uma dissociação em íons de cálcio e íons hidroxila. Os íons hidroxila produzem uma desnaturação proteica, dado ao seu elevado pH. A profundidade dessa atuação varia de acordo com o tipo de hidróxido de cálcio empregado (na forma de pó, pasta hidrossolúvel ou cimento) e, também em função do veículo utilizado. Em conjunto com esses íons hidroxila, penetram íons cálcio, que no limite entre o tecido desnaturado e o tecido vivo, precipitam-se na forma de carbonato de cálcio. Desta forma pode-se caracterizar cinco zonas, como resultado do contato do hidróxido de cálcio com o tecido pulpar: 1) zona de necrose de coagulação (correspondente à área de desnaturação proteica do tecido pulpar; 2) zona granulosa superficial (constituída por granulações grosseiras de carbonato de cálcio);3) zona granulosa profunda (exibe finas granulações de sais de cálcio e representa uma área de calcificação distrófica). Dois dias a aplicação do hidróxido de cálcio, na zona granulosa profunda e imediações, as fibras do tecido pulpar se dispõem paralelamente ao longo eixo do dente. Abaixo da zona granulosa profunda surgem numerosas células jovens em proliferação, sendo inclusive visíveis células em mitose. Aos sete dias, as fibras paralelas ao longo eixo do dente parecem torcidas lembrando as fibras de Van Koff. Alguns odontoblastos jovens podem se visualizados, dispostos de modo irregular. Aos trinta dias o reparo está completo, estando presente dentina, pré dentina e camada odontoblástica organizada. A ponte de tecido duro formada apresenta três camadas: Granulações de carbonato de cálcio, área de calcificação distrófica e dentina; 4) zona de proliferação celular;5) zona de polpa normal.
É de extrema importância que o mesmo tenha íntimo contato com as paredes dos canais radiculares, em todos os seus terços, visto que o hidróxido de cálcio apenas inicia suas ações antifúngica, bactericida, alcalinizante e mineralizante, através do contato direto com a matéria orgânica e seus fluidos19.
CONCLUSÃO
A pesquisa em ex vivo demonstrou que o hidróxido de cálcio, como um curativo intracanal, aumenta o pH do Sistema de Canais Radiculares.
REFERÊNCIAS
Leonardo MR, Araújo CH, Mendes AJD. Contribuição para o emprego de pastas à base de hidróxido de cálcio na obturação de canais radiculares – Estudo de propriedades físicas, químicas e biológicas. Parte I. Rev. Fac, Farm. Odont.1976;10:125-35.
Hermann BW. Calciumhydroxyd als mittel zurn behandel und vonxahnwurzelkanälen. (Thesis) Würzburg;1920.
Rhoner A. Calxyl als wurzellfullunqsmaterial nach pulpaextirpation . Schwez Zahnheilked Mschr Zahnheilked 1940;50:903-40.
Holland R. Processo de reparo da polpa dental após pulpotomia e proteção com hidróxido de cálcio.(Tese de Doutorado). Araçatuba: Faculdade de Odontologia, Universidade Estadual Paulista; 1966.
Estrela C, Sydney GB, Bammann LL, Felippe Jr O. Estudo sobre o efeito biológico do pH na atividade enzimática de bactérias anaeróbias. Rev Fac Odontol Bauru 1994;2:31-8.
Estrela C, Sydney GB, Bammann LL, Felippe Jr O. Mechanism of the action of calcium and hydroxyl ions of calcium hydroxide on tissue and bacreria. Braz Dental J 1995;6:5-9.
Estrela C. Ciência endodôntica, São Paulo: Artes Médicas, 2004.
Estrela C. Análise química de pastas de hidróxido de cálcio, frente a liberação de íons de cálcio, de íons hidroxila e ação do carbonato de cálcio na presença de tecido conjuntivo de cão. (Tese de Doutorado em Endodontia). São Paulo: Faculdade de Odontologia da Universidade de São Paulo – USP;1994.
Greenwood NN, Earnshaw A. Cheminsty of the elements.New York: Pergamon Press;1984 Shetty S, ManjunathMR, Tejaswi S. An In-vitro Evaluation of the pH Change Through Root Dentin Using Different Calcium Hydroxide Preparations as an Intracanal Medicament. J of Clin and Diag Research. 2014;8(10):13-16.
Ferreira CM, Gomes FA, Guimarães NLSL, Vitoriano MM, Ximenes TA, Santos RA. In vitro analysis of the pH alteration of the dentine after using different calcium hydroxide-based pastes. RSBO. 2013;10(2):122-7.
Sundqvist G. Ecology of the root canal flora. J Endod.1992;18:427-30. Estrela C, Pesce HF. Chemical analysis of the liberation of calcium and hydroxyl ions from calcium hydroxide pastes in connective e tissue in dog. Part I. Brazil Dent J 1996; 7: 41-6.
Özcelik B, Tasman F, Ogan C. A comparison of the surface tension of calcium hydroxide mixed with diferente vehicles. J Endod 2000;26:500-2.
Tronstad L, Andreasen JO, Hasselgren G, Kristerson L, Riis I. pH changes in dentaltissues after root canal filling with calcium hydroxide. J Endod 1981;7:17-21.
Leonardo MR, Araújo CH, Mendes AJD. Contribuição para o emprego de pastas à base de hidróxido de cálcio na obturação de canais radiculares – Estudo de propriedades físicas, químicas e biológicas. Parte I. Rev. Fac, Farm. Odont.1976;10:125-35.
Ingle, JI, Bakland LK. Endodontics, 6th edition, B.C Decker. Walton RE. Intracanal medicaments. Dent Clin North Am. 1984; 28:783-96.
Nerwich A, Figdor D, Messer HH. pH changesin root dentine over a 4 week periodfollowing root canal dressing with calcium hydroxide . J Endod 1993;19:302-6.
Nogueira CS, Freire DCAM. Avaliação da qualidade de inserção da medicação intracanal à base de hidróxido de cálcio: Uma revisão de literatura. Monografia (artigo científico) entregue para acompanhamento como parte integrante das atividades de TCC II do Curso de Odontologia da Faculdade de Ilhéus. 2020.
1. Cirurgião dentista
2. Especialista e Mestre em Endodontia. Professor de Endodontia Clínica da Faculdade de Ilhéus (CESUPI) e Coordenador do Curso de Especialização em Endodontia do Instituto Excellence (Ilhéus)
Autor Correspondente: Antônio Henrique Braitt
Av. Aziz Maron 1.117/703
Jardim União
45605-904 Itabuna Bahia
e mail: henrique_braitt@terra.com.br
