REGISTRO DOI: 10.69849/revistaft/th10249080726
Vitoria Ilana Rodrigues de Souza
Francisco Anderson Abreu do Nascimento
Dayse Nóbrega de Lima de Oliveira
Flávio Bitencourt da Silveira
RESUMO
INTRODUÇÃO: O câncer de mama é a neoplasia mais frequente entre as mulheres e espera-se que as suas taxas de incidência e mortalidade aumentem significativamente nos próximos cinco a dez anos. Mesmo frente aos avanços da descoberta de medicamentos quimioterápicos cada vez mais eficazes, a toxicidade associada ao tratamento ainda é frequente. Como consequência dos efeitos durante o tratamento, a neutropenia induzida por quimioterapia é a toxicidade hematológica mais séria. OBJETIVO: Descrever sobre a incidência e o manejo da neutropenia febril em pacientes portadores de câncer de mama, admitidos por protocolo de quimioterapia. METODOLOGIA: Trata-se de uma revisão integrativa, que teve como questão norteadora: “Qual a incidência e o manejo da neutropenia febril em pacientes com câncer de mama admitidos por protocolo de quimioterapia?”. Foram coletados dados nas bases de dados PubMed, Scielo, REBEN, Revista Brasileira em Cancerologia, por via da Biblioteca Virtual em Saúde (BVS). A busca foi realizada por acesso on-line, tendo sido encontrados 520 artigos; utilizando os critérios de inclusão como artigos publicados de 2017 a 2022, disponíveis em portugues e inglês, a amostra final desta revisão integrativa foi constituída de 10 artigos. RESULTADOS: No total de artigos incluídos, foi evidenciado através da literatura que existe uma relação entre o desenvolvimento de neutropenia febril e o paciente com câncer de mama, através da terapia antineoplásica, com ênfase nos tratamentos que envolveram platina/taxano e ciclofosfamida/antraciclinas. Nesse contexto, os Indivíduos que fazem o uso dos quimioterápicos, mas não fazem o uso de G-CSF, têm maior possibilidade de desenvolver a neutropenia febril, porém, os pacientes que fazem uso de G-CSF de forma profilática, são comprovados a redução dos casos de neutropenia febril. CONSIDERAÇÕES FINAIS: Em síntese, reitera-se que a ocorrência da NF, ao constituir um risco importante para o bem-estar e sobrevida dos pacientes em tratamento quimioterápico, requer a presença de profissionais de saúde qualificados e detentores do melhor conhecimento baseado em evidências científicas.
Descritores: Neutropenia Febril; Câncer De Mama; Quimioterapia.
ABSTRACT
INTRODUCTION: Breast cancer is the most common neoplasm among women and its incidence and mortality rates are expected to increase significantly over the next five to ten years. Even in the face of advances in the discovery of increasingly effective chemotherapy drugs, toxicity associated with treatment is still common. As a consequence of the effects during treatment, chemotherapy-induced neutropenia is the most serious hematological toxicity. OBJECTIVE: To describe the incidence and management of febrile neutropenia in breast cancer patients admitted by chemotherapy protocol. METHODOLOGY: This is an integrative review whose guiding question was: “What is the incidence and management of febrile neutropenia in breast cancer patients admitted by chemotherapy protocol?”. Data was collected from the PubMed, Scielo, REBEN and Revista Brasileira em Cancerologia databases via Biblioteca Virtual em Saúde (BVS). The search was carried out through online access, and 520 articles were found; using the inclusion criteria of articles published from 2017 to 2022, available in Portuguese and English, the final sample of this integrative review consisted of 10 articles. RESULTS: In the total number of articles included, the literature showed that there is a relationship between the development of febrile neutropenia and breast cancer patients, through antineoplastic therapy, with an emphasis on treatments involving platinum/taxane and cyclophosphamide/anthracyclines. In this context, individuals who use chemotherapy but do not use G-CSF are more likely to develop febrile neutropenia, but patients who use G-CSF prophylactically have been shown to reduce cases of febrile neutropenia. FINAL CONSIDERATIONS: To sum up, it should be reiterated that the occurrence of FN, as it constitutes an important risk to the well-being and survival of patients undergoing chemotherapy, requires the presence of qualified health professionals who have the best knowledge based on scientific evidence.
Keywords: Febrile Neutropenia; Breast Cancer; Chemotherapy.
INTRODUÇÃO
O câncer de mama é a neoplasia mais frequente entre as mulheres e espera-se que as suas taxas de incidência e mortalidade aumentem significativamente nos próximos cinco a dez anos (GREANEY et al,2015).É uma patologia incomum antes dos 35 anos, com incidência crescente principalmente após os 50 anos, que está associada a fatores genéticos, alterações hormonais, obesidade e tabagismo (GOZZO et al, 2011).
Para o Brasil, a estimativa para o triênio de 2023 a 2025 aponta que ocorrerão 704 mil casos novos de câncer, 483 mil se excluídos os casos de câncer de pele não melanoma. Sendo os casos de câncer de mama, correspondente a 73.610 novos casos, correspondendo a um risco estimado de 66,54 casos novos a cada 100 mil mulheres (INCA,2023).
No mundo, o câncer de mama é a principal causa global de incidência, com 11,7% do total de casos. Em 2020, ocorreram cerca de 2,3 milhões de casos novos, equivalente a 24,5% de todos os cânceres em mulheres, excluído o de pele não melanoma. Esse valor corresponde ao risco estimado de 47,80 casos a cada 100 mil mulheres. As maiores taxas de incidência estimadas foram na América do Norte, na Oceania e nos países do Oeste da Europa (FERLAY et al., 2021; SUNG et al.,2021).
As taxas de incidência de câncer de mama estão aumentando rapidamente em países de baixo e médio desenvolvimento, como os da América do Sul, da África e da Ásia. Esse aumento de casos está associado ao envelhecimento populacional, às mudanças no comportamento e no estilo de vida e ao sub-diagnóstico associado à difusão do rastreamento mamográfico, recomendado no Brasil de 50 a 69 anos (MIGOWSKI et al., 2018; SUNG et al., 2021).
Desse modo, o tratamento do câncer pode ser realizado de três formas principais, podendo ser através de: cirurgia, radioterapia e quimioterapia. Essas técnicas, contudo, podem ser usadas em conjunto, onde a variação é apenas quanto à suscetibilidade dos tumores a cada uma das modalidades terapêuticas e quanto à melhor sequência de tratamento. Todos os tratamentos acarretam diversos efeitos colaterais em tipos e graus variados.(CURT et al, 2000).
No cenário atual, as neoplasias malignas tratadas com apenas uma modalidade terapêutica constituem um número bem pequeno (INCA,2020). Apesar dos avanços tecnológicos, a quimioterapia antineoplásica continua sendo uma opção terapêutica indispensável. Constitui -se em um método que utiliza um ou mais fármacos com o objetivo de atingir diferentes populações celulares, em diversas fases do ciclo celular, enfraquecendo o desenvolvimento da célula com crescimento desordenado. Os quimioterápicos atuam sobre as células tumorais e também em distintas células no corpo, como na medula óssea, nos pelos e na mucosa do tubo digestivo. A quimioterapia é aplicada em ciclos repetitivos, pois a célula normal apresenta um tempo de recuperação (INCA,2015).
Mesmo frente aos avanços da descoberta de medicamentos quimioterápicos cada vez mais eficazes, a toxicidade associada ao tratamento ainda é frequente. Isso ocorre porque o mecanismo de ação dos quimioterápicos não atua exclusivamente sobre as células tumorais. As células normais que se renovam constantemente, como a medula óssea, são também atingidas pela sua ação, acarretando em seus efeitos colaterais de toxicidade.
Como consequência dos efeitos durante o tratamento, a neutropenia induzida por quimioterapia é a toxicidade hematológica mais séria. Podendo ser definida na literatura como a contagem absoluta de neutrófilos inferior a 1.500/m³, associado a um aumento isolado de temperatura axilar superior a 38 °C, no intervalo de pelo menos uma hora. Também se considera neutropenia quando há uma diminuição de 500 neutrófilos por mililitro de sangue durante as primeiras 48h de aparição da febre (HERNANDES et al, 2019).
A neutropenia ocorre devido à supressão do sistema hematopoiético e imunológico. Seu monitoramento deve ser acompanhado porque, em casos graves, pode ocorrer o evento de Neutropenia febril, gerada através do acometimento da medula óssea e na mucosa gastrointestinal, gerando mielossupressão, o que necessita de intervenção médica imediata. Portanto, sendo descrita como um dos principais eventos adversos da quimioterapia antineoplásica, é a toxicidade que mais interfere na continuidade do tratamento.
Segundo Pathak et al. 2015, a neutropenia, quando associada à febre, é uma complicação potencialmente fatal, remetendo a mais cuidados e gastos com a saúde, podendo afetar diretamente a continuidade do tratamento oncológico, bem como o risco de mortalidade e internação hospitalar por infecções que necessitam ser tratadas com antimicrobianos de amplo espectro, por via endovenosa.
O presente estudo tem como objetivo, por meio de uma revisão bibliográfica da literatura, descrever sobre a incidência e o manejo da neutropenia febril em pacientes portadores de câncer de mama, admitidos por protocolo de quimioterapia.
METODOLOGIA
Trata-se de uma revisão integrativa, que é considerada uma ferramenta ímpar, no campo da saúde, por possibilitar a síntese de pesquisas disponíveis sobre determinada temática e direcionar a prática fundamentando-se em conhecimento científico (SOUZA et al, 2010). Teve como questão norteadora: “Qual a incidência e o manejo da neutropenia febril em pacientes com câncer de mama admitidos por protocolo de quimioterapia?”
Para organizar a condução da revisão integrativa utilizou-se a estratégia PICO, acróstico de Paciente, Intervenção, Comparação e Outcomes ou desfecho (JOANA,2014). Tendo sido empregadas as letras e seus termos equivalentes “P” – pacientes com câncer de mama submetidos à Qt; “I” – manejo realizadas pelos profissionais, “C” – uso de profilaxia primária (pegfilgrastim, filgrastim , biossimilares e antibióticos) ou não; e “O” – redução da neutropenia febril.
Sendo descrito nas seguintes etapas: estabelecimento de hipóteses e objetivos, determinação de critérios de inclusão e exclusão de produtos (amostragem), definição de informações que podem ser obtidas dos artigos selecionados, análise de resultados, apresentação e discussão de resultados, e no final, uma apresentação da revisão.
Os critérios de inclusão foram previamente estabelecidos, sendo eles: artigos publicados em português e inglês, com os textos disponíveis, na íntegra, sendo estes gratuitos e pagos, nas bases de dados selecionadas, no período entre 2017 e 2022; artigos cuja metodologia evidenciasse a incidência e/ou o manejo relativas à neutropenia febril, sendo em conjunta ou em separado. Além disso, os critérios de exclusão foram os seguintes: artigos repetidos, textos não completos ou ilegíveis, e sem relação com o tema de pesquisa.
Foram coletados dados nas bases de dados PubMed, Scielo (Scientific Electronic Library Online), Revista Brasileira de Enfermagem (REBEN), Revista Brasileira em Cancerologia (RBC), por via da Biblioteca Virtual em Saúde (BVS). Conforme recomendam Lopes et al, 2010, devido às características específicas para o acesso às bases de dados selecionadas, as estratégias utilizadas para localizar os artigos foram adaptadas, tendo como eixos norteadores a pergunta de pesquisa e os critérios de inclusão e exclusão para manter a coerência na busca dos artigos e evitar possíveis vieses. Nessa perspectiva, os termos empregados na busca foram: Neutropenia Febril and Quimioterapia,Cancer de Mama and Neutropenia Febril.
A busca foi realizada por acesso on-line, tendo sido encontrados 520 artigos; utilizando os critérios de inclusão, a amostra final desta revisão integrativa foi constituída de 10 artigos, conforme apresentado na Figura 1.
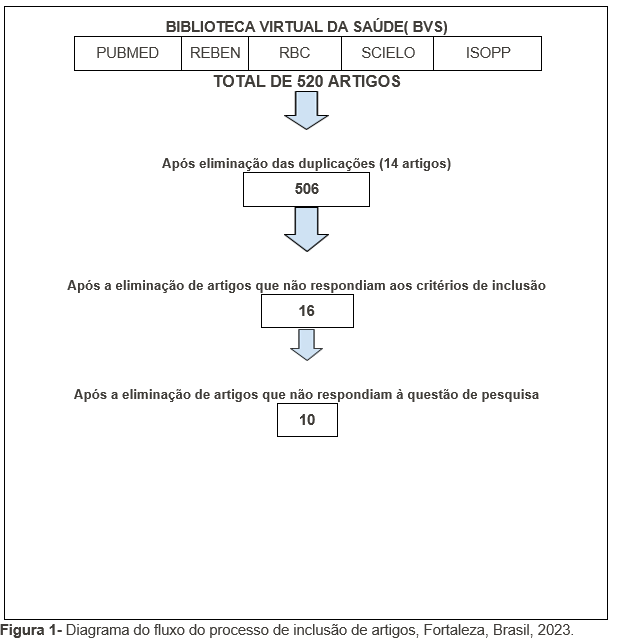
Figura 1- Diagrama do fluxo do processo de inclusão de artigos, Fortaleza, Brasil, 2023.
RESULTADOS
Nesta revisão integrativa obteve-se uma amostra de 10 artigos que atenderam aos critérios de inclusão, apresentados no quadro sinóptico a seguir (Quadro 1).
Quadro 1- Caracterização dos 10 artigos incluídos na revisão integrativa segundo título, autor, ano e país de origem, Fortaleza, Brasil, 2023.
Título Autor/ Ano País de origem Manejo da neutropenia febril em pacientes adultos oncológicos: revisão integrativa da literatura Ferreira JN, et al.; 2017 Brasil Neutropenia Associada ao Tratamento do Câncer de Mama: Revisão Integrativa da Literatura Conte FM, et al.; 2019 Brasil Prospective cohort study of febrile neutropenia in breast cancer patients administered with neoadjuvant and adjuvant chemotherapies: CSPOR-BC FN study Ishikawa T, et al.; 2021 Japão Impact of granulocyte-colony stimulating factor on docetaxel-induced febrile neutropenia in patients with breast cancer Zerki J, et al.; 2022 Arabia Saudita Febrile neutropenia and role of prophylactic granulocyte colony-stimulating factor in docetaxel and cyclophosphamide chemotherapy for breast cancer Kimura Y, et al.; 2021 Japão Primary Febrile Neutropenia Prophylaxis for Patients Who Receive FEC-D Chemotherapy for Breast Cancer: A Systematic Review Fernandes R, et al.; 2018 Não encontrado Febrile neutropenia in adjuvant and neoadjuvant chemotherapy for breast cancer: a retrospective study in routine clinical practice from a single institution Bacrie J, et al.; 2018 França Real-world evaluation of supportive care using an electronic health record text-mining tool: G-CSF use in breast cancer patients Van Laar SA, et al.; 2022 Holanda A prospective cohort study to evaluate the incidence of febrile neutropenia in patients receiving pegfilgrastim on-body injector versus other options for prophylaxis of febrile neutropenia: breast cancer subgroup analysis Mahtani RL, et al.; 2022 United States of America (USA) Treatment of infections in cancer patients: an update from the neutropenia, infection and myelosuppression study group of the Multinational Association for Supportive Care in Cancer (MASCC) Bernardo L, et al.; 2021 África do Sul
Todos os estudos analisados foram conduzidos em instituições hospitalares, sendo realizados por médicos, farmacêuticos e pesquisadores da área de cancerologia. Foram publicados nos periódicos: Supportive Care in Cancer (4), Journal of Oncology Pharmacy Practice (1), Review of Clinical Pharmacology (1), Journal of Oncology Pharmacy Practice (1), Journal of Global Oncology (1), Revista Brasileira de enfermagem (1), Revista Brasileira de Cancerologia (1).
Em relação aos tipos de estudos, obteve-se o seguintes resultados: um, “estudo observacional prospectivo multicêntrico” ; quatro, “estudos retrospectivos observacionais” ; um, “estudo de revisão sistemática” ; um, “estudo de coorte prospectivo” ; três, “estudos de revisão integrativa da literatura”.
Quadro 2- Apresentação da síntese das intervenções, resultados e recomendações /conclusões dos 10 artigos incluídos na revisão integrativa, Fortaleza, Brasil, 2023.
Intervenção estudada Resultados Recomendações/ Conclusões Analisar as intervenções realizadas por profissionais de saúde visando ao manejo da neutropenia febril induzida por Quimioterapia. Encontrou-se um estudo sobre manejo farmacêutico relativo à eficácia de dosagem de antibióticos e um estudo indicando que os enfermeiros poderiam contribuir para a identificação de pacientes idosos que se beneficiariam com uso profilático de fator de crescimento. Evidenciou-se a escassez de estudos com a participação de outros profissionais de saúde, além dos médicos, e a lacuna de conhecimento quanto à prática interprofissional na condução de intervenções específicas na sua área de competência, intervenções conjuntas e intervenções não farmacológicas. Avaliar, por revisão bibliográfica, a ocorrência de neutropenia em pacientes com câncer de mama, a partir de estudos que abordam diferentes regimes de tratamento quimioterápicos. Dos 13 medicamentos quimioterápicos relatados nos estudos selecionados, os regimes mais utilizados foram epirrubicina, fluorouracil, ciclofosfamida e docetaxel (FEC-D), docetaxel e ciclofosfamida (TC) e doxorrubicina, ciclofosfamida e docetaxel (AC-T). Todos os regimes terapêuticos estudados causaram neutropenia grau 3 ou 4 como toxicidade hematológica. A neutropenia apresenta elevada ocorrência, independente do tratamento quimioterápico utilizado para o tratamento do câncer de mama. Os esquemas mais associados foram platina / taxano e ciclofosfamida /antraciclinas/ taxanos, que são os mais frequentemente utilizados por sua elevada eficácia. Intervenção estudada Resultados Recomendações/ Conclusões Avaliações da incidência de NF e fatores de risco em asiáticos são importantes para o uso apropriado de pegfilgrastim primário (PEG-G). Ao comparar a proporção de FN de E(A)C em caucasianos com a dos asiáticos neste estudo, sugere-se claramente que pode existir uma diferença étnica na vulnerabilidade à FN. De 1005 pacientes incluídos, 980 mulheres tratadas com FEC, E(A)C e CT foram analisadas. As proporções de incidência de NF em todos os pacientes foram de 22,5%, 27,5% e 33,9% para FEC, E(A)C e CT, respectivamente. Os de NF-T foram 27,7%, 22,4% e 36,6%; os de S-FN foram 17,3%, 32,4% e 31,5% com uso mais frequente de PEG-G primário. As incidências de NF foram superiores a 20% nos 3 esquemas, sendo a TC a mais elevada. O IDI manteve-se a um nível elevado tanto nos grupos visitantes como nos grupos não visitantes. Os fatores de risco relacionados ao paciente foram idade e CA pré-tratamento. A origem étnica pode estar relacionada à incidência de FN, sendo relatado que os asiáticos são mais vulneráveis à FN do que os caucasianos. Avaliar o impacto do G-CSF sobre a FN e a tolerância à quimioterapia em pacientes que receberam DBRs para o tratamento de câncer de mama, comparando a taxa de FN, o tempo de internação hospitalar (LOS) devido à FN e a redução ou atraso da dose de DBR devido à FN em pacientes que receberam ou não G-CSF profilático O estudo atual demonstrou uma redução na taxa de FN induzida por DBR em pacientes com câncer de mama que foram tratadas com G-CSF profilático, particularmente quando iniciado após o primeiro ciclo de quimioterapia. O G-CSF também reduziu o tempo de internação das pacientes hospitalizadas com FN. Há fortes evidências na literatura de que o G-CSF tem um impacto positivo sobre a capacidade dos pacientes de alcançar o tratamento planejado. Investigar a frequência de NF e a intensidade de dose relativa (IDR) da quimioterapia com TC em pacientes com câncer de mama e identificar a população correta que necessita de G-CSF profilático. NF ocorreu em 70 pacientes (35,7%). A incidência de NF foi observada em 41,1% sem qualquer medida profilática e em 5,0% com G-CSF profilático. Na análise multivariada, os fatores de risco independentes de NF foram idade mais avançada (≥ 60 anos, P = 0,017) e sem G-CSF profilático primário (P = 0,011). Onze pacientes (5,6%) foram hospitalizados, dos quais 8 (72,7%) eram idosos. As medianas das IDR de docetaxel e ciclofosfamida foram de 96,7% e 99,7%, respectivamente. A frequência de NF durante a quimioterapia com TC foi alta, e o G-CSF profilático primário reduziu a incidência de NF. O G-CSF profilático primário é uma terapia eficaz na prevenção da NF durante a quimioterapia com CT. No entanto, o G-CSF profilático deve ser considerado para pacientes idosos com base na baixa taxa de hospitalização e na alta IDR.Portanto, o G-CSF profilático primário é uma terapia eficaz para prevenção de FN durante a quimioterapia com TC. Intervenção estudada Resultados Recomendações/ Conclusões Avaliar a incidência de FN com FEC-D (com e sem profilaxia primária), seu momento e estratégias ideais para a profilaxia primária de FN. Também identificamos lacunas na literatura disponível que requerem estudos mais aprofundados. A quimioterapia FEC-D com e sem profilaxia primária foi associada a taxas medianas de FN de 10,05% (variação de 0,2% a 25%) e 23,9% (variação de 5% a 27,7%), respectivamente. No que diz respeito a cada tratamento de profilaxia primária, o pegfilgrastim foi utilizado como profilaxia primária em dois estudos prospectivos. Um estudo mostrou que entre 32 pacientes tratados com FEC-D que receberam profilaxia primária de FN com pegfilgrastim, FN se desenvolveu em 5%. O outro estudo demonstrou que 9% dos 69 pacientes tratados com FEC-D apresentaram FN apesar de terem recebido profilaxia primária com pegfilgrastim. FN é muito mais frequentemente observada durante o componente docetaxel do tratamento do que durante os ciclos FEC. Finalmente, as toxicidades do G-CSF diferem das dos antibióticos, bem como diferem de acordo com a duração do uso. Dado o maior custo do medicamento pegfilgrastim em relação ao filgrastim, a maioria dos financiadores de cuidados de saúde cobrirá o filgrastim, embora alguns dados sugiram que o pegfilgrastim é superior e mais rentável do que o filgrastim (Informações sobre ensaios clínicos: NCT02173262 Determinar se os objetivos foram de determinadas características dos pacientes estavam associadas a um risco maior de NF, descrever o tratamento de pacientes com NF e determinar se o tratamento estava em conformidade com as diretrizes de prática clínica da ESMO. Em nosso estudo, ocorreu uma taxa de FN de 21% para FEC sem G-CSF contra 13% para outros regimes de quimioterapia. Para essa situação, o FEC não é considerado um fator de risco significativo nessa subpopulação (p = 0,27), mas é provável que haja uma falta de poder. a única comorbidade identificada em pacientes com câncer de mama foi a IA ou doenças inflamatórias, e essas doenças foram associadas a um risco maior de FN (RR 3,08; 95% CI [1,43-5,85]; p < 0,01). A profilaxia primária com G-CSF deve ser considerada com mais cuidado em pacientes tratados com FEC ou que apresentem IA ou doença inflamatória. De acordo com as diretrizes da ESMO, e conforme confirmado em nosso estudo, os pacientes com FN com baixo risco de complicações devem ser tratados como pacientes ambulatoriais e receber uma combinação de antibióticos orais. Esse tratamento terá um impacto positivo não apenas em termos de custos, mas também na qualidade de vida do paciente Aplicabilidade de uma ferramenta de mineração de texto EHR para avaliação do tratamento do G-CSF do mundo real em pacientes com câncer de mama. As diretrizes recomendam o uso primário de G-CSF para pacientes que recebem quimioterapia de alto (> 20%) risco (HR) ou Foram incluídas 190 pacientes do sexo feminino, que receberam 77 HR e 113 tratamentos de RI. Em 88,3% dos regimes de FC, foi administrado G-CSF; 7,3% desses pacientes desenvolveram NF vs. 33,3% sem G-CSF. Embora a maioria dos pacientes do esquema de RI apresentasse ≥ O uso profilático de fatores estimuladores de colônias de granulócitos (G-CSF), por exemplo, filgrastim, demonstrou reduzir a gravidade e a duração da neutropenia e a incidência de NF em 50–90%. O uso de G-CSF também pode resultar em eventos adversos, principalmente dor óssea leve a moderada (25–36%), Intervenção estudada Resultados Recomendações/ Conclusões intermediário (10–20%) de risco de FN (IR) se o risco geral com fatores de risco adicionais relacionados ao paciente exceder 20%. 2 fatores de risco, apenas 4% receberam G-CSF, dos quais nenhum desenvolveu neutropenia. Entretanto, sem G-CSF, 11,9% desenvolveram NF e 31,2% neutropenia grave. mas também neoplasias mieloides potencialmente secundárias. Além disso, o amplo uso do G-CSF foi anteriormente assumido como um fardo financeiro significativo para o sistema de saúde; o custo-efetividade do G-CSF está altamente relacionado tanto com o risco de NF quanto com os custos de G-CSF na prática clínica Examinar pacientes com câncer de mama que receberam quimioterapia com alto risco de NF, recebendo OBI (“OBI”) ou outras opções (outras G-CSF ou nenhuma; “outros”). O desfecho primário foi incidência de NF; os desfechos secundários incluíram administração de quimioterapia, adesão (G-CSF em todos os ciclos), adesão (G-CSF dia após a quimioterapia) e incidência de NF em pacientes recebendo tratamento curativo ou paliativo. A incidência global de FN foi menor em pacientes que receberam pegfilgrastim OBI no primeiro ciclo de quimioterapia em comparação com outras opções, independentemente do uso de pegfilgrastim OBI em ciclos subsequentes. O risco de desenvolver FN foi reduzido em 40% com pegfilgrastim OBI em comparação com outras opções. A incidência de atrasos e reduções na dose foi semelhante entre os pacientes que receberam pegfilgrastim OBI ou outras opções. O Pegfilgrastim OBI foi associado a uma menor incidência de FN em pacientes com câncer de mama em comparação com outras opções de profilaxia de FN. A adesão à profilaxia com G-CSF e a adesão ao pegfilgrastim foram maiores em pacientes que receberam pegfilgrastim OBI em comparação com pacientes que receberam outras opções. Pacientes que desenvolvem neutropenia de grau 3 e 4 ou FN durante tratamentos de quimioterapia geralmente requerem reduções de dose e/ ou atrasos de dose em seu programa de quimioterapia,resultando em redução da intensidade relativa da dose (RDI). Os benefícios dos cuidados ambulatoriais/ambulatoriais de emergência incluem evitar internações, reduzir a pressão em departamentos de emergência muitas vezes superlotados e sobrecarregados, economia de custos, risco reduzido de infecções nosocomiais e melhor experiência e satisfação do paciente. Além disso, a apresentação tardia de pacientes com FN continua a ser um risco significativo, por vezes motivado por preocupações de internamento hospitalar prolongado. Diretrizes baseadas em evidências foram desenvolvidas pela ASCO, NCCN e ESMO definindo o uso apropriado de G-CSF em pacientes oncológicos com câncer. As principais indicações para o uso do G-CSF estão resumidas: profilaxia primária (o uso de G-CSF no primeiro ciclo e nos ciclos subsequente) e profilaxia secundária ( como o uso de G-CSF em subse-ciclos frequentes após episódios iniciais de neutropenia grave e/ou FN). O uso profilático de G-CSF é uma estratégia terapêutica para manter o RDI durante o tratamento, diminuindo a incidência de neutropenia grave e FN e melhorando os resultados do tratamento e a qualidade de vida.
ESMO- Sociedade Europeia de Oncologia Médica; ASCO – Sociedade Americana de Oncologia Clínica; NCCN- National Comprehensive Cancer Network.
DISCUSSÃO
A Neutropenia Febril (NF) é um dos principais eventos adversos na terapia antineoplásica. Apesar dos avanços recentes nas drogas e protocolos utilizados nas diversas terapias antineoplásicas, a neutropenia febril é um dos principais fatores que exigem interrupção do tratamento e custos adicionais com internação hospitalar, além de interferir consideravelmente na qualidade de vida do paciente em tratamento.
Atualmente, o paciente portador de NF pode ser classificado como neutropênico de baixo risco, de risco intermediário e de alto risco. A divisão do escore de risco é determinado por meio do índice de gravidade MASCC
(Multinational Association for Supportive Care of Cancer), que credita pontos, de acordo com a importância, para cada variável: paciente assintomático a paciente apresentando sintomas leves, moderados ou graves; ausência de hipotensão; ausência de doença pulmonar obstrutiva crônica; portador de tumor sólido ou ausência de infecção fúngica; ausência de desidratação; não hospitalizados ao aparecimento da febre; e a idade menor que 60 anos (Freifeld AG,et al, 2010). O índice de gravidade MASCC pontua até 26 pontos no máximo e subsidia a classificação do paciente como de baixo risco (≥ 21 pontos) ou de alto risco (< 21 pontos)
Vale acrescentar que a mielossupressão decorrente do tratamento quimioterápico não é influenciada tão somente pela citotoxicidade medicamentosa. Existem fatores de risco que também influenciam, apesar de não serem bem esclarecidos em literatura. Alguns estudos citam: idade superior a 65 anos, sexo feminino, estado nutricional acometido, envolvimento prévio de medula óssea e contagem de linfócitos e hemoglobina previamente inferiores, no início do ciclo (SBO, 2012). Também são considerados fatores de risco: esquemas terapêuticos contendo fluoracil, um medicamento da classe dos antimetabólitos, que também é usado em tratamentos de câncer de mama.
Devido ao custo oneroso para tratamento do paciente, enquanto terapia antineoplásica deve ser adiada ou interrompida, afetando inclusive o sucesso da terapêutica, torna-se importante detalhar e conhecer os principais manejos clínicos para solucionar neutropenia febril da forma mais precoce possível, como: definir agente patológico para escalonar antimicrobiano adequadamente; monitorar exames bioquímicos; adotar medidas de precaução para imunossuprimidos a fim de evitar eventuais infecções cruzadas hospitalares, o que causaria prolongamento da internação hospitalar.
Nesse viés, o presente estudo orientou-se para a incidência e os manejos da NF, correlacionando as causas, as consequências, bem como, os impactos no paciente oncológico o que está diretamente relacionado com o uso da terapia antineoplásica, sendo platina/taxano e ciclofosfamida/antraciclinas. Atualmente, as antraciclinas, juntamente com os taxanos, são as classes mais escolhidas para tratamento adjuvante e neoadjuvante para câncer de mama, por apresentarem maior taxa de eficácia.
O protocolo mais comum é o uso associado de doxorrubicina, ciclofosfamida e docetaxel. A associação dessas drogas no tratamento corresponde a uma taxa de cerca de 60% de acometimento por neutropenia febril dos pacientes em tratamento (SBO, 2012). Além disso, a Doxorrubicina representa a classe das antraciclinas, que tem como mecanismo de ação ligar-se ao DNA da célula, impedindo sua replicação e síntese de proteínas. A ciclofosfamida é um agente alquilante, que também se liga ao DNA, formando ligações alquilantes interfilamentares, impedindo sua replicação. O docetaxel e paclitaxel pertencem a classe dos taxanos, e têm por função promover a quebra de microtúbulos durante a fase de mitose celular ( Neto et al, 2004).
Dessa forma, são drogas que interferem, de maneira disseminada, a reprodução celular tanto das células cancerígenas, quanto das saudáveis. Por isso, geram-se tantos efeitos adversos generalizados como: alopecia, fadiga, náuseas, diarréia, insuficiência cardíaca, mucosite e imunossupressão. Ademais, ressalta-se que a mielossupressão decorrente do tratamento quimioterápico não é influenciada tão somente pela citotoxicidade medicamentosa.
Nesse viés, destaca-se, a relação benéfica entre o uso de fator estimulador de colônia de granulócitos (G-CSF) e a redução dos quadros de neutropenia febril em pacientes portadores de câncer de mama, sendo evidenciado nas pesquisas, provenientes da revisão integrativa, envolvendo diversas as culturas em várias partes do mundo (europa, américa do norte e ásia) e seus respectivos manejos clínicos.
Segundo Van Laar SA, et al.; 2022 , durante um estudo retrospectivo realizado na Holanda, demonstrou que o uso profilático de fatores estimuladores de colônias de granulócitos (G-CSF), por exemplo, filgrastim, demonstrou reduzir a gravidade e a duração da neutropenia e a incidência de NF em 50–90%.
Concomitante a isso, o autor Mahtani RL, et al.; 2022, desenvolveu pesquisas nos EUA, identificaram que entre os pacientes com câncer de mama metastático, a utilização de recursos e a taxa de mortalidade foram ainda maiores: a taxa de hospitalização associada à FN foi de 89% e a taxa de mortalidade em pacientes hospitalizados foi de 7,3%, sem profilaxia. Sendo,o Pegfilgrastim é um G-CSF de ação prolongada que demonstrou reduzir o risco de FN em 94% com uso no primeiro ciclo em pacientes com câncer de mama recebendo docetaxel 100 mg/m 2 a cada 3 semanas.
Na sequência, um estudo feito no Japão demonstrou que a origem étnica pode estar relacionada à incidência de FN, sendo relatado que os asiáticos são mais vulneráveis à FN do que os caucasianos. Do total de 980 mulheres, as proporções de incidência de FN em todos os pacientes foram de 22,5%, 27,5% e 33,9% para FEC, E(A)C e TC, respectivamente. Para pacientes com alto risco de FN, a profilaxia primária com pegfilgrastim (PEG-G) é recomendada nas diretrizes de prática clínica. Uma meta-análise mostrou que o suporte primário de PEG-G melhorou a sobrevida global de pacientes com câncer de mama com FN submetidos a quimioterapia intensificada ( Ishikawa T, et al.; 2021).
Nessa perspectiva, diante das evidências fica claro que na literatura existe um consenso entre a neutropenia febril e o uso de fatores estimuladores de colônia de granulócitos(G-CSF), que beneficiam o paciente, pois reduzem consideravelmente o quadro e a evolução dos sinais e sintomas, da NF, em suas variadas formas, o que por sua vez também contribui para minimizar os gastos hospitalares, tempo de internação e atrasos do tratamento.
Portanto, o amplo conhecimento, diagnóstico precoce e correto manejo clínico, bem como medidas preventivas em âmbito ambulatorial tornam-se cada vez mais importantes para serem disseminadas entre equipe médica e multiprofissional, para garantir não só o sucesso do tratamento, como promover melhor qualidade de vida para o paciente oncológico.
CONSIDERAÇÕES FINAIS
Em síntese, a literatura evidenciou que a neutropenia febril em pacientes realizando tratamento quimioterápico para o câncer de mama apresenta elevada ocorrência, independente do medicamento utilizado. Sendo, os esquemas mais associados com neutropenia foram combinações de platina / taxano e ciclofosfamida / antraciclinas.
Então, diante dos resultados obtidos, reitera-se que a ocorrência da NF, ao constituir um risco importante para o bem-estar e sobrevida dos pacientes em tratamento quimioterápico, requer a presença de profissionais de saúde qualificados e detentores do melhor conhecimento baseado em evidências científicas.
Nesse ínterim, ressalta-se a necessidade do desenvolvimento de estudos que deem visibilidade à temática, pois fica evidente a escassez de estudos com a participação de outros profissionais de saúde e a lacuna de conhecimento sobre o assunto e o correto manejo, notadamente na condução de intervenções específicas a sua área de competência, de intervenções conjuntas e de intervenções não farmacológicas.
REFERÊNCIAS
Curt GA, Breitbart W, Cella D, Groopman JE, Horning SJ, Itri LM, Johnson DH, Miaskowski C, Scherr SL, Portenoy RK, Vogelzang NJ. Impact of cancer-related fatigue onthelives of patients: new findings fromthe Fatigue Coalition. Oncoogist. 2000; 5(5):353-60. Disponível em:https://theoncologist.onlinelibrary.wiley.com/doi/pdfdirect/10.1634/theoncologist.5 -5-353.
FERLAY, J. et al. Cancer statistics for the year 2020: an overview. International Journal of Cancer, New York, Apr. 2021. DOI 10.1002/ijc.33588.
Gozzo TO, Nascimento TG, Panobianco MS, et al. Ocorrência de neutropenia em mulheres com câncer de mama durante tratamento quimioterápico. Acta PaulEnferm. 2011;24(6):810-4. doi: http://dx.doi. org/10.1590/s0103-21002011000600014.
Greaney ML, Sprunck-Harrild K, Ruddy KJ, et al. Study protocol for Young & Strong: a cluster randomized design to increase attention to unique issues faced by young women with newly diagnosed breast cancer. BMC Public Health. 2015 Jan;31;15:37. doi: http://dx.doi. org/10.1186/s12889-015-1346-9.
HERNANDEZ, M.C.T; MARTINEZ,A.H. Neutropenia febril inducida por quimioterapia e infecciones asociadas: uma revision de La literatura. Gazeta mexicana de oncología. 2019; 18:333-338. Disponível em:https://www.semanticscholar.org/paper/Neutropenia-febril-inducida-por-quimioterapia-e-una-Thowinson-Hern%C3%A1ndez-Hern%C3%A1ndez-Mart%C3%ADnez/fd60f8479af3ac28967fa7a42e7ba2989699e54c
Instituto Nacional de Câncer Jose Alencar Gomes da Silva (INCA). Tratamento do câncer no SUS[Internet]. Rio de Janeiro; 2015[cited 2015 Oct 21];94-8. Available from: http://www.inca.gov.br/situacao/arquivos/acoes_tratamento_cancer_sus.pdf
Instituto Nacional de Câncer José Alencar Gomes da Silva. ABC do câncer: abordagens básicas para o controle do câncer. 6. ed. rev. e atual. Rio de Janeiro: INCA; 2020. Disponível em:https://www.inca.gov.br/sites/ufu.sti.inca.local/files//media/document/livro_abc_6ed_0 .pdf.
Lopes CMM, Galvão CM. Surgical Positioning: evidence for nursing care. Rev Latino-Am Enferm [Internet]. 2010 [cited 2016 Mar 03];18(2):287-94. Available from: » http://dx.doi.org/10.1590/S0104-11692010000200021
Ministério da Saúde Instituto Nacional de Câncer José Alencar Gomes da Silva Ministério da Saúde Instituto Nacional de Câncer. [s.l: s.n.]. Disponível em:<https://www.inca.gov.br/sites/ufu.sti.inca.local/files//media/document//estimativa-202 3.pdf>.
MIGOWSKI, A. et al. Guidelines for early detection of breast cancer in Brazil. II New national recommendations, main evidence, and controversies. Cadernos de Saúde Publica, Rio de Janeiro, v. 34, n. 6, 2018. DOI 10.1590/0102-311X00074817.
Souza MT, Silva MD, Carvalho R. Revisão integrativa: o que é e como fazer. Einstein[Internet]. 2010;8(1Pt1):102-6. Available from: http://www.scielo.br/pdf/eins/v8n1/pt_1679-4508-eins-8-1-0102.pdf » http://www.scielo.br/pdf/eins/v8n1/pt_1679-4508-eins-8-1-0102.pdf
SUNG, H. et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: Cancer Journal for Clinicians, Hoboken, v. 71, n. 3, p. 209-249, Feb. 2021. DOI 10.3322/caac.21660.
Ishikawa T, Sakamaki K, Narui K, Nishimura H, Sangai T, Tamaki K, Hasegawa Y, Watanabe KI, Suganuma N, Michishita S, Sugae S, Aihara T, Tsugawa K, Kaise H, Taira N, Mukai H; for Comprehensive Support Project for Oncological Research of Breast Cancer. Prospective cohort study of febrile neutropenia in breast cancer patients administered with neoadjuvant and adjuvant chemotherapies: CSPOR-BC FN study. Breast. 2021 Apr;56:70-77.doi:10.1016/j.breast.2021.01.005. Epub 2021 Feb 16. PMID: 33631458; PMCID: PMC7907535.
Ferreira JN, Correia LRBR, Oliveira RM, Watanabe SN, Possari JF, Lima AFC. Managing febrile neutropenia in adult cancer patients: an integrative review of the literature. Rev Bras Enferm [Internet]. 2017;70(6):1301-8. DOI: http://dx.doi.org/10.1590/0034-7167-2016-0247
Neutropenia Associada ao Tratamento do Câncer de Mama: Revisão Integrativa da Literatura.Fernanda Mocellin Conte ; Valéria Sgnaolin ; Vanessa Sgnaolin. Disponível em: https://rbc.inca.gov.br/index.php/revista/article/view/307/495> . Acesso em: 20 dez. 2023.
Zekri J, Nawaz A, Rasool H, et al. Impact of granulocyte-colony stimulating factor on docetaxel-induced febrile neutropenia in patients with breast cancer. Journal of Oncology Pharmacy Practice. 2022;28(8):1681-1686. i:10.1177/10781552211030974
Kimura, Y., Sasada, S., Emi, A. et al. Febrile neutropenia and role of prophylactic granulocyte colony-stimulating factor in docetaxel and cyclophosphamide chemotherapy for breast cancer. Support Care Cancer 29, 3507–3512 (2021).https://doi.org/10.1007/s00520-020-05868-1
Fernandes R, Mazzarello S, Stober C, Ibrahim MFK, Dudani S, Perdrizet K, Majeed H, Vandermeer L, Shorr R, Hutton B, Fergusson D, Gyawali B, Clemons M. Primary
Febrile Neutropenia Prophylaxis for Patients Who Receive FEC-D Chemotherapy for Breast Cancer: A Systematic Review. J Glob Oncol. 2018 Sep;4:1-8. doi: 10.1200/JGO.2016.008540. Epub 2017 Apr 21. PMID: 30241156; PMCID: PMC6180804.
Bacrie, J., Laurans, M., Iorio, P. et al. Febrile neutropenia in adjuvant and neoadjuvant chemotherapy for breast cancer: a retrospective study in routine clinical practice from a single institution. Support Care Cancer 26, 4097–4103 (2018). https://doi.org/10.1007/s00520-018-4280-4
Van Laar SA, Gombert-Handoko KB, Wassenaar S, Kroep JR, Guchelaar HJ, Zwaveling J. Real-world evaluation of supportive care using an electronic health record text-mining tool: G-CSF use in breast cancer patients. Support Care Cancer. 2022 Nov;30(11):9181-9189. doi: 10.1007/s00520-022-07343-5. Epub 2022 Aug 31. PMID: 36044088; PMCID: PMC9633501.
Mahtani RL, Belani R, Crawford J, Dale D, DeCosta L, Gawade PL, Huynh C, Lawrence T, Lewis S, MacLaughlin WW, Narang M, Rifkin R. A prospective cohort study to evaluate the incidence of febrile neutropenia in patients receiving pegfilgrastim on-body injector versus other options for prophylaxis of febrile neutropenia: breast cancer subgroup analysis. Support Care Cancer. 2022 Jul;30(7):6135-6144. doi: 10.1007/s00520-022-07025-2. Epub 2022 Apr 14. PMID: 35426046; PMCID: PMC9009498.
Portal Cancer de mama Brasil . AC-T (Doxorrubicina, ciclofosfamida e paclitaxel),2022. Disponivel em: https://www.cancerdemamabrasil.com.br/ac-t-doxorrubicina-ciclofosfamida-e-paclitax el
SOCIEDADE BRASILEIRA DE ONCOLOGIA. Guia Prático para oncologista clinico. São Paulo, SP. 2012.Disponívelem: http://www.sboc.org.br/app/webroot/downloads/Guia-Pratico-para-o-Oncologista-Cl%C3%ADnico-%20erratas-e-complementos.pdf
