THE DUALITY OF CANNABIDIOL TREATMENT: POSITIVE AND NEGATIVE PERSPECTIVES ON THE DEVELOPMENT OF INDIVIDUALS WITH AUTISM
REGISTRO DOI: 10.69849/revistaft/cs10202409071545
Maria Eduarda Teixeira Oliveira
Camilly Gouveia Pupio
Maria Fernanda de Almeida Theodoro
Orientadora: Sandra Cristina Catelan-Mainardes
RESUMO
A presente revisão objetiva compreender as perspectivas positivas e negativas do tratamento com canabidiol no desenvolvimento de indivíduos com autismo. A fim de alcançar o objetivo geral proposto _ Investigar a eficácia e os mecanismos de ação do canabidiol (CBD) no tratamento do transtorno do espectro do autismo (TEA), o estudo de cunho bibliográfico apresentado deu-se na forma de revisão integrativa de literatura, partindo das referências dos anos de 2019 a 2024, buscadas nas bases de dados PubMed e SciELO, a partir dos critérios de verificação do método PRISMA. O transtorno do espectro autista (TEA) é um transtorno do neurodesenvolvimento caracterizado por déficits persistentes na comunicação social e na interação social, associados à presença de padrões restritos e repetitivos de comportamento, interesses ou atividades. Os achados indicaram que os produtos de cannabis reduziram sintomas como hiperatividade, automutilação, problemas de sono, ansiedade, agitação, irritabilidade, agressividade e depressão, além de melhorar a cognição, sensibilidade sensorial, atenção, interação social e linguagem. Os efeitos adversos mais comuns foram distúrbios do sono, inquietação, nervosismo e alteração do apetite. Apesar desses resultados positivos, a revisão conclui que não há evidências suficientes para sustentar a eficácia do canabidiol como tratamento para o TEA, haja vista que a maioria dos estudos disponíveis é observacional com amostras pequenas e critérios pouco definidos, tornando o canabidiol uma intervenção experimental e hipotética para o autismo no momento.
Palavras-chave: Canabinóides. Transtorno do Neurodesenvolvimento. Benefícios e Riscos.
ABSTRACT
This review aims to understand the positive and negative perspectives of cannabidiol treatment on the development of individuals with autism. In order to achieve the proposed general objective _ Investigate the effectiveness and mechanisms of action of cannabidiol (CBD) in the treatment of autism spectrum disorder (ASD), the bibliographic study presented took the form of an integrative literature review, based on references from the years 2019 to 2024, searched in the PubMed and SciELO databases, based on the verification criteria of the PRISMA method. Autism spectrum disorder (ASD) is a neurodevelopmental disorder characterized by persistent deficits in social communication and social interaction, associated with the presence of restricted and repetitive patterns of behavior, interests or activities. Findings indicated that cannabis products reduced symptoms such as hyperactivity, self-harm, sleep problems, anxiety, agitation, irritability, aggression and depression, as well as improving cognition, sensory sensitivity, attention, social interaction and language. The most common adverse effects were sleep disturbances, restlessness, nervousness and changes in appetite. Despite these positive results, the review concludes that there is not enough evidence to support the effectiveness of cannabidiol as a treatment for ASD, given that most of the available studies are observational with small samples and poorly defined criteria, making cannabidiol an experimental intervention and hypothesis for autism at the moment.
Keywords: Cannabinoids. Neurodevelopmental Disorder. Benefits and Risks.
1. INTRODUÇÃO
O Transtorno do Espectro Autista (TEA) é uma condição neurológica complexa que afeta o desenvolvimento infantil e persiste ao longo da vida, caracterizada por déficits na comunicação, interação social e padrões repetitivos de comportamento. Embora as intervenções comportamentais e farmacológicas convencionais tenham sido amplamente utilizadas para gerenciar os sintomas do TEA, muitos indivíduos continuam a enfrentar desafios significativos e não respondem adequadamente aos tratamentos disponíveis.
Nesse contexto, uma área emergente de pesquisa e interesse clínico tem se concentrado na potencialidade terapêutica da cannabis, especificamente de seus componentes ativos, os canabinoides, para o tratamento do TEA. A cannabis tem sido historicamente utilizada por suas propriedades medicinais em várias culturas e, mais recentemente, tem havido um interesse renovado na investigação de seus possíveis benefícios para uma variedade de condições de saúde, incluindo distúrbios neuropsiquiátricos como o TEA.
O foco deste trabalho é explorar a relação entre a cannabis e a melhora dos sintomas do TEA, com um destaque particular no canabidiol (CBD), um dos principais canabinoides encontrados na planta de cannabis. O CBD tem ganhado atenção significativa devido às suas propriedades terapêuticas potenciais e à sua relativa ausência de efeitos psicoativos, em contraste com o tetraidrocanabinol (THC), outro canabinoide comumente encontrado na cannabis.
Embora ainda existam controvérsias e lacunas no conhecimento sobre o uso de cannabis, incluindo o CBD, no tratamento do TEA, evidências preliminares sugerem que essas substâncias podem oferecer benefícios significativos para os indivíduos afetados. Relatos de pais e cuidadores, bem como alguns estudos clínicos e pré-clínicos, destacam a melhoria de sintomas como agressão, ansiedade, hiperatividade e padrões repetitivos de comportamento após o uso de cannabis ou CBD.
No entanto, é fundamental abordar essa questão com cautela e rigor científico, considerando aspectos como eficácia, segurança, mecanismos de ação e potenciais efeitos adversos associados ao uso de cannabis, especialmente em uma população vulnerável como a de indivíduos com TEA.
Portanto, este trabalho busca fornecer uma revisão de dez artigos acerca da literatura atual sobre o uso de cannabis, particularmente o CBD, no tratamento do TEA, examinando as evidências disponíveis. Ao fazer isso, visa-se contribuir para uma compreensão mais aprofundada dos potenciais benefícios e limitações da cannabis como uma opção terapêutica para indivíduos com TEA e suas famílias.
O objetivo do trabalho é investigar a eficácia e os mecanismos de ação do canabidiol (CBD) no tratamento do transtorno do espectro do autismo (TEA), fornecendo uma análise de algumas evidências disponíveis, contribuindo para uma compreensão mais profunda dos benefícios terapêuticos e implicações clínicas do CBD para indivíduos com TEA. E os objetivos específicos foram analisar estudos clínicos e pré-clínicos que investigaram o uso de CBD no tratamento do transtorno autista, incluindo suas metodologias, resultados e conclusões. Avaliar a eficácia do CBD nos sintomas do TEA na redução de sintomas específicos associados ao transtorno autista, como ansiedade, agressividade, hiperatividade, problemas de sono e comunicação social. Identificar efeitos adversos e segurança associados ao uso de CBD no tratamento do transtorno autista.
A justificativa para o estudo do tema em análise é multifacetada e baseada em várias considerações:
Necessidade de Alternativas Terapêuticas:
Evidências e Precedentes de Pesquisa: Há uma quantidade crescente de relatos de pais e cuidadores sobre os efeitos positivos da cannabis no controle de sintomas associados ao autismo, como ansiedade, agressão e problemas de sono. Além disso, estudos pré-clínicos e clínicos emergentes sugerem que certos compostos presentes na cannabis podem ter propriedades terapêuticas relevantes para o TEA.
Necessidade de Pesquisa Adicional e Esclarecimento: Embora haja evidências preliminares sugerindo benefícios potenciais da cannabis para o TEA, ainda há muitas perguntas sem resposta e áreas que necessitam de mais investigação. Dessa forma, estudos dedicados a essa questão podem ajudar a consolidar o estado atual do conhecimento, além de fornecer orientações para estudos futuros.
Prevalência e Impacto Social: A crescente prevalência do transtorno do espectro autista coloca uma pressão significativa sobre as famílias, sistemas de saúde e a sociedade como um todo. Identificar tratamentos eficazes pode aliviar essa carga, proporcionando melhor suporte e intervenções para os indivíduos afetados e seus cuidadores.
Segurança e Eficácia: Avaliar a segurança e a eficácia do canabidiol é crucial, especialmente considerando os potenciais efeitos adversos e a necessidade de dosagens apropriadas. Uma análise rigorosa pode ajudar a estabelecer protocolos de uso seguros e eficazes, beneficiando os pacientes com TEA.
Contribuição Científica: A pesquisa sobre o canabidiol no tratamento do autismo pode contribuir significativamente para a ciência médica e a neurociência. Compreender os efeitos e o potencial terapêutico do canabidiol pode abrir novos caminhos para o tratamento de outros transtornos do neurodesenvolvimento.
Mediante o exposto e com a justificativa de compreender as perspectivas positivas e negativas do tratamento com canabidiol no desenvolvimento de indivíduos com autismo, o presente trabalho visa, através de uma revisão de literatura, fornecer subsídios para que os profissionais possam avaliar de maneira mais precisa os sinais comportamentais, cognitivos e motores que as crianças com TEA apresentam com o uso do canabidiol, de tal forma a aprimorar o diagnóstico e a intervenção precoce na prática médica, contribuindo para melhorar a qualidade de vida dessas pessoas.
Doenças neurológicas e psiquiátricas são condições médicas complexas e multifatoriais que afetam milhões de pessoas, prevalecendo dentre as causas incapacitantes mais comuns. Após a publicação, pela Agência Nacional de Vigilância Sanitária (Anvisa), de propostas para a regulamentação do cultivo e produção de medicamentos à base de cannabis no Brasil, o debate em torno do tema se acirrou.
De acordo com a Classificação Internacional de Doenças (CID-10), o autismo infantil é considerado um Transtorno Global do Desenvolvimento (CID 10 – F84.0) que, por sua vez, é caracterizado por um conjunto de condições que geram dificuldades de comunicação, prejudicando a interação social das pessoas acometidas (BRASIL, 2022). Segundo a OMS, em todo o mundo, estima-se que 1 em cada 160 crianças apresenta TEA .1
O autismo é um diagnóstico comportamental cuja causa exata é desconhecida e atualmente não foram identificados biomarcadores. Vários fatores, incluindo ambientais, biológicos e genéticos, desempenham um papel na patogênese do TEA. Aproximadamente 15–20% dos casos de TEA foram associados a mutações genéticas . O retardo mental do X 2 frágil 1 (FMR1) é a mutação genética única mais comum identificada em indivíduos autistas 3 . Outras mutações genéticas únicas que demonstraram estar associadas ao TEA incluem 4 5 6 7 esclerose tuberosa, neurofibromatose, síndrome de Angelman e síndrome de Rett . A 8 disfunção imunológica e a inflamação, bem como a exposição fetal a drogas antiepilépticas contribuem para a patogênese do autismo. 9 10 11 12 13 14 15
O canabidiol (CBD) é um composto encontrado na planta da cannabis. É um dos muitos canabinóides encontrados na cannabis, mas é o único que não tem efeitos psicoativos. O CBD tem sido estudado como uma terapia potencial para uma variedade de condições, incluindo o TEA. Há alguma evidência de que o CBD pode ser eficaz no tratamento de alguns sintomas do TEA. No entanto, pesquisas são necessárias para determinar a eficácia e a segurança do CBD para o tratamento do TEA.
O CBD é um dos canabinoides mais abundantes presentes nas plantas do gênero cannabis. Atua como antagonista dos receptores CB1 e CB2 e inibidor da recaptação e metabolismo da anandamida. O Canabidiol 200 mg/mL possui apenas autorização sanitária da ANVISA permitindo sua comercialização, uma vez que os testes clínicos necessários para o registro definitivo ainda estão em andamento. 16 17
2. MATERIAIS E MÉTODOS
Trata-se de uma pesquisa de caráter descritivo, do tipo revisão de literatura integrativa, que reuniu artigos coletados das seguintes fontes bibliográficas: Index SciELO (Scientific Electronic Library Online) e PubMed (United States National Library of Medicine). Optou-se por utilizar os dados referentes aos anos 2019 a 2024. Para cruzamento de dados e obtenção do maior número de amostras possível, as autoras utilizaram denominadores booleanos AND e OR, e os buscadores “Transtorno do Espectro Autista” e “Canadibiol”. O delineamento da pesquisa bibliográfica, organização e tratamento das informações foram realizados através de técnicas de leitura exploratória, interpretativa e seletiva. Como critério de elegibilidade, foram utilizados apenas artigos científicos completos e gratuitos, estudos de casos, estudos de coorte, estudos retrospectivos observacionais, revisões sistemáticas, meta-análises, estudos experimentais e quase experimentais, em língua inglesa e portuguesa. O escore Preferred Reporting Items for Systematic Reviews and Meta-Analysis (PRISMA) e PRISMA 2020 flow diagram serviram como ferramentas de verificação e pontuação de credibilidade das fontes utilizadas. As duplicatas e os artigos que não responderam à pergunta norteadora foram excluídos. Em última etapa, após organização e análise de dados, os artigos foram analisados por ambas as autoras e as informações necessárias para a realização da revisão foram extraídas.
3. APRESENTAÇÃO DOS DADOS (RESULTADOS)
A estratégia de busca resultou em um total de 45 artigos: PubMed (n = 34), SciELO (11), publicados entre os anos de 2019 e 2024. A comunidade biomédica latino-americana tem a PubMed e a SciELO como as melhores bases de dados para pesquisa de artigos científicos. Deve-se esclarecer que, no total, foram 96 artigos estudados, cuja maioria não se encaixava nos critérios estabelecidos pelas autoras. Após análise inicial e triagem por título e palavras chave, 51 artigos foram descartados por não responderem a pergunta norteadora da presente revisão ou por outros motivos, os quais foram elencados no fluxograma abaixo. Destaca-se que também foram descartados vários estudos por enfocar mais a epilepsia do que o autismo. Em segunda análise, os 45 artigos elegíveis até então, foram triados a partir do resumo, e selecionados apenas os 10 que responderam satisfatoriamente a pergunta norteadora. Durante ambas as pesquisas, não foram encontradas duplicatas ou qualquer outro problema que tornasse os registros inelegíveis para revisão, que não o motivo já mencionado previamente sobre a pergunta norteadora. Dentre os estudos elegidos para revisão, 09 deles foram redigidos na língua inglesa, 1 em língua portuguesa e nenhum em língua espanhola. Na figura abaixo, o fluxograma PRISMA demonstra a ordem de seleção e os motivos de exclusão das publicações avaliadas para elegibilidade na revisão.
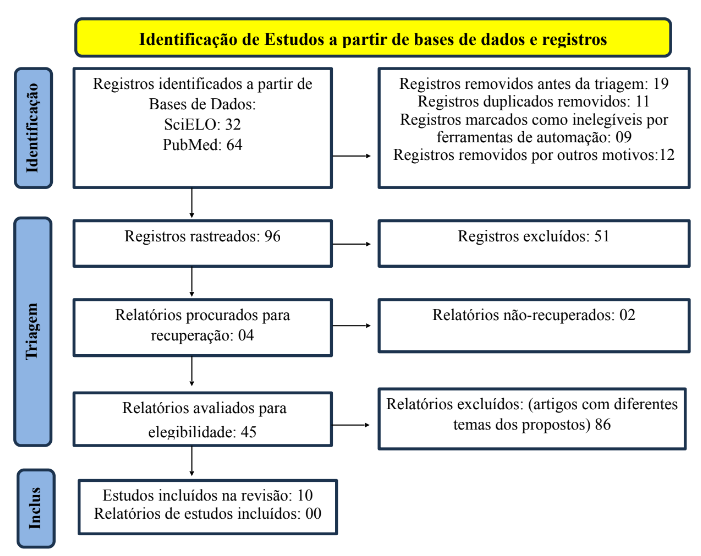
Figura 1. Fluxograma de Itens de Relatório Preferenciais para revisões Sistemáticas e Meta-análises (PRISMA) mostrando a identificação, triagem e trabalhos incluídos no artigo.
Fonte: As autoras (2023)
Quadro 1: Relação de artigos científicos levantados e analisados na pesquisa de revisão.
AUTORES DEFINIÇÃO Adi Aran , Hanoch Cassuto , Asael Lubotzky , Nadia Wattad , Ester Hazan (2019) Breve relatório: cannabis rica em canabidiol em crianças com transtorno do espectro do autismo e problemas comportamentais graves – um estudo retrospectivo de viabilidade Lihi Bar-Lev Schleider , Rafael Mechoulam , Naama Saban , Gal Meiri , Victor Novack (2019) Experiência da vida real de tratamento com cannabis medicinal no autismo: análise de segurança e eficácia Ana Maria Costa da Silva Lopes (2019) O autismo e suas conexões: qual medicação para o autista? Mojdeh Mostafavi , John Gaitanis (2020) Transtorno do espectro do autismo e cannabis medicinal: revisão e experiência clínica Adi Aran , Moria Harel , Hanoch Cassuto , Lola Polyansky , Aviad Schnapp , Nadia Wattad , Dorit Shmueli , Daphna Golan , F. Xavier Castellanos (2021) Tratamento com canabinóides para o autismo: um ensaio randomizado de prova de conceito Estácio Amaro da Silva Junior, Wandersonia Moreira Brito Medeiros, Nelson Torro , João Marçal Medeiros de Sousa , Igor Bronzeado Cahino Moura de Almeida , Filipe Barbosa da Costa , Katiúscia Moreira Pontes, Eliane Lima Guerra Nunes, Marine Diniz da Rosa , Katy Lísias Gondim Dias de Albuquerque (2022) Uso de cannabis e canabinóides no transtorno do espectro do autismo: uma revisão sistemática Abhinaya ganesh, safiullah shareef (2022) Segurança e eficácia da cannabis no transtorno do espectro do autismo Mariana Babayeva , Haregewein Assefa , Paramita Basu , Zvi Loewy (2022) Autismo e distúrbios associados: cannabis como terapia potencial Adi Aran , Moria Harel , Aminadav Ovadia , Shulamit Shalgy e Dalit Cayam Rand (2023) Mediadores da resposta do placebo ao tratamento com canabinoides em crianças com transtorno do espectro do autismo Estácio Amaro da Silva Júnior, Wandersônia Moreira Brito Medeiros, João Paulo Mendes dos Santos, João Marçal Medeiros de Sousa, Filipe Barbosa da Costa, Katiúscia Moreira Pontes, Thaís Cavalcanti Borges, Carlos Espínola Neto Segundo, Ana Hermínia Andrade e Silva, Eliane Lima Guerra Nunes, Nelson Torro Alves, Marina Diniz da Rosa, Katy Lísias Gondim Dias de Albuquerque (2024) Avaliação da eficácia e segurança do extrato de cannabis rico em canabidiol em crianças com transtorno do espectro do autismo: ensaio clínico randomizado, duplo-cego e controlado por placebo
1 Estácio Amaro da Silva Junior , Wandersonia Moreira Brito Medeiros , Nelson Torro , João Marçal Medeiros de Sousa , Igor Bronzeado Cahino Moura de Almeida , Filipe Barbosa da Costa , Katiúscia Moreira Pontes , Eliane Lima Guerra Nunes , Marine Diniz da Rosa , Katy Lísias Gondim Dias de Albuquerque . Uso de cannabis e canabinóides no transtorno do espectro do autismo: uma revisão sistemática.
Métodos: revisão sistemática de estudos que investigaram os efeitos clínicos do uso de cannabis e canabinoides no TEA, de acordo com o Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA checklist). A busca foi realizada em quatro bases de dados: MEDLINE/PubMed, Scientific Electronic Library Online (SciELO), Scopus e Web of Science. Não foram estabelecidos limites de idioma durante o processo seletivo. Nove estudos foram selecionados e analisados.
Resultados: alguns estudos mostraram que os produtos de cannabis reduziram o número e/ou intensidade de diferentes sintomas, incluindo hiperatividade, ataques de automutilação e raiva, problemas de sono, ansiedade, inquietação, agitação psicomotora, irritabilidade, agressividade, perseverança e depressão. Além disso, encontraram melhora na cognição, sensibilidade sensorial, atenção, interação social e linguagem. Os efeitos adversos mais comuns foram distúrbios do sono, inquietação, nervosismo e alteração do apetite.
Conclusão: a cannabis e os canabinóides podem ter efeitos promissores no tratamento dos sintomas relacionados ao TEA, podendo ser utilizados como alternativa terapêutica no alívio desses sintomas. No entanto, ensaios clínicos randomizados, cegos e controlados por placebo são necessários para esclarecer os resultados sobre os efeitos da cannabis e dos seus canabinóides em indivíduos com TEA.
2 Ganesh, Abhinaya, Shareef Safiullah. Segurança e eficácia da cannabis no transtorno do espectro do autismo.
Métodos: Investigadores do Centro Médico da Universidade Soroka, da Universidade Hebraica de Jerusalém e da Tikun Olam Ltd. em Israel estudaram a segurança e a eficácia do tratamento com cannabis medicinal em 188 pacientes durante seis meses. A segurança do CBD foi examinada através da avaliação dos efeitos secundários fisiológicos e cognitivos. O maior fornecedor nacional de cannabis medicinal em Israel empregou vários dos autores e patrocinou este estudo.
Resultados: os resultados dos pacientes e os efeitos colaterais foram registrados apenas nos meses um e seis; a seleção deste período de acompanhamento específico não é claramente explicada. A segurança a longo prazo do CBD para pacientes do espectro do TEA não é clara. O autorrelato subjetivo dos pais dos pacientes foi utilizado como base deste estudo. As expectativas dos pais provavelmente influenciaram os seus relatórios.
Conclusão: A avaliação das percepções e expectativas dos pais em relação à segurança e eficácia no início do estudo poderia ter elucidado esses fatores potencialmente confundidores. Além disso, este estudo foi patrocinado por um grande fabricante local de CBD e a população do estudo estava utilizando o produto. São necessários ensaios clínicos prospectivos, independentes e controlados por placebo para determinar a eficácia a longo prazo e as diretrizes de dosagem mais precisas para o CBD no TEA.
3 Mojdeh Mostafavi, John Gaitanis. Transtorno do espectro do autismo e cannabis medicinal: revisão e experiência clínica
Métodos: Esta revisão relata os dados pré-clínicos e clínicos disponíveis sobre o uso de cannabis e canabidiol no tratamento de sintomas principais, sintomas não essenciais e comorbidades associadas ao TEA. Além disso, os autores descrevem sua experiência clínica trabalhando com crianças e adultos jovens com TEA que usaram cannabis ou canabidiol.
Resultados: A descoberta dos canabinoides exógenos levou à subsequente descoberta do sistema endocanabinoide, responsável pela modulação de muitos sistemas orgânicos, incluindo o sistema nervoso central e periférico, o sistema endócrino, o sistema cardiovascular, o sistema imunológico, o trato gastrointestinal e o sistema reprodutivo. Dentro do sistema endocanabinóide, existem 2 tipos primários de receptores canabinóides, canabinóide tipo 1 (CB1) e canabinóide tipo 2 (CB2), cada um com distribuição tecidual única. Os CB1 pós-sinápticos parecem regular a excitabilidade e a plasticidade sináptica via modulação de canais de K+ e inibição da adenilciclase [com ativação da mitogen activated protein kinase (MAPK) e inibição da PKA]. Os CB2 são expressos, sobretudo, no sistema imunológico. Já foi descrita a presença de CB2 em algumas áreas do SNC, especialmente na microglia e em localização pós-sináptica. Verificou-se aumento da expressão de CB2 em determinados estados patológicos do SNC, nomeadamente dor crônica.
Conclusão: Atualmente, os dados pré-clínicos e clínicos sugerem um potencial benefício terapêutico entre algumas pessoas com PEA e que é globalmente bem tolerado. Mais pesquisas são necessárias para melhor identificar os pacientes que podem se beneficiar do tratamento sem efeitos adversos.
4. Adi Aran , Moria Harel , Aminadav Ovadia , Shulamit Shalgy, Dalit Cayam-Rand. Mediadores da resposta do placebo ao tratamento com canabinóides em crianças com transtorno do espectro do autismo
Métodos: Este estudo retrospectivo investigou possíveis mediadores da resposta ao placebo entre participantes de um ensaio controlado por placebo de tratamento com canabinóides para problemas comportamentais em crianças com TEA (ensaio CBA, idades entre 5 e 21 anos). Usou-se um questionário especificamente elaborado para explorar possíveis mediadores da resposta ao placebo em 88 participantes do estudo CBA que receberam placebo e tiveram resultados válidos. Os pais de 67 participantes responderam ao questionário. A resposta placebo foi positivamente associada à compreensão da criança sobre o objetivo do tratamento. Houve também uma tendência para os participantes que tiveram um agravamento relativo dos sintomas antes do início do tratamento melhorarem após o tratamento com placebo. Nenhum outro domínio, incluindo expectativas dos pais, experiência positiva anterior com tratamentos semelhantes (condicionamento comportamental), locus de controle dos pais, qualidade das relações médico-paciente e adesão aos medicamentos do estudo foram associados à resposta ao placebo.
Resultados: A resposta placebo foi positivamente associada à compreensão da criança sobre o objetivo do tratamento. Houve também uma tendência para os participantes que tiveram um agravamento relativo dos sintomas antes do início do tratamento melhorarem após o tratamento com placebo. Nenhum outro domínio, incluindo expectativas dos pais, experiência positiva anterior com tratamentos semelhantes (condicionamento comportamental), locus de controle dos pais, qualidade das relações médico-paciente e adesão aos medicamentos do estudo foram associados à resposta ao placebo.
Conclusão: Apesar da importância da resposta ao placebo em ambientes clínicos e de investigação, os estudos que investigam os mediadores da resposta ao placebo em crianças com deficiência são escassos. Em adultos com funcionamento cognitivo normal, a expectativa de tratamento é um dos principais mediadores da resposta ao placebo. Contudo, em crianças com deficiência, a associação entre a capacidade da criança de compreender o propósito do tratamento e a resposta ao placebo não foi explorada anteriormente. Numa coorte de crianças e adolescentes com TEA, descobriu-se que a resposta ao placebo estava principalmente associada à compreensão da criança sobre o propósito do tratamento, e não às expectativas dos pais. Estas conclusões enfatizam a importância de explicar o propósito do tratamento às crianças com deficiência de uma forma que elas possam compreender. Esta estratégia pode melhorar o resultado do tratamento na prática clínica e diminuir as diferenças na resposta ao placebo entre os participantes, o que potencialmente leva ao fracasso do estudo em ensaios clínicos.
5 Babayeva , Mariana, Haregewein Assefa , Paramita Basu , Zvi Loewy. Autismo e distúrbios associados: cannabis como terapia potencial
Métodos: O artigo apresenta uma revisão abrangente sobre: (i) Mudanças no sistema endocanabinoide no autismo (ii) Efeito da cannabis no autismo (iii) Efeito da cannabis nos transtornos associados ao autismo e apresenta vários estudos científicos sobre o efeito da cannabis nos indivíduos com autismo.
Resultados: com base nos dados disponíveis, a cannabis foi considerada uma escolha segura e eficaz para aliviar os sinais de TEA, porém a cannabis não produz apenas efeitos terapêuticos, mas também cria complicações perigosas para a saúde. Uma grande preocupação é o impacto da cannabis no cérebro, pois prejudica o seu desenvolvimento normal e pode resultar em alterações neurocognitivas potencialmente não reversíveis. Foi demonstrado que o uso de cannabis prejudica funções cognitivas básicas, como coordenação motora, até funções executivas mais complexas. Também foi associada a problemas cognitivos como dependência, percepções distorcidas, dificuldade de pensamento e resolução de problemas, déficits de memória de trabalho e comportamento social anormal. Além disso, descobriu-se que os indivíduos com deficiências relacionadas com a cannabis têm dificuldades para uma recuperação bem sucedida, colocando-os em maior risco de recaída no consumo de cannabis. Além disso, o término do uso de cannabis não restaurou totalmente o funcionamento neuropsicológico entre os usuários com início na adolescência, além de agir como agravante ou mascarador de sintomas psiquiátricos, especialmente em jovens.
Conclusão: Embora os estudos clínicos tenham mostrado resultados promissores do tratamento com cannabis no TEA e distúrbios associados, existem dados limitados que apoiam o efeito claro da cannabis/canabinóides em diferentes fenótipos de TEA. Mais investigações clínicas são necessárias para descobrir a eficácia, segurança e dosagem da terapia. Isto seria um avanço significativo no tratamento do autismo e poderia levar a uma melhoria do funcionamento e da qualidade de vida dos pacientes e suas famílias.
6 Ana Maria Costa da Silva Lopes. O autismo e suas conexões: qual medicação para o autista?
Métodos: Empregou-se como metodologia a revisão narrativa neste trabalho que enfoca a conexão entre psicanálise e psiquiatria, com base na questão: qual medicação para o autista? Embora não tenha, como objetivo principal, enfocar a eficácia, ou não, da cannabis no tratamento do autismo, o artigo analisa o uso de canabinoides para o manejo de sintomas de TEA.
Resultados: As evidências científicas demonstram que não há uma medicação específica para o autismo, mas sintomas específicos que perturbem a funcionalidade da vida diária, tais como insônia, agressividade, agitação, entre outros, podem ser medicados. A psiquiatria e seu arsenal terapêutico, por meio do ato de medicar, entram no lugar de parceiro do analista, possibilitando que o sujeito não seja reduzido a ser um simples objeto de diagnóstico, em nome de uma suposta “normalidade”. A medicação pode contribuir de forma pontual, descontínua ou, por vezes, contínua, possibilitando o percurso do tratamento analítico.
Conclusão: Estudos em modelos animais sugerem uma possível desregulação do sistema endocanabinoide no TEA (Bar-Lev Schleider, Mechoulam, Saban, Meiri, & Novack, 2019). O sistema endocanabinoide está envolvido na regulação de neurotransmissores excitatórios e inibitórios, sistemas esses comprometidos em indivíduos com TEA. Esse sistema também está envolvido na modulação da liberação de ocitocina e vasopressina, que, por sua vez, atuam modulando comportamentos sociais. Até o presente momento, o uso de canabinoides para o manejo de sintomas de TEA se baseia em relatos de casos ou ensaios clínicos abertos, não controlados, e com número restrito de participantes. Nesses casos, o canabinoide de escolha tem sido o dronabinol, formulação sintética do tetraidrocanabinol (THC), já em uso entre adultos, para o controle da náusea associada à quimioterapia, redução da hipertonia e da dor neuropática em pacientes com esclerose múltipla (Koppel et al., 2014).
7 Adi Aran , Moria Harel , Hanoch Cassuto , Lola Polyansky , Aviad Schnapp , Nadia Wattad , Dorit Shmueli , Daphna Golan , F. Xavier Castellanos. Tratamento com canabinóides para o autismo: um ensaio randomizado de prova de conceito
Métodos: o estudo testou um extrato de planta inteira de cannabis contendo canabidiol e Δ9-tetrahidrocanabinol na proporção de 20:1 e canabidiol e Δ9- tetrahidrocanabinol na mesma proporção, porém purificados. Os participantes (N = 150) receberam placebo ou canabinóides por 12 semanas (teste de eficácia), seguido por um washout de 4 semanas e um cruzamento predeterminado por mais 12 semanas para avaliar melhor a tolerabilidade. As mudanças nos escores totais do HSQ-ASD (desfecho primário) e APSI (desfecho secundário) não diferiram entre os grupos. O comportamento disruptivo no CGI-I (resultado co-primário) foi melhorado ou muito melhorado em 49% no extrato de planta inteira (n = 45) versus 21% no placebo (n = 47). A pontuação total SRS mediana (resultado secundário) melhorou em 14,9 no extrato de planta inteira (n = 34) versus 3,6 pontos após placebo (n = 36)). Não houve eventos adversos graves relacionados ao tratamento. Os eventos adversos comuns incluíram sonolência e diminuição do apetite, relatados para 28% e 25% no extrato de planta inteira, respectivamente (n = 95); 23% e 21% em canabinóides puros (n = 93), e 8% e 15% em placebo (n = 94).
Resultados: As alterações nas pontuações totais do HSQ-ASD (desfecho primário) e APSI (desfecho secundário) não diferiram entre os grupos. O comportamento disruptivo no CGI-I (resultado coprimário) melhorou muito ou muito em 49% no extrato de planta inteira (n = 45) versus 21% no placebo (n = 47; p = 0,005). A pontuação total mediana do SRS (desfecho secundário) melhorou em 14,9 no extrato de planta inteira (n = 34) versus 3,6 pontos após o placebo (n = 36); p = 0,009). Não houve eventos adversos graves relacionados ao tratamento. Os eventos adversos comuns incluíram sonolência e diminuição do apetite, relatados em 28% e 25% no extrato de planta inteira, respectivamente (n = 95); 23% e 21% em canabinóides puros (n = 93) e 8% e 15% em placebo (n = 94). Limitações A falta de dados farmacocinéticos e uma ampla variedade de idades e níveis funcionais entre os participantes justificam cautela na interpretação dos resultados.
Conclusão: Este estudo intervencionista fornece evidências de que BOL-DP-O-01-W e BOL-DP-O-01, administrados por 3 meses, são bem tolerados. As evidências da eficácia destas intervenções são confusas e insuficientes. Recomenda-se mais testes de canabinóides no TEA.
8 Lihi Bar-Lev Schleider , Rafael Mechoulam , Naama Saban , Gal Meiri , Victor Novack . Experiência da vida real de tratamento com cannabis medicinal no autismo: análise de segurança e eficácia
Métodos: Os dados prospectivamente coletados como parte do programa de tratamento de pacientes com TEA tratados com cannabis medicinal foram coletados entre 2015 e 2017. O tratamento na maioria dos pacientes foi baseado no óleo de cannabis contendo 30% de CBD e 1,5% de THC. O inventário de sintomas, a avaliação global do paciente e os efeitos colaterais aos 6 meses foram desfechos de interesse e foram avaliados por questionários estruturados.
Resultados: Depois de seis meses de tratamento, dos 188 pacientes que iniciaram o procedimento, 82,4% (155) estavam em tratamento ativo e 60,0% (93) foram avaliados; 28 pacientes (30,1%) relataram melhora significativa, 50 (53,7%) moderada, 6 (6,4%), discreta e 8 (8,6%), nenhuma mudança em sua condição. Vinte e três pacientes (25,2%) apresentaram pelo menos um efeito colateral; a mais comum foi a inquietação (6,6%). Cannabis em pacientes com TEA parece ser bem tolerada, segura e uma opção eficaz para aliviar os sintomas associados ao TEA.
Conclusão: Recentemente, a cannabis enriquecida com CBD demonstrou ser benéfica para crianças com autismo. Nesta retrospectiva, um estudo em 60 crianças mostrou que surtos comportamentais foram melhorados em 61% dos pacientes, problemas de comunicação em 47%, ansiedade em 39%, estresse em 33% e comportamento disruptivo em 33% dos pacientes. A justificativa para isso: O tratamento baseia-se nas observações anteriores e na teoria de que os efeitos do canabidiol podem incluir o alívio: psicose, ansiedade, facilitação do sono REM e supressão da atividade convulsiva. Um estudo de caso único com Dronabinol (um fármaco à base de THC) mostrou melhorias significativas na hiperatividade, letargia, irritabilidade, estereotipia e fala inadequada aos 6 meses de seguimento. Além disso, acerca do tratamento com Dronabinol, verificou-se que, de 10 adolescentes pacientes com deficiência intelectual resultaram em 8 pacientes apresentando melhora no manejo de comportamento auto-lesivo resistente ao tratamento.
9 Estácio Amaro da Silva Júnior, Wandersônia Moreira Brito Medeiros, João Paulo Mendes dos Santos, João Marçal Medeiros de Sousa, Filipe Barbosa da Costa, Katiúscia Moreira Pontes, Thaís Cavalcanti Borges, Carlos Espínola Neto Segundo, Ana Hermínia Andrade e Silva, Eliane Lima Guerra Nunes, Nelson Torro Alves, Marina Diniz da Rosa, Katy Lísias Gondim Dias de Albuquerque. Avaliação da eficácia e segurança do extrato de cannabis rico em canabidiol em crianças com transtorno do espectro do autismo: ensaio clínico randomizado, duplo-cego e controlado por placebo.
Métodos: Neste ensaio clínico randomizado, duplo-cego e controlado por placebo, 60 crianças, com idades entre 5 e 11 anos, foram selecionadas e divididas em dois grupos: o grupo de tratamento, que recebeu o extrato de cannabis rico em CBD, e o grupo controle, que recebeu o placebo. Ambos usaram seus respectivos produtos por um período de 12 semanas. A análise estatística foi feita por análise de variância mista de dois fatores (ANOVA two-way). Foram incluídas crianças de 5 a 11 anos residentes no estado da Paraíba, Brasil, ou em estados vizinhos (Pernambuco e Rio Grande do Norte), que tivessem diagnóstico médico de TEA, independentemente de terem quadro leve, moderado, ou níveis graves de comprometimento. Essa faixa etária foi selecionada porque crianças de 5 a 11 anos apresentam maior similaridade no desenvolvimento cerebral, tornando o grupo mais homogêneo para análise dos resultados. Além disso, crianças com mais de 5 anos teriam maior probabilidade de desenvolver linguagem verbal e seriam mais capazes de responder durante testes neuropsicológicos. Foram excluídas crianças que apresentavam comorbidades como diabetes mellitus, hipertensão, doenças autoimunes ou epilepsia refratária ou que usaram produto de cannabis nos últimos dois meses antes do início do estudo.
Resultados: Resultados significativos foram encontrados para interação social (F 1.116 = 14,13, p = 0,0002), ansiedade (F 1.116 = 5,99, p = 0,016), agitação psicomotora (F 1.116 = 9,22, p = 0,003), número de refeições por dia (F 1,116 = 4,11, p = 0,04) e concentração (F 1,48 = 6,75, p = 0,01), sendo esta última significativa apenas nos casos de TEA leve. Em relação à segurança, constatou-se que apenas três crianças do grupo de tratamento (9,7%) apresentaram efeitos adversos, nomeadamente tonturas, insónia, cólicas e aumento de peso.
Conclusão: Descobriu-se que o extrato de cannabis rico em CBD melhora um dos critérios diagnósticos para TEA (interação social), bem como características que muitas vezes coexistem com TEA, e tem poucos efeitos adversos graves. Indivíduos com TEA que usaram o extrato de cannabis rico em CBD apresentaram melhora nos seguintes sintomas: automutilação e crises de raiva, hiperatividade, problemas de sono, ansiedade, inquietação, agitação psicomotora, irritabilidade, agressividade, sensibilidade sensorial, cognição, atenção, social interação, linguagem, perseverança e depressão. Quanto aos benefícios da intervenção com cannabis, o sintoma inquietação apresentou maior melhora (91%) em relação aos demais sintomas estudados. Portanto, os resultados mostraram a eficácia na hiperatividade, inquietação e agitação psicomotora; na ansiedade; na cognição, atenção e concentração; na facilitação da aprendizagem; em nutrição e na interação social em crianças no espectro do autismo.
10 Adi Aran , Hanoch Cassuto , Asael Lubotzky , Nadia Wattad , Ester Hazan.
Breve relatório: cannabis rica em canabidiol em crianças com transtorno do espectro do autismo e problemas comportamentais graves – um estudo retrospectivo de viabilidade
Métodos: Este estudo retrospectivo avaliou a tolerabilidade e a eficácia da cannabis rica em canabidiol, em 60 crianças com TEA e problemas comportamentais graves (idade = 11,8 ± 3,5, faixa 5,0-17,5; 77% de baixo funcionamento; 83% meninos). A eficácia foi avaliada utilizando a escala de Impressão Global de Mudança do Cuidador.
Resultados: Os eventos adversos incluíram distúrbios do sono (14%), irritabilidade (9%) e perda de apetite (9%). Uma menina que usava tetrahidrocanabinol mais elevado teve um evento psicótico grave e transitório que exigiu tratamento com um antipsicótico.
Conclusão: Após o tratamento com cannabis, os surtos comportamentais melhoraram muito em 61% dos pacientes. Este estudo preliminar apoia a viabilidade de ensaios de cannabis baseados em CBD em crianças com TEA.
3.1 ELEMENTOS DE APOIO PARA ANÁLISE DOS RESULTADOS E DISCUSSÃO
A partir dos estudos realizados para elaborar o presente artigo, obteve-se uma pesquisa respaldada em artigos científicos que promovam uma reflexão sobre o uso do canabidiol a fim de auxiliar no desenvolvimento de pessoas com autismo, contudo, há na literatura alguns poucos estudos observacionais (séries de caso) com tamanho amostral pequeno, critérios de inclusão e medidas de desfecho pouco definidos que observaram alguma melhora no comportamento, o que fortalece a hipótese de seu benefício. No entanto, além das séries de caso, não há evidência que sustente o benefício da medicação em foco, tornando-a, no momento, tão somente uma hipótese e uma intervenção experimental para a condição em pauta.
De acordo com o Protocolo Clínico e Diretrizes Terapêuticas da Epilepsia (2018), até o presente momento, o FDA (Food and Drug Administration), órgão dos Estados Unidos da América (EUA) responsável pelo registro de medicamentos, aprovou o uso do CBD apenas para o controle de crises epilépticas na síndrome de Lennox-Gastaut e na epilepsia mioclônica da infância grave. O fato de que a epilepsia é uma comorbidade comum com o TEA proporcionou a observação de que pacientes com essa condição que usavam canabidiol para o tratamento das crises epilépticas apresentavam melhora comportamental.
Foi levantada a hipótese de que esse fármaco pudesse ter ação no controle comportamental de crianças com autismo sem epilepsia. No entanto, em busca realizada no banco de dados Pubmed por meio das palavras-chave (cannabidiol) AND (autism) não se encontraram ensaios clínicos que tenham avaliado essa hipótese.
Ainda, é primordial salientar que não há evidência de que seja superior aos tratamentos disponíveis pelo Sistema Único de Saúde (SUS), entre eles a risperidona,18 recomendada no protocolo do Ministério da Saúde. Ainda que não fosse suficiente essa ausência de conhecimento sobre a eficácia, a segurança, especialmente em longo prazo, não foi comprovada. Essa questão é importante uma vez que há evidência sobre o impacto negativo em longo prazo do consumo de derivados da Cannabis no sistema nervoso, especialmente por crianças e adolescentes.
No TEA, o tratamento não farmacológico, que inclui a educação dos pais em conjunto com a abordagem multidisciplinar de especialistas, é o método de escolha mais indicado. No entanto, muitos pacientes necessitam de fármacos a fim de controlar sinais e sintomas como agressividade, irritabilidade, comportamento restritivo, repetitivo, ansiedade e transtornos do sono. Até o momento, para o TEA, as evidências científicas para tratamento farmacológico convergem para o manejo da irritabilidade com a risperidona e o aripiprazol; e o uso de metilfenidato, atomoxetina, guanfacina para o transtorno do déficit de atenção e hiperatividade e a melatonina para os distúrbios do sono. 19 20
Entretanto, muitos casos de TEA são refratários, independentemente das terapias e do uso de fármacos. Os fitocanabinoides parecem ocupar um lugar de destaque, segundo algumas pesquisas, mas ainda são necessários estudos mais robustos a fim de comprovar sua real eficácia. A afirmativa se sustenta pelo fato da grande maioria dos pesquisadores analisados fazer uso do verbo parecer em suas conclusões, ou seja, afirmam que “parece que a intervenção com canabidiol é eficaz”.
Há vários trabalhos observacionais sobre o uso dos canabinoides no TEA. No entanto, identificou-se que a pesquisa mais estudada para tratar do assunto em pauta, foi a desenvolvida em Israel , cujos resultados foram publicados na revista Nature, a qual avaliou 21 188 crianças, com idade média de 13 anos, com tempo de seguimento de seis meses. Foi utilizado produto à base de óleo de cannabis, contendo alto teor de canabidiol, 30% de CBD e 1,5% THC, ou seja, proporção de 20 CBD: 1 THC, além de outros canabinoides em baixas concentrações, terpenos e flavonoides. Constatou-se 80% de melhora global e na qualidade de vida, existência de poucos efeitos colaterais, sendo o mais comum à sonolência e boa adesão terapêutica, haja vista que 60% dos pacientes optaram por manter o tratamento, mesmo após o término do estudo. Igualmente, um estudo duplo-cego e randomizado com uso do extrato de 22 cannabis no TEA observou melhora no comportamento disruptivo, boa tolerabilidade e poucos efeitos colaterais, como sonolência, náuseas e transtornos alimentares.
Os estudos mostram que a questão está longe de ser encerrada e ensaios clínicos randomizados e controlados com acompanhamento em longo prazo precisam ser feitos para ter a certeza do benefício e da segurança da intervenção.
4. CONCLUSÃO
Esse trabalho pretendeu compreender as perspectivas positivas e negativas do tratamento com canadibiol no desenvolvimento de indivíduos com autismo para explorar novas abordagens terapêuticas, incluindo o potencial uso da cannabis, a fim de buscar alternativas cujo fito é melhorar a qualidade de vida das pessoas com TEA. A partir disso, a fim de alcançar os objetivos propostos, o estudo de cunho bibliográfico apresentado, se deu na forma de revisão integrativa de literatura, partindo das referências dos anos de 2019 a 2024, buscadas nas bases de dados PubMed e SciELO. Perante os achados, as evidências científicas foram organizadas e previamente selecionadas, a partir dos critérios de verificação do método PRISMA, e, desta forma, os textos foram analisados para que fossem reunidos os elementos confluentes para a escrita da revisão.
Para se atingir uma compreensão da questão, o objetivo geral buscou investigar a eficácia e os mecanismos de ação do canabidiol (CBD) no tratamento do transtorno do espectro do autismo (TEA), fornecendo uma análise de algumas evidências disponíveis, contribuindo para uma compreensão mais profunda dos benefícios terapêuticos e implicações clínicas do CBD para indivíduos com TEA. Dessa forma, definiu-se três objetivos específicos. O primeiro objetivo foi revisar e analisar estudos clínicos que investigaram o uso de CBD no tratamento do transtorno autista, incluindo suas metodologias, resultados e conclusões. O segundo objetivo específico foi investigar a eficácia do CBD na redução de sintomas específicos associados ao transtorno autista, como ansiedade, agressividade, hiperatividade, problemas de sono e comunicação social. Finalmente, o terceiro objetivo específico focou em identificar e relatar possíveis efeitos adversos associados ao uso de CBD no tratamento do transtorno autista.
A análise permitiu concluir que há, na literatura, alguns poucos estudos observacionais (séries de caso) com tamanho amostral pequeno, critérios de inclusão e medidas de desfecho pouco definidos que observaram alguma melhora no comportamento, o que fortalece a hipótese de seu benefício. No entanto, além das séries de caso, não há evidência que sustente o benefício da medicação em foco, tornando-a, no momento, tão somente uma hipótese e uma intervenção experimental para a condição em pauta.
A pesquisa sobre a influência da cannabis em pacientes com autismo é um campo emergente e promissor, mas ainda requer mais estudos para compreender plenamente seus efeitos, benefícios e riscos. Nesse viés, tornam-se necessárias algumas sugestões para pesquisas futuras, como:
Estudos Longitudinais: Investigar os efeitos em longo prazo do uso de cannabis em pacientes com autismo, acompanhando os indivíduos ao longo de vários anos para avaliar a eficácia e possíveis efeitos adversos crônicos.
Efeitos em Diferentes Faixas Etárias: Explorar como a cannabis afeta pacientes com autismo em diferentes idades, desde crianças até adultos, para determinar se há variações significativas nos resultados e se a idade do paciente influencia a resposta ao tratamento.
Dosagem e Formulações: Examinar quais dosagens e quais formas de administração (óleo, cápsulas, inalação, etc.) são mais eficazes e seguras para pacientes com autismo. Estudos comparativos entre diferentes canabinoides, como CBD e THC, também são essenciais para entender suas contribuições individuais, assim como seus mecanismos de ação.
Interações com Outros Tratamentos: Investigar como a cannabis interage com outros tratamentos convencionais para autismo, como terapias comportamentais e medicamentos psiquiátricos, para entender se há sinergias ou contraindicações.
Efeitos Psicológicos e Comportamentais: Realizar estudos que avaliem o impacto da cannabis nos comportamentos específicos do autismo, como a comunicação, a socialização e os comportamentos repetitivos, usando metodologias quantitativas e qualitativas.
Percepções dos Cuidadores e Profissionais de Saúde: Pesquisar as percepções e experiências de pais, cuidadores e profissionais de saúde com relação ao uso de cannabis em pacientes com autismo, para entender melhor as barreiras, os facilitadores e as necessidades de informação e suporte.
Comparação com Placebo: Conduzir ensaios clínicos controlados por placebo para estabelecer a eficácia da cannabis em comparação com tratamentos não ativos, assegurando rigor científico e minimizando o viés.
Estudos de Segurança: Focar em estudos que avaliem a segurança do uso de cannabis, monitorando efeitos colaterais imediatos e tardios, e determinando perfis de risco para diferentes subgrupos dentro da população autista.
Essas direções de pesquisa podem fornecer uma compreensão mais abrangente e aprofundada sobre o uso da cannabis no tratamento de pacientes com autismo, ajudando a criar diretrizes clínicas baseadas em evidências.
1Bar-Lev Schleider L, Mechoulam R, Saban N, Meiri G, Novack V. Experiência da vida real no tratamento da cannabis medicinal no autismo: análise de segurança e eficácia. Representante Científico 2019, janeiro; 9 (1):200. doi: 10.1038/s41598-018-37570-y.
2Associação Psiquiátrica Americana. Manual diagnóstico e estatístico de transtornos mentais. 5. Washington (DC): Editora; 2013.
3Agarwal R, Burke SL, Maddux M. Estado atual das evidências da utilização de cannabis para tratamento de transtornos do espectro do autismo. Psiquiatria BMC. outubro de 2019; 19 (1):328. doi: 10.1186/ s12888-019-2259-4.
4Wei D, Dinh D, Lee D, Li D, Anguren A, Moreno-Sanz G, et al. O aprimoramento da sinalização endocanabinoide mediada pela anandamida corrige o comprometimento social relacionado ao autismo. Cannabis Cannabinóide Res. Fevereiro de 2016; 1 (1):81–9. doi: 10.1089/can.2015.0008.
5Barchel D, Stolar O, De-Haan T, Ziv-Baran T, Saban N, Fuchs DO, et al. Uso oral de canabidiol em crianças com transtorno do espectro do autismo para tratar sintomas e comorbidades relacionados. Frente Farmacol. Janeiro de 2019; 9 :1521. doi: 10.3389/fphar.2018.01521.
6QUEM. Centro de mídia. Transtornos do espectro do autismo. 2021. Disponível em: http://www.who.int/mediacentre/factsheets/autism-spectrum-disorders/en/. Acesso: 23 mar 2024. PubMed[Ghosh A, Michalon A, Lindemann L, Fontoura P, Santarelli L. Descoberta de drogas para transtorno do espectro do autismo: desafios e oportunidades. A Nature analisa a descoberta de medicamentos. 2013; 12: 777–790.
7Betancur C. Heterogeneidade etiológica em transtornos do espectro do autismo: mais de 100 distúrbios genéticos e genômicos e ainda contando. Pesquisa cerebral. 2011; 1380: 42–77.
8Rosti RO, Sadek AA, Vaux KK, Gleeson JG. A paisagem genética dos transtornos do espectro do autismo. Medicina do Desenvolvimento e Neurologia Infantil. 2014; 56: 12–18.
9Harris SW, Hessl D, Goodlin-Jones B, Ferranti J, Bacalman S, Barbato I, et al . Perfis de autismo em homens com síndrome do X frágil. Jornal Americano de Retardo Mental. 2008; 113: 427–438.
10Bailey DB Jr, Mesibov GB, Hatton DD, Clark RD, Roberts JE, Mayhew L. Comportamento autista em meninos com síndrome do X frágil. Jornal de Autismo e Transtornos do Desenvolvimento. 1998; 28: 499–508.
11Belmonte MK, Bourgeron T. Síndrome do X Frágil e autismo na intersecção de redes genéticas e neurais. Neurociência da Natureza. 2006; 9: 1221–1225.
12Z o g h b i H Y, B e a r M F. D i s f u n ç ã o S i n á p t i c a e m D e f i c i ê n c i a s I n t e l e c t u a i s d o Neurodesenvolvimento. Perspectivas de Cold Spring Harbor em Biologia. 2012; 4: 1–22.
13 Editora Bentham Science BSP. Imunoexcitotoxicidade como mecanismo central dos transtornos do espectro do autismo. Em Strunecka A (Ed.) Biologia Celular e Molecular dos Transtornos do Espectro do Autismo (pp. 47–72). Bentham Science Publishers Ltd: Sharjah, Emirados Árabes Unidos. 2010.
14Blaylock RL. Disfunção Imunológica no Transtorno do Espectro do Autismo. Em Strunecka A (Ed.) Biologia Celular e Molecular dos Transtornos do Espectro do Autismo (pp. 73–81). Bentham Science Publishers Ltd: Sharjah, Emirados Árabes Unidos. 2010.
15Meltzer A, Van de Water J. O papel do sistema imunológico no transtorno do espectro do autismo. Neuropsicofarmacologia. 2017; 42: 284–298.
16Onore C, Careaga M, Ashwood P. O papel da disfunção imunológica na fisiopatologia do autismo. Cérebro, comportamento e imunidade. 2012; 26: 383–392.
17Samsam M, Ahangari R, Naser SA. Fisiopatologia dos transtornos do espectro do autismo: revisitando o envolvimento gastrointestinal e o desequilíbrio imunológico. Jornal Mundial de Gastroenterologia. 2014; 20: 9942–9951.
18Aran A, Harel M, Cassuto H, Polyansky L, Schnapp A, Wattad N, Shmueli D, Golan D, Castellanos FX. Cannabinoid treatment for autism: a proof-of-concept randomized trial. Mol Autism. 2021;12(1):6
19Siafis S, Çıray O, Wu H, Schneider-Thoma J, Bighelli I, Krause M, Rodolico A, Ceraso A, Deste G, Huhn M, Fraguas D, San José Cáceres A, Mavridis D, Charman T, Murphy DG, Parellada M, Arango C, Leucht S. Pharmacological and dietary-supplement treatments for autism spectrum disorder: a systematic review and network meta-analysis. Mol Autism. 2022;13(1):10.
20Fuentes J, Hervás A, Howlin P; (ESCAP ASD Working Party). ESCAP practice guidance for autism: a summary of evidence-based recommendations for diagnosis and treatment. Eur Child Adolesc Psychiatry. 2021;30(6):961-84.
21Bar-Lev Schleider L, Mechoulam R, Saban N, Meiri G, Novack V. Real life experience of medical cannabis treatment in autism: analysis of safety and efficacy. Sci Rep. 2019;9(1):200.
22McPheeters ML, Warren Z, Sathe N, Bruzek JL, Krishnaswami S, Jerome RN, Veenstra-Vanderweele J. A systematic review of medical treatments for children with autism spectrum disorders. Pediatrics. 2011;127(5):e1312-21.
REFERÊNCIAS
ARAN A, CASSUTO H, LUBOTZKY A, WATTAD N, HAZAN E. Breve relatório: Cannabis rica em canabidiol em crianças com transtorno do espectro do autismo e problemas comportamentais graves – um estudo retrospectivo de viabilidade. J Autism Dev Disord. 2019 Mar;49(3):1284-1288. Disponível em: doi: 10.1007/s10803-018-3808-2. PMID: 30382443. Acesso em: 25 mar. 2023.
ARAN A, HAREL M, CASSUTO H, POLYANSKY L, SCHNAPP A, WATTAD N, SHMUELI D, GOLAN D, CASTELLANOS FX. Tratamento com canabinoides para o autismo: um ensaio randomizado de prova de conceito. Mol Autism. 2021 Feb 3;12(1):6. Disponível em: doi: 10.1186/s13229-021-00420-2. PMID: 33536055; PMCID: PMC7860205. Acesso: 22 mar. 2024.
BABAYEVA M, ASSEFA H, BASU P, LOEWY Z. AUTISMO E DISTÚRBIOS ASSOCIADOS: CANNABIS COMO TERAPIA POTENCIAL. FRONT BIOSCI (ELITE ED). 2022 JAN 13;14(1):1. DISPONÍVEL EM: DOI: 10.31083/J.FBE1401001. PMID: 35320905. ACESSO: 30 MAR. 2024.
BAR-LEV SCHLEIDER L, MECHOULAM R, SABAN N, MEIRI G, NOVACK V. Experiência da vida real de tratamento com cannabis medicinal no autismo: análise de segurança e eficácia. Sci Rep. 2019 Jan 17;9(1):200. Disponível em: doi: 10.1038/ s41598-018-37570-y. PMID: 30655581; PMCID: PMC6336869. Recuperado a partir de https://doi.org/10.1038/s41598-018-37570-y. Acesso: 23 mar. 2024.
BARROS NETO, Sebastião Gonçalves de; BRUNONI, Decio e CYSNEIROS, Roberta Monterazzo. Abordagem psicofarmacológica no transtorno do espectro autista: uma revisão narrativa. Cad. Pós-Grad. Distúrb. Desenvolv. [online]. 2019, vol.19, pp. 38-60 . D i s p o n í v e l e m : <http://pepsic.bvsalud.org/scielo.php?script=sci_arttext&pid=S1519-03072019000200004&lng=pt&nrm=iso>. ISSN 1519-0307. http://dx.doi.org/10.5935/cadernosdisturbios.v19n2p38-60. Acesso: 26 mai. 2023.
BRASIL. Agência Nacional de Vigilância Sanitária. Portaria nº 344, de 12 de maio de 1998. Aprova o regulamento técnico sobre substâncias e medicamentos sujeitos a controle especial. Diário Oficial da União 12 de mai 1998; Seção 1. Disponível em: https://bvsms.saude.gov.br/ bvs/saudelegis/svs/1998/prt0344_12_05_1998_rep.html. Acesso em: 25 mar. 2023.
BRASIL. Agência Nacional de Vigilância Sanitária. Resolução da Diretoria Colegiada – RDC N° 17, de 06 de maio de 2015. Define os critérios e os procedimentos para a importação, em caráter de excepcionalidade, de produto à base de Canabidiol em associação com outros canabinóides, por pessoa física, para uso próprio, mediante prescrição de profissional legalmente habilitado, para tratamento de saúde. Disponível em: http:// bvsms.saude.gov.br/bvs/saudelegis/anvisa/2015/rdc0017_06_05_2015.pdf. Acesso em: 25 mar. 2023.
BRASIL. Agência Nacional de Vigilância Sanitária. Resolução nº 17, de 16 de abril de 2010. Dispõe sobre as boas práticas de fabricação de medicamentos. Diário Oficial da União 16 de abr 2010; Seção 1. Disponível em: https://bvsms.saude.gov.br/bvs/saudelegis/anvisa/2010/ res0017_16_04_2010.html. Acesso em: 25 mar. 2023.
BRASIL. Agência Nacional de Vigilância Sanitária. Resolução nº 327, de 09 de dezembro de 2019. Procedimentos para a concessão da Autorização Sanitária para a fabricação e a importação, bem como estabelece requisitos para a comercialização, prescrição, a dispensação, o monitoramento e a fiscalização de produtos de Cannabis para fins medicinais, e dá outras providências. Diário Oficial da União 11 de dez 2019; Seção 1. Disponível em: https://rmconsult.blogspot.com/2019/12/resolucao-da-diretoria-colegiada-rdc-n_11.html. Acesso em: 26 mar. 2023.
BRASIL. Lei nº11.343, de 23 de agosto de 2006. Lei de drogas. Diário Oficial da União 23 de ago 2006. Disponível em: https://www.planalto.gov.br/ccivil_03/_Ato2004-2006/2006/ Lei/L11343.htm. Acesso em: 2 abr. 2023.
BRASIL. Ministério da Saúde. Agência Nacional de Saúde Suplementar. ANS amplia regras de cobertura para tratamento de transtornos globais do desenvolvimento. Brasília, 2022. Disponível em: https://www.gov.br/ans/pt-br/assuntos/noticias/periodo-eleitoral/ans-amplia regras-de-cobertura-para-tratamento-de-transtornos-globais-do-desenvolvimento. Acesso: 10 fev. 2024.
BRASIL. MINISTÉRIO DA SAÚDE. Comissão Nacional de Incorporação de Tecnologias no SUS (CONITEC). Protocolo Clínico e Diretrizes Terapêuticas da Epilepsia [Internet]. 2018. Disponível em: https://www.gov.br/saude/pt-br/assuntos/pcdt/arquivos/2021/portal portariano-17-pcdt-epilepsia.pdfABRACE. Anvisa simplifica importação de produtos a base de Cannabis. Disponível em: https://abraceesperanca.org.br/blog/anvisa-simplifica importacao-de-produtos-a-base-de-cannabis. G1. Acesso em: 15 abr. 2023.
DE OLIVEIRA, M. A. P.; PARENTE, R. C. M. Entendendo ensaios clínicos randomizados. Brazilian Journal of Videoendoscopic Surgery, v. 3, n. 4, p. 176-180, 2010. Disponível em: https://www.sobracil.org.br/revista/jv030304/bjvs030304_176.pdf. Acesso em: 26 mar. 2023.
EUA. AMERICAN PSYCHIATRIC ASSOCIATION. Manual diagnóstico e estatístico de transtornos mentais: DSM-5. ed. Porto Alegre: Artmed, 2014. Agência Nacional de Vigilância Sanitária [ANVISA]. (2015). Disponível em: http://institutopebioetica.com.br/ documentos/manual-diagnostico-e-estatistico-de-transtornos-mentais-dsm-5.pdf. Acesso em: 1 abr. 2023.
EUA. AMERICAN PSYCHIATRIC ASSOCIATION. Resolução RDC n°. 17 de 6 de maio de 2015. Define os critérios e os procedimentos para a importação, em caráter de excepcionalidade, de produto à base de Canabidiol em associação com outros canabinóides, por pessoa física, para uso próprio, mediante prescrição de profissional legalmente habilitado, para tratamento de saúde. Diário Oficial da União, Seção 1(86). 44- 56. Disponível em: https://www.psychiatry.org/. Acesso em: 7 mai. 2023.
GANESH A, SHAREEF S. Segurança e Eficácia da Cannabis no Transtorno do Espectro do Autismo. Pediatr Neurol Briefs. 2020 Dec 24;34:25. Disponível Em: DOI: 10.15844/ PEDNEURBRIEFS-34-25. PMID: 33376294; PMCID: PMC7759327. ACESSO EM: 25 MAR. 2023.
JUNIOR, Estácio Amaro da Silva, MEDEIROS, Wandersônia Moreira Brito, SANTOS, João Paulo Mendes dos, SOUZA, João Marçal Medeiros de, COSTA, Filipe Barbosa da, PONTES, Katiúscia Moreira, BORGES, Thaís Cavalcanti, SEGUNDO, Carlos Espínola Neto, SILVA, Ana Hermínia Andrade e, NUNES, Eliane Lima Guerra, ALVES, Nelson Torro, ROSA, Marina Diniz da, ALBUQUERQUE, Katy Lísias Gondim Dias de. Avaliação da eficácia e segurança do extrato de cannabis rico em canabidiol em crianças com transtorno do espectro do autismo: ensaio clínico randomizado, duplo-cego e controlado por placebo. Disponível em: https://www.scielo.br/j/trends/a/TVWvDrn75t5vHNbfYSvgzTz/abstract/?lang=en#. Acesso: 23 mar. 2024.
LOPES, Ana Maria Costa da Silva. O autismo e suas conexões: qual medicação para o autista? Psicologia em Revista. versão impressa ISSN 1677-1168. Psicol. rev. (Belo Horizonte) vol.25 no.3 Belo Horizonte set./dez. 2019 Disponível em: http://dx.doi.org/ 10.5752/P.1677-1168.2019v25n3p1343-1352. Acesso: 10 fev. 2024.
MOSTAFAVI M, GAITANIS J. Transtorno do Espectro do Autismo da Cannabis Medicinal: Revisão e Experiência Clínica. Semin Pediatr Neurol. 2020 Oct;35:100833. Disponível Em: DOI: 10.1016/J.SPEN.2020.100833. EPUB 2020 JUL 2. PMID: 32892960. Acesso em 26 março. 2023.
SCHIER, ALEXANDRE RAFAEL DE MELLO ET AL. SCIENCE DIRECT. Revista Brasileira de Psiquiatria. Volume 34, suplemento 1, junho de 2012 , páginas s104-s117. Disponível em: https://www.sciencedirect.com/science/article/pii/s1516444612700570. Acesso em: 14 mai. 2023.
SILVA, Estácio Amaro da Silva Júnior et al. PUBMED. Cannabis e uso de canabinóides no transtorno do espectro do autismo: uma revisão sistemática. Trends Psychiatry P s y c h o t h e r . 1 3 d e j u n h o d e 2 0 2 2 ; 4 4 : e 2 0 2 0 0 1 4 9 . d o i : 10.47626/2237-6089-2020-0149.PMID: 34043900 Artigo PMC. Disponível em: https:// pubmed.ncbi.nlm.nih.gov/34043900/. Acesso em: 25 mar. 2023.
