THE ASSOCIATION BETWEEN EXPOSURE TO VALPROATE IN THE PRENATAL PHASE AND THE INCREASED RISK OF DEVELOPING AUTISM SPECTRUM DISORDER: A SCOPE REVIEW.
REGISTRO DOI: 10.5281/zenodo.10642661
Mariana Roldão de Araújo¹
Morgana Fernandes dos Santos²
Laércio Pol Fachin³
RESUMO
O Transtorno do Espectro Autista (TEA) é definido como um transtorno do neurodesenvolvimento que não tem fisiopatologia totalmente compreendida, mas teorias estudadas apontam o uso de fármacos na gestação como fator relacionado ao desenvolvimento do autismo. Entre os medicamentos estudados estão os anticonvulsivantes com destaque para o valproato de sódio, portanto é necessário avaliar a relação entre o uso desse fármaco por gestantes e o potencial risco de desenvolvimento de TEA nas crianças expostas durante o período pré-natal. O estudo foi desenvolvido através de uma revisão de escopo, com pesquisa e seleção de artigos nas bases de dados LILACS e PUBMED, por meio da estratégia de busca Valproate AND Prenatal AND Autism, respeitando os critérios de inclusão e exclusão estabelecidos para seleção final dos artigos a serem usados como fonte para o estudo. Foram encontrados 812 artigos nas duas bases de dados utilizadas e 14 trabalhos foram selecionados para realização da revisão. A seleção dos artigos foi realizada de forma sequencial através da leitura de títulos, resumos e trabalho completo de acordo com os critérios de inclusão e exclusão. Os estudos selecionados abordam a relação da exposição fetal ao valproato com comprometimento neurocognitivo e os riscos do desenvolvimento de autismo associado ao uso desse anticonvulsivante durante a gestação. O uso do valproato de sódio durante a gestação está associado ao aumento do índice de desenvolvimento do TEA, portanto, é necessária a individualização terapêutica de acordo com os riscos e benefícios relacionados ao uso deste fármaco durante o período gestacional.
Palavras-chave: Autismo. Valproato. Gestação.
ABSTRACT
Autism Spectrum Disorder (ASD) is defined as a neurodevelopmental disorder that does not have a fully understood pathophysiology, but studied theories point to the use of drugs during pregnancy as a factor related to the development of autism. Among the medications studied are anticonvulsants, with emphasis on sodium valproate, therefore it is necessary to evaluate the relationship between the use of this drug by pregnant women and the potential risk of developing ASD in children exposed during the prenatal period. The study was developed through a scoping review, with research and selection of articles in the LILACS and PUBMED databases, using the Valproate AND Prenatal AND Autism search strategy, respecting the inclusion and exclusion criteria established for the final selection of articles to be used as a source for the study. 812 articles were found in the two databases used and 14 works were selected for the review. The selection of articles was carried out sequentially by reading titles, abstracts and complete work according to the inclusion and exclusion criteria. The selected studies address the relationship between fetal exposure to valproate and neurocognitive impairment and the risks of developing autism associated with the use of this anticonvulsant during pregnancy. The use of sodium valproate during pregnancy is associated with an increased rate of development of ASD, therefore, therapeutic individualization is necessary according to the risks and benefits related to the use of this drug during the gestational period.
Keywords: Autism. Valproate. Gestation.
INTRODUÇÃO
O Transtorno do Espectro Autista (TEA) é definido no Manual de Diagnóstico e Estatístico de Transtornos Mentais 5ª edição (DSM-V) como um transtorno do neurodesenvolvimento caracterizado pela dificuldade nas relações interpessoais, comprometimento na comunicação e desenvolvimento de estereotipias que se apresentam de formas e intensidade distintas em cada paciente do espectro. A fisiopatologia do TEA ainda não é totalmente compreendida, mas teorias estudadas apontam o uso de fármacos na gestação como fator relacionado ao desenvolvimento do autismo.
Entre os medicamentos estudados estão os anticonvulsivantes, com destaque ao valproato de sódio (VPA) que atua inibindo o sistema nervoso central pela estimulação do GABA. A análise comparativa demonstrou maior comprometimento no desenvolvimento do sistema nervoso fetal relacionado ao uso do valproato em relação a outros medicamentos da mesma classe terapêutica, como a lamotrigina e a carbamazepina (WESTON et al., 2016).
Essa medicação é muito usada, pois apresenta boa resposta não apenas para o manejo das crises convulsivas, mas também na psiquiatria no tratamento de pacientes com transtorno de humor bipolar (MADEIRA et al., 2015). Apesar dos benefícios relacionados ao valproato, é necessário avaliar os efeitos colaterais e as possíveis complicações relacionadas ao seu uso, principalmente em populações que necessitam de cuidados direcionados, como as gestantes, devido aos maiores riscos envolvidos.
Os estudos demonstraram que o uso deste fármaco durante a gestação está relacionado a maior incidência de patologias fetais, incluindo malformações do tubo neural. As avaliações também permitiram observar que o TEA se destacou como distúrbio do neurodesenvolvimento mais frequente relacionado ao uso do valproato por gestantes (BROMLEY et al., 2013).
A exposição intrauterina ao valproato se relaciona ao maior risco de comprometimento no desenvolvimento cognitivo quando comparadas a crianças não expostas ao fármaco durante a gestação. O impacto no desenvolvimento fetal depende do período de exposição aos anticonvulsivantes, sendo o uso durante o primeiro trimestre mais relacionado a malformações. Outro fator importante associado ao impacto negativo no desenvolvimento é a posologia utilizada, quanto maior a dose usada pela gestante, maior o risco de complicações (BROMLEY et al., 2014).
Dessa forma, ao se avaliar o atual cenário de crescimento exponencial de diagnósticos de TEA, a partir da análise de estudos anteriores, é possível estabelecer a relação entre o uso do valproato de sódio durante o período pré-natal e o comprometimento do neurodesenvolvimento. A avaliação direcionada da exposição intrauterina desse medicamento e o desenvolvimento do autismo é necessária para melhor compreender o risco-benefício do uso deste fármaco durante a gestação e auxiliar na escolha de tratamentos maternos mais seguros para o neurodesenvolvimento fetal.
METODOLOGIA
O estudo desenvolvido consiste em uma revisão de escopo com objetivo de entender a relação entre o uso do valproato de sódio em fase pré-natal e o maior risco de desenvolvimento do transtorno do espectro autista.
O protocolo de pesquisa seguiu a extensão de declaração do PRISMA para revisão de escopo publicada em 2018 (TRICCO et al., 2018).
O método seguiu cinco etapas consecutivas: identificação da questão de pesquisa; identificação de estudos relevantes; seleção dos estudos; organização dos dados e resumo dos dados e síntese dos resultados.
Etapa 1: Identificação da questão da pesquisa
Planejou-se responder à seguinte pergunta específica:
1. Existe aumento da incidência de TEA em crianças expostas ao valproato de sódio em fase intrauterina?
Etapa 2: Identificação de estudos relevantes
Foi realizada busca nas bases de dados LILACS e PUBMED, por meio da estratégia de busca “Valproate AND Prenatal AND Autism”. Após a realização da pesquisa, a seleção dos artigos respeitou os critérios de inclusão estabelecidos e, portanto, os artigos em inglês e português que abordavam a associação entre o uso de valproato durante a gestação e o desenvolvimento de autismo foram incluídos. O período de publicação dos artigos não foi delimitado e todos os estudos encontrados através da estratégia de busca, independente do ano de publicação, foram considerados para avaliação.
Foram excluídos os trabalhos realizados com animais, artigos relacionados ao uso de outros anticonvulsivantes durante a gestação ou que associaram o uso de valproato, exclusivamente, a outras injúrias neurológicas da infância. Pesquisas que abordavam apenas a síndrome do valproato fetal sem direcionar o estudo a relação do uso deste medicamento durante a gestação ao desenvolvimento do autismo também não foram selecionadas para esta revisão.
Etapa 3: Seleção dos estudos
Os primeiros estudos foram selecionados a partir da leitura dos títulos, assim, descartando os que não faziam parte do interesse da pesquisa. Em seguida, foram novamente selecionados e descartados trabalhos a partir da leitura dos resumos. E por fim, a leitura completa dos artigos foi realizada para concluir a última e definitiva seleção dos trabalhos que foram utilizados nesta revisão de escopo.
Etapa 4: Organização dos dados
A partir da leitura dos artigos selecionados foram extraídos dados referentes aos efeitos do uso de valproato durante a gestação e o desenvolvimento neurocognitivo com o objetivo de avaliar a relação desse fármaco com o TEA. O impacto da dosagem materna utilizada, bem como a relação do sexo das crianças expostas na vida intrauterina ao valproato de sódio foram variáveis analisadas para realização do estudo.
Etapa 5: Resumo dos dados e síntese dos resultados
Uma tabela com os resultados obtidos foi desenvolvida em conjunto por dois revisores para sintetizar as informações coletadas nos estudos selecionados para realização da revisão. Os dois revisores avaliaram os dados de forma manual e independente. As informações coletadas foram discutidas e atualizadas para finalização da tabela.
Os trabalhos agrupados para a realização da revisão de escopo consistem em estudos de coorte, revisões sistemáticas e estudos experimentais, que avaliam a relação entre o uso do valproato de sódio durante o período pré-natal e o desenvolvimento do transtorno do espectro autista. Os artigos foram revisados, avaliados e agrupados pelos revisores. O quadro elaborado é composto por 3 colunas de dados: autor e ano do trabalho estudado, tipo de estudo desenvolvido e síntese do artigo discutido (Quadro 1).
Quadro 1 – Artigos selecionados para o presente estudo
ALVESTAD et al., 2022. Estudo de coorte de base populacional. Entre os filhos de mães com epilepsia expostas ao valproato, a incidência cumulativa de TEA em 8 anos foi de 2,7% enquanto em crianças não expostas foi de 1,5%. ANDERSON et al., 2021. Estudo de coorte de base populacional. Os homens pontuaram de forma semelhante às mulheres expostas ao VPA, de forma oposta às porcentagens gerais em que o TEA é mais comum entre os homens. Os resultados sugerem que a relação do uso pré-natal do VPA e o TEA pode ser influenciada pelo sexo. ANDERSON et al., 2015. Estudo de coorte de base populacional. As crianças que tiveram exposição in utero ao valproato tiveram maior probabilidade de apresentar pontuações CARS elevadas, com 7,7% do grupo de monoterapia com valproato e 46,7% do grupo de politerapia com valproato apresentando sintomas de TEA. ANDRADE, 2018. Revisão sistemática e metanálise. O valproato foi a única droga antiepiléptica significativamente associada ao atraso cognitivo, de linguagem e psicomotor, além de autismo/ dispraxia. As politerapias que incluíam valproato também foram associadas ao aumento de certos riscos de desenvolvimento. BROMLEY et al., 2013. Estudo de coorte de base populacional. As crianças expostas ao VPA apresentaram alta prevalência, cerca de 6 a 10 vezes maior de distúrbios do neurodesenvolvimento (6/50: 12,0% para monoterapia com VPA e 3/20: 15,0% para politerapia com VPA). O distúrbio do desenvolvimento neurológico mais comum aos seis anos de idade em crianças expostas ao VPA foi o TEA. BROMLEY et al., 2014. Revisão sistemática de literatura Três estudos relataram a prevalência do diagnóstico do espectro autista em grupos de crianças expostas ao VPA, sendo 8% no grupo exposto ao VPA, em comparação com 1,8% no maior estudo e 12% e 15% nos outros 2 estudos avaliados. CUI et al., 2020. Estudo experimental O estudo com organóides demonstrou que a exposição ao VPA prejudica a neurogênese no estágio inicial do desenvolvimento do cérebro. Estes resultados sugerem que essa exposição contribui para para o desenvolvimento dos distúrbios neurais pós-natais no TEA. CHRISTENSEN et al., 2013. Estudo de coorte de base populacional As crianças expostas ao valproato apresentaram um risco absoluto de 4,42% (IC 95%, 2,59%-7,46%) para transtorno do espectro do autismo e um risco absoluto de 2,50% (IC 95%, 1,30%-4,81%) para autismo infantil. KELLOGG et al., 2017. Revisão sistemática de literatura O valproato é o medicamento antiepilético mais amplamente reconhecido por afetar significativamente negativamente o neurodesenvolvimento e demonstra maiores efeitos adversos do que qualquer outro medicamento antiepiléptico que tenha sido avaliado. Evidências crescentes sugerem que a exposição ao valproato durante períodos críticos de desenvolvimento pode induzir déficits de desenvolvimento neurológico transitórios ou duradouros nos domínios cognitivo, motor e comportamental. MEADOR et al., 2013. Revisão de literatura Dada a evidência acumulada que liga a exposição fetal ao valproato a malformações congênitas, deficiências cognitivas e autismo, a utilização de valproato em mulheres com potencial para engravidar deve ser minimizada. Medicamentos alternativos devem ser procurados. Se não for possível encontrar medicamentos alternativos eficazes, deve ser utilizada a dose eficaz mais baixa de valproato. MEADOR et al., 2011. Revisão de literatura As crianças expostas ao valproato em monoterapia ou em politerapia foram classificadas como tendo menor adaptabilidade, principalmente nas habilidades de vida diária e socialização. As pontuações foram mais elevadas nas escalas que medem a exigência, problemas de adaptação às mudanças na rotina, distração e humor infeliz, levando a pontuações mais elevadas nas escalas de stress parental. MENG et al., 2022. Estudo experimental A exposição pré-natal ao VPA como fator ambiental está associada ao aumento do risco de TEA, cujos mecanismos funcionais no cérebro humano não são claros. Nossa compreensão sobre os efeitos do VPA é amplamente baseada em culturas de células 2D e modelos animais que não conseguiram recapitular arquiteturas celulares complexas e trajetórias de desenvolvimento do cérebro humano, sendo necessárias investigações sob a base genética humana e condições fisiológicas semelhantes às in vivo. VERONIKI et al., 2017. Revisão sistemática e metanálise O NMA sobre atraso no desenvolvimento cognitivo (11 estudos de coorte, 933 crianças, 18 tratamentos) sugeriu que, entre todos os DEAs, apenas o valproato estava estatisticamente significativamente associado a mais crianças com atraso no desenvolvimento cognitivo em comparação com o controle. WESTON et al., 2016. Revisão sistemática de literatura e metanálise O VPA apresentou o maior risco de malformação (10,93%) quando comparado aos outros medicamentos antiepilépticos.
Fonte: Dados da pesquisa.
RESULTADOS
A pesquisa realizada nas bases de dados, utilizando a estratégia de busca estabelecida, disponibilizou 812 artigos, destes 452 via PUBMED e 360 via LILACS. Respeitando os critérios de inclusão e exclusão, 44 estudos foram selecionados através da avaliação dos títulos e, após excluídas as duplicidades, 35 seguiram para leitura do resumo, sendo 20 trabalhos escolhidos após essa etapa para realização da leitura completa. Após a avaliação integral dos artigos selecionados, 14 estudos atenderam os critérios propostos para a realização da revisão (Figura 1).
Figura 1 – Fluxograma de seleção dos artigos
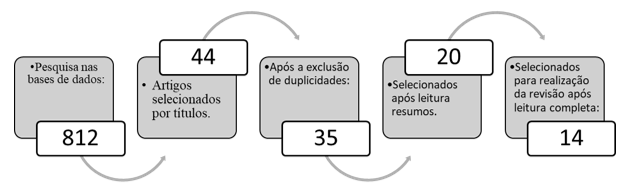
Fonte: Dados da pesquisa.
DISCUSSÃO
Nesta revisão de escopo, identificou-se 14 estudos primários e secundários abordando pesquisas de relação entre o uso do valproato de sódio e o desenvolvimento do transtorno do espectro autista publicados entre os anos de 2011 e 2022. Essas descobertas indicam uma escassez de pesquisas robustas focadas nessa associação em seres humanos.
O valproato de sódio é uma droga de importante atuação no controle de crises convulsivas em mulheres gestantes portadoras de epilepsia, porém estudos direcionados a ação desse fármaco vêm demonstrando um maior risco em comparação ao benefício na maioria das situações clínicas. As análises do uso deste medicamento durante a gestação demonstraram a maior relação entre o desenvolvimento de malformações fetais e a maior prevalência de comprometimento do neurodesenvolvimento. (BROMLEY et al., 2014; CHRISTENSEN et al., 2013; MEADOR et al., 2011).
Os estudos analisados confirmam de forma unânime os riscos elevados da exposição intrauterina ao valproato de sódio e o desenvolvimento do TEA. Foi observado que quando comparado aos demais anticonvulsivantes, o valproato de sódio é tido como a droga de maior potencial teratogênico do sistema nervoso central, estando diretamente associado a maiores índices de desenvolvimento de TEA em crianças expostas no período pré-natal (ALVESTAD et al., 2022; KELLOGG et al., 2017; VERONIKI et al., 2017, WESTON et al., 2016).
Os estudos experimentais avaliados demonstram que o comprometimento neurológico fetal associado a esse fármaco ocorre desde os estágios iniciais da neurogênese e que essa exposição está associada ao maior risco de desenvolvimento do autismo, porém os mecanismos desse comprometimento neurológico ainda não estão totalmente estabelecidos (CUI et al., 2020; MENG et al., 2022).
Os efeitos observados nos estudos selecionados demonstraram que essa exposição ao ácido valpróico durante a neurogênese apresenta relação com o comprometimento neurológico infantil em mono ou politerapia, porém índices superiores de autismo em crianças que foram expostas ao valproato em associação a outros anticonvulsivantes são observados (ANDRADE, 2018; BROMLEY et al., 2013; MEADOR et al., 2011).
Ao se avaliar os dados estatísticos do TEA na população geral, nota-se uma maior prevalência do desenvolvimento desse transtorno no sexo masculino, porém, essa revisão permitiu observar que em grupos de pacientes expostos ao valproato de sódio na vida intrauterina a divergência entre os sexos é minimizada e a prevalência entre esses grupos é praticamente equivalente (ANDERSON et al., 2021).
Dessa forma, os prejuízos para o desenvolvimento neurológico relacionados ao uso desse fármaco no período gestacional apontados nos estudos avaliados refletem a necessidade do uso com cautela por mulheres em idade fértil para minimizar a exposição fetal a esse fator de risco. A avaliação individualizada pelo especialista é necessária para que seja estabelecida a melhor terapêutica de acordo com os riscos e benefícios da medicação, a fim de promover o equilíbrio necessário entre controle da patologia materna e proteção do neurodesenvolvimento infantil (MEADOR et al., 2013).
CONCLUSÃO
O uso do valproato de sódio em monoterapia ou combinado com outros anticonvulsivantes durante a gestação está associado a um maior risco de comprometimento do adequado desenvolvimento neurocognitivo, estando diretamente relacionado ao aumento do índice de desenvolvimento do Transtorno do Espectro Autista. Assim, fica exposta a necessidade de avaliação de cada caso isoladamente para definir a terapia com maior benefício para a gestante e o feto em desenvolvimento.
REFERÊNCIAS
ALVESTAD, S. et al. Association of Prenatal Exposure to Antiseizure Medication With Risk of Autism and Intellectual Disability. JAMA Neurology, 2022. V. 79, n.7. p.672-681.
ANDERSON, A. et al. Prenatal valproate exposure and adverse neurodevelopmental outcomes: Does sex matter?. Epilepsia, 2021. V. 62, n. 3, p. 709-719.
ANDERSON, V. et al. Prospective assessment of autismo traits in children exposed to antiepileptic drugs during pregnancy. Epilepsia, Oceania, 2015. V. 56, n.7. p. 1047-1055.
ANDRADE, C. Valproate in pregnancy: recent research and regulatory responses. J Clin Psychiatry, 2018. v. 79, n. 3, 18f12351.
BROMLEY, R, L. et al; Liverpool and Manchester Neurodevelopment Group. The prevalence of neurodevelopmental disorders in children prenatally exposed to antiepileptic drugs. J Neurol Neurosurg Psychiatry, 2013. v.84, n.6, p. 637-43.
BROMLEY, R, L. et al. Treatment for epilepsy in pregnancy: neurodevelopmental outcomes in the child. Cochrane Database of Systematic Reviews, 2014.
CUI, K. et al. Neurodevelopmental impairment induced by prenatal valproic acid exposure shown with the human cortical organoid-on-a-chip model. Microsystems & Nanoengineering, 2020, China. V. 49, n. 6, p. 1-14.
CHRISTENSEN, J. et al. Prenatal valproate exposure and risk of autism spectrum disorders and childhood autism. JAMA, 2013. V.309, n. 16, p. 1696-703.
KELLOGG, M; MEADOR, K, J. Neurodevelopmental Effects of Antiepileptic Drugs. Neurochem Res, 2017, Estados Unidos. V. 42, n. 7, p. 2065-2070.
MEADOR, K, J; LORING, D, W. Risks of in utero exposure to valproate. JAMA, 2013. v. 309, n. 16, p. 1730-1.
MEADOR, K, J; PALAC, S. Antiepileptic Drugs and Neurodevelopment: An Update. Curr Neurol Neurosci Rep, 2011. v. 11, n. 4, p. 423-427.
MENG, Q. et al. Human forebrain organoids reveal connections between valproic acid exposure and autism risk. Transl Psychiatry, 2022. v. 12, n. 1, p. 130.
VERONIKI, A, A. et al. Comparative safety of antiepileptic drugs for neurological development in children exposed during pregnancy and breast feeding: a systematic review and network meta-analysis. BMJ Open, 2017. v. 7, n. 7.
WESTON, J. et al. Monotherapy treatment of epilepsy in pregnancy: congenital malformation outcomes in the child. Cochrane Database of Systematic Reviews, 2016, v. 11.
¹Graduanda em Medicina, Centro Universitário CESMAC, Rua Cônego Machado, 918, Farol, Maceió – AL, CEP: 57051-160, marianaroldaoa@gmail.com
²Graduanda de Medicina, Centro Universitário CESMAC, Rua Cônego Machado, 918, Farol, Maceió – AL, CEP: 57051-160, morganafds97@gmail.com
³Doutor em Biologia Celular e Molecular. Instituição: Centro Universitário CESMAC, Endereço: Rua Cônego Machado, 918, Farol, Maceió – AL, CEP: 57051-160 E-mail: laercio.fachin@cesmac.edu.br.
