NEW SCENARIOS FOR THE TREATMENT OF CHAGAS DISEASE: INTEGRATIVE LITERAATURE REVIEW
NUEVOS ESCENARIOS PARA EL TRATAMIENTO DE LA ENFERMEDAD DE CHAGAS: REVISIÓN INTEGRADORA DE LA LITERATURA
REGISTRO DOI: 10.5281/zenodo.8170305
Odália Moura Ibiapina1,
Tamires Robles2,
Carlos Eduardo Lins3
RESUMO
Objetivo: A doença de Chagas (DC), afeta milhões de indivíduos e continua sendo um importante problema de saúde mundial. A baixa eficácia e os efeitos colaterais dos tratamentos atuais exigem novas terapêuticas. Dessa forma, através de um levantamento bibliográfico este trabalho tem como objetivo abordar a atualidade das pesquisas e novas condutas de prevenção e tratamento da DC. Métodos: Este trabalho é caracterizado por uma revisão integrativa de literatura, permitindo a análise de estudos experimentais e não experimentais para a compreensão do fenômeno analisado. Neste trabalho, foi empregado um estudo exploratório com coleta de dados a partir de de artigos científicos, fornecendo a base teórica para as respostas propostas no objetivo. Resultados: As publicações foram selecionadas de acordo com o seguinte critério: busca por novas drogas para o tratamento da DC, no idioma inglês, utilizando os operadores bouleanos and, or e not e as palavras-chave: Chagas disease, treatment, molecular target (Doença de Chagas, tratamento e alvo molecular). Conclusão: Conclui-se que dentre os fármacos citados, a droga mais promissora é a radVax, vacina que atua de forma profilática e terapêutica contra o triatomídeo. Dessa forma, necessita-se de mais estudos para a confirmação de seu poder profilático e curativo.
Palavras-chave: Doença de Chagas, Tratamento, Alvo molecular.
ABSTRACT
Objective: Chagas disease (CD) affects millions of individuals and remains an important global health problem. The low efficacy and side effects of current treatments require new therapies. Thus, through a bibliographic survey, this work aims to address the current research and new practices for the prevention and treatment of CD. Methods: This work is characterized by an integrative literature review, allowing the analysis of experimental and non-experimental studies to understand the analyzed phenomenon. In this work, an exploratory study was used with data collection from scientific articles, providing the theoretical basis for the answers proposed in the objective. Results: The publications were selected according to the following criteria: search for new drugs for the treatment of CD, in English, using the Boolean operators and, or and not and the keywords: Chagas disease, treatment, molecular target (Chagas disease, treatment and molecular target). Conclusion: It is concluded that among the drugs mentioned, the most promising drug is radVax, a vaccine that acts prophylactically and therapeutically against triatomine. Thus, further studies are needed to confirm its prophylactic and curative power.
Key words: Chagas disease, Treatment, Molecular target.
RESUMEN
Objetivo: La enfermedad de Chagas (EC) afecta a millones de personas y sigue siendo un importante problema de salud mundial. La baja eficacia y los efectos secundarios de los tratamientos actuales requieren nuevas terapias. Así, a través de un levantamiento bibliográfico, este trabajo pretende abordar las investigacines actuales y las nuevas prácticas para la prevención y tratamiento de la EC. Métodos: Este trabajo se caracteriza por una revisión integrativa de la literatura, que permite el análisis de estudios experimentales y no experimentales para comprender el fenómeno analizado. En este trabajo se utilizó un estudio exploratorio con recolección de datos de artículos científicos, proporcionando la base teórica para las respuestas propuestas en el objetivo. Revisión bibliográfica: Las publicaciones fueron seleccionadas de acuerdo a los siguientes criterios: búsqueda de nuevos fármacos para el tratamiento de la EC, en idioma inglés, utilizando los operadores booleanos and, or and not y las palabras clave: Chagas disease, treatment, molecular target (Chagas disease, tratamiento y diana molecular). Consideraciones finales: Se concluye que entre los fármacos mencionados, el fármaco más prometedor es radVax, vacuna que actúa profiláctica y terapéuticamente contra triatominos. Por lo tanto, se necesitan más estudios para confirmar su poder profiláctico y curativo.
Palabras clave: Enfermedad de Chagas, tratamiento, diana molecular.
INTRODUÇÃO
A Doença de Chagas foi revelada no início do século XX pelo pesquisador e diretor do Instituto Oswaldo Cruz chamado Carlos Ribeiro Justiniano Chagas. A descoberta da enfermidade por Chagas foi um marco na medicina por se tratar de uma revelação tripla. Em uma só pesquisa, ele conseguiu desvendar o vetor – inseto do gênero Triatoma – mais conhecido como barbeiro, o agente etiológico que mais tarde foi denominado como Trypanosoma cruzi, em homenagem à Oswaldo Cruz, e conseguiu também descrever a patologia em seres humanos. (MARCOLIN N, 2022)
Nas últimas décadas, a situação epidemiológica da doença, no Brasil, mudou devido a resultados obtidos de ações de controle, de transformações ambientais, econômicas e sociais. No momento atual, avalia-se que, variam de 1,9 a 4,6 milhões de indivíduos contaminados pelo T. cruzi, provavelmente 1,0 a 2,4% da população, elevando a carga de mortalidade no país, tornando-se, assim, uma das quatro maiores causas de morte por doenças infecciosas e parasitárias, além de ser a principal doença negligenciada no Brasil. (BRASIL, 2018)
Essa doença e outras também negligenciadas são as principais causas de morbimortalidade no mundo (JORGE MJ, et al., 2022). A Chagas afeta mais de quinze milhões de pessoas e provoca perda de população economicamente ativa por sua condição de doença incapacitante e por seu alto índice de mortalidade prematura observada (WHO, 2007).
Pode ser transmitida de diferentes formas, sendo que a mais importante é a vetorial, mas também pode ocorrer pelo contato direto com fezes e/ou urina de triatomíneos hematófagos, ingestão de alimentos contaminados com parasitos de triatomíneos infectados, transfusão sanguínea ou transplante de órgãos, via materno-fetal, acidentes laboratoriais e transmissão sexual (BRASIL, 2018).
Na tripanossomíase americana, o “barbeiro” elimina as formas infectantes da doença nas fezes ao defecar durante ou após fazer a sucção do sangue, ocorrendo a penetração dessa forma infectante através da mucosa, ferida ou pelo orifício causado pela picada (GALVÃO C, 2014).
A doença de Chagas se expressa em dois estágios: agudo ou crônico. A fase aguda inicial tem duração de até 08 semanas após a infecção, na qual uma grande quantidade de parasitas circula no sangue (WHO, 2007). Clinicamente pode manifestar-se como uma síndrome febril duradoura, devido à elevada parasitemia; em alguns casos, pode acometer a bomba cardíaca e o sistema nervoso central (BRASIL, 2018). Devido aos seus sintomas serem semelhantes aos de várias outras infecções, essa fase pode vir a passar despercebida.
A caracterização na fase aguda da doença varia de acordo com a porta de entrada dos tripanosomas, podendo ser conjuntiva ocular – quando ocorre um edema bipalpebral unilateral, denominado sinal Romaña- Mazza; ou quando o protozoário irrompe em outros locais do corpo – esse tipo de lesão é chamado de chagoma de inoculação (BRASIL, 2010).
Já na fase crônica, os parasitas ficam escondidos no coração e nos músculos digestivos (WHO, 2007). O hospedeiro possue anticorpos circulantes; e a parasitemia não é mais detectável em microscopia direta. Nesta fase, a doença de Chagas possui uma forma indeterminada; sem acometimento clínico ou sintomas, e formas determinadas- como expressões cardíacas, digestivas ou cardiodigestivas, ou algumas menos comuns, como neurológicas (BRASIL, 2018).
Apesar de se observar um enorme financiamento voltado às pesquisas relacionadas a essas doenças, o conhecimento adquirido não é revertido em novos fármacos, métodos diagnósticos e vacinas. Isso acontece devido ao baixo interesse das indústrias farmacêuticas em investir em pesquisas relativas às doenças negligenciadas, justificado pelo baixo retorno lucrativo, já que a população atingida é, na maioria das vezes, de baixa renda (BRASIL, 2010). Algumas indústrias que produziam medicamentos para esses tipos de doenças não dão continuidade a pesquisas e à fabricação destes, devido ao baixo lucro proporcionado por eles (SOBRINHO JL, et al., 2007).
Considerada uma patologia de largo alcance, a doença de Chagas tem como premissa básica a prevenção e/ou a realização de diagnóstico rápido para que seja possível amenizar os danos à saúde dos indivíduos. Em qualquer fase da doença, existem apenas dois medicamentos: o Benzonidazol e o Nifurtimox, ambos usados para a redução da duração e da gravidade clínica da doença. Os principais benefícios no tratamento esperados com o uso desses medicamentos são a redução da parasitemia e da reativação da doença, o aumento da expectativa de vida e a redução das complicações clínicas. (BRASIL, 2018)
A quimioterapia da doença de Chagas tem se mostrado problemática devido à considerável toxicidade destes compostos e à existência de cepas do T. cruzi sensíveis e resistentes a drogas, existindo resistência cruzada entre esses medicamentos. (SGUASSERO Y, 2015)
Há uma busca constante por novos fármacos para um tratamento mais eficaz para a doença de Chagas, porém existem fatores que limitam o uso das drogas testadas. Podemos citar a baixa eficácia desses compostos sobre os pacientes crônicos, a fraca atividade contra muitas cepas de T. cruzi que circulam em zonas geográficas diferentes e os efeitos colaterais consideráveis desses compostos. Ainda, a identificação de novos candidatos tripanocidas que poderiam ser utilizados em estudos clínicos requer parcerias integradas e redes interdisciplinares que envolvem experiências em uma diversidade de campos como a biologia molecular e celular, química e bioquímica, farmacologia e toxicologia. (SOEIRO MN, et al., 2009)
Contudo, apesar do pouco investimento do setor privado, as pesquisas e buscas por novas formas mais eficazes para o tratamento da doença de Chagas têm sido desenvolvidas por diversas entidades em todo o mundo, por se tratar de uma doença que gera grande preocupação dos órgãos governamentais, principalmente por atingir populações mais pobres. Em vista disso, o progresso nessas pesquisas é a temática principal deste trabalho de revisão bibliográfica.
MÉTODOS
Este trabalho é caracterizado por uma revisão integrativa de literatura, permitindo a análise de estudos experimentais e não experimentais para a compreensão completa do fenômeno analisado. Neste trabalho, foi empregado um estudo exploratório com coleta de dados realizada a partir de fontes acessórias de artigos científicos, fornecendo a base teórica para as respostas propostas no objetivo.
A busca foi realizada na base de dados National Center for Biotechnology Information (NCBI), criada em 1988 pelo senado americano, que necessitava de um processamento de dados computadorizado para publicar os avanços obtidos nas pesquisas científicas na área médica. Tem como principais objetivos a criação de máquinas automatizadas que podem analisar e guardar dados da biologia molecular, genética e bioquímica; facilitar o uso de banco de dados e dos programas analíticos pela comunidade científica e reunir dados biológicos. O NCBI oferece vários bancos de dados para que as pesquisas sejam feitas; dentre eles, está o PubMed, que permite que seus usuários tenham acesso a inúmeras publicações da área médica (ROSA et al., 2016).
As publicações foram selecionadas de acordo com o seguinte critério: estudos relacionados à busca por novas drogas para o tratamento da doença de Chagas, no idioma inglês, utilizando os operadores bouleanos and, or e not e as palavras-chave: Chagas disease, treatment, molecular target (Doença de Chagas, tratamento e alvo molecular). Para a verificação dos critérios de inclusão, os títulos e resumos dos artigos selecionados foram analisados. Foram lidos, na íntegra, os artigos cujos resumos não forneciam informações suficientes para uma decisão sobre sua exclusão desta revisão. Após filtrar os artigos de interesse, todos foram lidos para a construção de uma tabela que resume os dados encontrados.
RESULTADOS
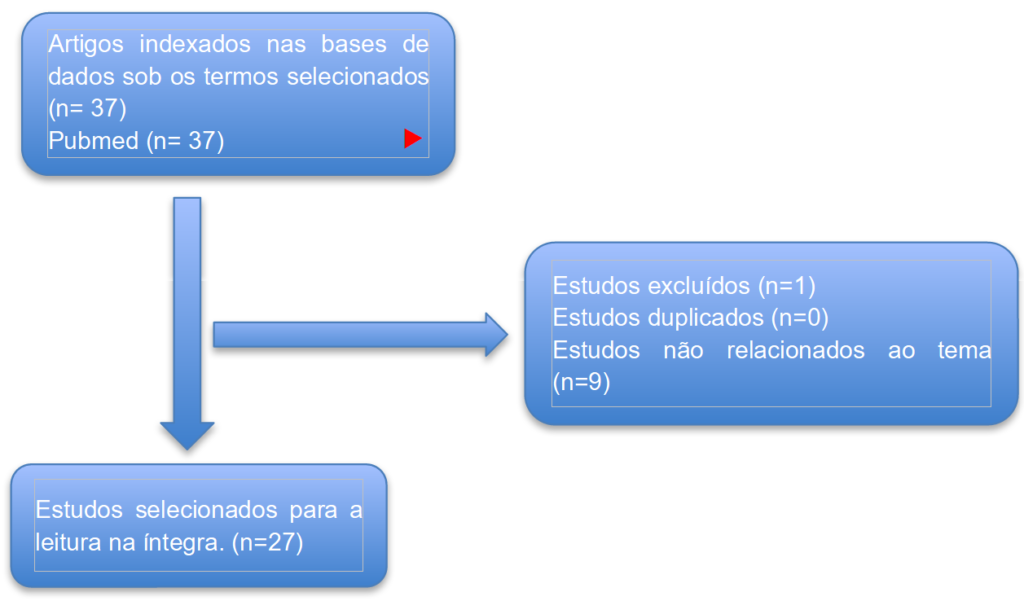
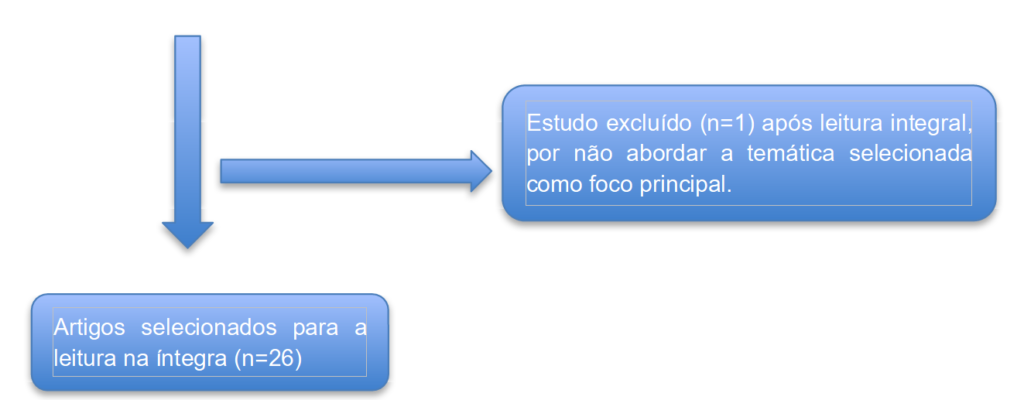
Tabela 5 – Medicamentos mais utilizados e compostos em fase de testes para a Doença de Chagas.
| N | Autores (Ano) | Principais achados |
| 1 | GASPAR L, et al. (2018) | O composto mostrou uma atividade tripanocida contra epimastigotas (presentes no tubo digestivo do inseto vetor) e uma atividade antiparasitária semelhante ao efeito causado pelo Benzonidazol. |
| 2 | FERREIRA DD, et al. (2018) | Estudo in vitro e in silico. Demonstrou eficácia in vitro contra amastigotas intracelulares de ambas as cepas de T. cruzi em diferentes células hospedeiras, incluindo cardiomiócitos e atividade contra tripomastigotas. |
| 3 | BATISTA CM, et al. (2018) | O tratamento com 2-bromopalmitato altera morfologia do parasita, endocitose, diferenciação e infectividade, indicando que 2-BP inibe os principais processos celulares de T. Cruzi. |
| 4 | SAYÉ M, et al (2017) | O ITP-1G inibiu fortemente a diferenciação do estágio do parasito de epimastigota para tripomastigota metacíclico. |
| 5 | KASHIF M, et al (2017) | A TS apresenta uma diversidade de propriedades biológicas (muitas delas independentes de sua atividade enzimática), que promovem a evasão das respostas imunes inata e adaptativa, atuando como um importante fator de virulência do T.cruzy. |
| 6 | ROGERS KE, et al. (2012) | Esforços anteriores identificaram vinilsulfonas, sulfonatos e sulfonamidas como inibidores de cruzaína de alta afinidade; uma dessas sulfonas de vinil, K11777, está atualmente passando por estudos de habilitação de novas drogas em investigação. |
| 7 | MARTÍN-ESCOLANO R, et al. (2021) | O composto 26 apresentou a melhor atividade tripanocida, ainda melhor que o BZN, confirmando o efeito curativo parcial em ambas as fases da DC na dosagem testada. |
| 8 | TORRICO F, et al. (2022) | O E1224 tem toxicidade controlável e mostra atividade antitripanossômica, porém, não tem efeito prolongado. A resposta sustentada (RS) do posaconazol após 12 meses de acompanhamento foi parcial/incompleta. |
| 9 | FERREIRA RR, et al. (2019) | Os compostos reguladores de TGF-β são uma alternativa para o tratamento da fibrose cardíaca, uma vez que o tratamento com GW788388 melhorou o ECG e perfis ECO. |
| 10 | PEREIRA IR, LANNES J (2017) | Apresentou melhor funcionamento das funções cardíacas, além de reprogramar a resposta imune do camundongo vacinado. |
DISCUSSÃO
Novos medicamentos em testes para Doença de Chagas
Inibidores de Sirtuína
As sirtuínas ou Sir (regulador de informações silenciosas) são uma classe de enzimas relacionadas à ligação ou silenciamento de genes. Muitos papéis foram atribuídos às sirtuínas em diferentes organismos, incluindo regulação do tempo de vida, progressão do ciclo celular, transcrição de genes, apoptose, reparo de DNA e metabolismo (JEONG SM, et al., 2015). A primeira sirtuína a ser descoberta foi a Sir2 (GASPAR L, et al., 2018).
Estudos recentes sobre as sirtuínas de Trypanosoma cruzi sugeriram a possibilidade de explorar essas enzimas como possíveis alvos de drogas. A proteína 1 relacionada a Sir2 (TcSir2rp1) é geneticamente validada como alvo de droga e caracterizada por sua atividade desacetilase dependente de NAD+ e sua inibição pela nicotinamida, bem como por derivados de bisnaftalimidopropilo (BNIP), um classe de parasitas inibidores da sirtuína (GASPAR L, et al., 2018).
BNIPs tem capacidade de inibir TcSir2rp1 e atividade antiparasitária contra amastigotas de T. cruzi in vitro. O composto BNIP espermidina (BNIPSpd), foi considerado o inibidor mais potente de TcSir2rp1. Além disso, este composto mostrou atividade tripanocida alterada contra epimastigotas e atividade antiparasitária semelhante ao benznidazol contra amastigotas. Infelizmente, o BNIPSpd falhou em tratar um modelo camundongo da doença de Chagas, possivelmente devido ao seu perfil farmacocinético (VIOTTI R, et al., 2009).
Segundo GASPAR L, et al. (2018) usaram como alvo molecular a Sirtuína – proteína encontrada no T. cruzi – e, como fármaco, a Nicotinamida. O composto mostrou uma atividade tripanocida contra epimastigotas (presentes no tubo digestivo do inseto vetor) e uma atividade antiparasitária semelhante ao efeito causado pelo Benzonidazol. Nessa pesquisa, o alvo molecular mostrou-se efetivo como linha de pesquisa promissora para a descoberta de um novo fármaco eficaz no tratamento e cura da doença de Chagas.
Compostos promissores para Doença de Chagas
Sertralina
Segundo FERREIRA DD, et al. (2018) o reaproveitamento de medicamentos tem sido uma abordagem interessante e econômica, especialmente para a doença de Chagas. A sertralina, um medicamento aprovado pela Food and Drug Administration (FDA), pertence à classe de agentes antidepressivos conhecidos como inibidores seletivos da recaptação da serotonina (ISRSs).
A sertralina demonstrou eficácia in vitro contra amastigotas intracelulares de ambas as cepas de T. cruzi em diferentes células hospedeiras, incluindo cardiomiócitos, com valores de concentração inibitória média (IC50) entre 1 a 10 μM, e atividade contra tripomastigotas da corrente sanguínea, com IC50 de 14 μM (FERREIRA DD, et al., 2018).
FERREIRA DD, et al. (2018) testaram a sertralina como fármacos para sua pesquisa e os resultados demonstraram um efeito letal sobre diferentes cepas do T. cruzi, por afetar o metabolismo energético do parasita. Essas descobertas fornecem um ponto de partida para futuros ensaios experimental e podem contribuir para o desenvolvimento de novos possíveis fármacos eficazes.
2- bromopalmitato
A palmitoilação de proteínas promove a localização da membrana, regulação da atividade enzimática, regulação da expressão gênica e estabilidade proteica (FUKATA Y, et al., 2016). Muitas proteínas palmitoiladas são importantes para diversos aspectos da patogênese em parasitas, incluindo a diferenciação em estágios do ciclo de vida e biogênese, montando o maquinário que alimenta a motilidade e direcionando fatores de virulência para a membrana plasmática.
No estudo de BATISTA CM, et al. (2018) foi analisado o efeito do 2-bromopalmitato (2-BP), um palmitato análogo que pode inibir a palmitoilação, nas diferentes estágios de vida do T. cruzi. Dessa forma, conclui-se que o tratamento com 2-bromopalmitato altera morfologia do parasita, endocitose, diferenciação e infectividade, indicando que 2-BP inibe os principais processos celulares de T. cruzi que pode ser regulado por palmitoilação de proteínas vitais.
A palmitoilação é um importante processo que pode ser um bom alvo para mais estudos celulares/moleculares estudos de biologia com inibidores de palmitoilação específicos a fim de elucidar o ciclo de vida do T. cruzi. Nosso achado importante em tripomastigotas metacíclicos sugere uma dependência de alvo único durante o desenvolvimento de T. Cruzi que é adequado para razões farmacológicas (BATISTA CM, et al., 2018).
Análogos de prolina
Trypanosoma cruzi é o protozoário que causa a doença de chagas, esta afeta cerca de 6 milhões de pessoas na América Latina (WHO, 2015). Este protozoário usa a prolina como sua principal fonte de carbono, essencial para o crescimento de parasitas em epimastigotas e amastigotas. Além de seu papel como fonte de carbono, a prolina sustenta a invasão celular e diferenciação de epimastigotas intracelulares para tripomastigotas (MARTINS RM, et al., 2009).
Além disso, a prolina também participa da resistência ao estresse nutricional e oxidativo, bem como de resistência às drogas (MAGDALENO A, et al, 2009; SAYÉ M, et al., 2014). Como a prolina está envolvida em muitos processos biológicos essenciais no T.cruzy, seu transporte e metabolismo são alvos interessantes de drogas.
Quatro análogos de prolina sintética (ITP-1B/1C/1D/1G) foram avaliados como inibidores do transporte de prolina através das permeases TcAAAP0069. A atividade tripanocida dos compostos também foi avaliada. Os compostos ITP-1B e ITP-1G inibiram o transporte de prolina mediado pela permease TcAAAP069 de maneira dose-dependente. Os análogos ITP-1B, -1D e -1G tiveram efeito tripanocida sobre epimastigotas de T. cruzi com valores de IC50 entre 30 e 40 μM. No entanto, apenas a atividade tripanocida do ITP-1G foi relacionada com seu efeito inibitório sobre o transportador de prolina TcAAAP069. Além disso, este análogo inibiu fortemente a diferenciação do estágio do parasito de epimastigota para tripomastigota metacíclico. Finalmente, os compostos ITP-1B e ITP-1G também foram capazes de inibir o transporte mediado por outras permeases da mesma família de permeases de aminoácidos, TcAAAP.
Anteriormente, Magdaleno A, et al. (2009) demonstraram que o ácido tiazolidina-4-carboxílico (T4C), análogo de prolina, interfere com o metabolismo da prolina e reduziu em até 56% os tripomastigotas que irrompe das células de mamíferos. Além disso, este composto inibe o transporte de prolina mediado pelo transportador TcAAAP069 (SAYÉ M, et al., 2014). Apesar destes resultados, o T4C análogo apresenta altos valores de IC50 (0,5-0,9 Mm) para culturas de epimastigotas, tornando-o um inibidor interessante, mas não um medicamento tripanocida.
Os análogos de prolina sintético constitui um alvo terapêutico múltiplo e promissor para o desenvolvimento de novos tratamentos contra a doença de chagas. O composto ITP-1G é um ponto de partida interessante para o desenho de novos medicamentos tripanocidas (SAYÉ M, et al., 2017).
Inibidores de trans-sialidase
De acordo com DIAS LC, et al. (2009) as trans-sialidades (TS), membros de uma família de glicoproteínas de superfície do T. cruzy, são enzimas que aceleram a transferência de ácido siálico das proteínas do meio extracelular para as moléculas de mucina que recobrem a superfície do parasita. Como o T. cruzy é incapaz de sintetizar o ácido siálico, o único mecanismo de sialilação das suas glicoproteínas de membrana consiste na transferência deste açúcar a partir das células hospedeiras através dessas enzimas, o que as torna um alvo promissor (NERES JR, et al., 2008).
Atividade da TS foi detectada no sangue de animais infectados com T. cruzi. A intensidade dessa atividade correlacionou-se bem com a parasitemia em camundongos imunodeficientes ou durante os primeiros nove a dez dias de infecção em camundongos normais. Nestes últimos camundongos houve uma correlação inversa entre parasitemia e intensidade de trans-sialidase circulante a partir do 11º dia pós-infecção. Foi demonstrado que este fenômeno deveu-se a anticorpos com capacidade de suprimir a atividade da TS.
Além disso, o T.cruzy usa a TS para se disfarçar do sistema imunológico do hospedeiro (RUBIN SS, SCHENKMAN S, 2012). A partir desta pesquisa, conclui-se que os inibidores de trans-sialidase atualmente eficaz ainda não foram alcançados. Várias abordagens têm sido usadas para projetar os melhores compostos de chumbo que pode ser usado como precursor inicial para a droga.
Primeiro, ácido siálico mimético como análogos baseados em doadores e aceitadores podem ser usados, mas devido à sua estrutura complexa e maior massa molecular, eles são pouco atraentes como drogas potenciais e ainda testes contra TcTS são necessários. Segundo, compostos não açucarados, especialmente derivados de ácidos carboxílicos tendo o grupo amino e hidroxila no anel fenil, têm uma vantagem sobre o aceitador à base de açúcar e análogos doador devido à sua estrutura simples, menor massa molecular e facilidade de síntese e substituição de substituintes.
Este estudo mostrou fortes evidências de que os derivados do ácido carboxílico mostram uma forte interação com sítios ativos de trans-sialidase. Nessa revisão, os efeitos inibitórios produzidos por derivados do ácido carboxílico com substituintes apropriados são notáveis, indicando que estes poderiam ser usados como andaimes para o projeto de novos fortes inibidores contra trans-sialidases do T.cruzy.
Os valores de inibição dos compostos revisados indicam uma necessidade para a concepção de inibidores de TcTS mais adequados, que, deve se ligar fortemente ao sítio ativo e ao mesmo tempo requerem concentrações mais baixas para inibição completa (KASHIF M, et al., 2017).
Inibidores da cruzaína
A principal cisteína proteinase do T.cruzy, a cruzaína (ou cruzipaína) demonstrou ser crucial para o ciclo de vida do parasita. Pensa-se que esta enzima semelhante à papaína desempenha um papel importante na diferenciação, invasão celular, multiplicação intracelular e evasão imunológica. Além disso, estudos demonstraram que inibidores da cisteína proteinase tem atividade tripanocida com toxicidade insignificante em mamíferos (MCKERROW JH, et al., 2008).
Esforços anteriores identificaram vinilsulfonas, sulfonatos e sulfonamidas como inibidores de cruzaína de alta afinidade (BRINEN LS, et al., 2008); uma dessas vinilsulfonas, K11777, está atualmente passando por estudos de habilitação de novas drogas em investigação (BRYANT C, et al., 2009). Embora esses sucessos sejam encorajadores, muitos medicamentos em potencial, incluindo aqueles que entram em ensaios clínicos, acabam falhando em obter aprovação (DIMASI JA, et al., 2001), e os que são aprovados estão sujeitos a crescente resistência parasitária.
Dos 30 compostos testados, oito inibiram a cruzaína a 100 μm. Usando condições padrão, o composto de melhor pontuação tinha um valor inicial de IC 50 de 471 nm. Experimentos subsequentes sugeriram que este composto inibia a cruzaína não especificamente por meio de agregação. Felizmente, três outros compostos, embora menos potentes, de fato parecem inibir especificamente a cruzaína. Esses três compostos, NSC 227186, NSC 67436 e NSC 260594, têm valores de IC 50 de 16, 63 e 66 μm , respectivamente.
Embora esses compostos não tenham a característica de afinidade nanomolar dos medicamentos aprovados, eles possuem a afinidade micromolar baixa típica dos compostos de chumbo. Com otimização adequada, incluindo adição de fragmentos, troca de frações e busca de similaridade, esses compostos podem ser transformados em candidatos a medicamentos viáveis. Esperamos que essas novas pistas sejam úteis para aqueles na comunidade de descoberta de medicamentos voltados para a DC (ROGERS KE, et al., 2012).
Derivados do selênio
Segundo MARTÍN-ESCOLANO R, et al., (2021) em resposta a necessidade por novos fármacos para a DC, uma biblioteca química de 41 amidas de selênio leishmanicidas e derivados de fosforamidato foram testados contra T. Cruzi. Os compostos mais ativos e seletivos contra a forma epimastigota (compostos 25, 26, 28, 29 e 33) foram testados nas formas amastigotas e tripomastigotas. Tendo em conta a atividade e seletividade dos derivados, 26 e 28 foram selecionados para os estudos vivos.
O composto 26 exibe um perfil melhor que o 28 e BZN, e atende aos mais rigorosos requisitos in vitro para potenciais agentes antichagásicos. Mostrou maior atividade e menor toxicidade do que o BZN após o tratamento in vivo, através do monitoramento de parasitemia, PCR, IS ou análise bioquímica. A análise do modo de ação sugere atividade tripanocida via necrose de maneira dependente da mitocôndria através de um colapso bioenergético causado por uma falha mitocondrial. Esses achados sugerem que esses derivados poderiam ser explorados e dar um passo à frente no desenvolvimento de novos agentes antichagásicos. Vale a pena considerando doses mais altas e/ou esquemas de tratamento diferentes, mesmo terapias combinadas, para obter uma cura estéril (MARTÍN-ESCOLANO R, et al., 2021).
O número médio de amastigotas por célula também foi medida, dando uma ideia da taxa de mortalidade. Esse valor foi medido após 72 h de exposição em diferentes concentrações de compostos e BZN, e os dados mostram que os compostos exibem comportamento semelhante ao BZN, que é considerado como um composto de ação rápida (CHATELAIN E, 2015). O número de amastigotas por célula diminuiu gradualmente em todos os casos após 72 h de exposição, destacando que o efeito dos compostos testados em 50 μM reduziu o número de amastigotas a praticamente zero.
Esses dados mostram que os compostos não apenas inibem a multiplicação do parasita, mas também causa a sua morte. Todas essas características são vantagens adicionais desde ação rápida e tripanocida capaz de eliminar o parasita em poucas doses, como bem como agir contra a forma dormente amastigota (forma responsável pelas recidivas após a quimioterapia) (SANCHEZ-VALDÉZ FJ, et al., 2018).
Para avaliar ainda mais a eficácia dos compostos na DC aguda e crônica, a presença do T. cruzi a em órgãos/tecidos-alvo foi medida por PCR após necropsia (145 dpi) nos 4 grupos de camundongos em ambas as fases. Como esperado, em camundongos não tratados mostrou a presença de parasitas em todos os órgãos/tecidos para ambas as fases. Em camundongos tratados com BZN, cérebro e pulmão pareciam livres de parasitas na fase aguda, e cérebro, esôfago e pulmão pareciam livres de parasitas na fase crônica (28,6 e 42,9% de órgãos/tecidos livres de parasitas, respectivamente).
Em camundongos tratados com o composto 26 houve melhores resultados do que com BZN. Neste caso, tecido adiposo, cérebro e pulmão apresentaram-se livres de parasitas na fase aguda, e medula óssea, cérebro, esôfago para a fase crônica (42,9% de órgãos/tecidos livres de parasitas em ambas as fases). Em contraste, o tratamento com composto 28 não diminuiu níveis suficientes de parasitas nos tecidos. Conforme observado, o composto 26 apresentou a melhor atividade tripanocida, ainda melhor que a demonstrada pelo BZN, confirmando o efeito curativo parcial em ambas as fases da DC na dosagem testada (MARTÍN-ESCOLANO R, et al., 2021).
Derivados azólicos
O ravuconazol (RAV) é um inibidor da biossíntese do ergosterol com potente atividade in vitro e in vivo contra a DC em modelos animais. (BUCKNER FS, 2008). Dados encorajadores aumentaram as esperanças de que o E1224, um pró-fármaco do ravuconazol solúvel em água, poderia ser um candidato para desenvolvimento clínico em DC, e a primeira nova entidade química desenvolvida em mais de três décadas.
As exposições sistêmicas globais ao RAV são substancialmente maiores em humanos com a administração do pró-fármaco E1224, levando ao aumento da biodisponibilidade e à meia-vida terminal plasmática mais longa. Com a estratégia de dose de carga de E1224, o estado estacionário é alcançado em ≤ 1 semana e permite a dosagem uma vez por semana para manutenção das concentrações plasmáticas alvo.
O estudo envolveu 231 pacientes. A depuração do parasita foi observada com E1224 durante a fase de tratamento, mas nenhuma resposta sustentada (SR) foi observado com esquemas de baixa dose (dose total = 2.000 mg) e de dose curta (dose total = 2.400 mg) de E1224, enquanto 28,9% dos pacientes tiveram SR com o regime de alta dose (dose total = 4000 mg). BZN (2,5 mg/kg/dia por via oral BID, 60 dias) teve um efeito rápido e sustentado na eliminação do parasita (82,2%, 95%). A SR do grupo placebo foi de 8,5%. A redução significativa do título de ELISA foi observada apenas em pacientes tratados com BZN. Ambos os tratamentos foram bem tolerados. Aumentos reversíveis e dose-dependentes das enzimas hepáticas foram observados com E1224 e BZN (TORRICO F, et al., 2022).
Após uma longa espera por novos medicamentos para DC, fornecemos evidências iniciais de que o E1224 tem toxicidade controlável e mostra atividade antitripanossômica durante o tratamento. Porém, dada a falta de efeito prolongado, o E1224 não será mais investigado em monoterapia. No entanto, devido ao seu perfil de segurança favorável, as combinações de E1224 com BZN ou nifurtimox, devem ser consideradas, porque estudos em animais mostram que a terapia combinada tem o potencial de melhorar a resposta ao tratamento e encurtar o tratamento (DINIZ LF, et al., 2013; BATISTA DGJ, et al., 2011).
Em conclusão, o E1224 exibiu um efeito supressor transitório, enquanto o BZN mostrou eficácia precoce e sustentada por PCR e ELISA. Esses resultados fornecem suporte para a ampliação do diagnóstico e acesso a regimes padrão de BZN e fornecem um roteiro para o desenvolvimento e registro de novos regimes alternativos de tratamento de BZN em monoterapia e em combinações com E1224 para o tratamento de adultos com DC crônica indeterminada (TORRICO F, et al., 2022).
Inibidores do TGF-beta
O TGF-β é uma das principais citocinas envolvidas no processo de fibrose (POHLERS D, et al.,2009). No estudo de OLIVEIRA FL, et al., (2012) demonstrou-se o efeito protetor da administração oral de GW788388, um inibidor da atividade do receptor TGF-β, a 20 dpi em um modelo agudo de DC experimental, diminuindo fibrose cardíaca e melhorando a sobrevida global.
No presente trabalho, teve-se como objetivo estudar o uso de GW788388 em um modelo pré-clínico com fibrose cardíaca chagásica crônica, situação mais frequente observada em humanos. Para testar essa hipótese, usou-se um camundongo com infecção crônica, que reproduz características clínicas relevantes da cardiopatia chagásica (POHLERS D, et al.,2009; PEREIRA IR, et al., 2014).
Esses dados demonstraram que o tratamento com GW788388 iniciado em 120 dpi, quando a cardiopatia chagásica crônica (CCC) já está estabelecida, melhorou a frequência cardíaca, diminuiu os eventos de BAV II, desencadeou a correção das placas intercelulares, reverteu a fibrose cardíaca, anormalidades elétricas e restaurou uma FEVE normal. Interessantemente, o tratamento com GW788388 foi capaz de regenerar o tecido cardíaco com entrada de novas células cardíacas.
Este estudo pré-clínico coloca o TGF-β como uma alternativa para o tratamento da fibrose cardíaca, uma vez que o GW788388 melhorou o ECG e perfis do ecocardiograma; níveis modulados de TGF-β e suas proteínas intracelulares; reverteu a perda de conexão 43 placas intercelulares; fibrose reduzida do tecido cardíaco; marcadores de recuperação cardíaca restaurada e reduziu a migração de células CD3+ para o coração. Além disso, a 180 dpi, 30 dias após a interrupção do tratamento, o grupo tratado com GW788388 permaneceu em melhor condição funcional cardíaca. Esses dados são promissores e a inibição da via TGF-β é uma relevante estratégia terapêutica da fibrose cardíaca na fase crônica da DC (FERREIRA RR, et al., 2019).
Vacina
Na busca por um meio de tratamento eficaz PEREIRA IR e LANNES J, (2017) apresentaram um estudo sobre uma promissora vacina que está sendo estudada. Com o avanço da tecnologia e pesquisas com o Trypanosoma cruzi, foi possível descobrir uma possível vacina contra a doença de Chagas que pode funcionar tanto para ação profilática quanto terapêutica, atribuíram o nome dessa vacina de rAdVax.
No processo de pesquisa da radVax foram descobertas duas proteínas importantes chamadas de ASP2 uma proteína de superfície de formas amastigotas, importantes para o estabelecimento da fase crônica da doença, e a outra foi a TS uma enxima de formas tripomastigotas que catalisa a transferência do ácido siálico de glicoproteínas do hospedeiro para moléculas receptoras na membrana do parasita.
Como principal resultado do uso da rAdVax foram observados o controle das funções cardíacas como batimentos cardíacos próximos do normal e melhora da lesão cardíaca , além do melhor funcionamento das funções cardíacas, a vacina reprogramou a resposta imune dos camundongos vacinados, diminuindo a produção de óxido nítrico, que pode ser tóxico, diminuiu também a produção de perforina, uma proteína que causa alterações elétricas e lesão nas fibras musculares do coração, nas afetou as citocinas benéficas, que ajudam a reduzir os danos cardíacos e a fibrose cardíaca.
CONSIDERAÇÕES FINAIS
Tendo em vista as pesquisas realizadas atualmente, entende-se que há baixos investimentos em pesquisas e experimentos para o tratamento da doença de Chagas, por se tratar de uma doença negligenciada e de baixo retorno lucrativo para as indústrias farmacêuticas, todavia algumas instituições como a Fundação Oswaldo Cruz (FIOCRUZ) ainda procuram por um tratamento mais eficaz e medidas profiláticas, reduzindo assim as reações adversas causadas pela doença de Chagas e a toxicidade de medicamentos existentes como benzonidazol. Dessa forma, chega-se a conclusão que a droga mais promissora dentre todas as discutidas acima é a radVax, que atuam em proteínas importantes para a sobrevivencia do Trypanosoma cruzi e foi capaz de melhorar a função cardíaca, assim como reduziu o grau de fibrose no tecido miocárdico. Além disso, atua tanto de forma profilática quanto terapêutica, entretanto são necessários mais estudos acerca do seu potencial terapêutico e curativo. Ademais, a droga com menor potencial terapêutico foi o E1224, que exibiu um efeito supressor transitório sobre PCR e ELIZA, no entanto, devido ao seu perfil de segurança favorável, as combinações de E1224 com BZN ou nifurtimox, devem ser consideradas.
REFERÊNCIAS
1. BATISTA DGJ, et al. Combined Treatment of Heterocyclic Analogues and Benznidazole upon Trypanosoma cruzi In Vivo. PLoS One. 2011; 6 e22155.
2. BATISTA CM, et al. Treatment of Trypanosoma cruzi with 2-bromopalmitate alters morphology, endocytosis, differentiation and infectivity. BMC Cell Biology. 19:19. 2018.
3. BRASIL. Doenças negligenciadas: estratégias do Ministério da Saúde. Rev. Saúde Pública, 2010; 44(1):200-2. Disponível em: https://doi.org/10.1590/S0034-89102010000100023. Acessado em: 10/01/2023.
4. BRASIL. Protocolo Clínico e Diretrizes Terapêuticas, Doença de Chagas. 2018. Disponível em: https://doi.org/10.20513/2447-6595.2018v58n4p6-7. Acessado em: 23/01/2023.
5. BRINEN LS, et al. Um alvo dentro do alvo: sondagem do sítio P1′ da cruzaína para definir determinantes estruturais da protease da doença de Chagas. Estrutura. 2000; 8 :831–840.
6. BRYANT C, et al. Novas vinilsulfonas não peptídicas visando os subsítios S2 e S3 das cisteína proteases do parasita. Bioorg Med Chem Lett. 2009; 19 :6218–6221.
7. BUCKNER FS. Sterol 14-demethylase inhibitors for Trypanosoma cruzi infections. Adv Exp Med Biol. 2008; 625: 61–80.
8. CHATELAIN E. Chagas disease drug discovery: toward a new era. 2015. J. Biomol. Screening 20 (1), 22−35.
9. DC-RUBÍN SS e SCHENKMAN S. Trypanosoma cruzi trans-sialidase as a multifunctional enzyme in Chagas’ disease. Cell Microbiol 2012;14:1522–30.
10. DIMASI JA. Riscos no desenvolvimento de novos medicamentos: taxas de sucesso de aprovação para medicamentos em investigação. Clin Pharmacol Ther. 2001; 69 :297–307.
11. DIAS LC, et al. Quimioterapia da Doença de Chagas: estado de Arte e Perspectivas no desenvolvimento de novos fármacos. Química Nova, v.32, p. 2444-2457, 2009.
12. DINIZ LF, et al. Benznidazole and posaconazole in experimental Chagas disease: positive interaction in concomitant and sequential treatments. PLoS Negl Trop Dis. 2013; Aug 15. 7 (8) e2367.26.
13. FERREIRA DD, et al. Efficacy of sertraline against Trypanosoma cruzi: an in vitro and in silico study. Journal of Venomous Animals and Toxins including Tropical Diseases. 24:30. 2018.
14. FERREIRA RR, et al. TGF-β inhibitor therapy decreases fibrosis and stimulates cardiac improvement in a preclinical study of chronic Chagas’ heart disease. PLOS Neglected Tropical Diseases.
15. FUKATA Y, et al. Local palmitoylation cycles and specialized membrane domain organization. Curr Top Membr. 2016;77:97–141.
16. GALVÃO C. Vetores da doença de chagas no Brasil [online]. Sociedade Brasileira de Zoologia, 2014 (20. ed.), p.289.
17. GASPAR L, et al. Inhibitors of Trypanosoma cruzi Sir2 related protein 1 as potential drugs against Chagas disease. PLoS Negl Trop Dis 12(1): e0006180. 2018. Disponível em: https://doi.org/10.1371/journal.pntd.0006180. Acesso em: 10 março 2023.
18. JORGE MJ, et al. Efeitos da inovação organizacional no desempenho da atenção integral em doença de chagas. Rev. UNA. 2016, v. 21, n. 4, p. 57-80.
19. KASHIF M, et al. Recent developments in trans-sialidase inhibitors of Trypanosoma cruzi. J Drug Target. 25:485–98. 2017.
20. MAGDALENO A, et al. Silber, Actions of a proline analogue, Lthiazolidine- 4-carboxylic acid (T4C), on Trypanosoma cruzi, PLoS One 4 (2009).
21. MARCOLIN N. Chagas: Há 100 anos o médico brasileiro descobria o ciclo completo da doença que leva seu nome. Pesquisa FAPESP, 2009; (163): 56- 9.
22. MARTINS RM, et al. Use of L-proline and ATP production by Trypanosoma cruzi metacyclic forms as requirements for host cell invasion, Infect. Immun. 77 (2009) 3023–3032.
23. MARTÍN-ESCOLANO R , et al. Derivados do selênio como terapia promissora para a doença de Chagas: estudos in vitro e in vivo. ACS Infect Dis. 11 de junho de 2021; 7(6): 1727–1738.
24. MCKERROW JH, et al. Desenvolvimento de inibidores de protease para infecções por protozoários. Curr Opin Infect Dis. 2008; 21 :668–672.
25. NERES JR, et al. Rational drug design in parasitology: trans-sialidase as a case study for Chagas disease. Drug Discov. Today, v.13, n.3-4, p. 110-7, 2008.
26. OLIVEIRA FL, et al. Oral Administration of GW788388, an Inhibitor of Transforming Growth Factor Beta Signaling, Prevents Heart Fibrosis in Chagas Disease. PLoS Negl Trop Dis. 2012; 6: e1696.
27. PEREIRA IR, et al. Tumor Necrosis Factor Is a Therapeutic Target for Immunological Unbalance and Cardiac Abnormalities in Chronic Experimental Chagas ‘ Heart Disease. Mediators Inflamm. 2014; 2014: 1–16.
28. PEREIRA IR, LANNES J. Vacina para doença de Chagas: realidade ou utopia?,2017. Portal da Doença de Chagas. Disponível em: http://chagas.fiocruz.br/doenca/vacinas/. Acessado em: 28 out. 2022.
29. POHLERS D, et al. TGF- β and fibrosis in different organs—molecular pathway imprints. Biochim Biophys Acta. 2009; 1792: 746–756.
30. ROGERS KE, et al. Novel Cruzain Inhibitors for the Treatment of Chagas’ Disease. Chem Biol Drug Des. n. 80: 398–405. 2012.
31. SÁNCHEZ-VALDÉZ FJ, et al. (2018) Spontaneous dormancy protects Trypanosoma cruzi during extended drug exposure. eLife 7, No. e34039.
32. SAYÉ M, et al. Proline modulates the trypanosoma cruzi resistance to reactive oxygen species and drugs through a novel D, L-proline transporter, PLoS One 9 (2014).
33. SAYÉ M, et al. Evaluation of proline analogs as trypanocidal agents through the inhibition of a Trypanosoma cruzi proline transporter. BBA – General Subjects. n.1861, 2913–2921. 2017.
34. SGUASSERO Y, et al. Course of Chronic Trypanosoma cruzi Infection after Treatment Based on Parasitological and Serological Tests: A Systematic Review of Follow-Up Studies. PLoS ONE. 2015. 10(10).
35. SOBRINHO JL, et al. Delineamento de alternativas terapêuticas para o tratamento da Doença de Chagas. Revista de Patologia Tropical. 2007, 36 (2): 103- 118.
36. SOEIRO MN, et al. Experimental chemotherapy for Chagas disease: 15 years of research contributions from in vivo and in vitro studies. Memórias do Instituto Oswaldo Cruz, 2009; 104(Suppl. 1), p 301-10.
37. TORRICO F, et al. Treatment of adult chronic indeterminate Chagas disease: proof-of-concept randomized placebo-controlled study of benznidazole and three E1224 dosing regimens. Lancet Infect Dis. Author manuscript; available in PMC 2022 April 01.
38. VIOTTI R, et al. Side effects of benznidazole as treatment in chronic Chagas disease: fears and realities. Expert Rev Anti Infect Ther, 2009, 7 (2), 157±163.
39. WHO. Reporte del grupo de trabajo cientifico sobre la enfermidad de Chagas. TDR. Argentina; 17-20 de abril de 2005, atualizado em julho de 2007, p. 1-104. Disponível em: https://apps.who.int/iris/handle/10665/69724. Acessado em: 15/01/202
40. WHO. Chagas disease in Latin America: an epidemiological update based on 2010 estimates, Wkly Epidemiol. Rec. (2015) 33–44. Disponível em: http://dx.doi.org/10.2147/IBPC.S70402. Acessado em: 24/03/2023.
1 Centro Universitário Maurício de Nassau (UNINASSAU), Barreiras – Bahia. *E-mail: odaliaibiapina@gmail.com
2 Pontifícia Universidade Católica de São Paulo (PUC-SP), São Paulo – SP. E-mail: tamires_robles@hotmail.com
3 Centro Universitário de Atenas (UniAtenas), Paracatu – MG. E-mail: dudu_lins7@hotmail.com
