REGISTRO DOI: 10.5281/zenodo.7316932
Marjorie Moura Passos1, Barbara Schneweiss de Queiroga Justiniano1, Maria Aparecida Taveiros de Lima1, Priscila Ferreira Silva2, Gabriela Ribeiro Ricci3.
RESUMO:
Na reprodução humana assistida existem diversos tratamentos que são utilizados para viabilizar uma gestação em casais que possuem fatores de infertilidade. Entre eles, a fertilização in vitro que consiste na estimulação ovariana através de medicamentos, seguida da punção de ovócitos, os quais são morfologicamente classificados de acordo com o seu grau de maturação e posteriormente, aqueles que apresentam qualidade, são fertilizados in vitro. Essa técnica apresenta cerca de 58,6% de sucesso de acordo com os dados de uma clínica de reprodução humana assistida, localizada em São Paulo/SP.
Outro tratamento que tem ganhado cada vez mais espaço dentro da reprodução humana, é a criopreservação de ovócitos. O procedimento ocorre após a punção dos ovócitos, submetendo-os a uma vitrificação em nitrogênio líquido. O principal objetivo das pacientes que optam por realizar esse tratamento é a preservação da fertilidade, pois observa-se na sociedade uma tendência nas mulheres de maternidade tardia, após os 36 anos.
Nesse sentido, o objetivo desse trabalho é comparar a taxa de sucesso entre tratamentos de fertilização in vitro realizados com ovócitos coletados à fresco e ovócitos que foram submetidos a criopreservação, a fim de verificar a taxa de sucesso de ambas as técnicas e concluir até que ponto a criopreservação de ovócitos pode preservar a fertilidade. Para isso, serão usados os dados retroativos de uma Clínica de Reprodução Humana Assistida, localizada em São Paulo, SP / Brasil referente ao ano de 2021, explorando os diferentes protocolos referentes a mesma técnica.
Palavras chaves: fertilização in vitro, criopreservação, ovócitos, infertilidade.
ABSTRACT
In assisted human reproduction, there are several treatments that are used to facilitate pregnancy in couples who have infertility factors. Among them, in vitro fertilization, which consists of ovarian stimulation through drugs, followed by oocyte puncture, which are morphologically classified according to their degree of maturation and, later, those that present quality, are fertilized in vitro. This technique has about 58.4% success according to data from Clínica Engravida in the year 2021.
Another treatment that has gained more and more space within human reproduction is the cryopreservation of oocytes. The procedure takes place after the oocytes are punctured, subjecting them to vitrification in liquid nitrogen. The main objective of patients who choose to undergo this treatment is the preservation of fertility, as there is a trend in society in women of late maternity, after 36 years of age.
In this sense, the objective of this work is to compare the success rate between in vitro fertilization treatments performed with freshly collected oocytes and oocytes that were submitted to cryopreservation, in order to verify the success rate of both techniques and to conclude to what extent the Oocyte cryopreservation can preserve fertility. For this, the retroactive data of the Engravida Clínica de Reproduction Humana Assisted referring to the year 2021 will be used, exploring the different protocols regarding the same technique.
Keywords: in vitro fertilization, cryopreservation, oocytes, infertility.
INTRODUÇÃO
O aparelho reprodutor feminino consiste em dois ovários, duas tubas uterinas, o útero, a vagina e a genitália externa, conhecida como vulva que é formada por clítoris, pequenos lábios, grandes lábios e pela abertura vaginal e da uretra. Suas funções são produzir gametas femininos (ovócitos) e manter um ovócito fertilizado durante seu desenvolvimento completo através da fase embrionária e fetal até o nascimento. O aparelho reprodutor feminino ainda produz hormônios sexuais que controlam órgãos do aparelho reprodutor e tem influência sobre outros órgãos do corpo. (L. C. Junquerira e José Carneiro, 2013)
O processo de formação e desenvolvimento dos gametas femininos se dão por um mecanismo complexo de interação entre os tecidos que compõem o sistema reprodutor feminino e os hormônios atuantes nesta fisiologia, dando origem a uma meiose célular. No primeiro passo da meiose 2, o DNA das células germinativas (2n) é replicado até que cada cromossomo seja duplicado (46 cromossomos duplicados 92 cromossomos). A célula, agora chamada de e ovócito primário, contém duas vezes a quantidade normal de DNA (4n). Entretanto, a divisão da célula e dos cromossomos não ocorre como na mitose. Em vez disso, cada cromossomo duplicado forma duas cromátides-irmãs idênticas. Os gametas primários, então, estão prontos para sofrer divisões meióticas e dar origem às células haploides.
(Silverthon, 2017)
Na primeira divisão meiótica, um gameta primário divide-se em dois gametas secundários (ovócito secundário). Cada gameta secundário recebe uma cópia de cada autossomo duplicado mais um cromossomo sexual (2n). Na segunda divisão meiótica, as cromátides-irmãs separam-se. Nas mulheres, a segunda divisão meiótica dá origem a um ovócito e a uma pequena célula, chamada de corpúsculo polar. O que acontece depois depende de se o ovócito é fertilizado ou não. (Silverthon, 2017)
O sistema reprodutor feminino, juntamente com seus órgãos e células tem como objetivo possibilitar uma gestação à mulher. No entanto, diversos fatores tanto patológicos, quanto relacionados ao estilo de vida, podem interferir neste processo. Alguns exemplos de patologias que interferem na fertilidade feminina são, a endometriose, obstrução tubária, alterações no tecido uterino, além de doenças que podem ser desencadeadas por infecções sexualmente transmissíveis. (Elvio Tognotti, 2014)
Alguns hábitos do cotidiano também podem interferir na homeostasia do sistema reprodutor feminino, se forem mantidos a longo prazo, como o tabagismo, falta de prática de exercícios físicos, má alimentação e falta de acompanhamento ginecológico periódico. Essas práticas podem levar a infertilidade gerando complicações a saúde íntima da mulher. (Rodrigo da Rosa Filho, 2015)
Além dos fatores já citados, a idade da mulher também interfere de forma direta na fertilidade pois a qualidade dos ovócitos é perdida ao longo dos anos através do envelhecimento celular que acarreta alterações genéticas e morfológicas, as quais dificultam o processo de fertilização. No Brasil, aumenta o número de mulheres que posterga a maternidade para depois dos 35 anos. Este fenômeno evidencia o tempo de educação da mulher e sua entrada no mercado de trabalho, que exigem o adiamento da maternidade. Logo, a idade materna avançada é um fator que tem influenciado diretamente na fertilidade. (Fernanda Travassos, Terezinha Carneiro, 2013)
Nesse contexto, foram desenvolvidas técnicas de reprodução humana assistida para proporcionar alternativas aos casais que não conseguem engravidar de forma natural. A Reprodução Humana Assistida teve início na Inglaterra em 1978, quando nasceu o primeiro bebê de proveta. A primeira FIV foi realizada pelos doutores Patrick Steptoe e Robert Edwards na Inglaterra e em 25 de julho de 1978 nasceu a primeira criança, Louise Brown, concebida pela Fertilização In Vitro. (Fert Embryo, 2020).
Existem inúmeros procedimentos dentro da reprodução humana assistida, como o coito programado, inseminação intrauterina, fertilização in vitro e injeção intracitoplasmática de espermatozoides. Cada técnica possui um protocolo laboratorial que tem como objetivo facilitar o processo de fecundação dos ovócitos pelos espermatozoides e posteriormente gerar uma gestação. Através desses procedimentos é possível driblar as patologias que geram a infertilidade e até mesmo reparar os danos gerados à fertilidade na escolha pela maternidade tardia (Elvio Tognotti, 2014).
Além dos tratamentos desenvolvidos para possibilitar a maternidade, também existem aqueles que foram criados para preservar a fertilidade. O congelamento de ovócitos tem possibilitado que muitas mulheres preservem a integridade das suas células reprodutoras durante a juventude e as usem anos depois, no momento em que se sentirem prontas para gestar. A primeira gravidez com oócito congelado ocorreu em 1986 e, desde então, houve grande progresso desta técnica. (Arnaldo Cambiaghi, 2022)
Quando se fala em tratamentos de reprodução humana assistida a FIV é considerada um tratamento de alta complexidade em infertilidade e consiste na fertilização realizada em laboratório, onde os gametas (ovócitos e espermatozoides) são manipulados e unidos com o intuito de formar embriões. O que a FIV faz é realizar no laboratório (in vitro) apenas uma das etapas da concepção. Após a implantação intrauterina do(s) embrião(ões), a evolução ocorre naturalmente. (Elvio Tognotti, 2014).
JUSTIFICATIVA
Atualmente a sociedade tem influenciado nos hábitos de vida da mulher. É notável que a maternidade tem sido postergada, muitas vezes, em detrimento de fatores intimamente relacionados. Entre esses, pode-se citar as exigências do mercado econômico; a formação profissional; a inserção no mercado de trabalho; a busca por uma posição igualitária aos homens; avanços da tecnologia e da medicina; o surgimento dos métodos contraceptivos e dos tratamentos de infertilidade. Segundo pesquisa realizada pelo IBGE, cresceu significativamente o número de mulheres que foram mães pela primeira vez entre os 40 e 49 anos. Devido a esse perfil a busca por tratamentos de reprodução humana assistida aumentou juntamente com a procura pelo congelamento de ovócitos. Com esse cenário, existem mulheres procurando a solução para uma maternidade tardia e outras que buscam preservar sua fertilidade. Nesse sentido, é importante analisar até que ponto os tratamentos disponíveis na atualidade são úteis para ajudar as mulheres que estão nessas situações.
OBJETIVOS
Geral: Realizar uma comparação entre a técnica de fertilização in vitro com injeção intracitoplasmática de espermatozoides (ICSI), feita com ovócitos que foram fertilizados à fresco após a estimulação ovariana e punção dos folículos, e ovócitos que foram submetidos ao processo de congelamento e posterior descongelamento.
Específicos:
- Verificar a taxa de sucesso das técnicas com os dois tipos de materiais a fim de concluir qual a porcentagem de ciclos realizados que evoluem para BhcG positivos, gerando gestação.
- Verificar até que ponto a técnica de congelamento de ovócitos pode garantir a preservação da fertilidade feminina, como uma alternativa para mulheres que optam pela maternidade tardia.
MATERIAL E MÉTODOS
Para a composição deste estudo foram usados artigos retirados das plataformas Scielo, Pubmed e Google Acadêmico, além de livros acadêmicos, dados da Redlara, Associação Brasileira de Reprodução Assistida (SBRA) e Sisembrio. Os critérios de inclusão de artigos também obedeceram ao caráter de serem materiais científicos que possuíam informações comparativas, analíticas e revisões sobre tratamentos de FIV/ICSI e congelamento de ovócitos. Dados do IBGE também foram usados para verificar a taxa de natalidade referente ao ano 2021 e a idade média das mulheres que conceberam neste ano. Matérias e reportagens que relatam na mídia casos de mulheres que foram submetidas a tratamentos de fertilização in vitro também foram usados.
Para embasar este trabalho, foram analisados dados retroativos referentes ao ano de 2021 retirados de planilhas de controle e relatórios de uma clínica de reprodução humana assistida, localizada na região central da cidade de São Paulo, a qual realiza em média 1.000 tratamentos de fertilidade e preservação da fertilidade por ano. Para a utilização desses dados, foi concedida autorização do diretor clínico do estabelecimento, e o estudo foi submetido ao comitê de ética para acompanhamento dele garantindo a correta utilização das informações concedidas. As estatísticas obtidas para comparação, foram limitadas ao número de ciclos realizados que tiverem, posteriormente, o teste de gravidez positivo. As demais estatísticas apresentadas são de caráter informativo e não comparativo, uma vez que, o número de variáveis existentes em ambas as técnicas não apresenta (n) suficiente para base de comparação.
RESULTADOS
Fertilização in vitro (FIV)
Existem dois tipos de fertilização in vitro disponíveis para realização nas clínicas de reprodução humana, a FIV clássica e a ICSI (Injeção intracitoplasmática de espermatozoides). Todos os casos analisados para elaboração deste estudo foram feitos com a técnica de ICSI, a qual segue as seguintes etapas:
1. A estimulação é feita com injeções subcutâneas de gonadotrofinas recombinantes (hormônios folículoestimulante [FSH] e luteinizante [LH]). Agonistas ou antagonistas do hormônio liberador das gonadotrofinas (GnRH) são utilizados para impedir ovulação prematura durante o ciclo de indução. A monitorização é feita por meio da ultrassonografia transvaginal seriada ou, em algumas circunstâncias, com dosagens de estradiol e progesterona. Essa etapa dura, em média, 10 a 12 dias. Quando os folículos ovarianos alcançam determinado tamanho (entre 17 e 20mm), o amadurecimento final dos ovócitos é desencadeado com uma injeção de gonadotrofina coriônica humana (hCG) que mimetiza o pico natural de LH pré-ovulatório.
2. Acompanhamento com ultrassonografia vaginal para avaliação da resposta às injeções e determinação do dia da coleta dos ovócitos.
3. Aspiração dos folículos ovarianos para obtenção dos ovócitos. Esse procedimento é realizado através de uma agulha acoplada a uma sonda de ultrassonografia transvaginal, em sala de cirurgia, com sedação, e deve ser realizado em torno de 34 horas após o uso de hCG. Caso esse tempo ultrapasse 36 horas, é grande o risco de que ocorra uma ovulação indesejada.
4. Os ovócitos obtidos são levados ao laboratório, onde são classificados de acordo com sua maturidade e viabilidade (Figura 1) para recepção do gameta masculino. O esperma é coletado pela masturbação, em seguida é levado para o laboratório de andrologia onde é realizado um processamento seminal para a seleção dos melhores espermatozoides, os quais serão injetados (Figura 2) diretamente no citoplasma do oócito, através de uma microagulha em uma placa contendo os meios de cultivo ideais para a estabilidade dos gametas que estão sendo manipulados
5. Os embriões obtidos são cultivados durante 6 dias, dependendo da indicação do tratamento, do número de embriões da evolução no laboratório. Serão transferidos depois de 5 a 6 dias de cultivo no estágio de blastocisto, ou podem ser congelados para posterior transferência, de acordo com o protocolo indicado pelo médico.
6. Os embriões são transferidos para o útero com o auxílio de um cateter de material inerte e atóxico, guiado por ultrassom. A transferência é semelhante a um exame ginecológico normal. Recomenda-se repouso relativo após a transferência. 7. O teste de gravidez é feito cerca de 14 dias após a aspiração dos ovócitos, dependendo do dia de desenvolvimento do embrião transferido, ou 9 dias após a transferência de embriões descongelados em D5 (5° dia de desenvolvimento embrionário).
Figura 1: Oócito maduro com a expressão do 1° corpúsculo polar. Está na metáfase 2, pronto para ser fertilizado.
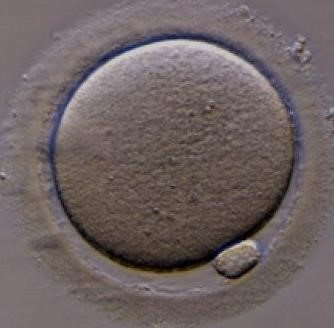
Figura 2: ICSI, espermatozoide sendo injetado no citoplasma do ovócito.
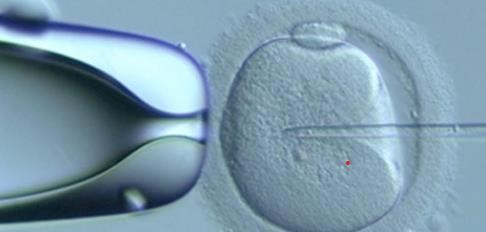
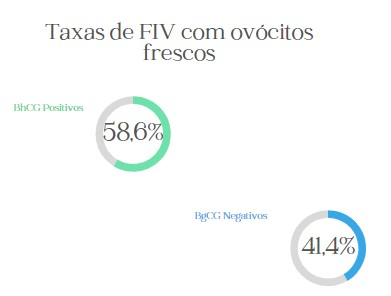
A taxa geral de sucesso da Fertilização in vitro com ICSI foi de de 58,6% de acordo com os dados obtidos de uma Clínica de Reprodução Assistida de São Paulo/SP. Levando em consideração as transferências embrionárias que evoluíram para um exame de BhcG positivo no ano de 2021, as quais foram feitas com embriões originados de ovócitos coletados e posteriormente fertilizados a fresco. Foram realizadas 559 transferências embrionárias, das quais 231 (Tabela 1) não evoluíram para gestação, gerando uma taxa de 41,4% de casos negativos. Os dados aqui analisados se referem a transferências realizadas no ano de 2021 que utilizaram embriões que não foram necessariamente gerados em ciclos realizados no mesmo ano. (Silva, Carlos Henrique Mascarenhas, 2018)
Tabela 1: Dados retirados das planilhas de controle da clínica em estudo, 328 BhcG positivos e 231 BhcG negativos.
Figura 2: Porcentagens dos dados apresentados na tabela 1.
Congelamento de ovócitos
O processo de congelamento de ovócitos ocorre em laboratório após a punção dos ovários de uma paciente que foi submetida a indução de ovulação, utilizando do mesmo protocolo de medicações aplicado na fertilização in vitro.
Após serem recebidos pelo embriologista, os ovócitos serão classificados de acordo com sua morfologia e maturidade afim de selecionar as células viáveis para o processo de congelamento. O protocolo de vitrificação usado no local de estudo deste trabalho, é referente ao material da marca Ingámed, o qual permite que as células sejam congeladas em um curto período. O processo deve ocorrer em temperatura ambiente (24° a 26°C) e é dividido em duas etapas, fase de equilíbrio e fase de vitrificação
– Fase de equilíbrio
É necessário preparar uma placa de dimensões 15×100 mm com 1 gota de 20 µl de Meio Tamponado (MT) próxima a 2 gotas de 20µl de solução de equilíbrio VI-I (gotas 1 e 2). Colocar mais 3 gotas de 20 µl de solução de equilíbrio VI-I mais afastadas (gotas 3, 4 e 5). Deixar em temperatura ambiente por 2-3 minutos antes do uso. Em seguida, após o tempo requerido, colocar os ovócitos na gota de MT. A fase de equilíbrio consiste em 3 etapas, conforme as especificações abaixo.
Etapa 1: Com o auxílio da Pipeta, juntar a gota 1 de VI-1 com a gota de MT e aguardar 3 minutos.
Etapa 2: Juntar a gota 2 de VI-1 com a gota 1 de VI-1 + MT e aguardar mais 3 minutos.
Etapa 3: A seguir, pipetar os ovócitos para a gota 3, homogeneizando cuidadosamente. De maneira similar, transferir para a gota 4 e homogeneizar cuidadosamente. Por fim, transferir para a gota 5, novamente homogeneizá-la de forma cuidadosa, e deixá-lo até a sua total recuperação osmótica celular (reidratação). Essa etapa terminará quando o volume do ovócito estiver completamente recuperado. Se a completa recuperação não puder ser confirmada, o tempo limite dessa etapa é de 9 minutos para ovócitos (somando-se as 3 etapas = 15 minutos). (Apostilia vitri, 2022)
– Fase de vitrificação
É necessário preparar uma placa de 15 x 100 mm com 3 gotas de 20 µl da solução de vitrificação VI-2 para cada haste a ser utilizada. Deixar à temperatura ambiente 2-3 minutos antes do uso. Esta placa deve estar pronta ao término da fase de equilíbrio.
Ao término da fase de equilíbrio, transferir os ovócitos da gota 5 de VI-1 para a primeira gota de VI2, com pequena quantidade de solução VI-1. Descartar o restante da solução de equilíbrio VI-1 que permaneceu na pipeta e aspirar a solução VI-2. Homogeneizar gentilmente os ovócitos. Devido à viscosidade da solução, os ovócitos devem ser bem homogeneizados, pois não se misturam facilmente. Além disso, estes tendem a flutuar na superfície da gota devido à diferença de osmolaridade dos meios intra e extracelular. Transferir os ovócitos para a segunda gota de VI-2 com o mínimo de solução. Descartar a solução remanescente na pipeta e homogeneizar cuidadosamente os ovócitos. Em seguida, deve-se colocar a haste de criopreservação sobre a placa de 15 x 100 mm e transferir o ovócito para a superfície da haste com volume mínimo de líquido. Visualizar o ovócito sobre a haste e retirar por aspiração todo o líquido excedente em torno dele. O ovócito deve permanecer na solução VI-2 entre 50-70 segundos (ideal 60 segundos). Por fim, introduzir a haste dentro do nitrogênio líquido e realizar o armazenamento dela em racks metálicas que ficarão guardadas em tanques de nitrogênio a 196 C° negativos. (Apostilia vitri, 2022)
Os ovócitos podem permanecer congelados por tempo indeterminado, até que a paciente queira submetê-los ao processo de reaquecimento para utilização do material em um processo de fertilização in vitro. (Marcelo Costa Ferreira, 2021)
Segundo um estudo da ASRM, em parceria com a Society for Assisted Reproductive Technology (SART), realizado em 2015, a taxa de fertilização a partir de ovócitos vitrificados e descongelados é de 71 a 79%. A taxa de implantação fica entre 17 e 41%.
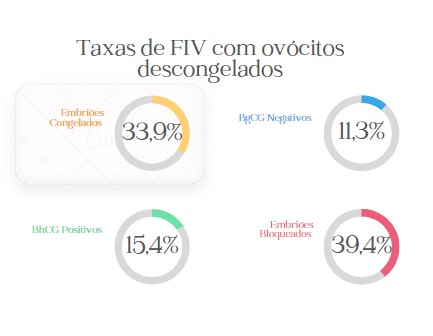
Analisando os dados de uma clínica de reprodução humana assistida, localizada no centro de São Paulo/SP, a qual foi alvo de estudo neste trabalho, a taxa de sucesso de fertilização in vitro com ovócitos descongelados, no ano de 2021, foi de 45% para casos que evoluíram para congelamento de embriões e gestações em ciclos que os embriões gerados foram transferidos a fresco. Em um total de 71 ciclos de FIV com ovócitos descongelados, 33,9% evoluíram para congelamento de embriões, 15,4% evoluíram para gestação analisando os casos em que os embriões formados foram transferidos a fresco. Enquanto, 38,4% dos casos originaram embriões que estabilizaram em uma determinada fase do desenvolvimento, não sendo viáveis para transferência embrionária e para congelamento. O restante dos ciclos que equivalem a 11,3% gerou embriões que foram transferidos a fresco e não evoluíram para gestação.
Tabela 2: Dados retirados das planilhas de controle da clínica em estudo. Foram 24 embriões congelados, 11 BhcG positivos, 28 embriões bloqueados no desenvolvimento e 8 BhcG negativos.
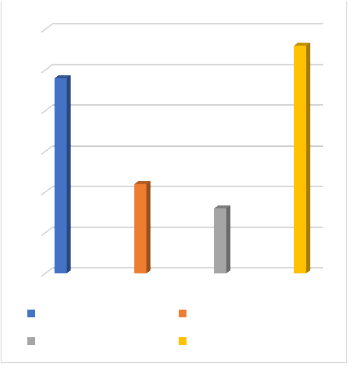
Figura 3: Porcentagens dos dados apresentados na tabela 2.
DISCUSSÃO
Através dos dados analisados foi constado que o número de casos de fertilização in vitro com ovócitos frescos é muito maior em relação aos casos realizados com ovócitos descongelados.Essa divergência numérica ocorre pois, a realização do processo de criopreservação de ovócitos é muito mais recente que a FIV convencional realizada com o material recém coletado. O congelamento de ovócitos é uma técnica relativamente nova (o primeiro humano gerado a partir de um ovócito congelado nasceu em 1986). Apenas em 2013, o procedimento foi aprovado pela American Society for Reproductive Medicine (ASRM) para o emprego além dos ensaios clínicos supervisionados. Nesse sentido, pode-se considerar que a alta dos casos de FIV com ovócitos descongelados passará a ocorrer dessa década em diante.
Um estudo realizado pelo Serviço de Medicina Reprodutiva do departamento de Obstetrícia, Ginecologia e Reprodução de Barcelona, Espanha comparou taxas de gravidez em curso e outros índices de viabilidade entre ovócitos vitrificados e ovócitos frescos. Neste estudo, foi realizado um total de 99 doações, com mais de 16 ovócitos maduros, em que os ovócitos foram alocados para uma destinatária síncrona (ovócitos frescos) e a uma destinatária assíncrona (ovócitos vitrificados).
No dia da punção dos folículos, os ovócitos alocados para as receptoras síncronas foram micro-injetados com espermatozoides ainda frescos e os alocados para o banco de ovócitos foram vitrificados.
Um total de 989 ovócitos foi aquecido (desvitrificado) e 85,6% sobreviveram. Não houve diferenças significativas observadas entre a taxa de fertilização de ovócitos frescos (80,7%) e a taxa de fertilização de ovócitos vitrificados (78,2%), também não houve diferença entre a taxa de embriões em curso provenientes de ovócitos frescos (71,0%) ou de ovócitos vitrificados (68,2%) nem mesmo diferença entre a taxa de embriões de alta qualidade. Além disso, o número médio de embriões transferidos foi semelhante em ambos os grupos. (Franciele Osmarini Lunardi, 2016)
Dessa forma foram evidenciadas que as taxas de implantação (33,3% versus 34,0%) e as taxas de gravidez múltipla (27,7% contra 20,8%) também foram semelhantes entre os dois grupos. Além disso, a taxa de nascidos vivos por ciclo foi de 38,4% nas receptoras de ovócitos frescos e de 43,4% nas receptoras de ovócitos vitrificados, também sem diferença estatística.
Por fim, foram avaliadas oitenta e cinco transferências de embriões congelados nos dois grupos. Comparando embriões a partir de ovócitos frescos e vitrificados não houve diferenças significativas na taxa de sobrevivência embrionária (70,1% contra 65,8%), na taxa de gravidez clínica (40,8% contra 33,3%) nem na taxa de implantação (21,8% contra 26,8%).
Após estes resultados foi possível concluir que a utilização de ovócitos previamente vitrificados é tão favorável quanto à utilização de ovócitos frescos. Esses resultados estimulam o uso da vitrificação de ovócitos, para outras aplicações, como, por exemplo, para a preservação de fertilidade de pacientes que desejam ou precisam adiar a maternidade. Com a vitrificação dos ovócitos a mulher pode atingir a maturidade sem preocupar-se com a diminuição significativa da capacidade para conceber no futuro, pois contará com amostras de ovócitos preservadas que não envelhecerão. (Franciele Osmarini Lunardi, 2016)
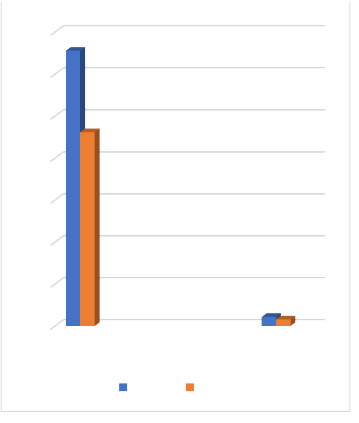
Verificando os casos realizados na clínica de reprodução humana assistida localizada em São Paulo/SP, no ano de 2021, foram realizados 71 ciclos de fertilização in vitro com ovócitos descongelados, dos quais, apenas 11 casos tiveram como finalidade a transferência dos embriões gerados. O restante dos embriões que evoluíram de forma adequada, foi congelado para posterior transferência. Nesse sentido, a taxa de sucesso da técnica foi de 15,4%, levando em consideração apenas os casos que obtiveram o exame de BhcG positivo ao final do ciclo.
Em contrapartida, foram realizadas 559 transferências de embriões originados de fertilização in vitro com ovócitos frescos, das quais 328 evoluíram para gestação, apresentando uma taxa de 58,6% de sucesso para esta técnica.
Tabela 3: Dados retirados das planilhas de controle da clínica em estudo. Foram 328 BhcG positivos e 231 negativos em ciclos frescos e 11 BhcG positivos e 8 negativos em ciclos descongelados.
De acordo com o periódico espanhol “El Mundo”, para analisar os benefícios dos procedimentos de FIV com ovócitos frescos e FIV com ovócitos descongelados, investigadores do Centro de Reprodução Humana de Nova Iorque realizaram um estudo retrospectivo em que foram verificados dados de 2013 incluídos no relatório anual dos resultados obtidos por clínicas de reprodução assistida nos EUA.
A equipe comparou dados de 11.148 ciclos com doação de ovócitos, dos quais 2.227 estavam criopreservados. A análise revelou que 12% dos ciclos de FIV foram canceladas quando o óvulo era fresco, contra 8,5% de cancelamentos daqueles que usaram ovócitos criopreservados. Este resultado pode sugerir que é melhor usar ovócitos criopreservados, no entanto, os dados apenas dizem respeito à percentagem de ciclos de IVF não iniciados.
Quando só se levou em conta os processos iniciados, os pesquisadores descobriram que a taxa de natalidade foi de 50% no grupo de ovócitos frescos e 43% para a criopreservação. Estes números foram semelhantes para cada embrião transferido, com a taxa de natalidade foi de 56% de ovócitos frescos em comparação com 47 com criopreservados.
CONSIDERAÇÕES FINAIS
Devido a reformulação do conceito de maternidade que vem ocorrendo nas últimas décadas, os tratamentos de reprodução humana assistida têm ganhado grande extensão na sociedade em geral. Principalmente na vida das mulheres que, cada vez mais, buscam por conquistar seu lugar no mercado de trabalho e expandir seus horizontes de conhecimento, prezando por organizar os acontecimentos de suas vidas, incluindo o planejamento familiar, a fim de definir o momento ideal para gestar. Nesse sentido, o congelamento de ovócitos vem sendo cada vez mais procurado como uma alternativa para pausar a idade fértil da mulher, de forma que ela possa planejar o momento ideal de sua maternidade, sem que as consequências trazidas pela idade aos seus ovócitos, interfiram na concepção de um filho.
De acordo com os dados expostos no presente trabalho, as técnicas de fertilização in vitro estão extremamente refinadas e tem trazido resultados positivos aos pacientes que se submetem a ele. Ao comparar as taxas produzidas pelos tratamentos de FIV com ovócitos frescos e ovócitos descongelados, foi possível identificar que ambas as técnicas são confiáveis e não trazem diferenças significativas para o sucesso dos ciclos realizados. Nesse sentido, pode-se afirmar que a técnica de congelamento de ovócitos pode garantir a preservação da fertilidade da mulher, uma vez que, o sucesso dos tratamentos feitos com ovócitos descongelados é muito semelhante aos feitos com ovócitos frescos, mesmo que as células tenham sido submetidas ao processo de vitrificação e desvitrificação.
REFERÊNCIAS BIBLIOGRÁFICAS
- L. C. Junqueira e José Carneiro, 12° ed. 2013.
- Elvio Tognotti, infertilidade da prática clínica, 2014.
- Rodrigo da Rosa Filho, 2015.
- Fernanda Travassos, Terezinha Carneiro, Maternidade tardia e ambivalência, 2013.
- Fert Embryo, 2020.
- Elvio Tognotti, infertilidade da prática clínica, 2014.
- Arnaldo Cambiaghi, 2022.
- Elvio Tognotti, infertilidade da prática clínica, 2014. 9. Silva, Carlos Henrique Mascarenhas, Manual SOGIMIG de reprodução assistida/Carlos Henrique Mascarenhas
- Silva, Sandro Magnavita Sabino, Ines Katerina Damasceno Cavallo Cruzeiro. 1. ed. Rio de Janeiro: Medbook, 2018.
- Apostila de protocolo de vitrificação e aquecimento, ingámed, 2022.
- Apostila pref Vitoria da conquista BA , 2022.
- Marcelo Costa Ferreira, 2021.
- Serviço de Medicina Reprodutiva do departamento de Obstetrícia, Ginecologia e Reprodução de Barcelona, Espanha. Publicada na Human Reproduction, Vol.28, No.8 pp. 2087–2092, no ano de 2013.
- Franciele Osmarini Lunardi, Óvulos frescos ou Franciele Osmarini Lunardi, previamente vitrificados faz Óvulos frescos ou diferença na taxa de previamente vitrificados faz gravidez, 2016. diferença na taxa de gravidez, 2016.
1. Discente da Universidade Anhembi Morumbi, São Paulo / SP, Brasil
2. Docente da Universidade Anhembi Morumbi, São Paulo / SP, Brasil
3. Responsável técnica de Embriologia da Clínica de Reprodução Humana – Engravida, São Paulo / SP, Brasil
